-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Post-JIP péče v ambulantním prostředí
Vyšlo v časopise: Svět praktické medicíny, 2, 2021, č. 5, s. 9-13
Kategorie: Medicína ve světě: překladový článek s komentáři
Souhrn
Za článkem následují komentáře
Více než 5 milionů pacientů ve Spojených státech je každoročně přijímáno na jednotky intenzivní péče (JIP) a rostoucí procento pacientů léčených na JIP přežije propuštění z nemocnice. Vzhledem k tomu, že tito pacienti vyžadují sledování v ambulantním prostředí, praktičtí lékaři by měli být připraveni poskytovat průběžnou péči a screening komplikací po hospitalizaci na JIP. Rizikové faktory pro komplikace po propuštění z JIP zahrnují předchozí přijetí na JIP, již existující duševní onemocnění, větší počet komorbidit a prodlouženou mechanickou ventilaci nebo vyšší expozici opioidům na JIP. Včasná nutriční podpora a mobilizace na JIP snižují riziko komplikací. Po propuštění z JIP by pacienti měli být vyšetřeni na depresi, úzkost, nespavost a kognitivní poruchy pomocí standardizovaných screeningových nástrojů. Lékaři by se také měli informovat o slabosti, únavě, neuropatii a funkčním poškození a provést cílené fyzikální vyšetření a laboratorní vyšetření; léčba závisí na základní příčině. Cvičební režimy jsou prospěšné pro snížení některých komplikací po hospitalizaci na JIP. Pacienti, kteří byli léčeni na COVID-19 na JIP, by měli dostat další pokyny ke snížení rizika přenosu viru. Telemedicína a telerehabilitace umožňují pacientům s COVID-19 získat účinnou péči bez zvýšení rizika expozice v komunitách, nemocnicích a lékařských ordinacích.
Více než 5 milionů pacientů ve Spojených státech je každoročně přijato na jednotky intenzivní péče (JIP).1 Úmrtnost mezi těmito pacienty se mezi lety 1988 a 2012 snížila o 35 %, a to navzdory rostoucí závažnosti onemocnění a zvyšujícímu se věku pacientů; současná úmrtnost se odhaduje na 10 až 29 %.1 Vzhledem k tomu, že větší počet pacientů přežívá po propuštění z JIP a vyžaduje sledování v ambulantním prostředí, rodinní lékaři by měli být připraveni poskytovat průběžnou péči a screening komplikací po JIP.
Bez všeobecně přijímaných pokynů by měly být načasování a frekvence sledování po hospitalizaci na JIP individualizovány a založeny na komorbiditách pacienta a závažnosti onemocnění. Ač koli asi 20 lékařských středisek ve Spojených státech má post-JIP přechodové kliniky,2 neexistují důkazy, že by takové programy snižovaly míru opětovného přijetí nebo úmrtnosti.3
Klíčová doporučení pro praxi 
JIP = jednotka intenzivní péče.
A = konzistentní, kvalitní důkazy orientované na pacienta; B = nekonzistentní důkazy nebo důkazy s omezenou kvalitou zaměřené na pacienta; C = konsenzus, důkazy zaměřené na nemoci, obvyklá praxe, znalecký posudek nebo série případů.
Informace o systému hodnocení důkazů SORT naleznete na https://www.aafp.org/afpsort.Ačkoli termín post-intensive care syndrom (PICS) byl použit k popisu různých komplikací hlášených u přeživších léčbu na JIP (Tab. 1),4 neexistuje žádná všeobecně přijímaná definice takového syndromu. Praktičtí lékaři by měli být obeznámeni s komplikacemi, které mohou nastat po propuštění (např. fyzické a psychické postižení), a to i u pacientů zotavujících se z onemocnění COVID-19.
Tab. 1. Časté komplikace po propuštění z JIP 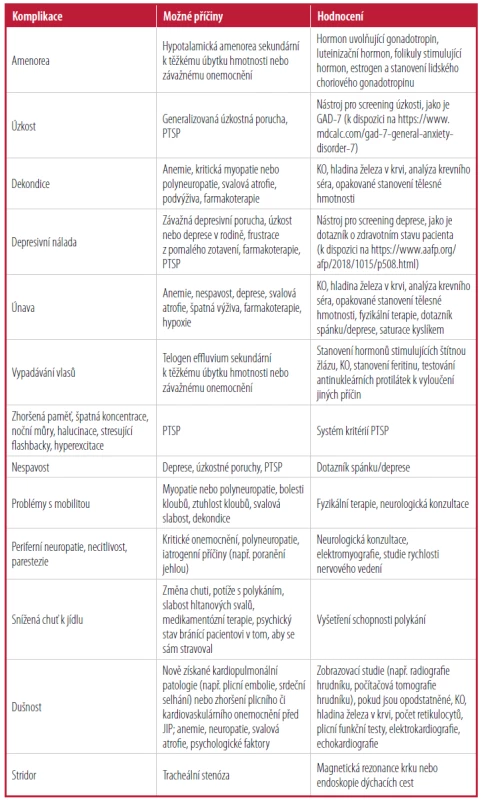
KO = kompletní krevní obraz; JIP = jednotka intenzivní péče; PTSP = posttraumatická stresová porucha.
Upraveno se svolením Volk B, Grassi F. Léčba pacienta po JIP v ambulantním prostředí. Am Fam Practise. 2009;79(6):460.Fyzické aspekty
Dekondice
Jeden rok po propuštění z JIP má více než 20 % pacientů bez funkčního omezení před přijetím určité potíže s dokončováním činností každodenního života.5 National Institute for Health and Care Excellence doporučuje znovu posoudit fyzické funkce pacientů dva až tři měsíce po propuštění.6 Cvičení a svépomocné rehabilitační programy zlepšují funkci svalů a kardiopulmonální funkci po kritickém onemocnění.7,8 Pacienti s dekondicí by měli být poučeni o domácím cvičebním režimu nebo by měli být odkázáni na rehabilitaci.
Obecně platí, že pacienti by měli být vyšetřeni na slabost při následném sledování a v případě potřeby by měli být doporučeni k fyzioterapii.5–8
Polyneuropatie kriticky nemocných
Pacienti léčení na JIP jsou ohroženi kritickým onemocněním (nebo získaným na JIP) polyneuropatií, onemocněním periferních nervů sekundárním k axonální degeneraci. Tento stav je způsoben složitými a špatně pochopitelnými procesy, které zahrnují abnormality mikrocirkulace, metabolické poruchy a další faktory.9–11 Polyneuropatie kriticky nemocných je charakterizována přítomností slabosti končetin a nevysvětlitelnými obtížemi při odvykání od mechanické ventilace. Sepse, prodloužená mechanická ventilace, hyperglykemie a multiorgánové selhání zvyšují riziko polyneuropatie.9, 10
Ačkoli nervové funkce se obvykle začínají zlepšovat, když jsou vyřešeny závažné zdravotní problémy, slabost a necitlivost mohou v těžkých případech přetrvávat. Existuje jen málo důkazů o účinku fyzické rehabilitace nebo farmakologických intervencí při léčbě polyneuropatie nemocných, ale včasná mobilizace na JIP může zlepšit mobilitu a svalovou sílu.12, 13 U bolestivé polyneuropatie je třeba zvážit gabapentin (Neurontin), pregabalin (Lyrica) nebo inhibitory zpětného vychytávání serotoninu a norepinefrinu.
Myopatie kriticky nemocných
Myopatie kriticky nemocných se také prezentuje jako svalová slabost a potíže s odvykáním od mechanické ventilace. Předpokládá se, že patofyziologie myopatie je podobná patofyziologii polyneuropatie kriticky nemocných.10, 11 Při rozlišování mezi těmito dvěma klinicky podobnými onemocněními mohou pomoci elektromyografie a studie rychlosti nervového vedení. Svalová biopsie je považována za diagnostický standard pro myopatii.12
Na rozdíl od kritické polyneuropatie se myopatie kriticky nemocných může zlepšit cvičením. Včasná mobilizace a fyzikální terapie mají největší důkaz o přínosu.10, 11
Podvýživa
Včasná nutriční podpora se stala standardem péče na JIP a dalších lůžkových zařízeních a je spojena se sníženou mírou infekce, délkou hospitalizace a rizikem opětovného přijetí.14, 15 Během sledování po léčbě na JIP by měla být posuzována hmotnost před příjmem a po příjmu, chuť k jídlu a kalorický příjem.
Nespavost
Mezi pacienty léčenými na JIP hlásí 10 % až 61 % potíže se spánkem šest měsíců po propuštění.16 Rizikové faktory pro nespavost zahrnují koexistující duševní onemocnění a vyšší expozici opioidům na JIP. Nespavost po léčbě na JIP je spojena se zvýšenou úrovní bolesti a sníženou fyzickou výkonností.17 Pacienti by měli být během sledování po hospitalizaci na JIP dotázáni na kvalitu spánku a nespavost. Osoby, které mají potíže se spánkem, by měly být léčeny nefarmakologickými intervencemi, včetně spánkové hygieny, kognitivně-behaviorální terapie a relaxačních technik.18
Sexuální dysfunkce
Sexuální dysfunkce se vyskytuje až u 44 % pacientů léčených na JIP.19 Neexistují žádné studie porovnávající prevalenci sexuální dysfunkce u pacientů léčených na JIP s běžnou populací a neexistují žádná doporučení pro screening sexuální dysfunkce během sledování po JIP.
Když je diagnostikována sexuální dysfunkce, mělo by být posouzeno psychické zdraví kvůli silné korelaci mezi sexuální dysfunkcí a posttraumatickou stresovou poruchou (PTSP). Léčba sexuální dysfunkce po JIP se zaměřuje na základní příčinu. Typická farmakologická terapie, jako jsou inhibitory fosfodiesterázy, nebyla u populace po hospitalizaci na JIP studována.
Psychologická hlediska
Kognitivní poruchy
U pacientů hospitalizovaných na JIP je vysoká prevalence kognitivních poruch a několik studií prokázalo přetrvávání kognitivních poruch po propuštění u více než 20 % pacientů.20, 21 Až u 2,5 % pacientů se po JIP rozvine nová a přetrvávající kognitivní porucha, se zvyšujícím se rizikem spojeným s vyšším počtem komorbidit a hospitalizací na JIP.20 Hypotenze, hypoxie, hypertermie, delirium a užívání vankomycinu nebo chinolonu může také zvýšit riziko kognitivních poruch.20, 21
Ačkoli existují omezené důkazy pro specifickou léčbu kognitivního poškození v prostředí po JIP, pacienti by měli být vyšetřeni na kognitivní poškození a také by měli být vyšetřeni na základní reverzibilní příčiny, jako je deprese, nutriční deficity a metabolické poruchy, pokud jsou přítomny.20–22 Prospěšné může být cvičení, duševní aktivita a optimalizace kardiovaskulárních rizikových faktorů.22
Deprese
Depresivní nálada a další problémy s duševním zdravím jsou u pacientů po hospitalizaci na JIP běžné. Mezi pacienty léčenými na JIP má 30 % alespoň mírnou depresi 12 měsíců po propuštění.23, 24 Jedna studie ukázala, že depresivní příznaky u pacientů léčených na JIP jsou častěji somatické (např. únava, snížená chuť k jídlu) a u pacientů s těžkou depresí je větší pravděpodobnost souběžné PTSP.5 Deprese byla spojena se zvýšenou mírou úmrtnosti až dva roky po propuštění z JIP.23
Pacienti by měli být vyšetřeni na depresi pomocí ověřeného screeningového nástroje, jako je dvoupoložkový nebo devítipoložkový dotazník o zdraví pacienta (dostupný na https://www.aafp.org/afp/2018/1015/p508.html).5, 24, 25 Pokud je diagnostikována deprese, je třeba zahájit vhodnou psychoterapii a/nebo farmakologickou léčbu.
Úzkost
Prevalence úzkosti 12 měsíců po propuštění z JIP se pohybuje od 12 % do 43 %.25 Více než 60 % pacientů s úzkostnou poruchou po pobytu na JIP má také PTSD nebo depresi.23 Pacienti by měli být vyšetřeni na úzkost pomocí standardizovaného screeningového nástroje, jako je General Anxiety Disorder-7 (dostupný na https://www.mdcalc.com/gad-7-general-anxiety-disorder-7).5, 24, 25 Pokud je diagnostikována úzkost, je třeba zahájit vhodnou psychoterapii a/nebo farmakologickou léčbu.
Posttraumatická stresová porucha
Mezi pacienty léčenými na JIP má 7 % až více než 20 % PTSP 12 měsíců po propuštění.5, 23 Pacienti by měli být vyšetřeni na PTSP pomocí standardizovaného nástroje, jako je test PTSP (dostupný na https://www.ptsd.va.gov/professional/assessment/screens/pc-ptsd.asp).5, 24, 25 Bylo prokázáno, že revize deníku JIP (tj. každodenní záznamy pacienta na JIP) během období rekonvalescence snižuje riziko PTSP.26
Vzhledem k tomu, že 18–31 % partnerů a rodinných příslušníků pacientů léčených na JIP má také příznaky PTSP šest měsíců po propuštění, rodinní lékaři by měli zvážit jejich screening na PTSP, úzkost a depresi.27, 28 Ženské pohlaví, již existující poruchy duševního zdraví a osobní anamnéza nedávného vážného onemocnění jsou spojeny s vyšší mírou PTSP v této populaci, stejně jako partnerství nebo rodinná příslušnost k dříve zdravému pacientovi.27, 28
Medikace
Aby se předešlo komplikacím po propuštění, je nezbytné sladit léky před hospitalizací a po hospitalizaci na JIP. Při přijetí na JIP je běžné neúmyslné vysazení léků, které léčí chronické stavy.29 Praktičtí lékaři by měli určit indikaci, vhodnost a dobu užívání nových léků předepsaných při propuštění. V jedné studii byly ve více než 40 % případů rozdíly mezi léky předepsanými při propuštění z JIP a léky dokumentovanými v ambulantních podmínkách.30 Starším pacientům mohou být na JIP předepisovány potenciálně nevhodné léky (např. opioidy, anticholinergika) a léčba těmito léky často pokračuje i při propuštění.31 Léky na chronické stavy, které byly vysazeny při propuštění, by měly být posouzeny a znovu nasazeny pouze v případě potřeby.
Plánování péče
Ve srovnání s běžnou populací mají pacienti léčení na JIP zvýšenou úmrtnost až 10 let po propuštění.1 Během sledování po pobytu na JIP by se rodinní lékaři měli zabývat cíli zdravotní péče pacientů a přáními na konci života a identifikovat zástupce odpovědné za zdravotní péči. Měly by být prodiskutovány preference pacienta týkající se resuscitace, umělé výživy, mechanické ventilace a případného budoucího přijetí na JIP. Tuto komunikaci mohou usnadnit nástroje, jako je Průvodce konverzací o vážné nemoci (dostupný na https://www.aafp.org/afp/2019/0301/p281.html).
Důležité informace o COVID-19
Pacienti přijatí na JIP s COVID-19 jsou vystaveni riziku typických komplikací po hospitalizaci na JIP i dalších komplikací, jako jsou trombotické a cévní problémy.32 Léčba COVID-19 po hospitalizaci na JIP se vyvíjí. Nedávná observační studie ukázala, že ačkoli počet obětí COVID-19 sahá daleko za hospitalizaci, jeden z pěti pacientů hospitalizovaných s COVID-19 nemá do 60 dnů od propuštění žádnou následnou primární péči.33
Sledování po propuštění z nemocnice
Ačkoli neexistuje všeobecná shoda na tom, kdy a jak by mělo dojít k následnému sledování po léčbě COVID-19 na JIP, odborná doporučení podporují pečlivé sledování s rozsáhlým vzděláváním pacientů a pečovatelů.34, 35
Centra pro kontrolu a prevenci nemocí doporučují přerušit opatření pro přenos u pacientů s počátečním mírným až středně závažným onemocněním, pokud uplynulo nejméně 10 dní od nástupu příznaků, pacient je afebrilní bez použití antipyretik po dobu nejméně 24 hodin a příznaky se zlepšily.35 U pacientů se závažným až kritickým onemocněním nebo u pacientů se závažnou imunokompromitací je třeba pokračovat v opatřeních pro přenos po dobu až 20 dnů a zvážit konzultaci s odborníky na kontrolu infekcí. Vzhledem k tomu, že Centra pro kontrolu a prevenci nemocí již nedoporučují strategii založenou na testech, pacienti propuštění domů musí dodržovat doporučení pro sebeizolaci a vlastní monitorování, pokud zůstávají v platnosti opatření proti přenosu. Medikace pro chronické stavy by měla pokračovat kromě jistých výjimek (Tab. 2).34–36
Tab. 2. Vybrané informace o medikaci pro pacienty s COVID-19 
NSAID = nesteroidní protizánětlivé léky
Informace z referencí 34–36.Rehabilitace
Cvičení a svépomocné rehabilitační programy zlepšují funkci svalů a kardiopulmonální funkci po kritickém onemocnění.7, 8 Se vznikem telemedicíny, která umožňuje sociální distanci, je telerehabilitace životaschopnou alternativou pro pacienty v izolaci. Studie pacientů se srdečním selháním nebo cévní mozkovou příhodou ukázaly, že telerehabilitace není horší než tradiční fyzikální terapie.37, 38 Během počáteční ambulantní fáze zotavení je však třeba se vyvarovat nekontrolovaného cvičení a vrcholového sportu, protože až 22 % pacientů hospitalizovaných s COVID-19 má důkazy o poškození myokardu a/nebo myokarditidě.39
I když jsou důkazy omezené, odborný konsenzus navrhuje postupný návrat k aktivitě, pokud nedávné nálezy srdečních biomarkerů a elektrokardiogramu a echokardiogramu byly během přijetí normální a pacient byl asymptomatický po dobu nejméně dvou týdnů.39 Další vyšetření srdce lze zvážit u dříve vysoce aktivních jedinců, kteří takové vyšetření během přijetí nepodstoupili.39
Telemedicína
Předchozí studie ukázaly podobné zdravotní výsledky u těch, kteří dostávají péči prostřednictvím telemedicíny, v porovnání s tradiční zdravotní péčí a mnoho pacientů uvádí, že dávají přednost virtuálním návštěvám před osobními návštěvami.40, 41 Bylo zjištěno, že péče poskytovaná prostřednictvím telemedicíny není horší než tradiční zdravotní péče během propuknutí jiných onemocnění, včetně těžkého akutního respiračního syndromu, MERS a chřipky.42 Mezi výhody telemedicínských návštěv pro pacienty, kteří se zotavují z COVID-19 nebo kteří mají mírné příznaky, patří snížené používání osobních ochranných prostředků a snížené riziko expozice v komunitách, nemocnicích a lékařských ordinacích.
Domácí ošetřovatelská péče
Pokud jsou klienti pečovatelských domů při podezření na COVID-19 převáženi do nemocnice za účelem vyšší úrovně péče, před převozem by měly být nastudovány předběžné pokyny. Pacienti hospitalizovaní s COVID-19 by měli být propuštěni do pečovatelského domu nebo zařízení skupinové péče pouze v případě, že jsou k dispozici osobní ochranné prostředky a pacient může být izolován od ostatních obyvatel. Pečovatelská zařízení by měla zavést screeningové protokoly pro personál a posílení kontroly infekcí.43
Tento článek aktualizuje předchozí článek na toto téma od Volk a Grassi.4
Zdroje dat: Rešerše literatury byla provedena pomocí PubMed, databáze Cochrane a Essential Evidence Plus. Vyhledávací dotazy zahrnovaly termíny: post-ICU, post intensive care, and post critical care, individually and collectively. Tyto pojmy byly také spárovány s následujícími pojmy: mental illness, weakness, malnutrition, rehabilitation, cognition, COVID-19 a SARS-Co-V2.
Termíny vyhledávání: květen až prosinec 2020.
Autoři jsou z katedry rodinné medicíny University of Iowa Carver College of Medicine, Iowa City, Iowa. Jason Wi lbur, MD, FAAFP, je zde místopředsedou pro vzdělávání a klinickým profesorem, Jessica Rockafellow, MD, je klinickou asistentkou a Brian Shian, MD, zde působí jako klinický docent.
Článek v původním znění:
Am Fam Physician. 2021;103(10):590–596.
Překlad: J. Moravcová
Publikováno se souhlasem AAFP
Chráněno autorským právem
Jason Wilbur, MD
University of Iowa Carver College of Medicine, Iowa City, Iowa
Jessica Rockafellow, MD
University of Iowa Carver College of Medicine, Iowa City, Iowa
Brian Shian, MD
University of Iowa Carver College of Medicine, Iowa City, Iowa
Zdroje
1. Society of Critical Care Medicine. Critical care statistics. Accessed September 9, 2020. https://www.sccm.org/Communications/Critical-Care-Statistics...
2. Kuehn BM. Clinics aim to improve post-ICU recovery. JAMA. 2019;321(11):1036–1038.
3. Stelfox HT, Bastos J, Niven DJ, et al. Critical care transition programs and the risk of readmission or death after discharge from ICU. Intensive Care Med. 2016;42(3):401–410.
4. Volk B, Grassi F. Treatment of the post-ICU patient in an outpatient setting. Am Fam Physician. 2009;79(6):459–464. Accessed October 29, 2020. https://www.aafp.org/afp/2009/0315/p459.html
5. Jackson JC, Pandharipande PP, Girard TD, et al.; Bringing to light the Risk Factors And Incidence of Neuropsychological dysfunction in ICU survivors (BRAIN-ICU) study investigators. Depression, post-traumatic stress disorder, and functional disability in survivors of critical illness in the BRAIN-ICU study: a longitudinal cohort study. Lancet Respir Med. 2014;2(5):369–379.
6. National Institute for Health and Care Excellence. Rehabilitation after critical illness in adults. September 7, 2017. Accessed June 10, 2020. https://www.nice.org.uk/guidance/qs158.
7. Jones C, Skirrow P, Griffiths RD, et al. Rehabilitation after critical illness: a randomized, controlled trial. Crit Care Med. 2003;31(10):2456–2461.
8. Lau HMC, Ng GYF, Jones AYM, et al. A randomised controlled trial of the effectiveness of an exercise training program in patients recovering from severe acute respiratory syndrome. Aust J Physiother. 2005;51(4):213–219.
9. Hough CL, Steinberg KP, Taylor Thompson B, et al. Intensive care unit–acquired neuromyopathy and corticosteroids in survivors of persistent ARDS. Intensive Care Med. 2009;35(1):63–68.
10. Shepherd S, Batra A, Lerner DP. Review of critical illness myopathy and neuropathy. Neurohospitalist. 2017;7(1):41–48.
11. Zhou C, Wu L, Ni F, et al. Critical illness polyneuropathy and myopathy: a systematic review. Neural Regen Res. 2014;9(1):101–110.
12. Tipping CJ, Harrold M, Holland A, et al. The effects of active mobilisation and rehabilitation in ICU on mortality and function: a systematic review. Intensive Care Med. 2017;43(2):171–183.
13. Shepherd SJ, Newman R, Brett SJ, et al.; Enhancing Rehabilitation After Critical Illness Programme Study Investigators. Pharmacological therapy for the prevention and treatment of weakness after critical illness: a systematic review. Crit Care Med. 2016;44(6):1198–1205.
14. Marik PE, Zaloga GP. Early enteral nutrition in acutely ill patients: a systematic review [published correction appears in Crit Care Med. 2002;30(3):725]. Crit Care Med. 2001;29(12):2264–2270.
15. Philipson TJ, Snider JT, Lakdawalla DN, et al. Impact of oral nutritional supplementation on hospital outcomes. Am J Manag Care. 2013;19(2):121–128.
16. Altman MT, Knauert MP, Pisani MA. Sleep disturbance after hospitalization and critical illness: a systematic review. Ann Am Thorac Soc. 2017;14(9):1457–1468.
17. Parsons EC, Hough CL, Vitiello MV, et al. Insomnia is associated with quality of life impairment in medical-surgical intensive care unit survivors. Heart Lung. 2015;44(2):89–94.
18. Maness DL, Khan M. Nonpharmacologic management of chronic insomnia. Am Fam Physician. 2015;92(12):1058–1064. Accessed October 29, 2020. https://www.aafp.org/afp/2015/1215/p1058.html.
19. Griffiths J, Gager M, Alder N, et al. A self-report-based study of the incidence and associations of sexual dysfunction in survivors of intensive care treatment. Intensive Care Med. 2006;32(3):445–451.
20. Sakusic A, Gajic O, Singh TD, et al. Risk factors for persistent cognitive impairment after critical illness, nested case-control study. Crit Care Med. 2018;46(12):1977–1984.
21. Marra A, Pandharipande PP, Girard TD, et al. Co-occurrence of post-intensive care syndrome problems among 406 survivors of critical illness. Crit Care Med. 2018;46(9):1393–1401.
22. Langa KM, Levine DA. The diagnosis and management of mild cognitive impairment: a clinical review. JAMA. 2014;312(23):2551–2561.
23. Hatch R, Young D, Barber V, et al. Anxiety, depression and post traumatic stress disorder after critical illness: a UK-wide prospective cohort study. Crit Care. 2018;22(1):310.
24. Wang S, Mosher C, Perkins AJ, et al. Post-intensive care unit psychiatric comorbidity and quality of life. J Hosp Med. 2017;12(10):831–835.
25. Myhren H, Ekeberg O, Tøien K, et al. Posttraumatic stress, anxiety and depression symptoms in patients during the first year post intensive care unit discharge. Crit Care. 2010;14(1):R14.
26. Jones C, Bäckman C, Capuzzo M, et al.; RACHEL group. Intensive care diaries reduce new onset post traumatic stress disorder following critical illness: a randomised, controlled trial. Crit Care. 2010;14(5):R168.
27. Lee RY, Engelberg RA, Curtis JR, et al. Novel risk factors for posttraumatic stress disorder symptoms in family members of acute respiratory distress syndrome survivors. Crit Care Med. 2019;47(7):934–941.
28. Wintermann GB, Petrowski K, Weidner K, et al. Impact of post-traumatic stress symptoms on the health-related quality of life in a cohort study with chronically critically ill patients and their partners: age matters. Crit Care. 2019;23(1):39.
29. Bell CM, Brener SS, Gunraj N, et al. Association of ICU or hospital admission with unintentional discontinuation of medications for chronic diseases. JAMA. 2011;306(8):840–847.
30. Moore C, Wisnivesky J, Williams S, et al. Medical errors related to discontinuity of care from an inpatient to an outpatient setting. J Gen Intern Med. 2003;18(8):646–651.
31. Morandi A, Vasilevskis E, Pandharipande PP, et al. Inappropriate medication prescriptions in elderly adults surviving an intensive care unit hospitalization. J Am Geriatr Soc. 2013;61(7):1128–1134.
32. Holshue ML, DeBolt C, Lindquist S, et al.; Washington State 2019-nCoV Case Investigation Team. First case of 2019 novel coronavirus in the United States. N Engl J Med. 2020;382(10):929–936.
33. Chopra V, Flanders SA, O’Malley M, et al. Sixty-day outcomes among patients hospitalized with COVID-19 [published online November 11, 2020]. Ann Intern Med. Accessed December 2, 2020. https://www.acpjournals.org/doi/10.7326/M20-5661
34. National Institutes of Health. Coronavirus disease 2019 (COVID-19). Treatment guidelines. Accessed July 11, 2020. https://covid19treatmentguidelines.nih.gov.
35. Centers for Disease Control and Prevention. Discontinuation of transmission-based precautions and disposition of patients with COVID-19 in healthcare settings (interim guidance). Updated August 10, 2020. Accessed December 2, 2020. https://www.cdc.gov/coronavirus/2019-ncov/hcp/disposition-hospitalized-patients.html
36. University of California San Francisco Health. UCSF inpatient adult COVID-19 interim management guidelines. March 28, 2020. Accessed July 11, 2020. https://infectioncontrol.ucsfmedicalcenter.org/content/ucsf-inpatient-adult-covid-19--interim-management-guidelines.
37. Hwang R, Bruning J, Morris NR, et al. Home-based telerehabilitation is not inferior to a centre-based program in patients with chronic heart failure: a randomised trial. J Physiother. 2017;63(2):101–107.
38. Tchero H, Tabue Teguo M, Lannuzel A, et al. Telerehabilitation for stroke survivors: systematic review and meta-analysis. J Med Internet Res. 2018;20(10):e10867.
39. Phelan D, Kim JH, Chung EH. A game plan for the resumption of sport and exercise after coronavirus disease 2019 (COVID-19) infection [published online May 13, 2020]. JAMA Cardiol. Accessed July 17, 2020. https://jamanetwork.com/journals/jamacardiology/fullarticle/2766124.
40. Flodgren G, Rachas A, Farmer AJ, et al. Interactive telemedicine: effects on professional practice and health care outcomes. Cochrane Database Syst Rev. 2015;(9):CD002098.
41. Boehm K, Ziewers S, Brandt MP, et al. Telemedicine online visits in urology during the COVID-19 pandemic-potential, risk factors, and patients‘ perspective. Eur Urol. 2020;78(1):16–20.
42. Ohannessian R. Telemedicine: potential applications in epidemic situations. Eur Res Telemed. 2015;4(3):95–98.
43. American Geriatrics Society policy brief: COVID-19 and nursing homes. J Am Geriatr Soc. 2020;68(5):908–911.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovoČlánek Nové evropské registraceČlánek Domácí měření krevního tlakuČlánek Hypertenze a fibrilace síníČlánek DoporučujemeČlánek Chronická žilní insuficience
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
2021 Číslo 5- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Úvodní slovo
- Komentář k článku Post-JIP péče v ambulantním prostředí
- Komentář k článku Post-JIP péče v ambulantním prostředí
- Top 20 výzkumných studií roku 2020 pro lékaře primární péče
- Komentář k článku Top 20 výzkumných studií roku 2020 pro lékaře primární péče
- Komentář k článku Top 20 výzkumných studií roku 2020 pro lékaře primární péče
- Terapie budoucnosti – CAR-T terapie
- Kombinační léčba hypertenze a změny kalemie
- Léčba hypertenze u nemocných s diabetes mellitus
- MUDr. Marie Svatošová: V hospici se dá zažít radost tak intenzivní, že člověku brání usnout
- Indapamid – kardioprotektivní přístup v léčbě hypertenze
- Postavení telmisartanu a candesartanu v léčbě arteriální hypertenze
- Léčba hypertenze v perioperačním období
- Domácí měření krevního tlaku
- 24hodinové ambulantní monitorování krevního tlaku: základní informace
- Jsou nové přístupy k měření krevního tlaku vhodné pro klinickou praxi?
- Diagnostika a léčba hypertenze u mladých lidí
- Erektilní dysfunkce u hypertenze a dalších kardiovaskulárních onemocnění
- Nové evropské registrace
- Hypertenze a fibrilace síní
- Primární hyperaldosteronismus
- Doporučujeme
- Feochromocytom a paragangliom: stručný souhrn pro praxi
- Profil léčivého přípravku Isoprinosine 500 mg tablety
- Chronická žilní insuficience
- Post-JIP péče v ambulantním prostředí
- Léčba nadváhy a obezity – významný nástroj v optimálním managementu diabetu
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Léčba hypertenze v perioperačním období
- Primární hyperaldosteronismus
- Diagnostika a léčba hypertenze u mladých lidí
- Profil léčivého přípravku Isoprinosine 500 mg tablety
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



