-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaInterpretace nejčastějších močových nálezů
Vyšlo v časopise: Svět praktické medicíny, 3, 2022, č. 1, s. 91-96
Kategorie: Medicína v ČR: přehledový článek
Souhrn
Ve srovnání s rychlým rozvojem ostatních laboratorních metod zdánlivě význam vyšetření moči a močového sedimentu ustupuje do pozadí. V řadě klinických situací bylo vyšetřování z moči nahrazeno podstatně jednodušším a přesnějším vyšetřením z krve. Například vyšetřování glykosurie (Benediktova zkouška) již kompletně ztratilo význam po zavedení glukometrů (dnes dokonce často s integrovanou detekcí ketolátek). Monitorace Bence-Jonesovy bílkoviny ve sbírané moči též pozbyla významu vzhledem k možnosti vyšetřovat volné lehké řetězce v séru. Přesto i nadále představuje vyšetření moči rutinní součást základního vyšetření pacienta, neboť může přinést cenné informace k diagnostice, a to i o dosud skrytě probíhajících onemocněních. V ordinaci praktického lékaře je pro tento účel k dispozici velmi jednoduché, rychlé, ekonomicky nenáročné a pro pacienta nikterak zatěžující vyšetření – diagnostickým proužkem (dipstick).
Článek pojednává stručně o přehledu nejběžnějších vyšetření moči a interpretaci jejich výsledků. Podrobněji se věnuje dvěma hlavním nálezům – proteinurii a hematurii.
Vzhled moči
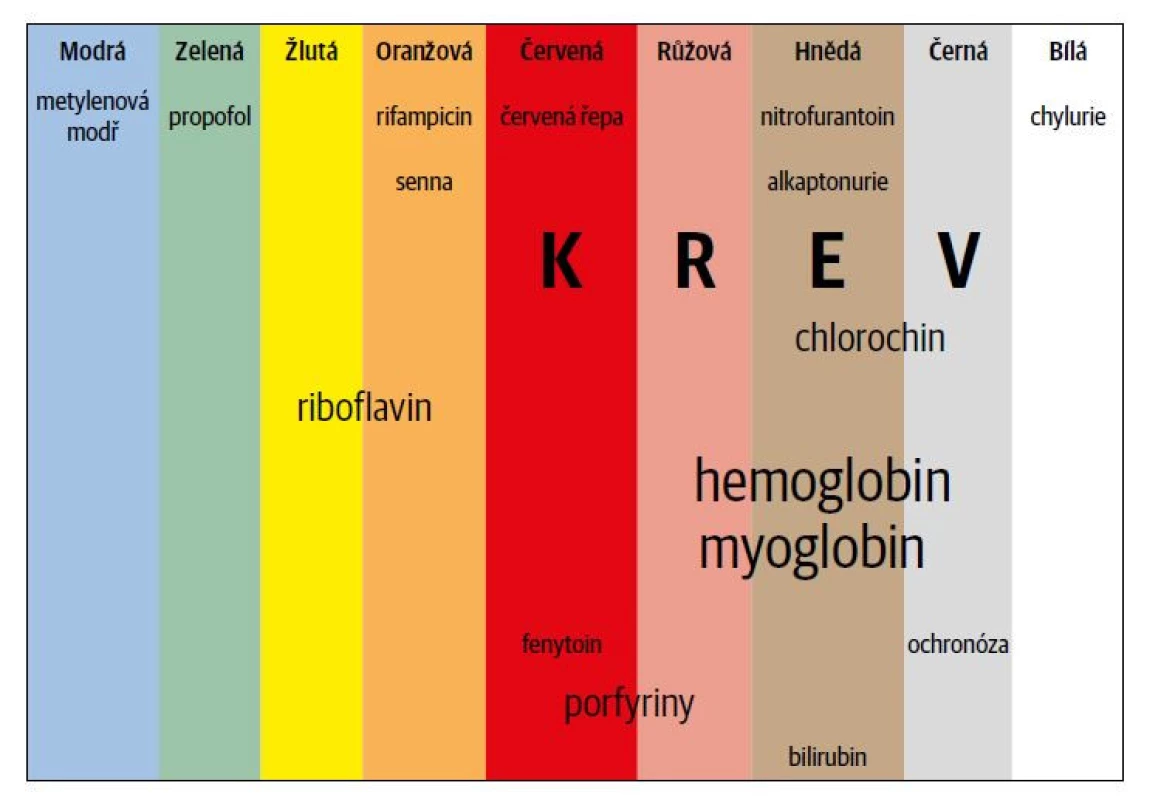
Normální moč je čirá, světle žlutá tekutina. Při delším stání tmavne (oxidací urobilinogenu na urobilin). Barva moči se může měnit po požití některých potravin, léků či v důsledku některých chorobných stavů (Obr. 1). Zákal moči bývá způsoben přítomností velkého množství leukocytů, epiteliálních buněk a bakterií při infekci močového traktu (IMT). Bublinky vzduchu ve zkalené, zapáchající moči budí podezření na vezikokolickou píštěl. Zpěněná moč bývá při velké pro teinurii.
Specifická hmotnost a osmolalita
Specifická hmotnost (norma 1,003–1,035) je poměr hustoty moči a destilované vody a závisí na koncentraci a molekulové hmotnosti rozpuštěných částic v moči. Lze ji vyšetřit orientačně papírkem, přesněji pak urinometrem. Osmolalita (norma 300–900 mmol/kg) se vztahuje pouze ke koncentraci roztoku, resp. je určena především koncentrací Na+, Cl− a urey (pokud není glykosurie). Nelze ji měřit pomocí papírku. Schopnost vylučovat moč o různé osmolalitě je základní mechanismus regulace plazmatické osmolality. Specifická hmotnost a osmolalita spolu korelují s výjimkou přítomnosti větších částic jako například bílkovin či kontrastní látky v moči. V tomto případě roste specifická hmotnost (z důvodu závislosti specifické hmotnosti na molekulové hmotnosti částic) za relativně normální osmolality. Tato vyšetření jsou důležitá především při diagnostice polyurických stavů a hypo/hypernatremií. Dále se v souvislosti s osmolalitou můžeme setkat s pojmem izostenurie, kdy moč má stejnou osmolalitu jako plazma. Izostenurie je typická pro chronickou renální insuficienci, kdy ledviny nedokážou generovat tak široké rozmezí hodnot osmolality moči jako u zdravých osob. Při pokročilé renální insuficienci je osmolalita moči fixována na hodnotě kolem 300 mmol/ kg, a proto při depleci/přetížení sodíkem a vodou není moč adekvátně koncentrovaná/zředěná.
pH moči
pH se v případě moči pohybuje v rozmezí 4,5–8,0, obvykle 5,0–6,0, a závisí na plazmatické hodnotě pH. Většina lidí (kromě veganů) vylučuje trvale kyselou moč. Jednorázové stanovení pH moči nemá příliš velkou informační váhu, ale je velmi důležité při vyšetřování systémové metabolické acidózy, při které by mělo dojít k poklesu pH moči k 5 vzhledem ke zvýšenému vylučování kyselin. Pokud k poklesu nedojde, je důvodné podezření z přítomnosti renální tubulární acidózy. Stanovení pH provádíme orientačně papírkem, při podezření na poruchu tubulárních funkcí se orientujeme podle vyšetření pH metrem, které se provádí v laboratoři.
Ostatní papírkové zkoušky
Leukocytární esterázy a nitrity
Pozitivní nález je indikátorem infekce. Pozitivní leukocytární esterázy prokazují pyurii. Většina močových patogenů je navíc schopna redukovat nitráty na nitrity. Kombinace pozitivity leukocyturie a nitritů má vysokou specificitu pro močovou infekci gramnegativními kmeny, avšak nižší senzitivitu, proto negativní výsledek při suspektní klinice infekci nevylučuje.
Bilirubin, urobilinogen
Přítomnost nekonjugovaného bilirubinu v moči je známkou jaterního onemocnění nebo cholestázy. Negativita urobilinogenu u ikterického nemocného svědčí pro biliární obstrukci.
Glukóza
Průkaz glykosurie papírkem je cenný jen jako nástroj screeningu. Nelze jej použít ke stanovení diagnózy diabetu ani jeho sledování. V posledních letech však nález glykosurie neznamená automaticky dekompenzaci diabetu či renální glykosurii, ale bývá i u pacientů léčených inhibitory SGLT2.
Ketony
Diagnostické proužky semikvantitativně detekují acetoacetát, ale nikoliv β-hydroxybutyrát. Pozitivita může být při diabetické ketoacidóze, delším hladovění, alkoholické ketoacidóze, těžší volumové depleci a některých otravách (rozpouštědla a dezinfekce obsahující izopropylalkohol).
Proteinurie
U zdravého člověka mohou být ztráty proteinů do moči v množství do 150 mg/den. Z toho do 30 mg představuje albumin, zbytek tvoří nízkomolekulární proteiny zahrnující β2-mikroglobulin, imunoglobulin A, enzymy a peptidové hormony. Malá část je představována proteiny vznikajícími v tubulech, především uromodulinem (Tammův-Horsfallův mukoprotein). Patologická proteinurie je definována jako perzistentní exkrece proteinu do moči v množství více než 150 mg/den (Tab. 1). Zjištění patologické proteinurie je důležitou známkou onemocnění ledvin, především glomerulárního poškození, rizikovým faktorem progrese renální insuficience a nezávislým rizikovým faktorem kardiovaskulární morbidity a mortality. Albuminurie, tedy renální exkrece albuminu více než 30 mg/den (ale méně než 300 mg/den), je rovněž senzitivním markerem glomerulárních onemocnění. Albuminurie a proteinurie však nejsou překrývající se pojmy. U některých chorob, obzvláště pak v jejich počátcích (typicky u diabetes mellitus), se může vyskytovat izolovaná albuminurie.
Tab. 1. Proteinurie podle velikosti denní exkrece proteinu 
V zásadě rozlišujeme pět typů proteinurií podle původu:
1. preglomerulární (overflow; při nadprodukci plazmatických LMW bílkovin, nejčastěji při mnohočetném myelomu),
2. glomerulární (selhání glomerulokapilární bariéry, dominuje albumin; při primárních proliferativních i neproliferativních glomerulopatiích, sekundárních glomerulopatiích – např. ANCA asociovaných vaskulitidách a v rámci některých systémových chorob – arteriální hypertenze a diabetes mellitus jako orgánová komplikace, mnohočetný myelom, amyloidózy),
3. tubulární (porucha funkce buněk proximálního tubulu vedoucí k nedostatečné resorpci LMW proteinů; při tubulointersticiálním poškození),
4. postrenální (příměs bílkovin vzniká v dolním močovém traktu; při tumorech močového měchýře, prostatitidě, při hematurii; jedná se o bílkoviny s velkou molekulovou hmotností, které glomerulární stěnou neprochází ani při jejím těžkém poškození),
5. smíšenou (kombinace uvedených typů proteinurií).
Orientačně vyšetřujeme proteinurii diagnostickým proužkem, což je specifické, avšak méně senzitivní vyšetření. Detekován je především albumin na základě svého negativního náboje, ale jiné proteiny nemusí být odhaleny – např. Bence-Jonesova bílkovina nebo tubulární proteinurie. K pozitivní reakci je zapotřebí koncentrace bílkovin minimálně 300 mg/l, resp. menší albuminurie může být prokázána proužky senzitivními speciálně na albumin (30–300 mg/l). K vyšetření je preferována koncentrovaná ranní moč, neboť ve vzorcích ne kon cen trované moči, která vzniká ve velkém objemu, může řada bílkovin uniknout detekci. Pozitivní výsledek z proužku je vhodné doplnit poměrem protein/kreatinin (PCR) nebo albu min/kre ati nin (ACR). Proteinurii lze stanovit jak z jednotlivého vzorku moči, tak z 24hodinového sběru moči. Poměry PCR a ACR se ale výhodně stanovují právě z jednorázového vzorku moči (rovněž nejlépe ranní). Platí, že močová exkrece kreatininu zůstává víceméně konstantní (10 mmol/den) a koriguje případné odchylky při různém stavu hydratace. Hodnoty PCR velmi dobře korelují s výsledky získanými vyšetřením vzorku moči 24hodinového sběru. Platí zhruba, že hodnota PCR vynásobená 10 je rovna dennímu odpadu bílkovin do moči. Hodnota ACR a PCR je podhodnocena u nemocných černé pleti a osob s velkou muskulaturou (zvýšené vylučování kreatininu) a nadhodnocena u starých osob a při kachexii, ale i tak je cenné u těchto nemocných sledovat trend jejich hodnot v čase. Stanovení ACR je velmi důležité u diabetiků, neboť je senzitivnější než PCR, a hodí se tedy ke screeningu této vysoce rizikové skupiny nemocných. Naopak v pokročilých stadiích nemocí s velkou proteinurií si všímáme hlavně PCR. U nemocných s proteinurií je vždy třeba doplnit základní biochemický a hematologický panel, podle okolností doplněný o sérologické a imunologické parametry. Při proteinurii nad 0,5 g/24 h vždy indikujeme nefrologické vyšetření (Obr. 2).
Obr. 2. Algoritmus vyšetření proteinurie. 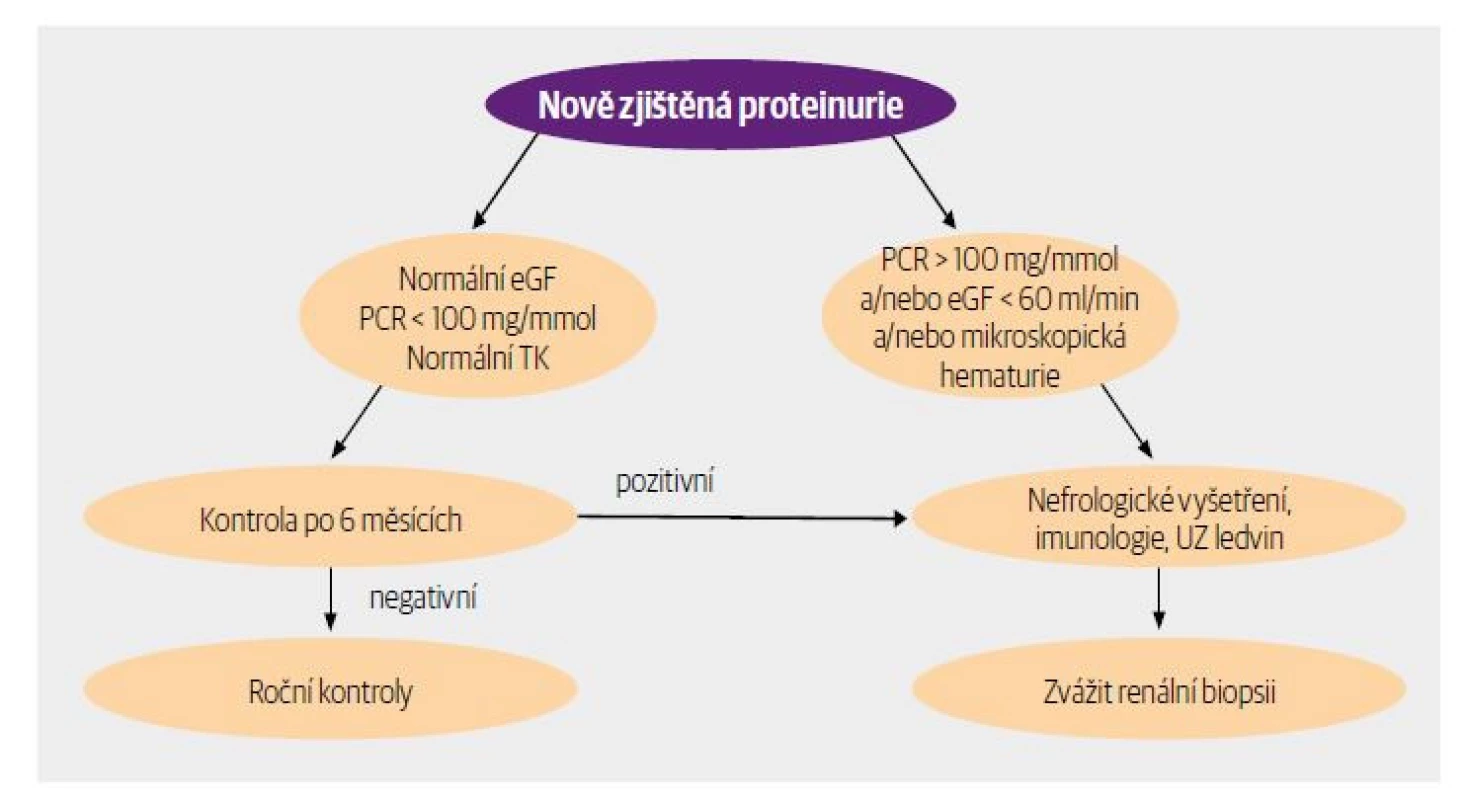
Benigní proteinurie
V určitých situacích může dojít ke zvýšeným ztrátám proteinů do moči, aniž by se jednalo o průvodní jev onemocnění ledvin. Přechodně se tak děje při horečce, v důsledku fyzického cvičení, podchlazení, po křečích, při epilepsii, při kongestivním kardiálním selhání a často v rámci těžkých akutních stavů. Perzistentní proteinurií se vyznačuje posturální (ortostatická) proteinurie, kdy při postavení dochází ke zvýšení exkrece proteinu do moči ve větší míře, než je tomu u zdravých osob, obvykle do 1,0 g/den. Jedná se o vcelku běžný jev vyskytující se u 3–5 % mladých dospělých osob. Ve věku nad 30 let je raritní. Diagnostikuje se ze dvou oddělených sběrů moči – 16 hodin během dne a 8 hodin v noci. Renální funkce je normální, proteinurie většinou v průběhu času vymizí. Příčina není zcela objasněna. Pravděpodobně hraje roli zvýšení glomerulární permeability vzestupem sekrece angiotenzinu II a noradrenalinu po postavení nebo se jako další možnost uvádí i nutcracker syndrom – stlačení renální žíly mezi aortou a arteria mesenterica superior po postavení.
Albuminurie a KV riziko
Albuminurie je kardiovaskulárním rizikovým faktorem nejen u diabetiků a hypertoniků, ale u celé populace. Představuje zvýšené riziko CMP, IM, selhání LKS, ICHDK a smrti (studie HOPE). Podstata vztahu albuminurie a KV rizika není zcela jasná, je však prokázána souvislost společného rozvoje a progrese albuminurie, endoteliální dysfunkce a chronického zánětu. Klíčové je z hlediska redukce albuminurie snížení TK blokádou RAAS inhibitory ACE nebo sartany, omezení NaCl ve stravě a v posledních letech též terapie inhibitory SGLT2.
Hematurie
Hematurie je definována jako přítomnost dvou a více erytrocytů ve vzorku moči na zorné pole mikroskopu, a to minimálně ve dvou nezávislých vzorcích moči. Podle toho, kolik erytrocytů v moči je, rozlišujeme pouhým okem viditelnou makroskopickou hematurii nebo skrytou mikroskopickou hematurii, jejíž průkaz vyžaduje mikroskopické vyšetření. Krvácení do moči může mít původ v jakékoliv části močového traktu od ledvin po ústí uretry. Při makroskopické hematurii nemusí být příměs krve v moči hned jasná, někdy se jedná spíše o změnu barvy dorůžova, vzhledu čaje či kokakoly. Makroskopická i mikroskopická hematurie se může vyskytovat při glomerulárním i neglomerulárním krvácení, ale těžké krvácení s tvorbou koagul téměř nikdy nebývá při glomerulárních onemocněních. Na prvním místě se vždy snažíme vyloučit jednoduché příčiny hematurie, jako je menses, infekce močového traktu, trauma, příměs krve po pohlavním styku nebo nadměrná fyzická námaha. Na dalším místě bychom měli vyloučit neglomerulární příčinu krvácení, a to především u osob starších 40 let, kde je vyšší riziko přítomnosti nádorového onemocnění (nejčastěji močového měchýře a ledvin). Současně provedeme základní náběry (včetně krevního obrazu, urey, kreatininu, koagulace, krevní skupiny podle závažnosti, PSA) a ze zobrazovacích metod CT s kontrastem a bez kontrastu (není-li kontraindikace), cystoskopie (event. ureteroskopie nebo ureterografie). Testační proužky jsou velmi senzitivní a měly by zaznamenat i zmíněné množství 2 ery/zorné pole, avšak při pozitivitě vždy provádíme konfirmaci mikroskopicky, a to proto, že proužek detekuje rovněž hemoglobin z rozpadlých erytrocytů a myoglobin. Při hemoglobinurii při intravaskulární hemolýze nebo myoglobinurii při rabdomyolýze však nenalezneme v mikroskopu erytrocyty. CAVE: Při silném krvácení bývá papírková zkouška pravidelně pozitivní i na protein, interpretace je tím ztížená. Klasická mikroskopie močového sedimentu, která představovala pro laboratoře velkou zátěž, byla nahrazena vyšetřením na principu průtokové cytometrie. Další metodou, umožňující současně posouzení vzhledu erytrocytů, je mikroskopické vyšetření močového sedimentu ve světelném mikroskopu (barvení eosinem) nebo mikroskopu s fázovým kontrastem/v zástinu (ne barví se). Cílem je rozlišení glomerulárního nebo neglomerulárního původu erytrocytů. U neglomerulárního typu erytrocyturie nacházíme tzv. izomorfní erytrocyty, které sice mohou být delším pobytem v moči určitým způsobem de formované (proto u hematurie je k analýze vhodnější jiný než ranní vzorek moči), ale nevykazují změny vzhledu typické pro tzv. dysmorfní erytrocyty (vznikají pasáží přes glomerulární membránu), jejichž přítomnost je pak s vysokou specificitou spojena s glomerulární hematurií. Výhodou těchto vyšetření je možnost hodnotit i jiné elementy v moči, které mohou diagnostiku posunout správným směrem (např. erytrocytární válce u glomerulární hematurie, jiný typ válců, leukocyty, některé mikroorganismy). Nevýhodou je časová náročnost, subjektivita hodnocení a u fázového kontrastu i nutnost speciálního technického vybavení. Navíc průkaz izomorfních erytrocytů sice vylučuje glomerulární původ hematurie, ale nikoliv intrarenální příčinu. Algoritmus vyšetření hematurie je uveden na obrázku 3.
Obr. 3. Algoritmus vyšetření hematurie. 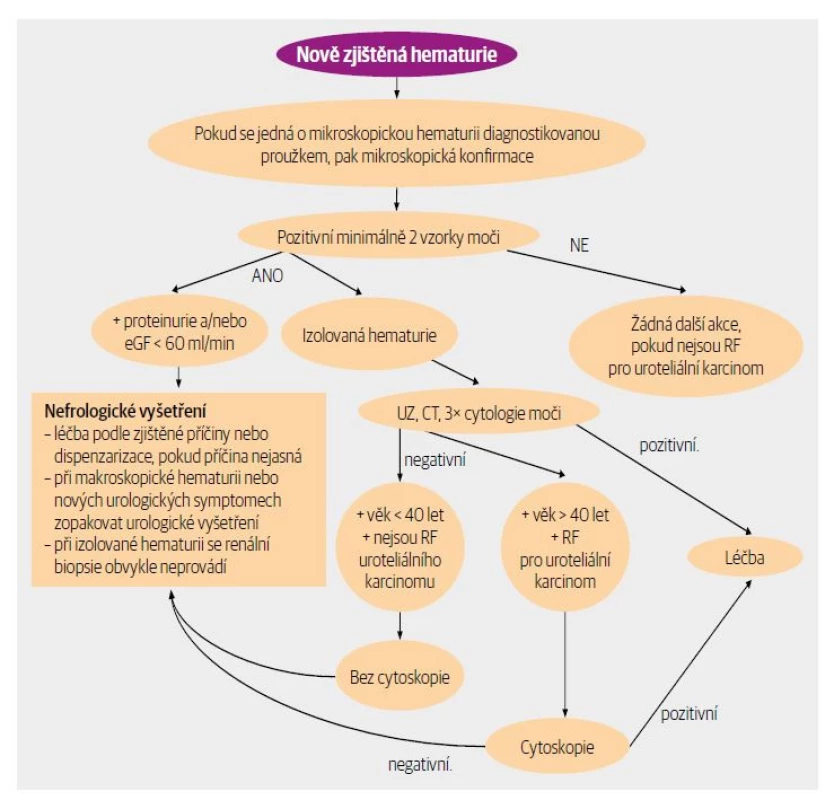
Mikroskopická hematurie
Přítomnost izolované mikroskopické hematurie je spojena s nižším rizikem malignity (2–10 %) než u makroskopické hematurie (5–22 %), ale riziko roste s věkem. Při hodnocení hematurie je třeba vždy pátrat po obecných rizikových faktorech uroteliální malignity: věk nad 40 let, významné krvácení v anamnéze, kouření, abúzus alkoholu, analgetik, iradiace v oblasti pánve, terapie cyklofosfamidem v anamnéze, profesní expozice (např. ropný průmysl, řidiči kamionů, instalatéři, práce s kovy, gumou, v textilním průmyslu). Příčiny izolované mikroskopické hematurie bývají nejčastěji malignita, urolitiáza, infekce močového traktu nebo onemocnění ledvin. V řadě případů se příčina neozřejmí. Mikroskopická hematurie může být přítomna buď trvale (perzistentní), nebo intermitentně. Při důvodném podezření na nádorovou etiologii hematurie se provádí cytologické vyšetření moči, které je samozřejmě doplněno o zobrazovací metody.
Anamnéza u hematurie
Již pečlivý odběr anamnézy může u hematurie významně napomoct ke stanovení správné diagnózy. Obvykle se ptáme následujícím způsobem:
• Jak je krvácení silné?
• Jaký je vzhled moči?
• Recentní trauma (i triviální při sportu)?
• Jsou známy předchozí epizody hematurie?
• Litiáza v anamnéze?
• Medikace? Antikoagulancia nezpůsobují hematurii, pokud jsou správně dávkována.
• Recentní instrumentace na močových cestách?
• Známky infekce močových cest? Bolest (renální kolika, IMT)? Nebolestivá makroskopická hematurie je vždy vysoce suspektní z tumoru.
• Je u žen hematurie cyklická? Při kladné odpovědi myslíme na endometriózu močového traktu.
• Jsou přítomny rizikové faktory uroteliální malignity?
• Recentní angína nebo kožní infekce/spála (poststreptokoková infekce)? Epizodická makroskopická hematurie s předcházející respirační infekcí je klasickou prezentací IgA nefropatie.
• Cestovatelská anamnéza? Schistosomiáza je nejčastější příčinou hematurie celosvětově – koupání v jezeře Malawi.
• Systémové příznaky (artralgie, exantém…)?
• Rodinná anamnéza hluchoty a renálních onemocnění (Alportův syndrom)?
Leukocyturie
Sterilní pyurie je situace, kdy jsou v moči přítomny leukocyty, ale kultivace moči je sterilní. Nejčastěji se vyskytuje při nedoléčené infekci močového traktu, při infekci atypickými patogeny (např. chlamydie, ureaplasma) a tbc, při urolitiáze, prostatitidě, tumoru močového měchýře, nekróze papily, tubulointersticiální nefritidě nebo apendicitidě. K vyloučení tuberkulózy močového traktu zasíláme ke kultivaci tři po sobě následující ranní vzorky moči.
Buňky
Epiteliální buňky pochází většinou z ústí močové trubice nebo jde o kontaminaci kožními či vaginálními buňkami. Může se jednat také o uroteliální buňky, nejčastěji při cystitidě.
Mikroorganismy
Současná přítomnost leukocytů a bakterií svědčí pro infekci. Mikroskopické vyšetření spolu s kultivací a citlivostí určí, zda se jedná o skutečnou infekci, nebo kontaminaci. Diagnostickým kritériem je pak průkaz více než 105 CFU/ml moči. Na tomto místě je nutné zmínit pojem asymptomatická bakteriurie, která znamená kultivační záchyt signifikantního množství bakterií (105 a více CFU/ml) ve dvou po sobě jdoucích vzorcích moči odebraných s minimálním odstupem 24 hodin u žen bez symptomů IMT. U mužů stačí průkaz signifikantní bakteriurie v jediném vzorku moči. Jedná se o běžný jev u žen, u mužů je vzácná. Zjištění asymptomatické bakteriurie má zásadní význam v těhotenství a před instrumentačními výkony na močovém traktu, při kterých může dojít ke slizničnímu poranění a následně již manifestní infekci včetně bakteriemie. Pouze v těchto dvou situacích je doporučeno nasazení léčby. Neléčit asymptomatickou bakteriurii je zásadní pravidlo z hlediska prevence nárůstu bakteriální rezistence vůči antibiotikům.
Z hub se v moči nejčastěji objevuje Candida, a to hlavně u predisponovaných jedinců s DM, imunosupresivní léčbou, po antibiotické léčbě nebo s cizími tělesy v močových cestách (PMK, stenty). Často se ale jedná o kontaminaci z genitálu. Stejně tak se může v moči ocitnout trichomonáda.
Válce
Přítomnost některých válců v moči může být cenným vodítkem k diagnostice onemocnění ledvin (např. erytrocytární při glomerulonefritidě nebo leukocytární při akutní pyelonefritidě). Za normálních okolností se mohou v moči nalézat válce z Tammova-Horsfallova proteinu nebo hyalinní válce v koncentrované moči.
Krystaly
Nález většiny krystalů v moči není klinicky relevantní. Urátové krystaly bývají v malém množství přítomny v moči normálně (vypovídají o značné konzumaci masa). Velké množství jich pak nacházíme při hyperurikosurii (nejvíce u akutní urátové nefropatie při tumor lysis syndromu). Kalciumoxalátové krystaly jsou rovněž v malém množství normální (např. po čokoládě nebo špenátu), patologicky při hyperkalciurii nebo hyperoxalurii. Diagnostické jsou při otravě etylenglykolem. Kalciumfosfátové krystaly jsou rizikovým faktorem pro tvorbu litiázy. Triplefosfát nalézáme při proteové infekci. Největší klinický význam má nález cystinových hexagonálních krystalů, které se v normální moči nevyskytují nikdy. Svědčí pro cystinurii.
Zajímavosti
Uromodulin
Dlouhou dobu se předpokládalo, že Tammův-Horsfallův protein (uromodulin) nemá v organismu žádnou významnější funkci a je spíše odpadním produktem. Nedávné studie však prokázaly, že se jedná o multifunkční protein hrající roli v udržování homeostázy moči a sloužící jako mediátor meziorgánové signalizace. Moduluje aktivitu ledvinových iontových kanálů, podílí se na rovnováze vody a soli, renální a systémové zánětlivé odpovědi, mezitubulární komunikaci, krystalizaci minerálů a bakteriální adhezi. Mutace uromodulinu a jeho následná pozměněná exprese je spojena se zvýšeným rizikem infekcí močového traktu, vzniku urolitiázy, hypertenze, hyperurikemie a akutních i chronických onemocnění ledvin. Není však ještě jasné, jaké zevní a vnitřní faktory uromodulin regulují, jak přesně jeho nedostatek vede k výše uvedeným patologickým stavům a v jakých klinických situacích jej lze využít jako biomarker nebo cíl ke zlepšení výsledků léčby.
Riziko závažného průběhu COVID-19 – význam močového nálezu ve stratifikaci rizika fatálního průběhu
Podle výsledku analýzy moči (anurie, osmolalita, leukocyturie, hematurie, albuminurie) a hodnoty sérového albuminu a antitrombinu III lze v rané fázi SARS-CoV-2 identifikovat rizikové pacienty. Tato jednoduchá vyšetření umožňují posoudit, zda se stav nemocného zhoršuje, lze očekávat těžký průběh onemocnění nebo zda bude nutná intenzivní péče. Postižení ledvin při onemocnění COVID-19 je spojeno s 10× větší mortalitou než u nemocných bez postižení ledvin. Vyšetření moči při přijetí do nemocnice je tedy z tohoto pohledu velmi důležité. V německé prospektivní, multicentrické, kohortové studii bylo zkoumáno, zda lze na základě určitých hodnot moči identifikovat vysoce rizikové pacienty se závažným průběhem COVID-19. Jednalo se o pacienty průměrného věku 60–66 let, s BMI průměrně kolem 27. Tři čtvrtiny nemocných měly chronické onemocnění (kardiovaskulární, plicní nebo ledvinové). Pacienti byli rozřazeni do tří skupin: nízké riziko (normální nález v krvi a moči), střední riziko (abnormální nález v moči, normální hodnoty v krvi) a vysoké riziko (abnormální moč a sérový albumin pod 20 g/l a/nebo aktivita antitrombinu III pod 70 %). Abnormální nález v moči byl definován jako anurie nebo alespoň dvakrát nález patologické osmolality nebo specifické hmotnosti, leukocyturie, hematurie nebo albuminurie/proteinurie. Vyšetření byla provedena v den přijetí do nemocnice. Primárním cílovým parametrem studie bylo přijetí na lůžko JIP nebo úmrtí. Celkem bylo zařazeno 145 pacientů, 43 mělo nízké riziko, 84 střední a 18 vysoké. Abnormální močový nález byl spojen s vyšším rizikem potřeby intenzivní péče nebo úmrtí (63,7 % oproti 27,9 %), ve vysoce rizikové skupině dokonce 100 %. Nemocní s patologickým močovým nálezem museli být častěji ventilovaní (44 % versus 14 %), častěji vyžadovali ECMO (10,8 % versus 2,3 %) nebo náhradu funkce ledvin (30,7 % versus 11 %).
Závěr
Současná doba nabízející technicky velmi pokročilá zobrazovací vyšetření staví analýzu moči do pozice zastaralých metod. Pravda je však taková, že se často jedná o vyšetření velmi jednoduchá a levná, ze kterých lze vytěžit mnoho cenných informací. Navíc odběr a následný rozbor moči nejsou pro pacienta nijak zatěžující. Některá onemocnění ledvin lze v počátcích zachytit jen z vyšetření moči a jejich včasná diagnostika a léčba může selhání ledvin odvrátit či alespoň oddálit. Vyšetření moči bychom tedy rozhodně měli chápat jako nedílnou součást fyzikálního vyšetření.
Přehled použitých zkratek:
• ACE – angiotenzin konvertující enzym
• ACR – albumin/creatinine ratio
• ANCA – anti-neutrophil cytoplasmic antibody
• CFU – colony forming unit
• CMP – cévní mozková příhoda
• CT – computed tomography, počítačová tomografie
• DM – diabetes mellitus
• ECMO – extrakorporální membránová oxygenace
• eGF – estimated glomerular filtration
• ICHDK – ischemická choroba dolních končetin
• IM – infarkt myokardu
• IMT – infekce močového traktu
• KV – kardiovaskulární
• LKS – levá komora srdeční
• LMW – low molecular weight
• PCR – protein/creatinine ratio
• PMK – permanentní močový katétr
• PSA – prostatický specifický antigen
• RAAS – renin-angiotenzin-aldosteronový systém
• RF – rizikové faktory
• SGLT2 – sodíko-glukózový kotransportér 2
• tbc – tuberkulóza
• TK – krevní tlak
• UZ – ultrazvuk
MUDr. Marie Vanková
Interní oddělení, Klatovská nemocnice a.s.
MUDr. Adéla Maříková
Hemodialýza, Klatovská nemocnice a.s.
Zdroje
1. Higashihara E, Nishiyama T, Horie S, et al. Hematuria: definition and screening test methods. Int J Urol 2008;15(4):281–4. [Medline].
2. Quigley R. Evaluation of hematuria and proteinuria: how should a pediatrician proceed? Curr Opin Pediatr 2008;20(2):140–4. [Medline].
3. Kalia A, Travis LB, Brouhard BH. The association of idiopathic hypercalciuria and asymptomatic gross hematuria in children. J Pediatr 1981;99(5):716–9. [Medline].
4. Samuel S, Bitzan M, Zappitelli M, et al. Canadian Society of Nephrology Commentary on the 2012 KDIGO clinical practice guideline for glomerulonephritis: management of nephrotic syndrome in children. Am J Kidney Dis 2014;63(3):354–62. [Medline].
5. Kashtan CE. Familial hematuria. Pediatr Nephrol 2009;24(10):1951–8. [Medline].
6. Expert Panel on Pediatric Imaging; Dillman JR, Rigsby CK, Iyer RS, Alazraki AL, Anupindi SA, et al. ACR Appropriateness Criteria® Hematuria-Child. J Am Coll Radiol 2018;15(5S): S91–S103. [Medline].
7. Feld LG, Stapleton FB, Duffy L. Renal biopsy in children with asymptomatic hematuria or proteinuria: survey of pediatric nephrologists. Pediatr Nephrol 1993;7(4):441–3. [Medline].
8. D’Amico G. The commonest glomerulonephritis in the world: IgA nephropathy. Q J Med 1987;64(245):709–27. [Medline].
9. Diven SC, Travis LB. A practical primary care approach to hematuria in children. Pediatr Nephrol 2000;14(1):65–72. [Medline].
10. Levey AS, Becker C, Inker LA. Glomerular filtration rate and albuminuria for detection and staging of acute and chronic kidney disease in adults: a systematic review. JAMA 2015;313(8):837–46. [Medline].
11. Springberg PD, Garrett LE Jr, Thompson AL Jr. Fixed and reproducible orthostatic proteinuria: results of a 20-year follow-up study. Ann Intern Med 1982;97(4):516–9. [Medline].
12. Uehara K, Tominaga N, Shibagaki Y. Adult orthostatic proteinuria. Clin Kidney J 2014;7(3):327–8. [Medline]. [Full Text].
13. Naderi AS, Reilly RF. Primary care approach to proteinuria. J Am Board Fam Med 2008;21(6):569–74. [Medline].
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé Onkologie Pneumologie a ftizeologie Radioterapie Urologie
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
2022 Číslo 1- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Úvodní slovo
- Pomáháme váhavým pacientům činit zdravá rozhodnutí o COVID-19
- Komentář k článku Pomáháme váhavým pacientům činit zdravá rozhodnutí o COVID-19
- Komentář k článku Pomáháme váhavým pacientům činit zdravá rozhodnutí o COVID-19
- Diagnóza prediabetu: prospěšná, nebo problematická?
- Komentář k článku Diagnóza prediabetu: prospěšná, nebo problematická?
- Diabetes mellitus a pandemie COVID-19
- Horší prognóza a vyšší úmrtnost u špatně kompenzovaných pacientů s diabetem v době pandemie COVID-19
- Má stoletý stařík inzulin budoucnost?
- Zjednodušení intenzifikované léčby biosimilárním inzulinem u starších pacientů
- Využití intermitentně skenované kontinuální monitorace glukózy v ambulantní praxi
- Hybridní systémy v léčbě a kontrole diabetu v období pandemie
- Využití empagliflozinu u kardiorenálního syndromu
- Inhibitory SGLT2 a chronické onemocnění ledvin
- Novější antidiabetika z pohledu nefrologa: zaměřeno na dapagliflozin
- Docentka Alena Šmahelová: Zhoršení kompenzace jde velmi často na konto toho, že ji pacient psychicky a mentálně nezvládá
- Dulaglutid v léčbě obézních diabetiků 2. typu
- Ambulantní předoperační příprava diabetika
- Dyslipidemie a diabetes
- Léčba obezity liraglutidem – praktické zkušenosti
- Používání přípravku Saxenda je u pacientů s tyreopatií bezpečné
- Diabetes a značení potravin Nutri-Score
- Terapie budoucnosti – mRNA technologie nejen jako prevence proti infekčním nemocem
- Lékový profil: Ryaltris
- Nové registrace na evropském poli
- Interpretace nejčastějších močových nálezů
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Lékový profil: Ryaltris
- Interpretace nejčastějších močových nálezů
- Používání přípravku Saxenda je u pacientů s tyreopatií bezpečné
- Léčba obezity liraglutidem – praktické zkušenosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání