-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Tuberkulózní ileokolitida – popis případu
Tuberculous ileocolitis – a case report
Tuberculous ileocolitis is quite a rare disease in our country, which usually presents secondary to pulmonary tuberculosis. We present a case of an 80-year-old patient who was examined for weight loss and anaemia. The endoscopic finding of granulomatous infection of the terminal ileum led to the diagnosis of pulmonary tuberculosis.
Key words:
Crohn's disease – tuberculosis
Autoři: M. Kovaříková
Působiště autorů: Gastroenterologická ambulance interního oddělení, Svitavská nemocnice, Svitavy
Vyšlo v časopise: Gastroent Hepatol 2014; 68(1): 36-38
Kategorie: IBD: kazuistika
Souhrn
Tuberkulózní ileokolitida je u nás vzácné onemocnění, které se vyskytuje převážně sekundárně při tuberkulóze plic. Uvádíme případ 80leté pacientky, která byla došetřována pro váhový úbytek a anemii. Nález granulomatózního zánětu terminálního ilea a tračníku byl vodítkem ke stanovení diagnózy tuberkulózy plic.
Klíčová slova:
Crohnova choroba – tuberkulózaTuberkulóza (TBC) je specifické infekční onemocnění vyvolané obligátně patogenními mykobakteriemi Mycobakterium tuberculosis komplex, kam řadíme např. M. tuberculosis, M. bovis a M. africanum. Je v současnosti druhou nejčastěji smrtící infekční chorobou světa hned po AIDS. Dle údajů WHO bylo v roce 2012 hlášeno 8,6 milionu nových případů TBC. Nejvíce zasaženy jsou oblasti jihovýchodní Asie a západního Pacifiku (58 % hlášených), dále pak Afrika, Indie a Čína. 1,3 milionu nemocných na TBC zemřelo, nejvyšší počet úmrtí je hlášen v africkém regionu. Celosvětově mají incidence i mortalita klesající tendenci [1].
Podle dat z Registru TBC v ČR se v roce 2012 vyskytlo 611 případů onemocnění (tj. 5,8 případu na 100 tis. obyvatel), 402 u mužů a 209 u žen, 22 lidí na TBC zemřelo. Nejčastější formou onemocnění byla TBC dýchacího ústrojí, v 59 případech šlo o TBC jiné lokalizace (periferní lymfadenopatie, TBC kostí a kloubů, kůže, močové a pohlavní soustavy i jiných orgánů). Nejvíce onemocnění bylo ve věkové kategorii nad 75 let. ČR patří k zemím s nízkým výskytem této nemoci [2].
Popis případu
Osmdesátiletá hypertonička, nekuřačka, byla přijata na interní oddělení pro váhový úbytek 20 kg za posledních šest měsíců, progredující nechutenství bez GIT symptomatologie a kašel. Ve fyzikálním nálezu dominoval astenický habitus – BMI 18, jinak bez významných odchylek. Laboratorně zjištěna anémie (Hb 100 g/l, MCV 76 fl, ferritin 200 ng/ml, Fe 3 umol/l), počet trombocytů 550 × 109/l, CRP 200 mg/l, albumin 33 g/l. Pátrali jsme tedy po zdroji infekce, v dif. dg po nádorovém onemocnění. Na RTG plic bylo vysloveno podezření na nádor pravého plicního hilu (obr. 1), na doplněném CT plic s podáním kontrastní látky a HRCT nález nesvědčil pro nádorový původ léze, ale byl charakteristický pro akutní zánětlivou intersticiální lézi. Sono břicha neukázalo patologii. Při gastroskopii byl nalezen peptický vřed bulbu duodena Forrest III na přední stěně velikosti 10 × 15 mm, nález v sestupném raménku duodena byl ve fyziologických mezích, vyšetření na Helicobacter pylori (rychlý ureázový test a histologické vyšetření z biopsie sliznice antra a žaludečního těla) bylo negativní. Byl nasazen omeprazol. Vzhledem k celkovému stavu pacientky, nálezu na HRCT plic i při nepřítomnosti patogenů ve sputu při standardním bakteriologickém vyšetření jsme zahájili podávání antibiotik (cefotaxim i.v. + klaritromycin per os). Nedobrý nutriční stav nemocné jsme se snažili upravit zavedením enterální výživy formou sippingu. Hospitalizace trvala čtyři týdny, CRP kleslo na 58 mg/l, kašel se zmírnil, pacientka afebrilní, nechutenství přetrvávalo s dalším váhovým úbytkem. Anorexie byla částečně přisuzována depresivnímu ladění pacientky a prodělanému respiračnímu infektu. Pacientka byla propuštěna a objednána k rehospitalizaci s dalším došetřením (kolonoskopie, kontrolní gastroskopie a snímek plic). Po měsíci domácí péče se laboratorní nálezy nijak nezlepšily (Hb 95g/l, MCV 75 fl, trombocyty 550 × 109, albumin 30g/l, CRP 80 mg/l) a došlo k dalšímu váhovému úbytku 2 kg. Endoskopicky duodenální vřed vyhojen, na kontrolním snímku plic rentgenolog opět popsal suspektní tumor pravého plicního hilu. Zajímavý výsledek přinesla kolonoskopie, kde byly nalezeny plošné vředové léze terminálního ilea s nepravidelnými okraji, droboučké eroze a malé ulcerace v tračníku (obr. 2). Jejich etiologie nám nebyla jasná. Dif. dg. jsme zvažovali NSA kolopatii (pacientka užívání NSA popírala) a Crohnovu chorobu. Překvapivý pro nás byl závěr patologa ze střevní biopsie, který zněl: histologický nález svědčí pro Crohnovu chorobu, nelze vyloučit ani specifickou ileitidu při eventuální tuberkulóze střev (obr. 3).
Obr. 1. RTG obraz infiltrace vpravo ve středním plicním poli s vytažením a zvětšením pravého hilu. Fig. 1. Chest X-ray image of infiltration of the right pulmonary mid-lobe with shift and enlargement of the right hilus. 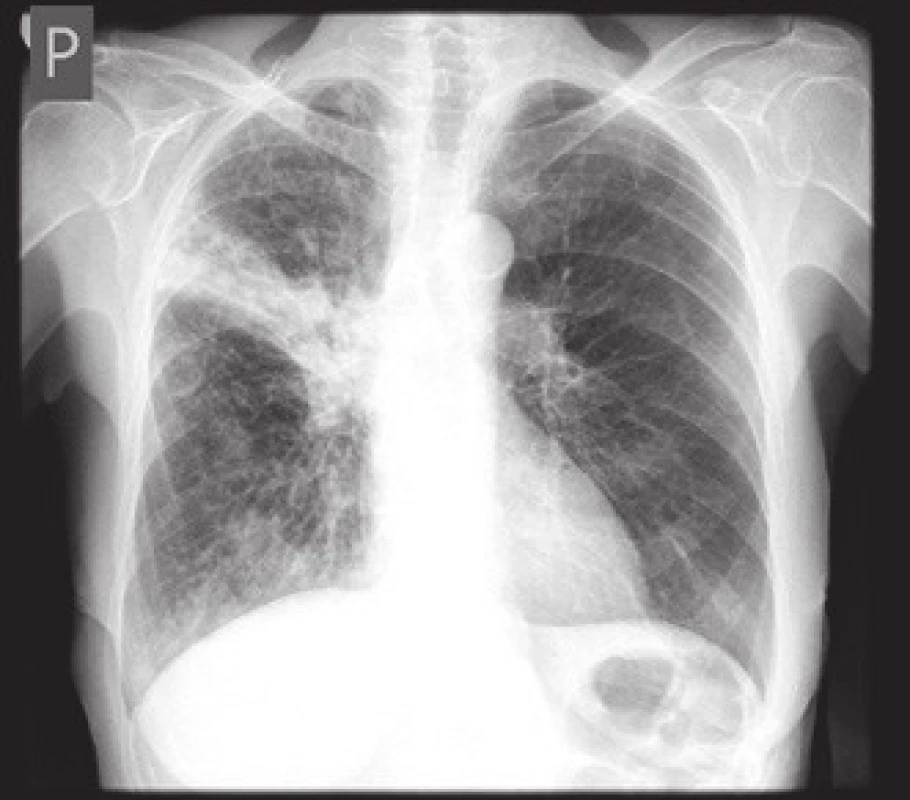
Obr. 2. Endoskopický obraz: A – vřed terminálního ilea, B – vřed v tračníku. Fig. 2. Endoscopic images: A – ulcer of terminal ileum, B – ulcer of colon. 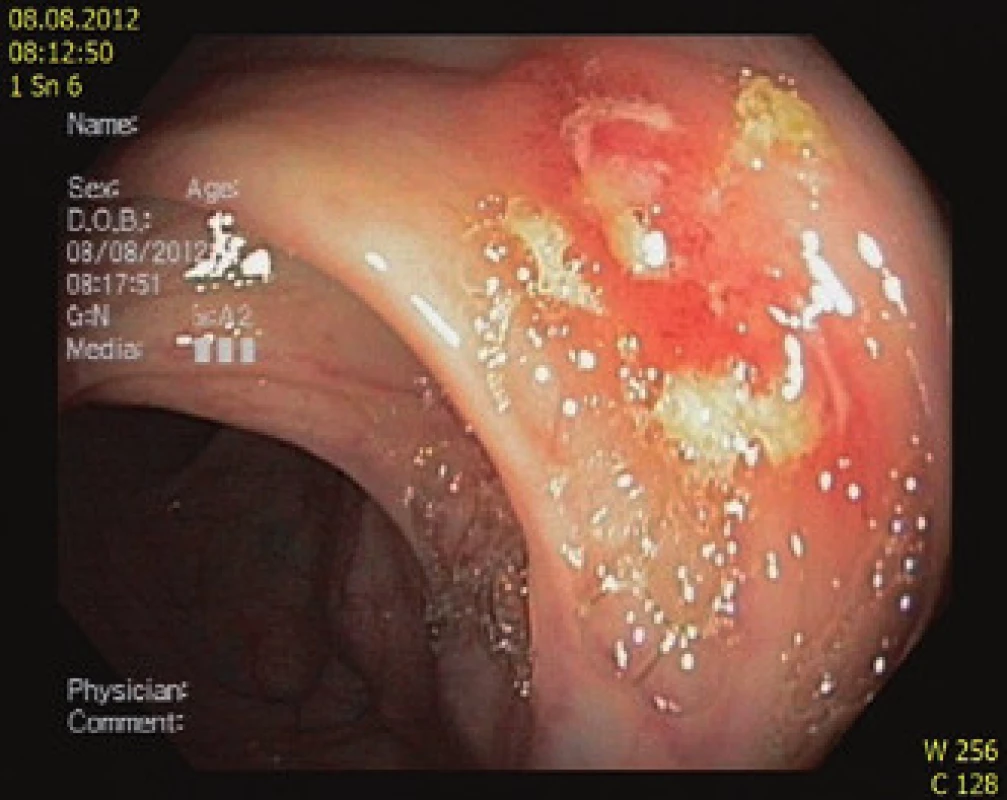
Obr. 3. Histologický obraz krypt sliznice tlustého střeva, pod kterými je patrný granulom složený z epiteloidních buněk a mnohojaderných histiocytů. Kaseózní nekróza zachycena není (barvení hematoxylin-eozin, Patologie Litomyšl s. r. o.). Fig. 3. Histological image of the colon mucomembranous crypts, with granuloma containing epitheliolid cells and multinucleated histiocytes. Caseous necrosis is not present (hematoxylin- -eosin staining, Department of Pathology, Litomysl s. r. o.). 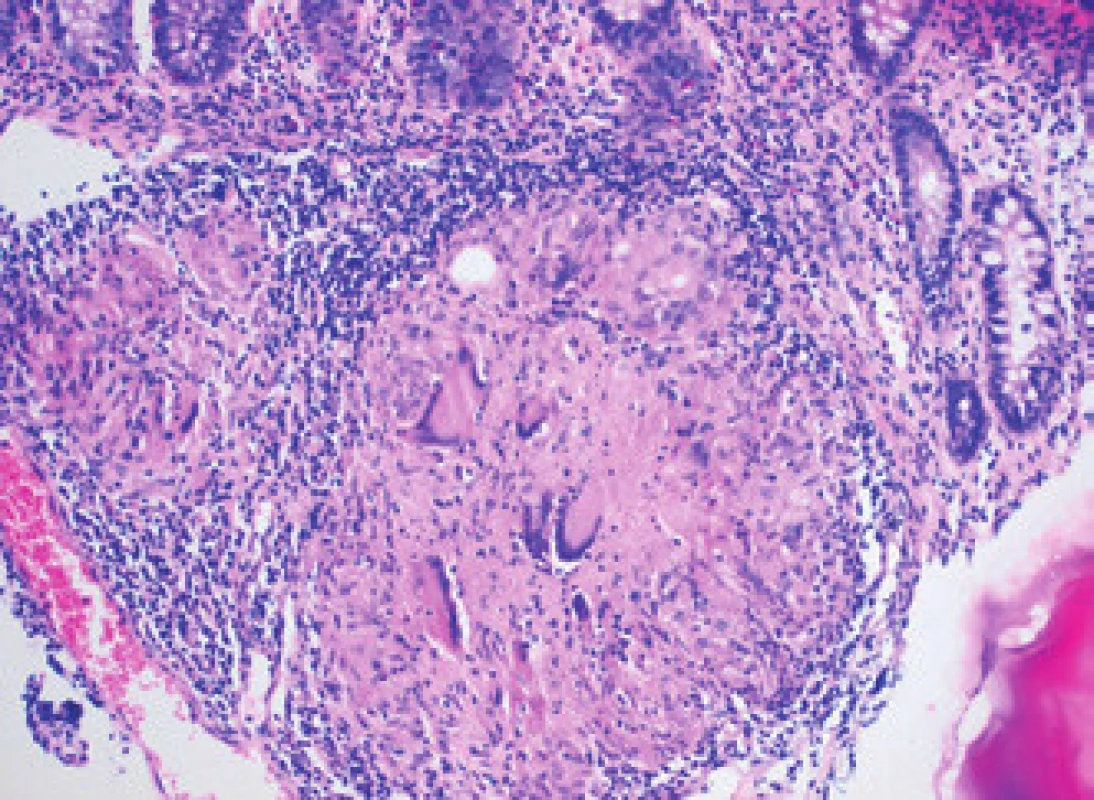
Vzhledem k těmto skutečnostem a přetrvávajícímu patologickému nálezu na snímku plic se nám jevila nejpravděpodobnější možnost sekun-dární TBC ileitidy. Pacientka podstou-pila bronchoskopické vyšetření, kde byla potvrzena mikroskopická pozitivita BK +++, tedy potvrzena TBC plic, následovala antituberkulózní léčba trojkombinací izoniazid, etambutol, rifampicin. Doplněna byla tato vyšetření: Mantoux II test negativní, QuantiFERON GOLD 1,43 IU ml – pozitivní. Z endobiotických vzorků bronchiální sliznice byly popsány epiteloidní granulomy s kaseózní nekrózou. Kultivačně z výplachu z bronchů byla prokázána M. TBC citlivá na běžná antituberkulotika. AT trojkombinace byla ponechána tři měsíce, dále pak pokračováno čtyři měsíce dvojkombinací izoniazid a rifampicin. Léčba byla efektivní. Došlo kompletně k normalizaci laboratorního nálezu (CRP, KO v normě), pacientka přibrala na váze 8 kg od ukončení léčby antituberkulotiky a je spokojená. Kontrolní kolonoskopii odmítla, doplnili jsme proto kalprotektin ve stolici, který je v normě, což svědčí proti zánětlivému střevnímu onemocnění.
Diskuze
Nález granulomatózního zánětu terminálního ilea a tračníku jsme hodnotili jako sekundární TBC střev při protrahované a neléčené TBC plic. Acidorezistentní tyčinky v biopsii střeva prokázány nebyly, ale mikroskopický průkaz je metoda méně citlivá, vyžadující přítomnost většího množství mykobakterií. V postižených orgánech u mimoplicní TBC jich bývá nízký počet, obvykle je nutné odběry i několikrát opakovat. Vzorek je třeba uchovat ve sterilní zkumavce bez fixačních prostředků, my jsme vzorek odeslali patologovi standardně ve formalinu. V rámci dif. dg. jsme zvažovali Yersiniovou ileokolitidu (granulomy yersiniové jsou typicky nekaseózní často s nápadným lymfoidním lemem) [3], přítomnost protilátek proti Yersiniím ve třídě IgG i IgM jsme neprokázali. Crohnova choroba se nám jevila nepravděpodobná vzhledem k věku pacientky a atypickému charakteru vředových lézí. S přihlédnutím k tomu, že po antituberkulózní léčbě došlo u pacientky k normalizaci laboratorního nálezu, k váhovému přírustku 8 kg a vzhledem k tomu, že léčba GIT TBC se nijak neliší od léčby plicní TBC, jsme další průkaz nepovažovali za nutný.
TBC trávicího ústrojí je v současnosti v ČR vzácnou formou mimoplicní tuberkulózy. V minulosti byla u nás častá primární TBC způsobená pitím syrového kontaminovaného mléka hlavně v dětském věku (infekce dobytka M. Bovis) [4], ta stále zůstává problémem v rozvojových zemích [5]. Dnes se můžeme setkat spíše se sekundární TBC trávicího ústrojí jako komplikací plicní formy, kdy se infekce šíří buď polknutím infikovaného sputa, nebo hematogenní cestou. A nemusí vždy provázet jen destruující a vleklé plicní procesy, ale i nenápadné či latentní formy (RTG plic může být normální) [6]. Vzácně může vzniknout i z mimoplicní TBC [4,5]. Nejčastěji je postižena oblast ileocekální pro nadbytek lymfatické tkáně v distálním ileu, dále oblast jejunoileální a c. ascendens. Ostatní lokalizace jsou velmi vzácné. TBC rektosigmoideální bývá sdružená s ileocekální lokalizací, má sklon k tvorbě píštělí, periproktálních infiltrátů a abscesů [7]. Izolované postižení rekta může imitovat malignitu [8]. Ezofageální TBC se projevuje hlavně dysfagií, může vznikat per continuitatem kolikvováním a provalením tracheobronchiálních uzlin. TBC žaludku provází tvorba obvykle prepylorických vředů, jizvení může být příčinou pylorostenózy [9]. Současně bývají postiženy spádové lymfatické uzliny, jejichž kolikvací může dojít k šíření infekce na pobřišnici, vzniku srůstů a poruch pasáže [7].
Klinické příznaky střevní TBC jsou nespecifické, zahrnují meteorizmus, bolesti břicha, průjem, hmatnou rezistenci v oblasti pravého podbřišku, může dojít ke krvácení i k perforaci střeva. Dále bývají přítomny celkové příznaky jako zvýšená teplota, slabost, noční pocení či váhový úbytek [4,7].
Charakteristickým endoskopickým znakem TBC trávicího ústrojí je slizniční vřed, který vzniká z postižení lymfatické tkáně, exsudací, kaseifikací, kolikvací a provalením ložiska do střevního lumen. Má typické nepravidelné okraje, na spodině vředu je obvykle patrná nespecifická zánětlivá reakce způsobená bakteriemi z GIT, hlouběji ve stěně vředu až při seróze jsou typické tuberkuly s kaseózní nekrózou. TBC vředy jsou typicky příčně uložené a šíří se kruhovitě po sliznici podél lymfatických cév (dlouhá osa vředu je kolmá na dlouhou osu střeva na rozdíl od vředu u Crohnovy nemoci, které jsou obvykle lokalizovány v podélné ose střeva) [7]. Sekundární TBC střev může také vypadat jako slizniční infiltrát, infiltrativní změny mohou postihovat celou střevní stěnu. Pokud se ke specifické granulační tkáni přidruží fibrogeneze, vzniká často hyperplastická forma v okolí Bahinské chlopně. Jizevnatými změnami a srůsty se střevními kličkami se pak vytváří tumorózní forma TBC [7]. Typickým histologickým nálezem je granulom s kaseózní nekrózou, ale může být i nekaseózní, s přítomností obrovských mnohojaderných Langhansových buněk submukózně, s lemem lymfocytů, může být i s kalcifikací [5,7].
Diagnóza TBC se opírá o anamnézu, klinické projevy, zobrazovací a laboratorní vyšetření. Vyžadován je mikrobiologický průkaz patogenu. Rychlou, ale nejméně citlivou metodou je mikroskopický průkaz mykobakterií v odebraném biologickém materiálu, který přináší výsledek prakticky okamžitě. Kultivace je 1 000× citlivější, umožní určit typ mykobakteria a citlivost k antituberkulotikům, ale trvá týdny [3,6,9,10]. Další možností jsou pak molekulárně genetické metody jako PCR, které mají výhodu v rychlosti i ve vysoké senzitivitě, prokazuje ale DNA i mrtvých mykobakterií, což může činit problém při interprentaci výsledku. Doplňkovým vyšetřením je Quantiferon – TB Gold, kdy lymfocyty u jedinců infikovaných M. tuberkulosis complex po stimulaci produkují a secernují cytokin interferon-gama, který se kvantifikuje metodou ELISA. Pozitivita testu podporuje diagnostiku latentní, nikoli aktivní TBC, kterou však nevylučuje [8,10]. Zobrazovacími metodami, např. ultrasonograficky nebo výpočetní tomografií, může být popsáno zesílení mezenteria na více než 15 mm se zvýšenou echogenitou, mezenteriální lymfadenopatií a prosáknutí střevní stěny [11].
Autorka deklaruje, že v souvislosti s předmětem studie nemá žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 10. 1. 2014
Přijato: 27. 1. 2014
MUDr. Martina Kovaříková
Gastroenterologická ambulance
Svitavská nemocnice a. s.
Kollárova 7, 568 02 Svitavy
kovamarti@seznam.cz
Zdroje
1. World Health Organization. Global Tuberculosis report 2013. Available from: http://www.who.int/tb/publications/global_report/en/index.html.
2. ÚZIS ČR. Tuberkulóza a respirační nemoci 2012. [online]. Dostupné z: http://www.uzis.cz/publikace/tuberku-loza-respiracni-nemoci-2012.
3. Kolek V. Tuberkulóza. In: Kolek V, Kašák V, Vašáková M. Pneumologie. 1. vyd. Praha: Maxdorf 2011 : 211–217.
4. Bursík K, Dobrota Š. Mimopľucna lokalizácia tuberkulózy. In: Virsík K, Dobrota Š a kol. Choroby dýchacího ústrojenstva II. 2.vyd. Bratislava: Vydavateľstvo Slovenskej akademie vied 1966 : 494–498.
5. Robins and Cotran. Infectious diseases. In: Robins and Cotran. Pathologic Basis of Disease. 7. ed. Saunders 2005 : 381–386.
6. Lukáš K, Dvořák K, Novotný A et al. Diferenciální diagnostika onemocnění ilea. Čas Lék Čes 2013; 152(1): 4–14.
7. Odze RD, Goldblum J, Crawford JM. Infectious diseases of the GI tract. In: Odze RD, Goldblum J, Crawford JM. Surgical pathology of the GI tract, liver, biliary tract and pancreas. 9. ed. Saunders 2004 : 39–40.
8. Houšková E, Koskuba J, Horová N. „Tumor rekta“ jako projev mimoplicní TBC. Interní Med 2009; 11(9): 418–421.
9. Bajan A. Tuberkulóza. 1. vyd. Martin: Osveta 1990 : 99–100.
10. Votava V, Homolka J. Tuberkulóza. 2. ed. Praha: Karolinum 1996 : 28–33.
11. Anand MK. Gastrointestinal Tuberculosis Imaging. Medscape 2013. Available from: http://emedicine.medscape.com/article/376015.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2014 Číslo 1- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Fekální kalgranulin C u nemocných s idiopatickými střevními záněty
- Infliximab nezvyšuje riziko časných pooperačních komplikací po trojdobé restorativní proktokolektomii s ileoanálním J-pouchem u nemocných s ulcerózní kolitidou
- Potenciálne škodlivá expozícia radiačnému žiareniu u pacientov s nešpecifickými zápalovými ochoreniami liečenými biologickou liečbou
- Idiopatický střevní zánět u pacientů s primární sklerozující cholangitidou – samostatný fenotyp IBD
- Tuberkulózní ileokolitida – popis případu
- Leading Change in IBD 2014 – konference zaměřená na zlepšení péče o IBD pacienty ukázala perspektivy dalšího vývoje
- Kvíz – plicní komplikace u pacienta s Crohnovou chorobou
- Zlepšuje aplikace probiotik klinické výsledky v kolorektální chirurgii?
- Projekt RISING STARS
- Standardy chirurgické léčby IBD – Karlovy Vary, 6.–9. 11. 2013
- Gastrofórum 2014
-
Gastrofórum 2014, XIX. ročník 28.–31. január 2014
Ochorenia hornej časti tráviaceho traktu – abstrakty - Několik slov k novému ročníku
- Z XIX. Gastrofóra vzhůru do jubilejního výročí v roce 2015
- Trochu IBD na úvod
- Správná odpověď na kvíz
- Životní jubileum profesora Jana Bureše
- Autodidaktický test: IBD
- Karboxymaltóza železa: vysoce efektivní a bezpečná léčba nedostatku železa
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Karboxymaltóza železa: vysoce efektivní a bezpečná léčba nedostatku železa
- Tuberkulózní ileokolitida – popis případu
- Životní jubileum profesora Jana Bureše
-
Gastrofórum 2014, XIX. ročník 28.–31. január 2014
Ochorenia hornej časti tráviaceho traktu – abstrakty
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




