-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Efekt midazolamu a dexmedetomidinu na funkci srdečních komor s využitím MRI – pilotní randomizovaná studie
Effect of midazolam and dexmedetomidine on heart ventricles function using MRI – a pilot randomized study
Objective: Comparison of changes in ventricular function during sedation with midazolam and dexmedetomidine by mag netic resonance imaging (MRI), assess the feasibility of the implemented study protocol and determine the sample size of our randomized study.
Design: A pilot randomized study.
Setting: District hospital.
Materials and methods: The study included participants who met the inclusion criteria. Enrollment was by the envelope method: 8 participants in each group. After signing the informed consent, cardiac MRI was performed before and after se dation. During the examination, the blood flow velocity through the mitral valve during the early (E diast) and late (L diast) phase of diastole, the flow velocity through the aortic (Ao flow) and pulmonary (Pul flow) valves were recorded. A monitor recorded values of mean blood pressure (MAP), pulse (P), blood oxygen saturation (SpO2) in 5-minute intervals.
Results: Dexmedetomidine decreased MAP (82.5 mmHg ± 6 vs. 75.5 mmHg ± 7.2, p-value 0.027). P a SpO2 in both groups were without significant changes. Midazolam sedation led to worsening in E diast (234.5 mL.s–1 ± 93.5 vs. 207.6 mL.s–1 ± 87.6, p-value 0.012) whereas dexmedetomidine didn’t have a significant impact on E diast. L diast was not influenced by the seda tion technique in both groups. Dexmedetomdine sedatoin led a decrease in Pul flow (87 cm.s–1 ± 17.1 vs. 73.5 cm.s–1 ± 10.5, p-value 0.016) indicating a decrease in right ventricle output.
Conclusion: The implemented study protocol is feasible. Midazolam sedation worsens early filling of the left ventricle compared to dexmedetomide. Dexmedetomidine leads to a greater decrease in mean blood pressure and worsens, when compared to midazolam, right ventricle output.
Keywords:
cardiac magnetic resonance – cardiac function – midazolam – dexmedetomidine
Autoři: N. Omran 1; V. Skálová 2; D. Fĺak 1; J. Manďák 3; R. Škulec 4; V.- Černý 4 8
Působiště autorů: Kardiologická Klinika, Masarykova nemocnice a Univerzita J. E. Purkyně v Ústí nad Labem 1; Radiologická Klinika, Masarykova nemocnice a Univerzita J. E. Purkyně v Ústí nad Labem 2; Kardiochirurgická klinika, Univerzita Karlova v Praze, Lékařská fakulta v Hradci Králové 3; Klinika anesteziologie, perioperační a intenzivní medicíny, Masarykova nemocnice a Univerzita J. E. Purkyně, v Ústí nad Labem 4; Institut postgraduálního vzdělávání ve zdravotnictví 5; Centrum pro výzkum a vývoj, Fakultní nemocnice Hradec Králové 6; Dept. of Anesthesia, Pain Management and Perioperative Medicine, Dalhousie University, Halifax, Canada 7; Klinika anesteziologie, resuscitace a intenzivní medicíny, Univerzita Karlova v Praze, Lékařská fakulta v Hradci Králové 8
Vyšlo v časopise: Anest. intenziv. Med., 31, 2020, č. 4, s. 146-151
Kategorie: Původní práce
Souhrn
Cíl studie: Porovnání změny funkce srdečních komor při sedaci midazolamem a dexmedetomidinem pomocí magnetické rezonance (MRI); posoudit proveditelnost implementovaného protokolu studie a určení velikosti tzv. sample size naší randomizované studie.
Typ studie: Pilotní studie. Typ pracoviště: Krajská nemocnice.
Materiál a metody: Studie se zúčastnili dobrovolníci, kteří splnili zařazovací kritéria. Zařazení bylo pomocí obálkové metody: 8 účastníků v každé skupině. Po podepsání informovaného souhlasu bylo provedeno MRI srdce před a po podání sedace. Během vyšetření byla sledována rychlost krevního toku přes mitrální chlopeň během časné (E diast) a pozdní (L diast) fáze diastoly, rychlost toku přes aortální (Ao flow) a pulmonální (Pul flow) chlopeň. Monitorem byly zaznamenávané hodnoty středního krevního tlaku (MAP), pulzu (P), saturace krve kyslíkem (SpO2) v 5minutových intervalech.
Výsledky: Dexmedetomidin vedl k poklesu MAP (82,5 mmHg ± 6 vs. 75,5 mmHg ± 7,2, p‑value 0,027). Ve skupině midazolamu došlo k poklesu E diast (234,5 mL.s–1 ± 93,5 vs. 207,6 mL.s–1 ± 87,6, p‑value 0,012). Dexmedetomadin způsobil nevýznamné snížení E diast. L diast byla v obou skupinách bez významné změny. V skupině dexmedetomidinu došlo k poklesu Pul flow (87 cm.s–1 ± 17,1 vs. 73,5 cm.s–1 ± 10,5, p‑value 0,016), svědčící pro pokles výdeje pravé komory.
Závěr: Implementovaný protokol studie je proveditelný. Sedace midazolamem ve srovnání s dexmedetomidem zhoršuje časné plnění levé komory. Dexmedetomidin vede k většímu poklesu středního krevního tlaku a zhoršuje, ve srovnání s midazolamem, výdej pravé komory.
Klíčová slova:
magnetická rezonance – srdeční funkce – midazolam – dexmedetomidin
Úvod
Sedace patří mezi časté postupy používané v intenzivní péči. Již bylo publikováno nespočet prací porovnávajících rozdílné techniky sedace a jejich vliv na hemodynamické parametry [1–7]. Žádná studie zatím ale nezkoumala vztah mezi sedací a funkcí srdce s využitím údajů získaných pomocí magnetické rezonance.
Studie testovala hypotézu, že použití dexmedetomidinu vede k menšímu negativnímu dopadu na funkci srdečních komor ve srovnání s midazolamem.
Cílem pilotní studie je ověřovat proveditelnost protokolu studie pro případné další randomizované studie s větším počtem randomizovaných účastníků.
Soubor a metoda
Charakteristika studie
Jedná se o pilotní randomizovanou studii, do které byli zařazeni pacienti, hospitalizovaní na Kardiologické klinice Masarykovy nemocnice v Ústí nad Labem pro bolesti na hrudi, u kterých se vyloučil akutní koronární syndrom. Všichni jedinci souhlasili s účastí v této studii. Účastníci měli normální systolickou funkci obou srdečních komor, neměli chlopenní vady, anamnézu srdečního selhání, onemocnění jater, ledvin či plic, a zároveň neměli kontraindikace provedení MRI srdce či podání sedace (tab. 1). Do úvodní screeningové fáze bylo osloveno celkem 30 účastníků. Ze studie bylo vyloučeno celkově 14 účastníků: 4 pro fibrilaci síní, 4 se odmítli zúčastnit, 3 měli strukturální poškození srdce a 3 účastníci byli vyřazeni pro klaustrofóbii. Poté 16 účastníků bylo obálkovou metodou rozděleno do dvou skupin: 8 účastníků ve skupině midazolamu a stejný počet ve skupině dexmedetomidinu (schéma 1). U každého účastníka studie bylo provedeno baseline vyšetření srdce pomocí MRI, následovalo ihned podání sedace buď midazolamem, nebo dexmedetomidinem dle větve studie, do které se účastník randomizoval (viz technika sedace). Za 5 minut od zahájení sedace bylo během jednoho sezení provedeno kontrolní MRI srdce (viz MRI srdce) za účelem detekce sedací navozené změny funkce srdečních komor.
Tab. 1. Charakteristika souboru 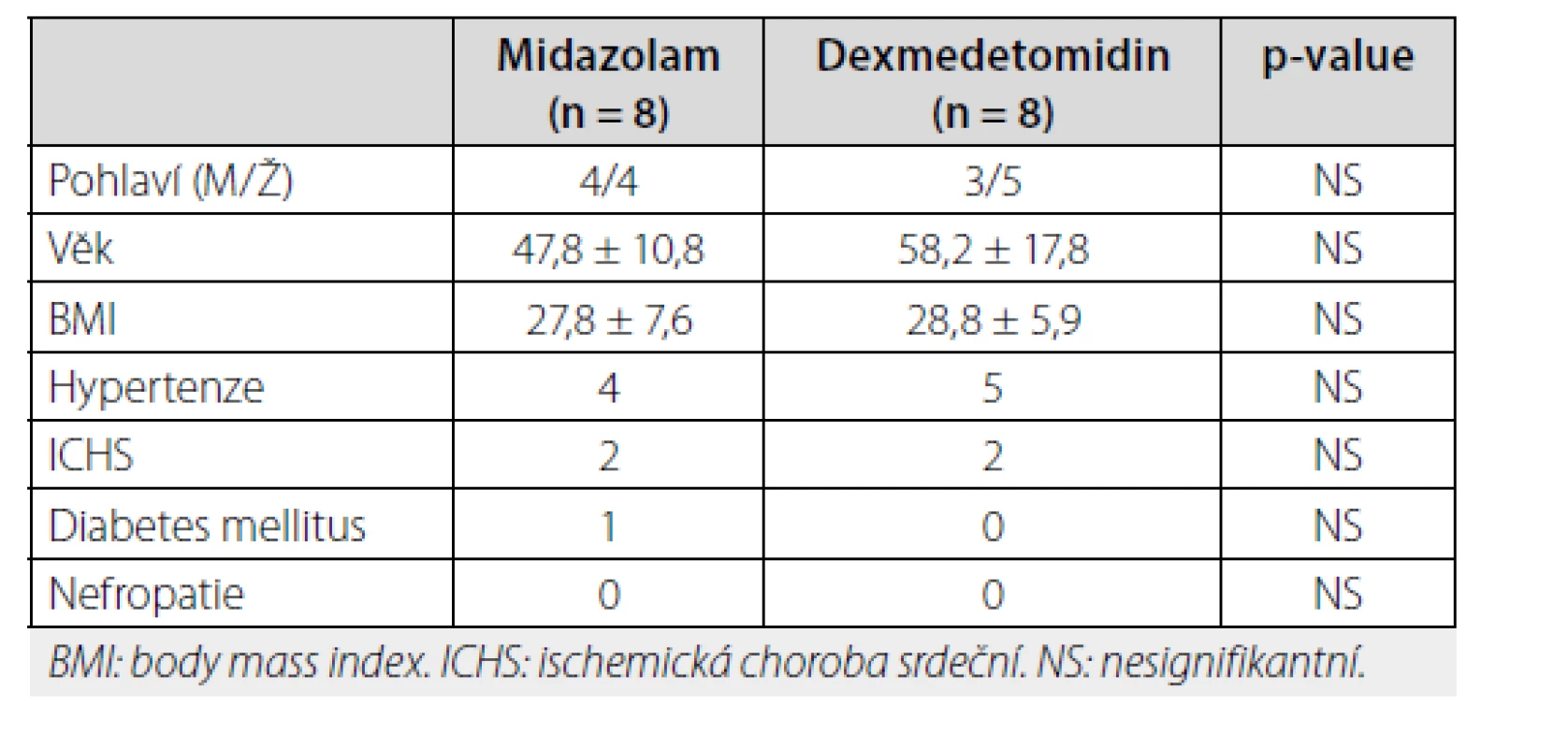
Schéma 1. CONSORT diagram o vývoji studie 
Protokol studie byl schválen etickou komisí. Všichni účastníci podepsali informovaný souhlas.
Technika sedace
Po 6 hodinách lačnění se vstupně provedlo úvodní vyšetření srdce magnetickou rezonancí, následně byla podána účastníkům sedace; první skupině 2 mg midazolamu intravenózně jako nejobvyklejší způsob podávání tohoto farmaka před ambulantními výkony. Druhé skupině dexmedetomidin formou kontinuální infuze v dávce 0,7 μg.kg–1.hod–1. Dexmedetomidin byl podán bez bolusu v relativně nízké dávce, a to z několika důvodů: riziko poškození účastníků hypertenzí a tachykardií při bolusovém podání [8]; riziko závažné hypotenze a bradykardie při vyšších rychlostech infuzního podávání dexmedetomidinu [8]; dále ovlivnění afterloadu při bolusovém podávání by mohlo zkreslit sledované parametry srdeční činnosti sledovaných pomocí MRI. K dávkování dexmedetomidinu byla použita infuzní pumpa umístěná mimo magnetické pole. Pět minut od zahájení podávání medikace byla provedena kontrolní magnetická rezonance srdce (schéma 2).
MRI srdce
Měření průtoků krve na srdečních chlopních bylo provedeno na 3 T MR přístroji (Philips Ingenia, Philips, Best, The Netherlands) s retrospektivní EKG synchronizací/gatingem, v opakovaně zadržovaném dechu. Po orientačních survey/lokalizérech následovaly řezy sloužící k nastavení odpovídajících rovin 2CH, 4CH a SA cine SSFP (steady state free precession) sekvencemi – v našem případě konkrétně BTFE (balancované turbo ‑ field echo sekvence). Pro účely měření průtoků se nastavovaly opět v BTFE cine sekvencích vhodné roviny kolmé ke krevnímu toku na výše zmíněných chlopních. Samotné měření průtoků v takto nastavených rovinách – Q flow (quantitative flow measurement) – na mitrální, aortální a pulmonální chlopni, jsme provedli pomocí sekvence phase contrast. Poté byla účastníkům aplikována sedace (midazolam/dexmedetomidin) a opět bylo zopakováno měření průtoků na všech výše zmíněných chlopních stejnými sekvencemi. Postprocesem jsme doplnili semikvantitativní analýzu – analýza průtoků na mitrální, pulmonální a aortální chlopni před a po podání sedativa.
Hemodynamické monitorování Sledování hemodynamických parametrů během studie bylo realizováno pomocí MRI – kompatabilního monitoru (Philips Expression MR 200, Philips, Best, The Netherlands). Byly sledovány následující parametry: MAP, P, SpO2 v 5minutových intervalech před a po podání sedace. Celkem bylo provedeno 5 měření před a 5 měření po podání sedace. Účastníci museli být při vyšetření spolupracující a vyhovět pokynům (opakované zadržování dechů), proto cílová míra sedace, sledována pomocí RASS škály, nepřesahovala –1. Po ukončení vyšetření byli účastníci sledováni po dobu 4 hodin od ukončení podávání sedace, během této doby byla monitorace standardní v rámci trvající hospitalizace. Pro bezpečnost účastníků byly během monitorace sledovány potenciální komplikace spojené s podáváním sedace, jako hypotenze, definována poklesem středního krevního tlaku pod 65 mmHg, hypertenze, definována vzestupem středního krevního tlaku nad 100 mmHg, bradykardie, definována poklesem tepové frekvence pod 50. min–1, tachykardie, definována vzestupem srdeční frekvence nad 90. min–1 a hyposaturace, definována poklesem saturace krve kyslíkem pod 93 %.
Statistická analýza
Naměřené hodnoty jsou prezentovány jako průměr ± směrodatná odchylka. K vyhodnocení byla použita jedno‑faktorová analýza rozptylu pro opakovaná měření s post‑hoc Fisherovým LSD testem. Data byla zpracovávána softwarem Statistica (data analysis software system, version 13 TIBCO Software Inc). Zvolená hladina významnosti byla α = 0,05.
Výsledky
Vyšetření magnetickou rezonancí i podávání sedace proběhlo u všech účastníků bez komplikací. Během monitorace nebyla zachycena žádná porucha srdečního rytmu a ani nebyla registrována závažná změna krevního tlaku, pulzu či pokles saturace krve kyslíkem.
Ve skupině dexmedetomidinu došlo ke statisticky významnému poklesu MAP (82,5 mmHg ± 6 vs. 75,5 mmHg ± 7,2, p‑value 0,027) (graf 1). Ostatní monitorem sledované hemodynamické parametry byly bez významné změny (graf 2).
Co se týče parametrů funkce srdce sledovaných pomocí MRI, došlo ve skupině dexmedetomidinu ke zhoršení E diast, tato změna nicméně nebyla statisticky významná (172 mL.s–1 ± 68,2 vs. 153,8 mL.s–1 ± 47,6, p‑value 0,089). Naopak, podávání midazolamu vedlo v našem souboru k podstatnému zpomalení E diast (234,5 mL.s–1 ± 93,5 vs. 207,6 mL.s–1 ± 87,6, p‑value 0,012) (graf 3). Dalším nálezem je statisticky významný pokles Pul flow při sedaci dexmedetomidinem svědčící pro pokles srdečního výdeje pravé komory (87 cm.s–1 ± 17,1 vs. 73,5 cm.s–1 ± 10,5, p‑value 0,016) (graf 4). Ostatní parametry funkce srdce sledované pomocí MRI byly bez statisticky významné změny (graf 5).
Výsledky hemodynamické monitorace účastníků v našem souboru jsou uvedené v tabulce 2. Jednotlivé naměřené parametry pomocí MRI jsou uvedené v tabulce 3.
Tab. 2. Získané hemodynamické parametry během studie 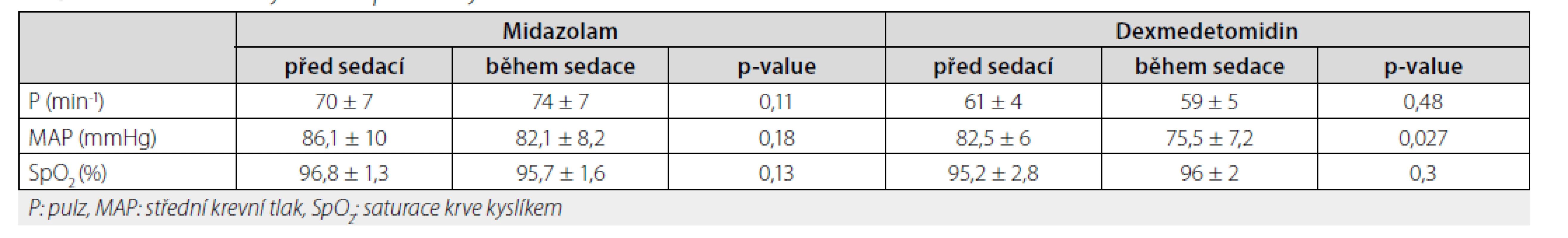
Tab. 3. Získané parametry funkce srdce měřené pomocí magnetické resonance 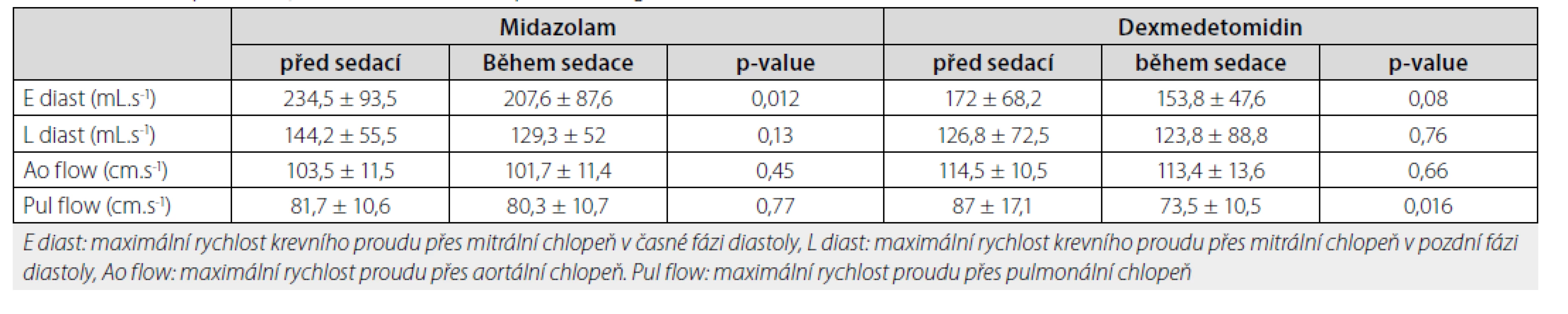
Diskuze
Naše práce je zatím jediná, která sledovala dopad sedace na funkci srdečních komor pomocí MRI srdce. Dalším faktorem, který přispívá k unikátnosti naší práce je skutečnost, že jde o soubor spontánně ventilujících účastníků, což eliminuje vliv a interferenci umělé plicní ventilace se srdeční funkcí.
V našem souboru byla malá dávka midazolamu po oběhové stránce dobře tolerována a nevedla k významným změnám krevního tlaku a srdeční frekvence. Dle literatury je popisován tzv. „vagolytic‑like effect“ midazolamu, který má za následek snížení aktivity parasympatického autonomního systému, relativní dominanci sympatického autonomního systému s následnou tachykardií [9, 10]. Tento trend byl pozorován i v námi vedeném souboru, ale byl statisticky nesignifikantní. Na opačné straně dle Macnab a spol. bolusové podávání midazolamu bylo beze změny srdeční frekvence díky zachování aktivity baroreceptorů [11].
Dexmedetomidin byl uveden do klinické praxe v roce 1999. Jeho stimulace α2 receptoru v locus coeruleus vede k sympatolýze s následným poklesem krevního tlaku a srdeční frekvence [12]. Proto je při podávání dexmedetomidinu nutná větší opatrnost u pacientů s pokročilou poruchou atrioventrikulárního vedení nebo se závažným srdečním selháváním. Na druhé straně je ovšem potřeba větší obezřetnosti při bolusovém podávání dexmedetomidinu, kdy díky stimulaci B subtypu α2 receptoru v periferním řečišti může být navozena tachykardie a hypertenze [8]. V našem souboru byla ve shodě popisována hypotenzní reakce, ale bez evidentní změny srdeční frekvence.
Během sledování rychlosti toku přes mitrální chlopeň ve skupině midazolamu došlo k významnému zhoršení E diast (o 15 %) oproti výchozím hodnotám. L diast byla též negativně ovlivněna (o 10 %), tato změna nicméně nebyla statisticky významná. Tento výsledek je ve shodě se závěrem Gare et al. Dle jejich sdělení midazolam v dávce 0,05 mg.kg–1 u pacientů bez preexistující diastolické dysfunkce způsobil statisticky významné snížení rychlosti časného plnění levé komory (o 13 %) a nevýznamné snížení rychlosti pozdní fáze plnění levé komory (o 7 %), které bylo hodnoceno pomocí transtorakální echokardiografie [1]. Možné vysvětlení tohoto efektu na diastolickou funkci levé komory je buď zhoršení žilního návratu v důsledku sedace – indukovaná venodilatace, anebo opožděné uvolnění Ca++ z kontraktilního mikrofilamentu kardiomyocytů v důsledku alterace Ca++ homeostázy během diastoly. Toto má za následek zpomalení relaxace komory a také zpomalení rychlosti proudu krve v časné fázi diastoly [1, 2]. Nelze samozřejmě vyloučit přímý negativní inotropní efekt midazolamu na mechanické vlastnosti síní, který se projeví zpomalením pozdní fáze diastoly [3].
Podávání dexmedetomidinu u spontánně ventilujících účastníků vedl v našem souboru ke snížení rychlosti časné diastoly (o 11 %), tato změna byla statisticky nevýznamná (p‑value 0,088). Podobný trend, přestože s významným statistickým výsledkem, byl zaznamenán v souboru Lee et al., kde podávání dexmedetomidinu jako adjuvans k celkové intravenózní anestezii zhoršilo významně (o 23 %) časnou fázi plnění levé komory [4].
Na opačné straně, dle literatury, podávání dexmedetomidinu u zdravých dobrovolníků [5] nebo pacientů jako adjuvans k totální intravenózní anestezii [6] bylo bez patrného vlivu na diastolickou funkci myokardu. Dalším zajímavým nálezem naše pilotní studii byl pokles Pul flow (o 16 %) při sedaci dexmedetomidinem, což svědčí nepřímo pro pokles srdečního výdeje pravé komory. Přesný mechanismus tohoto nálezu není dostatečně znám. Potenciální příčiny mohou být následující: 1. dexmedetomidin v nízké dávce má beta‑blocker‑like effect, což má za následek snížení inotropie pravé komory s následným poklesem jejího výdeje [4, 5], 2. sympatolýzou indukovaná venodilatace může vést ke zhoršení žilního návratu s poklesem preloadu pravé komory [7], 3. zvýšení afterloadu pravé komory v důsledku potenciálního nárůstu plicní vaskulární rezistence [13], 4. dalším možným důvodem poklesu výdeje pravé komory je zhoršení diastolické nasávací vlastnosti pravé komory s následným poklesem preloadu pravé komory.
Současné výsledky by měly být interpretovány s ohledem na několik potenciálních omezení: 1. výsledky našeho souboru prezentují předběžné výsledky pilotní studie a počet účastníků v části našeho souboru je malý, 2. nejedná se o placebem kontrolovanou studii, 3. nečetné měření parametrů diastolické funkce levé komory pomocí magnetické rezonance u každého účastníka. Případné opakování měření parametrů pomocí magnetické rezonance by bylo pro účastníky neúnosné. Další případnou limitací je absence porovnávání parametrů diastolické funkce levé komory získaných pomocí magnetické rezonance se zlatým standardem, což je ultrazvuk. Absolutní hodnoty rychlosti časného a pozdního plnění levé komory získaných pomocí fázového kontrastu se liší od absolutních hodnot získaných pomocí ultrazvuku. Tento rozdíl je daný metodou měření a způsobem získávání jednotlivých dat, nicméně by neměl vést k mylnému hodnocení diastolické funkce myokardu [14, 15]. Výše uvedené a „jen“ statisticky významné změny srdeční funkce při sedaci mohou nabírat klinickou významnost tam, kde se sedace podává ve větší dávce a během delšího časového horizontu, jako např. v případě kriticky nemocných.
Prezentované výsledky jsou výsledky pilotní studie, která ukázala, že protokol studie je proveditelný a bezpečný a může být jádrem pro další studie posuzující vliv sedace na funkce srdce pomocí MRI s větším počtem pacientů.
Závěr
Midazolam ve srovnání s dexmedetomidinem vedl k statisticky významnému zhoršení časného plnění levé komory. Dexmedetomidin na druhé straně vedl k statisticky signifikantnímu zhoršení výdeje pravé komory a významnému poklesu středního krevního tlaku.
PROHLÁŠENÍ AUTORŮ: Prohlášení o původnosti: Práce je původní a nebyla publikována ani není zaslána k recenznímu řízení do jiného média. Výsledky nebyly prezentovány na žádné odborné akci. Střet zájmů: Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem práce. Podíl autorů: Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína. NO se podílel na sběru dat, jejich hodnocení a sepsání článku. VS provedla vyšetření srdce pomoci magnetické rezonance. DF revidoval a editoval článek. JM provedl odbornou konzultaci při sepsání článku. RŠ pomohl při statickém zpracování získaných dat. VČ je hlavním vedoucím týmu. Financování: Žádné. Poděkování: Velké poděkování patří paní Hance Gabrielové a panu Petru Novákovi za pomoc při provedení vyšetření srdce pomocí magnetické rezonance. Velké poděkování patří také paní doktorce Evě Čermákové za statistické zpracování získaných dat. Projednání etickou komisí: Etická komise, Fakultní nemocnice Hradec Králové, registrační číslo: 201612S15P.
KORESPONDENČNÍ ADRESA AUTORA: Článek přijat redakcí: 21. 6. 2020; Článek přijat k tisku: 5. 8. 2020
MUDr. Nedal Omran
Cit. zkr: Anest intenziv Med. 2020; 31(4): 146–151
Zdroje
1. Gare M, Parail A, Milosavljevic D, Kersten JR, Warltier DC, Pagel PS. Conscious sedation with midazolam or propofol does not alter left ventricular diastolic performance in patients with preexisting diastolic dysfunction: a transmitral and tissue Doppler transthoracic echocardiography study. Anesth Analg. 2001; 93(4): 865–871. doi: 10.1097/00000539 - 200110000-00012.
2. Grossman W, Haering JM, Pagel PS, Warltier DC. Left Ventricular Diastolic Function in the Normal and Diseased Heart. Anesthesiology. 1993; 79(4): 836–854. doi: 10.1097/00000542 - 199310000-00027.
3. Couture P, Denault AY, Shi Y, Deschamps A, Cossette M, Pellerin M, et al. Effects of anesthetic induction in patients with diastolic dysfunction. Can J Anaesth. 2009; 56(5): 357 – 365. doi: 10.1007/s12630-009-9068-z.
4. Lee SH, Na S, Kim N, Ban MG, Shin SE, Oh YJ. The Effects of Dexmedetomidine on Myocardial Function Assessed by Tissue Doppler Echocardiography During General Anesthesia in Patients With Diastolic Dysfunction. Medicine (Baltimore). 2016; 95(6): e2805. doi: 10.1097/MD.0000000000002805.
5. Snapir A, Posti J, Kentala E, Koskenvuo J, Sundell J, Tuunanen H, et al. Effects of low and high plasma concentrations of dexmedetomidine on myocardial perfusion and cardiac function in healthy male subjects. Anesthesiology. 2006; 105(5): 902–910; quiz 1069–1070. doi: 10.1097/00000542-200611000-00010.
6. Lee SH, Choi YS, Hong GR, Oh YJ. Echocardiographic evaluation of the effects of dexmedetomidine on cardiac function during total intravenous anaesthesia. Anaesthesia. 2015; 70(9): 1052–1059. doi: 10.1111/anae.13084.
7. Yu T, Li Q, Liu L, Guo F, Longhini F, Yang Y, et al. Different effects of propofol and dexmedetomidine on preload dependency in endotoxemic shock with norepinephrine infusion: a randomized case ‑ control study. Crit Care. 2014; 18(1): P417. doi: 10.1186/cc13607.
8. Arcangeli A, D’Alò C, Gaspari R. Dexmedetomidine use in general anaesthesia. Curr Drug Targets. 2009; 10(8): 687–695. doi: 10.2174/138945009788982423.
9. Win NN, Fukayama H, Kohase H, Umino M. The different effects of intravenous propofol and midazolam sedation on hemodynamic and heart rate variability. Anesth Analg. 2005; 101(1): 97–102. doi:
10.1213/01.ANE.0000156204.89879.5C. 10. Galletly DC, Williams TB, Robinson BJ. Periodic cardiovascular and ventilatory activity during midazolam sedation. Br J Anaesth. 1996; 76(4): 503–507. doi: 10.1093/bja/76. 4. 503.
11. Macnab AJ, Levine M, Glick N, Macready J, Susak L, et al. Midazolam following open heart surgery in children: haemodynamic effects of a loading dose. Paediatr Anaesth. 1996; 6(5): 387–397. doi: 10.1046/j.1460-9592.1996.d01-6.x.
12. Szumita PM, Baroletti SA, Anger KE, Wechsler ME. Sedation and analgesia in the intensive care unit: evaluating the role of dexmedetomidine. Am J Health Syst Pharm. 2007; 64(1): 37–44. doi: 10.2146/ajhp050508.
13. Ebert TJ, Hall JE, Barney JA, Uhrich TD, Colinco MD. The effects of increasing plasma concentrations of dexmedetomidine in humans. Anesthesiology. 2000; 93(2): 382–394. doi: 10.1097/00000542-200008000-00016.
14. Webb J, Fovargue L, Tøndel K, Porter B, Sieniewicz B, Gould J, et al. The Emerging Role of Cardiac Magnetic Resonance Imaging in the Evaluation of Patients with HFpEF. Curr Heart Fail Rep. 2018; 15(1): 1–9. doi: 10.1007/s11897-018-0372-1.
15. Rathi VK, Doyle M, Yamrozik J, Williams RB, Caruppannan K, Truman C, et al. Routine evaluation of left ventricular diastolic function by cardiovascular magnetic resonance: a practical approach. J Cardiovasc Magn Reson. 2008; 10(1): 36. doi: 10.1186/1532-429X-10-36.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2020 Číslo 4- Jak souvisí postcovidový syndrom s poškozením mozku?
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse je bezpečný přípravek v krátkodobé léčbě bolesti
- Léčba akutní pooperační bolesti z pohledu ortopeda
-
Všechny články tohoto čísla
- Doporučené postupy anestezie u pacientů trpících vzácným onemocněním v češtině – „OrphanAnesthesia.cz“
- Efekt midazolamu a dexmedetomidinu na funkci srdečních komor s využitím MRI – pilotní randomizovaná studie
- Perioperační péče o transgender pacienty/pacientky
- Audit antibiotické profylaxe v chirurgii
- Sto šedesát let od izolace kokainu a 115 let od syntézy prokainu – historie lokálních anestetik a jejich objevitelů
- Renesance ketaminu v léčbě dospělých pacientů v akutním a v kritickém stavu
- Náš článek po 10 letech: The practice of therapeutic mild hypothermia in cardiac arrest survivors in the Czech Republic
- Hemadsorpční metody u kriticky nemocných – dvojitá sázka naslepo?
- Inzulinová rezistence, hyperglykemie a proteinový katabolismus u kriticky nemocných: hledání klíčů k uzamčeným dveřím
- Suspektní imunitní trombocytopenie při Morbus Crohn
- Diagnostika COVID-19 pneumonie pomocí výpočetní tomografie, naše zkušenosti
- Perioperační použití gabapentinoidů v léčbě akutní pooperační bolesti – systematický přehled a metaanalýza
- Infekce krevního řečiště u kriticky nemocných: expertní stanovisko
- Tranexamová kyselina
- Hypoxie a hyperkapnie – jak fungují chemoreceptory?
- Disrupce rytmicity melatoninu v kritickém stavu
- Zajímavosti, tipy a triky, informace z jiných oborů
- CO2 oproti vzduchu významně sníží riziko vzduchové embolie při intervenčních ERCP a GIT endoskopiích
-
MEZIOBOROVÉ STANOVISKO
(evidenční číslo ČSARIM: 11/2020)
ZÁSADY ÚČELNÉ INDIKACE REMDESIVIRU U PACIENTŮ S COVID-19
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Tranexamová kyselina
- Hypoxie a hyperkapnie – jak fungují chemoreceptory?
- Audit antibiotické profylaxe v chirurgii
- Sto šedesát let od izolace kokainu a 115 let od syntézy prokainu – historie lokálních anestetik a jejich objevitelů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání







