-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Iatrogenní embolizace hydrofilních polymerů jako komplikace endovaskulárních výkonů – nová jednotka
Hydrophilic polymer embolization as an iatrogenic complication of endovascular interventions – a new entity
Iatrogenic hydrophilic polymer embolization (HPE) is an underrecognised complication of endovascular procedures. In certain instances, HPE and related complications may lead to patiens death. Incidence of this phenomenon is not known. We evaluated retrospectively all autopsies of patients with a history of endovascular intervention performed by one pathology resident during a period of 8 months. There were 10 cases, which were examined histochemically and in polarized light. We detected HPE in 2 of the 10 cases. In both cases the involved organ were lungs. Hydrophilic polymer embolization is a potential and easy-to-miss complication of endovascular procedures. It must be considered during histological examination of autoptic material.
Keywords:
iatrogenic embolization – hydrophilic polymers – HPE – Catheterization
Autoři: Monika Manethová; Ivo Šteiner
Působiště autorů: Fingerlandův ústav patologie, Lékařská fakulta Univerzity Karlovy a Fakultní nemocnice Hradec Králové
Vyšlo v časopise: Čes.-slov. Patol., 57, 2021, No. 1, p. 40-43
Kategorie: Původní práce
Souhrn
Iatrogenní embolizace hydrofilních polymerů (HPE – hydrophilic polymer embolization) je málo známou komplikací endovaskulárních výkonů, která může vést až ke smrti pacienta. Incidence tohoto fenoménu není známa. Za časové období osmi měsíců byly retrospektivně zrevidovány vlastní pitvy všech pacientů s anamnézou endovaskulární intervence. Šlo o 10 případů, které byly vyšetřeny histochemicky a v polarizovaném světle. Z těchto 10 případů byla ve 2 prokázána embolizace hydrofilních polymerů. V obou případech se jednalo o embolizaci do plic. Embolizace hydrofilních polymerů je možnou komplikací endovaskulárních vyšetření, na níž je nutno pomýšlet při histologickém hodnocení autoptického materiálu a cíleně po ní pátrat
Klíčová slova:
iatrogenní embolizace – hydrofilní polymery – HPE – katetrizace
Koncem 90. let minulého století byl poprvé popsán fenomén embolizace polymerů po endovaskulárním výkonu. Hydrofilní polymery se používají jako povlak různých endovaskulárně zaváděných vyšetřovacích či léčebných zařízení, aby jako jakési povrchové „mazivo“ usnadnily manipulaci katetrem v místě kožního vstupu do cévy i v průběhu vlastního endovaskulárního zákroku, a rovněž jako prevence vzniku trombů (1).
S embolizací polymerů je možno se setkat po koronarografii, koronárním stentování, transkatetrové implantaci protézy aortální chlopně (TAVI), centrální žilní katetrizaci, použití extrakorporální membránové oxygenace (ECMO), intrakraniální angiografii, trombektomiích, intravaskulárních zákrocích na aortě a řadě dalších zákroků, mj. i po zavádění kovových spirálek do mozkových aneurysmat, tzv. coilingu (2,3).
Při endovaskulární manipulaci se může polymerní materiál z povrchu zařízení uvolňovat a embolizovat do periferie (4). Cílovými orgány jsou pak u centrálních žilních katetrů plíce (1), u tepenných intervencí nejčastěji mozek, srdce, ledviny a slezina, ale postižen může být prakticky kterýkoli orgán (3,5-7). Je popsán i případ, kdy uvolnění hydrofilních polymerů při implantaci stentgraftu do aortálního abdominálního aneurysmatu vedlo k anafylaktické reakci pacienta (8). Emboly se většinou nacházejí na úrovni malých cév (9) a rozsáhlejší embolizace mohou vést až ke smrti (10).
Protože různí výrobci používají různé polymery, může se histologický obraz embolů polymerů v jednotlivých případech lišit (11); většinou jde o amorfní, vláknitý či jemně granulovaný lamelární materiál, v barvení hematoxylinem eosinem amfofilní až bazofilní, který není dvojlomný a neotáčí rovinu polarizovaného světla. Může se přibarvovat konžskou červení, mucikarmínem a modře Massonovým trichromem. V přilehlé cévě embolus může v průběhu času vyvolat zánětlivou reakci s přítomností obrovských buněk, lymfocytů a neutrofilů, takže nález může být chybně interpretován jako granulomatózní vaskulitida (12).
Materiál polymerů časem může podléhat biodegradaci a ze tkáně mizet; interval mezi endovaskulárním zákrokem a histologickým nálezem embolů polymerů může tedy být maximálně týdny až několik málo měsíců. Pozdní závažné komplikace se mohou vyskytnout i po delším časovém intervalu na podkladě granulomatózního zánětu (13-16).
Prevalence iatrogenní embolizace hydrofilních polymerů není známa a z tohoto důvodu jsme se rozhodli provést malou retrospektivní studii na našem pracovišti a analyzovat nalezené případy pomocí rutinně dostupných histochemických metod.
MATERIÁL A METODY
Za časové období květen 2019 – prosinec 2019 byly zrevidovány pitvy pacientů s anamnézou endovaskulární intervence v časovém horizontu 1–90 dnů před smrtí, které provedla autorka článku na Fingerlandově ústavu patologie v Hradci Králové. Šlo o 10 případů, z nichž bylo pořízeno průměrně 23 sklíček na pitvu. Histologické vzorky byly barveny standardní metodou hematoxylinem eosinem a vzorky s nálezem polymerových embolů dále speciálními barveními: alciánová modř, Mayerův mucikarmín, periodic acid schiff (PAS), konžská červeň, Weigert van Gieson, saturnová červeň, Massonův modrý trichrom a zelený trichrom. Morfologické vyšetření bylo doplněno vyšetřením v polarizovaném světle. Ve dvou případech, kdy materiál morfologicky připomínal trombus či trombembolus, bylo doplněno imunohistochemické vyšetření protilátkou proti CD61 (klon Y2/51, 1 : 100, Dako A/S, Glostrup, Denmark); demaskování antigenu bylo provedeno metodou HIER (heat-induced epitope retrieval) po dobu 20 minut a k vizualizaci imunohistochemické reakce byl použit vizualizační systém EnVisionFlex (Dako A/S Glostrup, Denmark) využívající diaminobenzidin jako chromogen. Reakce byla provedena v přístroji Autostainer 48 (Dako A/S, Glostrup, Denmark).
VÝSLEDKY
Z 10 případů studie byla nalezena embolizace cizorodého materiálu ve dvou. V obou se jednalo o embolizaci do plic do malých větví plicnice a v jejich okolí nebyla přítomna zánětlivá reakce. V hematoxylinu eosinu se embolizovaný materiál barvil sytě bazofilně, ve speciálních barveních byl negativní. V obou případech materiál neotáčel rovinu polarizovaného světla. Ani v jednom případě nebyly nalezeny polymerové emboly v dalších orgánech.
Případ č. 1
Žena, 71 let, náhrada mitrální chlopně bioprotézou pro insuficienci 10 dní před úmrtím, se současnou implantací VA ECMO. Pro slepení cípů mitrální bioprotézy byla 6 dní před smrtí provedena její balónková dilatace. Polymerové emboly byly nalezeny v obou plicích v malých tepnách. V hematoxylinu eosinu byly jemně granulárního, bazofilního vzhledu. Cizorodý materiál jednak ulpíval na intimě cév, jednak vyplňoval lumina (obr. 1 a obr. 2). Ve speciálním barvení saturnovou červení se polymer přibarvoval hnědočerně (obr. 3).
Obr. 1. Případ č. 1. Bazofilní, amorfní, příp. jemně granulární cizorodý materiál v malých plicních cévách vyplňující lumina (HE, zvětšeno 200x). 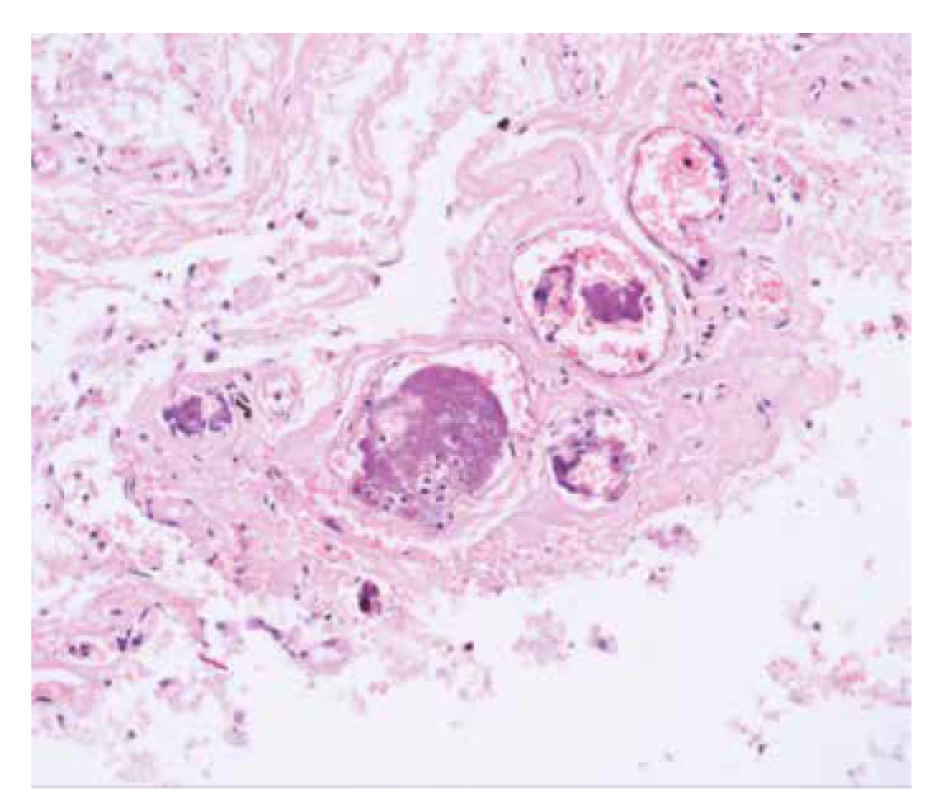
Obr. 2. Případ č. 1. Polymer ulpívající na intimě (HE, zvětšeno 200x). 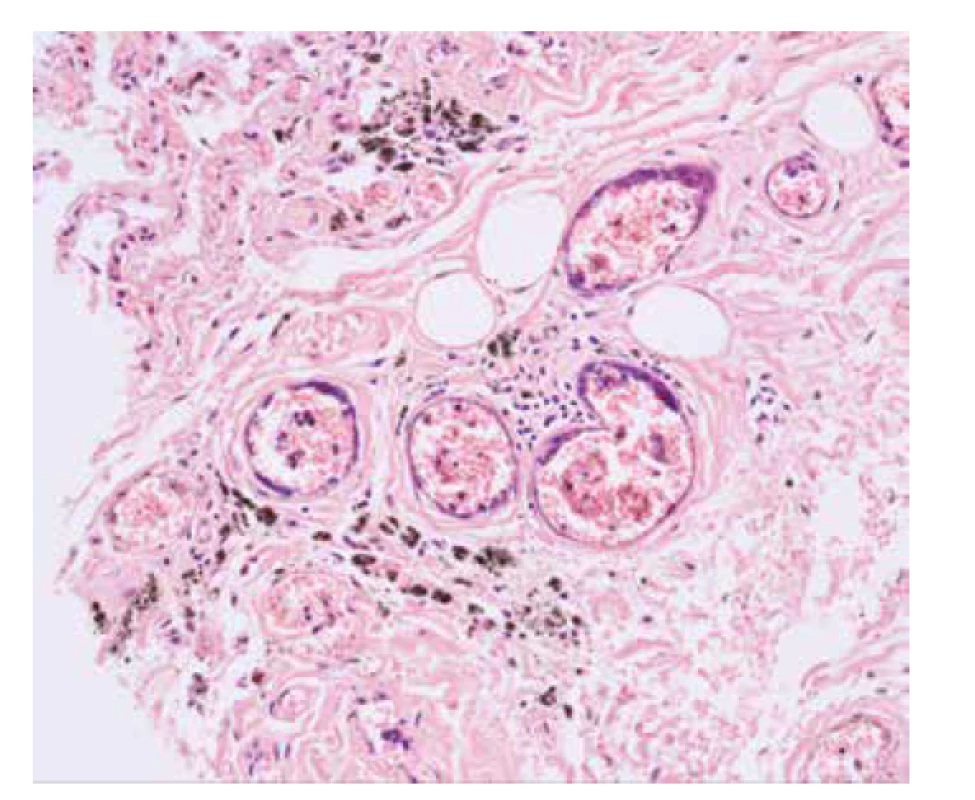
Obr. 3. Případ č. 1. Hnědočerné zbarvení polymeru ve speciálním barvení saturnovou červení (zvětšeno 200x). 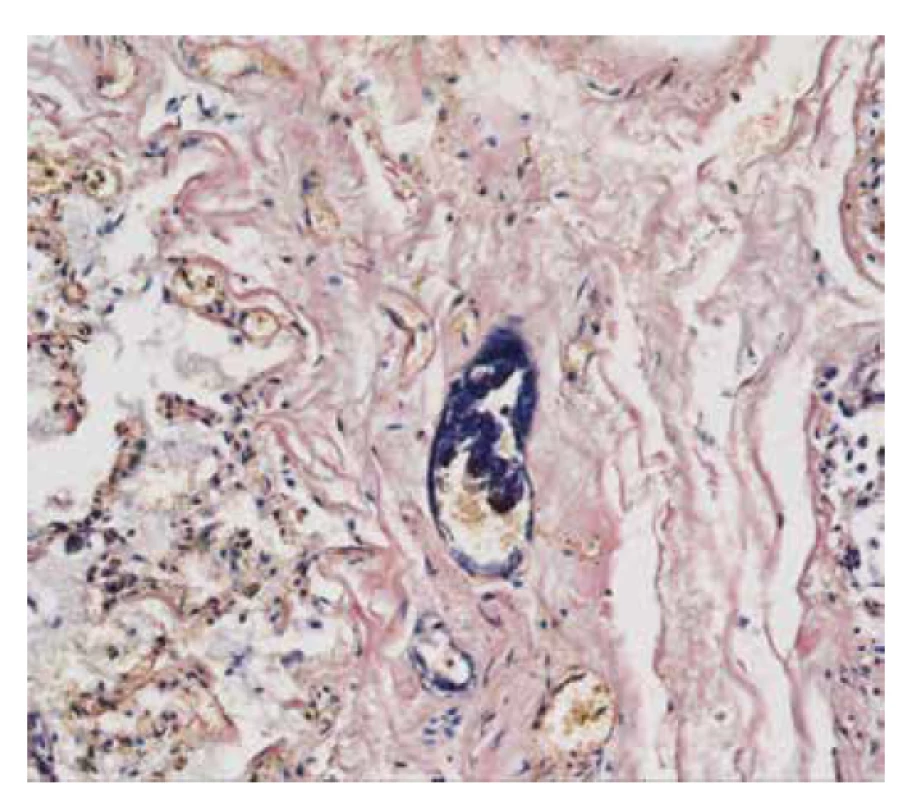
Případ č. 2
Muž, 67 let, roboticky asistovaná plastika mitrální chlopně pro její insuficienci s implantací VA ECMO 17 dní před smrtí.
Polymerové emboly měly vzhled obdobný jako v případě č. 1, jednalo se o jemně granulární bazofilní materiál částečně nebo zcela vyplňující malé tepny obou plic, který připomínal drobné tromby či trombemboly (obr. 4). Doplněné imunohistochemické vyšetření protilátkou proti CD61 bylo negativní (obr. 5). Obdobně jako v případu č. 1 se embolizovaný polymer ve speciálním barvení saturnovou červení přibarvoval hnědočerně.
Obr. 4. Případ č. 2. Polymer vyplňující lumina malých cév (HE, zvětšeno 200x). 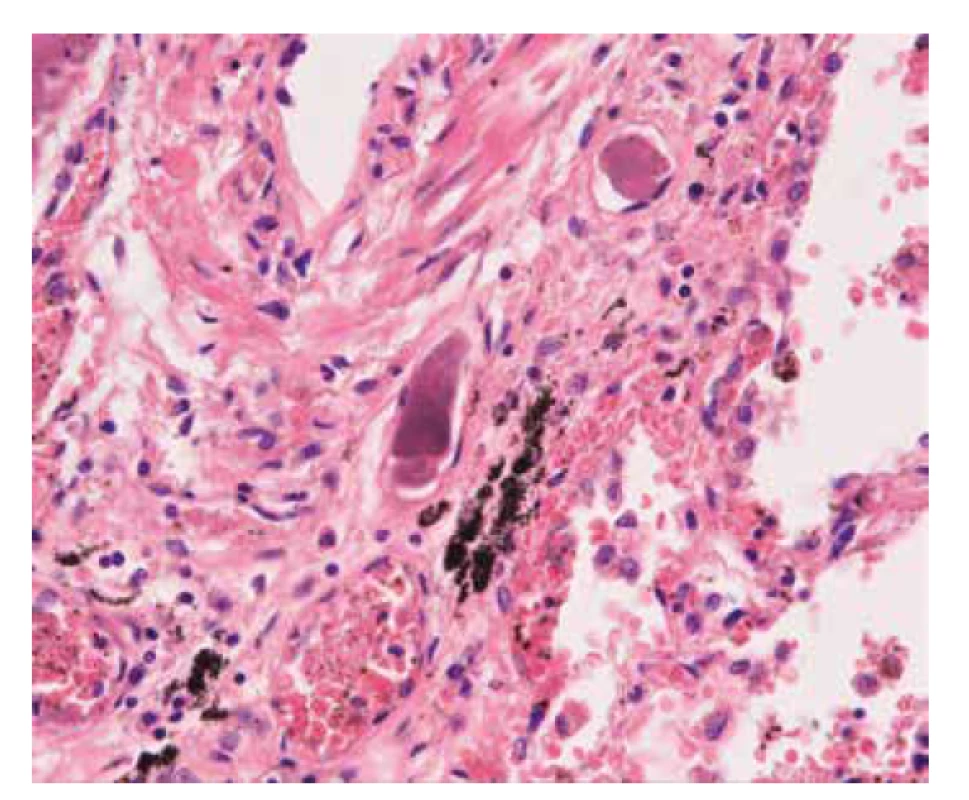
Obr. 5. Případ č. 2. Negativní imunohistochemicky průkaz CD61 v embolizovaném polymeru (zvětšeno 400x). 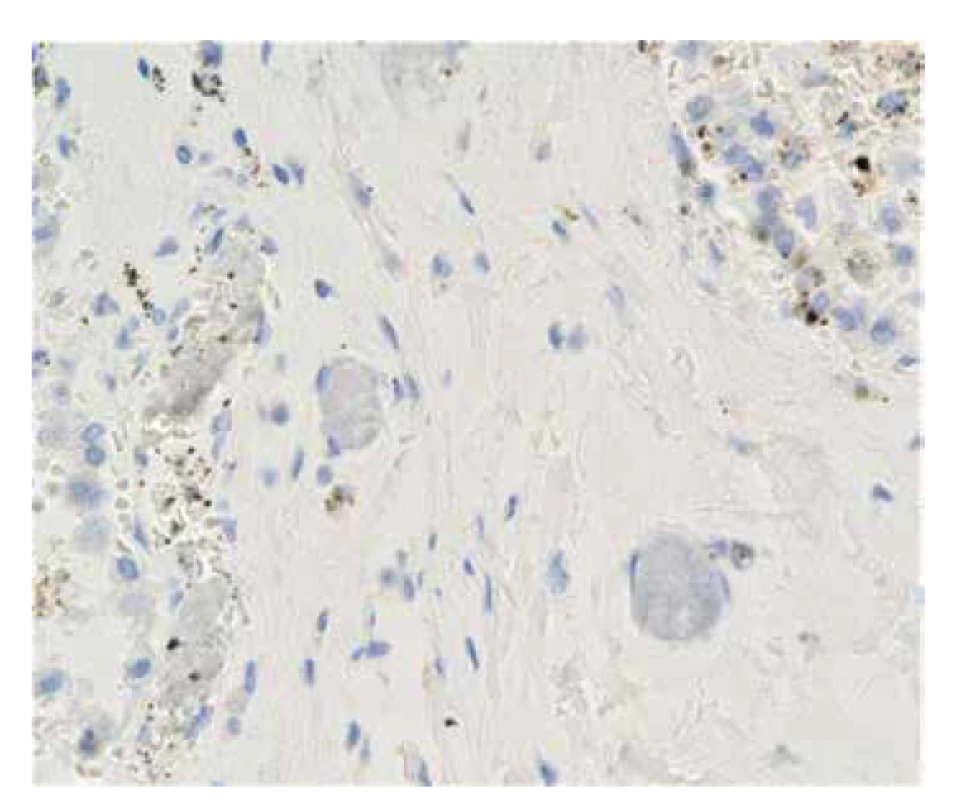
Mimo popsané dva případy byl u jednoho z dalších pacientů nalezen zbytek polymeru v obsahu destičkového trombu v koronárním stentu po provedené koronarografii 1 den před smrtí pacienta. Zde však nebyla zachycena embolizace do periferie, a proto případ neuvádíme mezi výše uvedené. Zachycený polymer amorfního vzhledu (obr. 6) je světle bazofilní v hematoxylinu eosinu a negativní ve speciálních barveních. Neotáčí rovinu polarizovaného světla.
Obr. 6. Polymer zachycený v destičkovém trombu v koronárním stentu (HE, zvětšeno 400x). 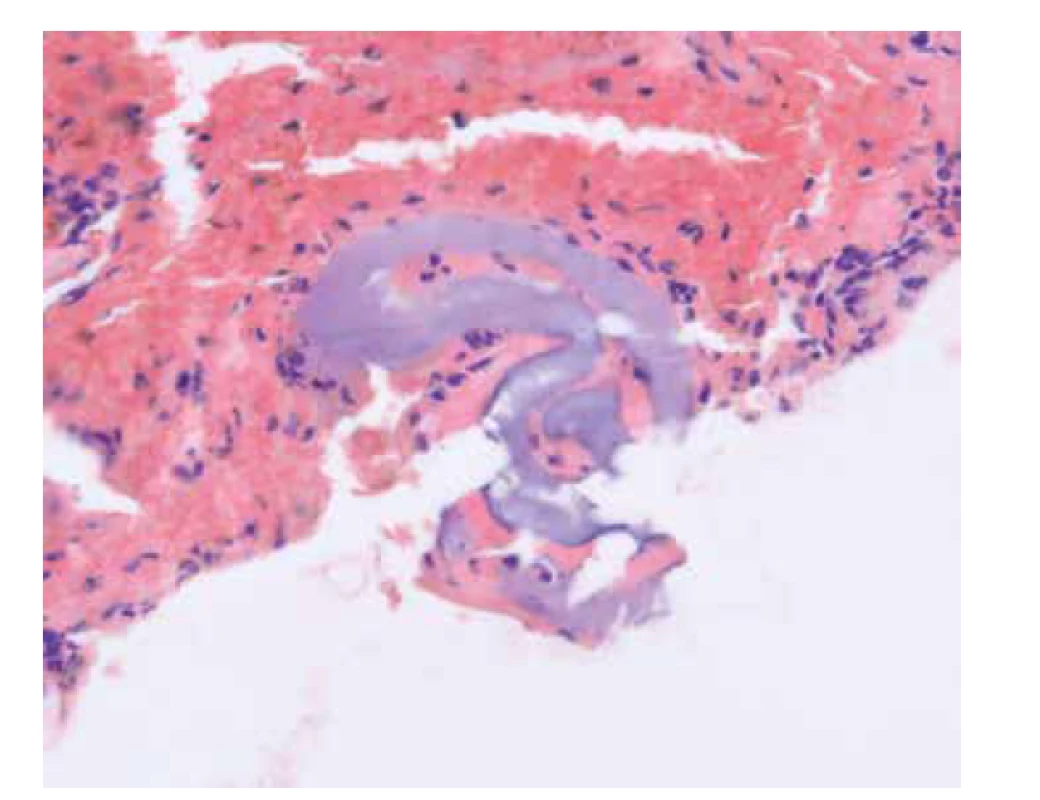
DISKUZE
Rutinní používání endovaskulárních nástrojů potažených polymery může při jejich manipulaci vyústit v disociaci a embolizaci tohoto materiálu. Dle rozsahu postižení embolizovaným materiálem může u pacientů vést k subklinickým změnám ve tkáních ve smyslu drobných infarktů, ale i k fatálním komplikacím vedoucím až ke smrti pacienta (17). A to nejen bezprostředně po embolizaci polymerů, ale i v delším časovém horizontu na podkladě granulomatózních zánětlivých změn (13-16).
V dosud největší retrospektivní studii embolů hydrofilních polymerů (2), autoři cíleně histologicky vyšetřili 110 pitevních případů s anamnézou recentního (1-41 dnů) endovaskulárního zákroku a prokázali v nich 25 případů (23 %) embolizace hydrofilních polymerů. Jednalo se o embolizaci do mozku, ledvin, plic, srdce, sleziny, jater, pankreatu a ojediněle pak do tlustého střeva, žaludku, nadledviny a kosterního svalu. Je pozoruhodné, že v původní nekroptické histologii těchto 25 případů byla zaznamenána přítomnost intravaskulárního cizorodého materiálu jen ve čtyřech. U tří pacientů byla embolizace hydrofilních polymerů možnou příčinou smrti. Obdobně ve studii (1) byla v 83 % původních nekroptických nálezech přehlédnuta přítomnost hydrofilních polymerů. Většina literárních údajů se týká autoptických případů, ojediněle jsou dokumentována podezření na intravitální záchyt (8). Incidence a prevalence tohoto fenoménu není známa. My jsme v naší limitované studii 10 nekroptických případů zachytili dva případy s embolizovaným polymerním materiálem. Ten nevykazoval pozitivitu v barveních speciálními metodami, neobvyklým způsobem se však přibarvoval v barvení saturnovou červení, a to hnědočerně. Tento nález nebyl doposud dokumentován a nejspíše reflektuje biochemické složení a vlastnosti konkrétního použitého polymeru. Vzhledem k omezenému množství případů tedy nelze s jistotou usuzovat na jeho obecnou platnost.
ZÁVĚR
Embolizace hydrofilních polymerů je nově popsanou komplikací endovaskulárních výkonů. Ukazuje se však, že může vést k velmi závažným až fatálním komplikacím. Při pitvě, respektive histologii pacienta, který recentně absolvoval endovaskulární zákrok, je nutno po embolech cíleně pátrat, přičemž si buďme vědomi, že tento cizorodý materiál může být obtížné nalézt a také že může být chybně považován za artefakt.
PROHLÁŠENÍ
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Tato práce vznikla za podpory projektu BBMRI-CZ: Síť biobank – univerzální platforma k výzkumu etiopatogeneze chorob, reg. č.: EF16 013/0001674 a projektu AZV České republiky č. NV19-01-00435.
∗ Adresa pro korespondenci:
MUDr. Monika Manethová
Fingerlandův ústav patologie LF UK a FN Hradec Králové
Sokolská 581, 500 05 Hradec Králové
tel: +420 495 832 896
e-mail: manethom@lfhk.cuni.cz
Zdroje
1. Mehta RI, Mehta RI, Choi JM, et al. Hydrophilic polymer embolism and associated vasculopathy of the lung: prevalence in a retrospective autopsy study. Hum Pathol 2015; 46 : 191-201.
2. Hickey TB, Honig A, Ostry AJ, et al. Iatrogenic embolization following cardiac intervention: postmortem analysis of 110 cases. Cardiovasc Pathol 2019; 40 : 12-18.
3. Mehta RI, Mehta RI. Hydrophilic Polymer Embolism: An Update for Physicians. Am J Med 2017; 130: e287-e290.
4. Shi H, Wang J, Vorvolakos K, et al. Pre-clinical evaluation of surface coating performance in guidewire surrogates: Potential implications for coated interventional surgical devices. J Biomater Appl 2019 : 885328219884453.
5. Thompson AK, Peters MS, El-Azhary RA, et al. Cutaneous microemboli from hydrophilic polymer after endovascular procedures. J Am Acad Dermatol 2015; 73 : 666-671.
6. Chen CL, Chen NC, Wang JS. Acute hydrophilic-polymer nephropathy and acute renal failure. N Engl J Med 2015; 372 : 1775-1776.
7. Chavez JA, Chen W, Frankel WL, et al. Hydrophilic Polymer-associated Ischemic Enterocolitis. Am J Surg Pathol 2017; 41 : 271-276.
8. Simonte G, Isernia G, Fiorucci B, et al. Polymer Embolization and Anaphylactic Reaction during Implantation of an Ovation Stent Graft for Abdominal Aortic Aneurysm Exclusion. Ann Vasc Surg 2018; 50 : 298 e297-298 e211.
9. Chopra AM, Mehta M, Bismuth J, et al. Polymer coating embolism from intravascular medical devices - a clinical literature review. Cardiovasc Pathol 2017; 30 : 45-54.
10. Rapkiewicz A, Hood B, Hutchins K. Fatal Case of Hydrophilic Polymer Emboli. J Forensic Sci 2016; 61 Suppl 1: S268-270.
11. Chopra AM. Analysis: Particulate Limits for Intravascular Devices: Considerations for Polymer Coating Embolism. Biomed Instrum Technol 2019; 53 : 426-432.
12. Allan RW, Alnuaimat H, Edwards WD, et al. Embolization of hydrophilic catheter coating to the lungs: report of a case mimicking granulomatous vasculitis. Am J Clin Pathol 2009; 132 : 794-797.
13. Meiers C, Abebe Y, Alberto NM, et al. Cerebral Granulomatous Inflammation Secondary to Hydrophilic Polymer Embolization Following Thrombectomy. Am J Case Rep 2017; 18 : 507-511.
14. Lorentzen AO, Nome T, Bakke SJ, et al. Cerebral foreign body reaction after carotid aneurysm stenting. Interv Neuroradiol 2016; 22 : 53-57.
15. Rosen LE, Singh RI, Mahon B. Myocardial hydrophilic polymer emboli following cardiac catheterization: a case report and literature review. Cardiovasc Pathol 2014; 23 : 175-177.
16. Geisbush TR, Marks MP, Heit JJ. Cerebral foreign body reaction due to hydrophilic polymer embolization following aneurysm treatment by pipeline flow diversion device. Interv Neuroradiol 2019;25 : 447-453.
17. Yang GK, Mordhorst A, Maguire J, et al. Hydrophilic polymer embolization after thoracic endovascular aortic repair. J Vasc Surg Cases Innov Tech 2019; 5 : 423-426.
Štítky
Patologie Soudní lékařství Toxikologie
Článek ′ CYTODIAGNOSTIKAČlánek ′ UROPATOLOGIEČlánek ′ KARDIOPATOLOGIEČlánek ′ PULMOPATOLOGIEČlánek ′ PATOLOGICKÁ DIAGNOSTIKAČlánek ′ PATOLOGIE MAMMYČlánek ′ PATOLOGIE GITČlánek ′ ORTOPEDICKÁ PATOLOGIEČlánek ′ HEPATOPATOLOGIEČlánek ′ GYNEKOPATOLOGIEČlánek ′ NEFROPATOLOGIEČlánek ′ PATOLOGIE ORL OBLASTIČlánek ′ HEMATOPATOLOGIEČlánek ′ NEUROPATOLOGIEČlánek ′ GYNEKOPATOLOGIEČlánek ′ PATOLOGIE MĚKKÝCH TKÁNÍ
Článek vyšel v časopiseČesko-slovenská patologie

2021 Číslo 1-
Všechny články tohoto čísla
- ′ CYTODIAGNOSTIKA
- ′ UROPATOLOGIE
- ′ KARDIOPATOLOGIE
- Doc. MUDr. Jaroslav Horáček, CSc.
- Základní imunohistochemický panel pro diagnostiku nádorů měkkých tkání
- Vybrané novinky v imunohistochemii a molekulární genetice nádorů měkkých tkání
- Novinky v patologii měkkých tkání a kostí
- Ložiskové léze kostí – diagnostické využití imunohistochemie a molekulární patologie
- Význam časopisu vidím hlavně v jeho doškolovací části
- Iatrogenní embolizace hydrofilních polymerů jako komplikace endovaskulárních výkonů – nová jednotka
- ′ NEUROPATOLOGIE
- Sekundárna hypoplázia pľúc asociovaná s kalcifikovaným Meckelovým divertikulom s oseálnou metapláziou
- ′ GYNEKOPATOLOGIE
- Fabryho choroba s kardiovaskulární manifestací u pacienta s terminálním selháním ledvin
- ′ PULMOPATOLOGIE
- ′ PATOLOGICKÁ DIAGNOSTIKA
-
Konsensuální doporučení České kooperativní skupiny pro nádory hlavy a krku (2019):
definice resekčních okrajů, reportování krčních disekcí a vyšetřování HPV/p16 - Spomienka na prof. MUDr. Ivana Slugeňa, DrSc.
- ′ PATOLOGIE MĚKKÝCH TKÁNÍ
- ′ PATOLOGIE MAMMY
- ′ PATOLOGIE GIT
- ′ ORTOPEDICKÁ PATOLOGIE
- ′ HEPATOPATOLOGIE
- ′ GYNEKOPATOLOGIE
- ′ NEFROPATOLOGIE
- ′ PATOLOGIE ORL OBLASTI
- ′ HEMATOPATOLOGIE
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Základní imunohistochemický panel pro diagnostiku nádorů měkkých tkání
- Ložiskové léze kostí – diagnostické využití imunohistochemie a molekulární patologie
- Sekundárna hypoplázia pľúc asociovaná s kalcifikovaným Meckelovým divertikulom s oseálnou metapláziou
-
Konsensuální doporučení České kooperativní skupiny pro nádory hlavy a krku (2019):
definice resekčních okrajů, reportování krčních disekcí a vyšetřování HPV/p16
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



