-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Postavení CT kolografie v algoritmu vyšetření tlustého střeva
The role of CT colonography in large bowel investigation
CT colonography (CTC, virtual colonoscopy) is a non-invasive colonic imaging method that uses computed tomography (CT) with advanced graphic software to create two-and three-dimensional images of the colon. CTC is indicated mainly for the diagnosis of colorectal neoplasia in cases where conventional colonoscopy is incomplete or contraindicated, as well as in cases where the patient finds conventional colonoscopy intolerable or refuses conventional colonoscopy. Compared to a barium enema, CTC has higher sensitivity for the detection of colorectal neoplasia and has similar or lower levels of radiation exposure. Sensitivity for the detection of polyps ≥ 6 mm is similar to that of conventional colonoscopy. Intravenous injection of iodine contrast media is usually not required; therefore, CTC is safe in patients with iodine allergy or chronic renal failure. Both adequate bowel cleansing and distension are essential to ensure optimal examinations, which are then assessed by radiologists and reported using the standardized C-RADS classification system (CT colonography reporting and data system). CTC does not cover all conventional colonoscopy indications; for instance, CTC is not recommended for the diagnosis of colon inflammatory conditions (including inflammatory bowel disease) or familial polyposis syndromes, and it has low diagnostic value for anal pathologies. CTC is not the official primary method for colorectal cancer screening in the Czech Republic. The aim of this paper is to discuss CTC specifics and indications.
Key words:
CT colonography – virtual colonoscopy – polyp – colorectal cancer – screening – colonoscopySubmitted:
24. 5. 2017Accepted:
26. 9. 2017
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Autoři: H. Straková 1; Ľ. Straka 2
Působiště autorů: Radiodiagnostické oddělení, Uherskohradišťská nemocnice a. s., Uherské Hradiště 1; Gastroenterologická ambulance, Uherskohradišťská nemocnice a. s., Uherské Hradiště 2
Vyšlo v časopise: Gastroent Hepatol 2018; 72(1): 66-72
Kategorie: Digestivní endoskopie: původní práce
doi: https://doi.org/10.14735/amgh201866Souhrn
CT kolografie (CTC, virtuální koloskopie) je neinvazivní vyšetření tlustého střeva výpočetní tomografií (CT), kdy se pomocí speciálního softwaru vytváří dvoj-a trojrozměrný virtuální obraz lumen tračníku. Vyšetření slouží především k diagnostice neoplastických lézí tračníku v případě, že je optická koloskopie neúplná, kontraindikovaná, pacientem netolerovaná či odmítaná. Ve srovnání s dříve prováděnou dvojkontrastní irigografií jde o vyšetření s vyšší senzitivitou pro detekci neoplazií, se stejnou nebo menší radiační zátěží. Senzitivita pro detekci polypů ≥ 6 mm je srovnatelná s optickou koloskopií. Obvykle není nutné parenterální podání jodové kontrastní látky, což činí vyšetření bezpečným i u pacientů s alergií na jód a s renální insuficiencí. Kvalita vyšetření výrazně závisí na dobré přípravě a dostatečné distenzi tračníku. Vyšetření hodnotí lékař radiolog a pro standardizaci radiologického nálezu bylo vytvořeno klasifikační schéma C-RADS (CT colonography reporting and data system). Je potřeba zmínit, že CTC nenahrazuje optickou koloskopii ve všech indikacích – není vhodná k hodnocení zánětlivých onemocnění tračníku, vč. idiopatických střevních zánětů, při podezření na familiární polypózní syndromy, nemá přínos při onemocněních anu. V České republice zatím není CTC schválena jako primární metoda v rámci screeningu kolorektálního karcinomu. Cílem tohoto sdělení je upřesnit postavení CTC v algoritmu vyšetření tlustého střeva.
Klíčová slova:
CT kolografie – virtuální koloskopie – polyp – kolorektální karcinom – screening – koloskopieÚvod
CT kolografie (CTC; používá se i termín virtuální koloskopie) je neinvazivní vyšetření tlustého střeva výpočetní tomografií (CT), kdy se pomocí speciálního grafického softwaru vytváří dvoj-a trojrozměrný virtuální obraz lumen tračníku (obr. 1 a 2). Vzhledem k možnosti hodnocení i extrakolonických změn je před termínem virtuální koloskopie preferováno označení CTC [1].
Obr. 1. Stopkatý polyp rekta na CTC – dvojrozměrný obraz. Fig. 1. Pedunculated rectal polyp on CTC – two-dimensional imaging. 
Obr. 2. Stopkatý polyp rekta na CTC – trojrozměrné zobrazení (stejný polyp jako na obr. 1). Fig. 2. Pedunculated rectal polyp on CTC – three-dimensional imaging (same polyp as shown in Fig. 1). 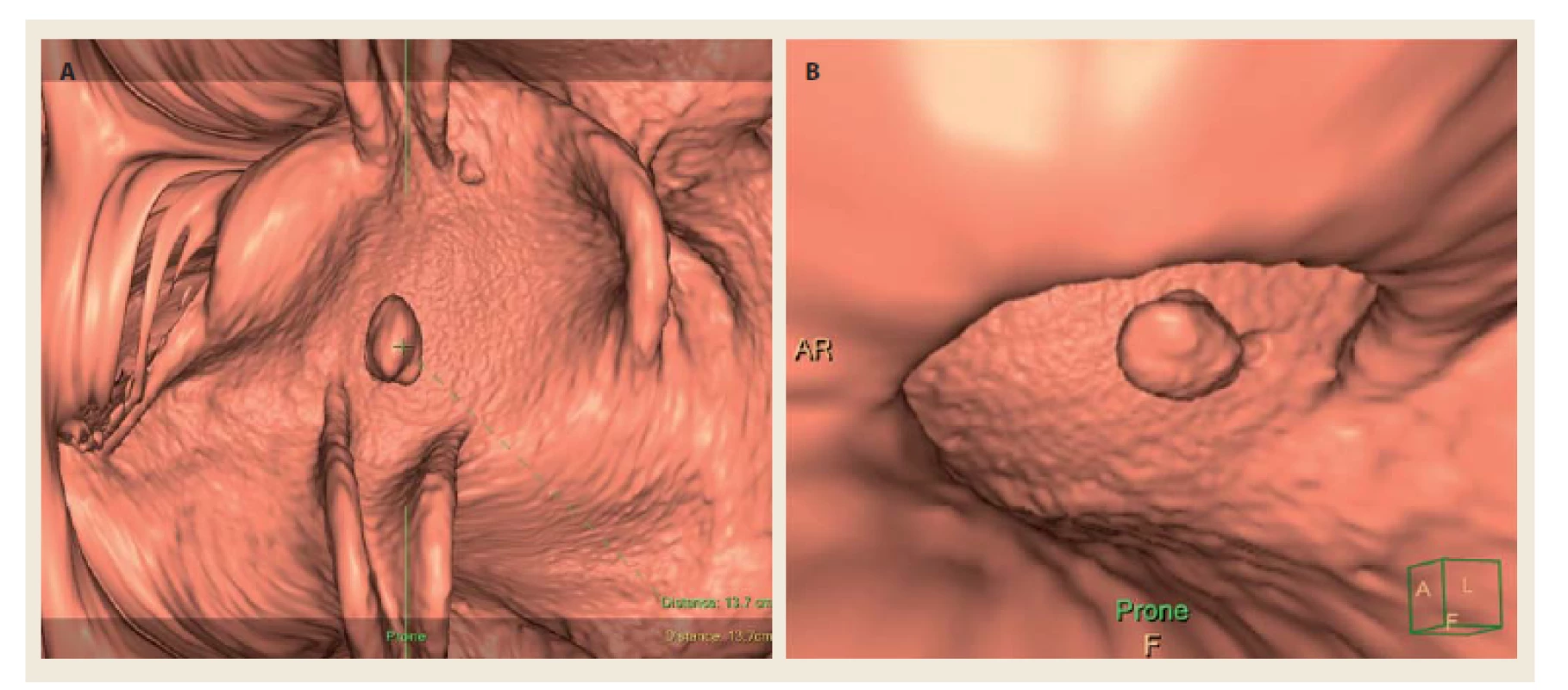
Cílené vyšetření tračníku je dnes doménou oboru gastroenterologie, který tuto část trávicí trubice vyšetřuje pomocí optické koloskopie (OC). Tato metoda v podstatě nahradila radiology prováděnou irigografii, která zejména ve formě dvojkontrastního vyšetření zažila svůj zlatý věk v 70.–90. letech minulého století, rychle se však díky dostupnosti a výhodám endoskopických metod dostala do pozice doplňkového vyšetření v případě, že endoskopie selhala [1,2]. Podobný vliv na snížení počtu irigografií mělo i postupně rutinní použití ultrazvuku (UZ), různých forem CT, popř. magnetické rezonance (MR) při diagnostice onemocnění tračníku.
Nástup CTC v první dekádě 21. století ovlivnilo několik faktorů. Na straně poptávky sehrálo svou roli zavedení Národního screeningu kolorektálního karcinomu, které vedlo ke zvýšení počtu endoskopických vyšetření a s tím souvisejícím zvýšením počtu nedokončených vyšetření a nutností tračník validně došetřit. Na straně nabídky to pak bylo plošné rozšíření multidetektorových CT přístrojů, které díky rychlým akvizičním časům s omezením artefaktů a rutinnímu izotropnímu zobrazení zajišťujícímu vysoké prostorové rozlišení v libovolné rovině umožnily provedení CTC relativně jednoduše a standardně ve vysoké kvalitě [1,2].
Příprava a průběh vyšetření
Aby bylo možno lumen spolehlivě prohlédnout, je při CTC nezbytné důkladné očištění tračníku od zbytků stolice a distenze všech jeho úseků v průběhu scanování.
Mezinárodní doporučení ESGAR (European Society of Gastrointestinal and Abdominal Radiology) [3] pro přípravu tračníku k CTC jsou poměrně obecná, zahrnují dietní opatření v rozumném rozsahu a očistu střevního lumen za použití laxativ. Radiologická literatura ovšem větší důraz než na režimy přípravy tračníku laxativy klade na značení zbytků stolice kontrastní látkou, tzv. faecal tagging. Na našem pracovišti proto vycházíme z doporučení ESGE (European Society of Gastrointestinal Endoscopy) pro přípravu tračníku před koloskopií a v podstatě přejímáme závěry těchto doporučení. Principiálně lze použít dělenou i nedělenou přípravu v závislosti na čase vyšetření. Vzhledem k tomu, že u nás provádíme CTC v ranních hodinách, používáme vždy nedělený režim přípravy. Volbu laxativa necháváme na indikujícím lékaři (obvykle gastroenterolog, chirurg nebo praktický lékař). Jako příklad uvádíme doporučení k přípravě před vyšetřením používané na našem pracovišti (tab. 1).
Tab. 1. Návod k přípravě před CTC na našem pracovišti. Tab. 1. Instructions for bowel cleansing prior CTC used at our department. 
CTC – CT kolografie Jak již bylo zmíněno, nezbytnou součástí přípravy tračníku je faecal tagging [3,4]. Je možné použít jodovou kontrastní látku, baryum, popř. i obě najednou [5]. Výhodou jodové kontrastní látky je homogennější značení zbytkové tekutiny, její použití nevylučuje eventuální OC tentýž den, nečiní problém při případné perforaci. Výhodou barya je absence možných alergických reakcí a podle některých lepší označení solidních zbytků stolice (obr. 3) [5]. Kontrastní látku dodá ve vhodném balení radiodiagnostické pracoviště, které vyšetření provádí. V případě elektivních vyšetření se pije den před vyšetřením, v případě CTC prováděné týž den po nedokončené koloskopii cca 3 hod před vyšetřením. Je vhodné vypracovat srozumitelný, psaný návod k přípravě na CTC, který dané pracoviště distribuuje indikovaným pacientům.
Obr. 3. Faecal tagging baryem – baryem označené zbytky stolice v hepatální flexuře. Fig. 3. Faecal tagging with barium – barium tagged stool in the hepatic flexure. 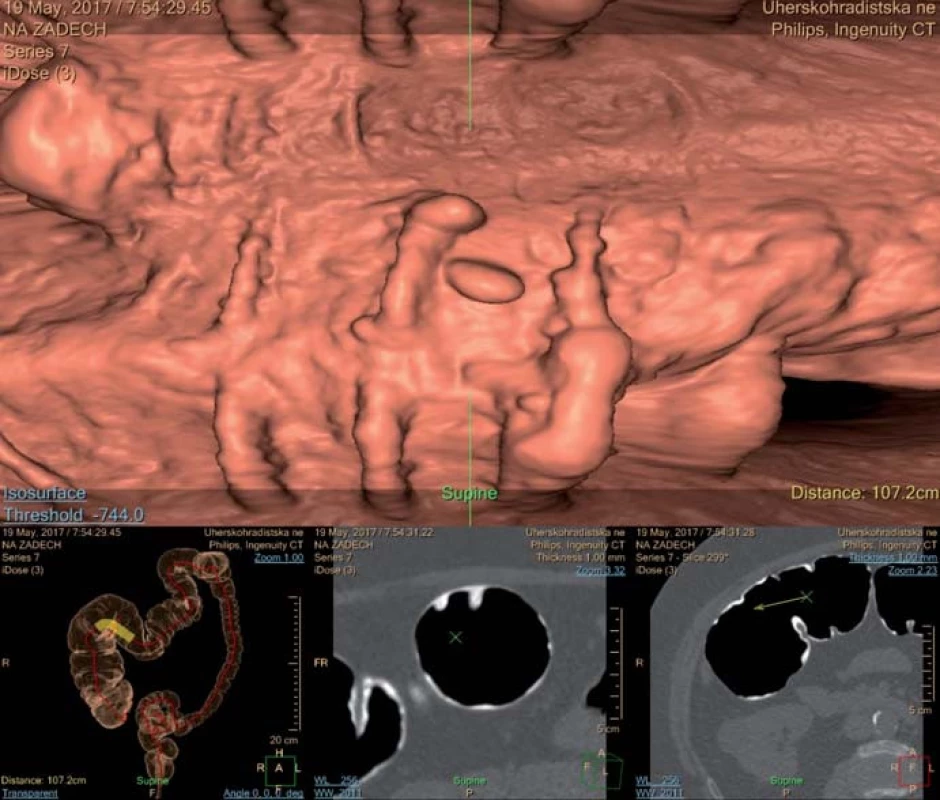
Vlastní vyšetření začíná insuflací tračníku. Tuto lze provést přes rektální rourku manuálně či pomocí speciální pumpy, která potřebný objem zvoleného plynu vhání za monitorace intraluminálního tlaku. Tračník lze distendovat vzduchem nebo oxidem uhličitým. Pokojový vzduch se obvykle insufluje manuálně, oxid uhličitý pumpou, distenze oběma způsoby je dostatečná, insuflace oxidem uhličitým ale vzhledem k rychlejšímu vstřebávání plynu z lumen tračníku zrychluje rekonvalescenci pacienta po vyšetření [2,4]. Insuflace oxidu uhličitého bývá většinou zpoplatněna.
Scanování probíhá obvykle 2×, nejčastěji v poloze na břiše a na zádech (lze doplnit i polohu na levém či pravém boku). To zajistí změnu uložení volného zbytkového intraluminálního obsahu a odkrytí částí stěny, které v předchozí poloze nebylo možno hodnotit. Mezi polohami je možná další insuflace, což umožňuje dodatečnou distenzi dříve kolabovaných úseků tračníku (obr. 4).
Obr. 4. Distenze tračníku. Částečně kolabované sigma v poloze na břiše (A), plně distendované sigma v poloze na zádech u téhož pacienta (B). Fig. 4. Colonic distension. Partially collapsed sigmoid colon in prone position (A), fully distended sigmoid colon in supine position (same patient) (B). 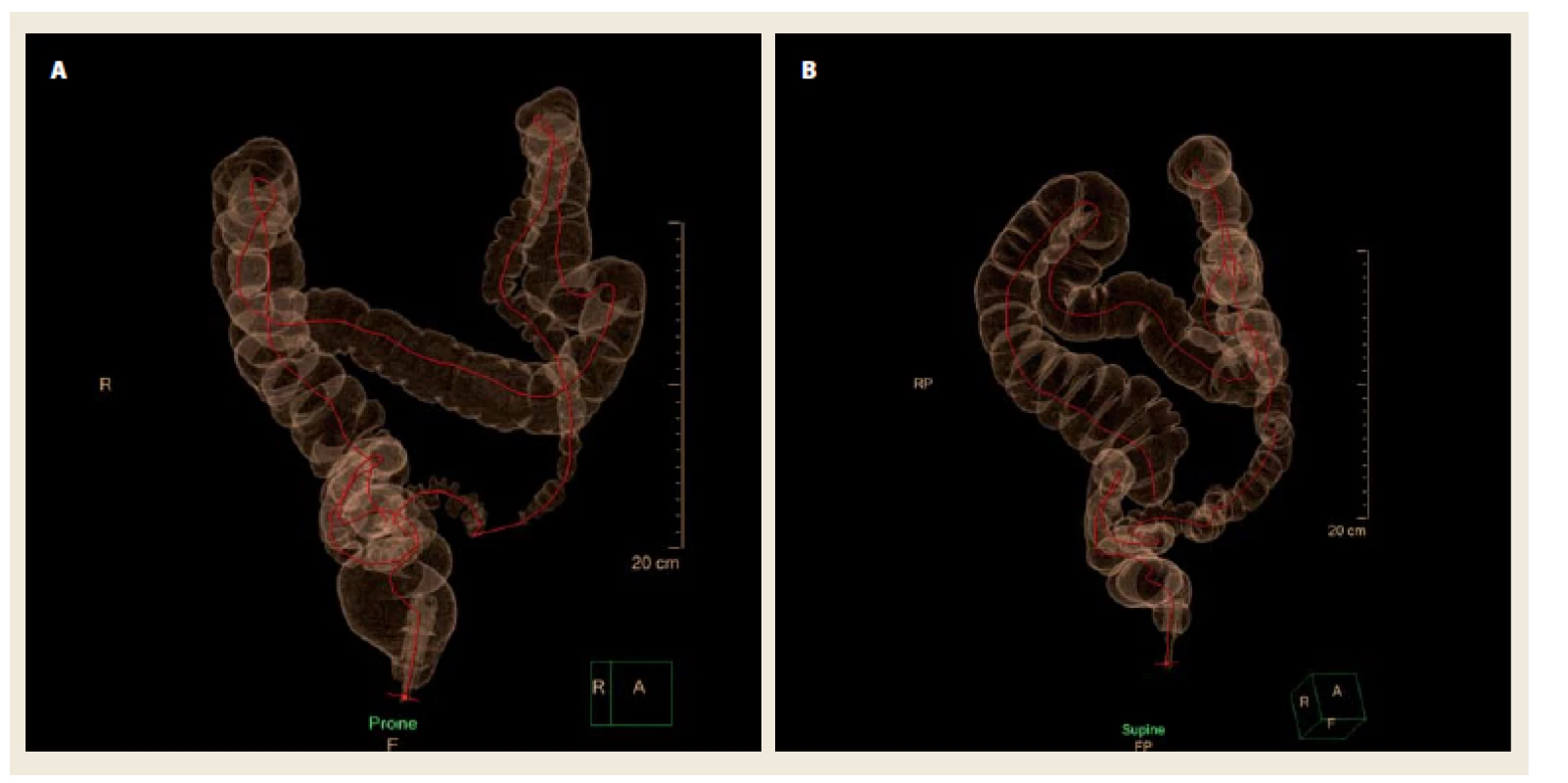
Velmi diskutované je použití spazmolytik v rámci vyšetření. Butylskopolamin bromid nebo glukagon před zahájením insuflace mírně zlepšuje distenzi tračníku, nicméně reálný přínos na zvýšení záchytu polypů nebyl prokázán [2]. Na našem pracovišti podáváme spazmolytika jen v případě současného intravenózního podání jodové kontrastní látky, kdy má pacient zajištěn žilní přístup.
Podání kontrastní látky intravenózně není pro diagnostiku polypů nutné. Kontrastní látka se podává při vysokém podezření na kolorektální karcinom [3] (např. došetření zbytku tračníku za maligní stenózou neprůchodnou pro endoskop), kdy tak lze již provést předoperační staging, popřípadě při nutnosti hodnotit jiný extrakolonický nález. Postkontrastní scanování se provádí v po-loze na zádech, nejčastěji v portální venózní fázi.
Hodnocení vyšetření
Vyšetření hodnotí lékař radiolog školený v této metodě, průměrný čas hodnocení se podle dostupných pramenů pohybuje v rozmezí 15–20 min [6,7]. Popisují se léze velikosti ≥ 6 mm [3,4], zaznamenává se jejich velikost (největší rozměr, u stopkatých bez stopky), tvar (sesilní, stopkatá, plochá), denzita (měkkotkáňová, tuk), poloha (rektum, sigma, descendens, transversum, ascendens, cékum). U lézí < 6 mm (diminutivních polypů) má CTC omezený diagnostický přínos – zvyšuje se pravděpodobnost falešně pozitivního nálezu, riziko malignity a malignizace je velmi nízké. Pro standardizaci radiologického nálezu bylo vytvořeno klasifikační schéma C-RADS (CT colonography reporting and data system), které přehledně zařazuje kolonické i extrakolonické nálezy dle závažnosti, a usnadňuje tak další léčebný postup (tab. 2) [4].
Tab. 2. C-RADS klasifikace. Tab. 2. C-RADS classifcation. 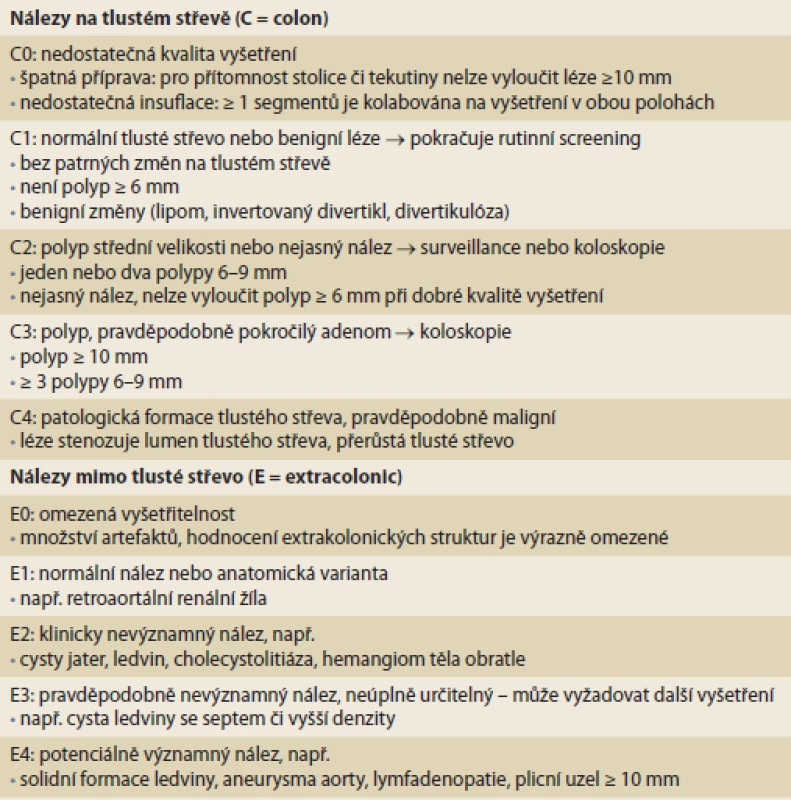
Indikace a kontraindikace
Vyšetření slouží především k diagnostice neoplastických lézí tračníku v případě, že je OC neúplná, kontraindikovaná, pacientem netolerovaná či odmítaná. Z radiologických vyšetření (irigografie, běžné CT břicha, event. UZ) jde o metodu s nejvyšší senzitivitou. Na tomto místě je třeba zdůraznit skutečnost, že CTC nenahrazuje endoskopické zobrazení tračníku ve všech indikacích – není vhodná k hodnocení zánětlivých onemocnění tračníku. Naopak, akutní kolitida a divertikulitida jsou kontraindikacemi CTC [4,8], zvyšují riziko komplikací CTC (perforace) [9], k jejich došetření obvykle postačí UZ, event. v kombinaci se standardním CT břicha. Pro diagnostiku idiopatických střevních zánětů je z radiologických metod vhodnější CT/MR enterografie, která lépe zobrazí tenké střevo. Vyšetření dále nemá přínos při onemocněních anu [1,4].
Podrobně se indikacím k CTC věnují doporučení vydaná v roce 2014 ESGE a ESGAR [9]. V případě nedokončené endoskopie doporučují doplňující CTC optimálně tentýž či následující den za podmínky, že při OC nebyla provedena polypektomie či mukosektomie. Z praktického hlediska je ale tento timing nutno přizpůsobit reálným možnostem daného radiodiagnostického pracoviště. V případě, že při OC byla zjištěna maligní stenóza neprůchodná pro endoskop, doporučuje se provést CTC k vyloučení synchronního kolorektálního karcinomu (vyskytuje se v cca 3,9 %) [10]. Jak již bylo zmíněno, při podání jodové kontrastní látky intravenózně je možno CTC použít i k předoperačnímu stagingu. Doporučení se také zabývají návazností endoskopie po provedené CTC – OC s polypektomií je doporučována již při nálezu jediného polypu ≥ 6 mm. Pokud polypektomie není z jakéhokoli důvodu možná, je alternativou sledování pomocí CTC.
Kontraindikacemi vyšetření jsou podezření na perforaci, ileus, toxické megalokolon, dále symptomatická břišní kýla obsahující tračník, akutní průjem, kolitida, divertikulitida cca do 6 týdnů po odeznění, stav po recentním chirurgickém výkonu na tračníku (4–6 týdnů), stavy po endoskopických resekcích (2 týdny) [4,8,9].
Přehledně jsou indikace a kontraindikace shrnuty v tab. 3 a 4.
Tab. 3. Indikace k CTC. Tab. 3. CTC indications. 
CTC – CT kolografie, OC – optická koloskopie Tab. 4. Kontraindikace CTC. Tab. 4. CTC contraindications. 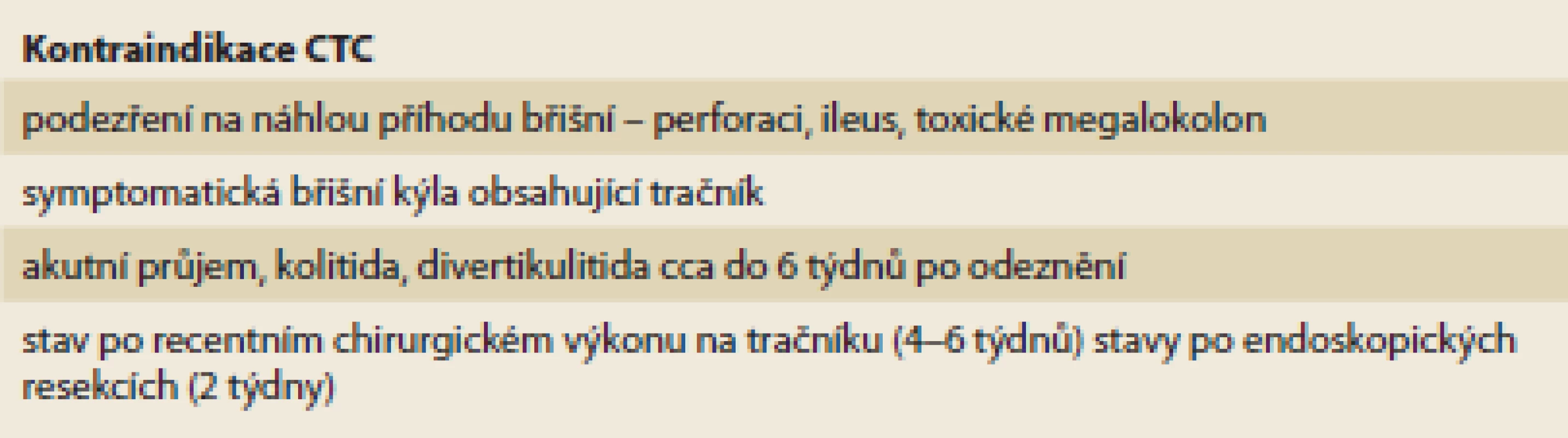
CTC – CT kolografie Srovnání CTC a optické koloskopie
Senzitivita CTC pro detekci polypů ≥ 6 mm je srovnatelná se senzitivitou OC [6,7,11,12].
Toto potvrdily např. výsledky studie Department of defense CT colonography screening trial z roku 2003, která zahrnovala 1 233 asymptomatických jedinců podstoupivších tentýž den CTC i OC. Výsledky jsou uvedeny v tab. 5 [7].
Tab. 5. Sensitivita optické koloskopie (OC) a CT kolografie (CTC) dle DoD Trial [7]. Tab. 5. Sensitivity of conventional colonoscopy (OC) and CT colonography (CTC) according to the DoD Trial [7]. ![Sensitivita optické koloskopie (OC) a CT kolografie (CTC) dle DoD Trial [7].
Tab. 5. Sensitivity of conventional colonoscopy (OC) and CT colonography (CTC) according to the DoD Trial [7].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/af5fff9934dcd105468c55cc138b8387.png)
Rovněž metanalýza z roku 2011 zahrnující celkem 11 151 pacientů ze 49 stu-dií, u nichž byla provedena CTC, OC i histologická verifikace, prokázala senzitivitu CTC pro záchyt kolorektálního karcinomu 96,1 % (senzitivita OC 94,7 %) [11].
Srovnatelný 11% záchyt (CTC i OC) kolorektálního karcinomu a polypů ≥ 10 mm (detection rate of colorectal cancer or large polyps) prokázala studie SIGGAR publikovaná v roce 2013 [12]. Zde bylo celkem 1 610 symptomatických pacientů s podezřením na kolorektální karcinom náhodně rozděleno do dvou skupin a vyšetřeno pomocí CTC či OC.
Literatura opakovaně uvádí nižší senzitivitu CTC pro ploché léze [1,13]. Tématem se zabývalo několik studií [14–16], všechny však pracovaly s malými počty pacientů a jejich výsledky se různí. Pro relevantní závěry bude nutné vyčkat na další data.
Hlavní výhody OC proti CTC představují možnost přímého zákroku na objevené lézi tračníku, absence radiační zátěže a vyšší senzitivita u malých (< 6 mm) a plochých lézí [13]. Výhody CTC proti OC jsou pak minimální invazivita, zanedbatelné riziko iatrogenní perforace (0,005–0,03% CTC; 0,1% OC; 0,004–0,2% irigografie [17]), absence potřeby analgosedace vyšetřovaného, možnost vyšetření tračníku za stenózou, přínos v podobě extrakolonických nálezů zjištěných při CTC.
Srovnání tolerance obou vyšetření samotnými pacienty řešila naposled Plumbova studie z roku 2017 [18]. Jednalo se o retrospektivní dotazníkové šetření, na něž odpovědělo 52 805 vyšetřených podstoupivších screeningovou koloskopii. Byly zjištěny jen minimální rozdíly ve vnímání dyskomfortu provázejícím jednotlivé metody.
Srovnání CTC a irigografie
Jak již bylo výše zmíněno, irigografické vyšetření tračníku, vč. metody dvojkontrastní irigografie, bylo postupně vytlačeno endoskopickými metodami a dostalo se do pozice doplňkové metody k došetření tračníku při inkompletní koloskopii. Literární data zabývající se senzitivitou dvojkontrastní irigografie pro detekci polypů se různí, uváděna je senzitivita od 45 % [19] po 87 % [2]. Recentní studie SIGGAR publikovaná v roce 2013 prokázala v případě CTC signifikantně vyšší záchyt kolorektálního karcinomu nebo polypů ≥ 10 mm 7,3% CTC, resp. 5,6% irigografii [20]. Vzhledem k reálně se snižujícím až mizejícím zkušenostem mladších radiologů s metodou irigografie lze navíc předpokládat další posun k nižším hodnotám senzitivity.
Nezanedbatelným faktem hrajícím ve prospěch CTC je rovněž skutečnost, že radiační zátěž při standardizované irigografii se odhaduje na 7,2 mSv [21], zatímco při CTC lze běžně dosáhnout efektivní dávky 3 mSv i méně [2,4].
Z praktického hlediska je nezbytné zmínit, že irigografie je ve srovnání s CTC vyšetření pracnější, časově náročnější, pacientem (i vyšetřujícím radiologem) hůře snášené.
V guidelines ESGE/ESGAR z roku 2014 je výslovně uvedeno, že irigografie se pro diagnostiku kolorektálního karcinomu nedoporučuje [9].
Screening kolorektálního karcinomu
V ČR zatím není CTC schválena jako primární metoda v rámci screeningu kolorektálního karcinomu. Ve Spojených státech ale některé společnosti (American Cancer Society, American College of Radiology) CTC jako oficiální screeningovou metodu uznávají [2]. Provádí se 1× za 5 let u jedinců s průměrným rizikem ve věku 50–80 let.
Guidelines ESGE/ESGAR z roku 2014 [9] CTC v této indikaci zatím plošně nedoporučují – jako hlavní problém uvádí dosud nejasnou rentabilitu metody (cost-effectiveness) (při CTC nálezu polypů je obvykle nutno provést OC, extrakolonické nálezy indukují další diagnostiku a léčbu). V případě pacientů s pozitivním testem na okultní krvácení (zjištěným v rámci screeningu), u nichž je OC nekompletní či neproveditelná, je však provedení CTC důrazně doporučováno.
Závěr
CTC v současné době představuje rozšířenou metodu, kterou je možno spolehlivě diagnostikovat polypy tračníku ≥ 6 mm, se senzitivitou srovnatelnou s OC. Kvalita vyšetření výrazně závisí na dobré přípravě a dostatečné distenzi tračníku. Indikací je především diagnostika neoplastických lézí tračníku v případě, že je OC neúplná, kontraindikovaná, pacientem netolerovaná či odmítaná. Vyšetření je metodou volby pro zobrazení tračníku za endoskopicky prokázanou stenózou neprůchodnou pro endoskop. V případě maligní stenózy je možné současné intravenózní podání jodové kontrastní látky a provedení stagingu onemocnění. CTC nenahrazuje endoskopické vyšetření tračníku ve všech indikacích – není vhodná k hodnocení zánětlivých onemocnění tračníku, vč. idiopatických střevních zánětů, při podezření na familiární polypózní syndromy, nemá přínos při onemocněních anu. V ČR zatím není CTC schválena jako primární metoda v rámci screeningu kolorektálního karcinomu.
Jak z výše uvedeného vyplývá, v diagnostickém algoritmu vyšetření tlustého střeva není vztah OC a CTC kompetitivní, ale za všech okolností komplementární.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 24. 5. 2017
Přijato: 26. 9. 2017
MUDr. Hana Straková
Radiodiagnostické oddělení
Uherskohradišťská nemocnice, a. s.
J. E. Purkyně 365
686 68 Uherské Hradiště
E-mail: pihana@centrum.cz
Zdroje
1. Bartušek D, Falt P, Tachecí I et al. Alternativní vyšetření tlustého střeva. In: Falt P, Urban O, Vítek P et al. Koloskopie. Praha: Grada Publishing, a. s. 2015 : 285–296.
2. Levine MS, Yee J. History, evolution, and current status of radiologic imaging tests for colorect-al cancer screening. Radiology 2014; 273 (2 Suppl): S160–S180. doi: 10.1148/radiol.14140 531.
3. Neri E, Halligan S, Helström M et al. The second ESGAR consensus statement on CT colonography. Eur Radiol 2013; 23 (3): 720–729. doi: 10.1007/s00330-012-2632-x.
4. Lambert L, Šimáková L. Přínos CT kolografie v klinické praxi. Vnitř Lék 2017; 63 (3): 183–187.
5. Pickhardt PJ, Kim DH. CT colonography: pitfalls in interpretation. Radiol Clin North Am 2013; 51 (1): 69–88. doi: 10.1016/j.rcl.2012.09. 005.
6. Johnson CD, Chen MH, Toledano AY. Accuracy of CT colonography for detection of large adenomas and cancers. N Engl J Med 2008; 359 (12): 1207–1217. doi: 10.1056/NEJMoa0800 996.
7. Pickhardt PJ, Choi JR, Hwang I. Computed tomographic virtual colonoscopy to screen for colorectal neoplasia in asymptomatic adults. N Engl J Med 2003; 349 (23): 2191–2200. doi: 10.1056/NEJMoa031618.
8. Morrin M, Fenlon H. Guidelines for use of CT colonography (CTC) as a part of the national colorectal screening programme in Ireland. [online]. Available from: http: //www.radiology.ie/wp-content/uploads/2012/01/Guidelines-for-Use-of-CT-Colonography-CTC-as-Part-of-the-National-Colorectal-Screening-Programme-in-Ireland1.pdf.
9. Spada C, Stoker J, Alarcon O et al. Clinical indications for computed tomographic colonography: European Society of Gastrointestinal Endoscopy (ESGE) and European Society of Gastrointestinal and Abdominal Radiology (ESGAR) Guideline. Endoscopy 2014; 46 (10): 897–915. doi: 10.1055/s-0034-1378092.
10. Mulder SA, Kranse R, Damhuis RA et al. Prevalence and prognosis of synchronous colorectal cancer: a Dutch population-based study. Cancer Epidemiol 2011; 35 (5): 442–447. doi: 10.1016/j.canep.2010.12.007.
11. Pickhardt PJ, Hassan C, Halligan S et al. Colorectal cancer: CT colonography and colonoscopy for detection – systematic review and meta-analysis. Radiology 2011; 259 (2): 393–405. doi: 10.1148/radiol.11101887.
12. Atkin W, Dadswell E, Wooldrage K et al. Computed tomographic colonography versus colonoscopy for investigation of patients with symptoms suggestive of colorectal cancer (SIGGAR): a multicentre randomised trial. Lancet 2013; 381 (9873): 1194–1202. doi: 10.1016/ S0140-6736 (12) 62186-2.
13. Dachman AH, Yee J. The challenges of CT colonography reimbursement. J Am Coll Radiol 2013; 10 (12): 937–942. doi: 10.1016/j.jacr.2013.09.014.
14. Park SH, Kim SY, Lee SS et al. Sensitivity of CT colonography for nonpolypoid colorectal lesions interpreted by human readers and with computer-aided detection. AJR Am J Roentgenol 2009; 193 (1): 70–78. doi: 10.2214/AJR.08. 2234.
15. Pickhardt PJ, Nugent PA, Choi JR et al. Flat colorectal lesions in asymptomatic adults: implications for screening with CT virtual colonoscopy. Am J Roentgenol 2004; 183 : 1343–1347. 10.2214/ajr.183.5.1831343.
16. Sakamoto T, Mitsuzaki K, Utsunomiya D et al. Detection of flat colorectal polyps at screening CT colonography in comparison with conventional polypoid lesions. Acta Radiol 2012; 53 (7): 714–719. doi: 10.1258/ar.2012.110 685.
17. Berrington de Gonzales A, Kim KP, Yee J. CT colonography: perforation rates and potential radiation risks. Gastrointest Endosc Clin N Am 2010; 20 (2): 279–291. doi: 10.1016/j.giec. 2010. 02.003.
18. Plumb AA, Ghanouni A, Rees CJ et al. Patient experience of CT colonography and colonoscopy after fecal occult blood test in a national screening programme. Eur Radiol 2017; 27 (3): 1052–1063. doi: 10.1007/s00330-016-4428-x.
19. Ramos C, De Jesús-Caraballo J, Toro DH et al. Is barium enema an adequate diagnostic test for the evaluation of patients with positive fecal occult blood? Bol Asoc Med P R 2009; 101 (2): 23–28.
20. Halligan S, Wooldrage K, Dadswell E et al. Computed tomographic colonography versus barium enema for diagnosis of colorectal cancer or large polyps in symptomatic patients (SIGGAR): a multicentre randomised trial. Lancet 2013; 381 (9873): 1185–1193. doi: 10.1016/S0140-6736 (12) 62124-2.
21. Věstník MZČR 11-2003. [online]. Available from: https: //www.mzcr.cz/Legislativa/dokumenty/vestnik_3662_1782_11.html.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2018 Číslo 1- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Kvalita života pacientů s idiopatickými střevními záněty v České republice – multicentrická studie
- Výsledky těhotenství u pacientek s idiopatickými střevními záněty léčených biosimilárním infliximabem
- Odporúčania Pracovnej skupiny pre IBD Slovenskej gastroenterologickej spoločnosti pre liečbu Crohnovej choroby
- Terapeutické monitorovanie infliximabu pri nešpecifických zápalových ochoreniach čreva
- Efekt ustekinumabu u pacienta refrakterního na ostatní biologickou léčbu
- Novinky v roce 2018
- Onemocnění gastrointestinálního traktu a choroby ledvin
- Porovnání nákladové efektivity okamžitě zahájené léčby oproti odložené terapii chronické hepatitidy C v České republice
- Můžeme zvýšit efektivitu léčby anti-TNF protilátkami?
- Postavení CT kolografie v algoritmu vyšetření tlustého střeva
- Endoskopické řešení Bueveretova syndromu
- K úmrtí doc. MUDr. Zdeňka Slezáka, CSc.
- Výběr z mezinárodních časopisů
- Mladá žena s expanzivním procesem v pravém hypogastriu
- Správná odpověď na kvíz
- Kreditovaný autodidaktický test: IBD
- VSL#3 – první vysoce koncentrované probiotikum s mnohočetnými probiotickými kulturami a ověřenou terapeutickou účinností
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- VSL#3 – první vysoce koncentrované probiotikum s mnohočetnými probiotickými kulturami a ověřenou terapeutickou účinností
- Onemocnění gastrointestinálního traktu a choroby ledvin
- Postavení CT kolografie v algoritmu vyšetření tlustého střeva
- Odporúčania Pracovnej skupiny pre IBD Slovenskej gastroenterologickej spoločnosti pre liečbu Crohnovej choroby
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



