-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Vliv dlouhodobé terapie inzulinovou pumpou (CSII) u pacientů s diabetes mellitus 1. typu na metabolickou kompenzaci a výskyt hypoglykemií. Porovnání s intenzifikovanou konvenční inzulinovou terapií (MDI)
The influence of long-term therapy with the insulin pump (CSII) in patients with type 1 diabetes mellitus on metabolic compensation and on the incidence of hypoglycaemia. Comparison with intensified conventional insulin therapy (MDI)
The principal objective of this paper is to verify, in clinical practice, the long-term affect (7 to 8 year follow up) and safety of insulin pump treatment in type 1 diabetes mellitus patients and to compare the results for diabetes compensation in patients treated with the insulin pump with a control group of patients treated with intensified insulin therapy using the MDI (multiple daily injection) method.
Patient sample and method:
We followed up 35 patients treated with the insulin pump and 35 patients in the control group. We evaluated the monitored parameters for both patient groups at the beginning and at the end of the follow up period. With respect to glycated haemoglobin, we evaluated the results on a yearly basis, and also on year by year changes. We assessed the incidence of hypoglycaemia in both groups on a yearly basis. The following aspects were considered in order to determine the level of statistical significance of the different parameters: 1. we compared the initial state with that seen at the end of the follow up, 2. we analysed the year by year changes in glycated haemoglobin, 3. we compared the patients treated with the insulin pump with those in the control group. Diabetes compensation was evaluated on the basis of measurement of glycated haemoglobin and calculation of glycaemia. Comparison of the incidence of hypoglycaemia was done for all hypoglycemic events and then separately for severe hypoglycaemia. Also evaluated were changes in weight and in insulin dose in 24 hours.Results:
The group of patients treated with the insulin pump recorded a dramatic decrease in glycated haemoglobin in the course of the follow up, p < 0.001, and also in average glycaemia, p < 0.001. In the control group only a transitory significant decrease of HbA1c, p < 0.05, was recorded in the first and second year of follow up, later the result was insignificant, i.e. p > 0.05, as compared with the initial state. In this group of patients, no significant improvement in average glycaemia, p > 0.05, was recorded when compared with the initial state. Comparison of the two groups of patients showed that HbA1c, p < 0.001, and average glycaemia, p < 0.001, were worse with statistical significance in patients treated with the insulin pump at the beginning of the follow up. At the end of the follow up period, there was no significant difference between the two groups in terms of glycated haemoglobin, p > 0.05, but a statistically significant difference was recorded in average glycaemia, p < 0.001, in favour of the group of patients treated with the insulin pump. The use of the insulin pump resulted in a statistically significant decrease in the incidence of severe hypoglycaemic events as compared with the control group, p = 0.010. This decrease was reflected in the measured parameters from the third year of the study to the end of follow up. However, at the beginning of the study and in the first and second years of follow up there was no statistically significant difference between the two groups in terms of incidence of severe hypoglycaemic episodes, p > 0.05. No statistically significant difference between the two groups was recorded in the incidence of all hypoglycaemic episodes from the beginning of the follow up to its end, p > 0.05. In both groups of patients, a statistically significant gain in weight was seen from the beginning of the study to the end of the follow up period, however, its statistical significance was lower (p < 0.05) in the group of patients treated with insulin pump than in the control group (p < 0.001). We proved a statistically significant decrease in daily insulin dose (p < 0.001)was required in the group of patients treated with insulin pump, whilst no statistically significant change in the dose was recorded in the control group (p > 0.05).Conclusion:
In the course of the follow up, we proved that treatment with the insulin pump in type 1 diabetes is more beneficial to patients than MDI treatment. This was reflected by both better compensation of diabetes and a lower incidence of severe hypoglycaemic episodes.Key words:
type 1 diabetes mellitus – insulin pump – diabetes compensation – glycated haemoglobin – average glycaemia – hypoglycaemia
Autoři: J. Olšovský 1; M. Beránek 2
Působiště autorů: II. interní klinika Lékařské fakulty MU a FN u sv. Anny, Brno, přednosta doc. MUDr. Miroslav Souček, CSc. 1; Ústav patologické fyziologie Lékařské fakulty MU Brno, přednostka prof. MUDr. Anna Vašků, CSc. 2
Vyšlo v časopise: Vnitř Lék 2007; 53(6): 637-645
Kategorie: Původní práce
Souhrn
Hlavním cílem práce bylo ověřit v klinické praxi dlouhodobou (7-8leté sledování) účinnost a bezpečnost léčby inzulinovou pumpou u pacientů s diabetes mellitus 1. typu a porovnat výsledky kompenzace diabetu u nemocných léčených inzulinovou pumpou s kontrolní skupinou nemocných léčených intenzifikovanou inzulinovou terapií metodou MDI (multiple daily injection).
Soubor nemocných a metody:
Sledovali jsme 35 osob léčených inzulinovou pumpou a 35 osob v kontrolní skupině. U obou skupin nemocných jsme vyhodnotili sledované parametry na počátku a konci sledování, u glykovaného hemoglobinu jsme hodnotili výsledky ročně a hodnotili i meziroční změny, výskyt hypoglykemií v obou skupinách jsme porovnávali každoročně. Pro zjištění statistické hladiny významnosti u jednotlivých parametrů jsme vycházeli z těchto hledisek: 1. porovnávali jsme výchozí počáteční stav se stavem na konci sledování, 2. analyzovali jsme meziroční změny u glykovaného hemoglobinu, 3. srovnali jsme pacienty léčené inzulinovou pumpou s kontrolní skupinou. Kompenzace diabetu byla hodnocena na základě měření glykovaného hemoglobinu a výpočtu průměrné glykemie. Porovnání výskytu hypoglykemických příhod jsme provedli zvlášť pro všechny hypoglykemické příhody a zvlášť pro závažné hypoglykemie, hodnotili jsme změny hmotnosti a také změny dávek inzulinu za 24 hodin.Výsledky:
Ve skupině nemocných léčených inzulinovou pumpou došlo v průběhu sledování ke statisticky významnému poklesu glykovaného hemoglobinu, p < 0,001 i průměrné glykemie, p < 0,001. V kontrolní skupině došlo jen k přechodnému signifikantnímu snížení HbA1c, p < 0,05, a to jen v 1. a 2. roce sledování , později byl výsledek v porovnání s počátečním stavem nesignifikantní, p > 0,05. V této skupině nemocných nedošlo také na konci sledování při porovnání s výchozím stavem k signifikantnímu zlepšení v průměrné glykemii, p > 0,05. Při porovnání obou skupin nemocných byl na počátku sledování statisticky významně horší HbA1c, p < 0,001 i průměrná glykemie, p < 0,001 ve skupině nemocných léčených pumpou. Na konci sledování při porovnání obou skupin nemocných nebyl shledán signifikantní rozdíl v glykovaném hemoglobinu, p > 0,05, ale byl shledán statisticky významný rozdíl v průměrné glykemii, p < 0,001, ve prospěch skupiny nemocných léčených inzulinovou pumpou. Využití inzulinové pumpy vedlo k statisticky významně nižšímu výskytu závažných hypoglykemií ve skupině nemocných léčených inzulinovou pumpou oproti kontrolní skupině, p = 0,010, které se projevovalo od 3. roku do konce sledování, jinak na počátku a v prvém a druhém roce sledování statisticky významný rozdíl ve výskytu závažných hypoglykemií mezi oběma skupinami nebyl, p > 0,05. Ve výskytu všech hypoglykemií nebyl pozorován statisticky významný rozdíl mezi oběma skupinami od počátku sledování až do jeho konce, p > 0,05. V obou skupinách nemocných jsme prokázali statisticky významný vzestup hmotnosti při porovnání stavu na počátku a na konci sledování, tento však měl menší statistickou významnost (p < 0,05) ve skupině nemocných léčených inzulinovou pumpou než ve skupině kontrolní (p < 0,001). Ve skupině nemocných léčených inzulinovou pumpou jsme prokázali statisticky významný pokles denní dávky inzulinu (p < 0,001), zatímco ve skupině kontrolní se dávka statisticky významně nezměnila (p > 0,05).Závěr:
V průběhu našeho sledování jsme prokázali skutečný benefit léčby inzulinovou pumpou u diabetiků 1. typu oproti léčbě MDI . Tento se projevil jednak v lepší kompenzaci diabetu i nižším výskytu závažných hypoglykemií.Klíčová slova :
diabetes mellitus 1. typu - inzulinová pumpa - kompenzace diabetu - glykovaný hemoglobin - průměrná glykemie - hypoglykemieÚvod
Diabetes mellitus 1. (DM1T) typu jako dosud nevyléčitelné onemocnění komplikuje svým nositelům další život rozvojem cévních komplikací, především mikrovaskulárních, ale i makrovaskulárních. Tyto komplikace zhoršují jak kvalitu jejich života, tak i délku. Vývoj mikrovaskulárních komplikací vychází nesporně z genetických základů, ale umocněn je především neuspokojivou metabolickou kompenzací - tedy hyperglykemií, tak jak to dokazují četná klinická pozorování [1,2]. Genetika komplikací je podrobována intenzivnímu studiu, ale případné terapeutické zásahy v této oblasti jsou dnes nemožné.
V současnosti jedinou racionální cestou ke zlepšení prognózy nemocných s DM1T je co nejlepší metabolická kompenzace, resp. normoglykemie [3-6]. Je to jistě i příčinou, proč se neustále zpřísňují kritéria kompenzace diabetu, a to také podle standardů České diabetologické společnosti (ČDS), kdy hodnoty glykemie nalačno nad 7 mmol/l, glykemie postprandiálně nad 9 mmol/l a HbA1c nad 6 % podle hodnocení International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) představují již neuspokojivou kompenzaci. O výbornou, případně uspokojivou kompenzaci diabetika usiluje diabetolog ve spolupráci s pacientem samotným s využitím všech léčebných prostředků. Těmito prostředky jsou edukace, dieta, pohyb, režimová opatření, ale především inzulinová léčba a selfmonitoring glykemií. Všechna tato opatření musejí být ve vzájemném propojení a souladu, jinak úspěch nelze očekávat.
Existuje řada inzulinových režimů, ve kterých lze ve prospěch kompenzace nemocného využít jak humánní inzuliny, tak také krátkodobá a dlouhodobá analoga inzulinu. Využití dlouhodobých analog inzulinu je považováno za určitý předstupeň léčby inzulinovou pumpou, protože dlouhodobá analoga (glargin, detemir) velmi dobře napodobují bazální sekreci inzulinu, na rozdíl od humánního Neutral-Protamin-Hagedorn (NPH) inzulinu. Krátkodobá analoga potom optimálně nahrazují stimulovanou sekreci inzulinu. Rozdíl léčby intenzifikovaným režimem s využitím kombinace krátkodobého a dlouhodobého analoga inzulinu oproti léčbě inzulinovou pumpou však zůstává v nemožnosti bazální dávku až do příští aplikace dlouhodobého analoga změnit, zatímco bazální dávku podávanou pumpou lze upravit kdykoliv okamžitě. Obecně existuje intenzifikovaná inzulinová terapie (IIT), představovaná 3 a více dávkami inzulinu za den a konvenční inzulinová terapie, představovaná 2 a méně dávkami inzulinu v průběhu dne. Intenzifikovaná léčba je nejčastěji vedena cestou mnohočetných denních injekcí inzulinu (multiple daily injections - MDI).
Pokud navzdory využití všech uvedených variant inzulinové léčby a také všech ostatních léčebných prostředků (edukace, dieta, režimová opatření, pohybový režim) nejsme nadále schopni uspokojivé kompenzace nemocného dosáhnout, případně se potýkáme s dalšími specifickými problémy, jako jsou hypoglykemie, potřeba flexibility režimu apod, přichází v úvahu jako určitý vrchol léčebných možností léčba inzulinovou pumpou. Tato je vnímána jako nejbližší fyziologii inzulinové sekrece, a tedy nejnadějnější v dosažení optimální metabolické kontroly - normoglykemie [7]. Tím také poskytuje potenciál pro snížení rizika mikrovaskulárních komplikací [4,8]. Zároveň ale klade jak na pacienta, tak i na zdravotnický tým zvýšené nároky [9,10]. Je také nákladnější, než ostatní způsoby terapie, proto je zapotřebí ji indikovat uvážlivě, zcela individuálně.
Zavedení terapie kontinuální subkutánní infuze inzulinu (CSII) je proces, který probíhá za hospitalizace a v průběhu kterého musí pacient zvládnout nejen dovednosti potřebné k obsluze a péči o pumpu, ale především pro prevenci a řešení všech možných problémů a komplikací, které se v souvislosti s touto metodou mohou objevit [10]. Byly přineseny důkazy o efektivitě této léčby na lepší metabolickou kontrolu [9,11,12], k řešení fenoménu úsvitu [13-15]. Účinnost metody CSII ke snížení rizika zejména těžkých hypoglykemií je dnes také akceptována [11,16]. Bazální sekreci u metody CSII nahrazuje předem naprogramované bazální dávkování, které je možné volit s velkou variabilitou podle potřeby u konkrétního nemocného. Prandiální potřebu inzulinu si potom nemocný obstarává pomocí bolusů, kterých může být libovolný počet, což zabezpečuje značnou flexibilitu ve stravovacím režimu nemocného. Bolusů může nemocný rovněž využívat k úpravě kompenzace, podle aktuálních měření glykemií glukometrem.
Předmětem této práce je srovnání kompenzace diabetu léčeného jednak konvenčně více dávkami inzulinu (MDI), jednak inzulinovou pumpou CSII v průběhu 8letého prospektivního sledování. Práce hodnotí glykovaný hemoglobin, průměrné glykemie, výskyt nežádoucích hypoglykemií, komplikace terapie, vývoj hmotnosti a použitých dávek inzulinu.
Soubor nemocných a metodika
Předmětem sledování byly dospělé osoby s DM1T, které byly dosud léčeny intenzifikovaným inzulinovým režimem s využitím humánních inzulinů, ale také krátkodobých inzulinových analog. Z řady důvodů, ale nejčastěji pro neuspokojivou metabolickou kompenzaci, přítomnost počínajících pozdních komplikací diabetu, výskyt hypoglykemií a potřebu flexibility denního režimu byla u nemocných zvažována léčba CSII. Jednalo se jednak o nemocné dispenzarizované dlouhodobě v naší ambulanci, ale také o nemocné, kteří byli k posouzení vhodnosti léčby inzulinovou pumpou odesláni na naše pracoviště. Celkem se jednalo za roky 1998 a 1999 o skupinu 70 nemocných. Z tohoto souboru nemocných jsme 35 pacientů, jako indikovaných a současně vhodných pro léčbu CSII, zavedli na terapii inzulinovou pumpou, ostatní nemocné jsme léčili nadále intenzifikovanou inzulinovou terapií metodou MDI se změnou režimu aplikace inzulinu, úpravami dávek a také s využitím dlouhodobých inzulinových analog. Všechna tato opatření byla vedena snahou o dosažení co nejlepší metabolické kompenzace. Při rozhodování o zavedení nemocných na terapii CSII jsme dodržovali indikační kritéria [17] a současně posuzovali obvyklým způsobem vhodnost, či nevhodnost nemocného pro tento způsob léčby [10]. Dodržovali jsme i další 2 zcela zásadní a nezbytné podmínky bezpečné léčby CSII. Těmi jsou dostupný technický servis a nejlépe 24hodinová možnost kontaktu nemocného s lékařem. Přesto jsme všechny nemocné léčené inzulinovou pumpou, abychom měli 100% jistotu, že je nemocný zabezpečen, vybavili vždy i náhradním inzulinovým programem - tedy konvenční intenzifikovanou inzulinovou terapií.
Celý soubor tvořilo celkem 70 osob - diabetiků 1. typu. Skupinu pacientů léčených CSII tvořilo 35 osob, 16 mužů a 19 žen; jejichž průměrný věk v době zahájení studie byl 34,1 ± 2,2 roku. BMI (body mass index) pacientů v počátku sledování byl 25,8 ± 1,0 kg/m2. Trvání DM u skupiny pacientů léčených CSII bylo 15,4 ± 1,5 roku. Průměrná dávka inzulinu byla na počátku studie 45,3 ± 2,0 IU/24 hodin. Kontrolní skupinu pacientů léčených MDI tvořilo 35 osob, 19 mužů a 16 žen, jejichž průměrný věk v době zahájení studie byl 34,7 ± 2,0 roky. BMI pacientů v počátku sledování byl 25,9 ± 1,0 kg/m2. Trvání DM u kontrolního souboru bylo 13,9 ± 1,3 roku. Průměrná dávka inzulinu byla na počátku studie 42,5 ± 2,0 IU/24 hodin. Při porovnání všech uvedených parametrů, tedy věku, trvání diabetu, BMI a dávky inzulinu jsme nezjistili na počátku sledování mezi oběma skupinami statisticky významné rozdíly, p > 0,05.
Celková denní dávka inzulinu v mezinárodních jednotkách (IU/24 hod) byla podskupině pacientů léčených CSII podávána subkutánně pomocí zavedené teflonové kanylky inzulinové pumpy rozděleně na bazální dávku kontinuálně v průběhu 24 hod a bolusové dávky aplikované preprandiálně. Použity byly pumpy H-tron plus V100, Accu-Check D-tron plus, Accu-Check Spirit, Minimed 507 c, 508, Minimed Paradigm 511 a Animas IR 1000 a IR 1200, ze všech na našem trhu dostupných, jak je uvádí Kožnarová [18]. Podáván byl krátkodobě působící humánní (HM) inzulin nebo analog. Podskupina pacientů léčených MDI si aplikovala inzulin subkutánně pomocí aplikátoru inzulinu (pera Humapen, Novopen, Optipen), a to dlouhodobý HM inzulin nebo dlouhodobý analog v 1-2 dávkách denně a krátkodobý HM inzulin nebo krátkodobý analog ve 3-6 dávkách preprandiálně denně. Obě skupiny byly stejně edukovány a prováděly selfmonitoring glykemií glukometrem s frekvencí 800-1 200 měření/rok.
Změny metabolické kompenzace byly hodnoceny podle glykovaného hemoglobinu (HbA1c) a průměrné glykemie. HbA1c byl stanoven metodou vysokotlaké kapalinové chromatografie (analyzátor TOSOHA1C 2,2, firma Bayer), hodnocení výsledků dle Diabetes Control and Complications Trial (DCCT), v posledních 3 letech byla změna referenční metody dle International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) a byl proveden přepočet výsledků podle matematického vztahu dle doporučení České diabetologické společnosti a České společnosti klinické biochemie(ČSKB) na hodnoty dle IFCC.
Průměrná glykemie byla vypočítána u jednotlivých pacientů z 21 naměřených hodnot glykemie pomocí glukometru, a to jak na počátku, tak na konci sledování. Jednalo se vždy o 3 sedmibodové profily glykemií z posledního týdne před návštěvou; 6 hodnot každého profilu tvořily vždy glykemie před snídaní, před obědem a před večeří a postprandiální měření 90 min po snídani, po obědě a po večeři a 7. hodnotu tvořily glykemie 1. den profilu ve 22 hod, 2. den profilu v 01 hod a 3. den profilu v 04 hodiny. Tím bylo zachyceno jak postprandiální kolísání glykemií, tak i denní a noční průběh glykemie. Pro měření pacienti využili glukometry, kterými jsou dlouhodobě vybaveni, jednalo se o registrované a běžně používané přístroje v ČR (Freestyle, Glucotrend, Accu-Check, One Touch II, One Touch Ultra, Medisense).
Byla hodnocena frekvence hypoglykemií, za těžké (závažné) hypoglykemie byly považovány všechny hypoglykemie vyžadující pomoc druhé osoby, od asistence při perorálním řešení hypoglykemie, přes aplikaci glukagonu subkutánně až po aplikaci glukózy intravenózně. Jinak do celkového počtu hypoglykemií byly započítávány jak symptomatické, tak asymptomatické glukometrem naměřené hodnoty kapilární glykemie < 3,3 mmol/l.
V obou skupinách jsme také hodnotili změny hmotnosti a změny dávky inzulinu. Pro zjištění statistické hladiny významnosti u jednotlivých parametrů jsme vycházeli z těchto hledisek:
- porovnávali jsme výchozí počáteční stav se stavem na konci sledování, případně v průběhu sledování
- analyzovali jsme meziroční změny u glykovaného hemoglobinu
- srovnali jsme pacienty léčené inzulinovou pumpou s kontrolní skupinou
Graf 1. Vývoj HbA<sub>1c</sub> u pacientů léčených inzulinovou pumpou. 
Pro hodnocení byl použit statistický test respektující charakter dat a jejich rozložení - neparametrický párový Wilcoxnův test. Při porovnání pacientů léčených inzulinovou pumpou a kontrolního souboru jsme použili neparametrický nepárový Mannův-Whitneyův U-test. Pro porovnání četností pacientů mezi oběma sledovanými skupinami byl použit χ2-test. Data byla hodnocena na hladině významnosti α = 5 %. Pro hodnocení výsledků byl použit software Statistica for Windows (StatSoft,ČR).
Výsledky
Kompenzace diabetu
V průběhu sledování docházelo ke změnám glykovaného hemoglobinu v obou skupinách nemocných. Výsledky jsme hodnotili v ročních intervalech. Zatímco ve skupině nemocných léčených inzulinovou pumpou byl od počátku pozorován statisticky významný pokles HbA1c, p < 0,001 a tento se udržel po celou dobu sledování až do konce, tak v kontrolní skupině pacientů léčených metodou MDI došlo k statisticky signifikantnímu poklesu HbA1c, p < 0,05 jen v prvních 2 letech a výsledky glykovaného hemoglobinu v dalších letech byly již v porovnání s počátečním stavem statisticky nesignifikantní. Při porovnání meziročních změn ve skupině CSII jsme zjistili rozdíl pouze mezi počátečním stavem a 1. rokem sledování (p < 0,001), ostatní meziroční změny byly statisticky nevýznamné, p > 0,05. Vývoj glykovaného hemoglobinu ve skupině pacientů léčených inzulinovou pumpou ukazuje graf 1. Na počátku sledování a v dalších 7 letech byl hodnocen celý soubor 35 nemocných, v 8. roce bylo hodnoceno 22 nemocných. Při porovnání meziročních změn v kontrolní skupině jsme zjistili statisticky signifikantní rozdíl pouze mezi počátečním stavem a prvním rokem sledování (p = 0,001), ostatní meziroční změny byly statisticky nevýznamné, p > 0,05. Pokud jsme porovnávali glykovaný hemoglobin u nemocných léčených inzulinovou pumpou oproti kontrolní skupině, nalezli jsme signifikantní rozdíly mezi oběma skupinami jen na počátku sledování a v 5. roce sledování, v ostatních letech byly rozdíly nevýznamné. Zatímco na počátku sledování byl HbA1c statisticky významně lepší ve skupině kontrolní (p < 0,001), v 5. roce sledování byl signifikantně lepší ve skupině pacientů léčených inzulinovou pumpou (p = 0,047).
Při analýze průměrných glykemií jsme nejprve testovali normalitu dat (Kolmogorovův-Smirnovův test, p > 0,05) a dále jsme analyzovali homogenitu rozptylu obou dvou skupin pomocí Levene’s testu; p < 0,05. Pro nedodržení homogenity rozptylu u obou sledovaných skupin byly aplikovány neparametrické testy pro porovnání průměrných glykemií u jednotlivých pacientů. Výsledky jsou uvedeny v tab. 1 a 2. Při porovnání průměrných hodnot glykemie u jednotlivých pacientů na počátku a na konci studie u skupiny pacientů léčených inzulinovou pumpou jsme zjistili statisticky významný rozdíl, p < 0,001, který dokumentuje pokles průměrné glykemie na konci sledování, což je dobře patrno v tab. 1. Při porovnání průměrných hodnot glykemie u jednotlivých pacientů na počátku a konci studie u kontrolní skupiny jsme nezjistili statisticky významný rozdíl, p = 0,507, tedy průměrná glykemie se na konci sledování signifikantně nezměnila, což je dobře vidět v tab. 2. Při porovnání průměrných hodnot glykemie mezi oběma sledovanými skupinami jsme zjistili statisticky významný rozdíl jak na počátku, tak na konci studie, p < 0,001. Zatímco na počátku byla průměrná glykemie signifikantně lepší v kontrolním souboru, což dobře dokumentuje graf 2, tak na konci sledování byla signifikantně lepší ve skupině pacientů léčených inzulinovou pumpou, což je patrno na grafu 3.
Tab. 1. Průměrné glykemie (mmol/l) na počátku a na konci sledování ve skupině pacientů léčených inzulinovou pumpou. 
Tab. 2. Průměrné glykemie (mmol/l) na počátku a na konci sledování v kontrolním souboru pacientů. 
Graf 2. Porovnání průměrné glykemie na začátku sledování mezi souborem pacientů léčených inzulinovou pumpou a kontrolním souborem. 
Graf 3. Porovnání průměrné glykemie na konci sledování mezi souborem pacientů léčených inzulinovou pumpou a kontrolním souborem. 
Hypoglykemie
Porovnání výskytu hypoglykemií jsme nejprve provedli pro všechny hypoglykemické epizody zaznamenané pacienty, v této kategorii jsme nenalezli v žádném roce od počátku až do konce sledování mezi oběma skupinami nemocných statisticky významný rozdíl, p > 0,05. Proto jsme se zvlášť zaměřili na vyhodnocení těžké (závažné) hypoglykemie. Při porovnání závažných hypoglykemií mezi oběma skupinami jsme nenalezli statisticky významný rozdíl na počátku a v 1. a 2. roce sledování, p > 0,05, ale od 3. roku sledování až do konce sledování již statisticky signifikantní rozdíl byl (χ2 = 6,63; df = 1; p = 0,010) ve prospěch nižšího výskytu závažných hypoglykemií ve skupině nemocných léčených inzulinovou pumpou. Na grafu 4 je dokumentováno porovnání všech hypoglykemických příhod mezi oběma skupinami pacientů ve 3. roce a tab. 3 dokumentuje porovnání závažných hypoglykemií mezi oběma skupinami pacientů rovněž ve 3. roce.
Graf 4. Porovnání všech hypoglykemických příhod mezi pacienty léčenými inzulinovou pumpou a kontrolní skupinou ve 3. roce sledování. 
Tab. 3. Porovnání výskytu závažných hypoglykemií mezi oběma skupinami ve 3. roce sledování. 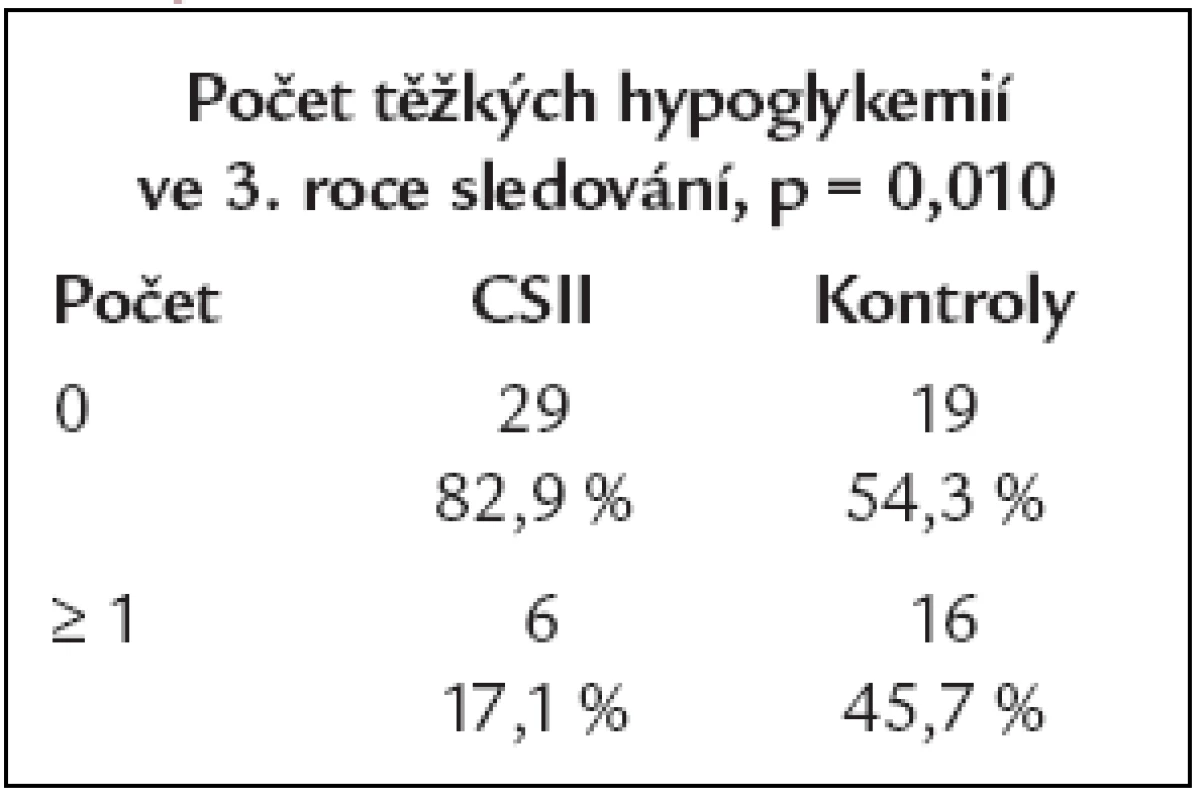
Komplikace terapie
V našem souboru nemocných se diabetická ketoacidóza (DKA) objevila celkem ve 4 případech. Ve skupině pacientů léčených inzulinovou pumpou jen ve 2 případech, po 1 příhodě u 2 nemocných, a to vždy v 1. roce sledování. V kontrolní skupině se DKA objevila za celou dobu sledování také ve 2 případech u dvou odlišných subjektů ve 3. a 5. roce sledování. Obturaci katétru jsme u souboru 35 nemocných léčených CSII za celou dobu sledování, tedy 267 pacient/roků, zaznamenali ve 131 případech s frekvencí v rozmezí 0-16 příhod u 1 pacienta za celou dobu sledování. Poslední komplikací, se kterou jsme se v našem souboru nemocných léčených inzulinovou pumpou setkali, byla lokální infekce v místě inzerce kanyly. Uvážíme-li, že u našeho souboru 35 nemocných léčených CSII se jednalo o 267 pacient/roků a přitom 84 případů této komplikace, připadá 1 případ lokální infekce v místě inzerce kanyly přibližně na 3 pacient/roky.
Změny hmotnosti
Hmotnost pacientů léčených CSII v počátku sledování byla 70,5 ± 1,9 kg. Hmotnost na konci studie byla 71,7 ± 1,9 kg. Při porovnání hmotnosti pacientů mezi počátkem a koncem studie jsme zjistili statisticky významný rozdíl, p = 0,047. Na této skutečnosti se podílelo jen 12 pacientů, protože u ostatních se hmotnost nezměnila, nebo dokonce mírně poklesla. Hmotnost pacientů v kontrolní skupině v počátku sledování byla 70,1 ± 2,3 kg. Hmotnost na konci studie byla 73,5 ± 2,4 kg. Při porovnání hmotnosti pacientů mezi počátkem a koncem studie jsme zjistili statisticky významný rozdíl, p < 0,001. Při porovnání hmotnosti mezi oběma skupinami na počátku i na konci sledování jsme nezjistili statisticky významné rozdíly, p > 0,05.
Změny denní dávky inzulinu
Průměrná dávka inzulinu ve skupině léčené CSII byla na počátku sledování 45,3 ± 2,0 IU/24 hod, na konci sledování 39,1 ± 1,8 IU/24 hod. Při porovnání počátečního a konečného stavu jsme zjistili statisticky významný pokles v dávce inzulinu na konci studie, p < 0,001, jak ukazuje graf 5. Průměrná dávka inzulinu v kontrolní skupině byla na počátku sledování 42,5 ± 2,0 IU/24 hod, na konci sledování 45,2 ± 2,3 IU/24 hod. Při porovnání počátečního a konečného stavu jsme neprokázali statisticky signifikantní rozdíl, p = 0,272. Při porovnání dávky inzulinu mezi oběma skupinami jak na počátku, tak na konci sledování jsme neprokázali statisticky signifikantní rozdíl, p = 0,272.
Graf 5. Vývoj dávky inzulinu u pacientů léčených inzulinovou pumpou. 
Diskuse
V literatuře existuje velké množství studií, porovnávající výsledky metabolické kontroly mezi léčbou pomocí inzulinové pumpy a intenzifikovanou inzulinovou léčbou metodou MDI [19-21], což není při téměř třicetileté historii terapie inzulinovou pumpou nikterak neobvyklé. Jedná se ovšem s ohledem na skutečnost, že tato léčba je špičkovou metodou aplikace inzulinu, využívanou obvykle až po selhání všech ostatních prostředků a léčebných možností k dosažení cílových hodnot kompenzace diabetu, většinou o relativně malé soubory s různou dobou sledování, případně metaanalýzy.
Situaci CSII v České republice dnes dokumentuje registr pacientů léčených pomocí inzulinové pumpy, který vedou plzeňští kolegové. Tento v roce 2006 registruje 2 060 pacientů, v roce 2004 to bylo 1 500 nemocných [22]. Naše výsledky korespondují s výsledky českého registru, prokázali jsme udržení zlepšené metabolické kontroly podle glykovaného hemoglobinu po celé období celkem 8letého sledování. Pacienti zařazení na terapii inzulinovou pumpou měli ve srovnání s kontrolní skupinou úvodně horší metabolickou kompenzaci podle HbA1c, a to v průměru o 1,2 %, což bylo statisticky významné, p < 0,001. Kompenzace se ve skupině pacientů léčených inzulinovou pumpou zlepšila v každém roce sledování oproti původní hodnotě před zahájením této léčby v průměru o 1,3-1,6 % se statistickou významností p < 0,001, zatímco u kontrolní skupiny pacientů léčených metodou MDI se kompenzace zlepšila jen v 1. a 2. roce sledování (p < 0,01), ale v dalším průběhu se opět mírně zhoršila, takže se již statisticky významný rozdíl oproti původní hodnotě neprokázal. Na konci sledování už nebyl mezi oběma skupinami statisticky významný rozdíl. Uvedené zlepšení lze považovat pro nemocné za přínosné, přestože ani po zlepšení kompenzace diabetu nejsou dosahovány cílové hodnoty kompenzace tak, jak byly například podle doporučení ČDS v úvodu uvedeny.
Kompenzaci diabetu významně ovlivňuje selfmonitoring glykemií. Diskutuje se, jak často by měly probíhat kontroly glykemií minimálně. Uvádí se, že minimálně by se měl pacient měřit 1-2krát denně, v době kdy je metabolicky stabilizován a výrazněji nezasahuje do svého běžného stravovacího a pohybového režimu. Většinou se doporučují kontroly glykemií častěji (4-6krát denně) a logická je přímá úměra mezi počtem měření a dosaženou kompenzací diabetu. Pochopitelně za podmínek, že změření glykemie je následováno adekvátní reakcí, tedy úpravou terapie. Potom platí, že čím častěji se dobře edukovaný nemocný kontroluje a aktuálně stav kompenzace upravuje, tím je samozřejmě schopen lépe využít možností, které mu tato terapie poskytuje, a dosáhnout tak lepší metabolické kompenzace. Edukace a motivace jsou nutné k dosažení lepší kompenzace za pomocí metody CSII.
V literatuře se hodně píše o tom, že je prospěšnější užití krátkodobých analog inzulinu oproti krátkodobému HM inzulinu v inzulinové pumpě. K dispozici je řada prací jak s inzulinem lispro, tak inzulinem aspart [23,25-29], a v poslední době je hodnocena i rovnocennost použití dalšího krátkodobého analoga inzulinu glulisin s výše uvedeným analogem aspart [30]. V našem souboru převažovali až do roku 2002 pacienti s HM inzuliny v inzulinové pumpě, poté má většina našich nemocných krátkodobý analog. Ze sledovaného souboru to bylo 34 nemocných. V kontrolní skupině léčené metodou MDI, protože do této doby již spadá možnost využití dlouhodobých analog inzulinu, která jsme našim pacientům, kteří nedosahovali uspokojivé kompenzace, poskytli. Na konci sledování je ze skupiny nemocných léčených MDI již dlouhodobým analogem léčeno 29 pacientů.
Podle MacCartera z roku 2006 [31] jsme vybrali jako další ukazatel kompenzace diabetu průměrnou glykemii (mean blood glucose - MBG). Ve skupině nemocných léčených inzulinovou pumpou se průměrná glykemie od počátku sledování do jeho konce statisticky významně zlepšila, zatímco ve skupině kontrolní léčené metodou MDI se při stejném porovnání statisticky signifikantně nezměnila. Při srovnání obou skupin byla průměrná glykemie v našem sledování na počátku statisticky významně horší ve skupině nemocných léčených inzulinovou pumpou oproti skupině kontrolní léčené metodou MDI. Na konci sledování byl mezi oběma skupinami opět statisticky signifikantní rozdíl, ale tentokrát ve prospěch pacientů léčených inzulinovou pumpou. Při hodnocení výskytu hypoglykemií jsou naše výsledky v souladu s řadou dalších klinických sledování [32-35].
Největší předností uvedené metody je schopnost zabránit velkým výkyvům glykemií, kdy i po lehké, a klinicky často nepoznané hypoglykemii dochází k reaktivní hyperglykemii. Zdá se, že právě enormní kolísání glykemií má nejzhoubnější vliv na rozvoj cévních komplikací. Diabetes Control and Complications Trial (DCCT) zavedla jako zlatý standard regulace glykemie glykovaný hemoglobin. I když byly hodnoty HbA1c u intenzivně léčených jedinců a jejich klasicky léčených protějšků srovnatelné, tak jak to ukazuje pokračující studie DCCT podle výsledků uveřejněných v roce 2004 - Epidemiology of Diabetes InComplications (EDIC), které vykázaly po 10 letech sledování 90 % pacientů z původní studie DCCT menší riziko závažných komplikací u intenzifikovaně léčených pacientů. Větší výskyt komplikací někteří autoři [36] vysvětlují právě jako důsledek většího kolísání glykemií s tvorbou většího množství volných kyslíkových radikálů (ROS) a tedy většího cévního poškození vlivem oxidačního stresu. Proto se v současnosti řeší otázka, zdali by se minimální variabilita glykemie neměla stát zlatým standardem regulace glykemie.
Mnoho si slibujeme od možnosti využít inzulinovou pumpu ve spojení s kontinuálním subkutánním monitorem glykemie, který je zdrojem nesrovnatelně většího množství dat než běžný selfmonitoring glukometrem, a může tedy být dobrým základem jak pro přesnější nastavení inzulinových dávek, tak i potřebné úpravy. Zmíněna byla bezprostředně vyšší nákladnost léčby inzulinovou pumpou, ale na druhé straně nesmí být opomenut širší pohled na farmakoekonomiku léčby diabetu, ta jednoznačně ukazuje, že léčebné strategie snižující výskyt komplikací jsou nákladově efektivní [37].
Závěr
V klinické praxi jsme ověřili metodu léčby inzulinovou pumpou jako účinnou k dosažení lepší metabolické kontroly s dalšími uvedenými pozitivy, ale současně také jako bezpečnou, jak ukazuje nejen uvedený nižší výskyt závažných hypoglykemií, ale i nižší výskyt obávané komplikace, totiž diabetické ketoacidózy, který se ukázal jako srovnatelný se skupinou kontrolní. Ostatní komplikace spojené s léčbou inzulinovou pumpou byly při současné kvalitě spotřebního materiálu málo frekventní a nezávažné a nemohly zdaleka převážit evidentní benefit, který představuje lepší kompenzace diabetu.
MUDr. Jindřich Olšovský
www.fnusa.cz
e-mail: jindrich.olsovsky@fnusa.cz
Doručeno do redakce: 3. 1. 2007
Přijato po recenzi: 19. 1. 2007
Zdroje
1. Brinchmann-Hansen O, Dahl-Jorgensen K, Sandvik L et al. Blood glucose concentrations and progression of diabetic retinopathy: the seven year results of the Oslo study. BMJ 1992; 304 : 19-22.
2. Mogensen CE. Management of diabetic renal involvement and disease. Lancet 1988; 1 : 867-870.
3 Tattersalll RB The quest for normoglycemia: a historical perspective. Diabetologia 1994; 11 : 618-635.
4. The Diabetes Control and Complications Trial research group: The effect of intensive treatment of diabetes on the development and progression of longterm complications in insulin-dependent diabetes mellitus. N Engl J Med 1993; 329 : 977-986.
5. Kohner EM. The effect of diabetic control on diabetic retinopathy. Eye 1993; 7 : 309-311.
6. Reichard P. Are there any glycemic thresholds for the serious microvascular diabetic complications? J Diab Compl 1995; 9 : 25-30.
7 Pickup JC, Keen H, Parsons JA et al. Continuous subcutaneous insulin infusion: an aproach to achieving normoglycemia. Br Med J 1978; 1 : 204-207.
8. Diabetes control and Complications Trial Research Group: Implementation of treatment protocols in the Diabetes Control and Complications Trial. Diabetes Care 1995; 18 : 361-376.
9. Strowig SM. Initiation and management of insulin pump therapy. Diabetes Educ 1993; 19 : 50-58.
10. Olšovský J. Inzulínová pumpa. In: Perušičová J. Trendy soudobé diabetologie. Praha: Galén 2004: Vol 9, 49-71.
11 Pickup J, Keen H. Continuous subcutaneous insulin infusion et 25 years. Diabetes Care 2002; 25 : 593-598.
12. Jankovec Z, Čechurová D, Krčma M et al. Dlouhodobý efekt léčby inzulínovou pumpou (CSII) - výsledky registru pacientů léčených CSII v České republice DMEV 2006; Suppl 2 : 26.
13. Koivisto VA, Yki-Yarvinen H, Helve E et al. Pathogenesis and prevention of the dawn phenomenon in diabetic patients treated with CSII. Diabetes 1986; 35 : 78-82.
14. Kane K, Jansenn MMU, Keulen ETP et al. Substitution of nighttime CSII therapy for bedtime NPH insulin in a multiple injection regimen improves contraregulatory hormonal response and warning symptoms of hypoglycemia in IDDM. Diabetologia 1998; 41 : 322-329.
15. Carrol MF, Schade DS. The dawn fenomenon revisited: implications for diabetes therapy. Endocr Pract 2005; 11 : 55-64.
16. Eichner HL, Selan JL, Hollemann CB et al. Reduction of severe hypoglycemic events in type 1 diabetic patients using continuous subcutaneous insulin infusion. Diabetes Res 1988; 8 : 189-193.
17. Brož J, Kožnarová R, Bartášková D et al. Současné možnosti léčby diabetes mellitus pomocí inzulínových pump. DMEV 2006; 4: 179-186.
18. Kožnarová R. Přehled pump dostupných v ČR. Remedia 2006; 2 : 188.
19 Retnakaran R, Zinman B. CSII vs. MDI: insights from a Health Technology Assessment review. International Diabetes Monitor 2006; 18 : 20-22.
20. Retnakaran R, DeVries JH, Hanaire-Broutin H et al. Continuous subcutaneous insulin infusion versus multiple daily injections: modeling predicted benefits in relationship to baseline A1c. Diabetes Care 2005; 28 : 1835-1836.
21. Hirsch IB, Bode BW, Garg S et al. for the Insulin Aspart CSII/MDI Comparison Study Group. Continuous subcutaneous insulin infusion of insulin aspart versus multiple daily injection of insulin aspart/insulin glargine in type 1 diabetic patients previously treated with CSII. Diabetes Care 2005; 28 : 533-538.
22. Jankovec Z, Krčma M, Lacigová S et al. Registr pacientů léčených inzulínovou pumpou v České republice. DMEV 2004; Suppl 1 : 22,
23. Melki V, Renard E, Lassmann-Vague V et al. Improvement of HBA1c and blood glucose stability in IDDM patients with lispro insulin analogue in external pump. Diabetes Care 2001; 24 : 69-72.
24. Renner R, Pfurzner A, Traurman M et al. Use of insulin lispro in CSII treatment. Diabetes Care 1999; 22 : 784-788.
25. Schmaus S, Konig A, Landgraf R. Human insulin analogue (lispro) the ideal pump insulin? Diabet Med 1998; 15 : 247-249.
26. Zinman B, Tildesley H, Chiasson J-L et al. Insulin lispro in CSII: results of a double-blind crossover study. Diabetes 1997; 46 : 440-443.
27 Bode B, Weinstein R, Bell D et al. Comparison of insulin aspart with buffered regular insulin and insulin lispro in CSII. Diabetes Care 2002; 25 : 439-444.
28. Bode B, Steed D, Davidson P. Long-term pump use and SMBG in 205 patients. Diabetes 1994; 43 (Suppl 1): 220A.
29. Bode B, Strange P. Efficacy, safety and pump compatibility of insulin aspart used in CSII therapy with Type 1 diabetes mellitus. Diabetes Care 2001; 24 : 69-72.
30. Hoogma RPLM, Schumicki D. Safety of Insulin Glulisine when Given by Continuous Subcutaneous Infusion Using an External Pump in Patients with Type 1 Diabetes. Horm Metab Res 2006; 38: 429-433.
31. McCarter RJ, Hempe JM, Chalew SA. Mean blood glucose and biological variation have greater influence on HbA1c levels then glucose instability: an analysis of data from the Diabetes Control and Complications Trial. Diabetes Care 2006; 29 : 352-355.
32. Ng Tang Pui S, Pickup J, Bending JJ. Hypoglycemia and counterregulation in insulin-dependent patients: a comparison of CSII and conventional insulin therapy. Diabetes Care 1986; 15 : 221-227.
33. Ronn B, Mathiesen ER, Vang L et al. Evaluation of insulin pump treatment under routine conditions. Diabetes Res Clin Pract 1989; 3 : 191-196.
34. Chantelau E, Spraul M, Muhlhauser I et al. Long term safety, efficacy and side-effects of continuous subcutaneous insulin infusion treatment for type 1 diabetes mellitus: a one centre experience. Diabetologia 1989; 32 : 421-426.
35. Bell DSH, Cutter G, Clements RS. The feasibility of long-term treatment of diabetes with continuous subcutaneous insulin infusion. Diab Nutr Metab 1993; 6 : 57-60.
36. Hirsch IB, Brownlee M. Should minimal blood glucose variability become the gold standard of glycemic control. J Diabetes Complications 2005; 19 : 178-181.
37. Doležal T. Farmakoekonomické aspekty léčby diabetu. Farmakoekonomika 2006; 1 : 8-12.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2007 Číslo 6- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
-
Všechny články tohoto čísla
- Délka antikoagulační léčby a riziko recidiv u TEN - editorial
- Klinické zkušenosti s léčbou dlouhodobým inzulinovým analogem glargin v diabetologickém centru
- Vliv dlouhodobé terapie inzulinovou pumpou (CSII) u pacientů s diabetes mellitus 1. typu na metabolickou kompenzaci a výskyt hypoglykemií. Porovnání s intenzifikovanou konvenční inzulinovou terapií (MDI)
- Subpopulace CD34+buněk a jejich význam pro přihojení štěpu u příbuzenských alogenních transplantací periferních kmenových buněk
- Esenciální trombocytemie a další myeloproliferace s trombocytemií v údajích registru pacientů léčených Thromboreductinem® do konce roku 2006
- Optimální délka antikoagulační léčby po žilní tromboembolické příhodě: obecný či individualizovaný přístup?
- Kardiotoxicita antracyklínovej liečby vo svetle nových biochemických diagnostických možností
- Genetické faktory a riziko kardiovaskulárnych ochorení
-
Nové poznatky v genetice autoimunitního diabetu
(1): Monogenně podmíněné typy autoimunitního diabetu - Je familiární hypercholesterolemie v České republice pod kontrolou?
- Hypogonadizmus - závažná komplikace chronické nedostatečnosti ledvin
- Postavení neoadjuvantní chemoterapie v léčbě nemalobuněčného plicního karcinomu
- Maligní arytmie u pacienta s variantní (Prinzmetalovou) anginou pectoris
- Ojedinělá komplikace při pokusu o zavedení dočasné kardiostimulace
- Zlepšování výsledků léčby vybraných krevních chorob a změny nákladů na tuto léčbu. Otázky pro ekonomy a další odborníky
- Jsou nezbytná kvalifikovaná rozhodnutí vycházející z věrohodných dat
- Náklady na léky v České republice - příčiny růstu a návrhy řešení
- Príspevok nefrológie vo Fakultnej nemocnici L. Pasteura a Lekárskej fakulty Univerzity P. J. Šafárika v Košiciach ku histórii českej nefrológie
- Zamrazil V. Hypotyreóza. Průvodce ošetřujícího lékaře.
- Vondráček L, Dvořáková V. Pochybení a sankce při poskytování lékařské péče.
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Náklady na léky v České republice - příčiny růstu a návrhy řešení
- Hypogonadizmus - závažná komplikace chronické nedostatečnosti ledvin
- Maligní arytmie u pacienta s variantní (Prinzmetalovou) anginou pectoris
- Genetické faktory a riziko kardiovaskulárnych ochorení
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



