-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Intersfinkterické resekce rekta
Autoři: J. Örhalmi 1; K. Klos 2; S. Jackanin 2; P. Holéczy 2
Působiště autorů: Chirurgická klinika Lékařské fakulty UK v Hradci Králové a Fakultní nemocnice Hradec Králové 1; Vítkovická Nemocnice, a. s., Centrum péče o zažívací trakt, Chirurgické oddělení 2
Vyšlo v časopise: Rozhl. Chir., 2012, roč. 91, č. 2, s. 101-104.
Kategorie: Postgraduální vzdělávání
Úvod
Léčba karcinomu rekta doznala za posledních 30 let značných změn. Zavedením a rychlým rozvojem staplerových technik významně poklesl podíl amputačních výkonů v oblasti rekta. Přehodnocení distální resekční linie z 5 cm na 2 cm a posléze na 1 cm [1, 2, 3] vedlo k rozšíření sfinkter zachovávajících výkonů, jako jsou ultra nízká resekce rekta s koloanální anastomózou (KAR) a intersfinkterické resekce rekta (ISR) bez ohrožení onkologických výsledků.
Předpokladem správné léčby, zejména v aborální třetině rekta, je důležité co nejpřesnější určení stadia, druhu a typu nádoru. To vedlo k rozvoji a zpřesnění předoperačních vyšetření – CT vyšetření, NMR pánve, endosonografie rekta a k rozvoji endoskopických metod.
Koloanální anastomóza pro benigní diagnózu byla poprvé popsána Parksem v roce 1972 [4], který provedl v roce 1982 i první intersfinkterickou resekci pro karcinom rekta [5]. Operaci zpopularizoval a představil i první větší soubor pacientů Schiessel v roce 1994 [6]. Intersfinkterická resekce je indikovaná pro selektivní skupinu pacientů, kteří se tímto výkonem mohou vyhnout trvalé kolostomii. Bezpečnost a účinnost metody byla potvrzena metaanalýzou [7], která prokázala nízkou pooperační letalitu – 1,6 %, morbiditu, obvyklé procento dehiscencí anastomóz 10 %, lokální recidivu v 9 % a pětileté přežívání v 81 %.
Dalším pokrokem bylo zavedení laparoskopických operací i pro kolorektální karcinom v aborální třetině rekta. Jsou známy krátkodobé výsledky po laparoskopické intersfinkterické resekci rekta, ale dlouhodobé výsledky zatím chybějí [8, 9].
Materiál a metoda
Jednalo se o retrospektivní analýzu prospektivně sbíraných dat podle protokolu. Všichni pacienti indikovaní k intersfinkterické resekci podstoupili koloskopii s biopsií, CT vyšetření břicha a malé pánve, NMR pánve, endorektální sonografii, digitální vyšetření per rectum, RTG vyšetření plic. Pacienti s T3 a/nebo N1 tumorem podstoupili dlouhodobou neoadjuvantní konkomitantní chemoradioterapii. Po ukončené neoadjuvantní terapii byl opět proveden restaging tumoru.
Indikační kritéria k intersfinkterické resekci:
- a) Tumor lokalizovaný v aborální třetině rekta do 4 cm od anu
- b) T1–T3 tumor, ověřený endorektální sonografií a NMR pánve
- c) G1 nebo G2 adenokarcinom
- d) Absence vzdálených metastáz
- e) Kontinence pro stolici, dobrá funkce análních svěračů
Kontraindikace pro intersfinkterickou resekci:
- a) Invaze tumoru do okolních orgánů
- b) Invaze tumoru do m. sphincter ani externus
- c) Invaze tumoru do mm. levatores ani
- d) Inkontinence před operací
- e) G3 tumor nebo hlenotvorný adenokarcinom
Případné N+ po restagingu není kontraindikací pro provedení intersfinkterické resekce.
Postup operace
Všichni pacienti ze souboru byli operováni na jednom pracovišti (Vítkovická Nemocnice, a. s., Ostrava-Vítkovice). Pacienti po neoadjuvantní onkologické terapii podstoupili po restagingu operaci s 6týdenním odstupem. V intervalu před operací byli v péči nutriční ambulance. Před operací byla u všech pacientů provedena mechanická příprava tlustého střeva 4 litry makrogolového roztoku (Fortrans, Beaufour Ipsen Pharma, Paříž, Francie). Pacienti měli zaveden epidurální katetr, selektivně centrální venózní katetr, standardně permanentní močový katetr. Antibiotická profylaxe byla podána na operačním sále Unasyn (Pfizer, s. r. o., Praha, Česká republika) a Metronidazole (Polpharma, Varšava, Polsko), po úvodu do kombinované celkové anestezie. Poté byl pacient polohován do Lloyd-Davisovy polohy. V případě konvenčního přístupu byla provedena dolní střední laparotomie rozšířena asi 5 cm nad pupek, v případě laparoskopického přístupu byl zaveden supraumbilikálně port pro optiku po předešlé insuflaci peritoneální dutiny CO2 Veresovou jehlou. Další 3 pracovní porty byly zavedeny v pravém hypogastriu a v levém hypogastriu. Po preparaci byla klipována a přerušena a. mesenterica inferior. Disekce byla prováděna harmonickým skalpelem (UltracisionTM, Ethicon Endosurgery, Cincinnati, Ohio, USA). Preparace mezokola byla vedena mediolaterálně a proximálně. Standardně bylo provedeno kompletní uvolnění lienální flexury. Po uvolnění kolon se přistoupilo k pánevní preparaci. Nejdříve se provedlo uvolnění mezorekta s protekcí nn. hypogastrici dorzálně a plexus hypogastricus inferior laterálně. Po uvolnění mezorekta dorzálně bylo provedeno uvolnění rekta ventrálně od prostaty a semenných váčků u mužů a od vaginy u žen. Pánevní část byla ukončena po dosažení dna pánevního. Dál pokračovala preparace až do úrovně m. sphincter ani internus, přerušením lig. anococcygeale. Po ukončení pánevní fáze byla provedena standardně u všech pacientů protektivní ileostomie dle Brookse v pravém hypogastriu. Poté bylo přistoupeno k perineální fázi. Byl použit Lone Star retraktor (Lone Star Medical Products Inc., Houston, Texas, USA). Měřidlem byla změřena vzdálenost tumoru od anu a od dentální linie. Vzdálenost tumoru od resekční linie nebyla nikdy menší než 1 cm. Poté byla provedena incize v místě dentální linie. Selektivně byla sliznice infiltrována roztokem adrenalinu v ředění 1 : 100 000. Rektum bylo po obvodu uvolněno. V místě tumoru byla provedena excize m. sfincter ani internus. Vždy byla provedena jen parciální excize sfinkteru – třetina až polovina výšky sfinkteru, v rozsahu odpovídajícím tumoru. Po dosažení prostoru, který byl ciselovaný v abdominální fázi, bylo dokončeno kompletní uvolnění rekta. Resekát rekta a sigmoidea byl extrahován přes konečník. Při perineální fázi byla dokončena skeletizace mezokola a sigmoideum bylo přerušeno staplerem NTLC 100 mm (Ethicon Endosurgery, Johnson & Johnson comp. Cincinnati, Ohio, USA). Následně byl v případě vhodných anatomických poměrů proveden kolický J pouch dalším nábojem NTLC 100 mm. V případě úzké pánve byla provedena anastomóza konec ke straně. Orálně nad anastomózou bylo sigmoideum před provedením anastomózy fixováno dvěma stehy k mm. levator ani. Následně byla provedena anastomóza ve dvou vrstvách pokračujícím stehem. Do oblasti pánve byl dle potřeby vložen easy flow drén (Dahlhausen, s. r. o., Kuřim, Česká republika). Laparotomie v případě konvenčního přístupu byla uzavřena PDS II stehem (Ethicon, Johnson & Johnson comp., Cincinnati, Ohio, USA)
Výsledky
Charakteristika souboru pacientů
V intervalu od 1. 1. 2007 do 1. 12. 2011 bylo provedeno ve Vítkovické Nemocnici, a. s., celkem 172 resekčních výkonů pro karcinom rekta (Tab. 1). Jednalo se o 105 mužů a 67 žen. Průměrný věk všech operovaných byl 66 let (40–90). Z celkového počtu resekčních výkonů bylo 106 nízkých resekcí rekta, z toho 58 % laparoskopickým přístupem, 26 abdomino-perineálních resekcí rekta (APR), 62 % laparoskopicky. Dále bylo provedeno i 19 Hartmanových operací. Vesměs se jednalo o paliativní resekce u polymorbidních pacientů nebo u pacientů v pokročilém věku. Z celého souboru bylo provedeno 24 paliativních resekčních výkonů při generalizovaném onemocnění.
Tab. 1. Spektrum resekčních výkonů pro karcinom rekta 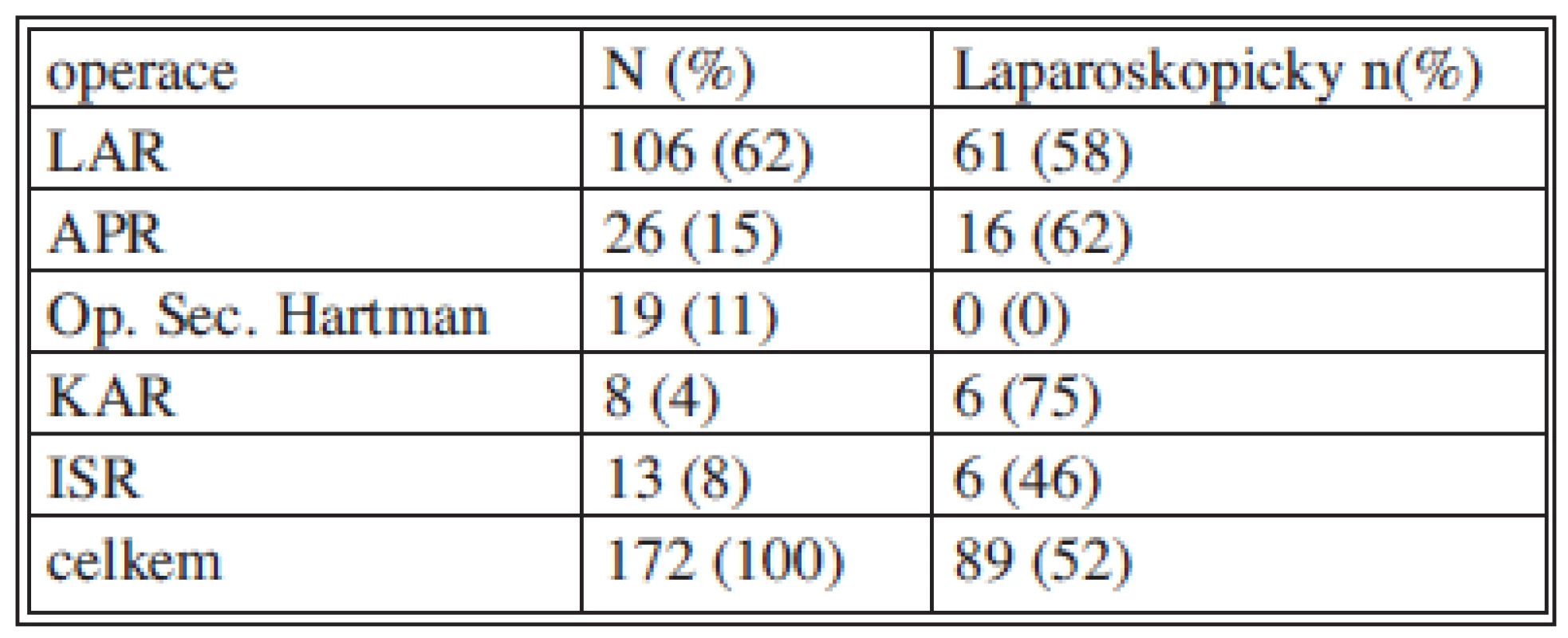
Zkratky LAR – nízká přední resekce APR – abdominoperineální resekce KAR – koloanální anastomosa ISR – intersfinkterická resekce Resekčních výkonů s anastomózou pro karcinom v aborální třetině rekta bylo provedeno celkem 21, z toho 8 resekcí rekta s koloanální anastomózou a 13 intersfinkterických resekcí. Laparoskopicky bylo provedeno 6 resekcí rekta s koloanální anastomózou a 6 intersfinkterických resekcí, 75 % a 46 %.
Pacientů s tumorem ve střední a aborální třetině rekta bylo celkem 122. Z tohoto počtu bylo provedeno 9 Hartmanových operací – 7 %, výše uvedených 26 abdominoperineálních amputací a 21 koloanálních a intersfinkterických resekcí a 66 nízkých resekcí rekta.
U pacientů před plánovou sfinkter zachovávající operací pro karcinom v aborální třetině rekta byla neoadjuvantní radioterapie provedena u 4 pacientů před ISR – 67 %. Před KAR nebyl k neoadjuvantní radioterapii s ohledem na předoperační staging indikován žádný pacient.
Ani u jednoho pacienta nedošlo ke kompletní patologické odezvě. Průměrná doba pooperační hospitalizace činila u celého souboru 11,8 dne (5–44), proti 8,3 dne (6–14) u pacientů s KAR a ISR.
Komplikace
V souboru pacientů s ISR a KAR se nevyskytla žádná peroperační komplikace. Morbidita pacientů s KAR a ISR byla 14,2 %, pooperační letalita byla 0. Komplikace hojení ran u pacientů s ISR a KAR nebyly žádné. Dehiscence anastomózy se vyskytla u dvou pacientů s KAR a ISR – 9,5 %. Nebyla nutná žádná konverze u pacientů s KAR a ISR. Operační časy u laparoskopické ISR a KAR a resekcí prováděných konvenčním přístupem se významně nelišily.
Onkologické výsledky
Všichni pacienti byli dispenzarizováni na onkologické ambulanci i na koloproktologické ambulanci dle doporučeného schématu. Průměrná doba sledování pacientů ze souboru je 38 měsíců (4–60).
Histologicky byl přítomen ve všech resekátech adenokarcinom v různém stupni diferenciace (Tab. 2). U jednoho pacienta byla původně provedena ISR s předoperačním stagingem T3N0M0, G2, ale po operaci byl histologicky verifikován hlenotvorný adenokarcinom. V tomto případě byla za jedné hospitalizace provedena APR. Pacient je zařazen do souboru APR. TNM klasifikace (Tab. 3). Nebyl operován žádný pacient s T1N0M0 tumorem ve skupině KAR a ISR.
Tab. 2. Typing a Grading tumorů 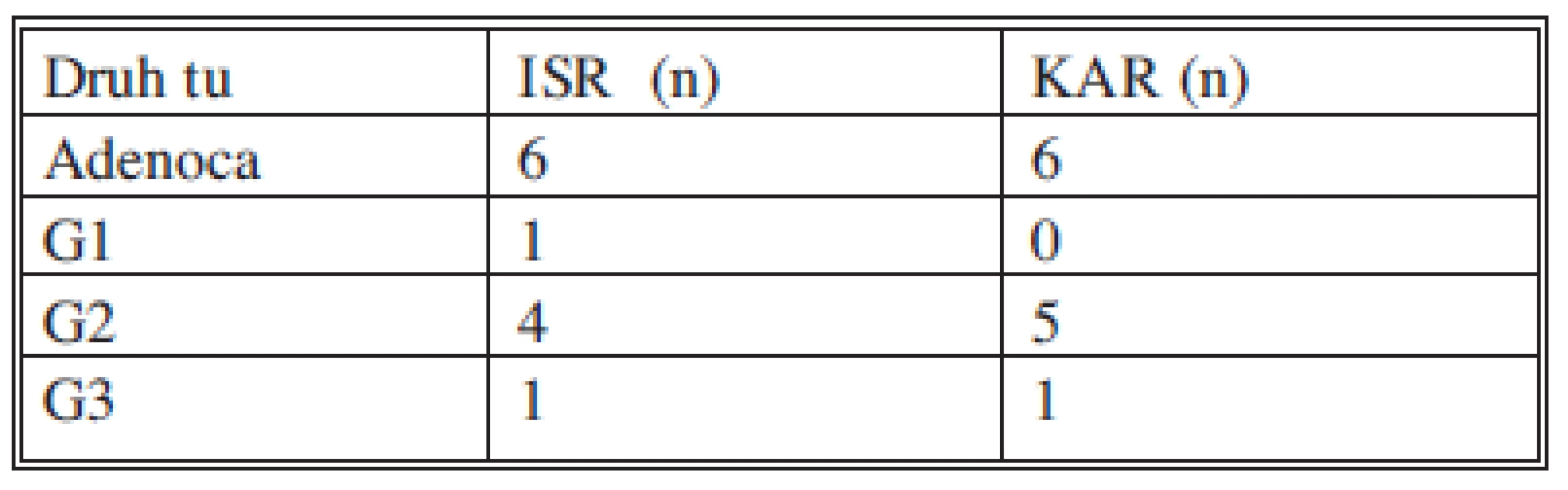
Průměrný počet uzlin byl 17 (3–35) a nijak se nelišil ve skupině s laparoskopickým přístupem a konvenčním přístupem. U pacientů po neoadjuvantní radioterapii byl průměrný počet uzlin 14,8 (5–35). Pozitivní nález v lymfatických uzlinách po neoadjuvantní radioterapii byl u jednoho pacienta. Lokální recidivy se vyskytly u 2 pacientů. Jednou po KAR – 12,5 % a jednou po ISR – 7,7 %. K progresi onemocnění došlo u jedné pacientky po ISR – 7,7 %.
Ve skupině ISR a KAR je pětileté přežívání pro rok 2007 100%. Jedná se pouze o čtyři pacienty operované v roce 2007. Tříleté přežívání ze skupiny ISR je 100% a ve skupině KAR 87,5% – jedno úmrtí.
Funkční výsledky
U pacientů plánovaných k ISR nebo ke KAR nebyla standardně prováděna anorektální manometrie. Výsledek by mohl být zkreslen přítomností tumoru. Všichni pacienti po ISR trpí nějakou formou fekální inkontinence. Okluzi ileostomie podstoupili všichni pacienti. Poté následovala rehabilitace pánevního dna a biofeedback. U 2 pacientů po ISR a jednoho pacienta po KAR se jednalo o fekální inkontinenci 3. stupně, kombinovanou s řidší stolicí. Jednalo se o dva pacienty po dehiscenci anastomózy. U třetího pacienta s fekální inkontinencí 3. stupně se nevyskytla žádná peroperační nebo pooperační komplikace. U těchto pacientů byla pak dokončena abdominoperineální amputace s terminální kolostomií. U většiny pacientů po ISR se jedná o inkontinenci 1. nebo 2. stupně. Ojedinělou inkontinenci 3. stupně pacienti řeší irigací. Koloanální anastomóza má lepší funkční výsledky než ISR.
Diskuze
Intersfinkterická resekce je indikovaná pro specifickou skupinu pacientů. Velmi důležité je co nejpřesnější předoperační vyšetření tumoru. V našem souboru bylo k ISR indikováno pouhých 7,5 % karcinomů rekta a pouze 10,6 % pacientů s tumorem ve střední a aborální třetině rekta.
Většina autorů indikuje k ISR jen časné tumory [2, 6, 7, 9, 10], ale vyskytly se i ojedinělé práce s indikací pro pokročilejší tumory [11]. Shirouzo a spol. dokonce uvádějí, že G3 adenokarcinom a hlenotvorný karcinom jsou nezávislé rizikové faktory pro invazi tumoru do intermuskulárních vrstev [12, 13].
Laparoskopický přístup pro ISR je velmi vhodný, protože zcela odpadá nutnost laparotomie a významně se tak snižuje riziko pooperační morbidity [13, 14, 15]. Pánevní disekce je snadnější, protože tumor je uložen aborálně pod pánevním dnem a umožňuje tak přehledné provedení totální mezorektální excize. O tom svědčí i 0 % počet konverzí. Krátkodobé i dlouhodobé výsledky laparoskopického přístupu jsou stejné jako u konvenčního přístupu [16, 17]. Samozřejmě laparoskopický přístup vyžaduje zkušeného laparoskopického kolorektálního chirurga, ale ještě více proktologa, který se orientuje v oblasti análního kanálu.
Hlavním rizikem ISR není onkologická radikalita, ale funkční výsledky. Gamagami uvádí až 50 % pacientů s dobrými funkčními výsledky po ISR [18]. Fyziologické studie ukázaly, že klidový anální tlak je vytvářen z 55 % vnitřním análním sfinkterem, z 15 % hemoroidálními plexy a z 30 % zevním análním sfinkterem. Anální tlak klesl ze 105 cm H2O na 75 po parciální resekci vnitřního sfinkteru a na 40 po kompletní excizi vnitřního sfinkteru [10]. Diskuze se vedou i o formě obnovy kontinuity rekta. Funkčně nejlepší výsledky má kolický J pouch, který není vhodný pro všechny pacienty, například pro muže s objemným mesokolem a úzkou pánví. V našem souboru jsme provedli anastomózy typu kolického J pouche, přímou anastomózu i end to side anastomozu, která měla nejhorší funkční výsledky. Koloplastiku jsme neprovedli ani jednou.
Další možností je posloupnost jednotlivých kroků. Někteří autoři přistupují k perineální fázi jako k první s tím, že je pak snadnější a rychlejší laparoskopický pánevní postup. K tomuto postupu máme několik výhrad: je zde nutné opakované polohování pacienta – perineální fáze, břišní fáze, perineální fáze, dále dle nás zde hrozí riziko úniku střevního obsahu do oblasti pánve a teoretické riziko uvolnění maligních buněk ze střevního lumen. Nevýhodou námi zvoleného postupu je možnost disekce v nestejné úrovni po pánevní preparaci a teoreticky větší únava operatéra při perineální fázi.
Závěr
Intersfinkterická resekce má své místo mezi resekčními výkony v oblasti rekta pro karcinom v aborální třetině rekta. Velmi důležité je správné a přesné předoperační vyšetření – endoskopie, patologie, endorektální sonografie, nukleární magnetická rezonance, digitální vyšetření a funkční stav análních sfinkterů. Laparoskopický přístup u intersfinkterických resekcí je velmi vhodný pro snížení rizika, zejména raných komplikací. I při malém počtu pacientů v našem souboru a krátkou dobu sledování jsou krátkodobé výsledky i procento pooperačních komplikací ve shodě s pracemi jiných autorů. K úspěšnému výsledku ISR je nutná rozvážná selekce pacientů. V našem souboru se až 10 % pacientů mohlo vyhnout definitivní kolostomii, což je nezanedbatelné číslo v hodnocení kvality života onkologicky nemocných.
MUDr. Julius Orhalmi
Jižní 796/5
500 03, Hradec Králové
e-mail: orhalmi@volny.cz
Zdroje
1. Williams NS, Dixon MF, Johnston D. Reappraisal of tahe 5 centimetre rule of distal excision for carcinoma of the rectum: a study of distal intramural spread and of patients survival. Br J Surg 1983;70 : 150–4.
2. Rullier E, Laurent C, Bretagnol F, Rullier A. Sphincter-saving resection for all rectal carcinomas The end of the 2-cm distal rule. Ann Surg 2005;241 : 465–469.
3. Vávra P, Rydlová M, Pelikán A, Guňková I, et al. Bezpečná vzdálenost dolní resekční linie při operaci karcinomu rekta. Rozhl Chir 2006;1 : 45–50.
4. Parks AG. Transanal technique in low rectal anastomosis. Proc R Soc Med 1972;65 : 975–976.
5. Parks AG, Percy JP. Resection and sutured colo-anal anastomosis for rectal carcinoma. Br J Surg 1982;69 : 301–304.
6. Schiessel R, Karner-Hanusch J, Herbst F, Teleky B, Wunderlich M. Intersphincteric resection for low rectal tumours. Br J Surg 1994;81 : 1376–8.
7. Tilney H.S, Tekkis PP. Extending the horizons of restorative rectal surgery: intersphincteric resection for low rectal cancer. Colorectal Dis 2008;10 : 3–15.
8. Watanabe M, Teramoto T, Hasegawa H, Kitajima M. Laparoscopic ultralow anterior resection combined with per anum intersphincteric rectal dissection for lower rectal cancer. Dis Colon Rectum 2000;43:S94–7.
9. Rullier E, Sa Cunha A, Couderc P, Rullier A, Gontier R, Saric J. Laparoscopic intersphincteric resection with coloplasty and coloanal anastomosis for mid and low rectal cancer. Br J Surg 2003,90,445–51.
10. Bretagnol F, Rullier E, Lurent Ch. Comparison of functional results and quality of life between intersphincteric resection adn conventional coloanal anastomosis for low rectal cancer. Dis Colon Rectum 2004;47 : 832–838.
11. Fucini C, Elbetti C, Petrolo A, Casella D. Excision of the levator muscles with external sphincter preservation in the treatment of selected low T4 rectal cancers. Dis Colon Rectum 2002;45 : 1697–705.
12. Shirouzu K, Ogata Y. Histopathologic tumor spread in very low rectal cancer treated with abdominoperineal resection. Dis Colon Rectum 2009;52 : 1887–1894.
13. Lim SW, Huh ÁY, Kim ÁH. Laparoscopic intersphincteric resection for low rectal cancer. World J Surg 2011;35 : 2811–2817.
14. Ströhlein MA, Grützner KU. Comparison of laparoscopic vs open Acess surgery in patients with rectal cancer: A prospective analysis. Dis.Colon Rectum 2008;51,385–391.
15. Fürst A, Schwandner O. Laparoscopic TME in rectal cancer – electronic supplementary: op.video. Langenbecks Arch Surg 2010;395 : 181–183.
16. Škrovina M, Bartoš J, Soumarová R. Laparoskopická resekcia karcinómu rekta: zhodnotenie perioperačných výsledkov primárnej resekcie a resekcie po neoadjuvantnej chemorádioterapii, Rozhl Chir 2008;87 : 417–425.
17. Martínek L, Dostalík J, Guňka I, Guňková P. Laparoskopická chirurgie karcinomu rekta – dlouhodobé výsledky. Rozhl Chir 2009;11 : 675–680.
18. Gamagami R, Istvan G, Cabarrot P. Fecal continence following partial resection of the anal canal in distal rectal cancer: long term results after coloanal anastomoses. Surgery 2000;127 : 291–295.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek Redakční komentáře
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2012 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Intersfinkterické resekce rekta
- Onkologické aspekty laparoskopických resekcí jater
- Pozdně rozpoznané ruptury bránice – soubor kazuistik
- Miniinvazivní léčba kolorektálního karcinomu a jaterních metastáz. Kam jsme zatím dospěli?
- 20 let české a moravské miniinvazivní chirurgie
- Miniinvazivní operace pectus excavatum u adolescentů a dospělých dle Nusse
- Redakční komentáře
- Videotorakoskopické operace přístupem z jedné incize – SITS
- Laparoskopie čistým transgastrickým NOTES přístupem v porovnání s klasickou laparoskopií
- Chirurgická léčba plicních metastáz kolorektálního karcinomu – desetileté výsledky
- Význam včasné chirurgické intervence v terapii nekrotizující vaskulitidy
- Burkittův lymfom céka jako vzácná příčina náhlé příhody břišní – kazuistika
- Chirurgie očima emeritních přednostů
- Ošetření pahýlu pankreatu u laparoskopické levostranné resekce
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Miniinvazivní operace pectus excavatum u adolescentů a dospělých dle Nusse
- Intersfinkterické resekce rekta
- Význam včasné chirurgické intervence v terapii nekrotizující vaskulitidy
- Pozdně rozpoznané ruptury bránice – soubor kazuistik
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání