-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Budd-Chiari syndrom a TIPS – 21 let zkušeností
Budd-Chiari syndrome and TIPS – 21 years’ experience
Budd-Chiari syndrome (BCS) often has an acute or fulminant course leading to ischaemia and necrosis of the liver parenchyma as consequence of venostasis. Restitution of blood drainage is then a key measure. In the chronic course, symptoms of portal hypertension are dominant. TIPS as a portosystemic shunt ensures both venous drainage as well as corrected portal hypertension.
Patients and methods:
TIPS has already been available for 21 years in the Czech Republic. Using this method we also treated 52 patients with BCS from thrombosis of hepatic veins. The median age was 37 years (13 to 82 years), 10% were children, 16 patients (31%) were men, 31% procedures were urgent. Myeloproliferative syndrome was the cause in 60%, another thrombophilic disorder was detected in 15%, and in 25% of them the cause was not elucidated. In the first five years, uncovered stents were used, but since 1997 different types of ePTFE covered stents have been available and since 2001 dedicated ePTFE covered stents became the standard.Results:
13 patients died: three of fulminant liver failure, one of extensive tumorous thrombosis, three of early septic complications, two of liver failure due to later acute shunt occlusion, two of progressions of haemato-oncological disease, one tragically, and one of unknown cause. Two patients later underwent OLTx. In 39 patients the shunt remains patent on anticoagulant therapy and occasional reinterventions, liver functions are stable and no portal hypertension complications occur. We have not noticed significant hepatic encephalopathy. The use of ePTFE covered stents reduced a number of mainly early occlusions. In imaging we often find nodular hyperplasia.Conclusion:
We consider TIPS an advantageous therapeutic approach in BCS due to thrombosis of the hepatic veins. If the follow-up treatment is rigorous, the TIPS usually ensures sufficient perfusion of the liver and prevents portal hypertension complications, saving most patients from liver transplantation.Key words:
Budd-Chiari syndrome – portal hypertension – transjugular intrahepatic – portosystemic shunt
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
12. 3. 2014Accepted:
7. 4. 2014
Autoři: V. Šafka 1; P. Hůlek 2,3; A. Krajina 4; T. Fejfar 2; P. Ďulíček 5; Š. Šembera 2; T. Vaňásek 2; V. Jirkovský 2; J. Žižka 4; V. Chovanec 4; Miroslav Lojík 4
; J. Raupach 4; O. Renc 4
Působiště autorů: Ústav fyziologie, LF UK, Hradec Králové 1; II. interní gastroenterologická klinika LF UK a FN Hradec Králové 2; Interní klinika LF OU, Ostrava 3; Radiologická klinika LF UK a FN Hradec Králové 4; IV. interní hematologická klinika LF UK a FN Hradec Králové 5
Vyšlo v časopise: Gastroent Hepatol 2014; 68(2): 116-123
Kategorie: Hepatologie: původní práce
Souhrn
Budd-Chiari syndrom (BCS) má mnohdy akutní až fulminantní průběh vedoucí k ischemii až nekróze jaterního parenchymu v důsledku venostázy. Obnova drenáže jaterních sinusoid je v takové situaci klíčová. Při chronickém průběhu dominuje spíše riziko komplikací portální hypertenze. TIPS jako portosystémová spojka zajistí jak venózní drenáž, tak korekci portální hypertenze.
Soubor a metodika:
TIPS je u nás dostupný již 21 let. S jeho pomocí jsme ošetřili též 52 nemocných s BCS na podkladě trombózy jaterních žil. Medián věku je 37 let (13–82 let), 10 % souboru tvoří děti, 16 nemocných (31 %) jsou muži, 31 % byl urgentní zákrok. Myeloproliferativní syndrom byl příčinou u 60 %, jiný známý prokoagulační stav byl identifikován u 15 % a u necelé čtvrtiny se příčinu nepodařilo objasnit. Prvních pět let se používaly nepotažené stenty, od roku 1997 se začaly uplatňovat různé ePTFE potažené stenty a od roku 2001 jsou standardem dedikované ePTFE potažené stenty.Výsledky:
Zaznamenali jsme třináct úmrtí: tři fulminantní jaterní selhání, jednu extenzivní tumorózní trombózu, tři časné septické komplikace, dvě jaterní selhání při pozdější akutní okluzi zkratu, dvě v důsledku hematoonkologického onemocnění, jedno úrazem a jedno z neznámé příčiny. Dva nemocní podstoupili transplantaci jater. U 39 nemocných zkrat zůstává při antikoagulační terapii a občasných revizích funkční, jaterní funkce stabilizované a komplikace portální hypertenze se neobjevují. Nezaznamenali jsme klinicky významnou jaterní encefalopatii po TIPS. Použití potažených stentů výrazně snížilo především výskyt časných okluzí zkratu. Při zobrazovacích vyšetřeních lze často pozorovat nodulární přestavbu.Závěr:
TIPS považujeme za velmi výhodnou terapeutickou volbu u BCS na podkladě trombózy jaterních žil. Za předpokladu důsledné následné péče TIPS obvykle zajistí potřebnou perfuzi jaterní tkáně a zabrání komplikacím portální hypertenze, čímž velkou většinu nemocných ušetří transplantace jater.Klíčová slova:
Budd-Chiari syndrom – portální hypertenze – transjugulární intrahepatální – portosystémový zkratBudd-Chiari syndrom (BCS) představuje syndrom postsinusoidální portální hypertenze, za níž mohou stát všechny možné příčiny venostázy mezi centrální žilou a pravou srdeční síní (je nutno odlišit venookluzivní chorobu, která představuje intrasinusoidální trombózu a má značně odlišné etiologické i klinické charakteristiky). Rozsah výsledného jaterního postižení a klinický obraz úzce souvisí s rozsahem překážky, jenž může být od nevýznamné fokální léze až po závažné plošné postižení jaterního parenchymu. Rychlost rozvoje překážky zásadně ovlivňuje charakter klinické manifestace, protože rychle vzniklá venostáza v příslušném okrsku jaterní tkáně znamená riziko ischemického poškození funkčního parenchymu [1].
V našich podmínkách se obvykle setkáváme s disperzním až difuzním postižením jaterního parenchymu na podkladě trombózy intrahepatálních větví jaterních žil. Tento typ BCS může být navíc kombinován s různým rozsahem trombózy portální žíly. Příčinou může být trombofilní stav, a to jednak na podkladě buněčné poruchy hemostázy při myeloproliferativním onemocnění (daleko častěji) či při poruše rovnováhy prokoagulačních a antikoagulačních faktorů (poměrně vzácně), ať již vrozené či získané. Diagnostika koagulační poruchy nebývá vždy jednoduchá, vyžaduje cílený přístup a i tak se u významného procenta případů žádnou známou příčinu nepodaří odhalit.
Rychlost rozvoje poruchy lze kategorizovat různými způsoby, v zásadě však je průběh buď dramatický (akutní až fulminantní), nebo pozvolný až nenápadný. V prvním případě klinickému obrazu dominuje bolest břicha s dyspeptickým syndromem a rychlým rozvojem refrakterního ascitu až hepatorenálního syndromu [2] provázená různě intenzivní ischemickou jaterní lézí, která může vyústit do fulminantního jaterního selhání. V pozadí tohoto obrazu typicky stojí hematoonkologická příčina a léčbou volby je vedle antikoagulační terapie portální dekomprese pomocí portosystémového zkratu, která zajistí alternativní perfuzi jaterního parenchymu a představuje i určitou prevenci šíření trombózy do portálního řečiště. Necílená trombolýza se v této situaci nejeví jako účinná. Kritickými momenty v klinické praxi bývají jednak včasná diagnóza příčiny akutní jaterní léze a dostupnost dekompresního zákroku. Diagnostika při dnešní úrovni zobrazovacích metod (dopplerovská ultrasonografie, angio-CT, magnetická rezonance) nebývá problém, pokud se ovšem na tuto eventualitu včas myslí. Klasická triáda bolesti břicha, hepatomegalie a rychle progredujícího ascitu v souvislosti s akutní jaterní lézí by vždy měla vést k této suspekci. Významným podnětem by měl být i relativně vysoký obsah bílkovin v ascitu (> 25g/l při gradientu proti séru > 11g/l) a jejich struktura odpovídající transsudátu (převaha albuminů) [3,4]. Hlavní překážkou včasné diagnózy je především vzácnost tohoto postižení – dle literárních údajů cca 2/10 mil./rok v evropské populaci.
Portosystémový zkrat by měl být vzhledem k relativně malému procedurálnímu riziku vytvořen vazografickou technikou, a to buď klasicky jako TIPS (transjugulární intrahepatální portosystémová spojka) mezi některou jaterní žilou a větví portální žíly (obr. 1), či jako DIPS (direct – přímá intrahepatální portosystémová spojka) mezi dolní dutou žilou a větví portální žíly. Varianta DIPS řeší častý problém, kdy je ústí jaterních žil okludováno a nelze do nich katetrem proniknout. Protože játra v určitém úseku naléhají na dolní dutou žílu, našlo se pro tento častý problém řešení: vpich cílený na větev porty se vede přímo z dolní duté žíly (obr. 2). Udržení průchodnosti zkratu stejně jako dlouhodobá perspektiva nemocného pak závisí především na dlouhodobé hematologické či hematoonkologické péči o základní onemocnění i o antikoagulační léčbu.
V druhém případě, kdy se okluze jaterních žil rozvíjí pozvolna, bývá diagnóza obtížnější. Rozvíjí-li se postižení v horizontu měsíců, podezření obvykle vzbudí diskrepance pokročilé portální hypertenze (opět dominuje ascites) a relativně dobrého stavu jaterní tkáně. Postižení též mnohdy bývají mladšího věku, než bývá obvyklé například u alkoholové cirhózy. Diagnózu nám může přinést jaterní biopsie s obrazem kongestivního charakteru postižení jaterního lalůčku. V případě ještě pozvolnějšího průběhu nemusí být ani jaterní biopsie diagnostická, protože histologickému obrazu dominuje cirhotická přestavba bez dostatečně specifických charakteristik. Šanci na správnou diagnózu dále snižuje nehomogenní postižení jaterního parenchymu. Zajímavou indicií v diagnostické rozvaze (u každého typu a fáze postižení) může být nízká sedimentace erytrocytů [5]. Základem léčby je opět antikoagulační léčba, léčba základního onemocnění a případně portokavální zkrat, který řeší komplikace portální hypertenze a brání progresi jaterní léze.
Na našem pracovišti je TIPS dostupný již přes 21 let a velmi záhy po jeho zavedení byla zvládnuta i technika DIPS. Ročně je pomocí tohoto zákroku ošetřeno cca 50 nemocných se závažnou portální hypertenzí, takže počet provedených zákroků již překročil 1 000. Valnou většinu ošetřených nemocných obvykle po zákroku dispenzarizujeme a prospektivně sledujeme z hlediska dalšího klinického vývoje. Cílem této studie je analyzovat naše zkušenosti s použitím TIPS v léčbě Budd-Chiari syndromu na podkladě plošné trombózy jaterních žil.
Charakteristika souboru
Od září 1992 do konce roku 2013 jsme TIPS (včetně varianty DIPS) úspěšně provedli u 995 nemocných. 52 z nich (5 %) zákrok podstoupilo z důvodu Budd--Chiari syndromu. Zatímco v obvyklých indikacích TIPS tvoří muži 2/3 souboru, jehož věkový medián se pohybuje okolo 54 let [6], v této specifické skupině bylo pouze 16 mužů (31 %) a věkový medián byl 37 let (min. 13, max. 82; 50 % v rozmezí 23–47 let) a pět nemocných bylo mladších 18 let (graf 1).
Graf 1. Věková struktura souboru. Graph 1. The age structure of the file. 
Technická úspěšnost zákroku byla 98 % (jeden neúspěšný pokus o TIPS z důvodu kompletní trombózy intrahepatálních větví porty v roce 1995), nebyla zaznamenána klinicky významná technická komplikace, zkrat přímo z dolní duté žíly (DIPS) byl vytvořen u 19 nemocných (obr. 1 a 2).
Obr. 1. Schéma transjugulární intrahepatální portosystémové spojky (TIPS). Fig. 1. Diagram of transjugular intrahepatic portosystemic shunt (TIPS). 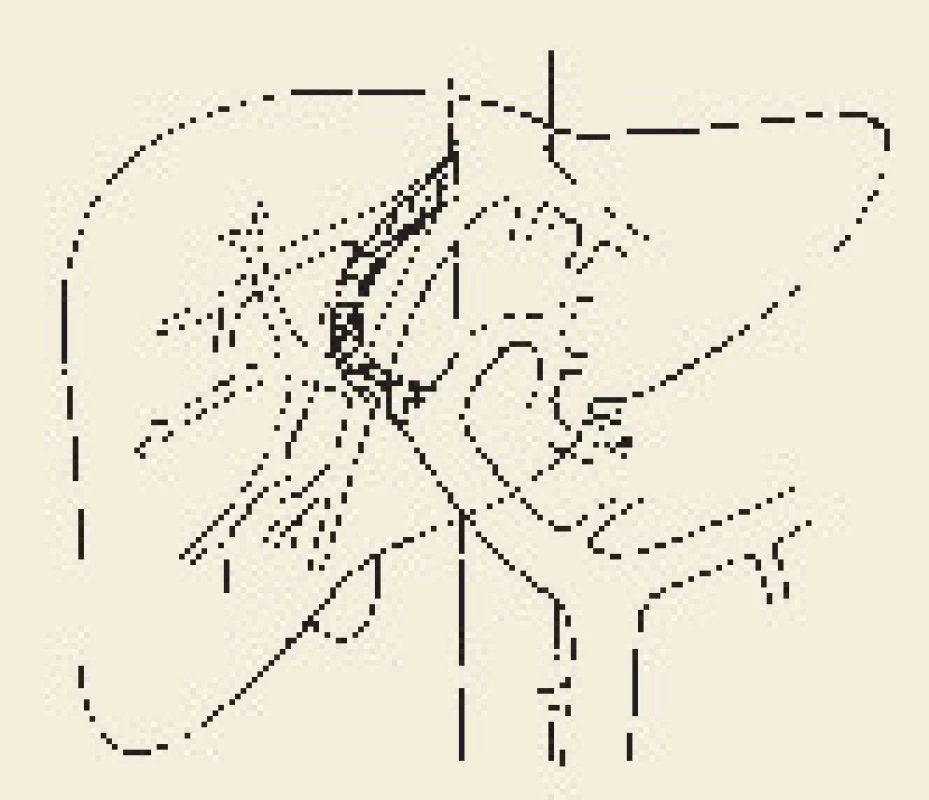
Obr. 2. Schéma přímé (direct) intrahepatální portosystémové spojky (DIPS). Fig. 2. Diagram of direct intrahepatic portosystemic shunt (DIPS). 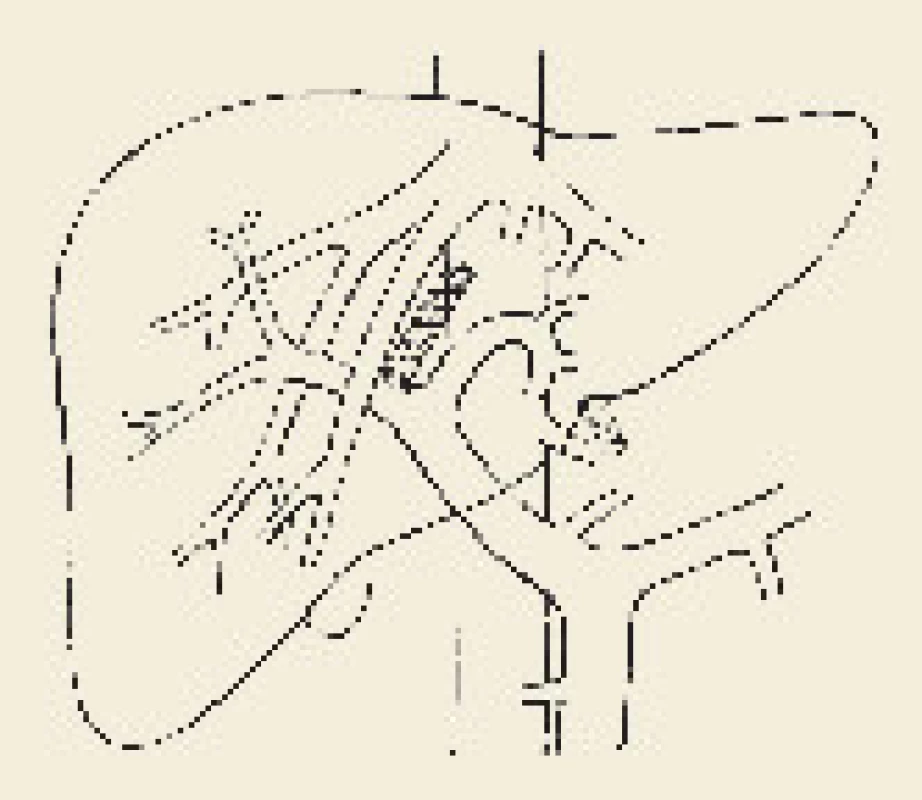
Jako základní onemocnění byl u 24 nemocných diagnostikován myeloproliferativní syndrom, z toho 14 polycytemia vera. U šesti nemocných nebyla přes cílené vyšetření příčina objasněna, u 11 nebyla vyšetřena nebo jsme se ji nedozvěděli, u dvou byla zaznamenána pouze orální kontracepce. Celkem tedy u 19 osob v našem souboru nebyla příčina uspokojivě objasněna. U zbývajících devíti osob jsme jako příčinu zaznamenali antifosfolipidový syndrom (3×), paroxysmální noční hemoglobinurii (2×), Leidenskou mutaci f. V (3×) a deficit prot. C, obě většinou v kombinaci s další příčinou, mutaci f. II a tumorózní trombózu. Celkem 4× se jednalo o kombinaci dvou známých příčin (graf 2).
Graf 2. Etiologie trombofilie. PV – polycytemia vera, jMP – jiné typy myeloproliferativního sy, x – známá příčina nenalezena, ? – nevyšetřeno nebo neznáme výsledek, x+OCC – kromě anamnézy orální kontracepce známá příčina nenalezena, jKP – jiné známé poruchy koagulace a jejich kombinace Graph 2. The etiology of thrombophilia. PV – polycythemia vera, jMP – other types myeloproliferative sy, x – a known cause not found, ? – not surveyed or unknown outcome, x + OCC – except for oral contraceptive history known cause not found, jKP – other known coagulation disorders and their combinations 
V 16 případech (31 %) byl TIPS indikován jako urgentní zákrok – u čtyř nemocných pro akutní krvácení do horního GIT, jednou pro podezření na akutní trombózu porty a jednou pro extenzivní trombózu dolní duté žíly, u zbylých deseti nemocných pro progresivní jaterní selhání či obavy z další rychlé progrese. Pouze u jednoho z těchto případů byla prokázána jiná základní etiologie než myeloproliferace; u tří nebyla příčina náležitě objasněna.
U třinácti nemocných byl k vytvoření zkratu použit nepotažený Wallstent či spirální Z-stent, z toho u devíti do roku 2000. Do roku 1997 nebyly potažené stenty vůbec k dispozici, od roku 2001 se s cílem snížit výskyt poruch průchodnosti zkratu již standardně používal dedikovaný ePTFE (Goretex) potažený stent. Takto potažené stenty se používají i k řešení případných okluzí a stenóz zkratů [7].
Výsledky
V průběhu sledování zemřelo třináct nemocných – u tří se zákrokem nepodařilo zvrátit již rozvinutou masivní jaterní nekrózu a nemocní zemřeli pod obrazem fulminantního jaterního selhání. U jednoho staršího nemocného se nepodařilo kontrolovat extenzivní tumorózní trombózu šířící se do dolní duté žíly, u jedné nemocné s polycytemií se nepodařilo navzdory mnohočetným intervencím terapeuticky zvládnout trombofilii v povodí porty komplikovanou sepsí, další dva rovněž v období do tří měsíců zemřeli na generalizovanou infekci, dva zemřeli na jaterní selhání, jež vzniklo v souvislosti s pozdější rozsáhlou akutní trombózou a okluzí zkratu (jeden a tři roky po zákroku), jeden zemřel v důsledku maligního zvratu základního onemocnění (čtyři roky po zákroku) a jeden po transplantaci kostní dřeně (11 měsíců po TIPS), jeden nemocný zemřel úrazem bez zřejmé souvislosti s onemocněním (dva roky po TIPS) a u jednoho příčina úmrtí mimo zdravotnické zařízení (po 10 měsících) není známá (tab. 1).
Tab. 1. Analýza úmrtí po TIPS pro BCS. Tab. 1. Analysis of death after TIPS for BCS. 
Jeden nemocný pro recidivy okluzí podstoupil transplantaci jater (28 měsíců po zákroku; šest revizí) a jeden čtyři roky po zákroku z důvodu jaterní insuficience. Dle kumulativní křivky přežití pět let od zákroku přežívá 70 % nemocných, přičemž tohoto horizontu sledování se dožilo 21 nemocných; 10 let přežívá osm nemocných a 15 let tři nemocní (graf 3).
Graf 3. Kumulativní Kaplan-Meierova křivka přežití po TIPS pro BCS (k.i. 80 %). Graph 3. Cumulative Kaplan-Meier survival curve after TIPS for BCS (c.i. 80%). 
Poruchu průchodnosti zkratu bylo nutno do jednoho roku řešit u 15 nemocných, z toho časně (do 10 dnů) u sedmi nemocných; vážnější poruchy průchodnosti (opakované revize či okluze s vážným následkem) byly zaznamenány u sedmi nemocných. Pozoruhodné je ale zjištění, že z 16 nemocných, u nichž nedošlo do tří let po zákroku k poruše průchodnosti, k ní později došlo u jediného z nich. U zbývajících 15 nebyla porucha průchodnosti nikdy zaznamenána, přestože medián jejich sledování je 86 měsíců s rozsahem 36–160 měsíců. Dva z těchto nemocných měli nepotažený stent (sledování 88 a 160 měsíců) (graf 4).
Graf 4. Kumulativní Kaplan-Meierova křivka primární průchodnosti TIPS pro BCS v závislosti na použitém stentu. Graph 4. Cumulative Kaplan-Meier curve for the primary patency of TIPS for depending on the type of stent. 
U pěti nemocných byl pro poruchu průchodnosti zaveden stent do intrahepatálního úseku dolní duté žíly (obr. 3).
Obr. 3. Obraz paralelního stentování dolní duté žíly při její významné stenóze hypertrofickou jaterní tkání. Fig. 3. Picture of parallel stenting of inferior vena cava in significant stenosis by hypertrophic liver tissue. 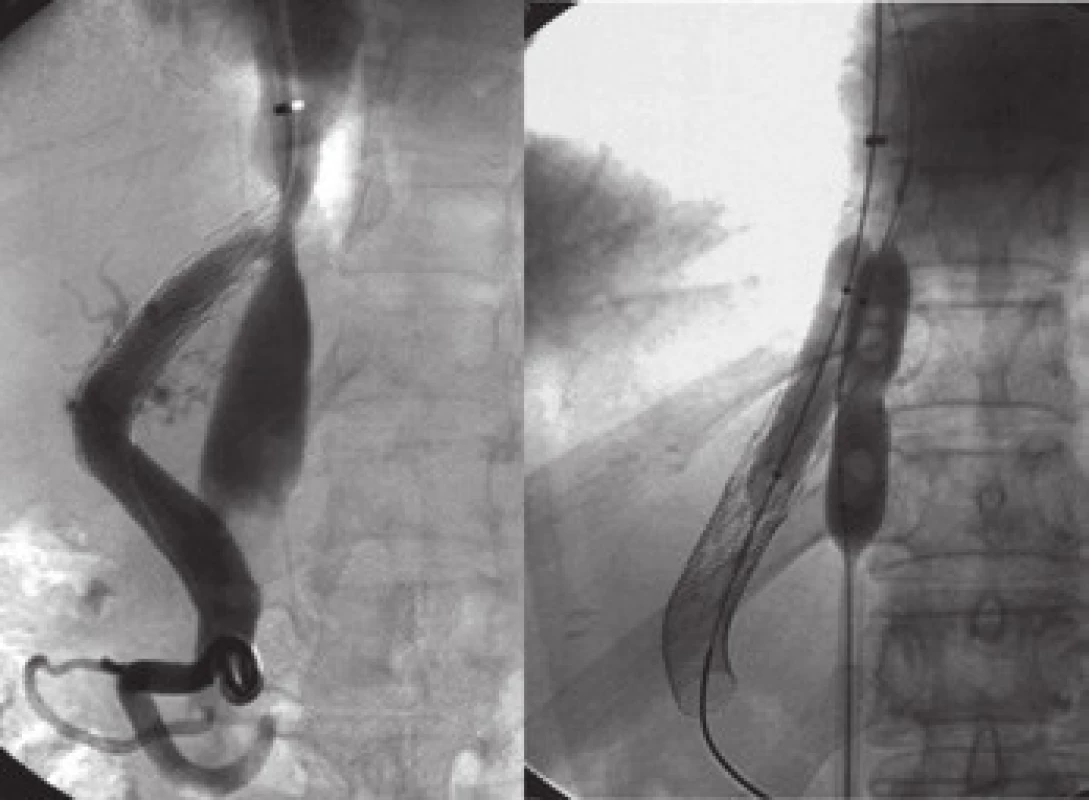
Při rozdělení souboru dle typu použitého stentu (tab. 2) je zřetelný rozdíl ve výskytu časných okluzí. Pokud jde o výskyt pozdních dysfunkcí zkratu po tomto období do jednoho roku po TIPS, zde již rozdíl není tak výrazný. Výskyt recidivujících stenóz byl mezi tyto skupiny rozdělen v poměru 3 : 4. V obou skupinách lze nalézt jedince, kteří nepotřebovali ani jednu revizi po mnoho let od zavedení zkratu. Graf 4 zobrazuje kumulativní křivku primární průchodnosti TIPS v závislosti na typu stentu. Dle log-rank testu je rozdíl signifikantní (p = 0,02).
Tab. 2. Obstrukce zkratu. Tab. 2. Shunt obstruction. 
Aktuálně evidujeme 39 žijících nemocných, z toho 29 nemocných s dobou sledování delší než jeden rok. U všech se daří udržovat zkrat průchodný. U žádného z nich jsme nezaznamenali jaterní encefalopatii v souvislosti se zavedením TIPS. Jaterní funkce jsou kromě zmíněného případu pokročilé jaterní cirhózy indikovaného k transplantaci jater stabilizované a nikdo z nich nemá známky závažné portální hypertenze (bez ascitu a recidiv krvácení). Všichni nemocní s prokázanou poruchou koagulace či myeloproliferativním onemocněním mají trvalou antikoagulační léčbu a jsou v dispenzární péči hematologa.
Diskuze
BCS představuje nepříliš časté, avšak klinicky závažné postižení, jež působí jednak portální hypertenzi se všemi významnými důsledky (ascites, krvácení do GIT, hepatorenální syndrom) a jednak ischemickou jaterní lézi s potenciálně fatálními následky. V našich podmínkách se typicky jedná o trombotickou komplikaci základního hematologického onemocnění, které nejčastěji představuje myeloproliferativní syndrom, konkrétně pravá polycytemie [8]. Příčinou jsou zřejmě genetické mutace, jež stojí za neadekvátní reakcí neutrofilů [9,10]. Jako diagnosticky klíčová se záhy ukázala specifická mutace Janusova genu pro tyrozinkinázu-2 (JAK2), která toto důležité hematologické postižení odhalí dlouho před jeho zřetelnou klinickou manifestací [11,12].
Pokud jde o poruchy koagulační kaskády, ty jako příčinu BCS nalézáme méně často. Dle literárních údajů jde nejčastěji o antifosfolipidový syndrom [13,14] a dále o kongenitální defekty, jako je Leidenská mutace V. koagulačního faktoru, mutace genu protrombinu (20210A) a deficit proteinu C a S [15,16], který však je z hlediska diagnostiky značně problematický [17]. Průběžně jsou objevovány další specifické defekty hemokoagulačního systému ve vztahu k trombózám splanchnických žil [18], jež slibují další rozšiřování diagnostického panelu a etiologického objasnění většího procenta případů. Užívání kontraceptiv, které jsme zaznamenali jako jedinou známou příčinu u dvou našich pacientek, však samo o sobě není literárně považováno za příčinu trombofilie, spíše za kofaktor obdobně jako v jiných případech trombózy [19]. Paroxyzmální noční hemoglobinurie představuje poruchu exprese povrchových proteinů na krevních elementech s neadekvátními reakcemi komplementu. Projevuje se hemolýzou či trombózami v různých lokalizacích včetně jaterních žil [20,21].
Obecně se však předpokládá, že ke vzniku trombózy v povodí jaterních žil je potřebná koincidence více než jednoho prokoagulačního faktoru, čímž je dána zřetelná vzácnost syndromu navzdory podstatně častějšímu výskytu uvedených prokoagulačních poruch [22].
Z uvedeného vyplývá, že dlouhodobá prognóza nemocných je po zvládnutí akutních komplikací především věcí léčby základního hematologického onemocnění. Hematolog je v našem centru nepostradatelným členem týmu zajišťujícího jak diagnostiku, tak následnou léčbu každého nemocného s rozpoznaným BCS, který je v našem centru dále dispenzarizován. Nedílnou součástí léčby je i trvalá antikoagulace, kterou též řídí hematolog.
Zavedení TIPS mezi běžné metody léčby portální hypertenze představuje přínos i pro terapii jaterního postižení a portální hypertenze u nemocných s BCS. Již před érou TIPS byla k léčbě BCS používána chirurgicky vytvořená portosystémová spojka, zákrok však vždy znamenal vážné riziko pro bezprostřední stav nemocného v akutním stavu jaterní léze. Miniinvazivní transluminální přístup v podobě TIPS (event. DIPS) tuto problematiku radikálně mění [23–25] a stal se nedílnou součástí terapeutických doporučení [22,26]. Chirurgické portosystémové zkraty v tomto ohledu ztrácejí svůj význam, především kvůli své klesající dostupnosti, přestože v určitých situacích mohou mít své výhody [27]. V našich podmínkách je TIPS dostupný v horizontu několika málo hodin a nepředstavuje významné riziko ani pro nemocné s fulminantním průběhem postižení. Umožňuje i lokální trombektomickou a trombolytickou léčbu. To je v situaci, kdy nebyl prokázán významný efekt necílené/systémové trombolýzy [28], další výhoda. Dle našich zkušeností urgentním vytvořením portosystémového zkratu obvykle dosáhneme promptního zvratu ve vývoji jaterního postižení. Toho se nepodařilo dosáhnout ve třech případech fulminantního průběhu, kdy již byla nekróza jaterní tkáně příliš rozsáhlá a nebyly dostupné nástroje, jak období akutního jaterního selhání překlenout, anebo použití podpůrného systému nebylo v nastalé klinické situaci indikováno [29]. V prvním případě tomuto vývoji napomohly dlouhé diagnostické rozpaky před odesláním nemocného do našeho centra, v dalších však již byla situace složitější a další vývoj se nepodařilo dobře predikovat. Jistou nevypočitatelnost klinického vývoje u akutních forem BCS dokumentuje i nespolehlivost indikačních skórovacích kritérií, jež byly v literatuře navrženy [30–32]. U nemocných s akutním nástupem příznaků a významným postižením jaterních funkcí lze tedy doporučit raději časnější indikaci TIPS a transfer nemocného do centra s úspěšným vazografickým pracovištěm než dlouhé pokusy o zvládnutí situace konzervativními postupy. Dle našeho názoru by měl přínos časného zavedení TIPS u takovýchto nemocných bez pokročilé jaterní cirhózy v principu vždy spíše převážit jeho rizika.
Technickým problémem při zákroku může být trombóza ústí velkých jaterních žil, jež brání vstupu katetru do jejich větví a vytvoření typického zkratu mezi jaterní žilou (obvykle pravou) a větví portální žíly (rovněž obvykle pravou). Zvládnutí v úvodu popsané techniky DIPS našimi radiology tento problém účinně řeší. S jeho pomocí bylo úspěšně ošetřeno 19 nemocných v našem souboru.
Důležitým úkolem po vytvoření zkratu je udržet jeho průchodnost. Ranná plocha v jaterním parenchymu v situaci trombofilního stavu přináší významné riziko jeho trombotické okluze. S ní se v časném období často setkáváme i přes řádně vedenou antikoagulační léčbu. Podle našich zkušeností riziko časné okluze zkratu sice výrazně snižuje, ale zcela neřeší ani potažení stentu expandovaným polytetrafluoretylenem (ePTFE). Tuto komplikaci lze ovšem zachytit pomocí kontrol průchodnosti dopplerovským ultrazvukem a dobře řešit vazografickým přístupem.
Pokud jde o problém pozdních a recidivujících obstrukcí zkratu (stenóz i trombóz), s nimiž se rovněž potýkáme, zde má dle našich výsledků ePTFE potah rovněž svůj kladný význam, i když poněkud méně výrazný [33]. V zásadě se u pozdějších akutních okluzí jedná o dekompenzaci základního hematologického postižení; v případě stenóz, které se vyvíjejí pozvolna, je mechanizmus obdobný jako u TIPS v obvyklých hepatologických indikacích. Proto nutnost trvalých důsledných kontrol průchodnosti zkratu pomocí dopplerovského ultrazvuku nadále platí, a to nejlépe centrem, které zákrok provádí. V případě necirhotického postižení a efektivní léčby základního onemocnění lze zřejmě riziko recidivy jaterního postižení či portální hypertenze v případě rozvoje stenózy považovat za méně závažné, přesto je nutno takovou situaci dobře klinicky zvážit. V našem souboru je i případ, kdy byl zkrat po několik let ponechán uzavřený, ale pro následnou pozvolnou progresi jaterní léze bylo opět přistoupeno k jeho rekanalizaci.
Dalším specifickým problémem nemocných s BCS je rozvoj stenózy dolní duté žíly. Ta se typicky rozvíjí v chronické fázi postižení, kdy kvůli odlišné žilní drenáži hypertrofuje lobus caudatus a utlačuje hepatální úsek dolní duté žíly. I v této situaci intervenční radiologie poskytuje řešení. U tří nemocných v našem souboru jsme v průběhu naší dispenzarizace pro známky klinicky významného tlakového gradientu v tomto úseku provedli angioplastiku a rovněž zavedli kovový stent (obr. 3). RTG snímek naznačuje, že tento úsek je třeba chránit i při samotném vytváření zkratu, kdy by místní expanze při dilataci tvořeného zkratu mohla zvýšit impresi jaterní tkáně do lumen dolní duté žíly.
Poslední otázkou zůstává místo transplantace jater v léčbě BCS, která je od počátku přirozeně považována za terapeutickou možnost [34,35]. Zkušenosti posledního desetiletí ji však logicky zařadili až jako ultimum refugium za selhání konzervativnějších přístupů [36]. V našich podmínkách se tento přístup uplatní spíše v elektivní indikaci při pozvolné progresi jaterní insuficience či při jiných vážných komplikacích než v akutní fázi, kdy je další vývoj, jak uvedeno výše, těžko předvídatelný a TIPS je pohotověji dostupný [37]. Vzhledem k tomu, že akutní až fulminantní průběh BCS je typicky spojen s proliferativním hematologickým onemocněním, je definitivní řešení pomocí TIPS rovněž výhodnější z hlediska dlouhodobé perspektivy.
Pokud BCS probíhá chronicky a dlouho latentně, může dospět do stadia pokročilé jaterní cirhózy se všemi obvyklými důsledky. Pak je indikace k transplantaci jater obdobná jako u jiných nemocných s cirhózou, a je-li v pozadí kongenitální porucha hemokoagulace, pak lze toto řešení považovat za výhodné i z pohledu korekce metabolického defektu.
V našem souboru byli k transplantaci jater indikováni dva nemocní, a to jednak pro úporné problémy s udržením průchodnosti zkratu v éře před zavedením potažených stentů (jeho další klinický průběh však byl nepříznivý, což mohlo souviset i s jeho základním hematoonkologickým onemocněním) a jednak pro rozvinutou jaterní cirhózu se známkami progrese jaterní insuficience.
Lze tedy shrnout, že TIPS řeší efektivně jak komplikace portální hypertenze, s nimiž nemocní s BCS obvykle přicházejí, tak i problém ischemické jaterní nekrózy, což je z hlediska perspektivy jaterní funkce podstatnější a ve srovnání s jinými indikacemi TIPS diametrálně odlišné. Ve většině případů je definitivní léčbou jaterního postižení při BCS na podkladě plošné trombózy jaterních žil. Podaří-li se dlouhodobě udržet jeho průchodnost, což se při správné hematologické léčbě základního onemocnění a současném dodržení harmonogramu kontrol obvykle daří, ochrání nemocné před jaterním selháním i problematickou a nákladnou jaterní transplantací. Další osud nemocného bývá určen vývojem základního onemocnění.
Publikace je spolufinancovaná Evropským sociálním fondem a státním rozpočtem České republiky. Registrační číslo projektu: CZ.1.07/2.3.00/20.054, název projektu: HEPIN II.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 12. 3. 2014
Přijato: 7. 4. 2014
MUDr. Václav Šafka, Ph.D.
Ústav fyziologie, LF UK Hradec Králové
Šimkova 870, 500 38 Hradec Králové
safkavac@lfhk.cuni.cz
Zdroje
1. Valla DC. The diagnosis and management of the Budd-Chiari syndrome: consensus and controversies. Hepatology 2003; 38(4): 793–803.
2. Sebastian S, Tuite D, Crotty P et al. Painful ascites. Gut 2004; 53(9): 1344, 1355.
3. Runyon BA, Montano AA, Akriviadis EA et al. The serum-ascites albumin gradient is superior to the exudate-transudate concept in the differential diagnosis of ascites. Ann Intern Med 1992; 117(3): 215–220.
4. Gines P, Cárdenas A, Arroyo V et al. Management of cirrhosis and ascites. N Engl J Med 2004; 350(16): 1646–1654.
5. Vanasek T, Dulicek P, Hulek P et al. Erythrocyte sedimentation rate (ESR) as diagnostic test for Budd-Chiari syndrome? J Hepatol 2001; 34 : 64. doi: 10.1016/S0168-8278(01)81094-1.
6. Sembera S, Jirkovský V, Fejfar T et al. Survival of patients after TIPS in the University Hospital Hradec Kralove. Vnitr Lek 2011; 57(12): 1038–1044.
7. Jirkovsky V, Fejfar T, Safka V et al. Influence of the secondary deployment of expanded polytetrafluoroethylene-covered stent grafts on maintenance of transjugular intrahepatic portosystemic shunt patency. J Vasc Interv Radiol 2011; 22(1): 55–60. doi: 10.1016/j.jvir.2010.09.016.
8. Safka V, Hůlek P, Krajina A et al. Budd-Chiari syndrome and TIPS – twelve years' experience. Cas Lek Cesk 2005; 144 (Suppl 3): 38–42.
9. Alvarez-Larrán A, García-Pagán JC, Abraldes JG et al. Increased CD11b neutrophil expression in Budd-Chiari syndrome or portal vein thrombosis secondary to polycythaemia vera. Br J Haematol 2004; 124(3): 329–335.
10. Smalberg JH, Darwish Murad S, Braakman E et al. Myeloproliferative disease in the pathogenesis and survival of Budd-Chiari syndrome. Haematologica 2006; 91(12): 1712–1713.
11. Patel RK, Lea NC, Heneghan MA et al. Prevalence of the activating JAK2 tyrosine kinase mutation V617F in the Budd-Chiari syndrome. Gastroenterology 2006; 130(7): 2031–2038.
12. Smalberg JH, Arends LR, Valla DC et al. Myeloproliferative neoplasms in Budd-Chiari syndrome and portal vein thrombosis: a meta-analysis. Blood 2012; 120(25): 4921–4928. doi: 10.1182/blood-2011-09-376517.
13. Bhattacharya M, Yeh BM, Qayyum A et al. Case 81: antiphospholipid antibody syndrome with adrenal hemorrhage and Budd-Chiari syndrome. Radiology 2005; 235(1): 53–55.
14. Nanke Y, Kotake S, Nakanishi Y et al. Budd-Chiari syndrome associated with primary antiphospholipid syndrome. Clin Exp Rheumatol 2002; 20(3): 433.
15. Janssen HL, Meinardi JR, Vleggaar FP et al. Factor V Leiden mutation, prothrombin gene mutation, and deficiencies in coagulation inhibitors associated with Budd-Chiari syndrome and portal vein thrombosis: results of a case-control study. Blood 2000; 96(7): 2364–2368.
16. Bhattacharyya M, Makharia G, Kannan M et al. Inherited prothrombotic defects in Budd-Chiari syndrome and portal vein thrombosis: a study from North India. Am J Clin Pathol 2004; 121(6): 844–847.
17. Valla DC. Thrombosis and anticoagulation in liver disease. Hepatology 2008; 47(4): 1384–1393. doi: 10.1002/hep.22192.
18. D'Amico M, Sammarco P, Pasta L. Thrombophilic Genetic Factors PAI-1, MTHFRC677T, V Leiden 506Q, and Prothrombin 20210A in Noncirrhotic Portal Vein Thrombosis and Budd-Chiari Syndrome in a Caucasian Population. Int J Vasc Med 2013 : 717480. doi: 10.1155/2013/717480.
19. Minnema MC, Janssen HL, Niermeijer P et al. Budd-Chiari syndrome: combination of genetic defects and the use of oral contraceptives leading to hypercoagulability. J Hepatol 2000; 33(3): 509–512.
20. Hauser AC, Brichta A, Pabinger-Fasching I et al. Fibrinolytic therapy with rt-PA in a patient with paroxysmal nocturnal hemoglobinuria and Budd-Chiari syndrome. Ann Hematol 2003; 82(5): 299–302.
21. Titton RL, Coakley FV. Case 51: paroxysmal nocturnal hemoglobinuria with thrombotic Budd-Chiari syndrome and renal cortical hemosiderin. Radiology 2002; 225(1): 67–70.
22. Valla DC. Primary Budd-Chiari syndrome. J Hepatol 2009; 50(1): 195–203. doi: 10.1016/j.jhep.2008.10.007.
23. Darwish Murad S, Valla DC et al. Determinants of survival and the effect of portosystemic shunting in patients with Budd-Chiari syndrome. Hepatology 2004; 39(2): 500–508.
24. Orug T, Soonawalla ZF, Tekin K et al. Role of surgical portosystemic shunts in the era of interventional radiology and liver transplantation. Br J Surg 2004; 91(6): 769–773.
25. Molmenti EP, Segev DL, Arepally A et al. The utility of TIPS in the management of Budd-Chiari syndrome. Ann Surg 2005; 241(6): 978–981.
26. Hefaiedh R, Cheikh M, Marsaoui L et al. The Budd-Chiari syndrome. Tunis Med 2013; 91(6): 376–381.
27. Gur I, Diggs BS, Orloff SL. Surgical portosystemic shunts in the era of TIPS and liver transplantation are still relevant. HPB (Oxford) 2013. doi: 10.1111/hpb.12163.
28. Sharma S, Texeira A, Texeira P et al. Pharmacological thrombolysis in Budd Chiari syndrome: a single centre experience and review of the literature. J Hepatol 2004; 40(1): 172–180.
29. Tan HK, Lim JS, Tan CK et al. MARS therapy in critically ill patients with advanced malignancy: a clinical and technical report. Liver Int 2003; 23 (Suppl 3): 52–60.
30. Garcia-Pagán JC, Heydtmann M, Raffa S et al. TIPS for Budd-Chiari syndrome: long-term results and prognostics factors in 124 patients. Gastroenterology 2008; 135(3): 808–815. doi: 10.1053/j.gastro.2008.05.051.
31. Rautou PE, Moucari R, Escolano S et al. Prognostic indices for Budd-Chiari syndrome: valid for clinical studies but insufficient for individual management. Am J Gastroenterol 2009; 104(5): 1140–1146. doi: 10.1038/ajg.2009.63.
32. Zhang K, Xu H, Zu M et al. Predictive value of five prognostic models for Budd-Chiari syndrome in China. Nan Fang Yi Ke Da Xue Xue Bao 2014; 34(1): 88–91.
33. Hernández-Guerra M, Turnes J, Rubinstein P et al. PTFE-covered stents improve TIPS patency in Budd-Chiari syndrome. Hepatology 2004; 40(5): 1197–1202.
34. Klein AS, Molmenti EP. Surgical treatment of Budd-Chiari syndrome. Liver Transpl 2003; 9(9): 891–896.
35. Attwell A, Ludkowski M, Nash R et al. Treatment of Budd-Chiari syndrome in a liver transplant unit, the role of transjugular intrahepatic porto-systemic shunt and liver transplantation. Aliment Pharmacol Ther 2004; 20(8): 867–873.
36. DeLeve LD, Valla DC, Garcia-Tsao G. Vascular disorders of the liver. Hepatology 2009; 49(5): 1729–1764. doi: 10.1002/hep.22772.
37. Kavanagh PM, Roberts J Gibney R et al. Acute Budd-Chiari syndrome with liver failure: the experience of a policy of initial interventional radiological treatment using transjugular intrahepatic portosystemic shunt. J Gastroenterol Hepatol 2004; 19(10): 1135–1139.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek Správná odpověď na kvízČlánek Projekt RISING STARSČlánek MUDr. Boris Pekárek (1978)Článek OznámeníČlánek OmluvaČlánek Kvíz
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2014 Číslo 2- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Léčba portální hypertenze pomocí transjugulární intrahepatální portosystémové spojky – prvních 1 000 výkonů ve FN Hradec Králové
- 1 000 TIPS ve FN Hradec Králové: indikace a přežívání nemocných
- Budd-Chiari syndrom a TIPS – 21 let zkušeností
- Transjugulární intrahepatální portosytémová spojka v terapii refrakterního ascitu: současný pohled jednoho pracoviště
- Dispenzarizace nemocných po zavedení transjugulární intrahepatální portosystémové spojky – diagnostika dysfunkce zkratu a možnosti intervence
- Transplantace jater pro hepatocelulární karcinom, dlouhodobé přežití a faktory ovlivňující rekurenci tumoru (zkušenosti jednoho centra)
- Využití EUS navigované choledochoduodenostomie v léčbě biliární obstrukce
- Hereditárny angioedém ako príčina bolestí brucha
- Malígny melanóm konečníka – zriedkavá kazuistika a prehľad literatúry
- Moderní diagnostika Lynchova syndromu
- Správná odpověď na kvíz
- Diskusia k príspevku „Moderní diagnostika Lynchova syndromu“
- Projekt RISING STARS
- doc. MUDr. Jan Martínek, Ph.D., AGAF (1969)
- MUDr. Ondřej Ryska, Ph.D. (1981)
- MUDr. Sylvia Dražilová (1972)
- MUDr. Boris Pekárek (1978)
- EUS workshop v Jablonci nad Nisou
- 13th Czech-Slovak IBD symposium
- 9th Congress of ECCO, Copenhagen, Denmark
- Oznámení
- Omluva
- Nový člen výkonné redakční rady
- Remsima™ – první biosimilární infliximab
- Autodidaktický test: hepatologie
- Hepatologie nejen z Hradce Králové
- Kvíz
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- doc. MUDr. Jan Martínek, Ph.D., AGAF (1969)
- MUDr. Sylvia Dražilová (1972)
- MUDr. Ondřej Ryska, Ph.D. (1981)
- Budd-Chiari syndrom a TIPS – 21 let zkušeností
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



