-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
INTRAKAVERNÓZNÍ VAZOAKTIVNÍ LÉČBA EREKTILNÍ DYSFUNKCE
INTRACAVERNOUS VASOACTIVE THERAPY OF ERECTILE DYSFUNCTION
Erectile dysfunction (ED) is, with an incidence rate of 10%, the most common sexual dysfunction in male adult populations. The intracavernous application of vasoactive agents has been used in treating ED for more than 20 years. This method is based on "self-injecting" vasoactive agents into the corpora carvernosa. The dosage is strictly individual and alprostadil is the most frequently used drug. This treatment gives two great advantages - high efficacy and erection without sexual stimulation, and disadvantages - discomfort associated with therapy and above all the risk of prolonged erection. This treatment is safe and adheres to the rules; however, it is necessary to follow up the patient with an urologist.
KEY WORDS:
erectile dysfunction, intracavernous therapy, prostaglandin E1
Autoři: MUDr. Jiří Heráček 1,2; doc. MUDr. Michael Urban 1,2; MUDr. Martin Lukeš 1; Doc. MUDr. Roman Zachoval, Ph.D.; MUDr. Miroslav Záleský 1 1; MUDr. Lukáš Bittner 1
Působiště autorů: Urologická klinika 3. LF UK a FNKV, Praha 1; Androgeos - soukromé urologické a andrologické centrum, Praha 2
Vyšlo v časopise: Urol List 2006; 4(1): 49-52
Souhrn
Erektilní dysfunkce (ED) je s incidencí 10 % nejčastější sexuální dysfunkcí v dospělé mužské populaci. Intrakavernózní aplikace vazoaktivních látek se užívá v léčbě ED již více než 20 let. Metoda spočívá v autoaplikaci vazoaktivní látky do kavernózního tělesa. Dávkování je přísně individuální, nejčastěji používané léčivo je alprostadil. Výhodou je vysoká účinnost léčby a vznik erekce bez nutnosti sexuální stimulace, nevýhodou pak diskomfort spojený s aplikací a především riziko prolongované erekce. Léčba je při dodržení pravidel bezpečná, dispenzarizace urologem je nutná.
KLÍČOVÁ SLOVA:
erektilní dysfunkce, intrakavernózní léčba, prostaglandin E1ÚVOD
Erektilní dysfunkce (ED) je minimálně 6 měsíců trvající neschopnost dosáhnout a/nebo udržet dostatečnou erekci pro uspokojivou sexuální aktivitu [1].
S incidencí 10 % je ED nejčastější sexuální dysfunkcí v dospělé mužské populaci, avšak pouze každý desátý postižený muž vyhledá pomoc lékaře. Nejčastěji citovaná Massachusetts Male Aging Study udává prevalenci různého stupně ED u 52 % mužů mezi 40 až 70 lety [2]. V průzkumu sexuálního chování reprezentativního vzorku české populace 19 % mužů uvedlo, že někdy v životě trpěli sexuální poruchou a 15 % mužů, že mají sexuální problémy aktuálně [3].
HISTORIE
Intrakavernózní aplikace vazoaktivních látek se užívá v léčbě ED již déle než 20 let.
Léčbu popularizovali v letech 1982 až 1983 francouzský cévní chirurg Virag a britský fyziolog Brindley, kteří prokázali, že intrakavernózní injekce papaverinu, fentolaminu a fenoxybenzaminu způsobuje erekci penisu [4]. Brindley doložil účinek papaverinu originálním způsobem na konferenci Americké urologické společnosti v Las Vegas v roce 1983. Na konci své přednášky si rozepnul kalhoty a ukázal auditoriu ztopořený penis po autoaplikaci papaverinu. V roce 1984 Virag navrhl léčebný protokol „intrakavernózních perfuzí papaverinem“ a představil „papaverinový test“ k vyhodnocení stupně ED. Je však třeba poznamenat, že reakci kavernózních těles po aplikaci papaverinu publikoval český cévní chirurg Vladimír Michal již v roce 1978 [5].
V roce 1985 popsal Zorgniotti užití kombinace papaverinu a fentolaminu v léčbě ED.
Intraarteriální aplikace prostaglandinu E1 (PGE1) se ve světě používala k léčbě periferních arteriálních okluzivních onemocnění a k prevenci amputací již od roku 1973. V Evropě byl PGE1 schválen v roce 1984 pro léčbu periferních arteriálních okluzivních onemocnění dolních končetin a v roce 1986 Ishii navrhl diagnostické a léčebné využití PGE1 v léčbě ED [6].
POUŽÍVANÁ LÉČIVA
Papaverin hydrochlorid je spazmolytikum, přirozený alkaloid opia. Patří mezi muskulotropní spazmolytika, inhibuje účinek a způsobuje zvýšenou koncentraci cAMP (cyklického adenozinmonofosfátu). Dilatuje hladké svalstvo cév, a tím přispívá ke zvýšení průtoku krve v orgánech. Papaverin způsobuje dilataci arterií, kavernózních sinusoid i vén penisu.
Fentolamin mesylát je alfa-sympatolytikum, kompetitivní inhibitor alfa-adrenergních receptorů se silným vazodilatačním účinkem. Intrakavernózní aplikace dilatuje arteriální řečiště penisu, neovlivňuje však jeho venózní systém.
Kombinace papaverinu a fentolaminu byla popsána v roce 1985 Zorgniottim a Lefleurem (30 mg papaverinu/1 mg fentolaminu v 1 ml). Papaverin používáme v dávkách 30–160 mg, fentolamin můžeme přidávat v dávce 0,1–1 mg [7], Verner et al uvádějí dávky 30 a 60 mg papaverinu, eventuálně v kombinaci s 0,5 mg fentolaminu [8], v Evropě je dostupný komerčně vyráběný Androskat® (30 mg papaverinu a 0,5 mg fentolaminu v 1 ml roztoku).
Alprostadil, synteticky připravený prostaglandin E1 s vazodilatačními a hemoreologickými účinky se v současné době používá takřka výlučně.
Farmakologický účinek intrakavernózně podaného alprostadilu spočívá ve zprostředkování inhibice v klidu převládající alfa1-adrenergní aktivity ve tkáni penisu (vazokonstrikce) a v jeho relaxačním účinku na hladkou svalovinu trámčiny kavernózních těles s následným zvýšením přítoku krve, plněním relaxovaných kavernózních lakun, a tím vytvoření podmínek pro uplatnění venookluzivního mechanizmu na úrovni odvodných cév. PGE1 v endotelu arteriol i lakun kavernózních těles aktivuje enzym adenylátcyklázu, který štěpí adenozintrifosfát na cyklický adenozinmonofosfát, otevírá tak následně kalciové kanály a způsobuje pokles intracelulární koncentrace vápenatých iontů s hyperpolarizací buněčných membrán hladkého svalstva a s relaxací buněk kavernózního a arteriálního hladkého svalstva.
Jako látka tělu vlastní je alprostadil metabolizován již v kavernózní tkáni, jeho průnik do systémového oběhu je za normálních podmínek (tj. při uplatnění venookluzivního mechanizmu) minimální a obtížně detekovatelný. V případě, že alprostadil pronikne do systémového oběhu, je metabolizován z 60–90 % již při prvním průchodu plicním řečištěm. Enzymatickou beta - a omega-oxidací vznikají 15-keto-PGE1, 15-keto-13,14-dihydro-PGE1 a 13,14-dihydro-PGE1. Na rozdíl od 15-keto - -PGE1 a 15-keto-13,14-dihydro-PGE1, které jsou téměř bez biologické aktivity, 13,14--dihydro-PGE1 snižuje krevní tlak a inhibuje agregaci destiček. U zdravého muže je 70–90 % alprostadilu rychle vyloučeno a metabolizováno při prvním průchodu plícemi s výsledným poločasem kratším než 1 minuta.
V roce 1990 byla Goldsteinem navržena kombinace PGE1, papaverinu a fentolaminu. Kombinace poskytují 2 velké výhody - nižší dávky jednotlivých léčiv, a tím i nižší finanční náklady na léčbu a vyšší účinek „trojité drogy“ ve srovnání s aplikací samotného PGE1 [9]. Bi-mix roztok obsahuje kombinaci s fentolaminem (20 µg alprostadilu a 0,5 mg fentolaminu v 1 ml), tri-mix navíc s papaverinem (10 µg alprostadilu, 30 mg papaverinu a 1 mg fentolaminu v 1 ml).
KLINICKÉ POUŽITÍ
Pacienta musíme před zahájením terapie pečlivě poučit, vysvětlit mu charakteristiku, potenciální omezení a vedlejší účinky léčby. Z právního hlediska je nutný písemný informovaný souhlas pacienta s léčbou a jeho poučení, že musí kontaktovat lékaře při erekci trvající déle než 4 hodiny. Součástí informovaného souhlasu jsou též informace o uskladnění preparátu a likvidaci použitého zdravotnického materiálu.
Dávkování je přísně individuální, doporučená zahajovací dávka je 2,5 µg, terapeutická dávka většinou 10–20 µg, maximální 60 µg v jedné injekci. U pacientů s kardiovaskulárními rizikovými faktory podáváme dávky vyšší než 20 µg s určitou opatrností (tab). Šetrná titrace a nízké iniciální dávky (1–5 µg) jsou nutné také u mužů s neurogenními příčinami ED (transverzální léze míšní, roztroušená skleróza) vzhledem k jejich výrazné hypersenzitivitě. Přípravek se používá maximálně 1krát denně, avšak ne častěji než 3krát týdně.
Tab. 1. Riziko kardiálních komplikací a léčba sexuálních dysfunkcí u pacientů s kardiovaskulárními onemocněními 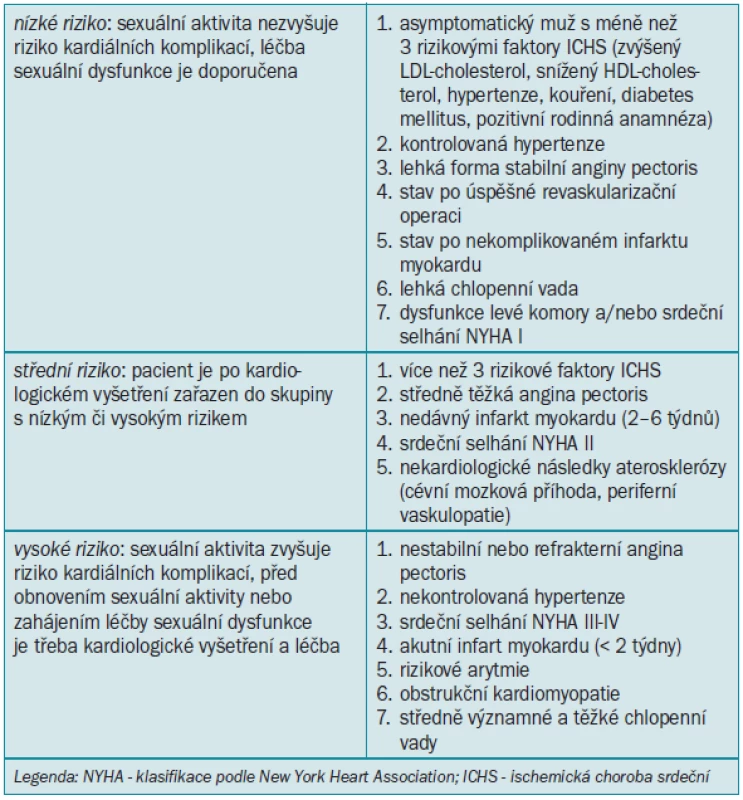
Intrakavernózní aplikace PGE1 vyvolá u mužů s funkčním cévním řečištěm během 5–15 minut erekci bez nutnosti sexuální stimulace. Erekce trvá podle použité dávky a citlivosti pacienta desítky minut až hodiny, cílem je dosáhnout trvání erekce po dobu 20–60 minut. Maximální doba bezpečné erekce jsou 3 hodiny.
Metoda spočívá v autoaplikaci vazoaktivní látky do jednoho z kavernózních těles. Po dezinfekci laterální strany penisu aplikujeme inzulínovou stříkačkou (jehla 29G) nebo autoinjektorem léčivo tak, aby špička jehly dosáhla do střední části kavernózního tělesa (obr. 1a,b). Injekci nepodáváme na dorzální nebo ventrální straně penisu, abychom zamezili poškození neurovaskulárního svazku nebo uretry. Montorsi et al doporučují pro dobré vstřebání léku tření báze penisu mezi pravým palcem a ukazovákem okamžitě po aplikaci injekce, zatímco volnou část penisu masíruje pacient až 5 minut na laterální straně po celé jeho délce mezi levým palcem, ukazovákem a prostředníkem [10].
Obr. 1a,b. Intrakavernózní autoaplikace vazoaktivní látky. 
Erektilní odpověď zhodnotí pacient i lékař. Terapeutická dávka způsobí 50–75 % maximální erekce uváděné pacientem. Pokud pacient dosáhne maximální rigidní erekce v průběhu titrační fáze, v domácím prostředí aplikuje dávky o 1/3 nižší. Současná sexuální stimulace potencuje účinek léčiva. Jestliže první injekce nezpůsobí uspokojivou erektilní odpověď, aplikujeme další injekci nejméně po 24 hodinách a dávku zvyšujeme zpravidla o 5–10 µg PGE1. Takto stanovíme pro každého pacienta optimální dávku i objem injikovaného léčiva. Pacienty kontrolujeme 1krát měsíčně v prvních 2 měsících léčby, poté každé 3 měsíce. Zaznamenáváme frekvence aplikací, trvání a charakter erekcí a spokojenost pacienta s léčbou. Penis vyšetřujeme na přítomnost uzlů, hematomů nebo indurací.
Autoinjekčním perem můžeme podávat dávky léčiva opakovaně a vyvarujeme se tak nekomfortní přípravy každé injekce pomocí inzulinové stříkačky. Relativní nevýhodou je vyšší pořizovací cena pera (800 Kč, nehradí pojišovna, např. Autoject2 firmy Owen Mumdorf) oproti inzulinové stříkačce (2 Kč).
Lék je dostupný po naředění v dávce 100 µg (Karon® Zentiva, 680 Kč) nebo v dávkách 10 či 20 µg (Caverject® Pfizer, 260, resp. 440 Kč). Roztok léčiva uchováváme po naředění v chladničce při teplotě 1–5° C, jeho použití je vhodné maximálně 4 týdny po naředění. Po uplynutí této doby postupně ztrácí svou účinnost. Před aplikací vždy zkontrolujeme, zda roztok nezměnil barvu nebo zda se v něm nevytvořil precipitát.
Kontraindikacemi léčby jsou těžší hemoragické diatézy, M. Peyronie, náchylnost k priapizmu (např. srpkovitá anémie, mnohočetný myelom, leukemie), idiopatický priapizmus, kardiopulmonální dekompenzace, závaznější psychiatrické onemocnění, ale i nespolupráce pacienta, jeho nedostatečná zručnost, slabozrakost nebo výrazná obezita.
Podle velikosti dávky a reaktivity pacienta může dojít k systémové vazodilataci, která se může projevovat zarudnutím, pocením, návaly horka, slabostí, tachykardií, poklesem krevního tlaku až závratí.
Dlouhodobý účinek PGE1 na kavernózní tkáň
Je běžné, že v průběhu intrakavernózní léčby se frekvence spontánních erekcí zvyšuje.
PGE1 vykazuje při dlouhodobém intrakavernózním podávání významný pozitivní vliv na arteriální cirkulaci a funkci kavernózních těles. Lue a Porst prokázali duplexní sonografií, že průsvit arterií a průtok krve v hlubokých kavernózních arteriích se u pacientů s arteriální okluzivní nemocí výrazně zvýšil po opakované intrakavernózní aplikaci PGE1. Je pravděpodobné, že mechanizmus, kterým lék účinkuje na periferní arteriální onemocnění, zlepšuje i průtok krve penisem. Papaverin i PGE1 způsobují hypertrofii kavernózní svaloviny, papaverin nadto také atrofii, fibrózu a změnu uspořádání kavernózní svaloviny. PGE1 přímo relaxuje buňky hladkého svalstva cév a kavernózních těles, „tonizuje“ sinusoidální svalovinu, stimuluje neovaskularizaci, inhibuje agregaci krevních destiček, snižuje propustnost lipoproteinů do stěn cév, snižuje presynaptické uvolňování noradrenalinu, a zabraňuje tak progresi aterosklerózy.
Moreland et al prokázali, že PGE1 potlačuje indukci kolagenové syntézy ovlivněním transformačního růstového faktoru beta 1 (Transforming Growth Factor ß1 - TGFß1) v buňkách hladkého svalstva kavernózních těles u člověka. Syntézu kolagenu pozorovali na primárních kulturách těchto buněk, které tvoří mRNA pro TGFß1 - hlavní regulátor syntézy extracelulární matrix. Buňky indukovaly za přítomnosti exogenních TGFß1 2,5-4,5krát vyšší nárůst syntézy kolagenu typu I a III, zatímco společně s PGE1 a s TGFß1 snižovaly indukci syntézy kolagenu typu I, III a V/XI. Prostaglandiny a TGFß1 mají klíčovou úlohu v ovlivnění syntézy kolagenu v kavernózních tělesech, a tím v regulaci fibrózy kavernózních těles [11].
VÝSLEDKY
Od roku 1983 byla účinnost a bezpečnost intrakavernózní aplikace vazoaktivních látek ověřena na více než 5 000 pacientech.
Monoterapie alprostadilem je účinná u 70 % pacientů, kombinovaná léčba je pak úspěšná u 90 % mužů s ED [12]. V evropské multicentrické studii trvající 4 roky vyhodnotili Porst et al výsledky intrakavernózní léčby alprostadilem u 162 pacientů s ED. Z celkového počtu 16 886 aplikovaných injekcí jich 93 % vedlo k erekci dostatečné k pohlavnímu styku. Prolongovaná erekce delší než 6 hodin nastala u 2 (1,2 %) pacientů, bolestivá erekce u 29 % (47) pacientů v 1. roce léčby s následným poklesem na 12 % ve 4. roce léčby, hematomy u 33 % (54) pacientů v 1. roce s poklesem na 12,1 % ve 4. roce léčby, uzly, plaky nebo deviace penisu u 19 (11,7 %) se spontánním odezněním u 9 pacientů. 4 roky léčby dokončilo však pouze 54 (33 %) pacientů (13). Shabsigh et al zkoumali 67 pacientů, kteří nereagovali na léčbu sildenafilem v dávce 50–100 mg. Pacienti prošli ambulantní titrací a následnou 6týdenní léčbou alprostadilem v domácím prostředí. Zlepšení odpovědí na otázky č. 3 a 4 IIEF bylo 90%, resp. 85%. Nejčastějším nežádoucím účinkem byla penilní bolest u 25 (29,4 %) pacientů [14]. Heráček et al vyhodnotili 2 protokoly léčby alprostadilem u 27 pacientů po radikální prostatektomii. Předoperační aplikace PGE1 a pooperační včasné zahájení léčby ED vedly ke zlepšení celkové erektilní funkce, výraznému snížení průměrné dávky dostačující k dosažení pohlavního styku a vyšší spokojenosti s léčbou [15].
Nevýhodou léčby je diskomfort spojený s autoaplikací a nutnost plánování sexuální aktivity. Možná i proto upustí do 2 let od této formy léčby přibližně 55 % pacientů [16]. Nejčastější důvody k ukončení léčby jsou snížená sexuální apetence, finanční náklady léčby, diskomfort spojený s aplikací a nezájem sexuální partnerky.
NEŽÁDOUCÍ ÚČINKY
Nejčastější nežádoucí účinky léčby jsou hematomy v místě vpichu (3–5 % pacientů), palčivá bolest po injekci (10–20 %), poškození uretry, fibrotické změny kavernózních těles, angulace penisu a prolongovaná erekce až priapizmus. Klinicky nejzávažnější komplikace jsou fibrotické změny kavernózních těles a prolongovaná erekce.
Nežádoucí účinky při monoterapii papaverinem mohou být kromě priapizmu nebo infiltrátu v tunica albuginea v místech vpichu také arytmie, tachykardie a hypotenze, méně časté jsou bolesti hlavy, vertigo, somnolence nebo kožní vyrážky.
Fibrotické změny kavernózních těles se vyskytují častěji u pacientů, kteří aplikují injekce velmi často a nekomprimují místo vpichu na dostatečně dlouhou dobu. Vznikají tak opakovaná mikrotraumata kavernózních těles a intrakavernózní hematomy. Výskyt se uvádí u 2–60 % pacientů, méně často při užívání PGE1 (3 %).
Prolongované erekce až priapizmus se vyskytují obvykle v průběhu titrace dávky. Mohou však nastat po úmyslném nebo neúmyslném zvýšení dávky pacientem a také v důsledku pozitivního psychologického účinku léčby nebo zlepšenou „kompliancí“ kavernózních těles. Jejich výskyt je mezi 2–15 %, nejčastěji při monoterapii papaverinem, méně často u PGE1 (2 %).
Již po několika hodinách městnání krve v kavernózních tělesech dochází k hypoxii, hyperkapnii a acidóze. Zvýšení viskozity krve způsobuje edém, a poté nekrózu endotelu s následnou trombotizací trabekul a eventuální fibrózní přestavbou trombu.
Při erekci, která je delší než 4 hodiny, musí pacient kontaktovat lékaře. Intrakavernózní tlak snižujeme aspirací krve z kavernózních těles jehlou 19 gauge. Pokud penis ani poté neochabuje, provádíme intrakavernózní aplikaci adrenalinu v koncentraci 10 µg/ml (1 mg adrenalinu ve 100 ml fyziologického roztoku); 1 ml takto naředěného roztoku adrenalinu aplikujeme intrakavernózně i opakovaně každých 5 minut.
ZÁVĚR
Lékem první volby ED zůstávají inhibitory fosfodiesterázy 5 (phosphodiesteraze 5 - - PDE 5), léčba je jednoduchá a při dodržení kontraindikací bezpečná. Absolutní kontraindikace je léčba nitráty nebo donory NO, jelikož inhibitory PDE 5 potencují jejich vazodilatační, hypotenzivní a antikoagulační účinky. Relativní kontraindikace jsou nestabilní nebo těžká kardiovaskulární onemocnění, zvýšené opatrnosti je třeba u pacientů s poškozením jaterních nebo renálních funkcí a u pacientů nad 65 roků, u nichž je snížena clearance léku.
U mužů, které nemůžeme léčit nebo léčíme bez úspěchu inhibitory PDE 5, používáme miniinvazivní léčbu intrakavernózní aplikací vazoaktivních látek (alprostadil, eventuálně v kombinaci s papaverinem a/nebo s fentolaminem). Výhodou je vysoká účinnost léčby a vznik erekce bez nutnosti sexuální stimulace, nevýhodou pak diskomfort spojený s aplikací a především riziko prolongované erekce. Léčba je při dodržení pravidel bezpečná, dispenzarizace urologem je nutná. Preskripce léčiv není omezena odborností a běžně není hrazena zdravotními pojišovnami.
MUDr. Jiří Heráček1,2
doc. MUDr. Michael Urban1,2
MUDr. Martin Lukeš1
doc. MUDr. Roman Zachoval, Ph.D.1
MUDr. Miroslav Záleský1
MUDr. Lukáš Bittner1
1Urologická klinika 3. LF UK a FNKV, Praha
2Androgeos - soukromé urologické a andrologické centrum, Praha
Zdroje
1. NIH Consensus Development Panel on Impotence. (NIH Consensus Conference. Impotence). JAMA 1993; 270 : 83-90.
2. Feldman HA, Goldstein I, Hatzichristou DG et al. Impotence and its medical and psychosocial correlates: Results of the Massachusetts Male Aging Study. J Urol 1994; 151 : 54-61.
3. Weiss P, Zvěřina J. Sexuální chování v ČR - situace a trendy. Praha: Portál 2001; 159.
4. Virag R. Intracavernous injection of papaverine for erectile dysfunction. Letter to the editor. Lancet 1982; 2 : 938.
5. Michal V, Pospíchal J. Phalloarteriography in the diagnosis of erectile impotence. World J Surg 1978; 2(2): 239-248.
6. Ishii Watanabe H, Irisawa C et al. Studies on male sexual impotence. Report 18. Therapeutic trial with prostaglandin E1 for organic impotence. Nippon Hinyokika Gakkai Kasshi 1986; 77 : 954-962.
7. Breza J. Erektilné poruchy. Martin: Osveta 1994.
8. Verner P, Zvěřina J, Kočí K. Intrakavernózní aplikace papaverinu a fentolaminu u pacientů s poruchami erekce. Prakt Lek 1988; 68 : 807-810.
9. Goldstein I, Borges FD, Fitch WP et al. Rescuing the failed papaverine/phentolamine erection: a proposed synergistic action of papaverine, phentolamine and prostaglandin E1 J Urol 1990; 143 : 304A (Abstrakt). 10. Montorsi F, Salonia A, Deho' F et al. Pharmacological management of erectile dysfunction. BJU Int 2003; 91 : 446-454.
11. Moreland RB, Traish A, McMillin MA et al. PGE1 suppresses the induction of new collagen synthesis by transforming growth factor beta-1 in human corpus cavernosum smooth muscle: mechanism of penile ischemia associated fibrosis. J Urol 1994; 151 : 431A (Abstrakt).
12. Barada JH, McKimmy RM. Vasoactive pharmacotherapy. Philadelphia: WB Saunders 1994 : 229-250.
13. Porst H, Buvat J, Meuleman E et al. Intracavernous Alprostadil Alfadex - an effective and well tolerated treatment for erectile dysfunction. Results of a long-term European study. Int J Impot Res 1998; 10(4): 225-231.
14. Shabsigh R, Padma-Nathan H, Gittleman M et al. Intracavernous alprostadil Alfadex (Edex/Viridal) is effective and safe in patients with erectile dysfunction after failing sildenafil (Viagra). Urology 2000; 55 : 477-480.
15. Heráček J, Lukeš M, Kuncová J et al. Intrakavernózní aplikace prostaglandinu E1 v léčbě erektilní dysfunkce po radikální prostatektomii. Čes Urol 2002; 2 : 6 (Abstrakt).
16. Purvis K, Egdetveit I, Christiansen E. Intracavernosal therapy for erectile failure - impact of treatment and reasons for drop-out and dissatisfaction. Int J Impot Res 1999; 295 : 287-299.
Štítky
Dětská urologie Urologie
Článek vyšel v časopiseUrologické listy
Nejčtenější tento týden
2006 Číslo 1- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Nostiriazyn – spolehlivá 1. volba u nekomplikovaných infekcí močových cest
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
- Prevence opakovaných infekcí močových cest s využitím přípravku Uro-Vaxom
- Vysoká hladina PSA a její rychlý nárůst jsou nepříznivými prognostickými faktory u karcinomu prostaty
-
Všechny články tohoto čísla
- HYPOGONADIZMUS OČIMA ČESKÉHO PRAKTICKÉHO LÉKAŘE: VÝCHODISKA (NEJEN) PRO UROLOGY
- ÚLOHA UROLOGA V IVF-PROGRAMU PŘI DIAGNOSTICE A LÉČBĚ NEPLODNÉHO PÁRU
- ANDROGENNÍ DEFICIT U STÁRNOUCÍCH MUŽŮ
- VASKULÁRNÍ RIZIKOVÉ FAKTORY U EREKTILNÍ DYSFUNKCE
- TRANSSEXUALIZMUS A CHIRURGICKÁ KONVERZE POHLAVÍ
- Editorial
- MÍSTO MEDIKAMENTÓZNÍ TERAPIE V LÉČBĚ KOMPLIKOVANÉ EREKTILNÍ DYSFUNKCE
- INTRAKAVERNÓZNÍ VAZOAKTIVNÍ LÉČBA EREKTILNÍ DYSFUNKCE
- PRIAPIZMUS
- INDURATIO PENIS PLASTICA: PEYRONIEOVA CHOROBA
- MUŽSKÝ FAKTOR INFERTILITY: VYŠETŘENÍ A LÉČBA
- ZE ZAHRANIČNÍCH PERIODIK
- PRVNÍ MEZINÁRODNÍ ANDROLOGICKÝ KONGRES V ČESKÉ REPUBLICE
- ABSTRAKTA
- WEBOVÁ STRÁNKA ČESKÉ UROLOGICKÉ SPOLEČNOSTI - HISTORIE A SOUČASNOST
- KVÍZ
- Urologické listy
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- INTRAKAVERNÓZNÍ VAZOAKTIVNÍ LÉČBA EREKTILNÍ DYSFUNKCE
- INDURATIO PENIS PLASTICA: PEYRONIEOVA CHOROBA
- TRANSSEXUALIZMUS A CHIRURGICKÁ KONVERZE POHLAVÍ
- MUŽSKÝ FAKTOR INFERTILITY: VYŠETŘENÍ A LÉČBA
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




