-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Inhibitory SGLT2 v léčbě diabetu 2. typu GLIFLOZINY a jeho komplikací
Autoři: prof. MUDr. Karásek David, Ph.D.
Působiště autorů: III. interní klinika – nefrologická, revmatologická a endokrinologická LF UP a FN Olomouc
Vyšlo v časopise: Svět praktické medicíny, 1, 2020, č. 3-4, s. 41-47
Kategorie: Medicína v ČR: přehledový článek
Souhrn
Inhibitory SGLT2 patří mezi relativně nová antidiabetika s prokázaným příznivým ovlivněním srdečního selhání, chronického onemocnění ledvin a hlavních kardiovaskulárních příhod. Původně byly určeny pro léčbu diabetu 2. typu, nyní některá data svědčí o možné prospěšnosti jejich podávání i u nediabetické populace. Sdělení obsahuje aktuální informace o současném postavení gliflozinů v léčbě diabetu 2. typu a jeho komplikací.
Inhibitory sodíko-glukózového kotransportéru typu 2 (inhibitory SGLT2, tzn. glifloziny) patří mezi relativně nová antidiabetika. V Evropě bylo jako první schváleno užívání dapagliflozinu koncem roku 2012 a v USA byl první uveden na trh kanagliflozin během roku 2013.1 V současné době máme k dispozici dapagliflozin, empagliflozin, kanagliflozin a ertugliflozin pro léčbu diabetu 2. typu. Navíc dapagliflozin a toho času na trhu nedostupný společný inhibitor SGLT2 i SGLT1 – sotagliflozin byly v Evropě schváleny i pro adjuvantní léčbu diabetu 1. typu. Hypoglykemický účinek gliflozinů spočívá v navození glykosurie, která je provázena osmotickou diurézou a poklesem glykemie. Monoterapie glifloziny je spojena se snížením glykovaného hemoglobinu (HbA1C podle DCCT) o 0,66 až 1,16 %, podle dávky a konkrétního preparátu.2 Ve srovnání s léčbou samotným metforminem vedou kombinace inhibitor SGLT2 + metformin k dalšímu poklesu HbA1C průměrně o 0,50–0,55 %.3, 4 Do popředí terapeutických algoritmů pro léčbu diabetu 2. typu se však tyto léky dostaly především díky příznivému ovlivnění diabetických komplikací, jež je ve většině případů na jejich hypoglykemickém působení nezávislé.
Inhibitory SGLT2 a kardiovaskulární příhody
Dosud byly publikovány čtyři randomizované klinické studie s primárními kardiovaskulárními (KV) endpointy (Tab. 1). Studie EMPA-REG OUTCOME s empagliflozinem, která zařadila jen diabetiky 2. typu v sekundární prevenci,5 a studie CANVAS s kanagliflozinem,6 kde nemocní s přítomným KV onemocněním také dominovali (asi dvě třetiny účastníků), dokumentovaly signifikantní pokles tří hlavních nežádoucích KV příhod (MACE) – KV úmrtí, nefatálních infarktů myokardu (IM) a cévních mozkových příhod (CMP). V klinickém hodnocení DECLARE-TIMI 58 s dapagliflozinem,7 kde naopak dominovali rizikoví nemocní v primární prevenci (tvořili asi 60 % nemocných), k významné redukci MACE však nedošlo. Metaanalýza, která zahrnula jedince z výše uvedených studií, potvrdila, že inhibitory SGLT2 u diabetiků 2. typu s již přítomným KV onemocněním vedou k signifikantnímu poklesu MACE (o 14 %).8 Naopak u nemocných, kteří byli dosud bez anamnézy KV onemocnění, k signifikantnímu poklesu MACE nedošlo. Vzhledem k tomu, že v nedávno publikované studii REWIND s agonistou receptoru pro glukagon-like peptid-1 (GLP-1) dulaglutidem, která zahrnula velmi podobnou populaci pacientů jako studie DECLARE-TIMI 58 (69 % jedinců bylo bez diagnostikovaného KV onemocnění) a trvala podobně dlouho, signifikantní pokles MACE (o 12 %) zaznamenán byl,9 změnil se částečně pohled na preferenci těchto dvou skupin léků u rizikových diabetiků. Recentní update doporučení ADA/EASD pro léčbu diabetu 2. typu preferuje u nemocných s dominujícím aterosklerotickým onemocněním a také u vysoce rizikových jedinců v primární prevenci GLP-1 agonisty před inhibitory SGLT2, zatímco gliflozinům by měla být dána přednost u pacientů se srdečním selháním a chronickým onemocněním ledvin.10
Tab. 1. Studie s inhibitory SGLT2 zaměřené primárně na hlavní kardiovaskulární příhody 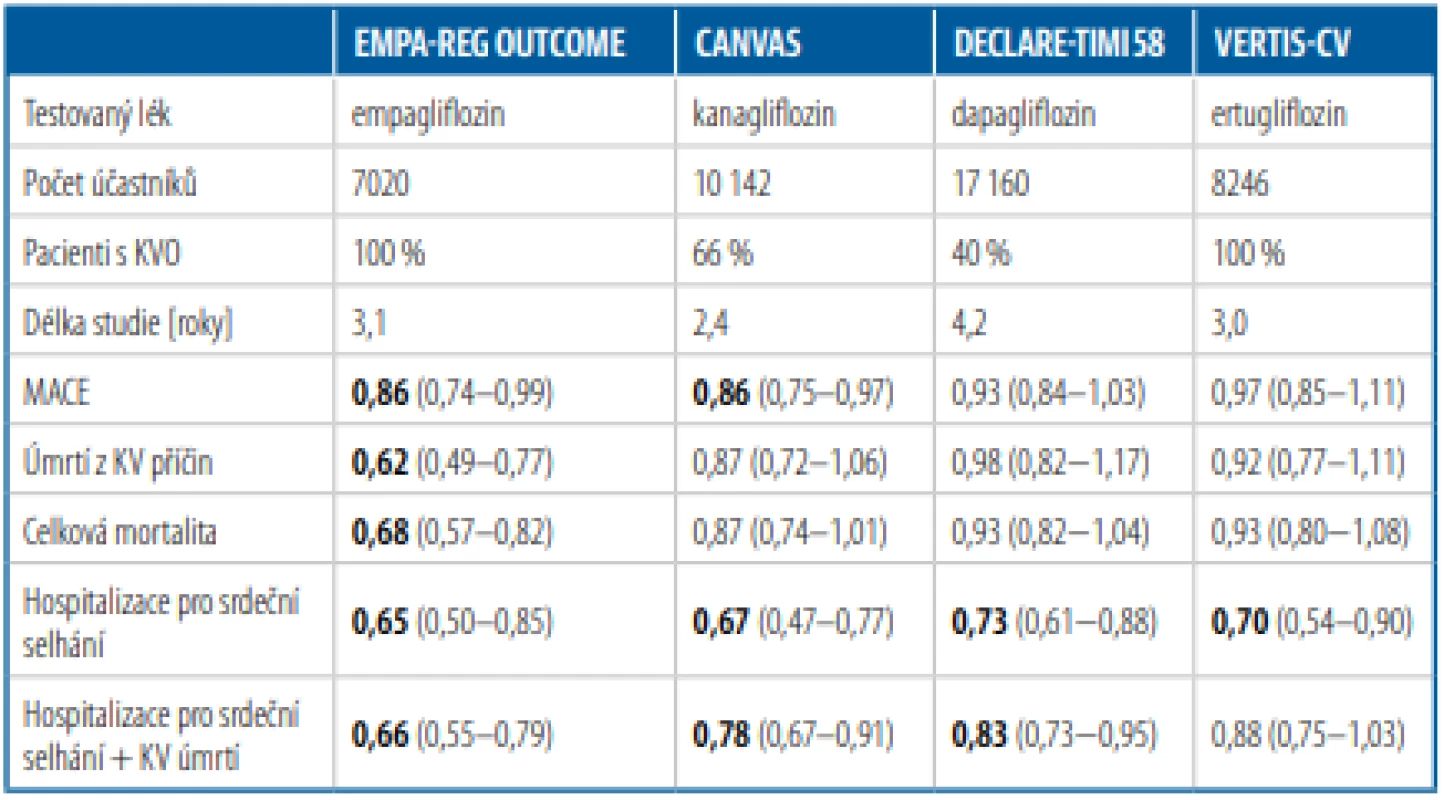
Rozdíl mezi aktivně léčenou a placebovou skupinou v testovaném znaku je vyjádřen relativním rizikem a konfidenčním intervalem, v případě statisticky významného rozdílu je hodnota relativního rizika uvedena tučně. Studie měly rozdílné populace, design a nelze je přímo srovnávat.
KVO – kardiovaskulární (KV) onemocnění, MACE – úmrtí z KV příčin, nefatální IM a CMP dohromady, IM – infarkt myokardu, CMP – cévní mozková příhodaU inhibitorů SGLT2 se nedá předpokládat primární ovlivnění aterosklerotického procesu. Mohou jistě mít vliv na aterosklerózu nepřímo tím, že redukují některé její rizikové faktory – hypertenzi, hyperglykemii, viscerální obezitu, hyperurikemii, renální insuficienci a další patogenetické mechanismy.11 Nicméně časný pokles KV mortality patrný především ve studii EMPA-REG OUTCOME,5 zřejmě nelze vysvětlit postupnou regresí aterosklerotických změn. A tak se kromě pozitivního vlivu na metabolismus kardiomyocytů, který se uplatňuje především v prevenci srdečního selhání, spekuluje i o možném jiném, např. antiarytmickém působení inhibitorů SGLT2.12 Diskutuje se jednak o působení nepřímém, pomocí kterého glifloziny zabrání zvýšení tepové frekvence při současném poklesu krevního tlaku, to znamená, že zablokují neurohumorální aktivaci sympatiku. A jednak je zřejmě možné i přímé ovlivnění myokardu prostřednictvím změn koncentrace iontů v jeho buňkách. Experimentálně bylo např. prokázáno, že empagliflozin snižuje koncentraci iontů Na+ a Ca2+ v cytoplazmě a zvyšuje koncentraci Ca2+ v mitochondriích kardiomyocytů.13 Inhibice výměny Na+ zaH+ ionty je spojována s redukcí hypertrofie i fibrózy myokardu při jeho patologické remodelaci a reperfuzním poškození. Bylo též zjištěno, že léčba empagliflozinem redukuje nezávisle na hypoglykemickém účinku heterogenitu komorové depolarizace (disperzitu intervalu QTc ), což by mohlo snižovat riziko závažných komorových arytmií.14 Nabízí se tedy otázka, zda tento účinek nemůže být odpovědný za příznivé ovlivnění KV mortality empagliflozinem. Ten je podle současných doporučení ESC pro léčbu diabetu a KV chorob zatím jako jediný ze skupiny inhibitorů SGLT2 určen také k prevenci KV úmrtí.15 Podle publikovaných výsledků studie VERTIS-CV, která zahrnula velmi podobnou populaci jako studie EMPA-REG OUTCOME (pouze nemocní v sekundární prevenci), nebyl prokázán přínos ertugliflozinu na redukci MACE. Byla zjištěna jen jeho non-inferiorita ve srovnání s placebem.16 Zdá se tedy, že na rozdíl od srdečního selhání není vliv všech gliflozinů na výskyt hlavních KV příhod stejný a že různé výsledky KV studií není možné vysvětlit pouze odlišným zastoupením jedinců v primární či sekundární prevenci.
Inhibitory SGLT2 a srdeční selhání
Glifloziny snižují počet hospitalizací pro srdeční selhání a většinou také kompozitní endpoint složený z hospitalizací pro srdeční selhání a KV mortality.5, 6, 7 To prokázaly jak jednotlivé randomizované KV klinické studie s empagliflozinem, kanagliflozinem i dapagliflozinem (Tab. 1), tak i metaanalýzy studií s těmito léky.8, 17 K významnému poklesu hospitalizací pro srdeční selhání a KV mortality došlo u diabetiků s anamnézou i bez anamnézy KV onemocnění či srdečního selhání.17 I výsledky studie VERTIS-CV potvrdily pozitivní účinek ertugliflozinu na snížení hospitalizací pro srdeční selhání (viz Tab. 1). 16 Dá se tedy říct, že tento efekt je společný pro celou třídu gliflozinů, které v něm předčí GLP-1 agonisty.8 Proto je současná doporučení preferují před GLP-1 agonisty u nemocných se srdečním selháním, zvláště u nemocných se sníženou ejekční frakcí (< 45 %).10
Existuje řada mechanismů, prostřednictvím kterých se inhibitory SGLT2 mohou uplatnit v léčbě srdečního selhání.1, 2 Zvýšená natriuréza a glykosurie působí diureticky, což je spojeno s poklesem cévního volumu a preloadu. Snížení tuhosti cévní stěny provází pokles krevního tlaku a afterloadu. Snížený preload i afterload vedou k redukci napětí stěny levé komory, což bylo v některých studiích provázeno i poklesem NT-proBNP (N-terminal pro-brain natriuretic peptide).12, 18, 19 Mimo hemodynamický efekt se předpokládá také příznivý metabolický účinek inhibitorů SGLT2 na buňky myokardu. Dostupnost kyslíku pro srdeční sval je podmíněna nárůstem koncentrace hemoglobinu, na čemž se kromě zvýšené diurézy a hemokoncentrace může podílet také nárůst koncentrace erytropoetinu jako projev nefroprotektivního účinku gliflozinů.19, 20 Zvýšená produkce glukagonu vede prostřednictvím zvýšené lipolýzy ke zvýšené nabídce mastných kyselin, které v játrech podléhají beta-oxidaci za vzniku beta-hydroxybutyrátu. Ten spolu s mastnými kyselinami slouží jako alternativní zdroj energie pro myokard, který je schopen ho využít lépe než glukózu.18, 19 Ketolátky navíc vykazují antioxidační a protizánětlivé působení, což může mít ochranný vliv na rozvoj diabetické kardiomyopatie. Podobný efekt mohou mít i některé adipokiny – zejména adiponektin, jehož zvýšená hladina provází léčbu inhibitory SGLT2 spolu s poklesem hmotnosti a s redukcí viscerální, perivaskulární i epikardiální tukové tkáně.12
Informace dokumentující příznivý vliv gliflozinů na srdeční selhání se zatím opíraly o výsledky KV studií a jejich subanalýzy.1, 2 Proto byla naplánována řada klinických hodnocení, která primárně sledují vliv gliflozinů na různé formy srdečního selhání, a to jak u nemocných s diabetem, tak bez diabetu. Probíhá také řada menších studií, které sledují efekt inhibitorů SGLT2 na kvalitu života nemocných se srdečním selháním, vliv na strukturální a funkční parametry selhávajícího srdce či na různé biomarkery metabolických a energetických změn.
Zatím máme k dispozici výsledky první studie zaměřené primárně na jedince se srdečním selháním DAPA-HF, která testovala efekt dapagliflozinu u nemocných s diabetem 2. typu i bez něj.21 Studie DAPA-HF zařadila 4744 nemocných se srdečním selháním a s dokumentovaným poklesem ejekční frakce levé komory < 40 %, z nichž asi polovina (45 %) měla diabetes. Pacienti měli nastavenou adekvátní léčbu srdečního selhání (> 90 % užívalo inhibitory renin-angiotenzinového systému nebo betablokátory a > 70 % bylo léčeno antagonisty mineralokortikoidních receptorů). Během průměrného sledování zhruba 18 měsíců vedla léčba dapagliflozinem k 26% redukci primárního složeného endpointu, který sestával z KV úmrtí, srdečního selhání a návštěv pro zhoršení srdečního selhání vyžadující intravenózní léčbu diuretikem. Dále byl registrován asi 30% pokles samotných hospitalizací pro srdeční selhání, významné snížení KV mortality (−18 %) i celkové mortality (−17 %). Velmi důležitým zjištěním bylo, že primární endpoint byl dapagliflozinem redukován u diabetiků stejně jako u nediabetiků.21
Recentně byly publikovány výsledky další studie – EMPEROR-reduced, která také testovala efekt empagliflozinu u jedinců se srdečním selháním.22 Ta zařadila 3730 nemocných s NYHA II–IV a poklesem ejekční frakce levé komory < 40 %, a to bez ohledu na přítomnost diabetu (ten mělo asi 50 % účastníků studie). Při průměrně šestnáctiměsíčním trvání byla ve srovnání s placebem terapie empagliflozinem provázena 25% redukcí hospitalizací pro srdeční selhání a/nebo KV úmrtí (primární cíl studie) a 30% redukcí počtu samotných hospitalizací pro srdeční selhání. Tak efekt empagliflozinu na primární endpoint byl konzistentní bez ohledu na přítomnost diabetu. Nabízí se tak rozšíření indikace SGLT2 inhibitorů jako léků pro srdeční selhání i u nemocných bez diabetu. Netrpělivě se očekávají i výsledky zatím probíhajících hodnocení u nemocných se zachovalou ejekční frakcí levé komory (EMPEROR-preserved, DELIVER). Mimo uvedená randomizovaná klinická hodnocení potvrzují příznivý vliv inhibitorů SGLT2 na srdeční selhání také výsledky řady observačních studií z běžné klinické praxe (EASEL, CVD-REAL, CVD - -REAL 2, CVD-REAL Nordic, OBSERVE 4-D) včetně některých výsledků zatím předběžných (EMPRISE).1, 2 Tyto studie rozšiřují znalosti o jejich působení na mnohem větším okruhu nemocných a ukazují též na reálný dopad léčby gliflozinů i z pohledu některých ekonomických ukazatelů.23
Inhibitory SGLT2 a diabetické onemocnění ledvin
Výsledky již zmíněných KV studií ukázaly i na nefroprotektivní působení gliflozinů u nemocných s diabetem,5, 6, 7 i když každá hodnotila tento účinek pomocí jiných parametrů. Metaanalýza, která zahrnula tyto studie a srovnala efekt inhibitorů SGLT2 vůči agonistům GLP-1 receptorů, zjistila, že pokud se použije kompozitní endpoint, který nebude obsahovat makroalbuminurii, a půjde tedy jen o tzv. „tvrdší“ renální ukazatele – zhoršení glomerulární filtrace (eGFR), progresi do konečného stadia selhání ledvin nebo úmrtí z renálních příčin – budou tyto parametry signifikantně ovlivněny pouze při léčbě inhibitory SGLT2, a to o celých 45 %.8 Glifloziny mají tedy významný nefroprotektivní efekt, který je zřejmě účinnější než působení GLP-1 agonistů.
Příznivý efekt inhibitorů SGLT2 na ledviny je vysvětlován pomocí několika mechanismů (Obr. 1). Za hlavní působení je považováno obnovení tubuloglomerulární zpětné vazby. Natriuréza navozená inhibicí sodíko-glukózového kotransportu v proximálním tubulu ledvin vede v oblasti macula densa nefronu ke zvýšené produkci adenosinu, což způsobí konstrikci aferentní arterioly glomerulu. To je provázeno normalizací glomelurální hemodynamiky, poklesem zvýšeného intraglomerulárního tlaku a omezením patologické hyperfiltrace, která je pro diabetickou nefropatii typická.18, 20, 24 Kromě hemodynamického účinku na glomerulus se zřejmě uplatňuje i prevence tubulárního poškození. Na něm se patrně účastní úprava hyperglykemie, redukce oxidačního stresu a zánětlivého poškození ledvin.20 Z hlediska dlouhodobého působení má pozitivní vliv také snížení krevního tlaku a pokles hmotnosti.18 Další možný mechanismus spočívá v prevenci hypoxického poškození ledvin, ke kterému u diabetiků dochází kvůli zvýšeným energetickým nárokům na reabsorpci glukózy v renálních tubulech. Jejím zablokováním dojde k ochraně tubulárních buněk před energetickým vyčerpáním.24 Navíc mohou inhibitory SGLT2 ovlivnit hypoxii ledvin zvýšenou dodávkou okysličené krve, a to jednak zvýšením koncentrace hemoglobinu (díky vyšší diuréze a zvýšené produkci erytropoetinu)20 a jednak zlepšením prokrvení ledvin. Na tom se může podílet korekce srdečního selhání a také ochrana kapilární mikrocirkulace renálního parenchymu vlivem zvýšené produkce vaskulárních růstových faktorů.24
Obr. 1. Nefroprotektivní efekt inhibitorů SGLT2. [Upraveno podle publikace Barutta F, et al. SGLT2 inhibition to address the unmet needs in diabetic nephropathy. Diabetes Metab Res Rev 2019;35:e3171.] ![Nefroprotektivní efekt inhibitorů SGLT2. [Upraveno podle publikace Barutta F, et al. SGLT2 inhibition to address the unmet needs in diabetic nephropathy.
Diabetes Metab Res Rev 2019;35:e3171.]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/35576e5dfab5c82c99d02b366f5efc78.png)
Z pohledu studia vlivu inhibitorů SGLT2 na renální ukazatele mají uvedené KV studie obdobné metodologické nedostatky jako v případě posouzení jejich účinku na srdeční selhání. Proto byla naplánována další klinická hodnocení, která primárně sledují efekt gliflozinů u jedinců s chronickým onemocněním ledvin (Tab. 2). Zatím byla publikována data ze studie CREDENCE25 a recentně také ze studie DAPA-CKD26. CREDENCE zařadila 4401 diabetiků 2. typu s diabetickým onemocněním ledvin. Asi 50 % z nich mělo vstupně KV onemocnění, zhruba 16 % srdeční selhání a téměř 100 % z nich užívalo inhibitory renin-angiotenzinového systému (RAS). Primární endpoint byl složen z dosažení dvojnásobné hodnoty sérového kreatininu, ekvivalentu konečné fáze renálního onemocnění (ESKD = dialyzační léčba, transplantace, trvalý pokles eGFR < 15 ml/min/1,73 m2 ) anebo úmrtí z renálních či KV příčin. Během asi 2,6letého sledování vedla léčba kanagliflozinem k významné 30% redukci tohoto sledovaného cíle a studie byla z etických důvodů pro jednoznačný průkaz účinnosti předčasně ukončena. Renálně specifický kompozitní endpoint (zdvojnásobení hodnoty kreatininu, ESKD anebo úmrtí z renálních příčin) poklesl v aktivně léčené větvi ve srovnání s placebem o 34 % a samotný výskyt ESKD se snížil o 32 %. Zároveň u léčené populace došlo k významné redukci hlavních KV příhod (o 20 %) a hospitalizací pro srdeční selhání (o 39 %). Na rozdíl od studie CANVAS nebyla léčba kanagliflozinem ve studii CREDENCE provázena zvýšeným rizikem osteoporotických fraktur a rizikem amputací dolních končetin. I přes simultánní podávání inhibitorů RAS nebylo zaznamenáno vyšší riziko hyperkalemie. Studie CREDENCE prokázala relativní bezpečnost podávání gliflozinů i u nemocných se středně závažnou poruchou funkce ledvin – CKD 3 (eGFR 30–60 ml/min/1,73 m2 ), což recentně reflektují také indikace pro zahájení a pokračování léčby kanagliflozinem u nemocných s chronickým onemocněním ledvin.27
Tab. 2. Studie zaměřené na efekt gliflozinů u nemocných s chronickým onemocněním ledvin 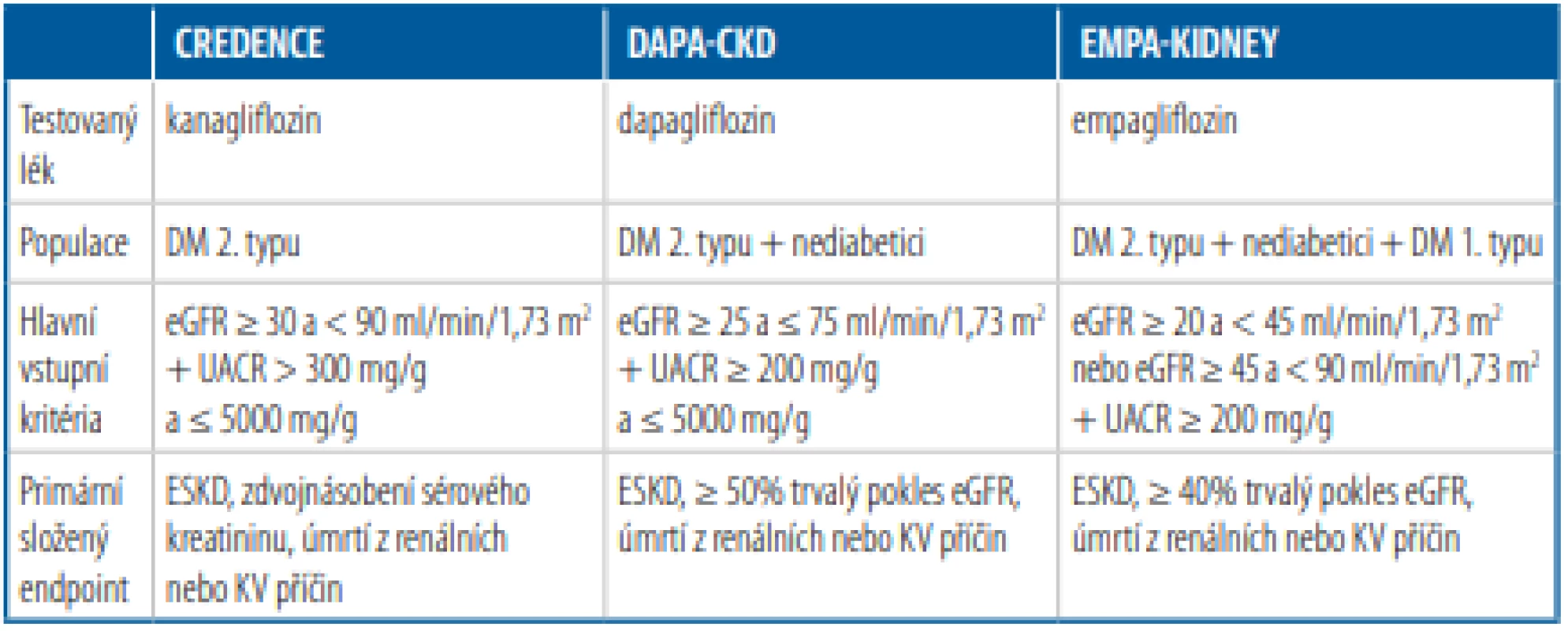
DM – diabetes mellitus, eGFR – odhadovaná glomerulární filtrace, ESKD – end-stage kidney disease (dialyzační léčba, transplantace, trvalý pokles eGFR < 15 ml/min/1,73 m2 ), UACR – urine albumin-to-creatinine ratio, KV – kardiovaskulární Studie DAPA-CKD zahrnula 4304 jedinců s chronickým onemocněním ledvin,26 které bylo šířeji definováno než ve studii CREDENCE, a kromě diabetiků 2. typu (67,5 %) se jí účastnili také nemocní bez diabetu (viz Tab. 2). Ve srovnání s placebem vedla léčba dapagliflozinem během průměrného sledování 2,4 roku k významnému snížení primárního endpointu o 39 %. Ten byl složen z trvalého poklesu eGFR ≥ 50 %, ESKD a/nebo úmrtí z renálních či KV příčin. Došlo také k signifikantnímu poklesu dalšího kompozitního endpointu zahrnujícího úmrtí z KV příčin a hospitalizace pro srdeční selhání (–29 %) a k redukci celkové mortality (–31 %). Stejně tak v této studii nebylo zaznamenáno zvýšené riziko osteoporotických fraktur či amputací dolních končetin. Signifikantní redukce primárního endpointu byla zjištěna bez ohledu na přítomnost diabetu, což opět skýtá potenciál pro využití gliflozinů i u nemocných s CKD bez diabetu. Bude zajímavé sledovat, zda se pozitivní účinky inhibitorů SGLT2 uplatní i u dalších nemocných s CKD ve studii EMPA-KIDNEY, která kromě diabetiků 2. typu a nediabetiků zahrnuje i jedince s diabetem 1. typu (viz Tab. 2).
Výsledky studie CREDENCE a DAPA-CKD jsou ve shodě s aktualizovanými ADA/EASD doporučeními pro léčbu diabetu 2. typu, která preferují inhibitory SGLT2 u jedinců s chronickým onemocněním ledvin (CKD), a to zejména u nemocných s CKD 3 a s albuminurií.10
Současné postavení inhibitorů SGLT2 v léčbě diabetu 2. typu
Již koncem roku 2018 byla publikována nová společná doporučení ADA/EASD pro léčbu diabetu 2. typu, která potvrdila výjimečné postavení inhibitorů SGLT2 a GLP-1 agonistů s prokázaným KV benefitem jako léků druhé volby indikovaných po změně životního stylu a zahájení léčby metforminem u diabetiků v případě aterosklerotického KV onemocnění, srdečního selhání či chronického onemocnění ledvin.28 V roce 2019 doporučení Evropské kardiologické společnosti (ESC) pro léčbu diabetu, prediabetu a KV onemocnění dokonce předřadila tyto léky v terapeutickém algoritmu před terapii metforminem, a to u dosud neléčených diabetiků 2. typu s aterosklerotickým KV onemocněním či u osob ve vysokém nebo velmi vysokém KV riziku.15 Je však nutno podotknout, že to vyvolalo řadu kritických ohlasů, zejména ze strany diabetologů. Jako určitou reakci na ESC guidelines lze vnímat i následný update doporučení ADA/EASD, který byl publikován koncem roku 2019.10 Ten ponechává první místo v léčbě diabetu 2. typu metforminu a částečně diferencuje mezi indikacemi pro inhibitory SGLT2 a agonisty GLP-1 receptorů u pacientů v sekundární prevenci a u vysoce rizikových jedinců (Obr. 2). Je z něj patrné, že glifloziny by měly být preferovány u diabetiků v sekundární prevenci, zejména v případě přítomného srdečního selhání či chronického onemocnění ledvin. Bude zajímavé sledovat, zda se v těchto indikacích uplatní i mimo diabetickou populaci, na což ukázaly výsledky některých recentně publikovaných studií. Glifloziny nadále zůstávají alternativou ostatních antidiabetik (jako lék druhé volby po metforminu) i u dalších nemocných s diabetem 2. typu, hlavně tam, kde klademe důraz na zabránění zvýšení hmotnosti nebo chceme omezit riziko hypoglykemie (Obr. 2). 11
Obr. 2. Algoritmus pro léčbu diabetu 2. typu podle aktualizovaného doporučení ADA/EASD z roku 2019. [Upraveno podle publikace Buse et al. 2019 Update to: Management of hyperglycemia in type 2 diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2020;43:487–493.] ![Algoritmus pro léčbu diabetu 2. typu podle aktualizovaného doporučení ADA/EASD z roku 2019. [Upraveno podle publikace Buse et al. 2019 Update to:
Management of hyperglycemia in type 2 diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the
Study of Diabetes (EASD). Diabetes Care 2020;43:487–493.]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/72f7bd6f3491a6412ea055ac5d7636d5.png)
Závěr
Inhibitory SGLT2 patří mezi účinná a poměrně bezpečná antidiabetika s prokázaným příznivým ovlivněním srdečního selhání, chronického onemocnění ledvin a hlavních KV příhod u diabetiků v sekundární prevenci. Jedná se o relativně nové léky, jejichž spotřeba kontinuálně narůstá a zřejmě bude narůstat s tím, jak se změnilo jejich postavení v léčbě diabetu a jak se objevují informace o jejich prospěšnosti i u nediabetických pacientů. V blízké době lze očekávat, že data z probíhajících klinických hodnocení dále upřesní jejich klinické využití.
Podpořeno grantem IGA_LF_2020_005 a MZ ČR – RVO (FNOl, 00098892).
prof. MUDr. David Karásek, Ph.D.
III. interní klinika – nefrologická, revmatologická a endokrinologická LF UP a FN Olomouc
Zdroje
1. Karásek D. Novinky v léčbě SGLT-2 inhibitory. Farmakoter Revue 2020;5 : 1–7.
2. Prázný M. SGLT-2 inhibitory a jejich postavení v současné medicíně. Vnitř Lék 2020;66 : 82–88.
3. Jingfan Z, Ling L, Cong L, et al. Efficacy and safety of sodium-glucose cotransporter-2 inhibitors in type 2 diabetes mellitus with inadequate glycemic control on metformin: a meta-analysis. Arch Endocrinol Metab 2019;63 : 478–486.
4. Milder TY, Stocker SL, Abdel Shaheed C, et al. Combination therapy with an SGLT2 inhibitor as initial treatment for type 2 diabetes: a systematic review and meta-analysis. J Clin Med 2019;8 : 45.
5. Zinman B, Wanner C, Lachin JM, et al.; EMPA-REG OUTCOME Investigators. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015;373 : 2117–2128.
6. Neal B, Perkovic V, Mahaffey KW, et al.; CANVAS Program Collaborative Group. Canagliflozin and cardiovascular and renal events in type 2 diabetes. N Engl J Med 2017;377 : 644–657.
7. Wiviott SD, Raz I, Bonaca MP, et al.; DECLARE-TIMI 58 Investigators. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2019;380 : 347–357.
8. Zelniker TA, Wiviott SD, Raz I, et al. Comparison of the effects of glucagon-like peptide receptor agonists and sodium-glucose cotransporter 2 inhibitors for prevention of major adverse cardiovascular and renal outcomes in type 2 diabetes mellitus. Circulation 2019;139 : 2022–2031.
9. Gerstein HC, Colhoun HM, Dagenais GR, et al.; REWIND Investigators. Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet 2019;394 : 121–130.
10. Buse JB, Wexler DJ, Tsapas A, et al. 2019 Update to: Management of hyperglycemia in type 2 diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2020;43 : 487–493.
11. Inzucchi SE, Zinman B, Wanner C, et al. SGLT-2 inhibitors and cardiovascular risk: proposed pathways and review of ongoing outcome trials. Diab Vasc Dis Res 2015;12 : 90–100.
12. Grubić Rotkvić P, Cigrovski Berković M, Bulj N, Rotkvić L. Minireview: are SGLT2 inhibitors heart savers in diabetes? Heart Fail Rev 2019; doi:10.1007/s10741-019-09849-3.
13. Baartscheer A, Schumacher CA, Wüst RC, et al. Empagliflozin decreases myocardial cytoplasmic Na(+) through inhibition of the cardiac Na(+)/H(+) exchanger in rats and rabbits. Diabetologia 2017;60 : 568–573.
14. Sato T, Miki T, Ohnishi H, et al. Effect of sodium-glucose co-transporter-2 inhibitors on impaired ventricular repolarization in people with type 2 diabetes. Diabet Med 2017;34 : 1367–1371.
15. Cosentino F, Grant PJ, Aboyans V, et al.; ESC Scientific Document Group. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J 2020;41 : 255–323.
16. Cannon CP, Pratley R, Dagogo-Jack S, el a. Cardiovascular outcomes with ertugliflozin in type 2 diabetes. N Engl J Med 2020; 383 : 1425-1435.
17. Zelniker TA, Wiviott SD, Raz I, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta - -analysis of cardiovascular outcome trials. Lancet 2019;393 : 31–39.
18. Verma S, McMurray JJV, Cherney DZI. The metabolodiuretic promise of sodium-dependent glucose cotransporter 2 inhibition: the search for the sweet spot in heart failure. JAMA Cardiol 2017;2 : 939–940.
19. Vaduganathan M, Januzzi JL Jr. Preventing and treating heart failure with sodium-glucose co-transporter 2 inhibitors. Am J Cardiol 2019;24(Suppl.1):S20–S27.
20. Barutta F, Bernardi S, Gargiulo G, et al. SGLT2 inhibition to address the unmet needs in diabetic nephropathy. Diabetes Metab Res Rev 2019;35:e3171.
21. McMurray JJV, Solomon SD, Inzucchi SE, et al.; DAPA-HF Trial Committees and Investigators. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med 2019;381 : 1995–2008.
22. Packer M, Anker SD, Bulter J, et al.; EMPEROR-Reduced Trial Investigators. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med 2020; 383 : 1413-1424.
23. Ali A, Bain S, Hicks D, et al.; As part of the Improving Diabetes Steering Committee. SGLT2 inhibitors: Cardiovascular benefits beyond HbA1c-translating evidence into practice. Diabetes Ther 2019;10 : 1595–1622.
24. Cherney DZ, Odutayo A, Aronson R, et al. Sodium glucose cotransporter-2 inhibition and cardiorenal protection: JACC Review Topic of the Week. J Am Coll Cardiol 2019; 74 : 2511–2524.
25. Perkovic V, Jardine MJ, Neal B, et al.; CREDENCE Trial Investigators. Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med 2019;380 : 2295–2306.
26. Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al.; DAPA-CKD Trial Committees and Investigators. Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020; 383 : 1436-1446.
27. https://www.ema.europa.eu/en/documents/product-information/invokana-epar -product-information_cs.pdf.
28. Davies MJ, D‘Alessio DA, Fradkin J, et al. Management of hyperglycemia in type 2 diabetes, 2018. A Consensus Report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2018;41 : 2669–2701.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovoČlánek Nový Etický kodex AIFP
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
2020 Číslo 3-4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Úvodní slovo
- Léčba depresí a dalších psychických nemocí nejen s ohledem na COVID-19
- Vši a svrab: Aktualizace léčby
- Komentář ke článku Vši a svrab: Aktualizace léčby
- Diagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
- Komentář k článku Diagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
- Možnosti antidiabetické léčby v roce 2020 – důvod ke skepsi, či optimismu?
- Bezpečnost antidiabetik v léčbě diabetu 2. typu
- Inhibitory SGLT2 v léčbě diabetu 2. typu GLIFLOZINY a jeho komplikací
- Hypoglykemie jako stále obávaná komplikace léčby diabetu a její prevence
- Profesor Miroslav Souček: Hypertenzi mám, jak jinak?
- Současná a perspektivní léčba obezity u diabetiků
- Nealkoholová tuková jaterní choroba a diabetes mellitus
- Testosteron u mužů s metabolickým syndromem, prediabetem a diabetem 2. typu Pozitivní účinky terapie testosteronem
- Nový Etický kodex AIFP
- Nemoci přenášené klíšťaty – jsou pacienti dostatečně informováni?
- Chřipka a její komplikace. Co nás čeká?
- Horké aktuality v registracích EMA
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Vši a svrab: Aktualizace léčby
- Diagnostika a terapie těžké akutní pankreatitidy v intenzivní medicíně
- Testosteron u mužů s metabolickým syndromem, prediabetem a diabetem 2. typu Pozitivní účinky terapie testosteronem
- Chřipka a její komplikace. Co nás čeká?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



