-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Testosteron a civilizační onemocnění
Testosterone and lifestyle diseases
Subnormal levels of testosterone are frequently found in men of advanced age. Hypogonadal men have lower life expectancy than men with full androgenisation, and cardiovascular disease, obesity or diabetes is often associated with hypotestosteronemia. Low testosterone level is a risk factor for these diseases. However, it is still not clear whether testosterone deficiency is a cause or consequence of atherosclerosis or metabolic syndrome. A handful of symptoms and metabolic parameters present in hypogonadal men can be ameliorated by testosterone supplementation. Testosterone has a beneficial effect on cardiovascular risk factors, but it is not clear whether it reduces mortality.
Key words:
testosterone, cardiovascular disease, obesity, metabolic syndrome, diabetes mellitus.
Autoři: L. Stárka
Působiště autorů: Ředitel: doc. MUDr. Vojtěch Hainer, CSc. ; Endokrinologický ústav, Praha
Vyšlo v časopise: Prakt. Lék. 2010; 90(11): 636-639
Kategorie: Přehledy
Souhrn
Subnormální hladiny testosteronu nejsou žádnou vzácností ve vyšších věkových skupinách mužů. Hypogonádní muži umírají dříve než muži dostatečně zásobení androgeny a kardiovaskulární onemocnění, diabetes a obezita se výrazně podílejí na tomto jevu. Nízký testosteron je rizikovým faktorem pro tato onemocnění. Není však jasno, zda nízký testosteron je příčinou nebo následkem těchto stavů. Řadu příznaků hypogonadismu i metabolických odchylek, které jej provázejí, lze zlepšit podáváním testosteronu. Nevíme však dosud, zda je náhradní testosteronovou terapií snížena i mortalita.
Klíčová slova:
testosteron, kardiovaskulární onemocnění, obezita, metabolický syndrom, diabetes mellitus.Úvod
Androgeny, jejichž hlavním představitelem je testosteron, jsou hormony, které výrazně zasahují do vývoje muže a jeho rozmnožovacích funkcí. Jsou i nezbytnou součástí reprodukčních schopností ženy. Jejich úloha však není omezena na zajištění reprodukce, zasahují i do řady metabolických pochodů, a mají vztah k řadě onemocnění, která označujeme někdy jako civilizační, jako jsou
- hypertenze,
- diabetes,
- metabolický syndrom,
- obezita, nebo
- kardiovaskulární onemocnění.
Něco málo z fyziologie testosteronu
Testosteron byl izolován v čisté formě právě před 80 lety a v r. 1939 byla za jeho izolaci, identifikaci a charakterizaci udělena Nobelova cena. Testosteron je hlavním androgenem člověka, ale celková androgenní účinnost není dána pouze jeho sekrecí a koncentrací v cirkulaci, ale vzhledem k jeho silné selektivní vazbě na sexuální hormony vázající globulin (SHBG) je aktivita testosteronu dána frakcí, která není vázána SHBG, a je proto biologicky pro organismus rychle dostupná.
Volný testosteron snižují
- vegetářská strava,
- obezita,
- alkohol,
- větší fyzická námaha,
- stres,
- chronické nemoci,
- kortizol,
- prolaktin,
- hypertyreóza.
Dalším faktorem, který určuje androgenní potenciál, je kvalita androgenního receptoru, jeho prostřednictvím plní testosteron svou signalizační úlohu pro děje, které označujeme jako androgenní a anabolické. Kromě možných mutací, které androgenní receptor v různém stupni inaktivují a jsou pak původcem patologických procesů, se v androgenním receptoru objevuje repetice CAG, která při častějším opakováním motivu CAG snižuje androgenní účinek.
V r. 1968 pak Bruchovsky zjistil, že dihydrotestosteron, metabolit testosteronu vzniklý jeho 5a-redukcí, je několikanásobně účinnějším androgenem v některých tkáních.
Dihydrotestosteron je hlavním androgenem
- kožních adnex,
- prostaty,
- epididymis,
- ledvin, a
- genitálu,
zatím co testosteron je androgenem nezbytným pro
- spermatogenezi,
- pro děje v CNS,
- pro sval, kost, játra, a
- hematopoezu.
Nejvýraznější úlohou androgenů je funkce testosteronu (a v pozdějším vývoji i dihydrotestosteronu) v sexuální diferenciaci plodu u mužského fenotypu, postnatálně je nezbytná úloha androgenů pro reprodukční funkce, zejména mužské, a pro vývoj sekundárních mužských pohlavních znaků (u žen pubického a axilárního ochlupení), a pro zpětnou vazbu, která řídí hypofyzární sekreci luteinizačního hormonu (LH). Tzv. aromatizovatelné androgeny – testosteron, androstendion a nepřímo i adrenální dehydroepiandrosteron, nikoli však dihydrotestosteron – jsou prekurzory estrogenů, a proto jejich tvorba je rozhodující i pro základní reprodukční funkce ženy, pro které jsou estrogeny nezbytné.
V dospělosti se u mužů pohybují hodnoty testosteronu v séru v poměrně širokém rozmezí mezi 11–35 nmol/l (3–10 ng/ml), ale u téhož jedince mají za shodných okolností poměrně značnou stabilitu.
U žen je referenční koncentrace v séru udávána mezi 0,5–3,0 nmol/l (0,2 až 1,0 ng/ml).
Hladina testosteronu má věkovou závislost. Diurnální variace hladiny se vyznačují nejvyšší úrovní ráno před vzbuzením.
Denní produkce testosteronu byla vypočítána na asi 6 mg a pochází převážně z Leydigových buněk varlete. Kolující testosteron pochází zčásti také z konverze jeho prehormonů v periférii. Tyto prekurzory periferně produkovaného testosteronu jsou převážně nadledvinového původu a zvyšují celkovou produkční rychlost proti sekreční rychlosti u mužů asi o 5 %. Celkově je u muže extra-testikulárního původu asi třetina všech androgenů, u žen je však extra-ovariálního původu podstatně větší podíl, asi 2/3. Důležité je, že u muže koncentrace testosteronu ve funkčním zdravém varleti je až 100 krát vyšší než v periferní krvi. To je také důvodem, proč při běžném podávání testosteronu při hypogonadismu lze sice dosáhnout normalizace hladiny androgenů v periferní krvi, ale nikoliv v gonádách, a proto takto nelze zajistit dostatečnou hladinu hormonu pro spermatogenezi, i když se sekundární pohlavní znaky mohou zlepšit.
Androgenní nedostatečnost – hypogonadismus
Klasická endokrinologie rozlišuje dva základní typy androgenní nedostatečnosti u mužů. Jsou to:
- primární hypogonadismus,
- sekundární hypogonadismus.
Prvý je dán neschopností Leydigových buněk ve varleti produkovat testosteron. Gonadotropiny jsou při něm zvýšené, odtud název hypergonadotropní hypogonadismus.
Sekundární hypogonadismus se vyznačuje nedostatečnou produkcí hypofyzárních gonadotropinů, což pak má za následek chybějící sekreci testosteronu ve varleti. Leydigovy buňky však mohou příznivě reagovat na podávání LH a FSH a hypogonadotropní hypogonadismus je proto léčitelný gonadotropními přípravky.
Oba tyto typy hypogonadismu jsou v mládí a ve věku optimálních reprodukčních schopností muže nepříliš časté (prevalence nízkých hodnot celkového testosteronu se v 3. dekádě pohybuje mezi 2 až 5 % a zvyšuje se s věkem) ve srovnání s dalším typem hypogonadismu.
Je to hypogonadismus s pozdním nástupem (late onset hypogonadism, LOH), který je vlastně smíšeným typem (12) primárního a sekundárního hypogonadismu s funkčním poklesem jak na úrovni gonád, tak hypotalamo-hypofyzárního systému. Tento typ postihuje významnou část mužské populace s narůstajícím věkem (obr. 1) – ve věku nad 80 let je jím postižen každý druhý muž.
Obr. 1. Relativní zastoupení mužů s hypotestosteronémií podle věku 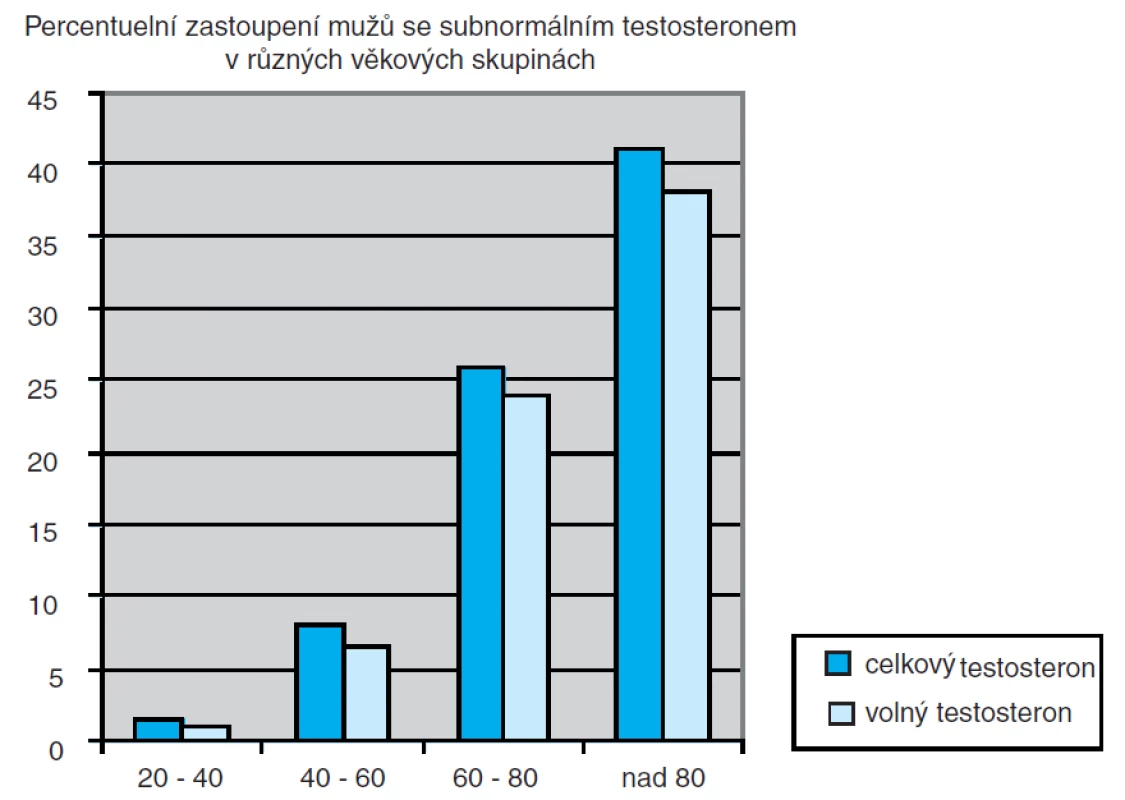
Příznaky hypoandrogenémie u mužů
Snížené zásobování organismu androgeny je provázeno řadou nepříznivých příznaků a symptomů, které však nejsou příliš specifické (tab. 1).
Tab. 1. Příznaky androgenního deficitu u stárnoucích mužů 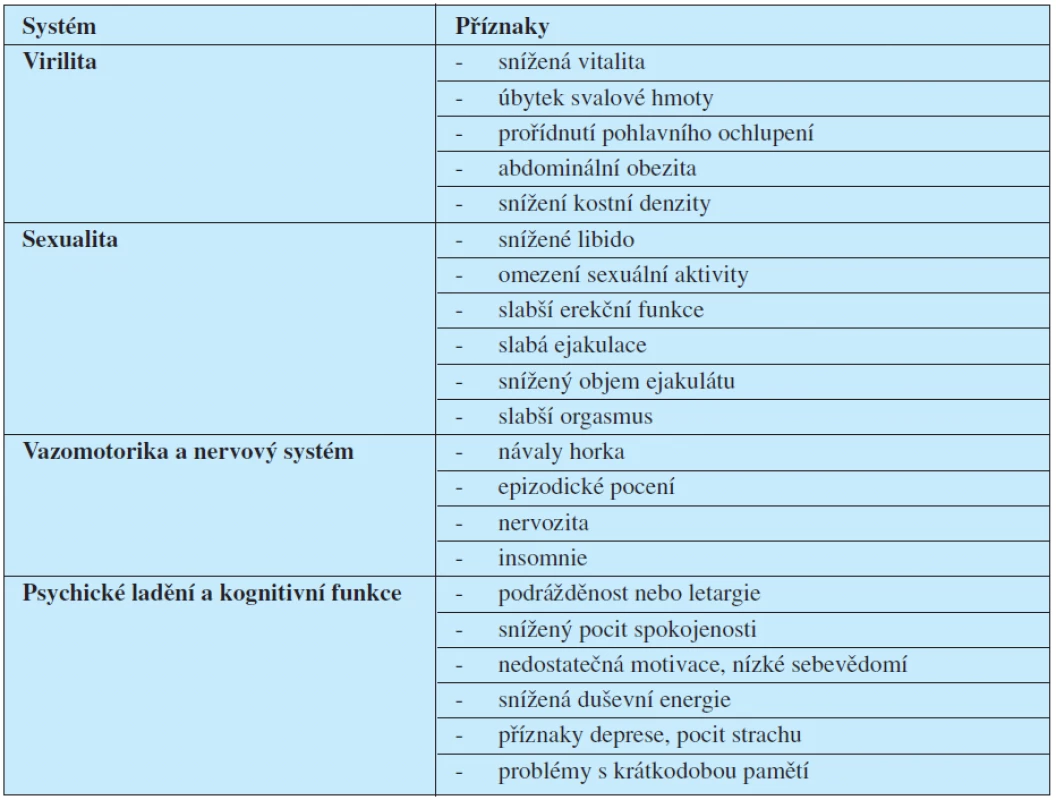
U mužů byl také zjišťován vztah mezi mírou nedostatku celkového testosteronu a nástupem jednotlivých příznaků (16). Výsledek je uveden v tabulce 2.
Tab. 2. Pořadí nástupu příznaků hypotestosteronémie u mužů podle závažnosti nedostatku testosteronu 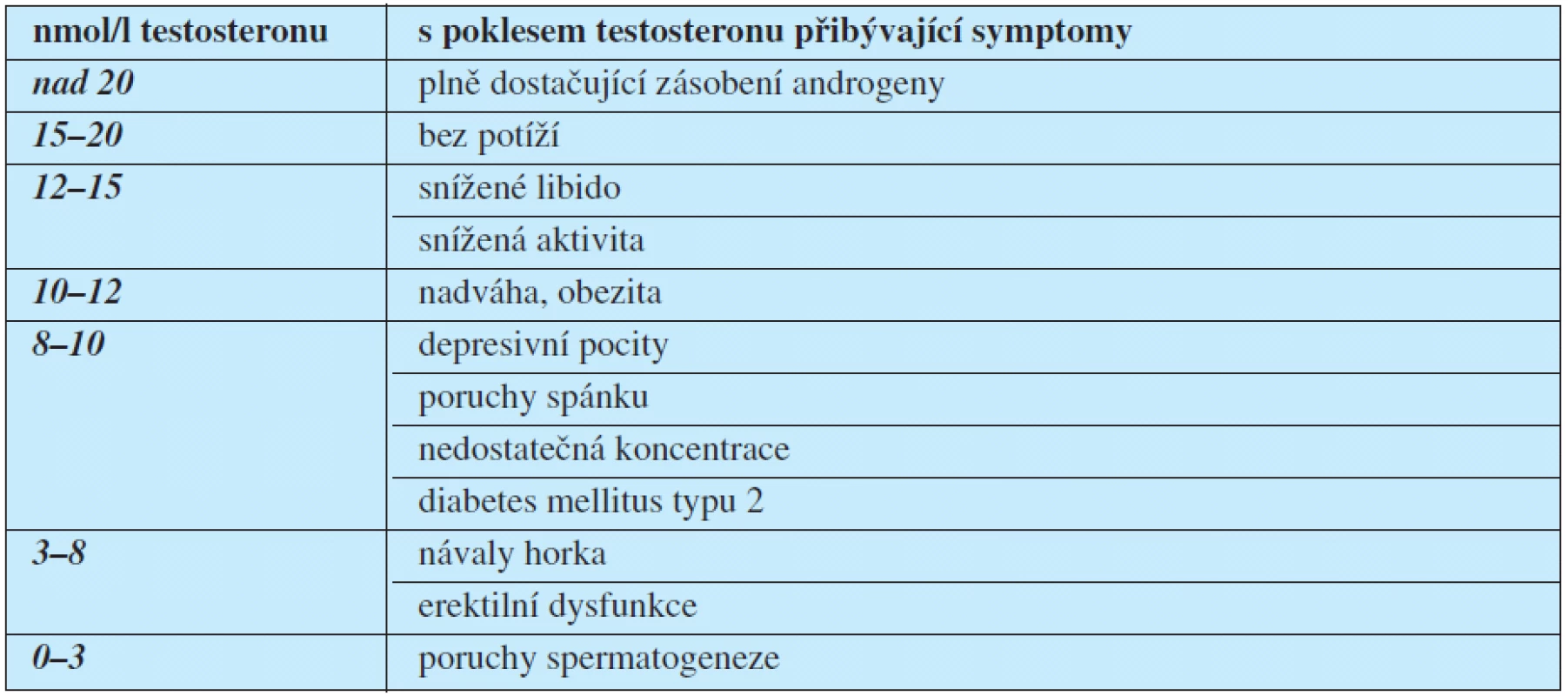
Pro přibližnou primární orientaci o zásobení androgeny by mohl sloužit i dotazník vypracovaný na univerzitě v St. Louis (tab. 3).
Tab. 3. Dotazník University St. Louis na androgenní nedostatečnost 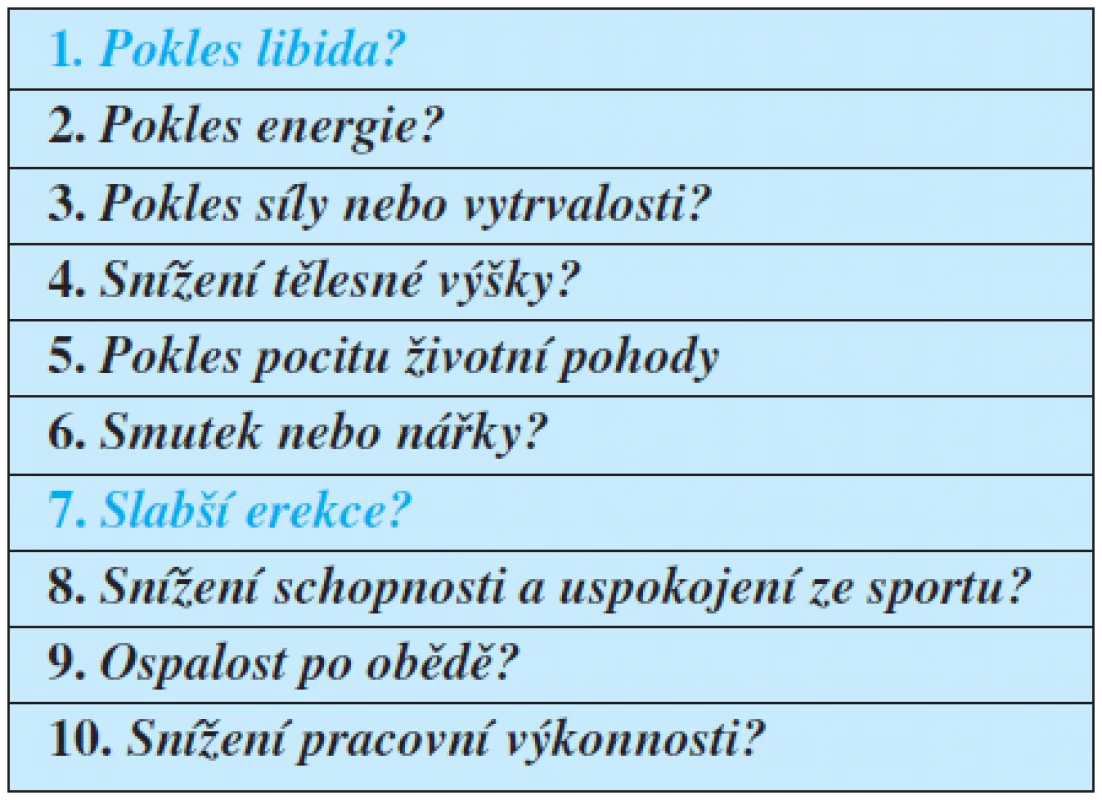
Legenda: Kladná odpověď na otázku 1 nebo 7 nebo tři jiné otázky je důvodem k dalšímu vyšetření a laboratornímu stanovení testosteronu Hypogonadismus by měl být potvrzen laboratorním vyšetřením. Protože hladina testosteronu kolísá v průběhu dne s maximem v raných denních hodinách (02–04) a minimem mezi 20–24 hod., je při rozpětí amplitudy rozdílu 30–50 % nejvhodnější doba k odběru mezi 7–10 hod. Referenční rozmezí testosteronu je pro muže 11–35 nmol/l, je však nutno se řídit hodnotami příslušné laboratoře.
Hladina celkového testosteronu u mužů mezi 7–11 nmol/l se zpravidla považuje za šedou zónu, pod 7 nmol/l jde o zřejmý hypogonadismus. Hraniční hodnoty podle Kellerhera et al. (4) pro celkový a volný testosteron pro muže i ženy jsou uvedeny v tabulce 4.
Tab. 4. Symptomatický práh testosteonu pro hypotestosteronémii (částečně podle Kelleher et al., 2004) 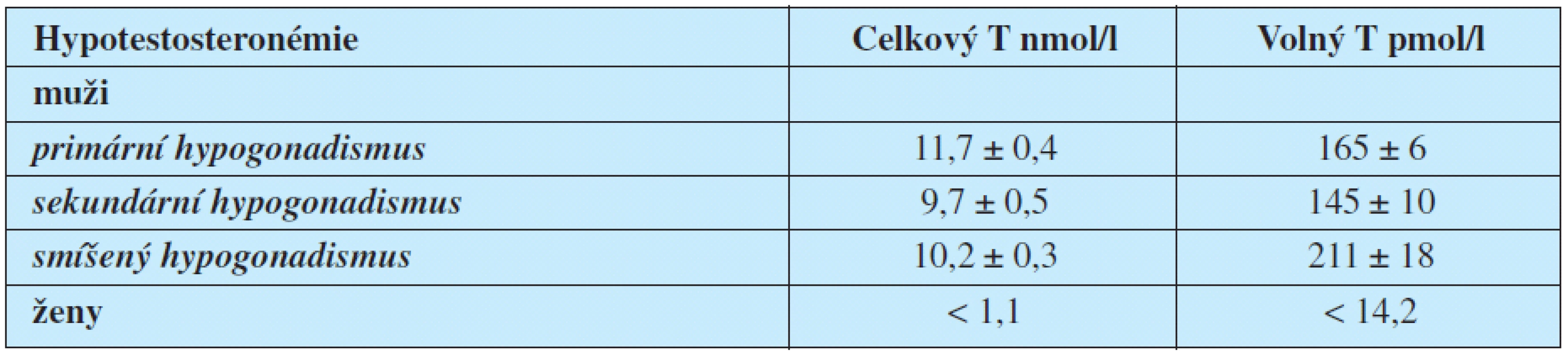
Hypotestosteronémie u žen
Poznatky o vlivu androgenů na mortalitu a výskyt kardiovaskulárních onemocnění neplatí jen pro muže – i u žen byla zjištěna asociace počtu úmrtí na všechny příčiny a incidence kardiovaskulárních onemocnění s nízkou úrovní bazální hladiny testosteronu (1, 10).
U žen je třeba s androgenní nedostatečností třeba počítat po přirozeném přechodu nebo po ovarektomii. S vyhasnutím reprodukční funkce ovarií se snižuje výrazně i produkce androgenů tímto zdrojem, také adrenální sekrece androgenů a jejich prekurzorů na rozdíl od sekrece kortikoidů má klesající průběh s vyšším věkem a jsou-li ženě podávány estrogeny, např. ve formě substituční léčby (HRT – hormone replacement therapy), dochází k vzestupu SHBG, a tím k významnému poklesu volné frakce androgenů.
Důsledkem poklesu androgenů u ženy po přechodu je snížení libida a sexuální vzrušivosti a fantazií, přetrvávající nevysvětlitelná únava a snížení pocitu pohody (well-being). Ke známkám hypoandrogenémie pak patří redukce tělesného ochlupení, redukce netukové tělesné tkáně – sarkopenie, osteopenie a osteoporóza.
Hypotestosteronémie a civilizační onemocnění
Kardiovaskulární (KV) onemocnění jsou nejčastější příčinou úmrtí v rozvinutých zemích. Muži umírají dva až třikrát častěji pro KV onemocnění než ženy. Proč je mužské pohlaví takovým rizikovým faktorem, není dosud zcela jasno, obvykle se soudí, že je to proto, že estrogeny jsou protektivním působkem u žen a že u mužů působí poněkud jinak.
Dnes je k dispozici řada pozorování, že nízký testosteron je asociován s přítomností stupně aterosklerózy a s některými kardiovaskulárními rizikovými faktory jako jsou
- viscerální obezita,
- inzulínová rezistence,
- dyslipidémie,
- hypertenze.
Souvisí tedy s metabolickým syndromem (3, 13, 14).
Epidemiologické studie prokazují, že muži s nízkým testosteronem se dožívají nižšího věku a mají vyšší úmrtnost na všechny příčiny, na kardiovaskulární onemocnění, na onkologická a respirační onemocnění (6). Nízký testosteron zvyšuje aterosklerózu a substituce testosteronem u hypogonadismu má příznivý vliv na některé rizikové faktory kardiovaskulárních onemocnění, potlačuje známky zánětu a zlepšuje symptomy hypogonadismu a zvyšuje pocit dobré životní pohody.
Testosteron potlačuje expresi tumor necrosis faktoru TNF-α, cytokinů IL-1b a IL-6 a zvyšuje tvorbu anti-aterogenního cytokinu IL-10. Testosteron zvyšuje také aktivitu NO-syntázy, a tím i produkce oxidu dusnatého, důležitého pro cévní dilataci. Testosteron příznivě ovlivňuje řadu rizikových faktorů pro poruchu funkce koronárních arterií a má příznivý vliv na vaskulární tonus, cévní dilataci a krevní průtok (14).
Není však jasno, zde nízký testosteron je v kauzální souvislosti s uvedenými onemocněními, nebo je jen jejich důsledkem.
Kardiovaskulární onemocnění (KVO)
Epidemiologické studie potvrzují (9), že nízký testosteron se častěji zjišťuje u pacientů s ischemickou srdeční chorobou a že hypotestosteronémie u straších mužů je prediktorem iktu a ischemických atak (15). Tyto vztahy k ateroskleróze jsou přesvědčivější, když místo celkového testosteronu se berou v úvahu přesnější parametry, jako je volný testosteron, biologicky dostupný testosteron nebo index volného testosteronu. Pro vznik aterosklerózy je důležitá zánětlivá složka s produkcí cytokinů, které pak potlačují osu hypotalamus – hypofýza - gonády. Nízký testosteron je možno tedy považovat za biomarker zánětu. Testosteron naopak sám má imunomodulační aktivitu a nízký testosteron urychluje progresi aterosklerózy.
Častým prvým pro pacienta nápadným příznakem kardiovaskulárního onemocnění nebo diabetu je erektilní dysfunkce, ke které kromě cévních faktorů přispívá i subnormální hladina testosteronu.
Obezita
S nízkým testosteronem koreluje abdominální a subkutánní nahromadění tuku. Příčiny, proč testosteron zvyšuje podíl netukové k tukové tkáni není dosud zcela objasněn. Snad je to schopností testosteronu stimulovat lipolýzu a inhibovat aktivitu lipoprotein-lipázy. Nahromadění tukových zásob vyvolává zvýšení inzulínové rezistence, ale samotné tukové depozitum nevysvětlí zvýšení inzulínové rezistence. Krátké dvoutýdenní přerušení suplementace testosteronem u mužů léčených pro hypogonadotropní hypogonadismus mělo totiž za následek prudké zhoršení inzulínové senzitivity, aniž by v této krátké době došlo k podstatnějším změnám hmotnosti.
Nízký testosteron u obezity se někdy vysvětluje vysokou aktivitou aromatázy v tukové tkáni, zejména abdominální, která vede k přeměně testosteronu na estrogeny. Obézní muži mají sice vyšší estrogeny, ale množství jejich produkce nevysvětluje kvantitativní pokles testosteronu. Testosteron zprostředkovává vznik myocytů na úkor adipocytů z pluripotentních kmenových buněk a redukuje záchyt mastných kyselin v adipocytech. Roli hrají i prozánětlivé cytokiny, leptin a estradiol, které inhibují osu hypotalamus - hypofýza - testes.
Inzulínová rezistence
U starších mužů je celkový testosteron, pokud je v subnormálním rozmezí, asociován s inzulínovou rezistencí nezávisle na ukazatelích centrální obezity (15). Naopak, u žen s hyperandrogenémií, např. u žen se syndromem polycystických ovarií, je častá inzulínová rezistence úměrná stupni nadprodukce androgenů (13). Nízký testosteron vede k poruše mitochondriální oxidativní fosforylace jako jednoho z možných míst zásahu do mechanismu působení inzulínu.
Metabolický syndrom
Metabolický syndrom je souhrnem nahromadění zvýšených rizik kardiovaskulárních onemocnění jako je
- viscerální obezita,
- porušená glukózová tolerance,
- zvýšené triglyceridy,
- nízký HDL-cholesterol, a
- hypertenze.
Nízký testosteron, i když částečně kompenzovaný nízkým SHBG, je silným nezávislým rizikovým faktorem pro metabolický syndrom, a tím i pro KV onemocnění (11), a to i u neobézních mužů (5).
Testosteronová nedostatečnost přispívá k dyslipidémii, typické pro metabolický syndrom. Pojí se s vyššími hladinami celkového i LDL-cholesterolu a triglyceridů a s nižším HDL-cholesterolem. Přispívá také k prokoagulačním pochodům, snižuje aktivátor plasminogenu a zvyšuje fibrinogen a inhibitor aktivátoru plasminogenu.
Angina pectoris
První úspěšný pokus o zlepšení anginy pectoris podáváním testosteronu byl uveřejněn už v r. 1942 nezávisle a téměř současně dvěma pracovišti, ale až v r. 1977 potvrdila kontrolovaná studie příznivé účinky testosteronu na ST segment EKG. Průkazů o zlepšení subjektivních potíží, o zlepšení objektivních ukazatelů srdeční ischemie je dnes celá řada (7). Perfuzní studie ukazují, že testosteron působí jako selektivní blokátor L-kalciových kanálů na úrovni vazebných míst pro nifedipin.
Srdeční selhání
Chronické srdeční selhání má vysokou mortalitu a je spojeno v terminálním stadiu s katabolickým stavem a kachexií. Nízký testosteron je nepříznivým prognostickým ukazatelem pro přežití. Zdálo by se, že pro zvrat katabolického metabolismu v anabolický by měly sloužit anabolicko-androgenní hormony. Testosteron se však nepodává pro nebezpeční retence tekutin. Ovšem podání suprafyziologiuckých dávek testosteronu snižuje periferní cévní rezistenci a zlepšuje srdeční výdej, funkční kapacitu a VO2max (2).
Diabetes mellitus
Diabetes mellitus je zpravidla provázen příznaky typickými pro metabolický syndrom. Diabetici mají nižší gonadotropiny a testosteron než zdraví muži a porucha sexuálních funkcí, zejména erektilní dysfunkce, je často prvým příznakem cukrovky.
Vliv náhradní androgenní terapie
Většina studií o vlivu podávání testosteronu na zlepšení kardiovaskulárních funkcí byla studie poměrně krátkodobých. Je třeba zdůraznit, že testosteron snižuje obvod pasu (nemění však BMI) a hladinu leptinu a zlepšuje inzulínovou rezistenci, ale pouze tam, kde výchozí hladiny androgenů byly nedostatečné. U diabetiků 2. typu zlepšuje glykemickou kontrolu.
Testosteron také vede k malému poklesu celkového cholesterolu a někdy i LDL-cholesterolu, ale nemění triglyceridy. Vliv na HDL-cholesterol se popisuje různě. Testosteronová suplementace příznivě ovlivňuje koagulační pochody, může však vést k polycytémii svým pozitivním vlivem na erytropoézu. Nadměrně zvýšení hematokritu je signálem ke snížení terapeutické dávky nebo jejímu vynechání (8).
Poděkování.
Práce byla vypracována v rámci grantového projektu IGA MZ ČR NS 9831-4.
Prof. MUDr. RNDr. L. Stárka, DrSc.
Endokrinologický ústav
Národní 8
116 94 Praha 1
E-mail: lstarka@endo.cz
Zdroje
1. Casson, P.R., Toth, M.J., Johnson, J.V. et al. Correlation of serum androgens with anthropometric and metabolic indices in healthy, nonobese postmenopausal women. J. Clin. Endocrinol. Metab. 2010, 95, p. 4276-4282.
2. Caminiti, G., Volterrani, M., Iellamo, F. et al. Effect of long-acting testostereone treatment on functional exercise capacity, skeletal muscle performace, insulin resistance, and baroreflex sensitivity in elderly patients with chronic heart failure. A double-blind, placebo-controlled, randomised study. J. Am. Coll. Cardiol. 2009, 54, p. 919-927.
3. Jones, T.H. Testosterone deficiency: a risk actor for cardiovascular disease? Trends Endocrinol. Metab. 2010, 21, p. 496-503.
4. Kelleher, S., Conway, A.J., Handelsman, D.J. Blood testosterone threshold for androgen deficiency symptoms. J. Clin. Endocrinol. Metab. 2004, 89, p. 3813-387.
5. Kupelian, V., Page, S.T., Araujo, A.B. et al. Low sex hormone binding globulin, total testosterone, and symptomatic androgen deficiency are associated with the decelopment of the metabolic syndrome, in no-obese men. J. Clin. Endocrinol. Metab., 2006, 91, p. 843-850.
6. Laughlin, G.A., Barret-Connor, E., Bergstrom. J. Low serum testosterone and mortality in older men. J. Clin. Endocrin. Metab. 2008, 93, p. 68-75.
7. Mathur. A., Malkin, C., Saeed, B. et al. Long-term benefits of testosterone replacement therapy on angina treshold and atheroma in men. Eur. J. Endocrinol., 2009, 161, p. 443-449.
8. Miner, M., Canty, D.J., Shabsigh, R. Testosterone replacement therapy in hypogonadal men: assessing benefits, risks, and best practices. Postgrad. Med., 2008, 120, p. 130-153.
9. Nettleship, J.E., Jones, R.D., Channer, K.S., Jones TH. Testosterone and coronary artery disease. Front. Horm. Res. 2009, 37, p. 91-107.
10. Sievers, C., Klotsche, J., Pieper, L. et al. Low testosterone leevels predict all-cause mortality and cardiovascular events in women: a prospective cohort study in German primary care patients. Eur. J. Endocrinol. 2010, 163, p. 699-708.
11. Stanworth, R.D., Jones, T.H. Testosterone in obezity, metabolic syndrome and type 2 diabetes. Front. Horm. Res. 2009, 37, p. 74-90.
12. Tajar, A., Forti, G., O’Neill, T.W. et al. Characteristics of secondary, primary, and compensated hypogonadism in aging men: Evidence from the European Male Ageing Study. J. Clin. Endocrinol. Metab. 2010. 95, p. 1810-18.
13. Vrbíková, J., Stanická, S., Vondra, K., et al. Insulin resistance in endocrine disorders. In: Insulin Resistance New Research. Ed. E.B. Yao, Nova Sci. Publ. Inc, 2009, p. 1-47.
14. Webb, C.M., Collins, P. Testosterone and coronary artery disease in men. Maturitas, 2010, 67, p. 15-19.
15. Yeap, B.B., Chubb, S.A., Hyde, Z. et al. Lower serum testosterone is independently associated with insulin resistance in non-diabetic older men. The Health In Men Study. Eur. J. Endocrinol., 2009, 161, p. 591-8.
16. Zitzmann, M., Faber, S., Nieschlag, E. Association of specific symptoms and metabolic risks with serum testosterone in older men. J. Clin. Endocrinol. Metab., 2006,. 91, p. 4335-4343.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2010 Číslo 11- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
-
Evoluce a evoluční teorie pro lékaře
XI. Vývoj jazyka - Testosteron a civilizační onemocnění
- Antiagregace a gastroprotektiva
- Stopové prvky a skelet
- Nové poznatky o rýmě, aneb seznámení s Evropským konsenzem o rinosinusitidě a nosní polypóze z roku 2007 (EP3OS 2007)
- Liečba hypertonikov v ambulantnej starostlivosti na Slovensku
- Dříve projevená přání pacientů a recepce tohoto problému v České republice a v Německu
- Proporcionální zastoupení léčebných postupů u pacientů s benigní hyperplazií prostaty
- Alkohol, tabák a jiné návykové látky a reprodukční rizika
- Astma bronchiale a alergická rhinitida u zadělávačky knedlíků
- Zakladatel klinické laryngoskopie Jan Nepomuk Čermák a jeho fyziologický ústav v Praze
- Miniportréty slavných českých lékařů Profesor MUDr. Karel Mathon, neurolog stíhaný nepřízní osudu
- Nové organizační složky ČLS JEP
- Ze života odborných společností ČLS JEP
-
XXII. kongres ČLS JEP v Brne
Zobrazovacie metódy v medicíne
Živá diskusia medzi odboníkmi a praktickými lekármi - Nový preparát pro léčbu von Willebrandovy choroby
- Sofiina volba onkologů: poškodit pacienta, nebo zadlužit zaměstnavatele?
- Knihy
- JUBILEA
-
Evoluce a evoluční teorie pro lékaře
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



