-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Komplementový systém I: vrozené poruchy komplementové kaskády vyjma hereditárního angioedému
The complement system I: innate defects of complement cascade proteins excluding hereditary angioedema
The complement system consists of more than 50 soluble and membrane-bound proteins. It is a crucial part of the innate immune system. Individual components of the complement cascade are cleaved during the activation process into smaller fragments with specific biological functions. Activation of complement cascade is finished by formation of a membrane-attacking complex associated with lysis of the target cell. The main functions of the complement system include opsonization, chemotaxis, and clearance of immunocomplexes and apoptotic cells.
Congenital disorders of the complement system are very rare diseases. The patients are prone to recurrent infections caused mainly by encapsulated microorganisms (pneumococcus, meningococcus, haemophilus and staphylococus) and most of them develop systemic autoimmune diseases (resembling systemic lupus erythematosus) during their lifetime. The secondary decrease of complement components may be caused by decreased liver production of complement components, excessive or prolonged activation of the immune system as a result of various immunopathological conditions or because of the formation of autoantibodies against the complement components. Basic therapeutic approaches include vaccination against meningococcus, pneumococcus and haemophilus and antibiotic prophylaxis.
Keywords:
complement system – inborn errors of complement system – encapsulated bacteria – autoimmune disorders
Autoři: Z. Chovancová; R. Hakl; J. Litzman
Působiště autorů: Ústav klinické imunologie a alergologie, Fakultní nemocnice u sv. Anny v Brně, Lékařská fakulta Masarykovy univerzity, Brno
Vyšlo v časopise: Čes-slov Pediat 2021; 76 (4): 211-217.
Kategorie: Sympozium: Imunologie
Souhrn
Komplementový systém je tvořen souborem více než 50 solubilních a membránově vázaných proteinů. Tvoří jednu ze základních humorálních složek vrozeného imunitního systému. Při jeho aktivaci dochází ke kaskádovitému štěpení jednotlivých jeho složek na menší fragmenty, což nakonec vyústí v tvorbu membránu atakujícího komplexu a lýze cílové buňky. Mezi hlavní funkce komplementového systému patří opsonizace, chemotaxe a odstraňování imunokomplexů a apoptotických buněk.
Vrozené poruchy komplementového systému jsou velmi vzácné. Pacienti s těmito defekty jsou náchylní k rekurentním infekcím způsobeným převážně obalenými mikroorganismy (pneumokoky, meningokoky, hemofily, stafylokoky) a u většiny z nich se během života rozvine systémové autoimunitní onemocnění (nejčastěji připomínající systémový lupus erythematodes). Sekundární snížení jednotlivých složek komplementové kaskády může být způsobeno jeho sníženou produkcí v játrech, excesivní nebo protrahovanou aktivací imunitního systému u různých imunopatologických stavů, nebo tvorbou autoprotilátek proti složkám komplementu. Mezi základní terapeutické přístupy u pacientů s vrozenými poruchami komplementového systému patří vakcinace proti meningokokům, pneumokokům, hemofilům a antibiotická profylaxe.
Klíčová slova:
komplementový systém – vrozené poruchy komplementu – opouzdřené bakterie – autoimunitní choroby
ÚVOD
Komplementový systém představuje jednu ze základních humorálních složek vrozeného imunitního systému. Je tvořen souborem více než 50 solubilních a membránově vázaných proteinů, kam patří složky aktivace či regulace komplementového systému nebo jeho receptory [1]. Klíčovými složkami komplementové kaskády je 9 proteinů, které se označují C1–C9. Při aktivaci komplementu dochází ke kaskádovitému štěpení jednotlivých složek komplementu na menší fragmenty, které vykazují různé fyziologické funkce.
Komplement je aktivován klasickou, alternativní nebo lektinovou cestou. Úvodní fáze aktivace jednotlivých komplementových drah se různí až do okamžiku vzniku C3-konvertázy. Další průběh aktivace komplementové kaskády je již společný (tab. 1). Výsledkem aktivace celé komplementové kaskády je vznik tzv. membránu atakujícího komplexu (MAC; tvořen komplexem C5b-C9), který se zanoří do lipidové membrány cílové buňky, která je na základě porušení osmotického gradientu lyzována. Jednotlivé štěpné fragmenty komplementové kaskády, které vznikají během procesu aktivace komplementu, se uplatňují jako opsonizační (C3b) nebo chemotaktická (C3a, C5a) činidla, vykazují prozánětlivou aktivitu (C3a, C5a) a podílejí se na odstraňování imunokomplexů (C3b, C4b). K aktivaci komplementové kaskády dochází na bakteriálních buňkách, ale také na buňkách našemu tělu vlastních (např. nádorově změněných). Proto je tento aktivační proces striktně regulován pomocí řady solubilních i membránově vázaných proteinů, aby nedošlo k nežádoucí aktivaci komplementové kaskády s následným poškozením organismu.
Tab. 1. Aktivace komplementového systému klasickou, alternativní a lektinovou cestou. 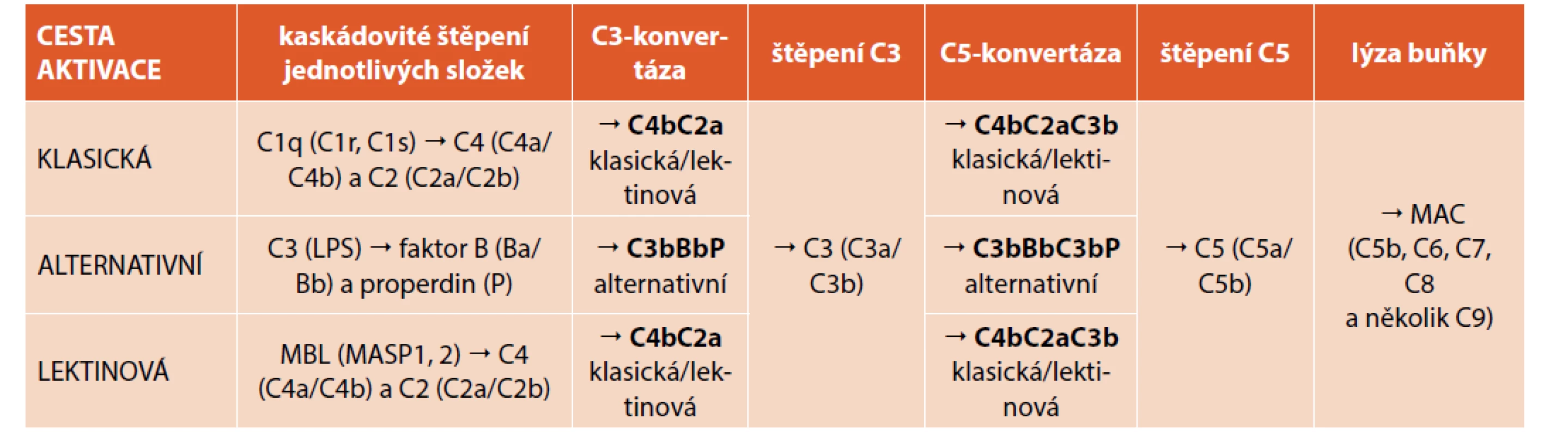
Klasická cesta aktivace komplementu je spouštěna složkou C1 (q, r, s) po navázání C1q složky na imunoglobulin IgM nebo IgG, který je navázán na antigen (imunokomplex) nebo pomocí C-reaktivního proteinu (CRP). Lektinová cesta aktivace komplementu je aktivována prostřednictvím MBL (a kolektinu- 10, kolektinu-11, fikolinu-1, fikolinu-2 nebo fikolinu-3) s uhlovodíkovými zbytky na bakteriálních površích. To vede k aktivaci MBL asociovaných serinových proteáz 1 (MASP1) a 2 (MASP2). Alternativní cesta aktivace komplementu je aktivována prostřednictvím neustálé spontánní degradace C3 složky komplementu, ale také pomocí lipopolysacharidu (LPS) gramnegativních bakterií. Vzniklá klasická/lektinová C3-konvertáza (C4bC2a) a alternativní C3-konvertáza (C3bBbP) dále štěpí složku C3 na fragmenty C3a (chemotaxe) a C3b (opsonizace). Vazbou C3b složky komplementu na klasickou/ /lektinovou a alternativní C3-konvertázu vzniká klasická/lektinová C5-konvertáza (C4bC2aC3b) a alternativní C5-konvertáza (C3bBbC3bP), které dále štěpí faktor C5 na fragmenty C5a (chemotaxe) a C5b. Po vazbě fragmentu C5b ke složkám C6, C7, C8 a několika složkám C9 je vytvořen tzv. membránu atakující komplex (MAC). Jedná se o kanál do buněčné stěny, který zprostředkovává osmotickou lýzu cílové buňky. K poruše komplementového systému může dojít buď v důsledku vrozené nebo získané poruchy tvorby, nebo funkce některé ze složek komplementu nebo jejich regulačních proteinů, či sekundárně v rámci onemocnění doprovázených porušenou aktivací komplementu nebo tvorbou inhibitorů některých složek komplementové kaskády.
VROZENÉ DEFICIENCE JEDNOTLIVÝCH SLOŽEK KOMPLEMENTOVÉ KASKÁDY
Vrozené poruchy imunitního systému (z anglického „inborn errors of immunity“; IEI) se dnes podle nejnovější IUIS klasifikace člení do 10 skupin, přičemž skupina č. 8 je tvořena právě vrozenými poruchami komplementového systému (tab. 2). Obsahuje celkem 30 nozologických jednotek, které jsou způsobeny 36 popsanými genetickými mutacemi [2]. Kongenitální deficience komplementového systému patří obecně mezi velmi vzácná onemocnění s prevalencí 0,03 % [1]. Výjimkou je deficience MBL s prevalencí kolem 5 % a deficience C4A nebo C4B izotypu C4 složky komplementu s prevalencí 11−22 %, resp. 30−45 %) [3].
Tab. 2. Vrozené poruchy komplementového systému. 
Deficience složek klasické cesty aktivace komplementu
Celosvětově bylo popsáno dohromady kolem 100 pacientů, kteří trpí deficiencí C1q, C1r, C1s nebo C4 složky klasické cesty aktivace komplementu. Častější je deficit C2 složky komplementu s incidencí 1 : 20 000 pacientů. Nejvíce zastoupený je pak deficit izotypu C4A nebo C4B složky komplementu s incidencí 1 : 250 pacientů [3].
Část pacientů s homozygotní poruchou některé ze složek klasické cesty aktivace komplementu může mít pozitivní autoprotilátky, a to zejména antinukleární faktor (ANA) a protilátky proti dvouvláknové DNA (anti-dsDNA). U většiny těchto pacientů dochází během života k rozvoji imunokomplexových onemocnění, která nejčastěji připomínají nebo splňují diagnostická kritéria pro systémový lupus erythematodes (SLE-like, případně SLE). Nicméně se u nich mohou rozvinout i další autoimunitní onemocnění, jako je revmatoidní artritida, dermatomyositida, Henochova-Schönleinova purpura nebo glomerulonefritida. Riziko rozvoje autoimunitního onemocnění je největší u pacientů s C1q, C1r, C1s a kompletní C4 deficiencí, menší pak u pacientů s kompletní C2 deficiencí [3]. Kromě příznaků autoimunizace jsou pacienti náchylnější k infekcím způsobeným obalenými mikroorganismy. Asi u poloviny těchto pacientů se objevují těžké bakteriální infekce (meningitidy, pneumonie, osteomyelitidy nebo septikémie) [4]. Recentní studie zkoumající klinické a genetické spektrum 107 pacientů s různými hemizygotními, homozygotními nebo heterozygotními mutacemi jednotlivých složek komplementového systému u celkem 14 dotčených genů potvrdila, že pacienti s deficiencí komplementového systému jsou ohroženi infekcemi způsobenými omezeným portfoliem pyogenních bakterií, a to zejména Neisseria meningitidis a Streptococcus pneumoniae [5]. Pacienti s heterozygotní C2 nebo C4 deficiencí bývají obvykle asymptomatičtí [5].
Deficience složek alternativní cesty aktivace komplementu
Properdin je pozitivní regulátor alternativní cesty aktivace komplementu, který stabilizuje C3-konvertázu. Porucha properdinu je jako jediná ze složek komplementové kaskády přenášena recesivní formou X-vázané dědičnosti. Existují tři formy deficience properdinu, a to kompletní deficience (typ I), částečná deficience (typ II), nebo jeho porušená funkce při normální koncentraci (typ III). Jedná se o vzácné onemocnění, které predisponuje pacienty ke zvýšené náchylnosti k infekcím způsobeným Neisseria meningitidis. Pacienti jsou ohroženi výrazně vyšším rizikem rozvoje diseminovaných fulminantních meningokokových infekcí v porovnání s ostatní populací, které se objevují především v adolescenci [6].
Pacientů s deficiencí složky C3 a jejích regulátorů (faktoru H a I) bylo celosvětově popsáno jen několik málo desítek. U pacientů s deficitem C3 složky komplementu se vyskytují těžké recidivující infekční komplikace způsobené převážně opouzdřenými mikroorganismy, jako je Haemophilus influenzae, Streptococcus pneumoniae, Staphylococcus aureus nebo Neisseria meningitidis [4]. Tyto infekce se většinou objevují v brzkém věku a mívají rekurentní charakter. Pacienti s deficiencí faktoru I trpí častějším a závažnějším průběhem infekcí v porovnání s pacienty s deficiencí faktoru H, ale příčina tohoto rozdílu není jasná [4]. U některých pacientů se může objevit také membranózní glomerulonefritida, zatímco rozvoj SLE-like klinických příznaků není tak častý [3].
Deficience složek lektinové cesty aktivace komplementu
Manózu vázající lektin (MBL) je jedním z proteinů akutní fáze, který je syntetizován v játrech. Je kódován genem MBL-2, který se nachází na 10. chromosomu [7]. Tvoří důležitou složku humorální části vrozeného imunitního systému. Kromě aktivace komplementu lektinovou cestou působí jako opsonin, má zřejmě modulační vliv na průběh některých infekčních a autoimunitních onemocnění, přispívá k odstraňování alergenů a účastní se apoptózy [8]. Deficience MBL je vůbec nejčastější deficiencí konkrétní molekuly imunitního systému, protože heterozygotní deficit MBL postihuje až 30 % dospělé bělošské populace a homozygotní deficit MBL dalších 5 % [9].
Klinická signifikance přítomnosti MBL deficience zůstává i přes intenzivní výzkum kontroverzní. Některé studie ukazují, že snížení hladiny MBL se může podílet na zvýšené frekvenci infekcí zejména v dětském věku [10−12]. Například nízké hladiny MBL byly dávány do souvislosti s náchylností k meningokokovým infekcím u dětí zejména v prvních 2 let života [1, 13]. Jiné studie zase prokázaly význam detekce hladin MBL ve vztahu k recidivujícím infekcím také v dospělosti [4, 14], přičemž recentní rozsáhlá populační studie toto nepotvrdila [9]. Je tedy možné, že k manifestaci imunodeficitu by mohlo docházet při současné přítomnosti další poruchy funkce imunitního systému, i když ani tato hypotéza není pravděpodobně zcela přesná. Na jedné straně bylo totiž publikováno, že závažnější infekce byly častější u pacientů s kombinovanou imunodeficiencí (selektivní IgA deficiencí a deficitem některé IgG podtřídy nebo deficiencí MBL) [15], na druhé straně však bylo popsáno, že současný výskyt deficience IgG podtříd a deficience MBL pacienty ke zvýšené frekvenci respiračních infekcí nepredisponuje [16, 17]. Snížená tvorba MBL by však mohla souviset se zhoršením příznaků již stávající klinicky významné poruchy funkce imunitního systému. Například snížení tvorby MBL predisponuje pacienty s diagnózou běžné variabilní imunodeficience (CVID) k tvorbě bronchiektázií, plicní fibrózy nebo respirační insuficience, nicméně nemá vliv na jejich další neinfekční komplikace [18]. Není také jasné, zda se MBL deficience nějak podílí na riziku rozvoje infekcí u imunosuprimovaných pacientů podstupujících chemoterapii [11].
Pro spíše asymptomatický fenotyp MBL deficience svědčí také to, že není uvedena mezi vrozenými poruchami imunitního systému v nejnovější IUIS klasifikaci [2]. Alely zodpovědné za nedostatečnou tvorbu MBL má ve svém genomu až třetina populace. Evoluční neutralita MBL2 genu tak naznačuje redundantní roli lektinové dráhy aktivace komplementu v obraně hostitele, což dále svědčí spíše pro omezený dopad deficitu MBL na snížení zdatnosti populace [19]. V posledních letech vyšla řada studií, které naznačovaly, že některé polymorfismy MBL2 genu mohou predisponovat pacienty k rozvoji některých intracelulárních infekcí, a že snížená koncentrace MBL může být dokonce protektivním faktorem rozvoje mykobakteriálních infekcí, jako je tuberkulóza nebo leishmanióza [20, 21]. To prokázaly i recentní metaanalýzy [22, 23], z nichž jedna navíc ukázala, že sérové koncentrace MBL by mohly být biomarkerem sloužícím k diagnostice plicní tuberkulózy [23]. Sérová koncentrace MBL byla totiž u pacientů s plicní tuberkulózou signifikantně nižší než u zdravých kontrolních osob. Nicméně pro potvrzení tohoto předpokladu je však třeba dalších studií. Stanovení definitivního konceptu role MBL v obranyschopnosti organismu je tedy ve světle dnešních poznatků značně obtížné.
Mezi další vzácné vrozené deficience komplementového systému patří deficience MBL asociované proteázy 1 (MASP1), která způsobuje 3MC (Malpuech, Michels, Mingarelli, Carnevale) syndrom, který je charakterizován faciální dysmorfií s rozštěpem rtu a patra, ale také postižením sluchu a kognitivních funkcí [24]. Deficience MBL asociované proteázy 2 (MASP2) bývá většinou asymptomatická, nicméně je rizikovým faktorem rozvoje febrilní neutropenie u dětí léčených chemoterapií [25]. Deficience fikolinu-3 predisponuje pacienty k rozvoji SLE [26].
Deficience terminálních složek aktivace komplementu
Deficience terminálních komponent komplementového systému (MAC, C5-C9) predisponují své nositele ke zvýšené náchylností k pyogenním infekcím způsobeným neisseriemi, a to zejména meningokoky. U pacientů s deficiencí MAC bývají meningokokové infekce sice rekurentní, ale spíše mírně probíhající s většinou nízkou úmrtností [27].
ZÍSKANÉ DEFICIENCE JEDNOTLIVÝCH SLOŽEK KOMPLEMENTOVÉ KASKÁDY
Sekundární deficience složek komplementu jsou poměrně časté, protože každý patologický proces, který vede k aktivaci komplementové kaskády, může vyústit v deficienci jednotlivých složek v důsledku jejich nadměrné konsumpce. Navíc se proti jednotlivým složkám komplementu mohou tvořit autoprotilátky, které neutralizují jejich funkci nebo s jejich funkcí interferují. Nejčastější příčinou sekundární deficience složek komplementového systému je však jeho snížená tvorba při poruchách jaterních funkcí nebo při ztrátách bílkovin.
Konsumpce složek komplementového systému nastává zejména u autoimunitních onemocnění. Příkladem mohou být imunokomplexová onemocnění (systémový lupus erythematodes, antifosfolipidový syndrom nebo urtikariální vaskulitida), ale také revmatoidní artritida, kryoglobulinémie, Henochova-Schönleinova purpura a granulomatóza s polyangiitidou. Dalším příkladem onemocnění, pro které je charakteristická konsumpce faktorů komplementu, je C3 glomerulopatie (C3G), poststreptokoková glomerulonefritida (PSGN), atypický hemolyticko-uremický syndrom (aHUS) a další mikroangiopatie. Stanovení koncentrace časných složek aktivace klasické cesty aktivace komplementu (C1q, C3, C4, někdy i C2) je užitečné pro diferenciální diagnostiku a monitorování aktivity těchto onemocnění [28].
Mezi nejdůležitější autoprotilátky namířené proti složkám komplementové kaskády patří autoprotilátky proti C1q složce komplementu (anti-C1q), faktoru H (anti-CFH), C1 inhibitoru (anti-C1-INH) nebo tzv. C3 nefritický faktor (C3Nef). Klinicky nejvýznamnějšími jsou autoprotilátky anti-C1q. Tyto autoprotilátky, které se vyskytují u významné části pacientů s diagnózou SLE, jsou asociovány s proliferativní lupusovou nefritidou, ale také urtikariální vaskulitidou [3]. C3Nef představuje autoprotilátku namířenou proti C3-konvertáze, kterou stabilizuje a neumožňuje její rozpad, proto dochází k protrahovanému štěpení C3 složky komplementu, což vede k její konsumpci. Vyskytuje se u pacientů s parciální lipodystrofií a určitým typem mesangioproliferativní glomerulonefritidy [29, 30]. Někteří pacienti se získaným angioedémem (AAE) mají pozitivní anti-C1-INH protilátky, které zvyšují konsumpci nebo blokují účinek C1-inhibitoru [31]. Protilátky anti-CFH se vyskytují u některých pacientů s atypickým hemolyticko-uremickým syndromem (aHUS) nebo s C3 glomerulopatií [32].
DIAGNOSTIKA A LÉČBA PORUCH JEDNOTLIVÝCH SLOŽEK KOMPLEMENTOVÉ KASKÁDY
Prvním krokem při imunologickém vyšetření zaměřeném na komplementový systém bývá funkční vyšetření aktivace celé komplementové kaskády pomocí alternativní a klasické cesty aktivace komplementu. V případě odhalení poruchy některé z aktivačních drah se následně stanovují koncentrace jednotlivých složek komplementové kaskády. Při potvrzení deficitu některé složky komplementu je možné doplnit také vyšetření genetické. Funkční vyšetření C-inhibitoru se provádí při podezření na diagnózu hereditárního angioedému (HAE). Jednotlivé složky komplementového systému se také chovají jako proteiny akutní fáze a při infekci se jejich koncentrace zvyšuje.
Mezi jednotlivými poruchami složek komplementu neexistují významné rozdíly v terapeutickém přístupu. Pacientům je obecně doporučováno očkování namířené proti meningokokovým, pneumokokovým a hemofilovým infekcím. V případě recidivujících infekcí i navzdory vakcinaci je vhodné přistoupit k antibiotické profylaxi pomocí penicilinových nebo makrolidových antibiotik. Asi čtvrtina pacientů musí být vzhledem k autoimunitním komplikacím zaléčena imunosupresivy [33].
KAZUISTIKA
Pacient s homozygotní deficiencí C2 složky komplementu
Dnes šestadvacetiletý pacient se narodil v termínu z fyziologické gravidity s nekomplikovaným poporodním průběhem. Bratr matky pacienta zemřel na bronchopneumonii ve věku 9 měsíců, ostatní rodinná anamnéza byla bezvýznamná.
Pacient byl poprvé imunologicky vyšetřen ve věku 11 měsíců, protože v 5 měsících prodělal purulentní pneumokokovou meningitidu, v 8 měsících pneumokokovou artritidu a osteomyelitidu pravého hlezna a následně byl hospitalizován poprvé pro otitis media. Při vstupním imunologickém vyšetření bylo zjištěno snížení koncentrace celkových imunoglobulinů ve třídě IgA (0,08 g/l; normální rozmezí 0,22–1,05 g/l) a snížení koncentrace C1q složky komplementu (58,4 mg/l; normální rozmezí 100–250 mg/l). Počty základních lymfocytárních subpopulací, koncentrace ostatních imunoglobulinů a dalších vyšetřených složek komplementové kaskády (C3, C4, C1 inhibitoru) byly v normě. Následně bylo opakovaně prokázáno porušení klasické cesty aktivace komplementu (CH50 ∀ 0 %; referenční rozmezí 50–150 %). Protože alternativní cesta aktivace komplementu byla v normě, byly došetřeny koncentrace jednotlivých časných složek klasické cesty aktivace komplementu (C1q, C1a, C4 a C2) a takto byl v jeho dvou letech odhalen deficit složky C2. Genetické vyšetření u něj prokázalo homozygotní deficit C2 složky komplementu (delece 28 bp zasahující 9 bp na 3´ konci exonu 6 a 19 bp na 5´ konci intronu 6) a nosičství defektní C2 alely u obou jeho rodičů.
Pacient podstoupil všechna pravidelná očkování neživými vakcínami včetně vakcíny proti meningokokovi. Během následujícího období dětství a dospívání trpěl především na recidivující a komplikované otitidy s nutností opakovaných hospitalizací a paracentéz, kterých za život prodělal více než dvacet. Proto byl také opakovaně zajišťován antibiotickou profylaxí. V sérologickém obraze bylo prokázáno občasné snížení koncentrace IgG2 podtřídy IgG imunoglobulinů, což by mohlo přispívat k recidivujícím otitidám. Z dalších infekcí prodělal bronchopneumonii a nekomplikovanou varicelu. V období puberty a rané dospělosti byl celkem bez obtíží, trpěl jen na běžná nekomplikovaná nachlazení. Ve 14 letech se však u něj objevil celotělový nesvědící erytém, kdy kožní biopsie prokázala postižení cév svědčící pro autoimunitní proces charakteru SLE. Proto byl stav uzavřen jako kožní forma SLE, která byla po dohodě s revmatology zaléčena jen lokálními kortikoidními mastmi bez nutnosti systémové imunosupresivní léčby. Pacient měl opakovaně negativní autoprotilátky typické pro SLE, v současné době je pravidelně sledován a je dlouhodobě bez výraznějších potíží.
ZÁVĚR
• Kongenitální deficience jednotlivých složek komplementové kaskády jsou velmi vzácné.
• U většiny těchto pacientů se během života rozvine systémové autoimunitní postižení nejčastěji připomínající systémový lupus erythematodes. Asi polovina pacientů je ohrožena zejména meningokokovými a pneumokokovými infekcemi.
• Kauzální léčba příčiny těchto genetických defektů není zatím možná. Pacienti jsou zajištěni antibiotickou profylaxí v případě recidivujících infekcí, nebo imunosupresivní léčbou v případě rozvoje autoimunitního onemocnění.
• Kromě vrozených poruch složek komplementové kaskády musíme myslet i na jejich získané formy, které vznikají v důsledku snížení tvorby složek komplementu při postižení jater, konsumpci složek komplementu při jeho nadměrné, dlouhotrvající aktivaci nebo jejich ovlivněním autoprotilátkami namířenými proti nim.
Korespondující autorka:
MUDr. Zita Chovancová, Ph.D.
Ústav klinické imunologie a alergologie
Fakultní nemocnice u sv. Anny v Brně
Pekařská 664/53
656 91 Brno
e-mail: zita.chovancova@fnusa.cz
Zdroje
1. Schröder-Braunstein J, Kirschfink M. Complement deficiencies and dysregulation: Pathophysiological consequences, modern analysis, and clinical management. Mol Immunol 2019; 114 : 299–311.
2. Tangye SG, Al-Herz W, Bousfiha A, et al. Human Inborn Errors of Immunity: 2019 Update on the Classification from the International Union of Immunological Societies Expert Committee. J Clin Immunol 2020; 40 (1): 24–64.
3. Brodszki N, Frazer-Abel A, Grumach AS, et al. European Society for Immunodeficiencies (ESID) and European Reference Network on Rare Primary Immunodeficiency, Autoinflammatory and Autoimmune Diseases (ERN RITA) Complement Guideline: Deficiencies, Diagnosis, and Management. J Clin Immunol 2020; 40 (4): 576–591.
4. Ram S, Lewis LA, Rice PA. Infections of people with complement deficiencies and patients who have undergone splenectomy. Clin Microbiol Rev 2010; 23 (4): 740–780.
5. El Sissy C, Rosain J, Vieira-Martins P, et al. Clinical and genetic spectrum of a large cohort with total and sub-total complement deficiencies. Front Immunol 2019; 10 : 1936.
6. Chen JY, Cortes C, Ferreira VP. Properdin: A multifaceted molecule involved in inflammation and diseases. Mol Immunol 2018; 102 : 58–72.
7. Sastry K, Herman GA, Day L, et al. The human mannose-binding protein gene. Exon structure reveals its evolutionary relationship to a human pulmonary surfactant gene and localization to chromosome 10. J Exp Med 1989; 170 (4): 1175–1189.
8. Turner MW. The role of mannose-binding lectin in health and disease. Mol Immunol 2003; 40 (7): 423–429.
9. Dahl M, Tybjaerg-Hansen A, Schnohr P, Nordestgaard BG. A population-based study of morbidity and mortality in mannose-binding lectin deficiency. J Exp Med 2004; 199 (10): 1391–1399.
10. Hartz A, Pagel J, Humberg A, et al. The association of mannose-binding lectin 2 polymorphisms with outcome in very low birth weight infants. PLoS One 2017; 12 (5): e0178032.
11. Heitzeneder S, Seidel M, Förster-Waldl E, Heitger A. Mannan--binding lectin deficiency – Good news, bad news, doesn‘t matter? Clin Immunol 2012; 143 (1): 22–38.
12. Özkan H, Köksal N, Çetinkaya M, et al. Serum mannose-binding lectin (MBL) gene polymorphism and low MBL levels are associated with neonatal sepsis and pneumonia. J Perinatol 2012; 32 (3): 210–217.
13. Šrotová A, Litzman J, Rumlarová Š, et al. Recurrent meningitis and inherited complement deficiency. Epidemiol Mikrobiol Imunol 2016; 65 (4): 238–242.
14. Holdaway J, Deacock S, Williams P, Karim Y. Mannose-binding lectin deficiency and predisposition to recurrent infection in adults. J Clin Pathol 2016; 69 (8): 731–736.
15. Santaella ML, Peredo R, Disdier OM. IgA deficiency: clinical correlates with IgG subclass and mannan-binding lectin deficiencies. P R Health Sci J 2005; 24 (2): 107–110.
16. Barton JC, Bertoli LF. Clinical and laboratory associations of mannose-binding lectin in 219 adults with IgG subclass deficiency. BMC Immunol 2019; 20 (1): 15.
17. Aittoniemi J, Koskinen S, Laippala P, et al. The significance of IgG subclasses and mannan-binding lectin (MBL) for susceptibility to infection in apparently healthy adults with IgA deficiency. Clin Exp Immunol 1999; 116 (3): 505–508.
18. Litzman J, Freiberger T, Grimbacher B, et al. Mannose-binding lectin gene polymorphic variants predispose to the development of bronchopulmonary complications but have no influence on other clinical and laboratory symptoms or signs of common variable immunodeficiency. Clin Exp Immunol 2008; 153 (3): 324–330.
19. Verdu P, Barreiro LB, Patin E, et al. Evolutionary insights into the high worldwide prevalence of MBL2 deficiency alleles. Hum Mol Genet 2006; 15 (17): 2650–2658.
20. Søborg C, Madsen HO, Andersen AB, et al. Mannose-binding lectin polymorphisms in clinical tuberculosis. J Infect Dis 2003; 188 (5): 777–782.
21. Santos IK, Costa CH, Krieger H, et al. Mannan-binding lectin enhances susceptibility to visceral leishmaniasis. Infect Immun 2001; 69 (8): 5212–5215.
22. Mandal RK, Khan MA, Hussain A, et al. Association of MBL2 gene polymorphisms with pulmonary tuberculosis susceptibility: trial sequence meta-analysis as evidence. Infect Drug Resist 2019; 12 : 185–210.
23. Tong X, Wan Q, Li Z, et al. Association between the mannose--binding lectin (MBL)-2 gene variants and serum MBL with pulmonary tuberculosis: An update meta-analysis and systematic review. Microb Pathog 2019; 132 : 374–380.
24. Gardner OK, Haynes K, Schweitzer D, et al. Familial recurrence of 3MC syndrome in consanguineous families: A clinical and molecular diagnostic approach with review of the literature. Cleft Palate Craniofac J 2017; 54 (6): 739–748.
25. Schlapbach LJ, Aebi C, Otth M, et al. Deficiency of mannose--binding lectin-associated serine protease-2 associated with increased risk of fever and neutropenia in pediatric cancer patients. Pediatr Infect Dis J 2007; 26 (11): 989–994.
26. Troldborg A, Steffensen R, Trendelenburg M, et al. Ficolin-3 deficiency is associated with disease and an increased risk of systemic lupus erythematosus. J Clin Immunol 2019; 39 (4): 421-429.
27. Lewis LA, Ram S. Meningococcal disease and the complement system. Virulence 2014; 5 (1): 98–126.
28. Ekdahl KN, Persson B, Mohlin C, et al. Interpretation of serological complement biomarkers in disease. Front Immunol 2018; 9 : 2237.
29. West CD, Witte DP, McAdams AJ. Composition of nephritic factor-generated glomerular deposits in membranoproliferative glomerulonephritis type 2. Am J Kidney Dis 2001; 37 (6): 1120–1130.
30. Misra A, Peethambaram A, Garg A. Clinical features and metabolic and autoimmune derangements in acquired partial lipodystrophy: report of 35 cases and review of the literature. Medicine (Baltimore) 2004; 83 (1): 18–34.
31. Castelli R, Zanichelli A, Cicardi M, Cugno M. Acquired C1-inhibitor deficiency and lymphoproliferative disorders: a tight relationship. Crit Rev Oncol Hematol 2013; 87 (3): 323–332.
32. Guo WY, Song D, Liu XR, et al. Immunological features and functional analysis of anti-CFH autoantibodies in patients with atypical hemolytic uremic syndrome. Pediatr Nephrol 2019; 34 (2): 269–281.
33. Turley AJ, Gathmann B, Bangs C, et al. Spectrum and management of complement immunodeficiencies (excluding hereditary angioedema) across Europe. J Clin Immunol 2015; 35 (2): 199–205.
Štítky
Neonatologie Pediatrie Praktické lékařství pro děti a dorost
Článek vyšel v časopiseČesko-slovenská pediatrie
Nejčtenější tento týden
2021 Číslo 4- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Stillova choroba: vzácné a závažné systémové onemocnění
-
Všechny články tohoto čísla
- EDITORIAL Vrodené poruchy imunity – najväčší učitelia modernej imunológie
- Ťažká kombinovaná imunodeficiencia v súbore pacientov liečených v Národnom ústave detských chorôb
- Kombinované imunodeficience spojené se syndromickými příznaky
- Kongenitálne neutropénie v detskom veku
- Komplementový systém I: vrozené poruchy komplementové kaskády vyjma hereditárního angioedému
- Vrozené poruchy komplementu II. – hereditární angioedém
- Autoinflamačné ochorenia v klinickej praxi pediatra – kazuistická séria
- Ako hľadali názov choroby. Münchhausenov syndróm
- MUDr. Pavel Frühauf, CSc., emeritní primář, sedmdesátníkem
- Česko-slovenská pediatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Autoinflamačné ochorenia v klinickej praxi pediatra – kazuistická séria
- MUDr. Pavel Frühauf, CSc., emeritní primář, sedmdesátníkem
- Kongenitálne neutropénie v detskom veku
- Komplementový systém I: vrozené poruchy komplementové kaskády vyjma hereditárního angioedému
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



