-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaNeinvazivní ventilace
Non-invasive ventilation
The paper describes the history and the present of non-invasive ventilation, the therapeutic method which plays an essential role in the therapy of acute as well as chronic respiratory illnesses. It focuses on indications and contraindications, adverse effects as well as some pitfalls of this therapy.
Key words:
non-invasive ventilation (NIV) – respiratory insufficiency
Autoři: David Havel; Jan Zeman
Působiště autorů: Klinika pneumologie a ftizeologie LF UK a FN Plzeň
Vyšlo v časopise: Vnitř Lék 2017; 63(11): 908-915
Kategorie: Přehledné referáty
Souhrn
Článek pojednává o historii i současnosti neinvazivní ventilace, léčebné metody, která hraje podstatnou roli v terapii akutních i chronických respiračních onemocnění. Zabývá se indikacemi a kontraindikacemi, nežádoucími účinky i některými nástrahami této léčby.
Klíčová slova:
neinvazivní ventilace (NIV) – respirační insuficienceÚvod
Termín „neinvazivní ventilace“ (NIV) zahrnuje všechny typy umělé plicní ventilace, při kterém nejsou dýchací cesty zajištěny endotracheální či tracheostomickou kanylou ani laryngeální maskou. Obvykle je chápána jako přetlaková ventilační léčba, ačkoliv je v současnosti možné využít i formy zevní podtlakové či kombinované ventilace.
NIV umožňuje podpořit či do určité míry zastoupit nedostatečnou činnost respiračního systému jako celku. Umožňuje splnit fyziologické i klinické cíle umělé plicní ventilace při redukci rizik spojených s invazivní plicní ventilací. Je určitou „přemosťující metodou“ mezi oxygenoterapií a invazivní plicní ventilací.
Je ale zároveň metodou přinášející specifická úskalí a rizika pro pacienty a do určité míry i pro personál. Její kvalitní aplikace proto vyžaduje erudovaný zdravotnický tým, nároky klade také na ventilovaného pacienta.
Historie
I dýchání z úst do úst je vlastně formou neinvazivní ventilační podpory směsí vzduchu se sníženou frakcí kyslíku. Z tohoto pohledu je možné nalézt nejstarší písemné zmínky již ve staroegyptských textech či v bibli. Existuje záznam z roku 1744 o oživení horníka, který byl apnoický a bez hmatného pulzu, pomocí dýchání z úst do úst [1].
Za tvůrce prvního automatizovaného neinvazivního ventilátoru může být považován Heinrich Dräger, který v roce 1907 patentoval Pulmotor, přístroj schopný pomocí obdoby hodinového strojku automaticky cyklovat inspirium a exspirium a prodechovat pacienty pomocí obličejové masky [2,3]. V počátku 20. století se přetlaková ventilační podpora vyvíjela zejména v leteckém průmyslu, a to především v souvislosti s oběma světovými válkami [4]. S tím souvisí fakt, že jedna z prvních klinických prací zabývajících se využitím neinvazivní ventilace u akutního respiračního selhání se objevila v roce 1940 v časopise o letecké medicíně [5]. S rozvojem podtlakové tankové ventilace (železné plíce) a zejména invazivní ventilace od 50. let 20. století došlo k omezení zájmu o přetlakovou neinvazivní ventilaci. Metoda nezanikla, byla v akutní péči poměrně široce užívána, ovšem nekontrolovaně, bez výraznějších pravidel a zpětné vazby [6].
Další rozvoj neinvazivní ventilace souvisel s více faktory: s rozvojem jednotek intenzivní péče, s vývojem nových typů ventilátorů, s rozvojem diagnostiky (analýza krevních plynů) a s rozšířením znalostí o nežádoucích účincích ventilace invazivní. V 70. letech 20. století se začaly objevovat první prospektivní studie zabývající se nežádoucími účinky invazivní plicní ventilace [7] a zajištění dýchacích cest [8].
V 80. letech 20. století se přetlaková terapie začíná v širším měřítku využívat v terapii chronických respiračních onemocnění. Objevují se práce o významném efektu neinvazivní ventilace na spánkovou respirační nedostatečnost u neuromuskulárních onemocnění [9]. Prof. Sullivan sestrojil s využitím motoru z vysavače CPAP (continuous positive airway pressure, viz níže) a publikoval první zkušenosti s využitím přístroje v léčbě poruch dýchání ve spánku [10], následovalo využití objemově řízené neinvazivní ventilace pozitivním přetlakem v chronické léčbě nemocných s neuromuskulárním onemocněním [11]. V roce 1992 si (ve snaze vylepšit CPAP) firma Respironics patentuje termín „BiPAP“ pro dvouúrovňovou neinvazivní ventilační tlakovou podporu u pacientů se spánkovou apnoí (číslo patentu US5433193 A). S určitým časovým odstupem si tento přístroj začíná razit cestu i mimo oblast spánkové medicíny a nalézá široké uplatnění. Od 90. let minulého století se tedy rozvíjí historie moderní neinvazivní ventilace (CPAP z let 80. minulého století také dosáhl celosvětového úspěchu, nejedná se ale o formu neinvazivní ventilace, pacienty neventiluje).
Postupně se zkušenosti s přetlakovou terapií začínají spojovat do multicentrických klinických studií, které umožňují nastolit určitá pravidla v léčbě touto modalitou. Vznikají první metaanalýzy a klinická doporučení.
Stále ale probíhá další vývoj metodiky, hledají se nová klinická využití, zdokonalují se přístroje i cesty, jak přenést přetlak z okruhu ventilátoru do dýchacích cest při minimalizaci mrtvého prostoru, redukovat asynchronní interakci pacient-ventilátor, minimalizovat diskomfort nemocného a zabránit nežádoucím účinkům. Toto se promítá do současných guidelines neinvazivní ventilace.
Vysvětlení základních termínů a zkratek
Terminologie neinvazivní ventilace a užívané zkratky nejsou celosvětově sjednocené, do určité míry mohou být termíny matoucí. Proto poskytujeme přehled užívaných zkratek a termínů.
NIV – neinvazivní ventilace – obecně se jedná o všechny formy ventilační podpory bez invazivního zajištění dýchacích cest. Protože existuje i marginálně využívaná možnost podtlakové či bifázické ventilace (ventilace pomocí plastového kyrysu, umožňující mezi kyrysem a hrudní stěnou vytvořit podtlak i přetlak, obr. 1), užívá se někdy pro přetlakovou neinvazivní ventilaci termín NIPPV (non-invasive positive pressure ventilation, neinvazivní ventilace pozitivním tlakem). Zavádějící ale je, že stejnou zkratku NIPPV bývá v literatuře označována nosní intermitentní ventilace pozitivním tlakem (nasal intermittent positive pressure ventilation).
Obr. 1. Bifázická kyrysová ventilace 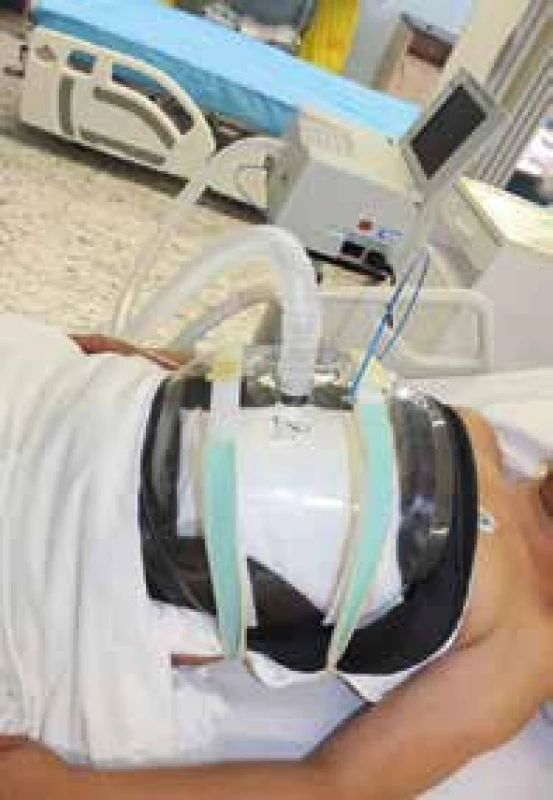
V současné době bývá v doporučeních britských, amerických či německých užíván pro neinvazivní ventilaci přetlakem pouze termín NIV [12–14] (s případnou poznámkou, že jiné než přetlakové formy neinvazivní ventilace nejsou příliš využívány), v jiných případech je volena zkratka NPPV (noninvasive positive-pressure ventilation) [15]. Pro potřeby naší práce bude dále v souvislosti s neinvazivní ventilací volena zkratka NIV.
Ventilátory pro NIV jsou téměř výhradně řízeny tlakově (tedy nastavením hodnoty inspiračního tlaku), nikoliv objemově (nastavení cílového dechového objemu). Kromě ventilace podpůrné (pacient ventiluje spontánně, přístroj mu vypomáhá v inspiriu) lze využít i ventilaci plně či částečně řízenou (fixně nastavená dechová frekvence přístrojem) [16].
IMV – invazivní mechanická ventilace. Tento termín budeme používat pro „konvenční“ umělou plicní ventilaci, při které jsou zajištěny dýchací cesty. Vyhneme se tak termínu umělá plicní ventilace (UPV), který považujeme za nadřazený pojem, pod který spadají podskupiny NIV a IMV.
CPAP – aplikace kontinuálního přetlaku. Nejedná se o formu neinvazivní ventilace, neboť touto formou přetlakové léčby pacient není ventilován, dýchá spontánně. Kontinuální přetlak pomáhá vytlačovat (vymývat) vydechovaný vzduch z oblasti masky, dilatuje horní cesty dýchací (využití u spánkové apnoe), může příznivě působit na velké dolní cesty dýchací (např. u syndromu nadměrného dynamického kolapsu dýchacích cest, tzv. EDAC syndromu) i na malé cesty dýchací včetně plicních alveolů a plicní intersticium (plicní edém).
PSV – pressure support ventilation – tlaková podpůrná ventilace, při které pacient spouští (triggeruje) všechny dechy. Ventilátor musí rozpoznat pacientovo inspirium a exspirium a podřídit mu tlakovou podporu.
Bi-PAP – aplikace dvouúrovňového tlaku (bi-level positive airway pressure, dvouúrovňový pozitivní tlak v dýchacích cestách). V literatuře se můžeme také setkat se zkratkami BiPAP (patentovaný nález) a BPAP. V závislosti na typu používaného přístroje se můžeme setkat i s jinými názvy. Princip je ale vždy obdobný:
Nižší (exspirační) tlak (označovaný jako EPAP či Pe) je aplikován v průběhu výdechu, jedná se o obdobu termínu PEEP (pozitivní end-exspirační tlak) užívaného v terminologii IMV. Hodnota Pe nesmí být příliš vysoká, aby se nezvyšovala zátěž respiračních svalů usilovným výdechem.
Vyšší (inspirační) tlaková hladina (Pi) funguje jako inspirační ventilační podpora. V optimálním případě dokáže přístroj detekovat fáze dechového cyklu nemocného a v inspiriu vypomoci pomocí Pi. Pokud tomu tak není, hrozí rozvoj asynchronie mezi pacientem a ventilátorem, která je jedním z rizikových faktorů selhání neinvazivní ventilace.
Ventilátory obvykle umožňují nastavit základní počet mandatorních dechů (a fungovat tak v režimu tzv. zástupové ventilace). Pacienti by pomocí NIV ve většině případů neměli být řízeně ventilováni, protože spontánní dechová aktivita je jednou z podmínek NIV. Existují ale situace, v nichž i řízenou ventilaci lze přechodně využít (např. vyčerpaný pacient s velmi nízkými dechovými objemy, u kterého je rozhodnuto, že z důvodu terminálního onemocnění nebude intubován).
PAV – proporcionální asistovaná ventilace – s pacientovým dechovým cyklem synchronizovaná částečná ventilační podpora. Ventilátor generuje tlak odpovídající pacientovu úsilí (čím víc musí pacient „zabrat“ respiračními svaly, tím větší je tlaková podpora) [17].
AVAPS – average volume assured pressure support – novější ventilační režim tlakové podpory se zaručeným průměrným dechovým objemem. Nastavíme cílový dechový objem a rozmezí maximálního a minimálního inspiračního tlaku, přístroj si v rámci tohoto rozmezí dopočítává optimální tlak k dosažení nastaveného dechového objemu.
Přístroj dedikovaný pro NIV – speciální ventilátor určený primárně pro neinvazivní ventilaci (obr. 2). „Klasické“ ventilátory pro IMV fungují pomocí uzavřeného okruhu, který je pro neinvazivní ventilaci méně výhodný. Zejména starší typy tolerují nižší úniky vzduchu z okruhu a detekce pacientova úsilí je méně citlivá, je vyšší riziko rozvoje respirační dyssynchronie mezi pacientem a ventilátorem [19–21]. Dle nastavení přístroje a použitého instrumentária existuje i riziko zpětného vdechování oxidu uhličitého.
Obr. 2. Ventilátor dedikovaný pro NIV s jednocestným okruhem a oronazální maskou 
Přístroje dedikované k NIV obvykle obsahují turbínu, schopnou rychlých tlakových změn, a pracují na principu úniku vzduchu ze systému: jejich součástí je otevřený okruh. Dýchací hadice vede přes masku k pacientovi. Vydechovaný vzduch uniká přímo maskou či speciálním kolénkem před maskou.
Britské standardy péče pro léčbu hyperkapnického respiračního selhání z roku 2016 [16] jsou prvními doporučeními, podle kterých mají být k neinvazivní ventilaci využity pouze pro NIV dedikované přístroje. Lze předpokládat, že s aktualizací doporučených postupů v dalších zemích se s tímto pravidlem budeme setkávat častěji.
Propojení mezi přístrojem a nemocným
Pod tímto kostrbatým názvem (v anglické literatuře se používá termín „interface“) se v intenzivní péči obvykle ukrývají helmy či masky. Všechny naše alternativy jsou:
- nazální maska
- oronazální maska
- celoobličejová (total-face) maska
- helma
- nosní špunty
- náustek
Nejčastěji jsou využívané oronazální (někdy nazývané full-face) masky (obr. 3).
Obr. 3. Oronazální maska, v oranžovém kolénku je umístěn exspirační port 
Jedná se o masky překrývající pouze ústa a nos. Jejich výhodou je malý mrtvý prostor mezi maskou a obličejem a možnost dobrého utěsnění masky k obličeji, obvykle se jedná o první volbu. Nevýhodou je, že nemocní nemohou mluvit, zhoršuje se i možnost kašle, maska může způsobovat anxiózní reakce. Maska naléhá na obličej mj. v oblasti kořene nosu, kde svým tlakem může při dlouhodobějším užívání narušovat kontinuitu kůže.
Nazální maska překrývá pouze nos. Je samozřejmě nutná jeho průchodnost. Pacient má volná ústa, může mluvit, kašlat. Masku lze využívat u přístrojů umožňující vyšší úniky vzduchu ze systému. Nazální maska může být výhodná v situaci, kdy nemocný z důvodu klaustrofobie jiný typ masky odmítá.
Výhodou celoobličejové (total-face) masky je, že netlačí na oblast kořene nosu, nýbrž po obvodu obličeje. Je indikována např. v situaci, kdy se na kořeni nosu rozvíjí oděrka od oronazální masky. Nevýhodou je větší mrtvý prostor mezi maskou a obličejem.
Stejně tak s helmou nehrozí poškození kořene nosu, pacient navíc může lépe mluvit. Nevýhodou je nutnost vyššího proudění vzduchu a vysoká hladina hluku přenášeného z ventilátoru [22].
Nosní špunty a náústky se v akutní péči prakticky nepoužívají.
Masky se liší podle typu okruhu. Máme-li otevřený, jednocestný okruh, je zásadní vědět, kde se nachází exspirační port: obvykle na masce či na kolénku před maskou (typ kolénka je někdy možné měnit dle úrovně hyperkapnie). Naopak, pokud ventilujeme uzavřeným okruhem, využívají se masky uzavřené, tedy bez exspiračního portu.
Bylo by velmi zásadní chybou propojit jednocestný okruh s uzavřenou maskou, takto může dojít k poškození pacienta (nedocházelo by k dostatečnému úniku vzduchu z okruhu). Personál pečující o nemocného na NIV si musí být vědom přesné funkce okruhu a masky, musí být schopen identifikovat, kudy bude vzduch během ventilace proudit.
Vyšetření krevních plynů
SpO2 – saturace hemoglobinu tepenné krve kyslíkem, měřená pulzním oxymetrem.
SaO2 – saturace hemoglobinu tepenné krve kyslíkem, měřená (resp. dopočtená) přístrojem pro analýzu krevních plynů.
paO2 – parciální tlak kyslíku v tepenné krvi.
paCO2 – parciální tlak oxidu uhličitého v tepenné krvi.
Smysl neinvazivní ventilace
Jakákoliv ventilační podpora je indikována v léčbě či prevenci respirační nedostatečnosti, tedy v situaci, v níž výměna krevních plynů (O2, CO2) v plicích nepostačuje metabolickým nárokům organizmu. Rozeznáváme respirační selhání akutní, chronické a akutně zhoršené chronické. Zásadní je dále dělení na hypoxemické a hyperkapnické respirační selhání.
Při hypoxemickém respiračním selhání dochází k poklesu hodnoty paO2 a SpO2, hodnota paCO2 se nezvyšuje (naopak vlivem kompenzatorní hyperventilace obvykle v akutní fázi klesá). Nejčastějšími mechanizmy vedoucími k hypoxemii jsou nepoměr ventilace a perfuze určité části plic a plicní zkrat.
Hyperkapnické respirační selhání je způsobeno především hypoventilací. Je charakterizováno kombinací hypoxemie a hyperkapnie a v případě akutní hyperkapnické poruchy respirační acidózou.
Invazivní plicní ventilace je v řadě indikací nezastupitelná, je ale spojena s řadou potenciálních nežádoucích účinků plynoucích z této metodiky. Stále se rozšiřují naše poznatky o ventilátorem indukovaném plicním postižení, roli hraje také přítomnost cizího tělesa (endotracheální rourka) v dolních cestách dýchacích, sedace, nemožnost adekvátního perorálního příjmu, snížená možnost rehabilitace, snížená efektivita kašle, riziko rozvoje deliria, atrofie a dysfunkce respiračních svalů při vleklejší invazivní ventilaci a další.
Neinvazivní ventilace podporuje funkci respiračního systému při redukci těchto komplikací. Současná doporučení NIV [13–15,23] vycházejí z randomizovaných kontrolovaných studií prokazujících, že neinvazivní ventilace snižuje dušnost a zlepšuje výměnu plynů. U dobře vybraných pacientů s akutním i chronickým respiračním selháním redukuje mortalitu, snižuje potřebu invazivní ventilace, zkracuje délku pobytu na jednotce intenzivní péče i v nemocnici.
Neinvazivní ventilace je schopna korigovat hyperkapnii, respirační acidózu i hypoxemii. Tím, že ventilátor částečně převezme práci, kterou musel pacient vynakládat na dechové úsilí, dochází k úlevě přetížených respiračních svalů. Tím dochází k redukci spotřeby kyslíku a k snížení produkce oxidu uhličitého respiračními svaly.
Vzhledem k tomu, že pro aplikaci NIV není nutná relaxace či analgosedace, je přípustné ji využít dle klinického stavu nemocného také mimo jednotky intenzivní péče. NIV se v posledních letech používá v péči přednemocniční, na odděleních urgentního příjmu, ale i v chronické domácí péči.
Je určitým paradoxem, že v situaci, kdy prakticky každá lékařská intervence vyžaduje důkladné poučení pacienta se sepsáním informovaného souhlasu, bývá IMV často indikována bez poskytnutí adekvátních informací nemocnému a bez jeho zapojení do rozhodovacího procesu [24]. NIV může pomoci „získat čas“ a adekvátně informovat pacienta o jeho onemocnění a léčebných možnostech.
Indikace NIV
Při léčbě akutního respiračního selhání (či dekompenzovaného chronického) lze obecně vycházet z postupného navyšování péče ve smyslu: oxygenoterapie – vysokoprůtoková oxygenoterapie – NIV – IMV – extrakorporální membránová oxygenoterapie. Již při přijetí pacienta je proto vhodné (je-li to možné) adekvátně kategorizovat maximální péči. V tomto směru může mít zásadní význam kvalita života nemocného, která by vždy měla být zmíněna v anamnéze, důležité je také pacientovo přání a pochopitelně celkový klinický stav a očekávatelné přežití.
Vzhledem k rizikovosti invazivní ventilace doporučují např. německé guidelines [14] vyhnout se IMV kdykoliv to je možné a využít NIV či časnou extubaci. Je ale nutné, abychom si byli vědomi limitací NIV (IMV např. umožňuje konzistentnější udržení tlaků v dýchacích cestách, což může být zásadní např. v léčbě akutního respiračního distress syndromu). Jiná guidelines [13,15,23] jsou konzervativnější a doporučují využití NIV v situacích:
- hyperkapnické respirační selhání s poklesem pH tepenné krve pod 7,35; zejména při exacerbaci chronické obstrukční plicní nemoci, deformitách hrudní stěny či neuromuskulárních onemocněních, nověji také při exacerbaci bronchiálního astmatu spojené s respirační acidózou, či obezitě s hypoventilací
- hypoxemické respirační selhání při plicním edému (zejména kardiogenním), zde nebyly doposud prokázány statisticky významné rozdíly mezi léčbou pomocí CPAP a NIV, lze použít obě metody
- časná extubace (zejména) pacientů s exacerbací chronické obstrukční plicní nemoci léčených IMV
- paliativní péče – využití NIV jako „stropové“ terapie v případě rozhodnutí terapii dále neeskalovat
Řada dalších indikací je pak považována za sporné (je vyšší riziko komplikací NIV), patří sem např. pacienti s pneumoniemi včetně pneumonií imunokompromitovaných, exacerbace bronchiálního astmatu spojená s hypoxemií, pooperační stavy, traumata hrudníku a další. Neinvazivní ventilaci je v těchto případech možno poskytnout pouze, je-li možné pacienta adekvátně monitorovat a pokud je v péči náležitě erudovaného zdravotnického týmu schopného promptního převodu na IMV.
Mezi nové indikace NIV patří některé intervenční výkony. Zde můžeme jmenovat zejména bronchoskopické vyšetření, které je možno pomocí NIV a specializovaného adaptéru provést i u nemocných s těžším respiračním selháním. Obdobně lze NIV využít např. u jícnové echokardiografie [25].
Objevují se kazuistiky demonstrující bezpečné užití NIV při respiračním selhání v těhotenství [26].
Specifickou problematikou je pak využití dlouhodobé domácí NIV u pacientů s poruchou dýchání ve spánku či s chronickým hyperkapnickým respiračním selháním.
Kontraindikace NIV
Mezi nejčastěji uváděnými kontraindikacemi jsou:
- zástava dýchání, gasping
- kóma
- těžká hemodynamická instabilita (kariogenní šok, akutní infarkt myokardu)
- těžká hypoxemie či acidóza
- neléčený tenzní pneumotorax
- nemožnost nasadit masku (traumata obličeje, stav po operaci obličeje)
- těžká agitovanost, delirium
- anatomická či funkční obstrukce velkých dýchacích cest
- nitrolební hypertenze
- aktivní hemoptýza
- vysoké riziko aspirace žaludečního obsahu: výrazná nauzea, vomitus; neošetřená tracheoezofageální píštěl; recentní operace jícnu
- odmítnutí léčby pacientem
Většina kontraindikací je relativní.
V posledních letech je patrný posun ve vnímání NIV v hraničních situacích. Dříve bylo doporučováno aplikovat NIV pouze, neklesne-li pH pod 7,26. Dle současných doporučení není těžká acidóza sama o sobě kontraindikací NIV, je-li pacient hospitalizován na pracovišti s personálem, schopným zajistit bezpečnou endotracheální intubaci. Co se týče poruchy vědomí či agitovanosti, je-li příčinou hyperkapnické respirační selhání, často se setkáváme se situacemi, kdy se pacient prudce vylepší již po několika minutách léčby NIV a je proto možné (vhodné) NIV využít [27]. Pociťuje-li nemocný nauzeu, je vhodné použít masku, kterou lze ihned sejmout, případně použít masku nosní. V indikovaných případech je doporučeno zavést nazogastrickou sondu, máme k dispozici adaptéry, které se umístí do oblasti kontaktu sondy s maskou, čímž redukujeme úniky vzduchu z okruhu.
Dříve se mezi kontraindikacemi objevovala extrémní obezita, ta je v současné době, jako závažný rizikový faktor poruch dýchání ve spánku a hyperkapnie, naopak jednou z indikací.
Nežádoucí účinky NIV a jejich řešení
Selhání neinvazivní ventilace
Selhání NIV je definováno nutností orotracheální intubace a IMV, či úmrtím pacienta [28]. Prolongovaná aplikace NIV v situaci, kdy dochází k selhání této metodiky, vede k zvýšenému riziku komplikací včetně mortality.
Selhání neinvazivní ventilace je vhodné rozlišit na bezprostřední (do 1 hod), časné (1–48 hod) a pozdní (více než 48 hod od zahájení NIV) [29].
Mezi příčinami bezprostředního selhání NIV hraje významnou roli dyssynchronie mezi pacientem a ventilátorem, tedy situace, kdy přístroj není schopen detekovat pacientovy spontánní nádechy a nedochází k adekvátnímu triggerování (spuštění) inspirační podpory a k cyklování ventilace dle potřeb nemocného. Pacient s ventilační podporou „bojuje“, ventilace ztrácí na efektivitě. Jedním ze základních úkolů ošetřujícího personálu je včasně detekovat negativní interakce mezi pacientem a ventilátorem a pokusit se o úpravu situace. Ve snaze snížit riziko dyssynchronie byly vyvinuty nové systémy (Auto-Trak) a ventilační mody (PAV), riziko je nižší při použití ventilátoru dedikovaného k NIV. Z dalších příčin bezprostředního selhání NIV je možno jmenovat excesivní zahlenění s neschopností odkašlat či závažnou poruchu vědomí.
Časné selhání NIV bývá spojováno mimo jiné s těžším průběhem akutního onemocnění (nepříznivé hodnoty skórovacích systémů kritického stavu).
Pozdní selhání NIV lze očekávat např. v případě funkční limitace (vyčerpaný, polymorbidní nemocný).
K selhání neinvazivní ventilace docházelo asi u 16 % pacientů [30]. V praxi by nás spíše než tento literární údaj mělo zajímat, proč NIV selhala u konkrétního pacienta. Je vhodné vést si interní přehled o počtu selhání NIV a o příčinách, mezi kterými může být nevhodně zvolený ventilátor či okruh včetně masky a nevhodné nastavení přístroje pro daného nemocného.
Je zapotřebí včasně zareagovat na hrozící selhání NIV a buďto adekvátně upravit NIV (kontrola systému včetně okruhu a masky, výměna masky, minimalizace úniků vzduchu, úprava tlakové podpory, šetrná sedace agitovaného pacienta, adekvátní diagnostika a korekce např. antibiotické terapie), nebo bez odkladů přikročit k intubaci a IMV. Protahováním neefektivní NIV bychom zhoršili prognózu nemocného a postupovali tak non-lege artis. Výjimku tvoří situace, v níž bylo předem rozhodnuto, že pacient (např. z důvodu terminální fáze chronického onemocnění) nebude intubován. Pak je možné využít NIV k tlumení dyspnoe.
Komplikace spojené s přetlakem v dýchacích cestách
Působení tlaku na dýchací cesty je někdy spojeno s nepohodlím, bolestmi (uši, paranazální dutiny). Vzácně bývá uváděna možnost dilatace jícnového svěrače s insuflací vzduchu do žaludku. Obávanou komplikací u nemocných s preexistujícím srdečním postižením je ovlivnění srdečního výdeje snížením pre-loadu vlivem zvýšeného nitrohrudního tlaku. Raritně bývá popisována možnost pneumotoraxu.
Řešením přetlakových komplikací může být snížení tlakové ventilační podpory, je-li to možné. Dojde-li k rozvoji pneumotoraxu, je (při nutnosti ventilační podpory) obvykle nutná urgentní hrudní drenáž.
V posledních letech se ale ukazuje, že i užití vyšších inspiračních tlaků (překračujících 20 cm vodního sloupce) je pravděpodobně bezpečné. Jasné doporučení pro maximální inspirační tlaky (na rozdíl od IMV) v oblasti NIV nemáme. Existuje poměrně široce uznávaný koncept „high-intensity NIV“ (použití inspiračních tlaků 20–30 cm vodního sloupce, případně i s vyšší mandatorní dechovou frekvencí) v chronické (domácí) terapii stabilizované chronické obstrukční plicní nemoci spojené s hyperkapnií [31].
Komplikace spojené s prouděním vzduchu
Proudění vzduchu horními dýchacími cestami může způsobovat např. otok nosní sliznice, při netěsnosti masky se může rozvíjet konjunktivitida. V případě obtíží s nosní sliznicí lze situaci řešit aplikací dekongestiv. Dochází-li k rozvoji konjunktivitidy, je zásadní pokusit se upravit masku, pomocí které aplikujeme přetlak, tak, aby pacientovi optimálně „seděla“ a nedocházelo k proudění vzduchu do oblasti očí.
NIV je považována za „kapénky generující proceduru“, kapénky unikající kolem masky či exspiračním postem mohou představovat riziko pro personál či ostatní pacienty. V případě neinvazivní ventilace pacientů s infekčními onemocněními přenášenými kapénkami (chřipka, tuberkulóza) je na místě využití adekvátních bariérových opatření.
Riziko pneumonie
Pneumonie je obávanou komplikací invazivní ventilace. Ve srovnání s touto metodikou NIV signifikantně redukuje riziko pneumonie [30], ve srovnání se standardní léčbou (oxygenoterapie) je výskyt pneumonií při NIV mírně vyšší. Zásadní je adekvátní péče o dýchací cesty: mukolytika, bronchodilatancia a zejména dechová rehabilitace s důrazem na odstraňování bronchiálních sekretů (kašel, rehabilitační pomůcky sloužící k mobilizaci hlenu z dolních cest dýchacích). Některá doporučení [16] zmiňují možnost zavedení minitracheostomie k odsávání bronchiálních sekretů u pacientů se špatným kašlacím reflexem či s bronchiální hypersekrecí.
Komplikace spojené s maskou
Jde o relativně časté komplikace. Aby bylo možné působit na dýchací cesty přetlakem, musí být maska, kterou je přetlak aplikován, fixována na obličeji popruhy. To může být spojeno s nepohodlím, projevy strachu, klaustrofobie. V místě, ve kterém maska přiléhá ke kůži, může vznikat enantém, otlaky, někdy i hlubší kožní léze. Řešením je adekvátní prevence dekubitů v této oblasti (existují pěnové podložky, hydrokoloidy či gelové podložky), případně střídání typů masky. Velmi důležité je nepřehánět to s utažením masky k obličeji. Je vhodné držet se tzv. pravidla dvou prstů (pod popruhy masky bychom měli být schopni vsunout volně 2 prsty), obr. 4 a obr. 5.
Obr. 4. Prevence otlaku na kořeni nosu pomocí antidekubitální náplasti 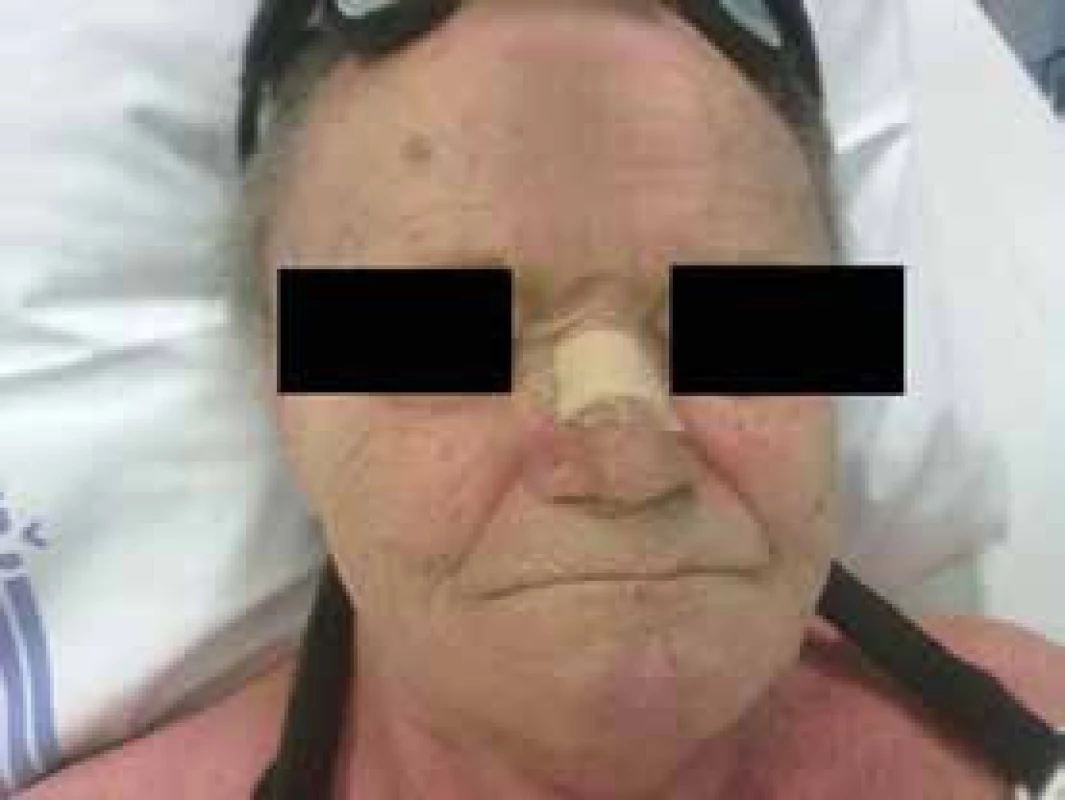
Obr. 5. Prevence otlaků způsobených maskou pomocí molitanové podložky (červená šipka) 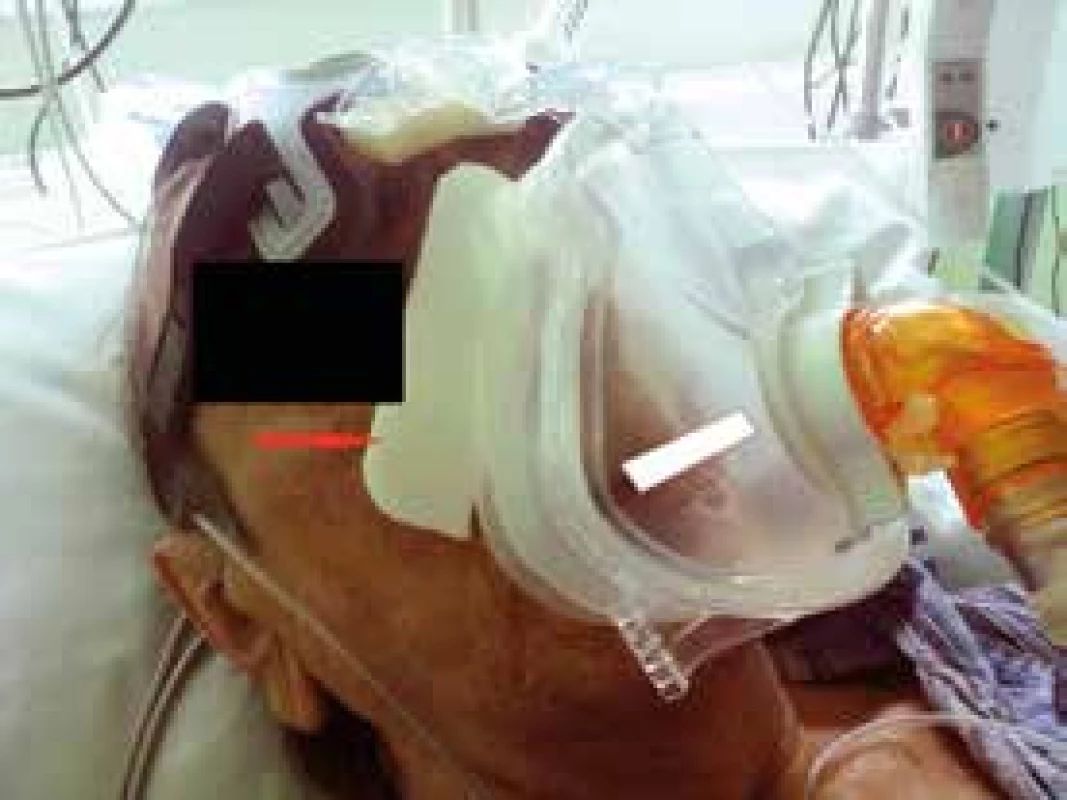
Pacient při plném vědomí
Jak již bylo výše uvedeno, to, že nemocného nesedujeme (respektive sedujeme minimálně), je spojeno s řadou výhod. Zároveň je ale nutné uvědomit si nevýhody z toho plynoucí: je obtížnější provádět některé intervence (zejména odběr biologického materiálu z dolních cest dýchacích, ale také např. kanylace centrálních žil či arterie, zavedení nazogastrické sondy), zejména střední zdravotnický personál je často vystaven stresu při péči o kriticky stonajícího nemocného, který je vystrašený, někdy omezeně spolupracující, ale při vědomí a často s velmi dobrou svalovou silou.
Případy z praxe
Hypoxemické respirační selhání, pneumonie
27letá doposud nestonající pacientka byla přijata pro oboustrannou komunitní pneumonii (obr. 6). Přes úvodní léčbu (empiricky antibiotika, podpůrná léčba včetně oxygenoterapie) progredovalo respirační selhání, SpO2 poklesla pod 85 %, rozvinuly se tachypnoe 30–40 dechů za minutu, neklid, těžká dušnost.
Obr. 6. CT vyšetření: oboustranné plicní infiltráty s negativním bronchogramem u pacientky s oboustrannou komunitní pneumonií 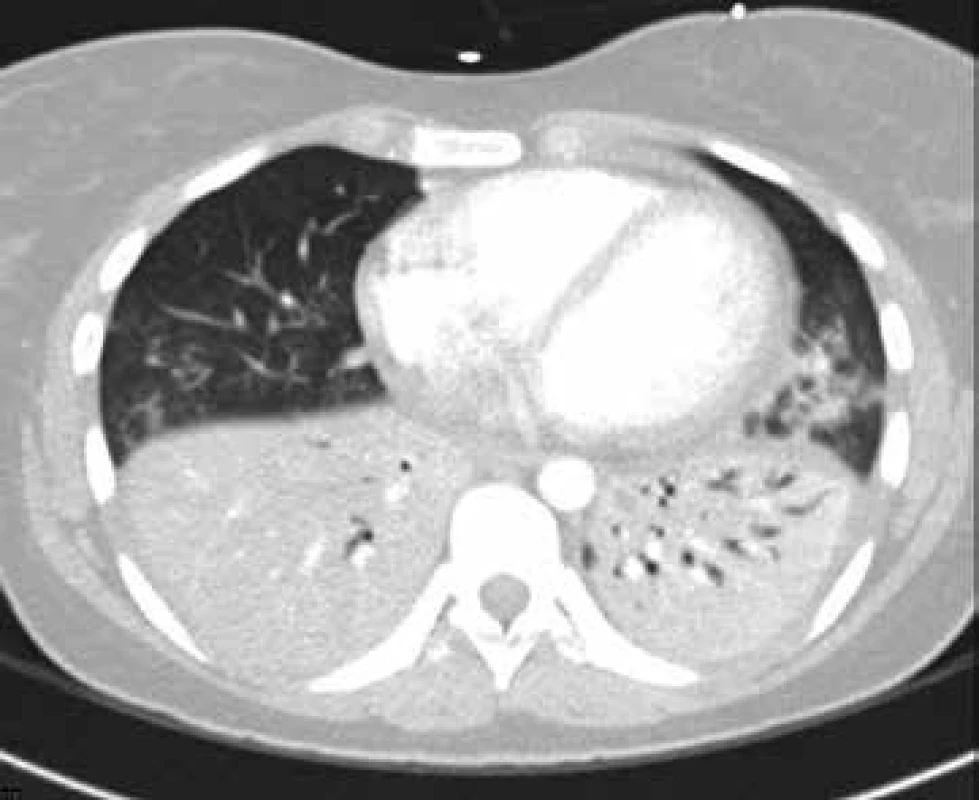
Nemocnou jsme po poučení o léčebných modalitách napojili na neinvazivní ventilátor a podali jí nízkou dávku morfinu. Zároveň byly učiněny přípravy k případnému zajištění dýchacích cest orotracheální intubací a zahájení invazivní ventilace (příprava instrumentária). Tato alternativa by byla zvolena, pokud by v řádu desítek minut nebylo patrné zlepšení.
Ventilace byla zahájena oronazální maskou, s inspiračními tlaky 11 a exspiračními 8 cm vodního sloupce, s vyšší frakcí kyslíku (50 %) – neinvazivní ventilátor nám tak do určité míry suploval vysokoprůtokovou oxygenoterapii.
Průběh byl příznivý, došlo k promptnímu zlepšení SpO2 na hodnoty přes 94 %, upravila se mechanika dýchání. Zafungovala antibiotika, neinvazivní ventilační podporu bylo možno po asi 24 hod intermitentní aplikace vysadit. Po 12 dnech hospitalizace byla nemocná v dobrém stavu dimitována do ambulantní péče.
Užití neinvazivní ventilace v případě hypoxemie při pneumonii může vzbuzovat kontroverzi, nejedná se o široce přijímanou indikaci NIV. Je ale přípustné efekt NIV vyzkoušet za situace, v níž je k dispozici tým s extenzivními zkušenostmi a adekvátním přístrojovým vybavením. Zásadní chybou by bylo neinvazivní ventilaci neúměrně protahovat v situaci, ve které by nedošlo k adekvátnímu zlepšení stav nemocné.
Extrémní respirační nedostatečnost
48letá pacientka s ACOS syndromem (overlap chronické obstrukční plicní nemoci a bronchiálního astmatu) byla přijata na naši kliniku pro hyperkapnické respirační selhání při exacerbaci svého chronického onemocnění během respiračního infektu.
Vstupně byla přítomna extrémní hypoxemie – paO2 byl 2,5 kPa, s odpovídající SpO2 23 %, paCO2 8,9 kPa, pH 7,29. Hodnota laktátu byla v normě (1,3 mmol/l), pacientka byla při vědomí, schopna komunikace. I přes extrémní hypoxemii byla s ohledem na klinický stav napojena na neinvazivní ventilaci (oronazální maska, tlaky 18/8 cm H2O), zahájena běžná farmakoterapie. V řádu desítek vteřin došlo k prudkému vzestupu SpO2 nad 80 %, došlo k příznivé úpravě dechového vzorce. Stav se dále zlepšoval, pacientka byla po zaléčení dimitována do ambulantní péče bez dechové nedostatečnosti.
Tento případ ilustruje nutnost individuálního přístupu k nemocným. Ani přítomnost těžkého respiračního selhání nemusí být indikací k okamžité IMV. U hyperkapnických pacientů může být s výhodou provedení testu NIV, v případě pozitivní odpovědi na přetlakovou léčbu je možné se IMV vyhnout. Týká se to zejména pacientů trpících chronickou pneumopatií, kteří jsou na své onemocnění adaptováni. Často vídáme stavy spojené s hlubokou hypoxemií, ale nikoliv s tkáňovou hypoxií. Lidský organizmus má mnoho cest, jak se s nízkou tenzí kyslíku vyrovnat, od těch obecně známých (redistribuce plicní perfuze, produkce erytropoetinu a další) až po úrovně genetické a molekulární [32]. Naši nemocní relativně často vykazují vstupně obdobné hodnoty paO2 jako horolezci pod vrcholem Mt. Everest [33]. Precizní kontrola oxygenace [34] se stanovením optimální spodní, ale i horní hranice SpO2 je jednou ze zásad současné léčby hyperkapnických pacientů.
Těžká acidóza
71letý kuřák s pokročilou (až terminální) chronickou obstrukční plicní nemocí se špatnou kvalitou života (chronická dušnost, špatná tolerance i lehčí zátěže) byl přijat pro exacerbaci a kardiální dekompenzaci. Vstupně byl v těžké respirační acidóze s pH tepenné krve 7,06 při paCO2 16,3 kPa, paO2 10,9 kPa (vliv oxygenoterapie, na které byl transportován na naši jednotku intenzivní péče). Byl spavý, ale na oslovení reagoval, jednoslovně odpovídal. Byla zahájena komplexní terapie včetně neinvazivní ventilace s vysokou diferencí mezi inspirační a exspirační tlakovou podporou (tlaky 20/5 cm H2O).
Od napojení na NIV byl patrný příznivý trend se zlepšením klinického stavu a pozvolnou úpravou pH (na 7,25 týž den, 7,34 druhý den, 7,38 třetí den hospitalizace). Po 21 dnech pobytu na jednotce intenzivní péče a asi týdnu pobytu na standardním oddělení byl nemocný dimitován do domácí péče. Pro perzistující metabolicky kompenzovanou hyperkapnii bude ambulantně zaveden na domácí neinvazivní ventilaci.
Pacient by s ohledem na špatnou kvalitu života nebyl indikován k IMV, sám případnou intubaci odmítal. Neinvazivní ventilaci lze v takovém případě považovat za léčbu maximální. Vždy při dimisi pacienta s perzistující hyperkapnií by měla být zvážena dlouhodobá neinvazivní ventilace [23]. V některých případech je zavedení na domácí NIV nutné v rámci hospitalizace po akutním stavu, aby vůbec byla dimise možná.
MUDr. David Havel
haveld@fnplzen.cz
Klinika pneumologie a ftizeologie LF UK a
FN Plzeň
www.fnplzen.cz
Doručeno do redakce 30. 8. 2017
Přijato po recenzi 26. 9. 2017
Zdroje
1. Fothergill J. Observations of a case published in the last volume of the medical essays of recovering a man dead in appearance, by distending the lungs with air. Phil Trans 1744–1745; 43(472–477): 275–281. Dostupné z WWW: <http://rstl.royalsocietypublishing.org/content/43/472–477/275.full.pdf+html>
2. Hess D, MacIntyre N. History of the Respiratory Care Profession. In: Hess D, MacIntyre N, Galvin WF. Respiratory Care: Principles and Practice. 3rd ed. Jones & Bartlett Learning 2015. ISBN-13: 978–1284050004.
3. Bahns E. It began with the Pulmotor – The History of Mechanical Ventilation. Dostupné z WWW: <https://www.draeger.com/Library/Content/pulmotor-bk-9097434-en.pdf>. [07.2017].
4. Sweeting G. Combat Flying Equipment: US Army Aviators’ Personal Equipment, 1917–1945. Reissue ed. Smithsonian: Washington DC 1994. ISBN 978–1560985020.
5. Motley HL, Werko L et al. Observations on the clinical use of intermittent positive pressure. J Aviation Med 1947; 18(5): 417–435.
6. Pierson DJ History and Epidemiology of Noninvasive Ventilation in the Acute-Care Setting. Respir Care 2009; 54(1): 40–50.
7. Zwillich CW, Pierson DJ, Creagh CE et al. Complications of assisted ventilation: a prospective study of 354 consecutive episodes. Am J Med 1974; 57(2): 161–170.
8. Stauffer J, Silvestri RC. Complications of endotracheal intubation, tracheostomy, and artifical airways. Respir Care 1982; 27 : 417–434.
9. Braun NM. Nocturnal ventilation--a new method. Am Rev Respir Dis. 1987; 135(3): 523–524.
10. Sullivan CE, Issa FG, Berthon-Jones M et al. Reversal of obstructive sleep apnoea by continuous positive airway pressure applied through the nares. Lancet 1981; 1(8225): 862–865.
11. Ellis ER, Bye PT, Brudere JW et al. Treatment of respiratory failure during sleep in patients with neuromuscular disease. Positive-pressure ventilation through a nose mask. Am Rev Respir Dis 1987; 135 : 148–152.
12. Schmidt GA, Girard TD, Kress JP et al. Official Executive Summary of an American Thoracic Society/American College of Chest Physicians Clinical Practice Guideline: Liberation from Mechanical Ventilation in Critically Ill Adults . Am J Respir Crit Care Med 2017; 195(1):115–119. Dostupné z DOI: <http://dx.doi.org/10.1164/rccm.201610–2076ST>.
13. [British Thoracic Society Standards of Care Committee]. Non-invasive ventilation in acute respiratory failure. Thorax 2002; 57(3): 192–211.
14. Schonhofer B, Kuhlen R, Neumann P et al. Clinical Practice Guideline: Non-Invasive Mechanical Ventilation as Treatment of Acute Respiratory Failure. Dtsch Arztebl Int 2008; 105(24): 424–433. Dostupné z DOI: <http://dx.doi.org/10.3238/arztebl.2008.0424>.
15. Keenan SP, Sinuff T,a Burns KE et al. A Clinical practice guidelines for the use of noninvasive positive-pressure ventilation and noninvasive continuous positive airway pressure in the acute care setting. CMAJ 2011; 183(3): E195-E214. Dostupné z DOI: <http://dx.doi.org/10.1503/cmaj.100071>.
16. Davidson AC, Banham S, Elliott M et al. [BTS Standards of Care Committee Member, British Thoracic Society/Intensive Care Society Acute Hypercapnic Respiratory Failure Guideline Development Group, British Thoracic Society Standards of Care Committee]. BTS/ICS guideline for the ventilatory management of acute hypercapnicrespiratory failure in adults. Thorax 2016; 71(Suppl 2): ii1–35. Dostupné z DOI: <http://dx.doi.org/10.1136/thoraxjnl-2015–208209>.
17. Ambrosino N, Rossi A. Proportional assist ventilation (PAV): a significant advance or a futile struggle between logic and practice? Thorax 2002; 57(3): 272–276.
18. Schettino GP, Tucci MR, Sousa R et al. Mask mechanics and leak dynamics during noninvasive pressure support ventilation: a bench study. Intensive Care Med 2001; 27(12): 1887–1891.
19. Thille AW, Lyazidi A, Richard JC et al. A bench study of intensive-care-unit ventilators: new versus old and turbine-based versus compressed gas-based ventilators. Intensive Care Med 2009; 35(8): 1368–1376. Dostupné z DOI: <http://dx.doi.org/10.1007/s00134–009–1467–7>.
20. Vignaux I, Tassaux D, Carteaux G Performance of noninvasive ventilation algorithms on ICU ventilators during pressure support: a clinical study. Intensive Care Med 2010; 36(12): 2053–2059. Dostupné z DOI: <http://dx.doi.org/10.1007/s00134–010–1994–2>.
21. Oliveri C, Costa R, Conti G et al. Bench studies evaluating devices for non-invasive ventilation: critical analysis and future perspectives. Intensive Care Med 2012; 38(1): 160–167. <http://dx.doi.org/10.1007/s00134–011–2416–9>.
22. Brill AK. How to avoid interface problems in acute noninvasive ventilation. Breathe 2014; 10(3): 230–242. Dostupné z DOI: <http://dx.doi.org/10.1183/20734735.003414>.
23. Koblížek V, Chlumský J, Zindr V. Doporučený postup ČPFS pro diagnostiku a léčbu stabilní CHOPN (Revize květen 2016). Dostupné z WWW: <http://www.pneumologie.cz/guidelines/>.
24. Ngandu H, Gale N, Hopkinson JB. Experiences of noninvasive ventilation in adults with hypercapnic respiratory failure: a review of evidence. Eur Respir Rev 2016; 25(142): 451–471. Dostupné z DOI: <http://dx.doi.org/10.1183/16000617.0002–2016>.
25. Ambrosino N, Guarracino F. Unusual applications of non‐invasive ventilation. Eur Respir J 2011; 38(2): 440–449. <http://dx.doi.org/10.1183/09031936.00192810>.
26. Allred CC, Esquinas AM, Caronia J et al. Successful use of noninvasive ventilation in pregnancy. Eur Respir Rev 2014; 23(131): 142–144. Dostupné z DOI: <http://dx.doi.org/10.1183/09059180.00008113>.
27. Diaz GG, Alcaraz AC, Talavera JC et al. Noninvasive positive-pressure ventilation to treat hypercapnic coma secondary to respiratory failure. Chest 2005; 127(3): 952–960.
28. Moretti M, Cilione C, Tampieri A Incidence and causes of non-invasive mechanical ventilation failure after initial succes. Thorax 2000; 55(10): 819–825.
29. Ozyilmaz E, Ugurlu AO, Nava S. Timing of noninvasive ventilation failure: causes, risk factors, and potential remedies. BMC Pulmonary Medicine 2014; 14 : 19. Dostupné z DOI: <http://dx.doi.org/10.1186/1471–2466–14–19>.
30. Carron M, Freo U, BaHammam AS et al. Complications of non-invasive ventilation techniques: a comprehensive qualitative review of randomized trials. Br J Anaesth 2013; 110(6): 896–914. Dostupné z DOI: <http://dx.doi.org/10.1093/bja/aet070>.
31. Dreher M, Storre JH, Schmoor C et al. High-intensity versus low-intensity non-invasive ventilation in patients with stable hypercapnic COPD: a randomised crossover trial. Thorax 2010; 65(4): 303–308. <http://dx.doi.org/10.1136/thx.2009.124263>.
32. Wenger RH. Cellular adaptation to hypoxia: O2-sensing protein hydroxylases, hypoxia-inducible transcription factors, and O2-regulated gene expression. FASEB J 2002; 16(10): 1151–1162.
33. Grocott MPW, Martin DS, Levett DZ et al. Arterial Blood Gases and Oxygen Content in Climbers on Mount Everest. N Engl J Med 2009; 360(2):140–149. Dostupné z DOI: <http://dx.doi.org/10.1056/NEJMoa0801581>.
34. Martin DS, Grocott MP. Oxygen Therapy in Critical Illness: Precise Control of Arterial Oxygenation and Permissive Hypoxemia. Crit Care Med 2013; 41(2): 423–432. Dostupné z DOI: <http://dx.doi.org/10.1097/CCM.0b013e31826a44f6>.
35. Roberts M, Young K, Plant P et al. The Use of Non-Invasive Ventilation in the management of patients with chronic obstructive pulmonary disease admitted to hospital with acute type II respiratory failure (With particular reference to Bilevel positive pressure ventilation). Concise Guidance to Good Practice series, No 11. London RCP 2008. Dostupné z WWW: <https://www.brit-thoracic.org.uk/document-library/clinical-information/niv/niv-guidelines/btsrcpics-guideline-on-niv-in-copd/>.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek Současná náplň pneumologieČlánek Nozokomiální pneumonieČlánek Cystická fibróza dospělýchČlánek Nemalobuněčný karcinom plic
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2017 Číslo 11- S MUDr. Štěpánem Budkou o rizicích obezity pro fertilitu ze všech úhlů pohledu
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
-
Všechny články tohoto čísla
- Současná náplň pneumologie
- Cílené vyhledávání nemocných s chronickou obstrukční plicní nemocí: stručný přehled
- Asthma bronchiale v kontextu vnitřního lékařství
- Diagnostika a léčba komunitní pneumonie – v jednoduchosti je klíč k úspěchu
- Nozokomiální pneumonie
- Pneumonie u imunokompromitovaných
- Idiopatická plicní fibróza. Umíme ji vždy správně diagnostikovat a léčit?
- Exogenní alergické alveolitidy: minimum pro praxi
- Sarkoidóza – nadále záhadné onemocnění
- Současný přístup k diagnostice, léčbě a prevenci tuberkulózy
-
Non-CF bronchiektázie dospělých: stručný přehled pro praxi
Dokument Sekce chorob s bronchiální obstrukcí České pneumologické a ftizeologické společnosti České lékařské společnosti J. E. Purkyně - Cystická fibróza dospělých
- Kardiovaskulární riziko spánkové apnoe a kazuistika
- Komplikace po transplantaci plic
- Nemalobuněčný karcinom plic
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
- Maligní mezoteliom pleury – dosud nepokořený nádor
- Spirometrie – základní vyšetření funkce plic
- Postavení bronchologie v pneumologické diagnostice
- Ultrasonografické vyšetření hrudníku v rukou lékaře klinika
- Neinvazivní ventilace
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Spirometrie – základní vyšetření funkce plic
- Neinvazivní ventilace
- Pneumonie u imunokompromitovaných
- Malobuněčný karcinom plic: epidemiologie, diagnostika a léčba
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



