-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Zpráva z konference Eurofora 2013
Autoři: M. Ghazal
Vyšlo v časopise: Urol List 2013; 11(4): 49-57
Itálie, Milano, 13.–14. září 2013
Letošní konference Eurofora se konala v historickém severoitalském městě Milánu, ve dnech 13.–14. září 2013. Toto druhé největší italské město, hlavní město oblasti Lombardie a provincie Milano, je slavné jako město obchodu, bank a módy, stejně jako sídlo opery La Scala a fotbalových klubů AC a Inter Milán. Je zde také velká gotická katedrála a řada dalších památek. Město se nachází v nížině v západní části Lombardie. Je i důležitým centrem lékařského a biotechnologického výzkumu. Samotná konference se konala v hotelu Marriott, což je známý a prestižní hotel, který obsahuje 22 prostorných konferenčních místností o celkové rozloze 2300 m2. Ty jsou dostatečné pro pořádání akcí s vysokými požadavky na multimediální zabezpečení.
Tuto akci hostila a pořádala společnost Eli Lilly, která je 10. největší farmaceutickou společností na světě. Klinický výzkum této firmy se provádí ve více než 55 zemích. Dále pak výzkum a vývoj zařízení se nachází v osmi zemích. Výrobní závody se nacházejí v 13 zemích a výrobky jsou uváděné na trh ve 125 zemích.
Titulem tohoto setkání je Mirroring advances and controversies in urology, challenging treatment decisions – Zrcadlení pokroků a sporů v urologii, náročné rozhodování o léčbě. Zaměřením letošního setkání byl přenos nových poznatků z různých urologických oblastí do každodenní praxe. V následujícím textu přinášíme některé informace a problematiku, která se týká oblasti onkologie, benigní prostatické hyperplazie a operačních technologií a postupů, erektilní dysfunkce a kardiovaskulárních nemocí.
- testikulární nemoci – aktualizované diagnostické a terapeutické guidelines pro neseminomové a seminomové nádory varlat,
- mužské LUTS – sexuální dysfunkce a komorbidity související s mužským LUTS, současné možnosti léčby pro muže s LUTS a vliv na kvalitu sexuálního života, jejich míru a individuální možnosti léčby stratifikované dle komorbidit a potřeby pacientů,
- sexuální výsledky po prostatektomii – kritická analýza různých operačních přístupů k léčbě lokalizovaného karcinomu prostaty se zvláštním zaměřením na onkologické a funkční výsledky,
- kardiovaskulární onemocnění – souvislost s erektilní dysfunkcí, erektilní funkce jako významný marker tichého kardiovaskulárního onemocnění, praktické guidelines pro rizika, stratifikované vyšetření a léčbu.
Přednášky byly doplněny interaktivními diskusemi o případech z každodenní praxe.
Vedoucí vědeckého výboru a prezident konference profesor Hartmut Porst vedl setkání vynikajícím způsobem s dokonalou organizací a profesionální úrovní. H. Porst je vedoucí soukromého ústavu urologie a andrologie v Hamburgu, Německo, docent urologie ve fakultní nemocnici v Bonnu a současně prezident Evropské společnosti sexuální medicíny. Jako autor přispěl do více než 35 knih a publikoval více než 300 původních prací v odborných časopisech.
Testikulární nemoci
1. Nádory varlat – co je nového v roce 2013
prof. Dr. H. Von der Maase, Dánsko
Léčebné postupy a obecné možnosti léčby počátečních a pozdních stadií seminomů a non seminomů, přednáška zejména projednala problematiku týkající se léčebného postupu počátečních stadií (early stage) nádorů po orchiektomii.
Obecné informace
Nádorová onemocnění varlat jsou nejčastější malignitou mužů mezi 15.–35. rokem. Incidence nádorů varlat je 3/100 000 obyvatel. Nejvíce postiženi jsou běloši v Evropě a Severní Americe, zatímco u černochů a v Asii jde o onemocnění poměrně řídce se vyskytující. Výjimku tvoří Maorové na Novém Zélandu, kde jde naopak o onemocnění dominující [1]. Více než 90 % testikulárních germinálních nádorů pochází z transformované zárodečné buňky. Poměrně zřídka se vyskytují před pubertou. Tyto nádory nevznikají transformací zárodečného epitelu, ale již intrauterinně, jako důsledek hormonálních vlivů. Jde především o nádory ze žloutkového váčku a zralý teratom. Rizikovými faktory pro vznik testikulárních germinálních nádorů jsou především kryptorchismus, ingvinální hernioplastika, orchitida po pubertě a úrazy varlete. Rovněž předčasná puberta a předčasný začátek sexuální aktivity u chlapců má vliv na vznik testikulárních germinálních nádorů. Také infertilita je rizikovým faktorem, protože zpětnou vazbou zvýšená produkce gonadotropinů, působící na menší počet spermatogonií, může vést až k rozvoji nádoru. Zvýšená hladina FSH po provedené orchiektomii představuje rovněž velké riziko pro vznik nádoru ve druhém varleti [2]. Histologická klasifikace z roku 1997 rozděluje nádory varlat do tří základních skupin [3]:
- carcinoma in situ,
- nádory jednoho histologického typu,
- nádory více histologických typů.
Do 2. skupiny patří největší množství testikulárních germinálních nádorů jako seminomy, embryonální karcinom, nádor ze žloutkového váčku, trofoblastické nádory a teratomy. Pro klinickou praxi je poměrně rozšířené ne zcela přesné rozdělení na seminomy, neseminomy a nádory smíšené.
- seminomy – vycházejí z částečně diferencovaných buněk semenotvorných kanálků,
- neseminomy – odvozené od pluripotentní zárodečné buňky nebo od částečně diferencovaných buněk.
Histopatologická klasifikace:
- seminom 26,9 %,
- embryokarcinom 3,1 %,
- teratom 2,7 %,
- choriokarcinom 0,03 %,
- yolk sac tumor 2,4 %,
- nádory smíšené z jednotlivých forem.
Velmi důležité pro diagnostiku a monitorování léčby testikulárních germinálních nádorů je zjištění přítomnosti a hladiny nádorových markerů [1]. Nejčastěji používanými nádorovými markery pro testikulární nádory jsou: AFP (alfafetoprotein), LDH (laktátdehydrogenáza), beta HCG (beta choriový gonadotropin), PLAP (placentární alkalická fosfatáza) a CEA (karcinoembryonální antigen).
Nejčastějším klinickým příznakem nádorového onemocnění varlete je jeho nebolestivé zvětšení. Pouze asi v 10 % případů je vznik nádoru provázen bolestí jako důsledkem krvácení v nádoru, infarktu ve varleti, torzí nádorově změněného varlete nebo i sekundárně vzniklou epididymitidou.
Diagnostický algoritmus:
- zjištění anamnézy a provedení fyzikálního vyšetření,
- odběr krve na stanovení nádorových markerů,
- ultrasonografické vyšetření varlat,
- RTG vyšetření plic,
- počítačová tomografie (CT) plic a retroperitonea.
Základním operačním postupem je provedení radikální ingvinální orchiektomie, s primárním podvazem funiculus spermaticus, který zabraňuje nádorové krevní diseminaci [1]. Následně provedení CT retroperitonea v případě nutnosti i CT plic. Podle získaných údajů stanovíme klasifikaci nemoci podle TNM klasifikace (WHO 1997). Pro přehlednost se v léčbě testikulárních germinálních nádorů používá zařazení nemocných do klinických stadií, např. podle Fraleyho [1].
Klinické stadium
I – nádor je omezen na varle
II A – postižení regionálních uzlin do 2 cm
II B – postižení regionálních uzlin do 5 cm
II C – paket regionálních uzlin
II S – vysoká hladina nádorových markerů
III – generalizace
Léčebné možnosti
Surveillance (aktivní sledování)
Radioterapie
Chemoterapie
Seminomy
Stadium I: ingvinální orchiektomie s následnou radioterapií (ozáření ipsilaterálních paraaortálních a pánevních uzlin do výše úponu bránice Th 10–11).
Stadium II A, B: ingvinální orchiektomie s následnou radioterapií (ozáření oboustranných paraaortálních a pánevních uzlin do výše úponu bránice Th 10–11).
Stadium II C, III: ingvinální orchiektomie s následnou chemoterapií, dále na oblast rezidua, eventuálně i radioterapie.
Neseminomy
Stadium I:
- ingvinální orchiektomie s následnou chemoterapií,
- ingvinální orchiektomie s retroperitoneální lymfadenektomií.
Stadium II A,B,C:
- ingvinální orchiektomie s retroperitoneální lymfadenektomií následovaná chemoterapií,
- ingvinální orchiektomie s následnou chemoterapií a eventuálně retroperitoneální lymfadenektomií při reziduu po chemoterapii.
Stadium III: chemoterapie v případě reziduálního nádoru. Po skončené chemoterapii následná resekce reziduálních mas.
Prognóza
Rozlišujeme následující prognostické faktory:
- vaskulární invaze,
- přítomnost histologicky specifikované neseminomové složky,
- pokročilý lokální nález (pT v rámci histologické klasifikace rozsahu nádoru),
- předoperační zvýšení markerů.
Prof. Von der Maase ve své přednášce hovořil o léčebném postupu a o obecných možnostech léčby počátečních, pozdních stadií seminomů a non seminomů, o tom, jak může nízká dávka radioterapie a optimální pole pomoci léčit nádor u pacienta po orchiektomii. Zdůraznil a rozvedl problematiku komplikace radioterapie a vznik recidivy primárního nádoru v 4–5 % po 5–13 letech. Přednáška byla obzvláště o možnostech léčby v počínající fázi. Autor preferuje pouze sledovaní „active surveillance“ těchto nádorů. Proběhly dvě studie (Mortensen MS et al, ASCO 2013 Abstract [4], Daugaard et al), prozkoumaly výsledek aktivního sledování v časných stadiích seminomu a non seminomu po orchiektomii.
Mortensen MS et al., ASCO 2013 studie (A nationwide cohort study of surveillance for stage I seminoma)
Od roku 1984 byla hlavní strategií léčby prvního stupně seminomu u pacientů v Dánsku orchiektomie, poté sledování. Pacienti ve stadiu I seminomu mají tumory, které jsou lokalizované pouze na varle a jsou bez známek klinického či biochemického diseminovaného onemocnění. Sledovací program sestával z klinických návštěv, CT/RTG snímků a vyšetření tumor markerů za 5 let. Cílem studie bylo zhodnotit strategii dánského sledování v celostátní kohortové studii.
Metody
- pacienti s diagnózou seminomu I. stadia v Dánsku 1984–2008,
- data byla shromážděna ze souboru pacientů z různých registrů,
- byly analyzovány údaje o výsledku, relapsech a léčbě recidiv a příčinách smrti,
- byla provedena analýza prognostických faktorů,
- údaje shromážděné až do prosince 2012.
Výsledky
- bylo zařazeno 1822 pacientů ve stadiu I seminomu,
- medián doby sledování: 15,4 roku (0–28 roků),
- bylo pozorováno 355 recidiv (19,5 %)
- pouze 10 pacientů (0,55 %) zemřelo na tumor či v souvislosti s léčbou,
- průměrná doba recidivy: 13,7 měsíce (1,2–173,3 měsíce),
- v 72,4 % (257) došlo k relapsu během prvních 2 let,
- v 20,3 % (72) došlo k relapsu během roku 2 až 5,
- v 7,3 % (26) došlo k relapsu po 5 letech sledování.
Prognostické faktory k relapsu
- velikost nádoru > 4 cm,
- cévní invaze,
- HCG > 200 IU/L
Obě studie dospěly k závěru, že u seminomů 15 let tumor free byl v 99,5 % a u non seminomů v 99 %.
Závěr: 80 % pacientů bylo ušetřeno zbytečné léčby po orchiektomii. Aktivní sledování je bezpečná volba pro stadium I seminomů a non seminomů.
2. Benigní onemocnění varlat – akutní stavy v každodenní praxi
Dr. I. Eardley, Velká Británie
Torze varlete
Torze varlete je superakutní stav, vyvolaný otočením varlete kolem cévní stopky a strangulací přívodných tepen (obr. 1). Při úplném zaškrcení cév v chámovodu vzniká ischemie a následná nekróza při částečné infarzaci. Aby mohlo dojít k záchraně varlete, musí být stav vyřešen do šesti hodin od vzniku potíží. Torze je způsobena silnou kontrakcí musculus cremaster. K torzi predisponuje delší a volnější cévní stopka, kryptorchismus, široká tunica vaginalis, dlouhé mezorchium, chabý závěsný aparát varlete na tunica dartos.
Obr. 1. Torze varlete. Zdroj: Mayo foundation for medical education and research 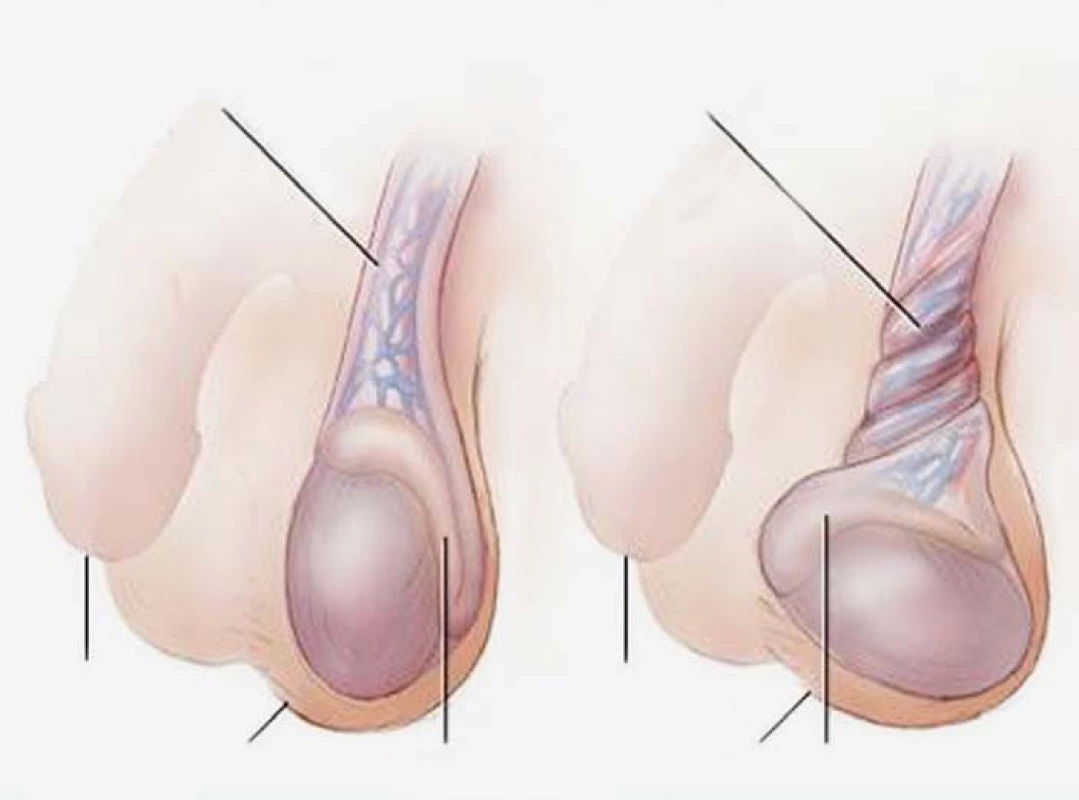
Existují čtyři rudimentární orgány skrota, které se mohou torkvovat:
- appendix testis (Morgagnův klk),
- appendix epididymitis,
- paradidymis (Giraldésův orgán),
- ductuli aberrantes (Hallerův orgán).
První z nich je pozůstatkem kraniální části Műllerova vývodu. Je nejčastější. Vyskytuje se až u 92 % mužů. Druhý je rudimentem vývodu Wolffova. Zbylé dva jsou z kanálků mesonefros [5]. Nejčastější výskyt torzí rudimentárních orgánů je mezi 10.–13. rokem věku, přičemž v 95 % případů se jedná o torzi apendixu varlete [6]. Méně často může dojít i k torzi apendixu nadvarlete [6]. Extrémně vzácně paradidymis či ductuli aberrantes [7,8]. V 9 případech z 10 jde právě o torzi přívěsku a pouze v jednom o torzi semenného provazce [8]. Torze semenného provazce má do 25 let věku incidenci 1 : 4000 [9], i když u nás se zdá být o něco vyšší [8]. V průběhu života muže jsou dvě nejpravděpodobnější období výskytu. Jedním je první rok života a druhým období puberty, po kterém se objevuje již vzácně.
Klinický obraz
Vyskytuje se v každém věku, nejčastěji mezi 10. a 25. rokem života. Maximální doba k záchraně varlete je 4 až 6 hodin. Subjektivně si pacient stěžuje na náhle vzniklou unilaterální orchalgii, propagaci bolesti do třísla, nauzeu. Objektivně pozorujeme oteklé a zarudlé skrotum, zvětšené a bolestivé varle, zvracení, schvácenost, opocení, bledost, neklid pacienta, subfebrilie, ipsilaterální elevaci varlete, negativní Prehnův příznak, nepřítomnost reflexu kremasterického svalu.
Akutní torze varlete vyžaduje k posouzení kvalitní UTZ přístroj s citlivým dopplerovským modulem, většinou se používá modus Power angio či Colour flow Doppler. Pokud je vidět výrazné překrvení varlete (obr. 2), symptomy imituje orchiepididymitida, pokud není prokrvení nalezeno, je vysoce pravděpodobná torze varlete. Colour flow doppler má až 86% citlivost, 100% specificitu a 97% přesnost [10].
Obr. 2. Testikulární UTZ s dopplerem: vpravo normální nález (prokrvení), vlevo torze varlete (není prokrvení). 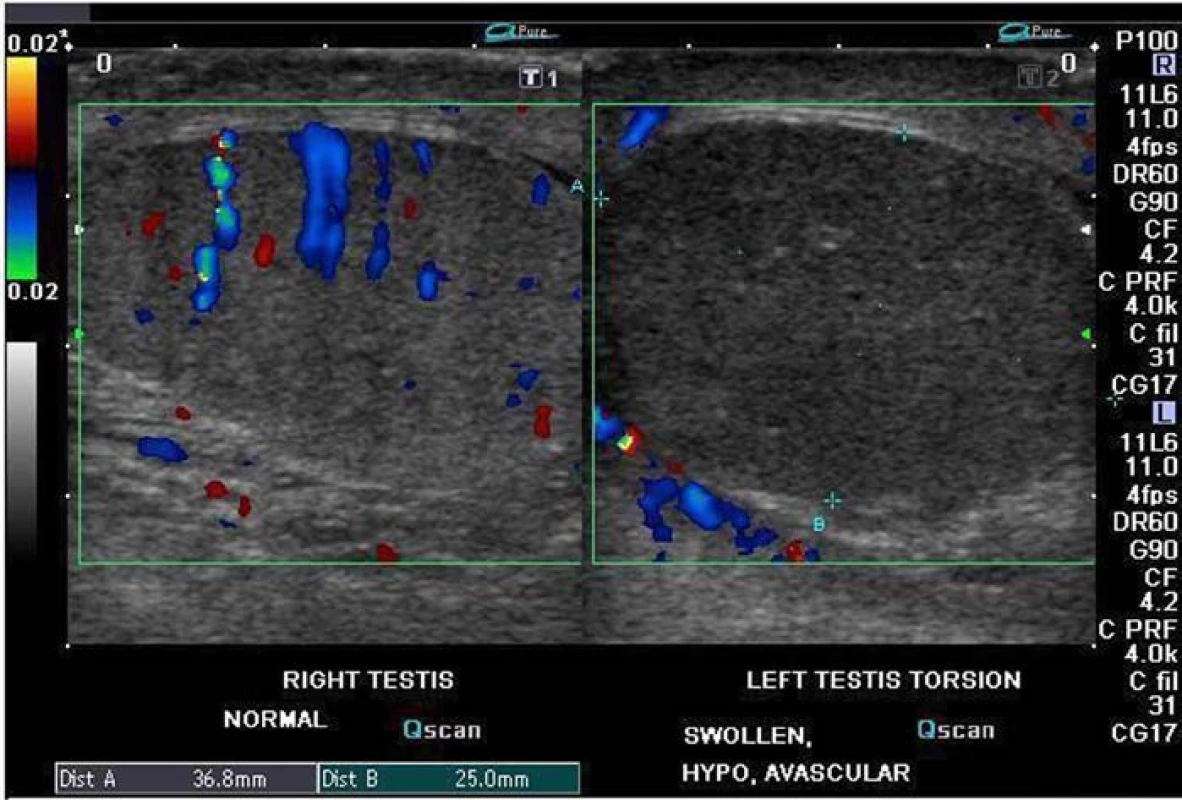
Následně by pacient byl indikován k akutní operační revizi. Vyloučení torze by vždy měl provádět zkušený lékař. Je menší chybou revidovat zbytečně, než když kvůli zanedbané torzi pacient varle ztratí. Orchidopexe je indikována u ipsilaterálního varlete.
Epididymitida
Akutní epididymitida představuje poměrně časté zánětlivé onemocnění. Infekce zasahuje nadvarle převážně ascendentní kanalikulární cestou při močových infekcích. Většinu vyvolavatelů epididymitidy lze rozdělit do dvou skupin. V jedné jsou infekční agens sexuálně přenosných infekcí (Neisseria gonorrhoe, Chlamydia trachomatis), ve druhé ostatní agens vyvolávající prostatitidu, infekce moči při dlouhodobé katetrizaci, po instrumentálních zákrocích, operacích na dolních močových cestách (prostatektomie), či při neléčené BPH, kdy infekce nadvarlete vzniká většinou refluxem infikované moči do vas deferens. Velmi vzácně je nadvarle postiženo krevní nebo lymfatickou cestou při jiném zánětlivém onemocnění nebo po traumatu. Refluxem sterilní moči do vývodu vzniká chemická urinózní epididymitida. Klinicky začíná akutní zánět nadvarlete teplotami, bolestmi ve zvětšeném nadvarleti, které se někdy propagují do třísel a bederní krajiny. Současně bývají symptomy uretritidy nebo prostatitidy. Skrotum na postižené straně bývá zvětšené, edematózní, nadvarle je palpačně zvětšené, tuhé a bolestivé. Při infekci značně virulentním kmenem se může rychle vyvinout abscedující epididymitida. Oboustranný proces vede ke sterilitě. Diferenciálně diagnosticky je nezbytné odlišit torzi varlete.
Ultrazvukový obraz zpočátku detekuje charakteristické edematózní zvětšení nadvarlete s výraznou hypervaskularizací nadvarlete, varlete i obalů. Teprve později dochází k výpadkům prokrvení v dopplerovském mapování, které se může při účinné terapii upravit, nebo dojde k nekróze až formování abscesů v nadvarleti. Později probíhá podobný proces i ve varleti.
Fournierova gangréna
Je to vzácná celulitida a nekrotizující fasciitida neznámé etiologie. Infekce vychází nejčastěji z kůže, močové trubice nebo oblasti rekta. Gangréna je zřejmě podmíněna synergním působením aerobních a anaerobních mikroorganismů (E. coli, Klebsiella, enterokoky – Bacteroides, Fusobacterium, Clostridium). Může se ale také vyskytnout bez jakýchkoli zjevných projevů zánětu nebo poranění. Postiženi jsou obvykle diabetici, alkoholici, nemocní s různým stupněm imunosuprese nebo těžkým celkovým onemocněním. Průběh onemocnění bývá velmi dramatický. Nejprve se objeví zarudnutí skrota s nevelkým otokem. Během 24–48 hodin otok mohutně naroste. V centru zarudnutí se po počáteční necitlivosti (poškození nervových zakončení fasciitidou) objeví žlutočervená tekutina. Takřka před očima kůže s podkožím a svalstvem propadá nekróze. Nekrózy se objevují rychle na různých místech skrota, tkáňové defekty se zvětšují a varlata nakonec zůstávají obnažena. Vzácně se gangréna šíří i na podbřišek nebo stehna. Častěji se šíří na kůži penisu. Nemocný bývá schvácený s vysokou horečkou, třesavkou, tachykardií a hrozí septický šok. U nemocných vyčerpaných základním onemocněním mohou systémové toxické projevy chybět. Mortalita je i při adekvátní léčbě stále vysoká, až 50 %. Léčba vyžaduje akutní chirurgickou revizi, nekrektomii, aplikaci baktericidních antibiotik ve vysokých dávkách, antigangrenózního séra a léčbu systémových projevů toxémie s protišokovým režimem.
3. LUTS/BPH – sexuální dysfunkce a komorbidity související s mužským LUTS
Dr. M. Gacci, Itálie
Úvod
Benigní hyperplazie prostaty (BPH) je zvětšení části prostaty, které může vyvolávat mikční obtíže. Dosud není přesně objasněna etiologie. Pro zvětšení prostaty je nezbytný testosteron a jeho aktivnější metabolit dihydrotestosteron (DHT) spolu s přítomností funkčních receptorů v prostatické tkáni. Nezbytnou podmínkou je androgenní stimulace, která ale není primární příčinou. Ze statistik vyplývá, že 60 % mužů ve věku 60 let má jistý stupeň příznaků z dolních močových cest (LUTS, „lower urinary tract symptoms“) [11]. Závažný stupeň LUTS má 13 % mužů ve věku 40–49 let a více než 28 % nad 70 let [12]. Dr. M. Gacci nejdříve sdělil výsledky jedné studie, která proběhla v USA k posouzení vlivu LUTS na kvalitu života včetně vlivu dalších komorbidit (např. dna, DM, angina pectoris). Studie se účastnilo 8 406 mužů, Dr. Gacci došel k závěru, že tyto nemoci včetně těžkého stupně LUTS mají velký negativní vliv na kvalitu života, a to fyzické funkce, bolest, vitalitu, emociální problémy, mentální problémy a omezení v oblasti sociálních funkcí [13]. BPH/LUTS má velký vliv na zhoršení sexuálních funkcí, může dojít k erektilní dysfunkci u 50 % mužů mezi 50 a 59 lety věku, pacienti se středně těžkým až velmi těžkým LUTS trpí erektilní dysfunkcí. Dále je nutno pomýšlet na metabolický syndrom jako další komorbiditu, která ovlivňuje ED. Mužská sexuální dysfunkce je stav, který souvisí s věkem. Například jedné studie (European Male Ageing Study, EMAS) se účastnilo 3 369 mužů ve věku 40–79 let (průměr 60 ± 11 let), 6 % těchto mužů uvedlo středně těžkou nebo těžkou erektilní dysfunkci (ED) ve svých čtyřiceti letech, podíl stoupá až k 64 % mužů ve věku nad 70 let [14]. Údaje o historii ED ukazují, že roční incidence (nových případů) ED je 1,2 %, 3,0 % a 4,6 % u mužů ve věku 40 až 49 let, 50 až 59 let a 60 až 69 let, resp. ejakulační poruchy (EJD) se také vyskytují více v pokročilém věku [15]. Ve studii skupiny holandských mužů ve věku 50 až 78 let významný podíl EJD vzrostl z 3 % u mužů ve věku 50–54 let na 26 % u mužů ve věku 70–78 let [16]. Jiné studie ukázaly, že věk je predisponující faktor ke snížení ejakulačního objemu a nárůstu anejakulace [17]. Studie za poslední desetiletí prokázaly vztah mezi BHP/LUTS a sexuální dysfunkcí u stárnoucích mužů, která je nezávislá na vlivu věku, ostatních komorbiditách (např. hypertenze, diabetes, dyslipidémie a ischemická choroba srdeční), faktorech životního stylu [18,19]. V jedné takové studii, ve které odpovědělo 4 489 mužů na ED dotazníky a byly hodnoceny mikční symptomy (IPSS), byla celková prevalence ED a LUTS 19,2 % a 31,2 %. Prevalence LUTS u mužů trpících ED byla 72,2 % ve srovnání s 37,7 % u mužů s normální erektilní funkcí (poměr rizik 2,11) [20]. V dalších analýzách bylo zjištěno, že LUTS je rizikový faktor pro ED a je nezávislý na věku. Multinational Survey of the Ageing Male (MSAM-7) je jedna z největších populačních studií stárnoucích mužů. Hodnotila souvislosti mezi věkem, LUTS, doprovodnými komorbiditami a mužskou sexuální dysfunkcí u > 12 000 mužů ve Spojených státech a v Evropě [21]. MSAM-7 došla k závěru, že celková prevalence LUTS byla 90 %, zatímco celková prevalence ED a EJD byla 49 %, resp. 46 % [21]. Míra obou ED a EJD byla významně závislá na věku a úzce koreluje se závažností LUTS (graf 1). Tyto asociace byly nezávislé na jiných faktorech, jako jsou komorbidity a užívání tabáku. Kromě toho, LUTS byla silnějším prediktorem sexuální dysfunkce než diabetes, onemocnění srdce nebo vysoký krevní tlak [21].
Graf 1. Vliv LUTS na erektilní funkci. Zdroj: Int J Clin Pract 2011, Blackwell Publishing 
Inhibitory fosfodiesterázy-5 (PDE5i)
PDE5 inhibitory jsou primární léčebnou volbou pro ED, jsou bezpečné, účinné a snadno se podávají [22]. Mezi třemi běžně předepisovanými perorálními inhibitory PDE5 (sildenafil, tadalafil a vardenafil) je jediný významný rozdíl v trvání účinku tadalafilu – vardenafil a sildenafil mají dobu účinku 4 hodiny, tadalafil je aktivní 36 hodin (T1/2 = 17,5 h). Tadalafil 5 mg je jediný lék schválený pro každodenní podávání při léčbě ED. Počáteční údaje podporují klinický přínos inhibitorů PDE5 k léčbě LUTS při BPH. Čtyři velké, dvojitě zaslepené, placebem kontrolované studie zkoumaly účinnost sildenafilu, tadalafilu a vardenafilu u mužů s LUTS a BPH [23–24]. Všechny studie souhlasně prokázaly, že tato třída léků zlepšuje LUTS u mužů s BPH (tab. 1).
Tab. 1. Randomizované, placebem kontrolované studie s inhibitory PDE5 pro léčbu BPH. 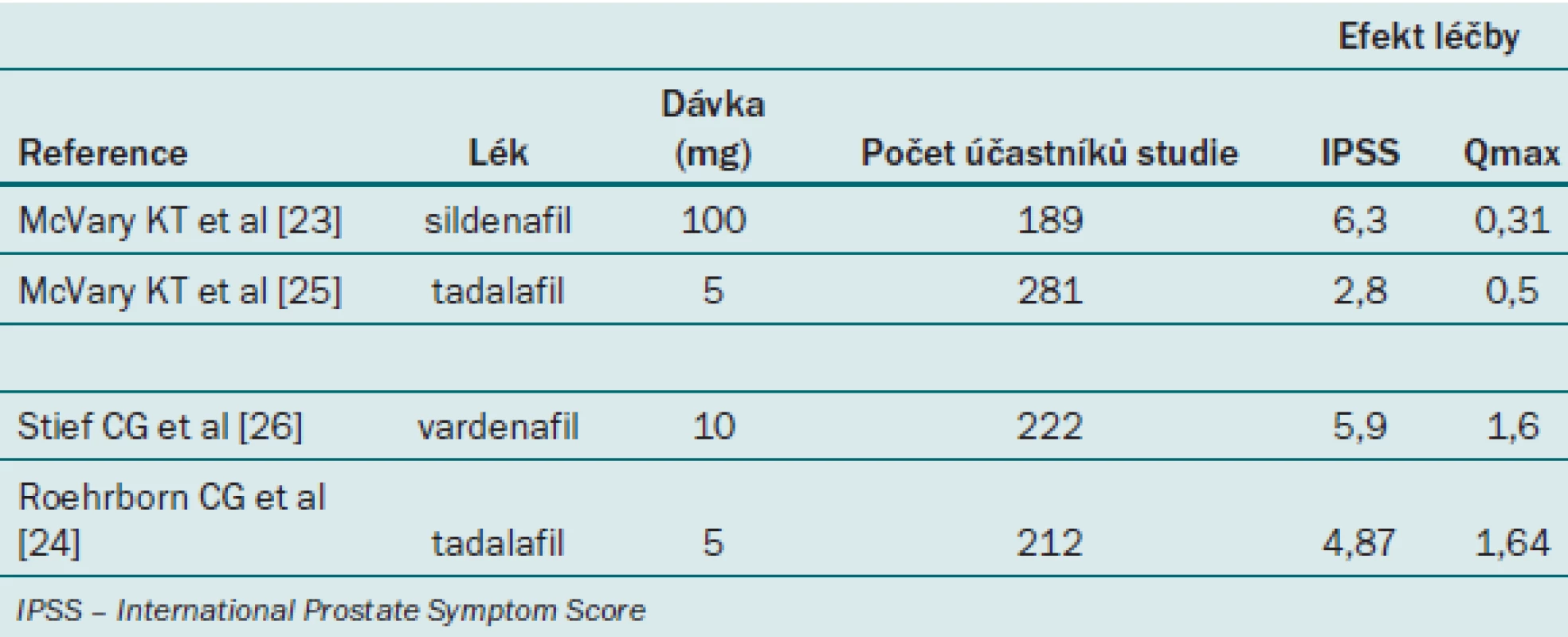
Závěr
Tadalafil snižuje mikční příznaky u pacientů s ED či bez ED. Pouze tadalafil (jednodenní dávka 5 mg) byl schválen v Evropě k léčení pacientů s LUTS. Neexistuje optimální léčba, symptomy jsou různé, každý pacient toleruje příznaky jinak, nutná je ale snaha o maximální spokojenost pacientů, nutno brát v úvahu také náklady léčby a patofyziologii LUTS.
4. Radikální prostatektomie
Různé přístupy, různé výstupy
Dr. J. Stolzenburg, Německo
Operační postupy při radikální prostatektomii (RP):
- otevřená operace,
- laparoskopická operace,
- robotická operace (roboticky asistovaná radikální prostatektomie – RARP).
Otevřenou operaci lze realizovat z retropubického či perineálního přístupu. Retropubická prostatektomie je zlatým standardem v operační léčbě karcinomu prostaty. Výhodou této techniky je její propracovanost, nevýhodou potom větší krevní ztráty během operace a častější výskyt pooperačních komplikací. Výkon předpokládá určité zkušenosti operatéra. Perineální prostatektomie byla historicky první provedenou radikální operací prostaty. Je považována za základní techniku, která byla modifikována v důsledku nových anatomických poznatků. Její hlavní výhodou je lepší přehlednost v oblasti apexu prostaty, kratší rekonvalescence a možnost provedení výkonu u silně obézních pacientů, nevýhodou je nemožnost provedení pánevní lymfadenektomie ze stejného operačního řezu. Laparoskopický přístup může být taktéž dvojí, a to transperitoneální nebo extraperitoneální.
Omezení přístupu extraperitoneálního
Obezita, objem prostaty, břišní operace v anamnéze, operace prostaty v anamnéze.
Roboticky asistovaná radikální prostatektomie je variací laparoskopie prováděné chirurgem pomocí robotického systému. Hlavní výhodou této metody je trojrozměrné vidění, větší flexibilita pohybu nástroji. Nevýhodou je ztráta taktilních vjemů při operaci. Jedna studie se 105 pacienty [27], kteří podstoupili robotickou prostatektomii, porovnala obě metody (extraperitoneální – EP a transperitoneální – TP) a došla k závěru, že čas v EP skupině byl kratší než čas v TP skupině. Škála bolesti byla menší u EP než u TP. Pooperační komplikace, jako např. ileus nebo hernie, se u EP vyskytly méně často než u TP, nicméně výskyt lymfokély byl častější v EP skupině než u TP. Obnova pooperační potence a kontinence byly téměř stejné u obou skupin, ale u EP byla rychlejší obnova kontinence.
Rizikové faktory pro močovou inkontinenci u pacientů po RARP
Vyšší věk, obezita, krátká membranózní uretra, pooperační striktura anastomózy, nezkušený chirurg, nezachování neurovaskulárního svazku, iatrogenní poškození hrdla močového měchýře, objemná prostata.
Typy technik šetřících nervy
- extrafasciální (široká excize),
- interfasciální,
- intrafasciální,
- intrafasciální technika je onkologicky bezpečná, je lepší časná kontinence a lepší míra potence.
Závěr
Roboticky asistovaná radikální prostatektomie má v literatuře lepší výsledky, ale výsledky závisejí spíše na zkušenosti chirurga/urologa než na operačním postupu či metodě.
Sexuální funkce po radikální prostatektomii
Dr. J. Mulhall, USA
Erekce je komplikovaným řetězcem hormonálního systému a neurovaskulárních změn v kavernózní tkáni, jejichž výsledkem je relaxace trabekul kavernózních těles, tedy hladkého svalstva, a dilatace arterií. Přeplnění trabekul arteriální krví vede k útlaku venul a zablokování odtoku krve z penisu, venookluzi. Pak dochází k erekci. Po ejakulaci dochází k opačnému jevu.
Epidemiologie
Výskyt erektilní dysfunkce po radikální prostatektomii je především ovlivněn předoperačním stavem erektilní funkce, komorbiditami, věkem pacienta a operační technikou použitou při operaci [28].
Prevalence erektilní dysfunkce závisí rovněž na kritériích, kterými je v jednotlivých studiích definována, a také na době, která uběhla od operačního zákroku do hodnocení erektilní funkce, neboť k návratu erektilní funkce obvykle dochází ve srovnání s restitucí kontinence pomaleji. Z toho vyplývá široký rozptyl prevalence ED po radikální prostatektomii, která je uváděna v rozmezí 15–100 %. Zatímco po RP s širokou excizí NVB (neurovascular bundle – neurovaskulární svazek) se vyskytuje ED prakticky u všech pacientů, po RP provedené nervy šetřící technikou (nsRP) je ED uváděna u 40–85 % pacientů [28]. Výskyt ED po RP je rovněž ovlivněn kvalitou a zkušenostmi operatéra.
Rehabilitace
Obnovení erektilní funkce je závislé na několika faktorech:
- stupeň šetření nervů,
- předoperační erektilní funkce,
- věk pacienta,
- pooperační erektilní hemodynamika,
- zkušenost urologa,
- vaskulární komorbidity,
- hladina testosteronu v séru.
V současné době neexistuje účinná předoperační prevence ED po RP. Experimentálně se zkouší několik látek potenciálně schopných regenerovat kavernózní nervy (růstové hormony, antirejekční preparáty apod.). K možnostem peroperační prevence ED patří provedení operace se šetřením NVB, elektrostimulace erektilních nervů a možnost interpozice neurálního štěpu. U pečlivě vybraných pacientů je možné provedení RP se šetřením NVB. I po splnění výše uvedených podmínek se o provedení šetření NVB rozhoduje až peroperačně. Určitý stupeň poškození – „neurapraxie“ – je nevyhnutelný i při precizní preparaci NVB.
Pooperační prevence ED, tzv. rehabilitace erektilní funkce, je zaměřena na omezení, lépe zabránění rozvoje patologických změn v kavernózních tělesech, a tím ke zvýšení počtu pacientů, kteří nebudou mít ED či budou schopni reagovat na perorální léčbu. Penilní rehabilitace má významný a potenciální přínos pro pacienta. Měla by být prováděna u pacientů po radikální prostatektomii.
Současné rehabilitační strategie
1. PDE5i
- prevence změn ve struktuře endotelu
- prevence změn ve struktuře hladkých svalů.
- prezervace relaxačního nastavení hladkých svalů
- neuroregenerace
- dosažení erekce nezávislé na kavernózním okysličení
Výhody: jednoduchý a vynikající bezpečnostní profil.
Nevýhody: cena a nejasná účinnost.
Výsledky studie post RP Nightly Sildenafil Study byly takové, že 27 % pacientů bylo považováno za reagující, podmínkou pro účast v této studii bylo IIEF skóre 8. Pacientům, kteří na sildenafil reagovali, vrátila funkci zpět do skóre 8 podle IIEF dotazníku [29].
2. Intrakavernózní injekce
Intrakavernózní aplikace vazoaktivních látek (ICI), kavernózní okysličení. U skupiny pacientů 6 měsíců po operaci bylo pomocí intrakavernózních injekcí prostaglandinu E1 dosaženo návrat spontánní erekce častěji než ve skupině bez léčby.
Výhody: efektivní erektogenická terapie po radikální prostatektomii a dobrá cena
Nevýhody: invazivní metoda a nejasná účinnost
3. Vakuová terapie (VT)
Kavernózní okysličení, penilní protáhnutí.
VT je efektivní pomůckou při léčbě ED. Její role v rehabilitaci erektilní funkce není zcela jasná. Erekce vyvolaná pomocí VT je výsledkem navození nízkého atmosférického tlaku kolem penisu, přičemž není přítomna svalová relaxace a kavernózní tělesa jsou naplněna ne arteriální, ale venózní krví. Pacienti, kteří používali VT, udávali subjektivně menší ztrátu velikosti penisu, avšak nebylo to možné objektivně prokázat. I přesto, že v léčbě ED po RP zaujala VT své místo, v rehabilitaci erektilní funkce zatím není tak efektivní.
Výhody: jednoduchá, neinvazivní a levná metoda.
Závěr
Univerzální strategie rehabilitace erektilní funkce zatím není nalezena, avšak zahrnuje časné a pravidelné použití prostředků k dosažení erekce. Je však důležité výše uvedenou informaci probrat s pacientem ještě před operací a pacient by si měl pro sebe vybrat vhodnou léčebnou strategii po operaci. Pro výběr nejlepší léčebné strategie zatím chybí větší množství placebem kontrolovaných studií. V následujícím desetiletí se předpokládá větší zaměření na možnosti ovlivnění faktorů v lidském těle (protekce endotelu, neuroprotekce a protekce hladkých svalů). Při selhání konzervativních možností je k dispozici jako defintivní chirurgická modalita implantace penilní protézy.
Cévní a revaskularizační operace
K penilním arteriálním rekonstrukčním operacím byli indikováni hlavně mladí muži s izolovanou tepennou stenózou bez jiných vaskulárních rizikových faktorů. Princip penilní revaskularizace spočívá v bypassu zúžených cév v hypogastrickokavernózním arteriálním řečišti, čili zajištění spojení dolní epigastrické arterie s kavernózními tělesy nebo s a. dorsalis penis. Pro neuspokojivé výsledky bylo od těchto operací upuštěno. Jiné typy cévních operací (výkony na drenážním žilním systému) jsou založeny na resekci ektopických nebo jiných žil, které způsobují předčasnou detumescenci penisu [39].
5. ED a kardiovaskulární nemoci (ED/CVD) – what comes first, what goes along?
Dr. G. Jackson, Velká Británie
U pacientů s ischemickou chorobou srdeční (ICHS) je vaskulární onemocnění nejčastější příčinou ED. První Princetonská konsensuální konference (Princeton I) v roce 1999 se zabývala důkazy spojujícími sexuální aktivitu a srdeční riziko a vytvořila pokyny pro bezpečné chování kardiaků u sexuálních aktivit a při léčbě ED [30]. Druhá konference (Princeton II) byla svolána k aktualizaci doporučení na základě rozšiřování znalostí a nových způsobů léčby [31].
Erektilní dysfunkce jako marker cévních onemocnění
ED a cévní onemocnění sdílejí stejné rizikové faktory. Z toho vyplývá, že ED u asymptomatických mužů může být markerem tichého cévního onemocnění, zejména ICHS [32]. Nyní bylo zjištěno, že tomu tak je, a ED představuje důležité nové způsoby identifikace osob, kterým hrozí cévní onemocnění. Bylo prokázáno, že menší tepny penisu (průměru 1–2 mm) s plakem trpí obstrukcí při zátěži dříve než větší koronární cévy (3–4 mm), krkavice (6–8 mm) nebo iliofemorální tepny (5–7 mm), proto se ED může projevit před vznikem koronárních příhod [33]. Řešení kardiovaskulárních rizik včas po prokázání ED s provedením intervence ke snížení rizika může být přínosem [34]. Většina akutních koronárních syndromů vyplývá z asymptomatického prasknutí plaků bohatých na lipidy, a proto ED může být markerem pro snížení rizika této události [35]. Časový interval mezi vznikem symptomů ED a výskytem symptomů ICHS a kardiovaskulární příhody se odhaduje na 2 až 3 roky a 3 až 5 let. ED tedy odpovídá prvním příznakům endoteliální dysfunkce a aterosklerózy a pacienti s ED jsou v mimořádně vysokém kardiovaskulárním riziku. Každý pacient s ED, který je asymptomatický a nemá zjevnou příčinu (např. trauma), by měl být vyšetřen na cévní onemocnění včetně hladiny glukózy v krvi, lipidů a změření krevního tlaku. V ideálním případě by měli být všichni dispenzarizováni jako riziková skupina.
Léčba ED u pacientů s kardiovaskulárním onemocněním
Princeton II konsenzuální studie doporučuje, aby všichni muži s ED podstoupili kompletní vyšetření. Nutno vytvořit základní fyzickou aktivitu, kardiovaskulární rizika by měla být zařazena do nízkého, středního nebo vysokého stupně. Většina pacientů s ED s nízkým nebo středním rizikem srdečních příhod by mohla být léčena v ambulantním režimu. Neexistuje žádný důkaz, že léčba ED nebo obnovení sexuálních aktivit zvyšuje riziko u pacientů s kardiovaskulárním onemocněním. Nicméně, to je tím, že pacient je řádně vyhodnocen. Orální farmakoterapie je nejrozšířenější pro svou přijatelnost a efektivnost, ale všechny terapie mají své místo v léčebné strategii.
Inhibitory fosfodiesterázy-5
Tadalafil byl značně hodnocen u pacientů s kardiovaskulárním onemocněním a má podobný profil bezpečnosti a účinnosti jako sildenafil [36]. Studie neprokázaly žádné nežádoucí účinky na srdeční kontrakce, ventrikulární repolarizaci nebo ischemický práh. Pro svůj dlouhý poločas tadalafil nemusí být první volbou pro pacienty s těžším kardiovaskulárním onemocněním. Vzhledem k tomu, že 80 % pacientů s kardiovaskulárním onemocněním je zařazeno do nízkého rizika, je alternativou pro většinu.
Jiné terapie
Injekce intrakavernózní terapie, transuretrální alprostadil a vakuové pumpy jsou alternativami při neúčinnosti perorálních léků, avšak vyžadují zvláštní doporučení a poradenství [37,38]. Neexistuje žádný důkaz, že zvyšují kardiovaskulární riziko. Pokud se zvažuje chirurgický zákrok s celkovou anestezií, je doporučeno celkové kardiologické vyhodnocení rizik.
Závěr
Léčba ED je sekundární prioritou, a to až po stabilizaci kardiovaskulárních funkcí a zvládnutí kardiovaskulárních příznaků. Léčba ED by neměla mít negativní vliv na kardiovaskulární stav a měly by být zváženy možné vedlejší účinky léků použité v léčbě kardiovaskulárních nemocí, které vedou k ED. Klinické důkazy podporují užívání PDE5i jako léčbu první volby u mužů s ICHS a ED jako komorbiditou.
Zdroje
1. Novák J. Nádory varlat. In: Dvořáček a kol. Urologie, Praha: ISV 1998 : 1145–1171.
2. Ondruš D, Kliment J, Novák J. Nádory testis. In: L. Jurga: K linická onkológia a rádioterapia. Bratislava: Slovak Academic Press 2000 : 839–900.
3. Bosi GJ, Bajorin DF, Sheinfeld J et al. Cancer of the testis. In: De Vita VT, Hellman S, Rosenberg SA et al. Cancer: Principles Practice of Oncology. Philadelphia: Lippincott – Raven Publishers 1997 : 1397–1425.
4. Mortensen MS, Gundgaard MG, Lauritsen J et al. A nationwide cohort study of surveillance for stage I seminoma. J Clin Oncol 2013; 31(Suppl): abstr. 4502.
5. Rolnick D, Kawanoue JW, Szanto P et al. Anatomical incidence of testicular appendages. J Urol 1968; 100, 755–756.
6. Skoglund RW, McRoberts JW. Radge H. Torsion of testicular appendages: presentation of 43 new cases and a collective rewiev. J Urol 1970; 104 : 598–600.
7. Cywes S. The painful testis in infants and children. S Afr J Surg 1966; 4 : 73–82.
8. Coppridge WM Roberts LC. Torsion of the appendix testis. J Pediatr 1948; 32 : 184–187.
9. Barada JH, Weingarten JL, Cromie WJ. Testicular salvage and age-related delay in the presentation of testicular torsion. J Urol 1989; 142 : 746–748.
10. Burks DD et al. Suspected testicular torsion and ischemia: Evaluation with color Doppler sonography. Radiology 1990; 175 : 815–821.
11. Arrighi HM, Metter EJ, Guess HA et al. Natural history of benign prostatic hyperplasia and risk of prostatectomy the Baltimore Longitudinal Study of Aging. Urology 1991; 35 : 4–8.
12. Chute CG, Panser LA, Girman CJ et al. The prevalence of prostatism: a population based survey of urinary symptoms. J Urol 1993; 150 : 85–89.
13. Welch G, Weinger K, Barry MJ et al. Quality-of-life impact of lower urinary tract symptom severity: results from the Health Professionals Follow-up Study. Urology 2002; 59 : 245–250.
14. Corona G, Lee DM, Forti G et al. Age-related changes in general and sexual health in middle-aged and older men: results from the European Male Ageing Study (EMAS). J Sex Med 2010; 7 : 1362–80.
15. Johannes CB, Araujo AB, Feldman HA et al. Incidence of erectile dysfunction in men 40 to 69 years old: longitudinal results from the Massachusetts Male Aging Study. J Urol 2000; 163 : 460–463.
16. Blanker MH, Bosch JL, Groeneveld FP et al. Erectile and ejaculatory dysfunction in a community-based sample of men 50 to 78 years old: prevalence, concern, and relation to sexual activity. Urology 2001; 57 : 763–768.
17. Gan M, Smit M, Dohle GR et al. Determinants of ejaculatory dysfunction in a community-based longitudinal study. BJU Int 2007; 99 : 1443–1448.
18. Rosen RC. Update on the relationship between sexual dysfunction and lower urinary tract symptoms/benign prostatic hyperplasia. Curr Opin Urol 2006; 16 : 11–19.
19. Rosen RC, Wei JT, Althof SE et al. Association of sexual dysfunction with lower urinary tract symptoms of BPH and BPH medical therapies: results from the BPH Registry. Urology 2009; 73 : 562–566.
20. Braun MH, Sommer F, Haupt G et al. Lower urinary tract symptoms and erectile dysfunction: co-morbidity or typical ‚Aging Male‘ symptoms? Results of the ‚Cologne Male Survey‘. Eur Urol 2003; 44 : 588–594.
21. Rosen R, Altwein J, Boyle P et al. Lower urinary tract symptoms and male sexual dysfunction: the Multinational Survey of the Aging Male (MSAM-7). Eur Urol 2003; 44 : 637–649.
22. Dorsey P, Keel C, Klavens M et al. Phosphodiesterase type 5 (PDE5) inhibitors for the treatment of erectile dysfunction. Expert Opin Pharmacother 2010; 11 : 1109–1122.
23. McVary KT, Monnig W, Camps JL Jr et al. Sildenafil citrate improves erectile function and urinary symptoms in men with erectile dysfunction and lower urinary tract symptoms associated with benign prostatic hyperplasia: a randomized, double-blind trial. J Urol 2007; 177 : 1071–1077.
24. Roehrborn CG, McVary KT, Elion-Mboussa A et al. Tadalafil administered once daily for lower urinary tract symptoms secondary to benign prostatic hyperplasia: a dose finding study. J Urol 2008; 180 : 1228–1234.
25. McVary KT, Roehrborn CG, Kaminetsky JC et al. Tadalafil relieves lower urinary tract symptoms secondary to benign prostatic hyperplasia. J Urol 2007; 177 : 1401–1407.
26. Stief CG, Porst H, Neuser D et al. A randomised, placebo-controlled study to assess the efficacy of twice-daily vardenafil in the treatment of lower urinary tract symptoms secondary to benign prostatic hyperplasia. Eur Urol 2008; 53 : 1236–1244.
27. Chung JS, Kim WT, Ham WS et al. Comparison of oncological results, functional outcomes, and complications for transperitoneal versus extraperitoneal robot-assisted radical prostatectomy: a single surgeon‘s experience. J Endourol 2011; 25 : 787–792.
28. Nandipati KC, Raina R, Agarwal A et al. Erectile dysfunction following radical retropubic prostatectomy: epidemiology, pathophysiology and pharmacological management. Drugs Aging 2006; 23 : 101–117.
29. Padma-Nathan H, McCullough AR, Levine LA et al. Randomized, double-blind, placebo-controlled study of postoperative nightly sildenafil citrate for the prevention of erectile dysfunction after bilateral nerve-sparing radical prostatectomy. IJIR 2008; 20 : 479–486.
30. DeBusk R, Drory Y, Goldstein I et al. Management of sexual dysfunction in patients with cardiovascular disease; the Princeton Consensus Panel. Am J Cardiol 2000; 86 : 175–181.
31. Kostis JB, Jackson G, Rosen R et al. Sexual dysfunction and cardiac risk (the Second Princeton Consensus Conference). Am J Cardiol 2005; 96 : 313–321.
32. Kirby M, Jackson G, Betteridge J et al. Is erectile dysfunction a marker for cardiovascular disease? Int J Clin Pract 2001; 55 : 614–618.
33. Montorsi P, Montorsi F, Schulman CC. Is erectile dysfunction the „Tip of the Iceberg“ of a systemic vascular disorder? Eur Urol 2003; 44 : 352–354.
34. Kirby M, Jackson G, Simonsen U. Endothelial dysfunction links erectile dysfunction to heart disease? Int J Clin Pract 2005; 59 : 225–229.
35. Montorsi F, Briganti I, Salonia A et al. Erectile dysfunction prevalence, time of onset and association with risk factors in 300 consecutive patients with acute chest pain and angiographically documented coronary artery disease. Eur Urol 2003; 44 : 360–365.
36. Jackson G, Kloner RA, Costigan TM et al. Update on clinical trials of tadalafil demonstrates no increased risk of cardiovascular adverse events. J Sex Med 2004; 1 : 161–167.
37. Feldman HA, Johannes CB, Derby CA et al. Erectile dysfunction and coronary risk factors: Prospective results from the Massachusetts Male Aging Study. Prev Med 2000; 30 : 328–338.
38. Solomon H, Man JW, Jackson G. Erectile dysfunction and the cardiovascular patient: Endothelial dysfunction is the common denominator. Heart 2003; 89 : 251–253.
39. Guay AT. Relation of endothelial cell function to erectile dysfunction: Implications for treatment. Am J Cardiol 2005; 96 : 52–56.
Štítky
Dětská urologie Urologie
Článek Editorial
Článek vyšel v časopiseUrologické listy
Nejčtenější tento týden
2013 Číslo 4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Infekce močových cest u dospělých – mezery v současných guidelines a doporučení pro klinickou praxi
- Prevence opakovaných infekcí močových cest s využitím přípravku Uro-Vaxom
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
- Aktuální doporučení EAU pro léčbu nekomplikovaných cystitid
-
Všechny články tohoto čísla
- Diagnostika a léčba komplikací souvisejících s rezervoárem inflatabilní penilní protézy: kazuistika a diskuze
- „Steal syndrom“ penilní arterie: případová studie a přehled literatury
- Předčasná ejakulace – diagnostika a moderní léčba
- Botulotoxin: proč jej užívat, jak na to a jaké jsou výsledky?
- Editorial
- Transabdominální nebo transvaginální rekonstrukce závažného prolapsu pánevních orgánů
- Komplikace související s operační léčbou stresové močové inkontinence u žen
- Objemný angiomyolipom pravé ledviny u mladé ženy
- Zpráva z konference Eurofora 2013
-
Zpráva z kongresu ECCO v Amsterdamu
17th ECCO – 38th ESMO – 32nd ESTRO - Současné postupy při rehabilitaci penisu
-
Guidelines AUA pro řešení benigní hyperplazie prostaty (BPH)
2. část
- Urologické listy
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Objemný angiomyolipom pravé ledviny u mladé ženy
- Současné postupy při rehabilitaci penisu
- Předčasná ejakulace – diagnostika a moderní léčba
- Botulotoxin: proč jej užívat, jak na to a jaké jsou výsledky?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




