-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Botulotoxin: proč jej užívat, jak na to a jaké jsou výsledky?
Key words:
botulinum toxin, urology, dosage, injection, urinary incontinence, detrusor hyperactivity
Autoři: M. B. Chancellor
Vyšlo v časopise: Urol List 2013; 11(4): 28-33
Souhrn
Klíčová slova:
botulotoxin, urologie, dávkování, injekční, močová inkontinence, hyperaktivní detruzorMoje zkušenost s botulotoxinem
S botulotoxinem (BoNT) jsem začal pracovat v roce 1998. Byl jsem frustrován situací mých tří pacientek s roztroušenou sklerózou, velkým objemem reziduální moči, recidivující infekcí močových cest a dyssynergií uretrálního svěrače. Navzdory všem snahám jsme nebyli schopni se zdravotní sestrou naučit pacientky (z důvodu horší obratnosti), jak provádět self-katetrizaci. Po konzultaci s neurologem se pacientky informovaly na možnost aplikace botulotoxinu namísto zavádění katetru nebo rekonstrukční operace. Tým neurologů mi ukázal, jak správně připravit toxin pro injekční aplikaci. Injekční aplikace BoNT do svěrače byla snadná a všechny tři pacientky byly schopny močit s významně menším zbytkovým objemem moči, aniž by došlo ke vzniku stresové močové inkontinence.
Konzultoval jsem tento neuvěřitelný výsledek s profesorem Williamem (Chet) de Groatem, který mě povzbudil, abych svou zkušenost využil ve výzkumu. Dr. Christophera Smithe, mého kolegu v rámci akademického vědeckého programu NIH K12, tato problematika taktéž zaujala a spolu jsme zahájili první sérii experimentů s aplikací BoNT do močových cest. Brzy jsme zjistili, že botulotoxin způsobuje nejen účinnou relaxaci proužků svaloviny močové trubice, ale rovněž svaloviny detruzoru. Dále jsme prokázali, že botulotoxin blokuje uvolňování acetylcholinu ze svaloviny močového měchýře a močové trubice a rovněž uvolňování norepinefrinu. To byla naprostá novinka. Před vyvinutím preparátu BoNT pro komerční využití v urologii jsme několik let pracovali na vlastním výzkumu. S Chrisem nadále spolupracujeme a v roce 2011 jsme publikovali první knihu na toto vzrušující téma.
Pravidla bezpečného užívání botulotoxinu v klinické praxi
- Lékařští pracovníci by měli být obeznámeni se skutečností, že součástí příbalového letáku botulotoxinu (BoNT) v USA je varování o tom, že BoNT se může rozšířit od místa vpichu a vyvolávat účinek podobný botulismu.
- Může dojít k výskytu následujících symptomů: nečekaná svalová slabost, ochraptělost nebo potíže při mluvení (dysfonie), potíže při artikulaci (dysartrie), neschopnost ovládat močový měchýř, potíže při dýchání a polykání, zdvojené nebo rozostřené vidění a slzení.
- Je třeba si uvědomit, že potíže při polykání a dýchání mohou ohrožovat život pacienta. V souvislosti s šířením BoNT byly popsány případy úmrtí.
- Dále je třeba si uvědomit, že největší riziko hrozí dětem, u nichž je tato terapie indikována pro léčbu spasticity; symptomy se však mohou vyskytnout i u dospělých léčených pro toto i jiná onemocnění.
- Je třeba vést v patrnosti, že případy šíření botulotoxinu se vyskytly při dávkování užívaném pro léčbu cervikální dystonie a dokonce i při nižších dávkách.
- Je třeba pochopit, že jednotlivé produkty BoNT nelze vzájemně zaměňovat. Zavedené názvy byly upraveny s cílem zdůraznit odlišný poměr dávkování ku síle preparátu. Dávkování vyjádřené v jednotkách nelze mezi různými BoNT produkty srovnávat. Jednotky jednoho produktu nelze převádět na jednotky jiného produktu.
Ve Spojených státech byl botulotoxin schválen pro dvě indikace:
- OnabotulinumtoxinA 200 U (BOTOX) pro léčbu močové inkontinence v důsledku hyperaktivity detruzoru, která souvisí s neurologickým onemocněním (např. poranění míchy, roztroušená skleróza) u dospělých pacientů, u nichž selhala léčba anticholinergiky nebo tuto léčbu špatně snášejí.
- OnabotulinumtoxinA 100 U (BOTOX) pro léčbu hyperaktivního močového měchýře se symptomy močové inkontinence, urgence a frekvence u dospělých pacientů, u nichž selhala léčba anticholinergiky nebo tuto léčbu špatně snášejí.
Tab. 1. V současné době dostupné formy botulotoxinu na trhu. 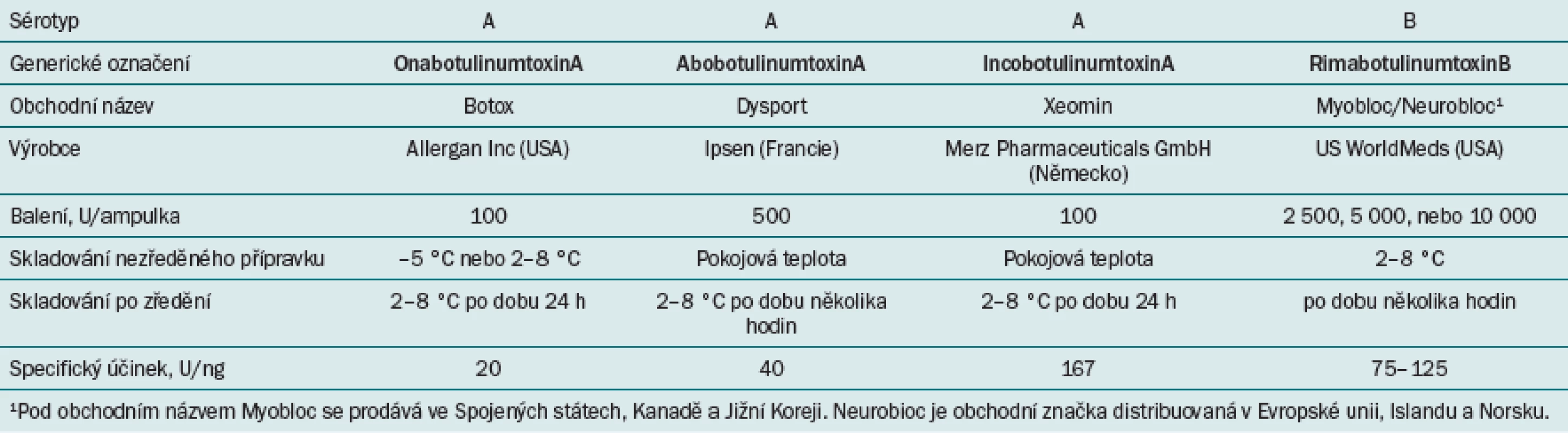
Jak na to: močový měchýř
Příprava pacienta
Před výkonem se doporučuje provést rozbor moči (v případě anamnézy chronické bakteriurie je před výkonem indikováno vhodné antibiotikum).
- Je třeba přechodně vysadit antikoagulancia.
- Od pacienta je třeba získat informovaný souhlas.
- Močový měchýř je vyprázdněn a je aplikováno lokální anestetikum (tj. 1–2% roztok lidokainu) s/bez sedace.
- Močový měchýř je naplněn přibližně 150–200 ml tekutiny pro lepší vizualizaci, je však třeba zabránit nadměrné distenzi.
- U pacientů s rizikem neurogenního hyperaktivního detruzoru je vhodné otestovat alergii na latex.
- U pacientů s poraněním míchy a pacientů s roztroušenou sklerózou s poraněním a /nebo lézemi nad úrovní T6 je třeba učinit potřebná opatření pro minimalizaci rizika autonomní dysreflexie. Monitorujeme krevní tlak pacienta a dbáme na to, aby nedošlo k přeplnění močového měchýře. Může být užitečné aplikovat lokální anestezii do močové trubice a močového měchýře, u vybraných pacientů může být vhodné zvážit celkovou anestezii.
Injekční aplikace
Při léčbě neurogenního hyperaktivního detruzoru je doporučovaná dávka 200 U onaBoNTA, rozředěná v 3 ml sterilního fyziologického roztoku, doporučený objem pro jednu injekci činí 1 ml, doporučovaná hloubka vpichu do detruzoru 2 mm, a doporučuje se celkem aplikovat 30 vpichů vzdálených od sebe po jednom centimetru, první vpich je umístěn 1 cm nad trigonum.
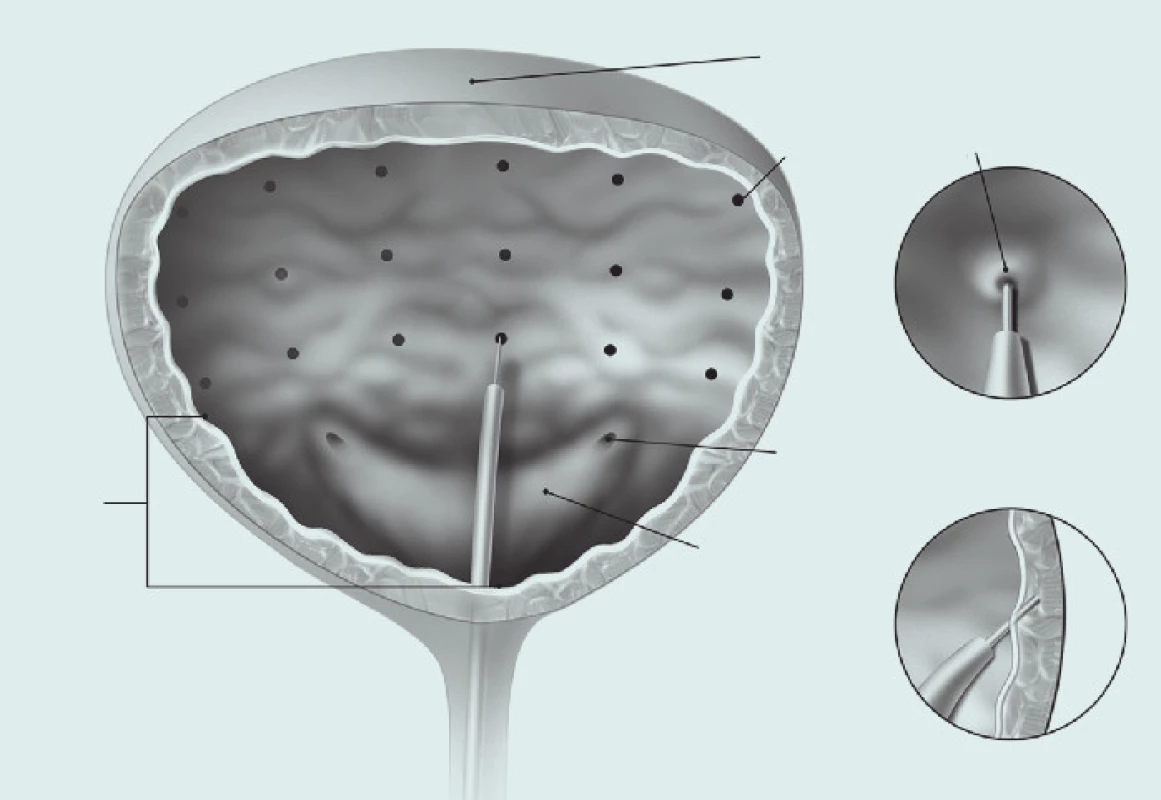
Při léčbě idiopatického hyperaktivního močového měchýře je doporučovaná dávka 100 onaBoNTA, rozředěná v 10 ml fyziologického roztoku – celkem se aplikuje na 20 místech a v každém vpichu je aplikováno 0,5 ml (obr. 1).
Cystoskop: Injekci BoNT lze aplikovat prostřednictvím flexibilního i rigidního cystoskopu. Volba techniky závisí na preferencích operatéra a zvyklostech v konkrétním centru.
Rigidní cystoskop: Ačkoli lze užít jakýkoli rigidní cystoskop, já obvykle pracuji s cystoskopy s optikou 12 nebo 30 stupňů, s použitím pracovní části, do níž vložíme jehlu 25 G. Rigidní cystoskop umožňuje snazší navigaci v močovém měchýři než flexibilní cystoskop, pracovní část zajišťuje rychlou aplikaci do močového měchýře a díky užití 25G jehly minimalizujeme krvácení a potenciální zpětný návrat toxinu z místa vpichu. Objem močového měchýře obvykle udržujeme na 150–200 ml a při vpichu se vyhýbáme krevním cévám.
Flexibilní cystoskop: Při většině ambulantních výkonů užívám flexibilní cystoskop (u mužů i žen), do něhož vložím 27G 4 mm dlouhou flexibilní jehlu. U většiny pacientů je postačující ambulantní výkon v lokální anestezii, což je pro pacienty mnohem příjemnější.
Ředění: Každá ampulka se 100 U onabotulinumtoxinuA je k dispozici v 10ml lahvičce. Toxin neředím, dokud si nejsem jistý, že byla vyloučena přítomnost infekce nebo nebyla zahájena vhodná léčba antibiotiky, abychom zabránili zbytečnému znehodnocení ampulky. Ampule s nezředěným onaBoNTA musejí být skladovány v lednici při teplotě 2–8 °C po dobu 36 měsíců. Po zředění se mohou ampule skladovat v lednici při teplotě 2–8 °C po dobu maximálně 24 hodin. Po uplynutí této doby je nutné ampulku zlikvidovat. Po zředění se nesmí OnaBoNTA zamrazovat. OnaBoNTA je nutné aplikovat ihned po zředění a neměl by být ponechán v injekční stříkačce.
Obvyklé dávkování abobotulinumtoxinuA u dospělých pacientů činí 500–1 000 U, dávkování rimabotulinumtoxinuB 2 500 až15 000 U (tj. nejčastěji se aplikuje 5 000 U).
Hloubka a lokalizace vpichu a aplikované množství: Abdel-Meguid (2010) publikoval prospektivní, randomizovanou, kontrolovanou studii zahrnující 36 pacientů, jimž byl botulotoxin aplikován do trigona. Pacienti byli randomizováni v poměru 1 : 1 k aplikaci botulotoxinu pouze do detruzoru (300 U onaBoNTA) (bez trigona) nebo do detruzoru (200 U onaBoNTA) plus do trigona (100 U onaBoNTA). Abdel-Meguid uvádí významné zlepšení všech parametrů v obou skupinách, při aplikaci toxinu do trigona však byl zaznamenán větší pokles počtu epizod inkontinence a vyšší míra úplné kontinence. V žádné ze skupin nedošlo ke vzniku vezikouretrálního refluxu ani ke zhoršení této obtíže. Ačkoli aplikace BoNT do trigona může potenciálně souviset se vznikem vezikouretrálního refluxu, tento předpoklad zatím není podložen žádnými důkazy. Je třeba zdůraznit, že pro aplikaci toxinu do tkání dolních cest močových neexistuje žádná standardizovaná technika. Byly popsány různé metody injekční aplikace do močového měchýře (tj. s/bez aplikace do trigona), ačkoli u žádného přístupu nebyl prokázán benefit oproti ostatním.
Co se stane po výkonu a další sledování: Upozorňuji pacienty, že po léčbě mohou pociťovat určitou bolest a pozorovat lehce krvavě zbarvenou moč, a případně se rovněž mohou vyskytnout potíže při močení. Tyto symptomy by měly samy vymizet během 24–48 hodin a pacientům doporučím, aby mě v případě jakýchkoli dotazů neváhali kontaktovat telefonicky. S pacienty, kteří častěji trpí infekcí v močovém měchýři, prodiskutuji volbu vhodného antibiotika a riziko infekce. Postupné zlepšování symptomů hyperaktivního močového měchýře může pacient zaznamenat až po několika dnech. Podobně i porucha mikce se může objevit až po několika dnech a v tomto případě pacientům doporučuji provádět self-katetrizaci. Přibližně po 14 dnech doporučuji kontrolní vyšetření, při němž je proveden rozbor moči a měření PVR.
Jak dlouho účinek přetrvá a kdy je třeba léčbu opakovat: K úlevě symptomů obvykle dochází po jednom až dvou týdnech. Pokud je léčba účinná, pacient obvykle s postupem času zaznamená další zlepšení, maximální benefit by se měl dostavit přibližně po jednom měsíci. Maximální efekt obvykle přetrvá 6–10 měsíců. Poté se frekvence mikce/katetrizace začíná opět zvyšovat a znovu se objeví symptomy inkontinence. Poté, co pacient zpozoruje tyto symptomy, je třeba se objednat na opakovanou injekci.
Velikost dávky při další léčbě: U většiny pacientů, u nichž je léčba pomocí BoNT účinná, aplikuji při dalším cyklu stejnou dávku. Na základě 12leté zkušenosti mohu říci, že u většiny pacientů s neurologickým onemocněním lze dosáhnout konzistentního zlepšení při aplikaci stále stejné dávky. Pokud pacient pozoruje jisté zlepšení, ale ani při aplikaci 200 U onaBoNTA nedojde k úplnému vymizení inkontinence, zvážím užití dávky 300 U onaBoNTA.
U pacientů s roztroušenou sklerózou, kteří neprovádějí self-katetrizaci, ovšem trpí močovou retencí nebo zaznamenali neúplné vyprázdnění močového měchýře, obvykle zahájím léčbu dávkou 100 U onaBoNTA. Pokud však pacient při aplikaci dávky 200 U onaBoNTA zaznamená ještě větší potíže při vyprazdňování měchýře, snížím dávku z 200 na 100 nebo 150 U onaBoNTA. Titrace dávky je tedy možná a v některých případech užitečná, ovšem procento pacientů, kteří budou vyžadovat modifikaci dávky (jakýmkoli směrem), je, jak ukazuje má zkušenost, velmi malé.
Riziko vzniku protilátek: Absence účinku BoNT může být důsledkem již existujících protilátek proti BoNT (BoNT-AB; tzv. primární selhání léčby) nebo jejich vzniku v reakci na aplikaci BoNT (tzv. sekundární selhání léčby). Od vyvinutí novějších forem onaBoNTA v roce 1998 byl v literatuře zaznamenán dramatický pokles incidence tvorby protilátek onaBoNTA u pacientů s cervikální dystonií. Sám jsem od roku 1998 (kdy jsem poprvé aplikoval BoNT) nezaznamenal jediný pozitivní případ BoNT-AB. V případě, že pacient (u něhož byla léčba dříve úspěšná) nezaznamená žádný účinek, obvykle indikuji test FronTalis Antibody Test.
Výsledky aplikace botulotoxinu do močového měchýře
Neurogenní hyperaktivní detruzor: Mangera et al (2011) v nedávné době publikovali systematický přehled publikací; jejich kritéria pro zařazení do přehledu splňovalo celkem 43 článků. Pro léčbu dospělé populace pacientů jsou k dispozici důkazy 2. úrovně: jedna studie uvádí výsledky aplikace onabotulinumtoxinuA, druhá studie výsledky aplikace abotulinumtoxinuA, třetí studie uvádí výsledky léčby pomocí obou preparátů. Nejčastěji bylo uváděno následujících 7 parametrů: obnova kontinence u 54 % pacientů, denní únik moči/den u 20 % pacientů, potřeba každodenní katetrizace u 20 % pacientů, průměrná cystometrická kapacita u 95 % pacientů, průměrný tlak detruzoru u 61 % pacientů, průměrný mikční tlak u 27 % pacientů a spokojenost pacienta/kvalita života u 24 %.
Cruz et al (2011) před nedávnem publikovali studie III. fáze, které na podzim roku 2011 vedly ke schválení této léčby u pacientů s NDO v USA i EU. Do studie bylo zařazeno celkem 691 pacientů s poraněním míchy nebo roztroušenou sklerózou, u nichž selhala léčba pomocí ≥ 1 typu anticholinergika, nebo tuto léčbu špatně snášelo. Pacienti byli randomizovaná k aplikaci 200 U onaBoNTA (n = 227), 300 U onaBoNTA (n = 223), nebo placeba (n = 241). V obou studiích bylo při aplikaci 200 U onaBoNTA prokázáno významné zlepšení primárního výsledného parametru – četnosti epizod UI/týden oproti počátečnímu stavu (ve srovnání s placebem). Aplikace 300 U nedosahovala lepšího výsledku než aplikace 200 U a byla spojena s větším výskytem vedlejších účinků. Zlepšení se dostavilo po dvou týdnech a léčba působila průměrně po dobu 10 měsíců. Léčba pomocí onaBoNTA vedla k významnému zlepšení maximální cystometrické kapacity přibližně o 150 ml. Po aplikaci 200 U onaBoNTA byla katetrizace z důvodu močové retence nezbytná u 30,6 % pacientů, kteří před léčbou nevyžadovali zavádění katetru, a u 6,7 % pacientů léčených pomocí placeba. Nejčastější nežádoucí příhody v průběhu prvních 12 týdnů zahrnovaly infekci močových cest (24 %), močovou retenci (17 %), hematurii (4 %), únavu (4 %) a nespavost (2 %).
Idiopatický hyperaktivní detruzor: Dvě klinické studie hodnotí bezpečnost a účinnost onaBoNTA u pacientů s hyperaktivním močovým měchýřem, u nichž užívání anticholinergik nevedlo k adekvátnímu zmírnění symptomů (Nitti et al, 2012). Po 12 týdnech vedla léčba (ve srovnání s placebem) ke snížení frekvence příhod úniku moči oproti počátečnímu stavu o ≥ 50 % (u pacientů léčených pomocí onaBoNTA došlo k následujícímu zlepšení: v první studii redukce o 2,5 příhod oproti počátečnímu stavu 5,5, ve druhé studii o 3 příhody oproti počátečnímu stavu 5,5, u pacientů užívajících placebo došlo k redukci o 0,9 příhod oproti počátečnímu stavu 5,1 v první studii a redukci o 1,1 příhody oproti počátečnímu stavu 5,7 příhod ve druhé studii).
Efekt onaBoNTA na redukci úniku moči a dalších symptomů hyperaktivního močového měchýře přetrval po dobu až šesti měsíců. Po dvanácti týdnech bylo (ve srovnání s placebem) zaznamenáno zmírnění dalších symptomů hyperaktivního močového měchýře, snížení frekvence močení během dne a zvětšení objemu vymočené moči. Nejčastější vedlejší účinky související s léčbou onaBoNTA v klinických studiích zahrnují infekci močových cest (18 % vs 6 % placebo), dysurii (9 % vs 7 % placebo), tedy bolest nebo potíže při močení; a močovou retenci (6 % vs 0 % placebo), tedy přechodnou neschopnost úplně vyprázdnit močový měchýř vyžadující provádění ČIK. Pacienti s diabetem měli vyšší riziko močové retence.
Jak na to: svěrač
Technika u mužů: Mužům obvykle aplikuji 200 U onaBoNTA rozředěného ve 4 ml fyziologického roztoku bez konzervačních látek v lokální nebo celkové anestezii pomocí rigidního cystoskopu, do něhož vložím endoskopickou jehlu (např. 25G Cook® Williams). Stejné množství roztoku onaBoNTA aplikujeme na pozicích 12., 3., 6. a 9. hodiny na ciferníku. Injekci aplikujeme hlouběji než při aplikaci bulking látek do močové trubice, abychom zacílili nervová zakončení inervující zevní (příčně pruhované svalstvo) svěrač. V literatuře byly popsány techniky aplikace do zevního svěrače s navigací pomocí perineálního nebo transrektálního ultrazvukového vyšetření.
Technika u žen: Ženám obvykle aplikuji 100 U onaBoNTA rozředěného ve 4 ml fyziologického roztoku pomocí 22G spinální jehly, kterou zavádím do hloubky 1,5 cm, vpichy umístíme na pozicích 3. a 9. hodiny na ciferníku, 1 cm laterálně od uretrálního meatu v periuretrálním záhybu. V každém místě aplikuji 1 ml onaBoNTA (tj. 50 U). Obvykle používám rigidní cystoskop, který usnadňuje manipulaci.
Neurogenní detruzoro-sfinkterická dyssynergie (DSD): Pro léčbu DSD a onemocnění pánevního dna se nejčastěji užívá toxin ve formě onaBoNTA. Účinné mohou být i jiné sérotypy a jiné preparáty BoNT, dávkování je však třeba zvolit na základě konkrétního užitého preparátu.
Non-neurogenní DSD: Technika aplikace BoNT při léčbě non-neurogenní DSD je stejná jako výše popsaná technika užívaná při léčbě neurogenní DSD. Pacienti s non-neurogenní poruchou však častěji vyžadují anestezii. Při periuretrální aplikaci u žen se osvědčila topická aplikace krému EMLA. U pacientů s hypoaktivním močovým měchýřem, kteří si přejí močit pomocí břišního lisu, a u pacientů s dysfunkcí mikce nebo nedostatečnou relaxací močového svěrače užívám 100 U onaBoNTA. Pakliže pacient pozoruje klinické zlepšení, lze po 1–2 týdnech vysadit preparáty vyvolávající redukci odporu v močové trubici (jako např. alfa-blokátory).
Pánevní dno a bolestivost: Při léčbě spasmu levatoru lze aplikovat transvaginální injekci 100–200 U onaBoNTA přímo do m. levator. V tomto případě existuje set na jedno použití k provádění blokády pudendálního nervu, pomocí něhož je možné pouze s navigací pomocí prstu snadno aplikovat injekci vaginální cestou do svaloviny pánevního dna (ve standardní hloubce). Trokar zavedeme k příslušnému orientačnímu bodu pomocí špičky prstu, následně vložíme jehlu a vaginální stěnu penetrujeme tak, že špička jehly míří ke svalovině levatoru. V každém ze čtyř vpichů je aplikován 1 ml roztoku, obvykle posterolaterálně, aplikaci je třeba provést po předchozí aspiraci, abychom zabránili aplikaci roztoku do cévního řečiště. Jehlou cílíme m. pubococcygeus na pozici 5. a 7. hodiny na ciferníku, proximo-mediálně a distálně od spony kosti sedací. Distální vpich míříme k m. puborectalis na pozici 5. a 7. hodiny na ciferníku přímo za hymen. U pacientek s vulvodynií lze injekci (tj. 25–50 U onaBoNTA) aplikovat pomocí malé spinální jehly pod přímou zrakovou kontrolou směrem k povrchové svalovině perinea. Vpichy se nalézají posterolaterálně na pozici 5. a 7. hodiny na ciferníku v zadní klenbě a vulvě (Chancellor a Smith 2011).
Jaký je výsledek léčby DSD: Léčbou DSD pomocí BoNT se zabývá jedna studie I. třídy a dvě studie II. třídy. Studie I. třídy srovnává účinek BoNT vs placebo u 86 pacientů s roztroušenou sklerózou (Gallien et al, 2005). Pacienti byli léčeni pomocí jediné transperineální injekce onaBoNTA, 100 U ve 4 ml normálního fyziologického roztoku, nebo placeba, do příčně pruhované svaloviny svěrače pod kontrolou EMG. Jediná dávka BoNT nevedla u této populace pacientů s roztroušenou sklerózou k redukci objemu PVR. Tyto výsledky se liší od výsledků u pacientů s SCI a mohou být způsobeny menším tlakem detruzoru (u pacientů s roztroušenou sklerózou). Americká neurologická akademie doporučuje možnost léčby DSD pomocí BoNT, ovšem upozorňuje na omezené množství přímých srovnání jednotlivých terapeutických modalit pro léčbu DSD.
Non-neurogenní DSD, pánevní dno a bolestivost: Kuo (2007) hodnotí účinek aplikace onaBoNTA do močové trubice u 27 pacientů s idiopatickým detruzorem s nízkou kontraktilitou. U 48 % pacientů došlo ke zlepšení kontraktility. Nejčastěji uretrální aplikace onaBoNTA zabrala u pacientů s močovým měchýřem s normální senzitivitou v kombinaci s narušenou relaxací nebo hyperaktivním uretrálním svěračem. U 38 % pacientů terapeutický efekt (obnovy kontraktility detruzoru) přetrval po dobu déle než jeden rok. Ghazizadeh a Nikzad (2004) aplikovali 150–400 U abobotulinumtoxinuA (Dysport®) do m. levator ani u 24 pacientek s recidivujícím vaginismem. Léčba vedla k významnému zlepšení symptomů, takže 75 % pacientek bylo schopno uspokojivého pohlavního styku. Naopak dvojitě zaslepená randomizovaná klinická studie srovnávající onaBoNTA vs fyziologický roztok u 60 pacientů, kteří po dobu ≥ 2 let trpěli chronickou pánevní bolestí [80 U (20 U/ml) onaBoNTA nebo normální fyziologický roztok do m. puborectalis a m. pubococcygeus (Abbott et al, 2006)], uvádí smíšené výsledky. Po 26 týdnech sledování došlo ke zlepšení kvality života u pacientů léčených pomocí BoNT i placeba, rozdíly mezi oběma skupinami nedosahovaly statistické významnosti. U pacientů léčených pomocí BoNT však došlo ke snížení tlaku pánevního dna ve srovnání s placebem.
Nežádoucí účinky: Výskyt komplikací při aplikaci BoNT do zevního svěrače je vzácný, výjimku představují pouze pacienti se stresovou močovou inkontinencí. Aplikace BoNT do svěrače je v současné době off-label.
Jak na to: prostata
Ředění BoNT: Při léčbě prostaty obvykle užívám 200 U onaBoNTA rozředěné ve 4 ml fyziologického roztoku bez konzervačních látek.
Příprava: Před výkonem je předepsána profylaxe antibiotiky. Užívám stejnou medikaci jako při transrektálním ultrazvukovém vyšetření a biopsii prostaty. Pacient může ráno před výkonem provést rektální nálev, takže je rektum před výkonem vyprázdněné.
Technika injekční aplikace BoNT do prostaty: Do prostaty lze BoNT aplikovat transperineálně, transrektálně nebo transuretrálně, volba přístupu závisí na individuálních preferencích. Transperineální přístup je spojen s minimálním rizikem infekce, většina evropských a amerických urologů však preferuje transrektální aplikaci naváděnou ultrazvukovým vyšetřením. Pacient je připraven a napolohován stejně jako před biopsií prostaty naváděnou pomocí transrektálního nebo transperineálního ultrazvukového vyšetření. Někteří urologové mohou preferovat transuretrální cystoskopický přístup, kdy je jehla zavedena do blízkosti zvětšené prostaty. Tato metoda může být účinnější při léčbě prostaty se zvětšením všech tří laloků (obr. 2).
Obr. 2. Vlevo: Potvrzení, že jehla (černá šipka) je zavedena do prostaty, podélné zobrazení. Uprostřed: Příčné zobrazení. Vpravo: Difuze hyperechogenního BoNT (černá šipka) v prostatě bezprostředně po aplikaci. (Chuang a Chancellor 2006) 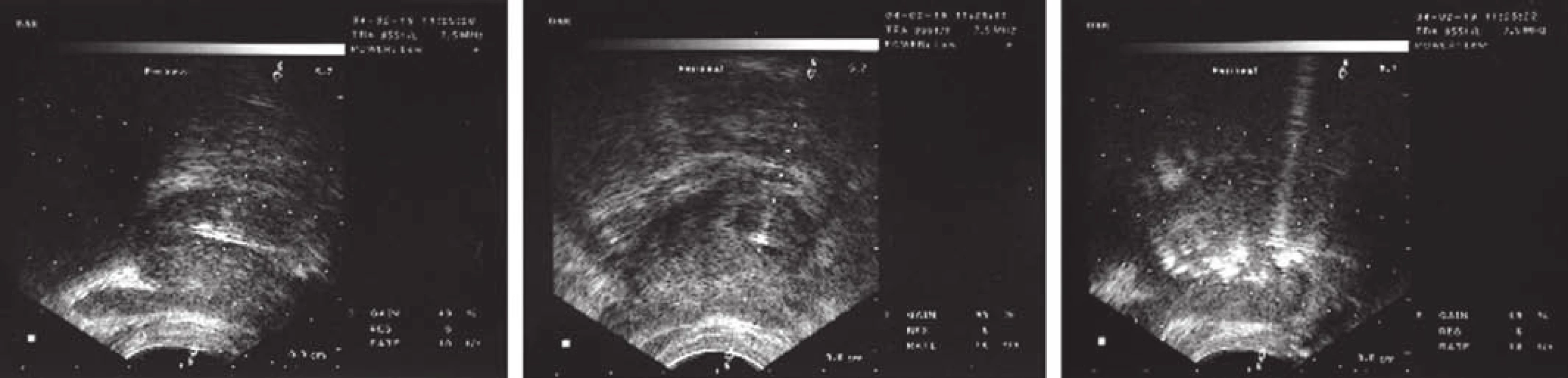
Obvykle ředím 200 U onaBoNTA ve 4 ml normálního fyziologického roztoku. Používám 23G jehlu dlouhou 15 nebo 20 cm naváděnou pomocí transrektálního ultrazvukového vyšetření. Pomocí příčného a sagitálního zobrazení se ujistím o správném zavedení jehly (jehla je zobrazena jako jasný bod uprostřed laloku; na každou stranu aplikujeme 2 ml BoNT). Difuze hyperechogenního BoNT v laterálním laloku prostaty je jasně vidět pomocí transrektálního ultrazvukového zobrazení.
Monitorování pacienta bezprostředně po léčbě: Po výkonu je pacient monitorován až do první mikce a dokud se ošetřující lékař nedomnívá, že zdravotní stav dovoluje propuštění pacienta. Pacientovi je třeba připomenout, aby doužíval antibiotika.
BPH: Účinek onaBoNTA při léčbě symptomů dolních cest močových souvisejících s BPH hodnotí několik studií, které zahrnují muže, u nichž došlo k selhání standardní léčby v podobě aplikace alfa-adrenergních antagonistů + inhibitorů 5alfa-reduktázy. První off-label aplikaci onabotulinumtoxinuA při léčbě BPH u člověka popisují Maria et al (2003) v randomizované, placebem kontrolované studii (úroveň důkazu 1b). Celkem 30 mužů se symptomatickou BPH bylo randomizováno k aplikaci fyziologického roztoku nebo 200 U onabotulinumtoxinuA. Do všech laloků prostaty bylo z perineálního přístupu pomocí 22G spinální jehly aplikováno 100 U onabotulinumtoxinuA ve 2 ml fyziologického roztoku (nebo samotný fyziologický roztok) při navigaci pomocí transrektálního ultrazvuku. U pacientů léčených pomocí onabotulinumtoxinuA bylo měsíc po výkonu pozorováno zjevné klinické zlepšení. Dva měsíce po léčbě uvedlo 13 pacientů podstupujících aktivní léčbu (87 %) a 3 pacienti v kontrolní skupině (10 %) subjektivní úlevu symptomů BPH. Po 12 měsících došlo k poklesu IPPS skóre (International Prostate Symptom Score) o 62 %, zvýšení maximální rychlosti průtoku moči o 85 %, redukci objemu postmikčního rezidua o 85 % a zmenšení objemu prostaty (měřeno pomocí ultrazvukového vyšetření) o 61 %. Došlo rovněž k poklesu hladiny PSA o 38 %. Tento rozsah zlepšení lze považovat za významný, pokud uvážíme, že u většiny pacientů byly před léčbou přítomny závažné symptomy (průměr IPSS = 23) a prostata o velkém objemu (tj. 52 g). V průběhu 19,6měsíčního sledování nebyl zaznamenán žádný případ inkontinence ani výskyt systémových vedlejších účinků.
Chuang et al (2006) stratifikovali pacienty, u nichž došlo k selhání medikamentózní léčby, následujícím způsobem: pacientům s prostatou o objemu < 30 g bylo perineálním přístupem pod kontrolou ultrazvukového vyšetření aplikováno 100 U onaBoNTA a pacientům s prostatou > 30 g 200 U. Po 12 měsících autoři uvádějí srovnatelné zlepšení IPSS, maximální rychlosti průtoku moči a objemu PVR jako Maria et al (2003), s výjimkou redukce objemu prostaty, která byla v této studii významně menší (13–19 % versus 61 %). U 29 % mužů nedošlo k žádné změně objemu prostaty, přestože u 58 % těchto mužů došlo k > 30% redukci IPSS, zvýšení maximální rychlosti průtoku moči a zmenšení objemu PVR, což nasvědčuje tomu, že onabotulinumtoxinA může působit úlevu symptomů BPH prostřednictvím nervových drah spíše než prostřednictvím redukce objemu prostaty. Marchal et al (2012) v nedávné době publikovali pěkný přehled článků zabývajících se problematikou léčby BPH pomocí BoNT.
Nežádoucí příhody: V literatuře se uvádí pouze minimum nežádoucích příhod v souvislosti s léčbou BPH pomocí BoNT (Crawford et al, 2011). Byly popsány případy dysurie a občasné nezávažné hematurie a epididymitidy. Nebyl prokázán negativní dopad na funkci spermií. Další rizika jsou stejná jako při ultrazvukově naváděné biopsii prostaty, např. hematurie, hematospermie, hematochezie a infekce.
Závěr pro léčbu prostaty: Vzhledem ke krátkému časovému období, kdy se terapie BoNT užívá pro léčbu prostaty, je třeba teprve stanovit patřičná doporučení. Nejvhodnějšími kandidáty mohou být muži s recidivujícími LUTS v důsledku BPH nebo prostatitidou, kteří se chtějí vyhnout operační léčbě. Počáteční předpoklad, že by aplikace BoNT mohla vést k významné redukci objemu prostaty a poklesu hladiny PSA, většina nejnovějších studií nepotvrdila. V současné době probíhají studie fáze IIB.
Michael B. Chancellor, MD
Professor and Director of Neurourology Program
Department of Urology
Oakland University William Beaumont School of Medicine
438 Medical Office Building
3535 W
13 Mile Road, Royal Oak, MI 48073
T: 248-551-0805
Michael.chancellor@beaumont.edu
Zdroje
1. Abbott JA, Jarvis SK, Lyons SD, Thomson A, Vancaille TG. Botulinum toxin type A for chronic pain and pelvic floor spasm in women: a randomized controlled trial. Obstet Gynecol 2006; 108 : 915–923.
2. Abdel-Meguid TA. Botulinum toxin-A injections into neurogenic overactive bladder--to include or exclude the trigone? A prospective, randomized, controlled trial. J Urol 2010; 184(6): 2423–2428.
3. Chancellor, M.B., Smith, C.P.: Botulinum Toxin in Urology, 2011, Springers, http://www.springer.com//medicine/urology/book/978-3-642-03579-1?changeHeader
4. Chuang YC, Chiang PH, Yoshimura N, De Miguel F, Chancellor MB. Sustained beneficial effects of intraprostatic botulinum toxin type A on lower urinary tract symptoms and quality of life in men with benign prostatic hyperplasia. BJU Int 2006; 98(5): 1033–1037.
5. Crawford ED, Hirst K, Kusek JW, Donnell RF, Kaplan,SA, McVary KT, Mynderse LA, Roehrborn CG, Smith CP, Bruskewitz R. Effects of 100 and 300 Units of Onabotulinum Toxin A on Lower Urinary Tract Symptoms of Benign Prostatic Hyperplasia: A Phase II Randomized Clinical Trial. J Urol 2011; 186 : 965-970.
6. Cruz F. Herschorn S. Aliotta P. Brin M. Thompson C. Lam W. Daniell G. Heesakkers J. Haag-Molkenteller C. Efficacy and safety of onabotulinumtoxinA in patients with urinary incontinence due to neurogenic detrusor overactivity: a randomised, double-blind, placebo-controlled trial. Eur Urol 2011; 60 : 742–750.
7. Gallien P, Reymann JM, Amarenco G, Nicolas B, de Seze M, Bellissant E. Placebo controlled, randomised, double blind study of the effects of botulinum A toxin on detrusor sphincter dyssynergia in multiple sclerosis patients. J Neurol Neurosurg Psychiatry 2005; 76 : 1670–1676.
8. Ghazizadeh S, Nikzad M. Botulinum toxin in the treatment of refractory vaginismus Obstet Gynecol 2004; 104 : 922–925.
9. Kuo HC. Recovery of detrusor function after urethral botulinum A toxin injection in patients with idiopathic low detrusor contractility and voiding dysfunction. Urology 2007; 69 : 57–61; discussion 61–62.
10. Mangera A. Andersson KE. Apostolidis A. Chapple C. Dasgupta P. Giannantoni A. Gravas S. Madersbacher S. Contemporary management of lower urinary tract disease with botulinum toxin A: a systematic review of botox (onabotulinumtoxinA) and dysport (abobotulinumtoxinA). Eur Urol 2011; 60 : 784–795.
11. Maria G, Brisinda G, Civello IM, Bentivoglio AR, Sganga G, Albanese A. Relief by botulinum toxin of voiding dysfunction due to benign prostatic hyperplasia: results of a randomized, placebo-controlled study. Urology 2003; 62(2): 259–264.
12. Marchal C, Perez JE, Herrera B, Machuca FJ, Redondo M. The use fo botulinum toxin in benign prostatic hyperplasia. Neurourol Urodyn 2012; 31: 86–92.
13. Nitti VW, Dmochowski R, Herschorn S, Sand P, Thompson C, Nardo C, Yan X, Haag-Molkenteller C; EMBARK Study Group. OnabotulinumtoxinA for the Treatment of Patients with Overactive Bladder and Urinary Incontinence: Results of a Phase 3 Randomized Placebo-Controlled Trial. J Urol 2012; 189 : 2186–2193.
Štítky
Dětská urologie Urologie
Článek Editorial
Článek vyšel v časopiseUrologické listy
Nejčtenější tento týden
2013 Číslo 4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Nostiriazyn – spolehlivá 1. volba u nekomplikovaných infekcí močových cest
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
- Prevence opakovaných infekcí močových cest s využitím přípravku Uro-Vaxom
- Vysoká hladina PSA a její rychlý nárůst jsou nepříznivými prognostickými faktory u karcinomu prostaty
-
Všechny články tohoto čísla
- Diagnostika a léčba komplikací souvisejících s rezervoárem inflatabilní penilní protézy: kazuistika a diskuze
- „Steal syndrom“ penilní arterie: případová studie a přehled literatury
- Předčasná ejakulace – diagnostika a moderní léčba
- Botulotoxin: proč jej užívat, jak na to a jaké jsou výsledky?
- Editorial
- Transabdominální nebo transvaginální rekonstrukce závažného prolapsu pánevních orgánů
- Komplikace související s operační léčbou stresové močové inkontinence u žen
- Objemný angiomyolipom pravé ledviny u mladé ženy
- Zpráva z konference Eurofora 2013
-
Zpráva z kongresu ECCO v Amsterdamu
17th ECCO – 38th ESMO – 32nd ESTRO - Současné postupy při rehabilitaci penisu
-
Guidelines AUA pro řešení benigní hyperplazie prostaty (BPH)
2. část
- Urologické listy
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Objemný angiomyolipom pravé ledviny u mladé ženy
- Současné postupy při rehabilitaci penisu
- Předčasná ejakulace – diagnostika a moderní léčba
- Botulotoxin: proč jej užívat, jak na to a jaké jsou výsledky?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání