-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Technika implantace a zkušenosti s dočasnou mechanickou srdeční podporou při selhání pravé komory
Technique of Implantation and Experience with Temporary Mechanical Cardiac Support in Right Ventricular Failure
Aim:
Severe right heart failure remains unfrequent but fatal complication of cardiac surgical procedures. Implantation of temporary right ventricular assist device may be life-saving procedure in various situations of right heart failure as: heart transplantation, LVAD therapy and post-cardiotomy failure. The aim of the study is an introduction of the implantation technique and retrospective review of current experience with the method.Material and Methods:
Since January 2007 isolated right ventricular assist device Levitronix CentriMag has been implanted in 16 patients. Patients were divided into 3 groups: post transplantation (post-Tx), post LVAD implantation (post-LVAD) and other cardiac procedures (OCP). Success rate of weaning from RVAD, 30-days mortality and major complications has been assessed.Outcomes:
Distribution of implants in groups was: post-Tx 5 pts (31%), post-LVAD 6 pts (38%) and 5 in OCP group (31%). The mean support time was 12 days. Off-pump implantation was achieved in 9 pts. The device was successfully weaned in 13 (81%) patients. 30-days mortality occurred in 1 case only.Conclusion:
Presented outcomes are encouraging for broader acceptance of the therapy. Excellent success rate has been reached in post-Tx and post-LVAD. This study emphasises decesive role of proactive approach in early indication of RVAD implantation for achieving satisfactory results.Key words:
right heart failure – ventricular assist device – heart transplantation – right ventricle – implantation
Autoři: I. Netuka; J. Malý; O. Szárszoi; H. Říha 1; D. Turek; M. Urban; I. Skalský; T. Kotulák 1; Z. Dorazilová 2; J. Pirk
Působiště autorů: Klinika kardiovaskulární chirurgie, Institut klinické a experimentální medicíny, Praha a Centrum výzkumu chorob srdce a cév 4, Praha, Česká republika ; Klinika anesteziologie a resuscitace, Institut klinické a experimentální medicíny, Praha a Centrum výzkumu chorob srdce a cév 4, Praha, Česká republika 1; Klinika kardiologie, Institut klinické a experimentální medicíny, Praha a Centrum výzkumu chorob srdce a cév 4, Praha, Česká republika 2
Vyšlo v časopise: Rozhl. Chir., 2011, roč. 90, č. 2, s. 88-94.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Cíl:
Těžké pravostranné srdeční selhání je méně častou, avšak vysoce obávanou komplikací kardiochirurgických výkonů. Mezi nejčastější příčiny patří pravostranné selhání štěpu po transplantaci srdce, přetrvávající nebo indukované selhání pravé komory po implantaci levostranné srdeční podpory a tzv. postkardiotomického selhání zahrnující pacienty s akutním infarktem koronárního povodí pravé komory nebo selhání po komplexních chirurgických výkonech na srdečních chlopních. Pokud není farmakologická úprava funkce pravé komory úspěšná, je mortalita této komplikace extrémně vysoká. Technologický pokrok přinesl nové možnosti v terapii těchto jinak infaustních případů pomocí implantace dočasné pravostranné srdeční podpory. Cílem je seznámit s chirurgickou technikou a zkušenostmi s využitím této metody.Materiál a metody:
Od 18. 1. 2007 byla izolovaná podpora pravé komory implantována u 16 pacientů. Ve všech případech byl použit systém Levitronix CentriMag. Pacienti byli rozděleni do skupin podle primární etiologie a data retrospektivně analyzována. Hodnocenými parametry byla 30denní mortalita, úspěšnost zotavení pravé komory a výskyt komplikací.Výsledky:
Rozdělení implantací po jednotlivých skupinách bylo: post-TxS 5 pacientů (31 %), post-LVAD 6 pacientů (38 %) a OKV 5 nemocných (31 %). Průměrná doba mechanické srdeční podpory dosáhla 12 dnů. Implantace bez použití mimotělního oběhu byla schůdná u 9 pacientů. Úspěšné odpojení od RVAD po zotavení funkce pravé komory bylo dosaženo celkem u 13 nemocných (81 %). Třicetidenní mortalita byla zaznamenána u 1 nemocného.Závěr:
Prezentované výsledky jsou povzbudivé pro širší akceptaci této terapie. Vynikající byla úspěšnost u selhání po transplantaci srdce a implantaci levostranné srdeční podpory. Studie podtrhuje zásadní význam aktivního přístupu a včasné indikace před rozvojem prolongovaného těžkého pravostranného selhávání pro dosažení dobré úspěšnosti.Klíčová slova:
mechanická srdeční podpora – transplantace srdce – srdeční selhání – pravá komora – implantaceÚVOD
Těžké pravostranné srdeční selhání patří mezi méně časté, avšak vysoce obávané komplikace kardiochirurgických výkonů s vysokou morbiditou a mortalitou. Mezi nejčastější příčiny patří pravostranné selhání štěpu po transplantaci srdce [1] a přetrvávající nebo indukované selhání pravé komory po implantaci levostranné mechanické srdeční podpory (MSP) [2]. Třetí významnou skupinu, tzv. postkardiotomického selhání, zahrnuje například pacienty s akutním infarktem koronárního povodí pravé komory nebo selhání po komplexních chirurgických výkonech na srdečních chlopních. Incidence pravostranného selhání v jednotlivých skupinách se značně liší od 1% výskytu u konvenčních rekonstrukčních výkonů až po 30 % v některých publikovaných souborech pacientů po předchozí implantaci levostranné srdeční podpory [3]. U této skupiny pacientů je zároveň identifikováno jako nejvýznamnější rizikový faktor mortality [4].
Manifestace selhání pravé komory a s ní většinou spojenou trikuspidální insuficiencí různé závažnosti má v pooperačním období velmi proměnlivou intenzitu, hlavními projevy jsou však bezpochyby syndrom nízkého minutového srdečního výdeje a vyžadují tak vysoké dávky inotropní podpory. Vzestup centrálního žilního tlaku negativně ovlivňuje orgánové funkce, vede k jaterní kongesci a s ní spojené koagulopatii a může vést i k fatálním následkům, jakými je např. neokluzivní ischemie střeva a další. Oba dva faktory pak negativně ovlivňují eliminační funkci ledvin.
Přestože se většinou daří přečerpávací funkci optimalizovat pomocí inotropní podpory, modulace srdeční frekvence a snižování afterloadu pravé komory včetně podávání vazodilatačních látek včetně inhalace oxidu dusnatého, u nezanedbatelné části pacientů však tato terapie nevede k normalizaci parametrů se všemi negativními důsledky.
V těchto případech, kdy se nepodaří obnovit adekvátní srdeční výdej pravou komorou je nezbytné neodkladné zavedení dočasné MSP; její opožděná implantace, při které se již začíná prohlubovat multiorgánová dysfunkce při protrahované nízké systémové dodávce kyslíku je spojena s výrazně horšími klinickými výsledky [5].
Autoři si kladou za cíl seznámit čtenáře s chirurgickou technikou a jejich zkušenostmi s využitím krátkodobé pravostranné mechanické srdeční podpory.
MATERIÁL A METODA
Soubor pacientů
U souboru byla provedena retrospektivní analýza všech pacientů, u kterých byla implantována samostatná pravostranná mechanická srdeční podpora (RVAD – right ventricular assist device). Zahrnuje pacienty od zahájení programu 18. 1. 2007 do současnosti. Detailnímu hodnocení byla podrobena demografická a procedurální data včetně časné 30denní mortality. Ze souboru byli z hlediska homogenity dat vyřazeni pacienti, u kterých byl vřazen do okruhu oxygenátor pro extrakorporální membránovou oxygenaci.
Z hlediska indikace výkonu byli pacienti dále rozděleni do 3 skupin: pacienty po transplantaci srdce (post-TxS), pacienty s primárně implantovaným systém levostranné (LVAD – left ventricular assist device) podpory (post-LVAD) a pacienty po ostatních kardiochirurgických výkonech (OKV).
Použitý přístroj a implantační technika
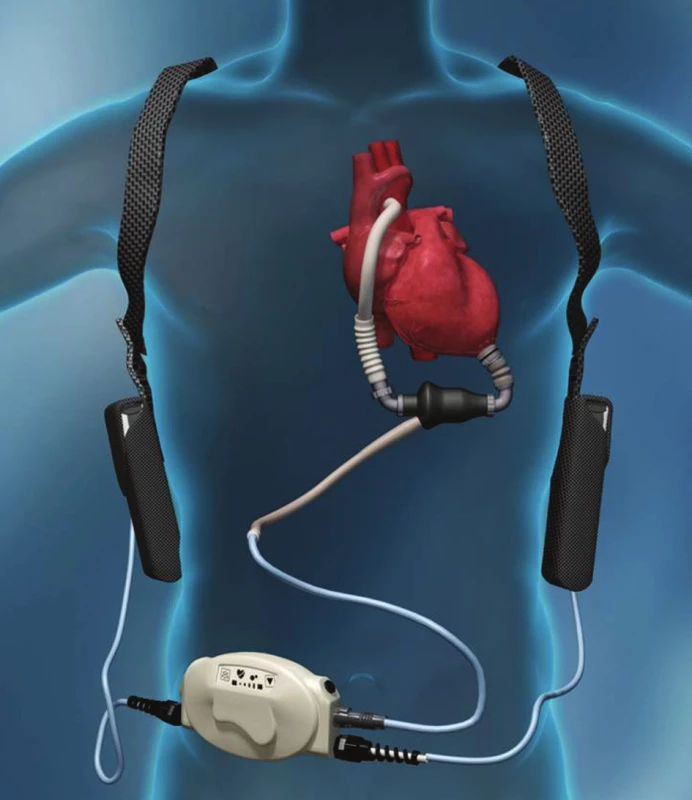
Používaný systém Levitronix CentriMag (Levitronix GmbH, Curych, Švýcarsko) je versatilní krátkodobá MSP, která je zaváděna zejména v emergentních situacích, obvykle po předcházejícím kardiochirurgickém výkonu. Většinou se jedná o univentrikulární MSP (levostranný – LVAD nebo pravostranný – RVAD), systém však nicméně umožňuje i biventrikulární zapojení. Jedná se o přístroj parakorporální [6], kdy je čerpadlo umístěno na konzoli a spojení se srdečními oddíly je zajištěno pomocí kanyl a spojovacího setu (Obr. 1). Čerpadlo se skládá z transparentní komory a magneticky levitujícího rotoru, který je v celém rozsahu omýván krví. Tak je zajištěno minimální tření a mechanická destrukce krevních elementů (Obr. 2). Tento design zároveň snižuje trombogenicitu systému a umožňuje i v případě nezbytnosti provoz bez antikoagulační terapie. Běžné terapeutické rozmezí průtoku je 4–6 l/min. Přestože je systém certifikován na 30 dnů provozu, klinická potřeba často vede k nekomplikovanému prodloužení intervalu [7].
Pro jednoduchost zavedení je systém většinou implantován bez nutnosti použití mimotělního oběhu. V případě RVAD je vtoková kanyla umístěna do pravé síně na její pravé laterální stěně pod ouškem. Kanyla je fixována 2 tabákovými monofilamentózními stehy 4/0 s perikardiálními podložkami přes turnikety. Pro stabilitu kanyly je zásadní její následná fixace k turniketům několika polyfilamentózními vlákny. Výtokovou kanylu pak zavádíme buď do 8 mm cévní protézy našité na plicnici nebo přímou kanylací do plicnice Seldingerovou technikou se zavaděčem. Fixace je zajištěna identickým způsobem jako u síňové komponenty. Obě kanyly pak vyvádíme preperitoneálně přes břišní stěnu v pravém epigastriu.
Kanyly se fixují běžným způsobem ke kůži jako drény, propojí se s okruhem hadic s vřazeným rotorem MSP a postupně je dosaženo zvyšováním otáček požadovaného průtoku, obvykle 4–6 l/min.
Pooperační péče
Bezprostředně po implantaci jsou nemocní umístěni za plné monitorace vitálních funkcí na oddělení intenzivní péče, postup je totožný jako pro jiné kardiochirurgické pacienty. Výjimku tvoří prodloužená kombinovaná antibiotická profylaxe, obvykle do doby odstranění drénů (4.–6. pooperační den) a antikoagulační terapie, která je zahajována po dosažení kontroly krevních ztrát z perikardiálních drénů. První fázi zahajuje intravenózní kontinuální podávání Heparinu (cílové aPTT 50–60 s), po obnovení perorálního příjmu jsou pacienti při prolongované srdeční podpoře nad 14 dnů převáděni na léčbu Warfarinem (cílové INR podle Quicka 2,0).
Při příznivém průběhu je zahájena vertikalizace, intenzivní rehabilitace a renutrice. Probíhá pravidelné sledování hodnot Quickova testu, zánětlivých markerů a převazy operačních ran a prostupů kanyl do těla pacienta (interval 1–3 dny). Trvalá antibiotická terapie není nutná, přistupuje se k ní selektivně pouze v případě lokálních nebo celkových známek infekce.
Protokol odpojování od MSP a explantace systému
Po hemodynamické stabilizaci je pravidelně testována echokardiograficky funkce pravé komory, pro dosažení relevantní informace je zásadní během testování snížení průtoku systémem, aby došlo k naplnění pravé komory. V případě povzbudivého návratu kontraktility pravé komory je možné zahájit odpojovací protokol. Je podána inotropní podpora, obvykle s podáním levosimendanu a následně zahájeno pravidelné snižování průtoků o 0,5 l/min každých 12 hodin. Průběžně probíhá kontrola metabolických i hemodynamických parametrů (laktát, glomerulární filtrace, centrální žilní tlak, vazopresorická podpora a další). Umístění pravostranné MSP znemožňuje monitoraci srdečního výdeje pomocí Swanova-Ganzova katétru, proto byla u části našich pacientů využita neinvazivní metoda kontinuální monitorace na principu analýzy arteriální křivky po kalibraci litiovou dilucí LiDCO (LiDCO Ltd., Spojené království).
V případě dobré tolerance je postupně snížen výdej MSP na 2 l/min, kdy je již vyžadována efektivní heparinizace s cílovým aPTT 2.0–2.5. Po převozu na operační sál je pacient v celkové anestezii zarouškován na operační výkon, zavedena sonda TEE a pacient je plně heparinizován podle pravidel pro mimotělní oběh. Následně je výkon pumpy snížen postupně až na 0,5 l/min a za stálé monitorace TEE a hemodynamiky je observován 30–60 minut. V případě příznivých parametrů je následně ze sternotomického přístupu provedeno vyjmutí obou kanyl, hemostáza je dosažena zatažením při implantaci zavedených podložkových stehů. Před extrakcí je třeba nasadit peány na kanyly, aby nedošlo při uvolnění pulmonální kanyly k jejímu vystřelení, neboť MSP je stále v provozu. Okraje ran po prostupech kanyl jsou excidovány a staženy monofilamentózními stehy s podložkami.
Systém levostranné srdeční podpory
U skupiny post-LVAD byl u všech pacientů použit systém implantabilní axiální nepulzatilní srdeční podpory HeartMate II (Thoratec Corp., Pleasanton, USA) (Obr. 3).
Statistika
Ke statistickému hodnocení byl pro srovnání průměrů spojitých veličin použit t-test a pro srovnání četnosti Fischerův jednostranný test. Kontinuální proměnné jsou určeny jako střed ± směrodatná odchylka. Kategorické proměnné jsou vyjádřeny jako relativní četnosti. Rozdíly byly statisticky významné při p < 0,05.
VÝSLEDKY
Systém Levitronix CentriMag byl implantován jako izolovaná RVAD u 16 pacientů se syndromem nízkého srdečního výdeje na podkladě těžkého pravostranného selhání. Výskyt v jednotlivých skupinách představoval: post-TxS 5 pacientů (31 %), post-LVAD 6 pacientů (38 %) a OKV 5 nemocných (31 %). Předimplantační charakteristiku pro jednotlivé skupiny shrnuje tabulka 1. Etiologicky zajímavou jednotkou bylo pravostranné selhání na podkladě infarktu pravé komory při progresi akutní disekce typu A do pravé koronární tepny.
Tab. 1. Předimplantační charakteristika souboru Tab. 1. Pre-implantation characteristics of the patient group 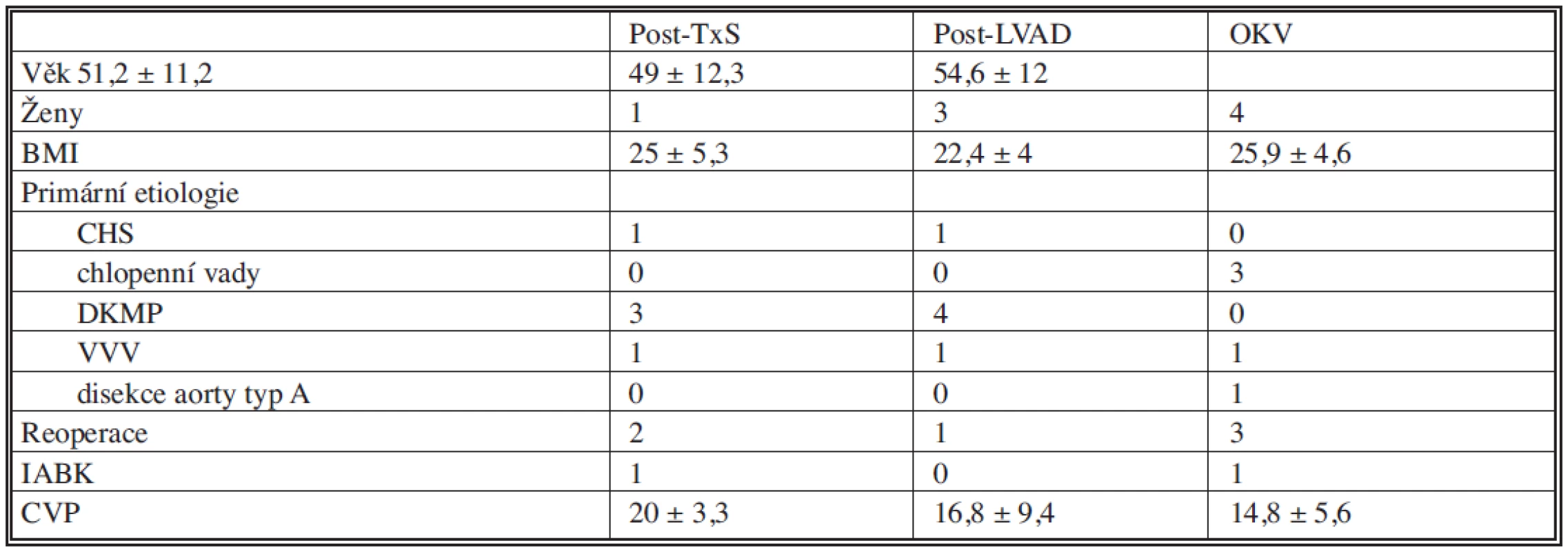
Průměrná doba mechanické srdeční podpory dosáhla 12 dnů, výskyt v jednotlivých skupinách a další přehledné zhodnocení úspěšnosti sumarizuje tabulka 2. Implantace bez použití mimotělního oběhu byla schůdná u 9 pacientů. Úspěšné odpojení od RVAD po zotavení funkce pravé komory bylo dosaženo celkem u 13 nemocných. Příčinou úmrtí během napojení na pravostrannou srdeční podporu byl 1x septický šok, 2x krvácení, z toho jednou na podkladě diseminované intravaskulární koagulopatie. Časnou mortalitu po explantaci systému jsme zaznamenali u 1 pacienta, příčinou byla těžká sepse. Nejčastější komplikace v jednotlivých skupinách shrnuje tabulka 3.
Tab. 2. Úspěšnost terapie Tab. 2. Success rate of the therapy 
Tab. 3. Komplikace terapie RVAD Tab. 3. Complications of the RVAD therapy 
V dlouhodobém sledování jsme zaznamenali pouze jednu pozdní komplikaci v podobě opětovné pozvolné manifestace pravostranného srdečního selhání u pacientky ze skupiny OKV primárně reoperované pro pokročilou dysfunkci chlopenní náhrady v aortální pozici. Pacientka byla po 3 měsících od explantace zařazena na čekací listinu transplantace srdce a následně i úspěšně transplantována. Úmrtí pacientů v pozdním sledování pak nebylo zaznamenáno žádné.
Statisticky významné rozdíly mezi skupinami nebyly vzhledem k velikosti souboru dosaženy.
DISKUSE
Dysfunkce pravé komory po transplantaci srdce je obávanou a život ohrožující komplikací. Pravá komora je vystavena i přes optimální ochranu štěpu ischemii a následně reperfuznímu poškození. Hlavním negativně působícím faktorem je následně zvýšené afterload v podobě plicní vaskulární rezistence. Ta bývá prakticky vždy u příjemce zvýšena, velmi často až k hraničně akceptovatelným hodnotám. Přestože poměrně časně dochází k normalizaci tlakových poměrů, v mnoha případech může proces trvat i několik týdnů [8]. Další negativně přispívající faktory, jako výškový a váhový nepoměr dárce a příjemce nebo využití marginálních dárců [9] v éře výrazného nedostatku štěpů mohou mít u konkrétního pacienta až fatální následky.
Méně těžké formy je po transplantaci možné zvládnout optimálním farmakologickou podporou, kontrolou srdeční frekvence a dalším snižováním plicní vaskulární rezistence např. pomocí oxidu dusnatého v respirační směsi, v dalším období pak perorálně podávaným sildenafilem.
V případě těžkého pravostranného selhání prokázaného hemodynamicky i echokardiograficky je však třeba přistoupit aktivně k včasnému zavedení pravostranné MSP. Výhodou námi používaného systému je jednoduchost zavedení, to, že kanylační technika nepoškozuje intaktnost pravé komory i jeho relativně dostupná cena. U souboru post-TxS bylo dosaženo 100% úspěšnosti zotavení pravé komory, což je výrazně lepší výsledek než v jiných pracích (odpojení 70 %, časné přežití 60 %) [10]. Kriticky je však třeba přiznat, že se jedná o soubory malých čísel. Předpokládáme však, že úspěšnost v našem souboru můžeme bezpochyby připsat včasné indikaci před rozvojem závažných důsledků pravostranného selhávání, u 3 pacientů proběhla implantace přímo po transplantaci, u zbývajících 2 maximálně do 48 hodin po ní.
U pacientů, kterým je implantována dlouhodobá levostranná je prakticky vždy v různé míře vyjádřeno i preexistující pravostranné srdeční selhání. Dále je prokázáno, že ke zhoršení funkce pravé komory po implantaci LVAD přispívá mechanismus tzv. interventrikulární interakce. Po dekompresi levostranných srdečních oddílů dochází k celé řadě patofyziologických projevů, jako je změna transseptálních tlakových gradientů, posun polohy mezikomorového septa a funkce volné stěny pravé komory [11]. Dalším negativním faktorem je pak plicní vazokonstrikce způsobená mimotělním oběhem a četnými transfuzemi krevních derivátů. Přestože jsou tyto faktory většinou upravitelné vhodnou farmakologickou terapií a optimalizací výdeje čerpadla LVAD, v případě rozvoje manifestní těžké dysfunkce pravé komory se jedná o jednu z nejvážnějších komplikací se zásadním negativním dopadem na morbiditu a mortalitu nemocných [12]. Je však třeba dodat, že i nutnost zavedení pravostranné MSP po LVAD je zásadním rizikovým faktorem pro pacienty s LVAD [4]. Podstatné je opět načasování implantace pravostranné MSP. V případě pozdního odložení za více než 72 hodin byla publikována 100% mortalita v souboru [13], stejně tak v další studii [14] bylo jasně dokumentováno, že u skupiny s časným rozšířením LVAD na biventrikulární systém v případě nepříznivého klinického vývoje bylo přežívání signifikantně vyšší oproti skupině pacientů s pozdním rozšířením o RVAD (51 % vs. 29 %). V našem souboru jsme dosáhli přežití u 8 3% a to až do propuštění pacientů do ambulantního sledování. U pacienta, který zemřel v naší skupině, byla RVAD implantována až v době progresivně se zhoršujícího oběhového stavu a selhávání LVAD při těžkém pravostranném selhání. Dalším faktorem bylo jistě i to, že se jednalo o pacienta s fixovanou těžkou plicní hypertenzí. U ostatních pacientů umožnilo následné zotavení pravé komory a optimalizace plicní vaskulární rezistence explantaci RVAD během 14 dnů a následné bezproblémové pokračování terapie LVAD.
Nezbytnost rozšíření LVAD o pravostrannou srdeční podporu je udávána v rozmezí 20–40 % [3, 15]. V našem souboru se z celkového počtu 51 implantací LVAD vyskytla pouze u 6 (11,7 %). Tento příznivý poměr patrně souvisí s přesnou předoperační indikací, kdy v případě vysokého rizika jsou pacienti ve shodě se skórovacími systémy [3, 15, 16] primárně indikováni k biventrikulárním podpůrným systémům.
U rutinních kardiochirurgických výkonů je primární pravostranné selhání řídkou, avšak vysoce obávanou komplikací. Popisovaná úspěšnost v případě nutnosti RVAD pak u jiných systémů nepřesahuje 50 % [17, 18]. V souladu s ostatními publikovanými výsledky i v naší OKV skupině byly výsledky nejméně příznivé. Na MSP zemřeli 2 z 5 pacientů. Na výsledku se jistě podílí celkový těžký stav pacientů a neuniformita diagnóz ve skupině, která znesnadňuje indikační včasnost oproti ostatním skupinám.
Nedostatkem po implantaci pravostranných MSP je z hlediska umístění systému nemožnost přímé monitorace srdečního výdeje Swanovým-Ganzovým katétrem pro objektivizaci srdečního výdeje. Rizikem je rozvoj plicního edému za situace, kdy dochází k poklesu levostranného srdečního výdeje a fixní průtok přečerpávané krve přes RVAD do plicnice převýší kapacitu levé komory. Dalším nedostatkem je pak nedostatečná evidence o přečerpávací funkci pravé komory při protokolu odpojování. Naši strategii jsme proto rozšířili o modalitu neinvazivní monitorace srdečního výdeje na principu analýzy arteriální křivky s kalibrací pomocí litiové diluce [19]. Přestože probíhají odborné diskuse na téma absolutní přesnosti získávaných dat, je nepochybné, že trendové hodnoty stability srdečního výdaje jsou cenným indikátorem u této terapie.
Systém CentriMag umožňuje dvě možnosti napojení na plicnici. Někteří autoři preferují zavedení kanyly do našité cévní protézy na plicnici [20]. Přestože na našem pracovišti v případě zavedení do vysokotlakého systémového řečiště do aorty u levostranné MSP používáme tuto techniku vždy, v případě RVAD se přikláníme k přímému zavedení do plicnice. Riziko krvácení v nízkotlakém řečišti je podstatně menší a stěna plicnice je oproti často sklerotické aortě poddajnější, čímž je riziko krvácení v místě zavedení menší. Přímé zavedení pak zkracuje čas při zavádění, které probíhá za většinou emergentních podmínek. U pacientů po transplantaci srdce je pak další nesnází našití anastomózy protézy v oblasti, kde již je sutura dárcovské a příjemcovské části plicnice.
Raritně popsanou komplikací při odpojovacím protokolu od RVAD jsou pravostranné tromboembolické komplikace [21]. Tito autoři je zaznamenali při prolongovaném odpojovacím protokolu, kdy byl průtok RVAD 36–72 pod 2 l/min. V našem souboru jsme takové komplikace nezaznamenali, zásadně však nesnižujeme dlouhodobě průtok systémem pod tuto hodnotu, přistupujeme k němu až při finální fázi odpojování za plné heparinizace pacienta. Naše předchozí publikace naopak demonstruje, že při dostatečném průtoku systémem MSP je možné vzhledem k jeho nízké trombogenicitě přerušit v případě nezbytnosti heparinizaci i na dobu 10 dnů bez negativních následků [7].
ZÁVĚR
V naší práci jsme se pokusili prezentovat povzbudivé výsledky využití mechanické srdeční podpory Levitronix CentriMag v léčbě těžkého pravostranného selhání. Chirurgická implantace je rychlá, bezpečná a většinou nevyžaduje použití mimotělního oběhu.
U pacientů po transplantaci srdce prokázal vynikající úspěšnost z hlediska zotavení funkce pravé komory štěpu, jejíž přetrvávající dysfunkce je významným prediktorem časné mortality. V terapii rozšiřující primární implantaci dlouhodobé levostranné srdeční podpory byly výsledky opět velmi dobré a u 5 ze 6 nemocných umožnily úspěšnou explantaci RVAD během 14 dnů. To podporuje hypotézu reverzibility dysfunkce pravé komory v horizontu dnů nebo prvních dvou týdnů po optimalizaci hemodynamických poměrů v malém oběhu a dekompresi levostranných srdečních oddílů po implantaci LVAD. Strategie dočasné RVAD v tomto případě umožňuje snížení počtu primárních implantací dlouhodobých biventrikulárních systémů. Ty jsou umístěny vně těla pacienta, jsou spojeny s vyšším výskytem komplikací a zároveň i podstatně větším omezením kvality života pacientů.
V souladu s odbornou literaturou byly výsledky ve skupině ostatních kardiochirurgických výkonů nejméně příznivé, avšak nikoliv demotivující. Vysvětlením je jistě různorodost etiologií a urgentnost situací v této skupině.
Na rozdíl od prvních dvou skupin, které jsou doménou pouze transplantačních center, otevírá třetí indikační skupina široké pole působnosti pro všechna kardiochirurgická pracoviště. Naše studie pak dokumentuje, že zásadním faktorem pro dosažení příznivých výsledků je aktivní přístup a včasnost indikace před rozvojem fatálních důsledků prolongovaného těžkého pravostranného selhávání.
MUDr. Ivan Netuka, Ph.D.
IKEM
Vídeňská 1958/9
140 21 Praha 4
e-mail: ivne@ikem.cz
Zdroje
1. Chen, J. M., Levin, H. R., Rose, E. A., et al. Experience with right ventricular assist devices for perioperative right-sided circulatory failure. Ann. Thorac. Surg., 1996; 61 : 305–310.
2. Moazami, N., Pasque, M. K., Moon, M. R., et al. Mechanical support for isolated right ventricular failure in patiens after cardiotomy. J. Heart. Lung. Transplant., 2004; 23 : 1371–1375.
3. Farrar, D. J., Hill, J. D., Pennington, D. G., et al. Preoperative and postoperative comparison of patients with univentricular and biventricular support with the Thoratec ventricular assist device as a bridge to cardiac transplantation. J. Thorac. Cardiovasc. Surg., 1997; 113 : 202–209.
4. Deng, M. C., Edwards, L. B., Hertz, M. I., et al. Mechanical circulatory support device database of the International Society for Heart and Lung Transplantation: Third annual report-2005. J. Heart. Lung. Transplant., 2005; 24 : 1182–1187.
5. Kavarana, M. N., Pessin-Minsley, M. S., Urtecho, J., et al. Right ventricular dysfunction and organ failure in left ventricular assist device recipients: a continuing problem. Ann. Thorac. Surg., 2002; 73 : 745–750.
6. Netuka, I., Maly, J., Szarszoi, O. Mechanické srdeční podpory v terapii terminálního srdečního selhání. Cor. Vasa., 2008; 50 : 207–214.
7. Netuka, I., Szarszoi, O., Maly, J. Comprehensive Management of Severe Intestinal Bleeding in a Patient Supported for 94 Days by the Biventricular Levitronix CentriMag System. Heart. Surg. Forum, 13 (6), 2010, v tisku.
8. Kirklin, J. K., Naftel, D. C., Kirklin, J. W., et al. Pulmonary vascular resistance and the risk of heart transplantation. J. Heart. Transplant., 1988; 7 : 331–336.
9. Jeevanandam, V., Furukawa, S., Prendergast, T. W., et al. Standard criteria for an acceptable donor heart are restricting heart transplantation. Ann. Thorac. Surg., 1996; 62 : 1268–1275.
10. Bhama, J. K., Kormos, R. L., Toyoda, Y., et al. Clinical experience using the Levitronix CentriMag system for temporary right ventricular mechanical circulatory support. J. Heart. Lung. Transplant., 2009; 28 : 971–976.
11. John R., Lee S., Eckman P. Right Ventricular Failure-A Continuing Problem in Patients with Left Ventricular Assist Device Support. J. Cardiovasc. Transl. Res., 2010.
12. Dang, N. C., Topkara, V. K., Mercando, M., et al. Right heart failure after left ventricular assist device implantation in patiens with chronic congestive heart failure. J. Heart. Lung. Transplant., 2006; 25 : 1–6.
13. Shuhaiber, J. H., Jenkins, D., Berman, M., et al. The Papworth experience with the Levitronix CentriMag ventricular assist device. J. Heart. Lung. Transplant., 2008; 27 : 158–164.
14. Fitzpatrick, J. R., Frederick, J. R., Hiesinger, W., et al. Early planned institution of biventricular mechanical circulatory support results in improved outcomes compared with delayed conversion of a left ventricular assist device to a biventricular assist device. J. Thorac. Cardiovasc. Surg., 2009; 137 : 971–977.
15. Kormos, R. L., Gasior, T. A., Kawai, A., et al. Transplant candidate’s clinical status rather than right ventricular function defines need for univentricular versus biventricular support. J. Thorac. Cardiovasc. Surg., 1996; 111 : 773–783.
16. Matthews, J. C., Koelling, T. M., Pagani, F. D., et al. The right ventricular failure risk score a preoperative tool for assessing the risk of right ventricular silure in left ventricular assist device candidates. J. Am. Coll. Cardiol., 2008; 51 : 2163–2172.
17. DeRobertis, F., Rogers, P., Amrani, M., et al. Bridge to decision using the Levitronix CentriMag short-term ventricular assist device. J. Heart. Lung. Transplant., 2008; 27 : 474–478.
18. Noon, G. P., Lafuente, J. A., Irwin, S. Acute and temporary ventricular support with BioMedicus centrifugal pump. Ann. Thorac. Surg., 1999; 68 : 650–654.
19. McCoy, J. V., Hollenberg, S. M., Dellinger, R. P., et al. Continuous cardiac index monitoring: A prospective observational study of agrement between a pulmonary artery catheter and a calibrated minimaxy invasive techniqe. Resuscitation, 2009; 80 : 893–897.
20. Loforte, A., Montalto, A., Monica, P. L. D., et al. Simultaneous temporary CentriMag right ventricular assist device placement in HeartMate II left ventricular assist system recipients at higt risk of right ventricular failure. Interact. Cardiovasc. Thorac. Surg., 2010; 10 : 847–850.
21. Velik-Salchner, C., Hoermann, Ch., Hoefer, D., et al. Thromboembolic complications during weaning from right ventricular assist device support. Anesth. Analg., 2009; 109 : 354–357.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2011 Číslo 2- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Kardiochirurgické operace u pacientů odmítajících krevní transfuze: výsledky v IKEM
- Cévní komplikace při transkatetrové implantaci aortální chlopně v IKEM
- Simultánní transplantace ledviny a Langerhansových ostrůvků
- Transplantace jater u pacientů s trombózou portální žíly
- Časné biliární komplikace po transplantaci jater
- První Česko-Slovenská domino transplantace jater
- Vývoj chirurgické techniky transplantací pankreatu v IKEM
- Imunosuprese po transplantaci žilních allograftů – naše zkušenosti
- Vliv biologických lepidel na cévní stěnu v modelu disekce aorty v experimentu
- IKEM – Institut klinické a experimentální medicíny – na prahu páté dekády úspěšné existence
- IKEM – odborné, politické a další souvislosti vzniku a dosavadního vývoje
- Technika implantace a zkušenosti s dočasnou mechanickou srdeční podporou při selhání pravé komory
- Výsledky kombinované plastiky mitrální a náhrady aortální chlopně v IKEM Praha
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Časné biliární komplikace po transplantaci jater
- Kardiochirurgické operace u pacientů odmítajících krevní transfuze: výsledky v IKEM
- Výsledky kombinované plastiky mitrální a náhrady aortální chlopně v IKEM Praha
- Vývoj chirurgické techniky transplantací pankreatu v IKEM
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání