-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Akutní disekce aorty u gravidních žen s Marfanovým syndromem
Acute aortic dissection in pregnant women with Marfan syndrome
Marfan syndrome is an inheritable connective tissue disorder. Pregnant women with Marfan syndrome are at risk of cardiovascular events, one of which is the life threatening acute aortic dissection. That is why it is important to diagnose a dilatation of aortic root in time, preferably before conception, and to propose the optimal treatment since dilatation of aortic root mostly anticipates the aortic dissection. Treatment strategy includes pharmacotherapy and cardiosurgical reconstruction of aorta and eventually aortic valve replacement. The cooperation of cardiologists, cardiosurgeons, gynecologists, anaesthesiologists and pediatricians is necessary to ensure a safe pregnancy, delivery and puerperium of women with Marfan syndrome.
Key words:
Marfan syndrome, pregnancy, aortic aneuryzm, acute aortic dissection, aortic valve replacement, aortic root replacement.
Autoři: T. Dierzé; F. Toušek; Š. Šindelářová; A. Mokráček
Působiště autorů: Primář: MUDr. František Toušek, FESC. ; Kardiocentrum – kardiologie, Nemocnice České Budějovice, a. s.
Vyšlo v časopise: Prakt. Lék. 2010; 90(2): 97-101
Kategorie: Kazuistika
Souhrn
Marfanův syndrom je vrozené onemocnění pojivové tkáně. Gravidita v kombinaci s Marfanovým syndromem představuje reálné riziko kardiovaskulárních komplikací, ze kterých je nejzávažnější život ohrožující akutní disekce ascendentní aorty. Proto je důležité včas, nejlépe ještě před otěhotněním, diagnostikovat dilataci kořene aorty, která akutní disekci aorty většinou předchází a navrhnout optimální řešení. Léčebná strategie zahrnuje farmakoterapii a kardiochirurgický rekonstrukční výkon na aortě, eventuálně na aortální chlopni. K zajištění bezpečného průběhu gravidity, porodu a šestinedělí u žen s Marfanovým syndromem je nezbytná mezioborová spolupráce kardiologa, kardiochirurga, gynekologa, anesteziologa a pediatra.
Klíčová slova:
Marfanův syndrom, gravidita, aneuryzma aorty, akutní disekce aorty, náhrada aortální chlopně, náhrada ascendentní aorty.Úvod
Akutní disekce aorty u gravidní ženy je často spojena s fatálními následky pro matku i plod, a to i v případě, že žena bezprostředně podstoupí operaci na specializovaném pracovišti. U zdravé mladé ženy je tato komplikace velmi vzácná, ale pokud je gravidní žena současně nositelkou tzv. Marfanova syndromu (dále je MFS), riziko akutní disekce dramaticky stoupá (10, 30).
Cílem tohoto sdělení je informovat širokou lékařskou veřejnost o tomto riziku a upozornit na postupy vedoucí k včasné diagnostice MFS jak u již těhotných žen, tak u dívek a mladých žen ještě před početím. Pacientky, u kterých je podezření na MFS, musí být včas odeslány ke specialistovi, který navrhne optimální strategii zajištění bezpečného průběhu současné nebo budoucí gravidity. Součástí článku je kazuistika z našeho pracoviště, která dokazuje, jak nebezpečnou a obtížně řešitelnou situaci musí lékařský tým zvládnout.
Marfanův syndrom etiologie, patofyziologie a prognóza
Marfanův syndrom je autozomálně dominantně dědičné onemocnění s uváděnou prevalencí výskytu 1 : 10 000 (6). Rodinný výskyt onemocnění je popisován v 75 %, přibližně 25 % případů vznikne mutací de novo (8). Patofyziologickou podstatou je mutace genu pro fibrilin 1 (FBN-1), lokalizovaného na chromozomu 15q21 (9).
Fibrilin 1 je glykoprotein, tvořící hlavní strukturální komponentu mikrofibril v extracelulární matrix, které jsou základem elastických vláken. Konečným důsledkem mutace je fragmentace a dezorganizace těchto vláken, tedy méněcennost pojivové tkáně (13). Prognóza pacientů s MFS je určena především kardiovaskulárními komplikacemi. Nejrizikovější komplikací je postupné aneuryzmatické rozšiřování vzestupné aorty, následované dilatací Valsalvových sinů a prstence aortální chlopně. Tento stav souhrnně nazýváme anuloaortální ektasie (obr. 1). Ta je přítomná u 75–85 % nositelů MFS. Možným následkem je vznik aortální regurgitace s pozdější dilatací a selháváním levé komory, které bývá nejčastější příčinou úmrtí. Dalšími smrtelnými komplikacemi jsou ruptura a disekce vzestupné aorty (1). Typická je také myxomatozní degenerace cípatých chlopní.
Obr. 1. Aneuryzma ascendentní aorty u MFS 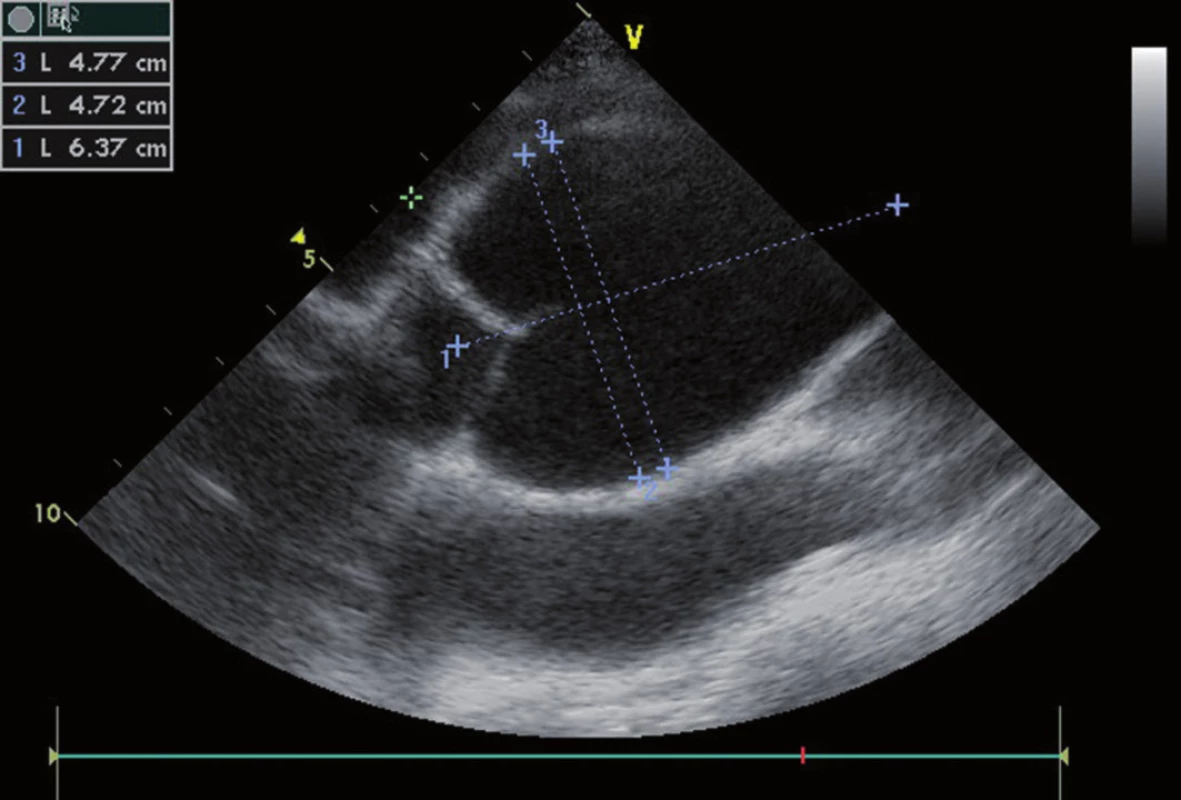
K manifestaci kardiovaskulárních potíží včetně náhlé smrti dochází u MFS již ve 2. a 3. dekádě života. V případě rodinného výskytu MFS bývají typická opakovaná náhlá úmrtí pokrevních příbuzných v relativně mladém věku. Neléčení pacienti s MFS se dožívají v průměru 32–40 let (6, 19). Prognóza léčených pacientů se během posledních let výrazně zlepšila. V roce 1972 se průměrně dožívali 37 let, v roce 1995 již více než 61 let (23, 32). Důvodem je zdokonalení a dostupnost kardiochirurgických rekonstrukčních výkonů na aortě.
Diagnostika Marfanova syndromu
Pro MFS je typická velká klinická variabilita onemocnění, které není často diagnostikováno v průběhu života a jehož první manifestací je až rozvinuté závažné kardiovaskulární onemocnění, nebo jeho smrtící komplikace. V současné době jsou k diagnostice MFS používána tzv. Ghentova kriteria, zahrnující jak rodinnou anamnézu, genetické vyšetření, tak symptomatologická kriteria z kardiovaskulárního, pohybového, kožního, očního a plicního systému (6, 26).
K typickým znakům marfanoidního habitu patří dlouhé tenké končetiny, uvolněné kloubní vazy, arachnodaktylie, někdy nacházíme gotické patro, deformity hrudního koše, méně vyvinutou svalovou hmotu. V objektivním nálezu můžeme někdy slyšet diastolický šelest z aortální regurgitace. Z očního nálezu je častá luxace, nebo subluxace oční čočky následkem rozvolněného vaziva závěsného aparátu, tzv. ectopia lentis.
Z objektivních diagnostických metod prokáže RTG plic rozšíření mediastina, nebo defiguraci kontury aorty. Zásadní je u podezření na MFS provedení echokardiografie. Ta umožní zhodnotit levou komoru srdeční, chlopenní aparát, kořen aorty, části ascendentní aorty a eventuálmě oblouku aorty. Jícnová echokardiografie navíc zobrazuje hrudní descendentní aortu. Ke zlatému standardu patří doplnění spirálního CT s kontrastem k vyšetření celé hrudní a břišní aorty, eventuálně kontrastní MR.
Horní limit šíře aorty v úrovni Valsalvových sinů je 21 mm/m2. Za dilataci je považován rozměr přesahující tuto normu. Aneuryzma je definováno rozšířením aorty, které přesahuje o 50 % horní hranici normy, tj. 31mm/m2 (18, 22).
Akutní disekce aorty definice, epidemiologie, etiologie
Disekce aorty je stav, kdy vzniklou trhlinou v intimně aorty proniká pod tlakem krev až do médie, aortální stěna se trhá a vznikají dva kanály – pravé a falešné lumen (obr. 2).
Obr. 2. Akutní disekce ascendentní aorty 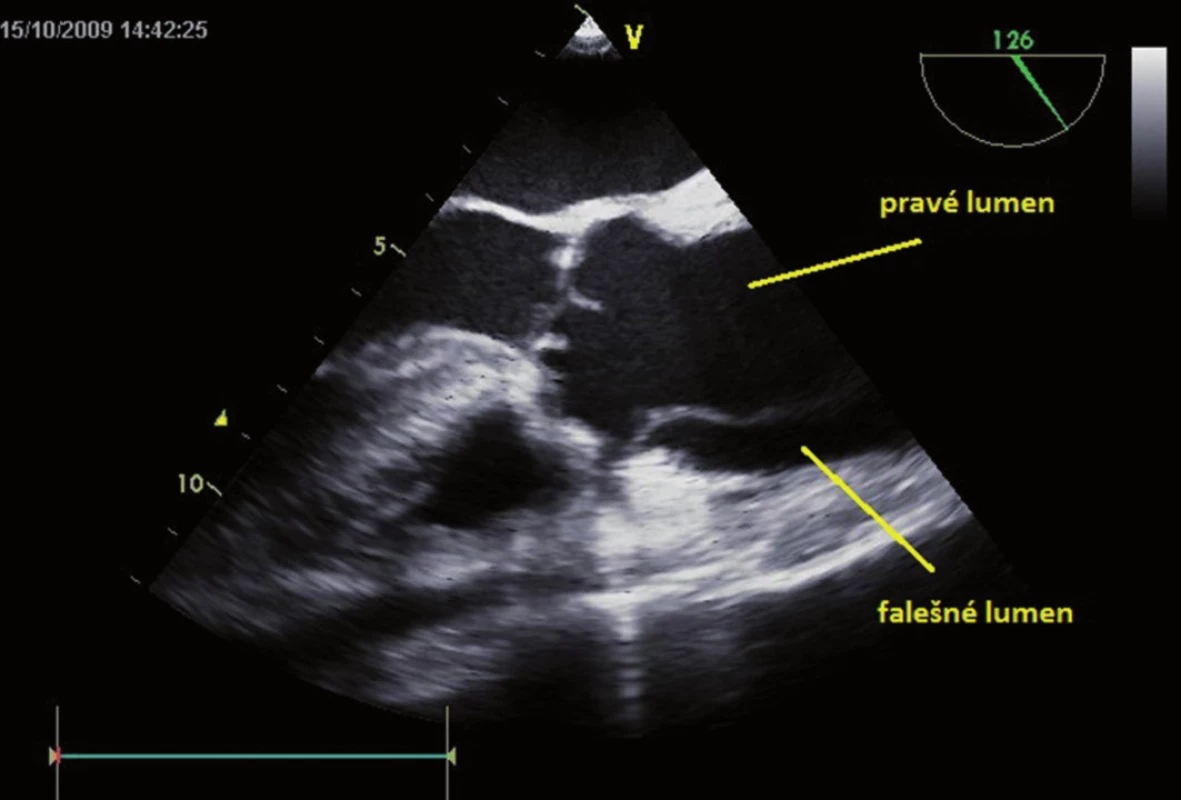
Někdy se krev dostává jen do stěny aorty bez rozštěpení její stěny a bez vzniku dvou kanálů. Vzniká tzv. intramurální hematom. Stanfordská klasifikace rozlišuje dva typy disekcí:
- Typ A – disekcí je postižena vzestupná aorta a disekce může postupovat i na další úseky hrudní nebo břišní aorty.
- Typ B – disekcí je postižena sestupná hrudní aorta s případnou progresí na břišní aortu.
Incidence disekce aorty v populaci je asi 10–20 případů na 1 milion obyvatel za rok. Více než tři čtvrtiny pacientů jsou starší 40-ti let. Ve věkové skupině 50–70 let se vyskytuje 2–5x častěji u mužů než u žen a je spojena s hypertenzí a aterosklerózou (1). Akutní disekce aorty je vzácná u mladých pacientů avšak s výjimkou osob s vrozenou poruchou pojiva, vyskytující se např. u Marfanova syndromu, Turnerova syndromu, Ehlers-Danlosova syndromu, u pacientů s vrozenou bikuspidální aortální chlopní (3), s koarktací aorty a také v graviditě (17). Traumatické a iatrogenní disekce jsou vzácné.
Klinická symptomatologie akutní disekce
Náhle vzniklá „trhavá“ krutá bolest za hrudní kostí nebo mezi lopatkami je nejčastějším příznakem onemocnění. Hypotenze nebo šokový stav jsou příznakem tamponády, krvácení, akutní aortální insuficience nebo srdečního selhání. Při klinickém vyšetření je varovným znamením diastolický šelest z aortální insuficience v kombinaci s výše popsanou bolestí na prsou (obr. 3). Podle lokalizace případné ischémie se může objevit hemiparéza, hemiplegie, ischémie horní nebo dolní končetiny, náhlá příhoda břišní, oligurie až anurie nebo paraplegie. U disekce typu A chybí asi ve 20 % pulzace na radiální tepně, neurologický deficit je přítomen až ve 40 %.
Obr. 3. Sekundární významná aortální regurgitace při akutní disekci ascendentní aorty 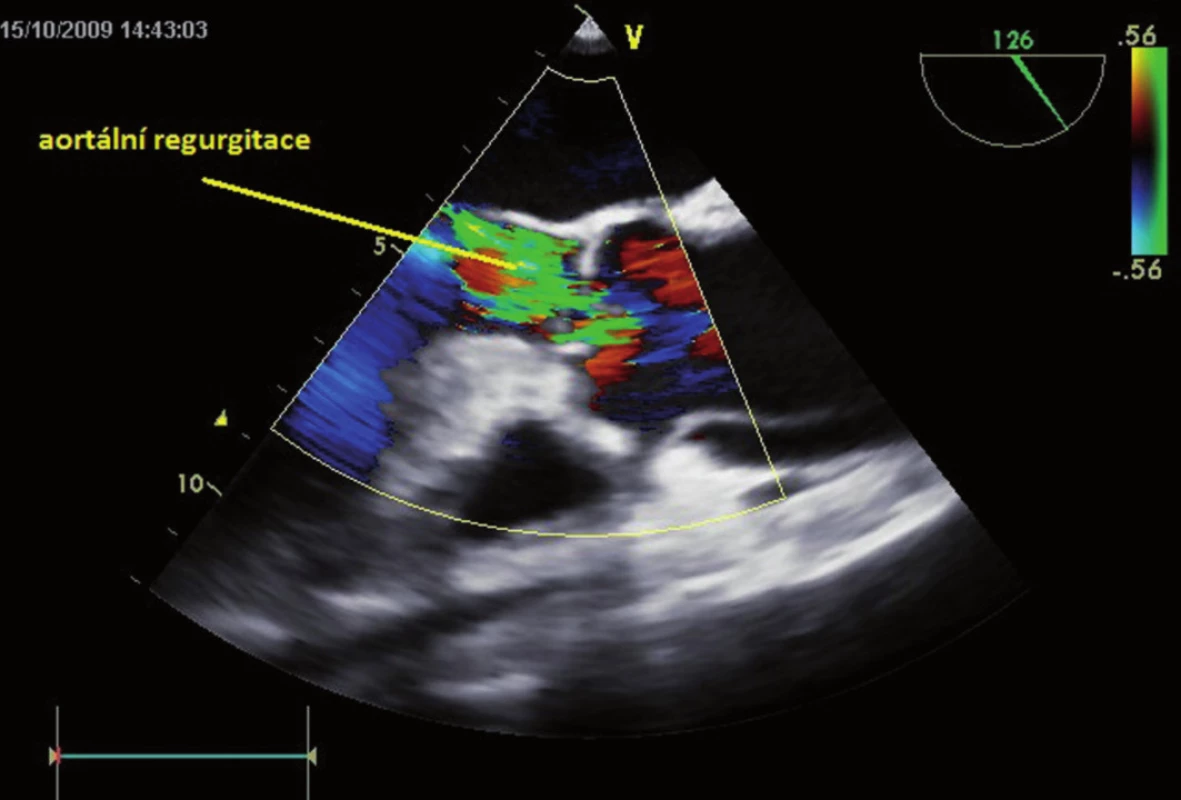
Riziko úmrtí neléčených pacientů s akutní disekcí je velmi vysoké. Literatura uvádí, že 10 až 15 % postižených zemře náhlou smrtí v prvních 15 minutách, přibližně 50 % přežívá prvních 48 hodin a pouze 5–10 % je naživu po 3 měsících (toto platí dohromady pro disekci ascendentní i descendentní aorty). U disekce ascendentní aorty přežije první měsíc pouze 8 %, u disekce descendentní aorty až 75 % pacientů. Mortalita léčených (operovaných) pacientů je dnes již pod 50 % (1).
Rizika gravidity
Polovina všech disekcí u žen do 40 let se objeví právě v graviditě, a to z důvodů fyziologických změn probíhajících v organismu během těhotenství. Může k ní dojít kdykoliv během těhotenství, při porodu i v šestinedělí, ale téměř polovina vznikne ve třetím trimestru. Během každého těhotenství stoupá cirkulující objem krve, počet červených krvinek, srdeční frekvence, stoupá srdeční výdej. Obecným důsledkem těchto změn je stoupající napětí a zatížení cévní stěny v průběhu celé aorty. Navíc vlivem hormonálních změn dochází k celkovému oslabení pojivové tkáně, tedy i stěny aorty (15).
Riziko disekce se výrazně kumuluje při graviditě žen s MFS (30). Uváděná incidence závažných kardiovaskulárních komplikací během gravidity u žen s MFS je 3–7 % (21) a celkové riziko fatálních komplikací je přibližně 1 % (20).
Léčebná strategie
Ženy, nositelky MFS, mají být včas ještě před otěhotněním poučeny o potenciálním riziku plánované gravidity a současně o 50% pravděpodobnosti přenosu MFS na svého potomka. Postupující dilatace aortálního kořene nebo rozměr nad 40 mm a více již ukazuje na zvýšené riziko aortální disekce a gravidita se v tomto případě nedoporučuje (28). Pokud je žena již těhotná a má rozměr kořene aorty 50–55 mm, doporučujeme umělé přerušení těhotenství z lékařské indikace (30).
Další léčebná strategie v případě dilatovaného kořene aorty u ženy s MFS zahrnuje 3 přístupy:
1. Farmakologická léčba
spočívá v podávání léků s chronotropně a inotropně negativním účinkem (betablokátorů), eventuálně v kombinaci s jinými antihypertenzivy. U betablokátorů je prokázán efekt na zpomalení progredující dilatace aortálního kořene, signifikantně redukují rychlost výskytu aortální regurgitace, aortální disekce, nutnost kardiovaskulární chirurgie, progresi srdečního selhání i mortalitu (25).
Použití betablokátorů v graviditě je možné, ale jsou popisovány nežádoucí účinky. U matky je to zvýšený tonus a kontraktilita dělohy, u plodu snížený krevní tok umbilikální tepnou a zpomalení fetálního růstu (16).
Účinek na novorozence zahrnuje bradykardii, hypoglykémii, hyperbilirubinémii a možnou apnoe. Betablokátory jsou bezpečné během 1. trimestu. Růst je signifikantně narušen při této medikaci ve 2. trimestru. Léčba ve 3. trimestu ovlivňuje hlavně hmotnost placenty.
Ne všechny betablokátory jsou stejně rizikové během těhotenství a laktace. Na základě zkušeností a klinických studií je za nejbezpečnější považován propranolol, který je vhodný i během laktace (31), nověji pak bisoprolol.
Při léčbě betalokátory v těhotenství i v době kojení je nutné sledovat tepovou frekvenci a celkový vývoj plodu a novorozence.
2. Chirurgická léčba
spočívá v provedení tzv. Bentallovy operace, tj. náhradě vzestupné aorty a aortální chlopně umělou cévní protézou s již zabudovanou mechanickou nebo biologickou chlopní „tzv. conduit“ (obr. 4).
Obr. 4. Náhrada vzestupné aorty a aortální chlopně conduitem (1) 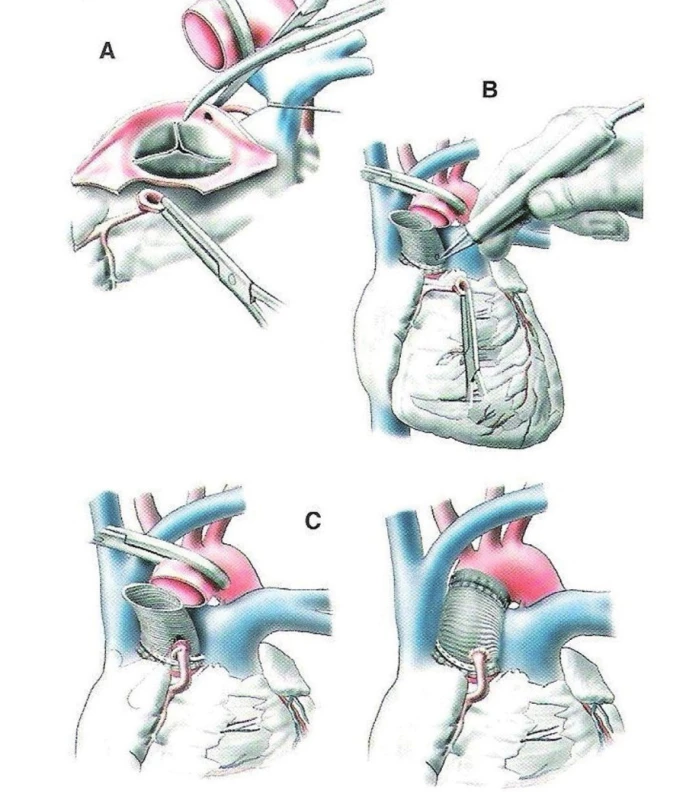
Dlouhodobé přežívání po tomto typu zákroku bylo po 5 letech 80% a po 10 letech 60%. Od roku 1979 se provádí v indikovaných případech tzv. modifikovaná Bentallova operace se zachováním aortální chlopně (operace podle Davida nebo Yacouba) (7). Bohužel literatura uvádí na konkrétním souboru těchto pacientů, že vlivem méněcennosti pojiva je až 70% pravděpodobnost vývoje sekundárního aneuryzmatu na dosud neošetřeném úseku aorty, vyžadující reoperaci (12). Z těchto důvodů je terapie betablokátory indikována trvale (36).
Aktuální guidelines doporučují preventivní chirurgické řešení u všech pacientů s MFS nebo s bikuspidální aortální chlopní, pokud je kořen aorty větší něž 50 mm bez ohledu, je-li přítomná aortální regurgitace, či nikoliv. Pro ženy s MFS navrhují někteří autoři preventivní operaci již při rozměru kořene aorty nad 45 mm nebo nad 25mm/m2 (14), jiní dokonce doporučují jako léčebně preventivní strategii náhradu kořene aorty u žen s MFS plánujících těhotenství již při rozměru kořene aorty nad 40 mm (17).
U pacientek s menšími výdutěmi je indikována elektivní operace při zvětšování aneuryzmatu o více jak 5mm/rok (2). Operační výkon je při elektivní indikaci zatížen nízkou mortalitou 1–2 % (5). Pro srovnání – u pacientů bez podezření na vrozenou poruchu pojiva je indikace k operaci asymptomatického aneuryzmatu ascendentní aorty až při rozměrech kořene 55–60 mm (2).
3. Endovaskulární léčba
se používá pro léčbu morfologicky vhodných aneuryzmat descendentní aorty. Spočívá v implantaci tubulárního stentgraftu cestou arteria femoralis a překrytí postiženého úseku descendentní aorty. U aneuryzmat vzniklých na základě vrozené poruchy pojiva je však tento typ výkonu z důvodu méněcennosti cévní stěny kontraindikován (11).
Průběh gravidity u žen s Marfanovým syndromem
U žen s MSF a kořenem aorty pod 40 mm je obvykle gravidita dobře tolerována s dobrými vyhlídkami pro matku i plod. Pokud se dilatace kořene aorty nad 40 mm zjistí již v pokročilém stádiu gravidity, nebo žena s umělým přerušením nesouhlasí, doporučuje se klidový režim. Nezbytné jsou časté echokardiografické kontroly (1x za 6–10 týdnů), kontroly krevního tlaku, je nutné podávání betablokátorů. V této léčebné a kontrolní strategii je nezbytné pokračovat minimálně 6 měsíců po porodu. Stejně těsné sledování je indikováno i u žen s diametrem kořene aorty pod 40 mm, neboť ani zde není riziko disekce zcela zanedbatelné.
Dále je doporučena preventivní fetální maturace plic plodu kortikoidy ve 26. týdnu gestace a jako u všech gravidit s vysokým rizikem komplikací je indikována od 28–32. týdne těhotenství hospitalizace až do porodu v centru pro riziková těhotenství s dostupností kardiocentra a možností urgentního chirurgického zákroku na aortě.
Literatura uvádí nemnoho případů úspěšné operace akutní disekce aorty během gravidity (4, 34, 35). Výsledky naznačují relativně vysokou četnost ztráty plodu (27). Z těchto důvodů, pokud je dokumentována zralost plodu, nebo je těhotenství starší alespoň 30-ti týdnů, je možné indikovat provedení císařského řezu ještě před kardiochirurgickou operací. Preventivní náhrada dilatované ascendentní aorty během těhotenství je možná ve zcela výjimečných případech (24).
Přirozený porod vaginální cestou v epidurální anestézii je doporučen u žen s MFS a diametrem kořene aorty pod 40 mm během gravidity. Použití kleští nebo vakuum extrakce ke zkrácení 2. doby porodní je možné, ale není u pacientek s minimálními kardiálními abnormalitami nutné (33).
Provedení elektivního císařského řezu v epidurální anestézii je doporučeno u žen s diametrem kořene aorty nad 40 mm. Nejlepší metoda anestézie u pacientek podstupujících císařský řez s preexistující dilatací kořene aorty je kontroverzní. Celková anestézie bývá nezbytná u antikoagulovaných pacientek, ale hypertenzní odpověď na intubaci a chirurgická stimulace může zvýšit kardiovaskulární stres a náchylnost k ruptuře, nebo způsobit progresi již přítomné disekce (29).
Jen v několika případech je popisováno úspěšné těhotenství u žen po náhradě kořene a oblouku aorty. Obecně tyto ženy tolerovaly těhotenství dobře, byly těsně echokardiograficky sledovány a všechny užívaly betablokátory. Není jasné, jaký způsob porodu je v těchto případech nejvhodnější. Podle literatury některé pacientky rodily spontánně, jiné formou elektivního císařského řezu. Vzhledem k nízkému počtu těchto případů není žádný z postupů preferován (36, 37).
Na tomto místě je však nutno také uvést, že i pacientkám, které podstoupí před plánovanou graviditou elektivní kardiochirurgický rekonstrukční výkon na aortě, nelze zaručit bezproblémový průběh těhotenství. Vycházíme-li z předpokladu, že příčinou akutní disekce aorty je méněcennost cévní stěny, náhradou její části řešíme riziko disekce pouze v nahrazeném úseku. Ve většině případů je nahrazována ascendentní aorta, která je z anatomických a patofyziologických důvodů rupturou nebo disekcí ohrožena nejvíce, ale disekcí nebo rupturou je ohrožena aorta v celém svém průběhu.
Jsou bohužel popisovány i případy úmrtí žen s MFS v souvislosti s graviditou, u kterých byl před otěhotněním proveden elektivní rekonstrukční kardiochirurgický výkon na ascendentní aortě, právě z důvodů snížení rizika plánované gravidity. Příčinou úmrtí byla ruptura nebo disekce aorty v úseku, který nebyl nahrazen cévní protézou (30).
Každý pacient s anamnézou disekce by měl být pravidelně sledován nejen spádovým kardiologem, ale i v kardiocentru a měl by mít provedenou CT-angiografii za půl a za 1 rok od operace.
Vlastní pozorování
Jedná se o 32-letou ženu, která měla od dětství diagnostikovaný MFS a posledních 7 let byla v péči kardiologa pro dilataci ascendentní aorty. V rodinné anamnéze byl otec po náhradě aortální chlopně, matka byla nositelkou MFS. V minulosti byl pacientce opakovaně navrhován preventivní rekonstrukční výkon na ascendentní aortě, ten však odmítala. Tato žena byla přijata v květnu 2008 na gynekologii jako primigravida ve 22. týdnu gravidity na doporučení ošetřujícího kardiologa.
V chronické medikaci měla Carvedilol v dávce 6,25 mg 1/2-0-1. Na ultrazvuku srdce byl nález dilatace ascendentní aorty na 48–49 mm, aortální regurgitace I–II. st., normální funkce levé komory srdeční, prolaps cípů mitrální i trikuspidální chlopně s regurgitacemi II. st.
Ze subjektivních potíží udávala paroxyzmální palpitace a námahovou dušnost do stupně NYHA II. Potíže se objevily až v souvislosti s graviditou. Při Holterovském monitorování EKG a krevního tlaku byly prokázány intermitentní bigeminicky vázané komorové extrasystoly a opakovaně sklon k hypotenzi. Gynekologický nález byl příznivý. Konzultovaný kardiochirurg neindikoval akutní operaci, výkon doporučil až po porodu.
Pacientka byla přeložena na kardiologické oddělení, poučena o rizicích a byla jí doporučena hospitalizace až do porodu. Toto odmítla a po 14 dnech byla na vlastní žádost propuštěna. Během hospitalizace se echokardiografický nález neměnil. Ambulantně docházela na pravidelné echokardiografické kontroly, při kterých byl ultrazvukový nález stále stacionární. Porod císařským řezem byl naplánován na 35. týden gravidity. Dva dny před plánovaným porodem se náhle objevily bolesti na prsou a slabost. Pacientka byla přivezena urgentně do kardiocentra. Při přijetí byla oběhově stabilní, při vědomí, echokardiograficky byl zjištěn nález akutní disekce aorty typu A. Pacientka byla okamžitě převezena na kardiochirurgický sál, a v celkové anestézii byl proveden bez komplikací urgentní císařský řez s vybavením zdravého plodu a vzápětí provedena úspěšná kardiochirurgická operace s náhradou ascendentní aorty a aortální chlopně mechanickou protézou (tzv. Bentallova operace), plus plastika mitrální a trikuspidální chlopně. Pacientka byla propuštěna do domácího ošetření bez závažnějších potíží 9. pooperační den spolu se zdravým dítětem. Při poslední kontrole po více než 1,5 roce od operace se pacientka cítí dobře. Její přání znovu otěhotnět jsme jí však již důrazně nedoporučili.
Diskuse
U každé ženy ve fertilním věku je nutné důsledně věnovat pozornost rodinné anamnéze a aktivně pátrat po případných náhlých úmrtích v rodině. Pokud se v rodině přímo vyskytne diagnóza disekce nebo ruptury aorty v mladším věku, vždy myslet na možnou vrozenou poruchu pojiva. Na tuto poruchu by měli myslet již pediatři, praktičtí lékaři a hlavně gynekologové a včas indikovat echokardiografické vyšetření srdce.
Kardiolog, který se setká u ženy ve fertilním věku s nálezem dilatace ascendentní aorty, bikuspidální aortální chlopní nebo s pozitivní rodinou anamnézou, by měl zhodnotit míru rizika a včas pacientku informovat o možných komplikacích gravidity a jejich řešeních. Informovat by měl také ošetřujícího praktického lékaře a gynekologa. V případě, že jde již o ženu gravidní, zahájit farmakoterapii antihypertenzivy, naplánovat nutné opakované echokardiografické kontroly a léčebný režim v období gravidity i šestinedělí. V indikovaných případech je nutné doporučit i předčasné ukončení gravidity.
Péče o vysoce rizikové těhotné by měla probíhat ve zdravotním zařízení, jehož součástí je komplexní kardiocentrum schopné zajistit urgentní rekonstrukční operaci aorty a péči o nezralý plod. Za mezioborové spolupráce kardiologa, gynekologa, kardiochirurga, anesteziologa a neonatologa je nutné naplánovat optimální těhotenskou péči, stanovit optimální termín a způsob porodu a poporodní péče o matku i plod tak, aby bylo maximálně sníženo riziko možných fatálních kardiovaskulárních komplikací.
Závěr
Tento konkrétní případ ukazuje, že pro lékaře není často jednoduché přesvědčit ženy s již známou chorobou pojiva, jak velké riziko pro ně gravidita může představovat. Dochází poté k takto dramatickým, život bezprostředně ohrožujícím situacím. Bohužel nelze předpokládat, že i při dodržení všech lékařských postupů, při dostupné moderní diagnostice a při možnostech současné kardiochirurgie, se podaří zachránit všechny gravidní ženy s vrozenou poruchou pojiva. Je ale naší povinností snažit se těmto dramatickým situacím maximálně předcházet.
MUDr. Tomáš Dierzé
Kardiocentrum – kardiologie
Nemocnice České Budějovice, a.s.
Boženy Němcové 585/54
České Budějovice
E-mail: dierze@email.cz
Zdroje
1. Aschermann, M. Kardiologie. Praha: Galén, 2004.
2. Bonow, R.O., Carabello, B.A., Chatterjee, K., et al. ACC/AHA 2006 practice guidlines for the management of pacients with valvular heart diesese. J. Am. Coll. Cardiol. 2006, 48, p. 598-675.
3. Braverman, A.C., Guven, H., Beardslee, M.A. et al. The bicuspid aortic valve. Curr. Probl. Cardiol. 2005, 30, p. 470-522.
4. Cola, L.M., Lavin, J.P. Pregnancy complicated by Marfan’s syndrome with aortic arch replacement and dissection, subsequent aortic arch replacement and triple coronary artery bypass graft. J. Reprod. Med. 1985, 30, p. 685-688.
5. David, T.E., Armstrong, S., Ivanov, J. et al. Results of aortic valve-sparing operation. J. Thorac. Cardiovasc. Surg, 2001, 122, p. 39-46.
6. De Paepe, A., Devereux, R.B., Dietz, H.C., et al. Revised diagnostic criteria for the Marfan syndrome. Am. J. Med. Genet. 1996, 62, p. 417-426.
7. Dean, J.C. Management of Marfan syndrome. Heart 2002, 88, p. 97-103.
8. Dietz, H.C., Cutting, G.R., Pyeritz, R.E. et al. Marfan syndrome caused by a recurrent de novo missense mutation in the fibrillin gene. Nature 1991, 352, p. 337-339.
9. Dietz, H.C., Pyeritz, R.E., Hall, B.D. et al. The Marfan syndrome locus: conformation of assignment to chromosome 15 and identification of tightly linked markers at 15q15-q21.3. Genomics 1991, 9, p. 355-361.
10. Elkayam, U., Ostrzega, E., Shotan, A., Mehra, A. Cardiovascular problems in pregnant women with the Marfan syndrome. Ann. Intern. Med. 1995, 123, p. 117-122.
11. Ferko, A., Krajina, A. Arteriální aneuryzma: základy endovaskulární a chirurgické léčby. Hradec Králové: ATD, 1999.
12. Finkbohner, R., Johnston, D., Crawford, E.S. et al. Marfan syndrome. Long-term survival and comlications after aortic aneuryzm repair. Circulation 1995, 91, p. 728-733.
13. Fleischer, J.K., Nousari, H.C., Anhalt, G.J. et al. Immunohistochemical abnormalities of fibrillin in cardiovascular tissues in Marfan’s syndrome. Ann. Thorac. Surg. 1997, 63, p. 1012-1017.
14. Gott, V.L., Cameron, D.E., Alejo, D.E. et al. Aortic root replacement in 271 Marfan patiens: a 24-years experience. Ann. Thorac. Surg. 2002, 73, p. 438-443.
15. Huter, S., Rondon, S.C. Adaptation of the maternal heart in pregnancy. Br. Heart J. 1992, 68, p. 540-543.
16. Cheng, T.O. Caution in use of beta blockers during pregnancy. Cathet. Cardiovasc. Diagn. 1995, 34, p. 186-188.
17. Immer, F.F., Bansi, A.G., Immer-Bansi, A.S. et al. Aortic dissection in pregnancy: analysis of risk factor and outcome. Ann. Thorac, Surg. 2003, 76, p. 309-314.
18. Johnston, K.W., Rutherford, R.B., Tildin, M.D. et al. Suggested standards for reporting on arteria aneurysms. J. Vasc. Surg. 1991, 13, p. 452-458.
19. Kirklin, J.W., Barrat-Boyes, B.G. Cardiac surgery New York: Churchill Livingstone, 1993.
20. Lalchandani, S., Wingfield, M. Pregnancy in women with Marfan’s syndrome. Eur. J. Obstet. Gynecol. Reprod. Biol. 2003, 110, p. 125-130.
21. Lind, J., Wallenburg, H.C. The Marfan syndrome and pregnancy: a retrospective study in a Dutch population. Eur. J. Obstet. Gynecol. Reprod. Biol. 2001, 98, p. 28-35.
22. Meijboom, L.J., Timmermans, J., Zwinderman, A. et al. Aortic root growth in men and women with the Marfan’s syndrome. Am. J. Cardiol. 2005, 96, p. 1441-1444.
23. Mudroch, J.L., Walker, B.A., Halpern, B.L. et al. Life expectancy and causes of death in the Marfan syndrome. N. Engl. J. Med. 1972, 286, p. 804-808.
24. Naito, H., Tada, K. Open heart operation for a pregnant patien with Marfan syndrome. Masui 2005, 54, p. 525-529.
25. Ose, L., McKusick, V.A. Prophylactic use of propranolol in the Marfan syndrome to prevent aortic dissection. Birth. Defects Orig. Artic. Ser. 1977, 13, p. 163-169.
26. Pyeritz, R.E., McKusick, V.A. The Marfan syndrome: diagnosis and management. N. Engl. J. Med. 1979, 300, p. 772-777.
27. Pyeritz, R.E. Maternal and fetal complications of pregnancy in Marfan syndrome. Am. J. Med. 1981, 71, p. 784-790.
28. Rahman, J., Rahman, F.Z., Rahman, W. et al. Obstetric and gynecologic complication in women with marfan syndrome. J. Reprod. Med. 2003, 48, p. 723-728.
29. Ray, P., Murény, G.J., Shift, LE. Recognition and management of maternal cardiac disease in pregnancy. Br. J. Anaesth. 2004, 93, p. 428-439.
30. Rossiter, J.P., Repke, J.T., Morales, A.J. et al. A prospective longitudinal evaulation of pregnancy in the Marfan syndrome. Am. J. Obstet. Gynecol. 1995; 173, p. 1599-1606.
31. Shorek, J., Berger, K.R., Murény, E.A., Pyeritz, R.E. Progression of aortic dilatation and the benefit of long-term beta-adrenergic blockade in Marfan’s syndrome. N. Engl. J. Med. 1994, 330, p. 1335-1341.
32. Silverman, D.I., Buton, K.J., Gray, J. et al. Life expectancy in the Marfan syndrome. Am. J. Cardiol. 1995, 75, p. 157-160.
33. Simpson, L.L., Athanassious, A.M., D’Alton, M.E. Marfan syndrome in pregnancy. Curr. Opin. Obstet. Gynecol. 1997, 9, p. 337-341.
34. Smith, V.C., Eckenbrecht, R.D., Nankine, G.D., Leach, C.L. Marfan’s syndrome, pregnancy and the cardiac surgeon. Mil. Med. 1989, 154: p. 404-406.
35. Snir, E., Levinsky, L., Salomon, J. et al. Dissecting aortic anerysm in pregnant women wihout Marfan syndrome. Surg. Gynecol. Obstet. 1988, 167, p. 463-465.
36. Treasure, T. Elective replacement of the aortic root in Marfan’s syndrome. Br. Heart J. 1993, 69, p. 101-103.
37. Williams, A., Child, A., Rowntree, J. el al. Marfan’s syndrome: succesuful pregnancy after aortic root and arch replacement. BJOG 2002, 109, p. 1187-1188.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2010 Číslo 2- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Léčba refrakterní hyperaktivity detruzoru
- Kořenový syndrom v ambulanci praktického lékaře
- Zúžení průdušnice, diagnostika a možné způsoby řešení
- Diferenciálna diagnóza edému (edémových stavov)
- Miniportréty slavných českých lékařů Profesor MUDr. Antonín Přecechtěl – zakladatel moderní české otorinolaryngologie
- Populace, její zdraví a proměny (2. část)
- Spolupráce zaměřena na zlepšení diagnostiky a léčby
- Výživa a její vliv na zdravotní stav dětí
- JUBILEA
-
Evoluce a evoluční teorie pro lékaře II.
Evoluce – vědecký fakt - Klíšťová meningoencefalitida
- Zoonózy a psychické poruchy, jejich význam pro klinickou praxi
- Advance directives v Evropě
- Kardiální komplikace chronické obstrukční plicní nemoci
- Projekt COPAT – současné možnosti léčby obezity v ambulanci praktického lékaře pro děti a dorost
- Pamatují si naši pacienti rizikové faktory kardiovaskulárních onemocnění?
- Prevence zneužívání léků a přístupy při zvládání lékové závislosti
- Akutní disekce aorty u gravidních žen s Marfanovým syndromem
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Zúžení průdušnice, diagnostika a možné způsoby řešení
- Kořenový syndrom v ambulanci praktického lékaře
- Diferenciálna diagnóza edému (edémových stavov)
- Prevence zneužívání léků a přístupy při zvládání lékové závislosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



