-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Klíšťová meningoencefalitida
Tick-borne meningoencephalitis
The tick-borne meningoencephalitis virus has probably circulated among animals in localised natural habitats for a very long time. Human infections appeared for the first time in central Europe in the 1940’s, however they rapidly spread to most of the countries of the continent. There are currently about 10,000 reported cases of tick borne meningoencephalitis in Europe, of which 500–1 000 are in the Czech Republic. Small rodents act as a reservoir of infection, the Ixodes ricinus tick in any developmental phase then becomes infected from sucking the blood of the rodent. These ticks then spread infection in both healthy animals and humans. Safe protection against this potentially life threatening disease is provided by an inactivated vaccine.
Key words:
ticks, meningoencephalitis, natural habitats, inactivated vaccines.
Autoři: J. Havlík
Působiště autorů: 1. Infekční klinika 2. LF UK, FN Na Bulovce, Praha ; Přednostka: doc. MUDr. Vilma Marešová, CSc. ; Univerzita Karlova v Praze
Vyšlo v časopise: Prakt. Lék. 2010; 90(2): 69-72
Kategorie: Přehledy
Souhrn
Virus klíšťové meningoencefalitidy koloval mezi živočichy v přírodních ohniscích patrně odedávna. Lidské infekce se prvně objevily ve střední Evropě ve čtyřicátých letech minulého století, ale rychle se rozšířily do většiny zemí tohoto kontinentu. V posledních letech je ročně v Evropě hlášeno kolem 10 000 klíšťových meningoencefalitid, z toho v České republice 600 až 1 000. Zdrojem nákazy jsou nejčastěji drobní infikovaní lesní hlodavci, od nichž se sáním krve nakazí kterékoliv z vývojových stádií klíšťat Ixodes ricinus. Ta pak šíří infekci jak na dosud zdravé živočichy, tak na člověka. Bezpečnou ochranou před touto i život ohrožující infekcí je inaktivovaná vakcína.
Klíčová slova:
klíšťata, meningoencefalitis, přírodní ohniska, inaktivované vakcíny.Úvod
Klíšťová meningoencefalitida patří mezi přírodní ohniskové nákazy, neboť její výskyt plně odpovídá Pawlovskeho definici: vyskytuje se v ohraničených přírodních oblastech, v nichž v průběhu evoluce došlo ke speciálním vztahům mezi mikroorganismem (virem) a jeho nosičem-vektorem, což je klíště (1). To při sání krve přenáší patogeny na obratlovce, u nichž dochází k různě dlouho trvající virémii. Pokud na nich sají v té době krev neinfikovaná vývojová stadia klíšťat, stávají se transstadiálními nosiči viru, kteří v průběhu dalšího vývojového stádia při sání krve dosud neinfikovaných obratlovců je nakazí a celý koloběh viru v ohnisku se opakuje.
Epidemiologie
Přírodní ohnisko klíšťové meningoencefalitidy (dále (KME) musí splňovat podmínky umožňující přežívaní klíšťat i jejich hostitelů, především drobných obratlovců – hlodavců, ptáků i plazů. Mezi tyto podmínky patří klimaticky vhodné prostředí s dostatečnou vlhkostí a teplotou. Taková místa jsou ve značné části mírného pásma Evropy a Asie v nadmořských výškách do 800 m, v Alpách až do 1 300 m, nízký podrost na okrajích listnatých lesů, lesní mýtiny, křovím obrostlé cesty podél luk, zarostlých údolí potoků, řek i vodních nádrží.
Klíšťata nejsou v hustých monokulturách jehličnatých lesů. V závislosti na klimatických i územních podmínkách se počet infikovaných klíšťat v přírodním ohnisku může měnit. Za příznivých podmínek se oblasti výskytu KME mohou rozšiřovat, jsou-li nepříznivé (rekultivace, vyklučení křoví a mlází), mohou dočasně nebo trvale vyhasínat (2).
Přírodní ohniska s kolováním viru KME mezi klíšťaty a drobnými i většími obratlovci jistě existovala odedávna, ale k jejich poznání došlo teprve po výskytu častějších lidských nákaz až ve třícátých (3) až padesátých letech 20. století (4). V té době byla lidská onemocnění KME hlášena pouze z několika oblastí střední Evropy a ze Sibiře. V uplynulých desetiletích se oblasti výskytu KME značně rozšířily do mnoha zemí – což dosud pokračuje – a zatím není objasněno, proč tomu tak je (5).
V současné době se přírodní ohniska KME vyskytují jednak v souvislém pásmu od střední Evropy až na Dálný východ Asie, jednak ostrůvkovitě v severní i jižní Evropě.
V ČR je nejvyšší výskyt infikovaných klíšťat i lidských onemocnění KME v jižních, středních a západních Čechách podél toků řek Vltavy, Malše, Sázavy a Berounky, vodních nádrží Lipno, Orlík a Slapy, v okolí Ústí nad Labem, na Moravě jižně od Brna a ve Slezsku. ČR patří v Evropě k zemím s nejvyšším výskytem KME, a ročně je v posledních letech hlášeno 600, ale i přes tisíc manifestních lidských onemocnění (6, 7) (graf 1). K 30. 12. 2009 bylo podle neúplných údajů již hlášeno 815 nových onemocnění KME.
Graf 1. Výskyt KME v ČR (MUDr. Č. Beneč, SZ/Praha) 
Virus KME
Virus KME patří mezi arboviry (arthropod-borne viruses), čeleď Flaviviridae. Do této skupiny virů přenášených členovci (klíšťata, komáři) patří vedle viru KME devět dalších virů vyvolávajících encefalitidy. Jde o sférické viry velikosti přibližně 50 nm; virus KME vytváří cytopatický efekt na embryonálních kuřecích buňkách i na Vero buňkách. Obsahuje 3 strukturálně odlišné bílkoviny:
- kapsidový protein C s jednovláknovou RNA,
- protein M v lipidové membráně, a
- povrchový glykoprotein E, proti němuž jsou zaměřeny virusneutralizační protilátky, které jsou odpovědné za imunitu.
Ničí ho pasterizace i teplota nad 60° C, snáší nízké pH. Odlišují se subtypy viru KME, a to
- evropský,
- sibiřský, a
- dálněvýchodní, jakož i virus
- looping ill, který vyvolává encefalitidu u ovcí, zatímco lidské infekce tímto virem jsou zcela vyjímečné.
Všechny uvedené viry mají z 96 % shodný glykoprotein E, takže vakcína proti KME chrání před nákazou všemi těmito viry, i když klinický průběh neuroinfekce způsobené jednotlivými subtypy je rozdílný (8, 9).
Evropský virus KME byl prvně izolován v roce 1948 českými autory Galliou a Rampasem z klíšťat z oblasti Berounska, Strakonicka a Vyškovska a vykultivován na myších mozcích (10). Holandští virologové izolovali v roce 1954 shodný virus z klíšťat z několika oblastí v Rakousku. Tento subtyp je dominující v evropských zemích a také v evropské části bývalého Sovětského svazu.
Sibiřský subtyp izoloval v roce 1937 Zilber z mozků zemřelých na Sibiři a vyskytuje se v pobaltských republikách, západní části Ruské federace, Bělorusku, Ukrajině a v oblastech jižně od Uralu.
Dálněvýchodní subtyp přenášejí klíšťata Ixodes scapularis a infekce se vyskytuje na východ od Uralu až po japonský ostrov Hokkaido.
Virus looping ill byl poznán již v roce 1929 a jeho výskyt je omezený na Skotsko a některé části Norska (2).
Klíšťata
Nejčastějším přenašečem evropského subtypu viru KME je klíště obecné – Ixodes ricinus. Jeho vývoj je jako i u dalších druhů klíšťat třífázový a trvá podle klimatických podmínek 6 měsíců až 8 let, zpravidla aspoň 2 roky. Pro přežití vývojových stádií klíšťat je nezbytná dostatečná relativní vlhkost prostředí (92 %) a teplota půdy nesmí ani v zimě klesnout pod -7 °C, jinak dojde k jejich úhynu. Oplozená samice ukládá zpravidla na podzim nebo také v letních měsících pod listí 500–5 000 vajec, z nichž se na jaře po hibernaci, či v pozdních letních měsících již za 1 měsíc líhnou droboučké téměř bezbarvé šestinohé larvy velikosti 0,6–1,0 mm. Z uvedeného vysokého počtu vajec se vyvine jen 5 %, tj. kolem 100 larev, ostatní uhynou nebo je zničí predátoři.
Larvy, které přežijí, vylézají na trávy do výšky asi 10 cm, kde vyčkávají na procházející drobné savce, jako jsou myšice křoviná, norník rudý a další malí hlodavci, ptáci nebo plazi. Larvy reagují na pohyb živočichů, spouštěji se ze spodní strany trávy a přichycují se na tyto živočichy nejčastěji kolem očí, na uši a kolem řitního otvoru, kde sají krev po dobu 2 až 5 dní.
Pro přetrvávání viru KME v ohnisku je nezbytná přítomnost rychle se množících drobných hlodavců. Ti, kteří byli nakaženi sáním infikované nymfy, se stávají při virémii zdrojem infekce pro dosud nenakažené larvy, které zůstanou infekční i po přeměně v nymfy a dospělce. Na napadených obratlovcích bývají desítky larev. Bezpříznaková virémie trvá u drobných obratlovců několik dní – zatímco u větších obratlovců je jen krátkodobá. Po nasátí krve larvy odpadnou a v hrabance na zemi prodělávají během 6–12 měsíců přeměnu v již osminohou nymfu. Ta je o něco větší, vylézá také na byliny, ale již vyšší, do 30–50 cm a zase vyčkává, až bude procházet malý nebo i větší živočich (myšovití hlodavci, králík, veverka, lasice nebo i vysoká zvěř, ale i člověk), na něhož se přichytí a po 2–7 dní saje krev.
Larvy i nymfy jsou bezpohlavní a sají do přeměny krev jen jednou. Vydrží hladovět i několik měsíců a jejich přežití závisí především na dostatečné vlhkosti prostředí a vnější teplotě, která při jejich přezimování v úkrytu nesmí klesnout pod -7 °C. Ve střední Evropě je nejvyšší výskyt larev i nymf koncem dubna a v květnu a pak během září. Nepříznivé podmínky a predátory přežije jen asi 10 % nymf, které po nasátí krve opět spadnou na zem, skryjí se pod listí a po 3–6 měsících se vyvíjejí hnědavě zbarvení dospělci, samci a samice.
Samice měří 3–4 mm a po ssání krve může svou hmotnost zvýšit až stokrát, samec je menší, měří 2–3 mm a nesaje krev. Z původních několika tisíc vajec dospěje asi 5 klíšťat (obr. 1). Krve nasátá samice klíštěte po kopulaci snáší na zemi do listí vejce a krátce poté hyne. Infikovaná samice může virem kontaminovat vejce – k takovému transovariálnímu přenosu viru KME však dochází jen asi v 1 %, významnější je však přenos transstadiální. Pro klíšťata virus není patogenní. Ovšem infekci na člověka může přenést kterékoliv vývojové stádium.
Obr. 1. Vývojová stádia klíšťat a jejich úhyn během vývoje 
Promořenost dospělých klíšťat i jejich vývojových stádií virem je značně rozdílná v různých zemích, ale i v jednotlivých ohniscích a mění se i během let. Prevalence promořenosti v populaci klíšťat může kolísat podle literárních údajů od 0,05 % (Itálie) až po 27 % i více (Pobaltské republiky – Litva průměr 7–8 %). V ČR se pohybuje od 0,5 do 2 %; je rozdílná v jednotlivých krajích (nejvyšší v Jihočeském) i letech v závislosti na klimatických podmínkách (1, 2).
Všechna vývojová stadia klíšťat mají shodné bodavé a sací ústrojí a jejich sliny obsahují četné bioaktivní látky. Ty působí jednak proti srážení krve, jednak anesteticky (sání klíštěte nebolí) a imunosupresivně. Obsahují také toxiny a látku, která po několika hodinách vytvoří tzv. cement, který zanořené sací ústrojí do ranky „zacementuje“. Proto se přisáté klíště obtížně odstraňuje. Teprve po nasátí krve se cement rozpouští a klíště odpadne. Klíšťata mají orgány, které umožňují reagovat na tepelné i chemické stimuly, jakož i na pohyby způsobené probíhajícím živočichem.
Sliny infikovaného klíštěte obsahují virus KME, jehož množství stoupá při sání krve, které může trvat až 10 dní. K přenosu nákazy však může dojít již při krátkodobém sání. Klíště před sáním vyhledává nejvhodnější místo k přisátí, proto je vhodné po návratu z rizikové oblasti vyklepat šaty a prohlédnout oblasti s nejtenčí kůží (gluteální krajina, pod kolenem, v podpaží, u dětí kolem uší) a nalezené klíště co nejdříve odstranit, aby nedošlo k přisátí.
Patogeneze KME
Po přisátí infikovaného klíštěte se virus jeho slinami dostává do kůže, v jejichž buňkách se množí a až u dvou třetin postižených dochází k tvorbě specifických protilátek, aniž dojde k manifestnímu onemocnění – došlo k bezpříznakové infekci. Tímto způsobem dochází k latentnímu promořování populace. U zbývající třetiny osob dochází k průniku viru mízou do lymfatických uzlin, v nichž probíhá další replikace viru, a ten se dostává za 7–10 dní do krevního oběhu, nastává primární virémie. Objevuje se horečka a necharakteristické příznaky s bolestí hlavy, svalů a únavností. Tento stav trvá jeden či dva dny, a pokud tím onemocnění končí, označujeme je jako abortivní průběh KME.
Pokud onemocnění pokračuje, pak šlo o prodromální příznaky a po krátkém bezpříznakovém období dochází k sekundární virémii, při níž virus proniká do mozku a objevují se neurologické příznaky.
Klinický obraz
Inkubační doba KME do primární virémie je nejčastěji 7–10 dní, v rozmezí 2–28 dní. Děti do 15 let tvoří v ČR jen 10–15 % nemocných. Nejvyšší počet nemocných je ve stáří 35 – 65 let.
Manifestní onemocnění KME probíhá až v 80 % ve dvou fázích.
První fáze je s horečkou a únavností a trvá jen několik dní. Po jednom až třech dnech bez klinických potíží dochází k druhé virémii, kdy se již objevují příznaky z postižení centrálního nervového systému. Onemocnění pak probíhá buď jako serózní meningitida, což bývá nejčastěji u dětí, nebo jako meningoencefalitida, pokud dojde k parézám jako encefalomyelitida nebo vzácněji jako nejzávažnější forma bulbocervikální.
Při formě meningitické stoupá horečka přes 38 °C, jsou bolesti hlavy a svalů a rozvíjí se meningeální syndrom. Pacienti trpí nevůli nebo i zvracejí, jsou světloplaší, mají tuhá záda a bez opory rukou se nemohou posadit. Lumbální punkce přináší nemocným subjektivně zmenšení potíží. Při punkci vytéká mok pod zvýšeným tlakem, jsou v něm desítky až stovky většinou lymfocytů a hladina proteinů bývá lehce zvýšená. Takto probíhá KME především u dětí s dobrou předpovědí na úplné uzdravení během dvou až tří týdnů (7, 11).
Se stoupajícím věkem narůstají počty nemocných se závažným až život ohrožujícím průběhem. Tehdy je nejčastější forma meningoencefalitická, při které kromě dříve uvedených příznaků u formy meningitické trpí pacienti poruchou spánku či jeho reverzí, mají třes jazyka i prstů u rukou, ale i končetin, řeč je zpomalená, někdy špatně srozumitelná, je psychický útlum, někdy i dezorientace až delirantní stav. Tyto příznaky ustupují pomalu, trvají i týdny, v rekonvalescenci přetrvává nesoustředěnost a značný pocit únavy i řadu měsíců. Ojediněle může tato forma nemoci skončit smrtí.
Při encefalomyelitické formě KME se připojují i po skončení horeček chabé parézy, které nejčastěji postihují n. facialis a n. obducens, ale při postižení některých částí krční míchy dochází k asymetrické obrně svalů pletence pažního. Obrna lícního nervu se zpravidla pomalu upraví, ale postižené svaly pletence pažního mnohdy atrofují a i po intenzivní rehabilitaci známky postižení přetrvávají celý život.
Při bulbární formě může dojít ke kvadruparéze, obrny postihují i dýchací svalstvo, je porušená činnosti sfinkterů, častá je retence moči a přes resuscitační péči tito nemocní nejčastěji podléhají buď samotné nemoci, nebo připojeným komplikacím. Doléčování paretických nemocných probíhá v lázeňských zařízeních a trvá i léta.
I když formy encefalomyelitické a bulbární se vyskytují především u starších osob, mohou postihnout i děti. V ČR umírají na KME každý rok 2–4 nemocní, tj. 0,1-0,3 % z celkového počtu onemocnělých (6, 11).
Od paretických forem KME je třeba odlišit tzv. „klíšťovou obrnu“, což je benigní neuralgie způsobená ixodinem ze slin neinfikovaných klíšťat.
Klinický průběh KME způsobené sibířským a dálněvýchodním typem viru je mnohem závažnější. Pravidlem je těžká encefalitická a encefalomyelitická forma s psychickými poruchami a parézami. Zhruba 10–20 % postižených nemoci podléhá a u značné části těch, kteří přežijí, zůstávají trvalé změny psychické i chabé parézy (12).
Diagnóza a diferenciální diagnostika
Vedle klinického obrazu je významný anamnestický údaj o přisátí klíštěte v možné inkubační době. Sérózní meningitidy mohou vyvolat četné enteroviry (Coxsackie, ECHO), virus příušnic i některé respirační viry. Podobný klinický obraz mohou mít anikterické leptospirózy, ale nejčastěji neuroborelióza. Promoření klíšťat mikrobem Borrelia burgdorferi je podstatně častější než virem KME, a nejsou vzácné duální infekce oběma uvedenými patogeny.
Je více laboratorních metod, které mohou potvrdit diagnózu KME, ale ta se zpravidla potvrzuje pozitivními titry IgM protilátek zjištěných metodou ELISA, které stoupají již krátce po nákaze. Přetrvávají jen několik týdnů, ale během té doby stoupají hodnoty IgG protilátek. Ty jsou pozitivní dlouhodobě a jejich hladina se nemění i u pacientů, kteří KME prodělali již v minulosti. Uvedené vyšetření metodou ELISA je v našich podmínkách pro KME specifické, protože zkříženě pozitivní jsou hodnoty pouze při infekci jinými flaviviry (jako při dengue nebo žluté zimnici), což jsou infekce, které se u nás nevyskytují. Sérologická vyšetření také pomohou potvrdit, nebo vyloučit jiné původce serózní meningitidy.
Léčba
Specifická antivirová terapie KME zatím není známa. Specifický gamaglobulin se neosvědčil. Nezbytný je klid na lůžku (vesměs při hospitalizaci), při světloplachosti omezit přístup světla, při krutých bolestech hlavy odlehčovací lumbální punkce, dle potřeby protiedémová terapie, symptomatické tlumení potíží, úprava vodního i minerálního hospodářství, jakož i péče o kůži. Vzhledem k často přetrvávajícím potížím (psychická labilita, bolesti hlavy, únavnost) jsou nezbytné ambulantní kontroly po dobu jednoho roku po onemocnění, u paretických nemocných lázeňské doléčování.
Profylaxe a prevence
V rizikových oblastech výskytu KME je základním profylaktickým opatřením vhodné oblečení a obutí při návštěvě lesa. Nejvhodnější je světlé šatstvo (aby klíšťata byla vidět) zakrývající větší část těla a uzavřené boty. Nekrytá část těla i oblečení se má postříkat vhodným repelentem. Po návratu z lesa oděv vyklepat a zvláště u dětí prohlédnout intertriginózní místa, zda někde není dosud pohyblivé nebo přisáté klíště. Přisáté klíště pinzetou odstranit kývavými pohyby co nejdříve. Pokud v rance zůstala část klíštěte, ihned je odstranit. Nepoužívat k odstranění klíštat prsty, oleje, masti nebo dezinfekční prostředky.
Rozhodující preventivní ochranou je očkování. Používají se inaktivované vakciny pro dospělé i děti od dvou let FSME IMMUN a ENCEPUR, které zaručují při časově správné i.m. aplikaci spolehlivou tříletou ochranu s minimálním výskytem nežádoucích účinků (13). Nejvhodnější doba pro očkování jsou zimní měsíce, což zajistí tvorbu protilátek již od začátku jarní aktivity klíšťat.
Vakcina FSME IMMUN (nyní Baxter) byla poprvé uvedena v Rakousku v roce 1979 (14) a od té doby prošla několika stupni vývoje. V současné době je připravována pomnožením viru KME typ Neudörfl na fibroblastech kuřecích embryí. Virus je inaktivován formaldehydem a je provedena purifikace ultracentrifugací. Každá šarže je testována na účinnost a bezpečnost, antigen je adsorbován na aluminium hydroxyd a jako stabilizátor přidáno lidské sérum. Dávka pro dospělé obsahuje v 0,5 ml 2,4 nm antigenu, pro děti od 2–15 let dávka Junior obsahuje v 0,25 ml 1,2 nm antigenu. Aplikují se tři dávky nejlépe do m. deltoideus v intervalech den 0, druhá za 1 až 3 měsíce a třetí 5–12 měsíců po druhé dávce. Doplňující dávka se podává za 3 roky a dále vždy za 3–5–(8) let. Očkovat se ovšem může kdykoliv během roku, což je tzv. urychlené očkování, kdy podávají injekce v den 0 a 14 a třetí dávka za 5–12 měsíců.
V roce 1989 byla v Německu připravena obdobným způsobem jako FSME vakcina z viru KME typ K23 (Karlsruhe) vakcina ENCEPUR (15) (Behringwerke, nyní Novartis) a v roce 1996 její pediatrická varianta (16). V dalších letech prošly obě tyto vakcíny výrobními změnami a současná očkovací látka neobsahuje stabilizátor a v 0,5 ml dávky pro dospělé je 1,5 nm antigenu, v pediatrické verzi v 0,25 ml je 0,75 nm antigenu. Při běžném očkování v zimních měsících jsou aplikační termíny všech tří dávek shodné jako u FSME, při zrychleném očkování se vakcíny aplikují ve dnech 1–7–21, první booster za 12–18 měsíců a pak každých 3–5 let. Ochranný efekt obou typů očkovacích látek je shodný a zabraňuje vzniku nákazy kterýmkoliv typem viru KME.
Nežádoucí reakce po očkování se vyskytují zřídka a jsou vesměs mírné. V Rakousku je vakcinou FSME proočkováno více než 80 % obyvatelstva a dřívější výskyt stovek onemocnění ročně se snížil na několik desítek, a tato infekce zcela vymizela v dětském věku (17). Proočkovanost v ČR je v celostátním průměru kolem 17 % (obr. 2), v jednotlivých krajích kolísá od více než 30 % v nejrizikovějším kraji Jihočeském až pod 10 % v krajích s nižším výskytem KME. Ve všech krajích je podstatně vyšší proočkovanost dětské populace, a ve věku do 15 let je také nemocnost KME nejnižší. Aby se snížil enormně vysoký výskyt KME v ČR je nezbytná vyšší proočkovanost občanů střední a starší věkové skupiny, u nichž je průběh onemocnění vždy závažný (18).
Obr. 2. Mapa proočkovanosti v ČR podle regionů (Baxter Czech, 2008) 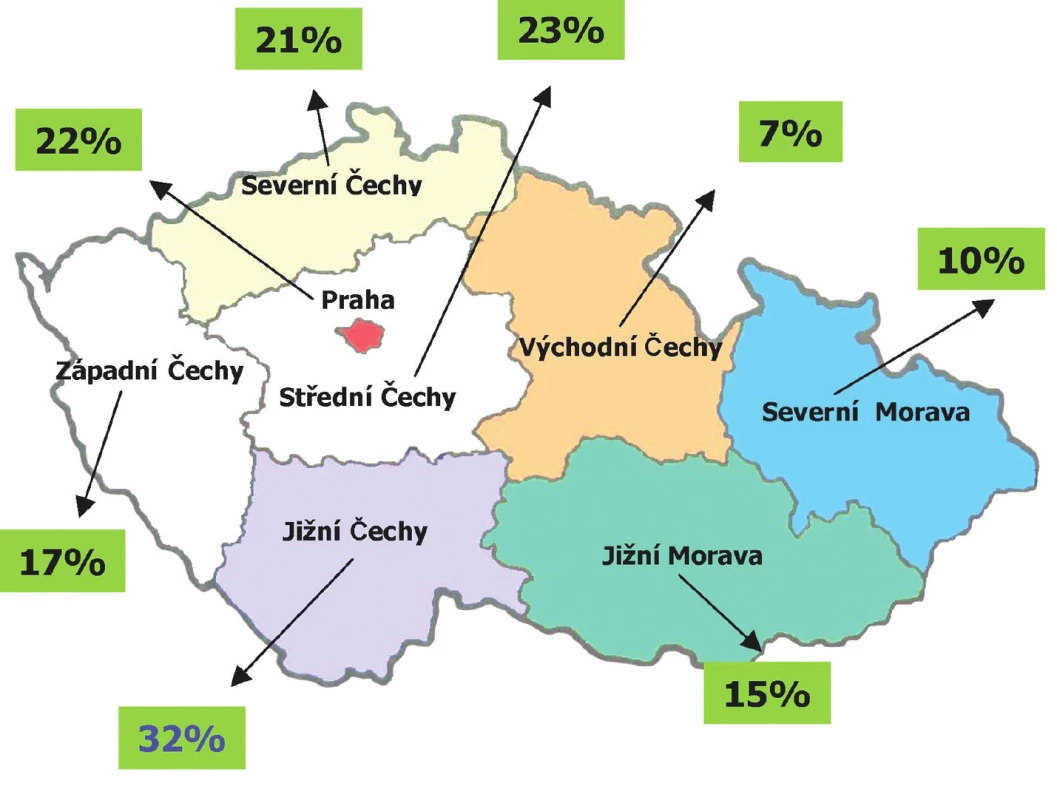
Prof. MUDr. Jiří Havlík, DrSc.,
emeritní profesor
1. Infekční klinika 2. LF UK
FN Na Bulovce
Budínova 2
180 81 Praha 8
E-mail: jiri.havlik@vakcinace.cz
Zdroje
1. Heinz, F.X. Etiology. In: Management of tick-borne encefalitis. Baxter 2006, p. 7-16.
2. Danielová, V. Epidemiologie klíšťové encefalitidy. Zdravotnické noviny-Diagnoza 2000, 5, s. 8.
3. Schneider, H. Über epidemische akute „Meningitis serosa“. Wien Klin Wochenschrift 1931, 44, s. 350-352.
4. Havlík, J., Marsa, J., Potužník, V. Klíšťová encefalitida na Českobudějovicku. Prakt. Lék. 1956, 36(12), s. 271-273.
5. Zeman, P., Benes, C. A tick-borne encefalitis ceiling in Central Europe has moved upwards during the last 30 years: possible impact of global warming? Int. J. Med. Microbiol. 2004, 293, Suppl 37, p. 48-54.
6. Havlík, J. Klíšťová encefalitida a jak nákaze předejít. Postgrad. Med. 2006, 8(3), s. 926-929.
7. Havlík, J. Onemocnění přenášená klišťaty – prevence a léčba u dětí. Pediatrie po promoci 2005, II/5, s. 25-30.
8. Heinz, F.X. Molecular aspects of TBE virus research. Vaccine 2003, 21(1), p. 3-10.
9. Holzmann, H., Vorobyova, M.S., Landyshenskaya, I.P. et al. Molecular epidemiology of tick-borne encefalitis virus: cross-protection between European and Far Eastern serotypes. Vaccine 1992, 10, p. 345-349.
10. Galia, F., Rampas, J., Hollender, L. Laboratorní infekce encefalitickým virem. Čas. Lék. Čes. 1949, 88, s. 224-229.
11. Chmelík, V. Klíšťová meningoencefalitida. Pediatrie pro praxi 2009, 10(5), s. 306-310.
12. Ternovoi, V.A., Korzhukov, G.P., Sokolov, Y.V. et al. Tick-borne encephalitis with hemorrhagic syndrome, Novosibirsk region, Russia, 1999. Emerg. Infect. Dis. 2003, 9(6), p. 743-746.
13. Zent, O., Broker, M. Tick-borne encephalitis vaccines: past and present. Expert. Rev. Vaccines. 2005, 4, p. 747-755.
14. Kunz, C.H., Hofmann, H., Stary, A. Field studies with a new tick-borne encephaitis (TBE) vaccine. Zbl. Bakt. Orig. 1976, 243, p. 141-144.
15. Bok, H., Klockmann, U., Juengst, C. et al. A new vaccine against tick-borne encefalitis: initial trial in man including a dose-response study. Vaccine 1990, 8, p. 22-24.
16. Girsgdies, O.E., Rosenkranz, G. Tick-borne encephalitis development of a pediatric vaccine. A controlled, randomised, double-blind and multicentre study. Vaccine 1996, 14, p. 1421-1428.
17. Kunz, C.H. TBE vaccination and the Austrian experience. Vaccine 2003, 21(1), p. 50-55.
18. Havlík, J. Vliv očkování na výskyt klíšťové meningoencefalitidy v České republice. Postgrad. Med. 2009, 11(6), p. 615-618.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2010 Číslo 2- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Léčba refrakterní hyperaktivity detruzoru
- Kořenový syndrom v ambulanci praktického lékaře
- Zúžení průdušnice, diagnostika a možné způsoby řešení
- Diferenciálna diagnóza edému (edémových stavov)
- Miniportréty slavných českých lékařů Profesor MUDr. Antonín Přecechtěl – zakladatel moderní české otorinolaryngologie
- Populace, její zdraví a proměny (2. část)
- Spolupráce zaměřena na zlepšení diagnostiky a léčby
- Výživa a její vliv na zdravotní stav dětí
- JUBILEA
-
Evoluce a evoluční teorie pro lékaře II.
Evoluce – vědecký fakt - Klíšťová meningoencefalitida
- Zoonózy a psychické poruchy, jejich význam pro klinickou praxi
- Advance directives v Evropě
- Kardiální komplikace chronické obstrukční plicní nemoci
- Projekt COPAT – současné možnosti léčby obezity v ambulanci praktického lékaře pro děti a dorost
- Pamatují si naši pacienti rizikové faktory kardiovaskulárních onemocnění?
- Prevence zneužívání léků a přístupy při zvládání lékové závislosti
- Akutní disekce aorty u gravidních žen s Marfanovým syndromem
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Zúžení průdušnice, diagnostika a možné způsoby řešení
- Kořenový syndrom v ambulanci praktického lékaře
- Diferenciálna diagnóza edému (edémových stavov)
- Prevence zneužívání léků a přístupy při zvládání lékové závislosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



