-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Hyponatriémia – vzácna komplikácia nefrotického syndrómu
Hyponatremia – serious complication of nephrotic syndrome
Hyponatremia (s-Na <135 mmol/L) is the most common electrolyte abnormality in hospitalized children. A decrease in serum sodium concentration leads to neurological symptomatology and in severe cases is responsible for significant morbidity and mortality. Dreaded and potentially fatal complication of a rapid hyponatremia correction is the osmotic demyelination syndrome. Important risk factors for hyponatremia include nephrotic syndrome. Only anecdotal case reports of hyponatremic encephalopathy associated with nephrotic syndrome are described in the literature. The authors present a rare case report of a severe symptomatic hyponatremia (s-Na 111 mmol/L, relative urinary potassium excretion 92%) in a 6-year-old boy with relapse of nephrotic syndrome and transient renal dysfunction (AKI pRIFLE).
The treatment of severe hyponatremia with edema is demanding and requires considerable clinical experience. According to the classical hypothesis, in the pathophysiology of nephrotic edema large proteinuria and hypoalbuminemia can lead to intravascular hypovolemia and the kidneys retain sodium and water via compensatory mechanism in an attempt to maintain adequate circulatory volume („underfill hypothesis”). On the other hand, in glomerulonephritis the primary intrarenal retention of sodium and water applies to edema formation („overfill” hypothesis). The main task for a clinician is to recognize the basic mechanism of edema and to determine the correct treatment. In practice, relative urinary potassium excretion in the initial urine sample might be helpful. Excretion index higher than 60% suggests an intravascular hypovolemia.
Conclusion: Hyponatremia is a serious complication of relapse of nephrotic syndrome. The treatment of such complication should be managed by skilled clinician. The goal of the correction is a slow and gradual increase of serum sodium concentrations by a maximum of 12 mmol/L/24 hours in hyponatremic encephalopathy.
Keywords:
hypervolemic hyponatremia – Edema – nephrotic syndrome – underfill and overfill hypothesis
Autoři: S. Szórádová; M. Chocholová; Ľ. Podracká
Působiště autorů: Detská klinika LFUK a NÚDCH, Bratislava, Slovensko
Vyšlo v časopise: Čes-slov Pediat 2020; 75 (2): 103-107.
Kategorie: Kazuistika
Souhrn
Hyponatriémia (s-Na <135 mmol/L) je najčastejšia elektrolytová abnormalita u hospitalizovaných detí. Prudký pokles sérovej koncentrácie sodíka vedie k neurologickej symptomatológii a v závažných prípadoch zodpovedá za signifikantnú morbiditu a mortalitu. Obávanou a potenciálne fatálnou komplikáciou rýchlej korekcie hyponatriémie je syndróm osmotickej demyelinizácie.
K zriedkavým príčinam hypervolemickej hyponatriémie patrí nefrotický syndróm. V literatúre sú opísané len anektodálne klinické prípady hyponatriémickej encefalopatie komplikujúcej rozvinutý nefrotický syndróm. Autori prezentujú vzácnu kazuistiku závažnej symptomatickej hyponatriémie (s-Na 111 mmol/L, relatívna exkrécia močového kália 92 %) u 6-ročného edematózneho chlapca s relapsom nefrotického syndrómu a tranzientnou renálnou dysfunkciou.
Liečba závažnej hyponatriémie pri opuchoch je náročná a vyžaduje značnú klinickú skúsenosť. V patofyziológii nefrotických opuchov sa podľa klasickej hypotézy uplatňuje veľká proteinúria a hypoalbuminémia, ktorá môže viesť k intravaskulárnej hypovolémii a obličky v snahe udržať adekvátny cirkulačný objem kompenzačnými mechanizmami sekundárne retinujú sodík („underfill“ hypotéza). Na druhej strane, opuchy pri glomerulonefritídach vznikajú na podklade primárnej intrarenálnej retencie sodíka a vody („overfill“ hypotéza). Hlavnou úlohou klinika je rozlíšiť základný patomechanizmus opuchov a podľa toho určiť správny liečebný postup. V praxi je nápomocné vyšetrenie relatívnej exkrécie močového kália v iniciálnej vzorke moču, pričom hodnota nad 60 % svedčí pre intravaskulárnu hypovolémiu.
Záver: Hyponatriémia je závažnou komplikáciou relapsu nefrotického syndrómu, ktorej liečba patrí do rúk skúseného klinika. Cieľom korekcie je pomalá a postupná úprava sérových koncentrácií sodíka maximálne o 12 mmol/l/24 hodín pri hyponatriemickej encefalopatii.
Klíčová slova:
hypervolemická hyponatriémia – edémy – nefrotický syndrom – underfill a overfill hypotéza
ÚVOD
Hyponatriémia (s-Na <135 mmol/L) je najčastejšia elektrolytová porucha, ktorá sa vyskytuje u 17 až 45 % detí hospitalizovaných v terciárnych pediatrických centrách [1, 2]. Varujúce demografické údaje sú veľkou výzvou pre pediatrov, lebo prudký pokles sérovej koncentrácie sodíka môže spôsobiť závažné neurologické poškodenie so signifikantnou morbiditou a mortalitou. Náhly pokles s-Na pod 125 mmol/L je zvyčajne sprevádzaný emergentnou neurologickou symptomatológiou ako nauzea, malátnosť, iritabilita a môže v závažných prípadoch vyústiť do hyponatriémickej encefalopatie s poruchou vedomia a tonicko-klonickými kŕčmi. Príčiny hyponatriémie sú rôznorodé. Diferenciálna diagnostika sa odvíja od stavu hydratácie pacienta a vyšetrenia sodíka v jednorázovej vzorke moču.
Hypervolemickú hyponatriémiu pri nefrotickom syndróme typicky sprevádzajú edémy. Masívny generalizovaný opuch zvyčajne postihuje deti s idiopatickým nefrotickým syndrómom na podklade minimálnych zmien glomerulov. Veľká proteinúria a závažná hypoalbuminémia signifikantne znižujú onkotický kapilárny tlak a efektívny cirkulačný objem. To vedie k opuchovému stavu označovanému ako tzv. „underfill“ (underfill hypotéza). V patogenéze hrá kľúčovú úlohu nadmerná aktivácia endokrinnej osi renín-angiotenzín-aldosterón (RAAS), ktorá vedie k sekundárnej retencii sodíka a vody v obličkách, zvýšenej sekrécii antidiuretického hormónu (ADH) a rezistencii tubulov na átriálne natriuretický peptid (ANP) [3]. Klinický obraz „underfill“ opuchov sprevádzajú charakteristické známky cirkulačnej instability ako tachykardia, hypotenzia, chladné akrá či oligúria. Manifestné prejavy sú dôsledkom fyziologických kompenzačných mechanizmov organizmu s cieľom nastoliť normálnu perfúziu tkanív.
Na druhej strane, edémy pri chronických glomerulonefritídach vznikajú odlišným mechanizmom. V obličkách dochádza k primárnej a/alebo patologickej retencii nátria, ktorá spolu so zníženou filtráciou vedie k zvýšeniu kapilárneho hydrostatického tlaku a vzostupu cirkulačného objemu. Tento opuchový stav sa označuje ako tzv. „overfill“. Pacient s „overfill opuchmi“ nemá klinické známky cirkulačnej instability ale naopak, prítomná je hypertenzia, oligúria a znížená glomerulová filtrácia (GFR). Hoci sa primárna retencia nátria pozoruje najmä u nefrotických pacientov s opuchovým stavom „overfill“, tento patofyziologický mechanizmus sa čiastočne uplatňuje aj u chorých s proteinúriou v stave „underfill“. K aktivácii sodíkových kanálov v obličkových tubuloch prispieva únik plazmínu a serínových proteáz močom (obr. 1).
Obr. 1. Patofyziológia vzniku edémov pri nefrotickom syndrome.
GFR – glomerulová filtrácia
p-cap – kapilárny hydraulický tlak tekutiny
π-cap – kapilárny onkotický tlak tekutiny
Kf – koeficient glomerulovej ultrafiltrácie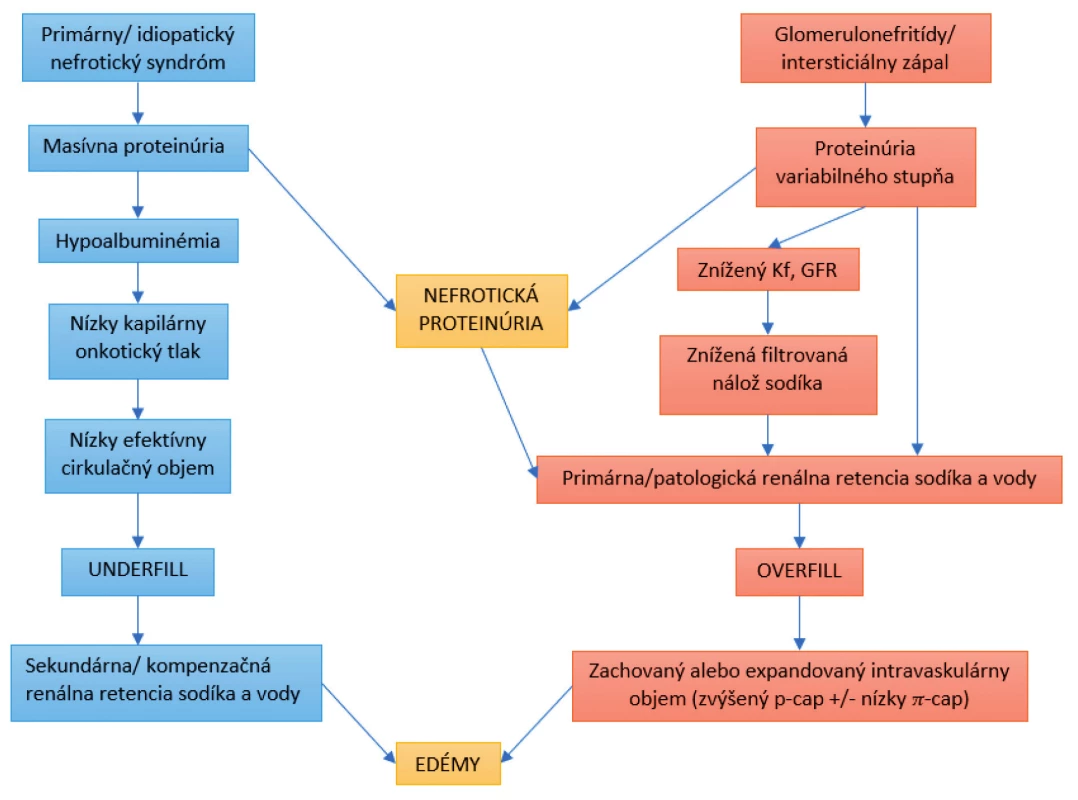
Rozlíšenie opuchov má zásadný význam pre určenie správnej liečby. U chorých s nefrotickým edémom v stave „underfill“ treba byť s diuretickou liečbou obozretný, lebo pri cirkulačnej nedostatočnosti môžu diuretiká indukovať renálne poškodenie a zhoršovať hypoperfúziu tkanív. V praxi sa na diferenciáciu opuchov odporúča jednoduché vyšetrenie relatívnej exkrécie močového kália (odpad sodíka a draslíka v jednorázovej vzorke moču UK/(UK + UNa). Relatívna exkrécia močového kália viac ako 60 % svedčí pre aktivovaný systém RAAS a sekundárnu retenciu nátria so zníženým cirkulačným objemom. Dostatočnú náplň cievneho riečiska a normálnu/nízku aktivitu aldosterónu potvrdzuje nižší index relatívnej exkrécie močového kália (<60 %). Frakčná exkrécia nátria (FENa) per se nedokáže spoľahlivo rozlíšiť jednotlivé typy, lebo k retencii sodíka dochádza aj pri underfill i overfill opuchoch (tab. 1) [4–6].
Tab. 1. Klinicko-laboratórne charakteristiky underfill a overfill hypotézy. 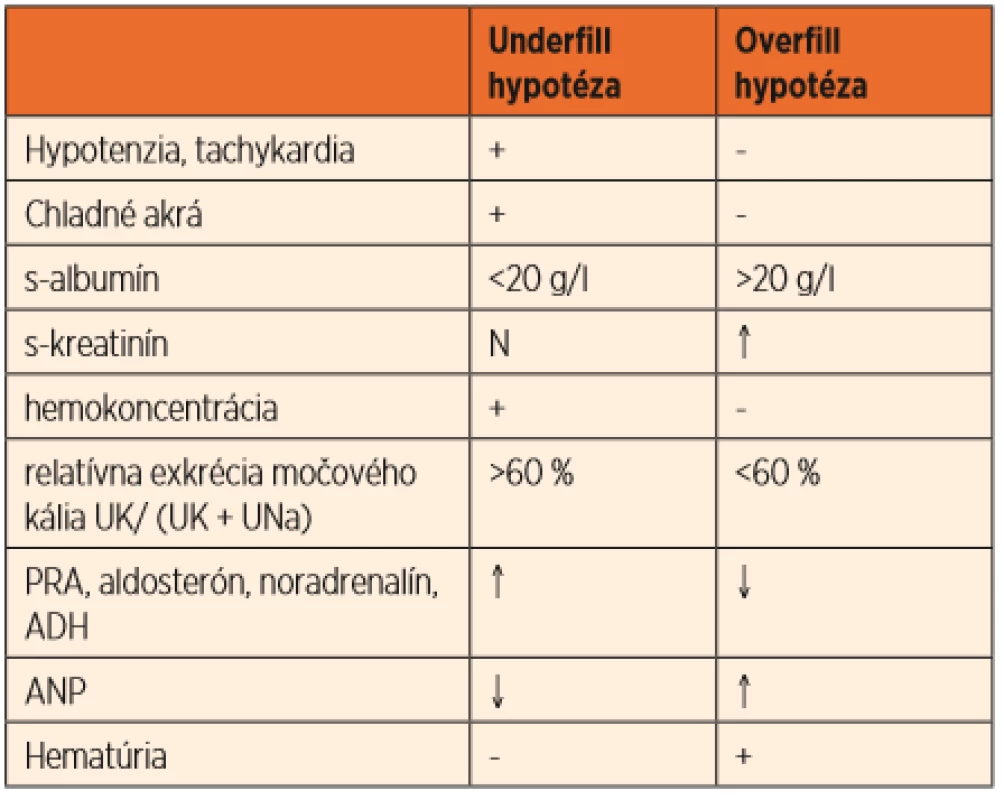
UK – odpad draslíka v jednorázovej vzorke moču
UNa – odpad sodíka v jednorázovej vzorke moču
PRA – plazmatická renínová aktivita
ADH – antidiuretický hormón
ANP – atriálny nátriuretický peptidNapriek heterogenite klinických a biochemických prejavov renálnych opuchov sa symptomatická hyponatriémia pri nefrotickom syndróme vyskytuje ojedinele. Na rozvoji hyponatriémie sa významne podieľa ADH, ktorý stimuluje intravaskulárna hypovolémia v snahe udržať cirkuláciu. Výsledkom kompenzačných procesov je retencia bez-solútovej vody, ktorá môže viesť k dilučnej hyponatriémii [3]. Mozog reaguje na pokles tonicity plazmy adaptačnými zmenami, ktoré spôsobujú náhly únik sodíka, draslíka a organických solútov z mozgových buniek v snahe chrániť mozog pred hroziacim edémom. Obranné kompenzačné mechanizmy sa naplno rozvinú do 48 hodín. Z toho dôvodu je nutné dodržať pomalú rýchlosť korekcie sérového sodíka. Pri rýchlej korekcii deficitu hrozí syndróm osmotickej demyelinizácie, ktorý sa s latenciou niekoľkých dní manifestuje dramatickou neurologickou symptomatológiou [7].
V kazuistike opisujeme zriedkavý prípad 6-ročného chlapca so závažnou symptomatickou hyponatriémiou, ktorá sa náhle rozvinula pri torpídnom relapse nefrotického syndrómu.
KAZUISTIKA
Pacient sa od 3 rokov života liečil pre idiopatický nefrotický syndróm s histologickým obrazom malých abnormalít glomerulov a pre časté relapsy užíval viaceré línie imunosupresív vrátane biologickej liečby rituximabom. Mesiac po vysadení cyklosporínu A došlo k dramatickému relapsu základného ochorenia s masívnymi opuchmi, náhlou dyzartriou, progredujúcou kvalitatívnou poruchou vedomia a zmätenosťou.
Chlapec pri prijatí mal anasarku s ascitom, sklon k hypotenzii (93/41 mmHg), tachykardiu (110/min) a anúriu (diuréza 10 mL/12 hodín). V laboratórnych parametroch boli priekazné známky hemokoncentrácie (hematokrit 46,1 %, hemoglobín 17 g/L), prerenálnej insuficience (urea 30 mmol/L, kreatinín 126 μmol/L) a závažná hypoalbuminémia (12,4 g/L). Prekvapivým nálezom bola výrazná hyponatriémia (111 mmol/L) s hypoosmolalitou séra (270 mOsm/kg). Nízka natriuréza v jednorázovej vzorke moču (menej ako 5 mmol/L) a vysoká relatívna exkrécia močového kália (až 93 %) suponovali aktiváciu hormonálnej osi RAAS (tab. 2, tab. 3).
Tab. 2. Vstupné laboratórne parametre. 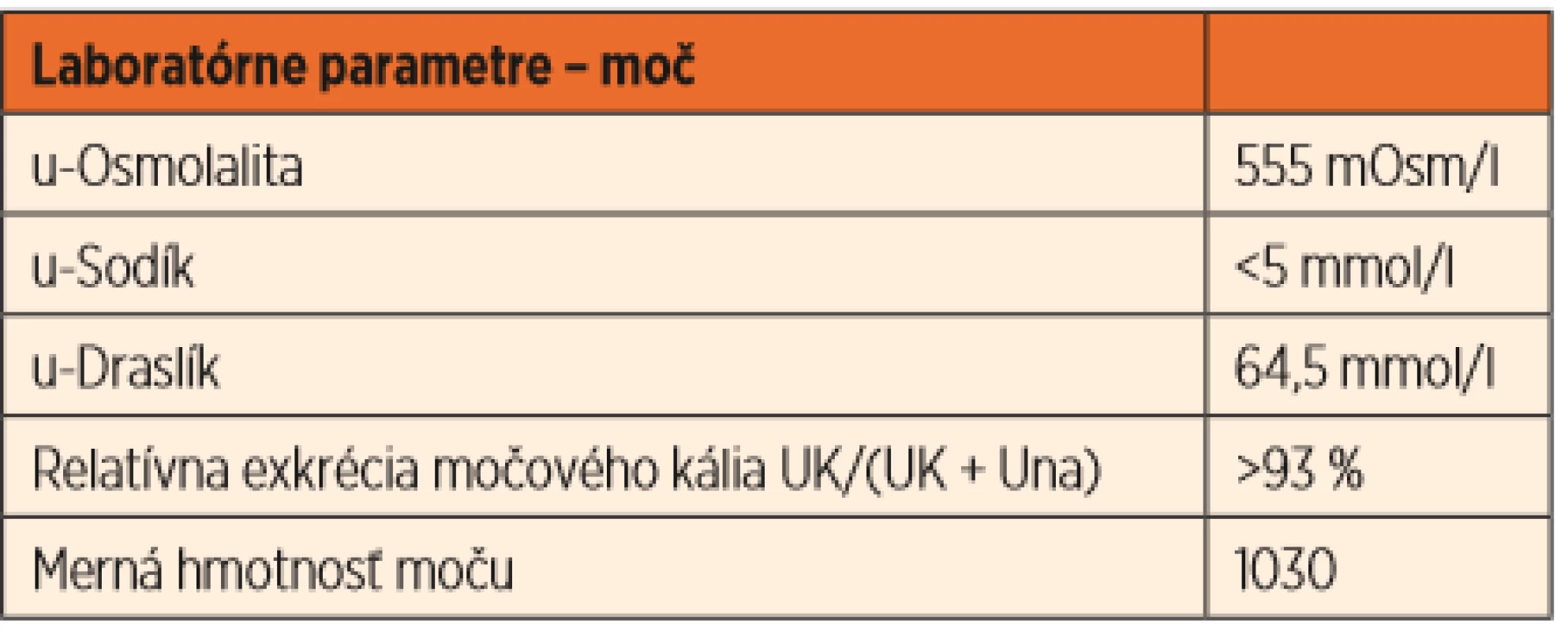
UK – odpad draslíka v jednorázovej vzorke moču
UNa – odpad sodíka v jednorázovej vzorke močuTab. 3. Úprava natriémie v priebehu liečby. 
s-Na – sérová koncentrácia sodíka Pre charakteristický klinický a laboratórny obraz hypervolémie s nízkym efektívnym cirkulačným objemom (underfill opuchový stav) sme v úvode indikovali pomalú infúziu 20% ľudského albumínu 2 g/kg a neskôr furosemid v dávke 1 mg/kg,čo viedlo k obnoveniu diurézy (170 mL moču). Následne sme podávali izotonický fyziologický roztok (10 mL/h) a obmedzili príjem čistej vody. V priebehu 24 hodín stúpla sérová koncentrácia sodíka o 13 mmol/L, upravil sa stav vedomia, chlapec odpovedal adekvátne, bol normotenzný (109/62 mmHg) a mal dostatočnú diurézu 2,1 mL/kg/h. S obnovením cirkulácie sa promptne upravili aj obličkové parametre (urea 8,4 mmol/L, sérový kreatinín 39 μmol/L) (tab. 3). Neskorú neurologickú symptomatológiu suponujúcu rozvoj syndrómu osmotickej demyelinizácie asociovaného s rýchlou korekciou hyponatriémie sme nepozorovali.
DISKUSIA
V literatúre sú opísané len andekdotálne kazuistické prípady závažnej symptomatickej hyponatriémie pri relapse nefrotického syndrómu. Hurley a spol. publikovali v roku 1980 vzácnu kazuistiku 21-mesačného dieťaťa s nefrotickým syndrómom a iniciálnou natriémiou 112 mmol/L, ktorá po infúzii fyziologického roztoku ešte poklesla na 98 mmol/L. Pacient bol dezorientovaný, mal halucinácie, preto bol intravenózne aplikovaný bolus 3% hypertonického roztoku NaCl a následne izotonický fyziologický roztok a diuretiká. Je prekvapivé, že napriek „prestrelenej“ korekcii s prudkým vzostupom natriémie až o 29 mmol/L (!) počas 24 hodín, sa autori nezmieňujú o syndróme osmotickej demyelinizácie a iniciálnu hyponatriémiu vysvetľujú neslanou diétou [8].
Prudké osmotické zmeny spôsobené rýchlou úpravou sérovej koncentrácie sodíka u chorých s prolongovanou a závažnou hyponatriémiou (Na <120 mmol/L) vyvolávajú demyelinizáciu nervových vlákien. Klinické spektrum neurologických prejavov je veľmi pestré. Demonštruje to nedávno publikovaný raritný prípad 2-ročného dievčatka s nefrotickým syndrómom a symptomatickou hyponatriémiou. U pacientky sa po rapídnej korekcii intravenóznym 3% roztokom chloridu sodného, ktorý podávali v infúzii 6 mL/kg po dobu 6 hodín, manifestovala generalizovaná hypotónia, akútna kvadruparéza a pseudobulbárne kŕče. Magnetická rezonancia mozgu potvrdila symetrické hyperintenzívne lézie v bazálnych gangliách korešpondujúce s osmotickou demyelinizáciou. V literatúre ide o prvý opísaný prípad extrapontínovej myelinolýzy u dieťaťa s nefrotickým syndrómom. Zaujímavosťou raritnej kazuistiky je tiež včasná manifestácia neurologickej symptomatológie, lebo klinické a rádiologické známky zvyčajne nastupujú s latenciou 7 až 14 dní po akútnych osmotických zmenách [9]. U nášho pacienta vymizli iniciálne neurologické prejavy s úpravou hyponatriémie do 24 hodín. V ďalšom priebehu bol asymptomatický, preto sme MRI mozgu neindikovali.
Patogenéza opuchov pri nefrotickom syndróme je heterogénna. Z klinického hľadiska sa treba zamerať na prítomnosť známok intravaskulárnej hypovolémie, ktoré určujú iniciálny liečebný postup. U týchto chorých môže infúzia albumínu zlepšiť cirkulačné pomery v organizme, utlmí sa hypovolémiou indukovaná sekrécia ADH a dôjde k autokorekcii hyponatriémie [10].
V našej kazuistike opisujeme charakteristický obraz hypervolemickej hyponatriémie pri relapse nefrotického syndrómu s akútnym prerenálnym poškodením. Relatívna exkrécia močového kália 93 % odrážala nadmernú aktivitu plazmatického aldosterónu a sekundárnu retenciu nátria. Možno predpokladať, že k závažnej hyponatriémii významne prispela aj neosmotická stimulácia ADH s následnou retenciou bezsolútovej vody. Pacient nemal obmedzený príjem soli a v čase akútnej prezentácie neužíval diuretiká. V prvom kroku sme zvolili infúziu 20% ľudského albumínu na obnovenie efektívnej cirkulácie a následne izotonický fyziologický roztok. Pri nefrotických edémoch sa preferuje 20% ľudský albumín, lebo 5% roztok síce zvyšuje krvný objem, ale nie onkotický tlak [4]. Expanzia plazmatického objemu suprimuje sekréciu ADH indukovanú hypovolémiou, zvyšuje sa renálna exkrécia bezsolútovej vody a upravuje hyponatriémia. Navyše, infúzia albumínu môže efektívne zvýšiť diurézu [11–14]. Aj u nášho pacienta sa po infúzií 20% albumínu promptne obnovila diuréza. Napriek opatrnej korekcii a pravidelnom monitorovaní elektrolytov došlo k vzostupu sérovej koncentrácie sodíka o 13 mmol/L za 24 hodín, čo prevyšuje odporúčaný limit o 1 mmol/L, avšak celkový vzostup natriémie neprekročil „bezpečný prah“ 20 mmol/48 hodín [3] (tab 3). K rýchlejšej úprave elektrolytovej rovnováhy v prvých hodinách mohol prispieť autokorekčný mechanizmus indukovaný albumínom.
V bežnej praxi môže riziko hypovolémie a dilučnej hyponatrémie pri nefrotickom syndróme nepriamo predikovať vysoký stupeň hemokoncentrácie (Hb >170 g/L). Vyplynulo to z retrospektívnej analýzy kohorty 46 detí s relapsom nefrotického syndrómu. U pacientov s hypovolémiou sa zistila signifikantne vyššia hemokoncentrácia (Hb 196 ± 22 g/L) a hyponatriémia (127,3 ± 7,2 mmol/L) ako u nefrotických detí bez hypovolémie [15]. Tieto závery podporuje aj naše pozorovanie.
ZÁVER
Symptomatická hyponatriémia je zriedkavá, ale závažná komplikácia nefrotického syndrómu. V klinickej praxi je dôležité rozpoznať prítomnosť intravaskulárnej hypovolémie (underfill edémy). V týchto prípadoch sa odporúča najprv zaistiť dobrú tkanivovú perfúziu 20% albumínom a až potom indikovať diuretiká. Pri úprave dilučnej hyponatriémie s opuchmi treba postupovať veľmi obozretne, optimálna rýchlosť korekcie je vzostup sodíka o 6–8 mmol/L/24 hod. Ak je hyponatriémia sprevádzaná neurologickými prejavmi (hyponatriemická encefalopatia), odporúča sa vzostup koncentrácie sodíka o 12 mmol/L/24 hod [16]. Prudké zvýšenie sérového nátria je asociované s poškodením CNS.
Došlo: 10. 9. 2019
Přijato: 25. 10. 2019
Adresa pre korešpondenciu:
Prof. MUDr. Ľudmila Podracká, CSc.
Detská klinika LFUK a NÚDCH
Limbova 1
833 40 Bratislava
Slovenská republika
e-mail:ludmila.podracka@dfnsp.sk
Zdroje
1. Hasegawa H, Okubo S, Ikezumi Y, et al. Hyponatremia due to an excess of arginine vasopressin is common in children with febrile disease. Pediatr Nephrol 2009; 24 : 507.
2. Don M, Valerio G, Korppi M, Canciani M. Hyponatremia in pediatric community acquired pneumonia. Pediatr Nephrol 2008; 23 : 2247.
3. Zieg J. Hyponatrémie u dětí. In: Lebl J, et al. Poruchy vodní a elektrolytové rovnováhy u dětí. 1. vyd. Praha: Galén, 2019 : 37-46. ISBN 978-80-7492-405-7.
4. Ellis D. Pathophysiology, evaluation, and management of edema in childhood nephrotic syndrome. Front Pediatr 2016; 3 : 111.
5. Cadnapaphornchai MA, Tkachenko O, Shchekochikhin D, et al. The nephrotic syndrome: pathogenesis and treatment of edema formation and secondary complications. Pediatr Nephrol 2014; 29 : 1159.
6. Siddall CE, Radhakrishnan J. The pathophysiology of edema formation in the nephrotic syndrome. Kidney Int 2012; 82 : 635–642.
7. Sterns RH, Riggs JE, Schochet SS Jr. Osmotic demyelination syndrome following correction of hyponatremia. N Engl J Med 1986; 314 : 1535.
8. Hurley JK. Symptomatic hyponatremia in nephrotic syndrome. Am J Dis Child 1980; 134 (2): 204–206.
9. Tullu MS, Deshmukh I, Muranjan MN, et al. Extrapontine myelinolysis in a child with nephrotic syndrome. Pediatr Neurol 2010; 43 : 139–141.
10. Filippatos TD, Liamis G, Christopoulou F, Elisaf MS. Ten common pitfalls in the evaluation of patients with hyponatremia. Eur J Intern Med 2016; 29 : 22–25.
11. Kapur G, Valentini RP, Imam AA, Mattoo TK. Treatment of severe edema in children with nephrotic syndrome with diuretics alone – a prospective study. Clin J Am Soc Nephrol 2009; 4 : 907–913.
12. Fliser D, Zurbrüggen I, Mutschler E, et al. Coadministration of albumin and furosemide in patients with the nephrotic syndrome. Kidney Int 1999; 55 : 629.
13. Hodson E. The management of idiopathic nephrotic syndrome in children. Paediatr Drugs 2003; 5 : 335–349.
14. Haws RM, Baum M. Efficacy of albumin and diuretic therapy in children with nephrotic syndrome. Pediatrics 1993; 91 : 1142–1146.
15. Wang SJ, Tsau ZK, Lu FL, Chen CH. Hypovolemia and hypovolemic shock in children with nephrotic syndrome. Acta Paediatr Taiwan 2000; 41 : 179–189.
16. Royal Children‘s Hospital Melbourne Australia. Clinical Practice Guideline on Hyponatremia. Dostupné na: www.rch.org.au/clinicalguide/index.cfm.
Štítky
Neonatologie Pediatrie Praktické lékařství pro děti a dorost
Článek vyšel v časopiseČesko-slovenská pediatrie
Nejčtenější tento týden
2020 Číslo 2- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Syndrom Noonanové: etiologie, diagnostika a terapie
-
Všechny články tohoto čísla
- Hyponatriémia – vzácna komplikácia nefrotického syndrómu
- Úspěšná sklerotizace cyst štítné žlázy alkoholem pod ultrasonografickou kontrolou u adolescentů
- Moje úsmevné spomienky na Olomouc
- Editorial: Když si děti hrají, někdy z toho problém mají
- Cizí tělesa v polykacích cestách u dětí
- Pevné exogénne cudzie telesá v dolných dýchacích cestách u detí
- Aspirovaná cizí tělesa u dětí – kazuistiky
- Hračka – bezpečný předmět na dětských odděleních?
- Stravovací a pohybové zvyklosti v rodině – ověření reliability dotazníku
- Léčba trombotických příhod u novorozenců a kojenců
- Stanovenie hladín sukcinylacetónu u časti zdravej detskej populácie na Slovensku
- Opakovaná spontánní remise atypického hemolyticko-uremického syndromu vyvolaného chřipkou – kazuistika
- Česko-slovenská pediatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Cizí tělesa v polykacích cestách u dětí
- Úspěšná sklerotizace cyst štítné žlázy alkoholem pod ultrasonografickou kontrolou u adolescentů
- Léčba trombotických příhod u novorozenců a kojenců
- Aspirovaná cizí tělesa u dětí – kazuistiky
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



