-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C
Autoři: P. Urbánek 1; P. Husa 2; J. Šperl 3
; S. Fraňková 3
; S. Plíšek 4; L. Rožnovský 5; P. Kümpel 6
Působiště autorů: Pracovní skupina pro virové hepatitidy České hepatologické společnosti ČLS JEP Pracovní skupina pro virové hepatitidy Společnosti infekčního lékařství ČLS JEP ; Interní klinika 1. LF UK a ÚVN Praha 1; Klinika infekčních chorob LF MU a FN Brno 2; Klinika hepatogastroenterologie, Transplantcentrum, IKEM, Praha 3; Klinika infekčních chorob LF UK a FN Hradec Králové 4; Klinika infekčního lékařství LF OU a FN Ostrava 5; Infekční oddělení, Slezská nemocnice v Opavě, p. o. 6
Vyšlo v časopise: Gastroent Hepatol 2015; 69(5): 455-471
Kategorie: Hepatologie: doporučené postupy
doi: https://doi.org/10.14735/amgh2015455Níže uvedená doporučení pro diagnostiku a terapii infekce virem hepatitidy C (HCV) byla vytvořena členy pracovních skupin pro virové hepatitidy České hepatologické společnosti ČLS JEP a Společnosti infekčního lékařství ČLS JEP. Jsou založena především na doporučeních vydaných Evropskou asociací pro studium jater (EASL) vydaných v dubnu 2015. Doporučení definují preferovaný přístup k řešení problematiky HCV infekce. V oblasti léčby chronické HCV infekce je vždy zmíněno několik variant postupu. Tato skutečnost je dána rychlým vývojem nových protivirových preparátů a jejich nerovnoměrným zaváděním do rutinní praxe v jednotlivých zemích. Dostupnost preparátů proto může být v konkrétním případě faktorem limitujícím užití optimálního postupu.
Maximální možné dodržování odborných doporučení je podmínkou dosažení efektivní péče o nemocné s virovou hepatitidou C v celostátním měřítku. Předkládaný dokument je oporou při jednání obou odborných společností se státními orgány a s plátci zdravotní péče.
1. Epidemiologie HCV
Celosvětová prevalence infekce HCV se pohybuje v běžné populaci kolem 3 %. V roce 2001 bylo pomocí sérologického přehledu zjištěno, že prevalence protilátek anti-HCV v běžné populaci ČR je 0,2 %. HCV infekce je nejčastější příčinou jaterních onemocnění ve vyspělých zemích světa.
Infekce virem hepatitidy C patří mezi krví přenosné infekce. Hlavními cestami šíření HCV infekce jsou:
- přenos krevními deriváty,
- injekční aplikace drog,
- tetování a piercing neprováděné za aseptických podmínek (zejména amatérsky),
- pravidelné dialyzační léčení (PDL),
- profesionální riziko expozice HCV,
- sexuální kontakt s osobou HCV pozitivní (častější mezi muži, kteří mají styk s muži),
- rodinný kontakt s osobou HCV pozitivní,
- vertikální přenos z HCV pozitivní matky na novorozence (perinatální přenos),
- iatrogenní přenos,
- přenos orgánovým štěpem před rokem 1992,
- od zahájení rutinního testování krevních dárců na přítomnost infekce HCV (v roce 1992) je hlavní cestou šíření infekce sdílení infikovaných nástrojů při injekční aplikaci drog.
1.1 Prevence přenosu HCV
HCV pozitivní osoba musí být poučena, jak zabránit přenosu HCV na další osoby, zejména:
HCV pozitivní osoba nesmí darovat krev, krevní deriváty, orgány, tkáně či sperma. HCV pozitivní osoba by si měla řádně ošetřit každou otevřenou ránu tak, aby nedošlo k jakékoli expozici jiné osoby infikovanou krví. HCV pozitivní injekční uživatelé drog by měli být zařazeni do programu kontrolované výměny injekčního instrumentária a všech dalších potřeb, pokud nejsou indikováni k odvykací léčbě. HCV pozitivní osoba by měla být poučena, že riziko přenosu HCV sexuální cestou je malé a infekce sama o sobě není indikací k používání bariérové antikoncepce v dlouhodobém monogamním vztahu. Doporučení použití bariérové antikoncepce při náhodném sexu tím není dotčeno. Metody bezpečného sexu jsou dostatečnou prevencí přenosu. HCV pozitivní osoba by měla bránit i náhodnému použití svého zubního kartáčku, holicích potřeb apod. další osobou.
2. Přirozený průběh HCV infekce
Studie o přirozeném průběhu HCV infekce ukazují, že 55–85 % pacientů, kteří se infikují virem hepatitidy C, není schopno přirozeným způsobem virus eliminovat, a infekce u nich tudíž přejde do chronického stadia. U 5–20 % osob z tohoto počtu dojde během 20–25 let k rozvoji jaterní cirhózy. Osoby s jaterní cirhózou při chronické HCV infekci mají riziko rozvoje end-stage-liver disease (cca 30 % během 10 let) a riziko vzniku hepatocelulárního karcinomu (HCC, 1–2 % ročně). Faktory asociované s progresí jaterního postižení při chronické HCV infekci jsou:
- přenos infekce ve vyšším věku (riziko narůstá po 40.–45. roce věku),
- konzumace alkoholu ≥ 50 g denně,
- obezita a jaterní steatóza z jakéhokoli jiného důvodu,
- koinfekce HCV/HBV a HCV/HIV,
- vyšší stupeň jaterního postižení nežli portální fibróza v iniciální jaterní biopsii (METAVIR ≥ 2 a Ishak ≥ 3)
Chronická HCV infekce je rovněž asociována s celou řadou tzv. extrahepatálních manifestací. Nejdůležitějším stavem z této skupiny je smíšená kryoglobulinemie. Symptomatická smíšená kryoglobulinemie je indikací k protivirové léčbě bez ohledu na stupeň jaterního postižení.
3. Laboratorní vyšetřovací metody
3.1 Sérologické detekční metody
Jedná se o sérologickou detekci anti-HCV protilátek. Protilátky jsou markerem expozice – kontaktu dané osoby s virem hepatitidy C. Protilátky anti-HCV nemají neutralizační efekt, nejsou nositelem imunity organizmu. Přetrvávají ve značném titru i u pacientů úspěšně vyléčených. Technicky se jedná o detekci protilátek metodou EIA či některých jejích variant. V současné době se používají metody III. generace, které mají senzitivitu 97 % a specificitu až 99 %.
Pro screeningová stanovení anti-HCV lze nově využít i rychlé diagnostické testy. Tyto testy stanovují anti-HCV v různých tělních tekutinách, např. v séru, plazmě, kapilární krvi. Dostupné jsou i testy pro stanovení anti-HCV ve slinách. Všechny tyto rychlé diagnostické testy lze použít bez nutnosti odběru venózní krve a jejího dalšího zpracování. Další výhodou je jejich jednoduchost, proveditelnost při pokojové teplotě bez nutnosti speciálního vybavení, není třeba ani složitá výuka personálu, který s daným testem zachází.
3.2 Molekulárně genetické metody
Molekulárně genetické metody prokazují přítomnost virové nukleové kyseliny (HCV RNA) v séru či tkáních infikovaného jedince. Největšího rozšíření v současné době dosáhla metoda polymerázové řetězové reakce v reálném čase (RT-PCR). Dostupná je kvalitativní varianta, většinou se však používá ve variantě kvantitativní. Koncentrace HCV RNA se udává v IU/ml.
Za standardní detekční limit je považována citlivost použité techniky (polymerázové řetězové reakce) 15 IU/ml HCV RNA a méně. Protože řada laboratoří používá metody na stanovení HCV RNA, jejichž citlivost nedosahuje požadovaného standardního detekčního limitu, je třeba, aby lékař zadávající vyšetření v souvislosti s hodnocením terapie dle těchto standardních postupů požadoval na laboratoři informaci, že citlivost jejich stanovení splňuje uvedený limit.
Součástí molekulárního vyšetření by mělo být i stanovení genotypu a subtypu HCV. Genotypizace je důležitá z pohledu rozdílných léčebných postupů a rozdílné účinnosti léčby u jednotlivých genotypů HCV. Určení subtypu, zejména genotypu 1, je významné pro určení rizika vzniku virologické rezistence v případě podání simepreviru (SMV, viz dále).
4. Screening HCV infekce
Velká část osob infikovaných HCV v tuto chvíli vůbec neví, že by mohli být infikováni. Identifikace infikovaných osob je přitom jednou ze základních podmínek efektivní péče o toto onemocnění. V ČR nejsou k dispozici data, která by mohla odůvodnit uskutečnění populačního screeningu HCV infekce. Jedinou možností, jak efektivního screeningu dosáhnout, je plná informovanost lékařů primární péče (praktičtí lékaři, gynekologové, porodníci) a specialistů, kteří se podílejí na péči o pacienty ve vysoce rizikových skupinách.
Screeningovým vyšetřením HCV infekce je vyšetření anti-HCV protilátek. Reaktivita anti-HCV by měla být vyšetřena u všech osob, u kterých je podezření, že byly někdy v průběhu života exponovány některému z rizikových faktorů přenosu HCV. Na základě znalostí o možnostech přenosu je doporučováno testování HCV infekce zejména u těchto skupin osob:
- osoby s anamnézou injekční aplikace drog, a to i v případě jediné aplikace před více lety,
- osoby ve skupinách s vysokou prevalencí HCV infekce:
- 1. příjemci krevních derivátů či příjemci orgánových transplantátů před rokem 1992,
- 2. HIV pozitivní osoby,
- 3. hemofilici léčení před rokem 1987,
- 4. osoby s anamnézou hemodialýzy (i akutní a krátkodobé),
- 5. osoby s nevysvětlitelnou elevací aminotransferáz,
- děti narozené HCV pozitivním matkám (testování až po 18. měsíci věku),
- zdravotničtí pracovníci a další osoby s anamnézou poranění injekční jehlou (bez ohledu na sérologický stav, event. zdroje) nebo osoby se slizniční expozicí krvi HCV pozitivní osoby,
- sexuální partneři HCV pozitivní osoby,
- osoby vystavené invazivním lékařským zákrokům, osoby s anamnézou komplikovaného chirurgického výkonu nebo osoby s anamnézou dlouhodobější hospitalizace (rizika iatrogenního přenosu).
Je-li vyšetřovaná osoba anti-HCV pozitivní, není jakákoli indikace k opakování vyšetření kdykoli v budoucnosti. Sérologická pozitivita anti-HCV nekoreluje se žádnou z charakteristik onemocnění (s pokročilostí jaterního postižení, s pravděpodobností dosažení vyléčení apod.). Každá anti-HCV pozitivní osoba musí být vyšetřena specialistou.
5. Diagnostická kritéria
5.1 Akutní HCV infekce
Akutní HCV infekce je diagnostikována velmi vzácně pro častou absenci klinických příznaků v akutním stadiu HCV infekce.
Spolehlivě lze stanovit diagnózu akutní HCV infekce pouze tehdy, je-li dokumentována sérokonverze na anti-HCV reaktivitu. Příčinou je skutečnost, že neexistuje sérologický marker akutní infekce HCV. O akutní HCV infekci lze také hovořit v případech, kdy jsou klinické příznaky v souladu s obrazem akutní hepatitidy. Jde především o tyto příznaky:
- sérová aktivita ALT > 10× horní hranice normy,
- ikterus,
- nejsou známky chronického jaterního onemocnění nebo jiné možné příčiny akutní hepatitidy.
Pozitivním momentem může být i identifikace možného rizikového faktoru přenosu infekce HCV. Ve fázi akutní infekce je pozitivní HCV RNA v krvi, nicméně během akutní fáze infekce byla popsána krátká období negativity HCV RNA v krvi. Jedno negativní vyšetření HCV RNA diagnózu HCV infekce nevylučuje a také nemusí znamenat v konkrétním případě spontánní eliminaci viru. Stanovení HCV RNA je třeba opakovat. Vhodný interval mezi vyšetřeními HCV RNA k potvrzení eliminace viru je 12 týdnů.
5.2 Chronická HCV infekce
Diagnóza chronické HCV infekce je založena na pozitivním průkazu HCV RNA v krvi i anti-HCV protilátek v přítomnosti známek chronické hepatitidy, tj. elevaci sérové aktivity ALT nebo histologických známek chronické hepatitidy. V případech akutní HCV infekce prakticky nedochází k eliminaci viru po více než 4–6 měsících od přenosu, proto může být pro definici chronické HCV infekce užit i tento časový parametr.
5.3 Hodnocení léčebné odpovědi
Terminologii pro hodnocení virologické odpovědi uvádí tab. 1.
Tab. 1. Definice virologické odpovědi v průběhu protivirové terapie a po jejím skončení. Tab. 1. Definitions of types of virological response during antiviral treatment and after its cessation. 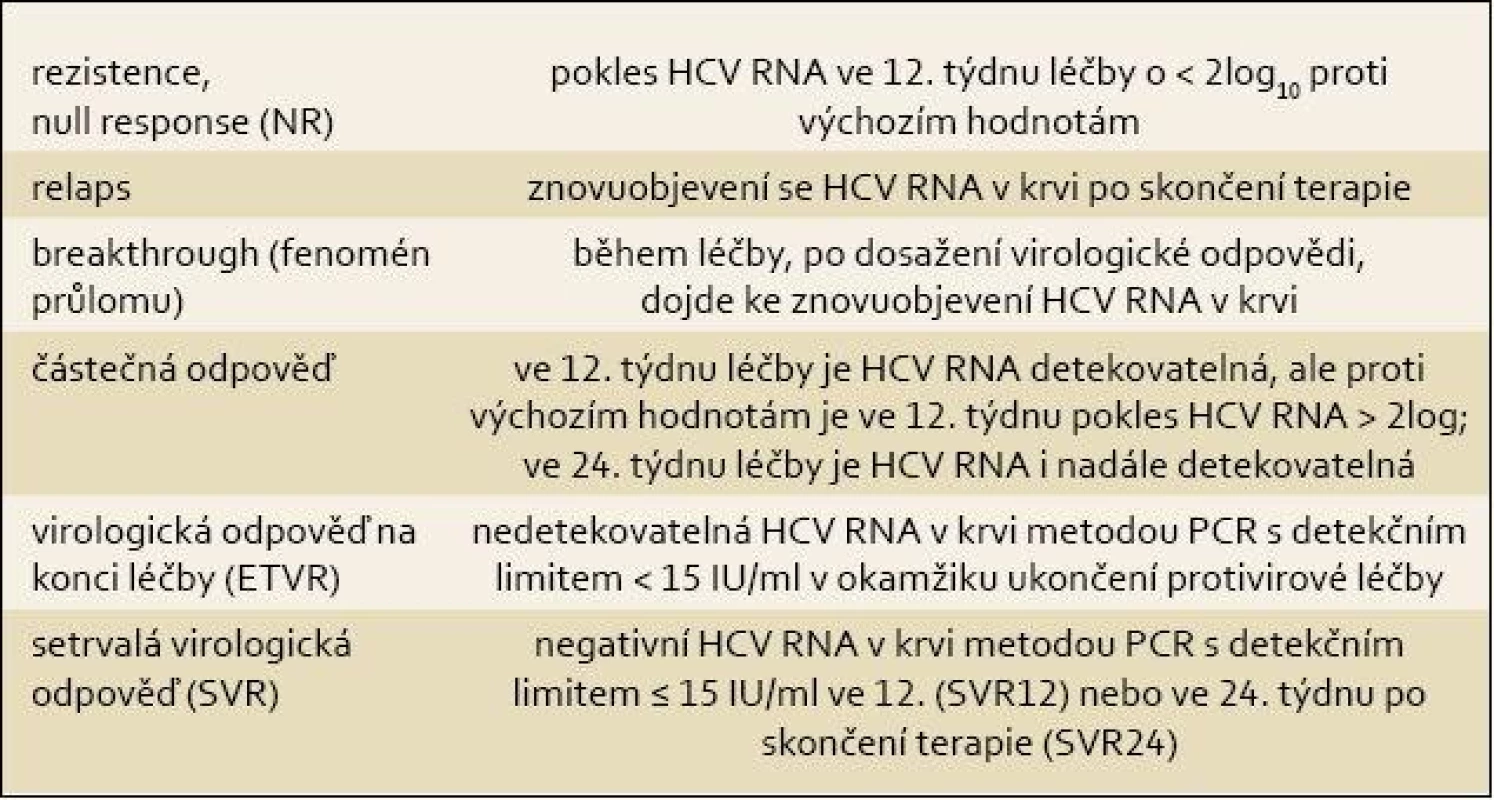
Setrvalá virologická odpověď (SVR)12 i SVR24 jsou akceptovaná kritéria vyléčení HCV infekce, jejich shoda je kolem 99 %. Dlouhodobé studie rovněž ukázaly, že SVR skutečně znamená trvalou eliminaci HCV infekce ve více než 99 % případů.
6. Vyšetření před zahájením protivirové léčby
Před zahájením protivirové léčby by měla být stanovena pokročilost jaterního onemocnění. Důvodem je především snaha identifikovat osoby s jaterní cirhózou či pokročilou (přemosťující) fibrózu, protože prognóza osob po protivirové léčbě je definována stadiem postižení jater před zahájením léčby. I pacienti s trvale normální aktivitou ALT mohou mít významnou fibrózu, i u těchto osob je proto indikováno vyšetření pokročilosti jaterního postižení. Znalost stadia jaterního poškození je rovněž důležitá pro načasování zahájení protivirové léčby. Tento moment se jeví v současné době rychlého rozvoje možností léčby jako velmi důležitý. Stejně tak musí být před zahájením léčby vyšetřeny vstupní virologické parametry, které mají vztah k volbě protivirové léčby.
6.1 Jiné příčiny jaterního onemocnění
U každého pacienta s chronickou HCV infekcí by měla být provedena vyšetření, která umožňují odhalit jiná jaterní onemocnění nebo faktory ovlivňující vývoj HCV infekce. Jedná se zejména o:
- vyšetření sérologie HBV a HIV (HBsAg, anti-HBs, anti-HBc, anti-HIV1 a anti-HIV2),
- posouzení vlivu příjmu alkoholu,
- základní vyšetření jaterních autoimunitních onemocnění,
- vyšetření možného podílu genetických a metabolických jaterních onemocnění (hereditární hemochromatóza, diabetes, nealkoholická steatohepatitida),
- posouzení možné hepatotoxicity současně podávaných léků.
6.2 Stanovení pokročilosti jaterního postižení
Před protivirovou léčbou by měl být stanoven stupeň pokročilosti jaterního postižení, tj. stupeň jaterní fibrózy (stage). Zvláštní důležitost má identifikace pacientů s jaterní cirhózou nebo přemosťující fibrózou, protože jejich dlouhodobá prognóza po skončení léčby je dána právě tímto výchozím stupněm postižení. Pacienti s jaterní cirhózou jsou i po úspěšné protivirové léčbě indikováni k doživotní dispenzarizaci a surveillanci HCC. Průkaz absence fibrózy je však také důležitý, a to především z pohledu urgence a načasování protivirové léčby s ohledem na rychle se měnící možnosti léčby. U pacientů s klinicky jasnou jaterní cirhózou není třeba verifikovat stupeň fibrózy. Normální hladiny ALT nevylučují přítomnost významné jaterní fibrózy.
Referenční metodou pro stanovení pokročilosti onemocnění byla po mnoho let jaterní biopsie. Umožňuje hodnocení zánětlivé aktivity (grading) i stupně fibrózy (staging). V současné době již lze na základě mnoha publikovaných výsledků a studií přijmout jako alternativu provedení jaterní biopsie některou z metod neinvazivního stanovení stupně jaterní fibrózy. Nejširšího uplatnění na tomto poli dosáhly metody měření jaterní elasticity, které mají v případech chronické HCV infekce akceptovatelnou výpovědní hodnotu. Nicméně je třeba určité zkušenosti při jejich použití, existuje řada faktorů, které mohou jejich výsledky negativně ovlivnit, např. obezita.
Ke stanovení pokročilosti lze užít i některé tzv. krevní biomarkery jaterní fibrózy. Tato vyšetření jsou však spolehlivá pouze v diskriminaci jaterní cirhóza vs. non-cirhóza. K hodnocení jednotlivých stadií jaterní fibrózy se nehodí.
Kombinace vyšetření jaterní elasticity a krevních biomarkerů jaterní fibrózy zvyšuje přesnost hodnocení pokročilosti jaterního procesu.
6.3 Virologické parametry
Před zahájením protivirové léčby by měly být vyšetřeny tyto parametry:
- viremie – kvantitativní stanovení HCV RNA v krvi v IU/ml,
- genotyp a subtyp viru.
Testování rezistenčních variant (RAV) HCV před první protivirovou léčbou není indikováno. Detekce rezistenčních variant přítomných před první terapií nemá větší klinický význam a tzv. populační sekvenace není dostatečně citlivá technika pro tento účel. Jedinou výjimku může tvořit snaha o detekci RAV Q80K oblasti NS3 genotypu HCV 1a ve vztahu k léčbě založené na SMV.
6.4 Vyšetření genetických parametrů hostitele
Určování genotypu IL28B ztratilo při používání vysoce účinných kombinací perorální virostatik svůj význam. Genotypizace IL28B je proto užitečná pouze tehdy, je-li jedinou dostupnou variantou léčby kombinace PEG-IFN + RBV, nebo tehdy, je-li třeba zvolit nákladově efektivní variantu léčby v zemích s limitovanými léčebnými i ekonomickými možnostmi.
6.5 Registrovaná virostatika
Podle dosavadních znalostí neexistují žádné absolutní kontraindikace podání jakéhokoli přímo působícího virostatika registrovaného v EU k dubnu 2015. Otázky podání jednotlivých kombinací u pacientů s určitým stupněm renální insuficience jsou v současné době řešeny samostatnými klinickými studiemi. Stejně je řešena i otázka léčby pacientů s dekompenzovanou jaterní cirhózou.
7. Indikace zahájení terapie chronické HCV infekce
Všichni pacienti s chronickou HCV infekcí dosud protivirově neléčení, v minulosti léčení neúspěšně (tj. bez dosažení SVR), kteří léčeni být chtějí a nemají žádnou kontraindikaci léčby, jsou kandidáty protivirové terapie. Léčba by měla být upřednostněna u pacientů s pokročilou fibrózou (METAVIR F3–F4) a u pacientů s projevy mimojaterního postižení (symptomatická kryoglobulinemie nebo HCV-asociovaná imunokomplexová nefropatie, HCV asociované non-Hodgkinské lymfomy). U pacientů s projevy mimojaterního postižení by měla být léčba vedena bez ohledu na stupeň jaterní fibrózy. Přednostní léčba je indikována i u pacientů, kteří představují významné epidemiologické riziko šíření HCV infekce.
Léčba by dále měla být přednostně poskytnuta pacientům s dekompenzovanou jaterní cirhózou. Tato skupina osob má velmi často kontraindikace léčby založené na podání IFN, ale může být naopak bezpečně a vysoce účinně léčena kombinací perorálních virostatik. Data z klinických studií i z reálné praxe podporují závěry, že právě tato skupina pacientů má největší krátkodobý přínos z úspěšné léčby HCV infekce. Tento spočívá v poklesu MELD skóre, Child-Pugh klasifikace a významné je i snížení incidence všech nežádoucích událostí, jako je např. dekompenzace onemocnění, rozvoj hepatocelulárního karcinomu apod. Léčba těchto pokročilých pacientů by měla být vedena ve specializovaných centrech s rozsáhlými zkušenostmi s léčbou pomocí perorálních virostatik. Mezi další skupiny osob s HCV infekcí, u kterých je přednostní indikace zahájení moderními variantami léčby, patří osoby s HIV a HBV koinfekcí, pacienti před transplantací jater a po ní.
Léčba je indikována také u pacientů se středně pokročilou fibrózou (METAVIR F2). Léčba pacientů s minimální fibrózou (METAVIR F0–F1) může být odložena. Odložení léčby by nicméně mělo být s pacientem diskutováno a finální rozhodnutí by mělo jeho názor zohlednit. Pacienti s odloženou léčbou by měli být sledováni v pravidelných intervalech za účelem včasného zachycení významné progrese onemocnění a diskuze o zahájení léčby s ohledem na rychlý vývoj a rozšiřování terapeutických možností. Skupiny pacientů s různým stupněm upřednostnění – prioritizace léčby ukazuje tab. 2.
Tab. 2. Skupiny pacientů podle stupně urgence zahájení protivirové léčby. Tab. 2. Prioritisation for antiviral therapy in different groups of HCV-infected patients. 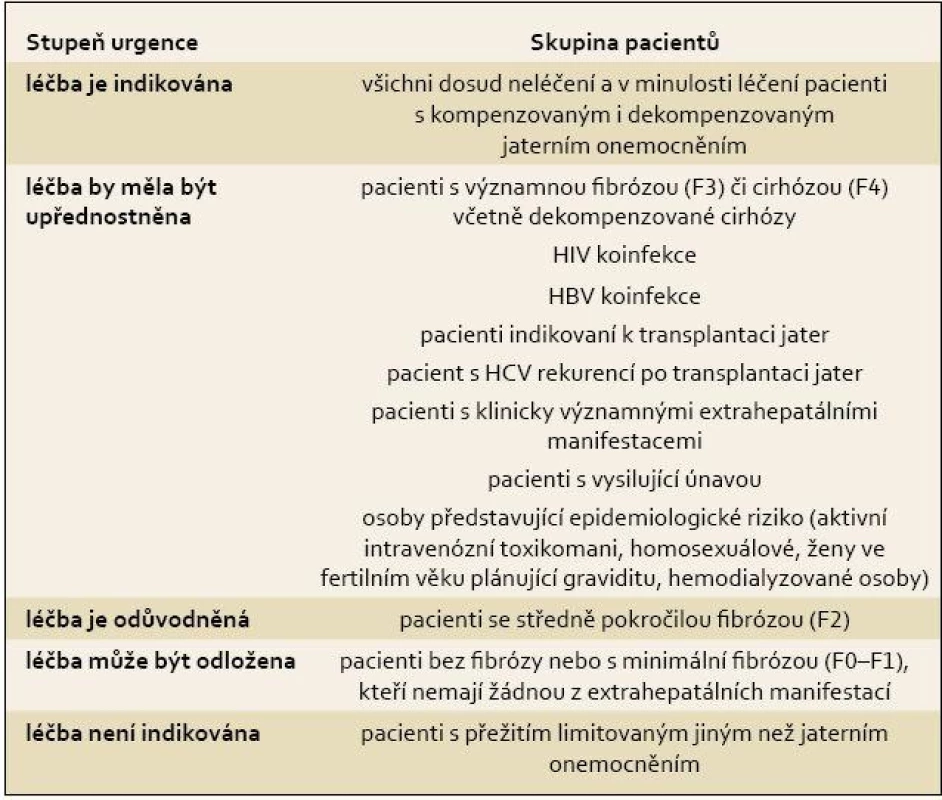
8. Cíle terapie chronické infekce virem hepatitidy C
Cílem terapie je vyléčení HCV infekce – trvalá eliminace viru. Eliminace viru brání rozvoji jaterních i mimojaterních komplikací HCV infekce, včetně pokročilé jaterní fibrózy, cirhózy, dekompenzované cirhózy a hepatocelulárního karcinomu. Eliminací infekce je myšleno dosažení SVR ve smyslu výše uvedené definice (tab. 1). SVR12 a SVR24 spolu korelují v 99 % případů. Podle dlouhodobých studií SVR v 99 % případů znamená trvalé vyléčení HCV infekce, tj. u osob se SVR nedochází k pozdním relapsům onemocnění.
U osob se SVR dochází k významnému snížení jaterní morbidity i mortality. Pacienti s jaterní cirhózou, u nichž bylo dosaženo eradikace HCV infekce, mají významně snížené riziko dekompenzace cirhózy a HCC. Minimální riziko rozvoje HCC však trvá, proto je u těchto osob indikována standardní surveillance HCC.
9. Kontraindikace protivirové léčby
9.1 IFN-α a ribavirin
Protivirová léčba založená na podání pegylovaného IFN-α v kombinaci s ribavirinem je absolutně kontraindikovaná v následujících případech:
- osoby s nekontrolovanou depresí, epilepsií či s nekontrolovaným psychotickým onemocněním,
- těhotné ženy,
- osoby s nekontrolovaným autoimunitním onemocněním štítné žlázy a sítnice,
- osoby s dekompenzovanou jaterní cirhózou,
- osoby po orgánových transplantacích kromě jater.
Použití pegylovaného IFN-α není doporučováno dále u osob s počtem trombocytů ≤ 90 000/ml a/nebo s absolutním počtem neutrofilů < 1 500/ml.
9.2 Přímo působící virostatika
Podle současných znalostí o tzv. přímo působících virostaticích (DAA – directly acting antivirals) nejsou absolutní kontraindikace podání léků z této skupiny.
10. Protivirová léčiva
10.1 Úvod
V posledních 10–12 letech byla standardní terapie chronické infekce HCV založena na podání kombinace pegylovaných interferonů α (PEG-IFN) s ribavirinem (RBV). V roce 2011 vstoupila léčba virové hepatitidy C do zcela nového období, které je charakterizováno rychlým průnikem DAA do terapeutických kombinací HCV infekce. Přímo působící virostatika mají svůj název odvozen od mechanizmu účinku. Látky této skupiny přímo inhibují některý z enzymů uplatňujících se v průběhu replikačního cyklu HCV. V rámci replikace HCV dochází k syntéze jediného prekurzorového proteinu, který je translačním produktem celého virového genomu. Jeho následné štěpení zahajuje virová proteáza, která postupně uvolňuje jednotlivé strukturální i nestrukturální proteiny. Posledním krokem procesu je uvolnění RNA polymerázy, která je klíčovým enzymem celé replikace. DAA jsou látky inhibující nejčastěji buď právě proteázu (produkt NS3/4 oblasti virového genomu), či RNA polymerázu (produkt NS5B).
V průběhu let 2013, 2014 a první poloviny roku 2015 byly schváleny k užití u chronické HCV infekce i další preparáty, především SOF, SMV, daclatasvir (DCV) a kombinace dasabuvir, paritaprevir/ritonavir a ombitasvir. U řady dalších probíhají schvalovací procedury na úrovni FDA a EMA v současné době. Předkládané standardy se podrobně věnují použití preparátů registrovaných k použití u HCV infekce ke 30. květnu 2015. V ČR jsou v době vydání těchto doporučení ze skupiny DAA v běžném užití s definovanou úhradou pouze boceprevir, telaprevir a SMV. U většiny dalších zmiňovaných preparátů byla zahájena správní řízení o stanovení úhrady. Vzhledem k této situaci, rychlému vývoji a obtížně odhadnutelnému okamžiku ukončení správních řízení je v předkládaných doporučeních (stejně jako v doporučeních EASL) uvedeno vždy několik racionálních variant léčby v daných podskupinách pacientů s chronickou HCV infekcí. Při rozhodování o optimálním léčebném postupu je třeba individuálně zohlednit především skutečně dostupné preparáty a načasování zahájení léčby.
Jednoznačným trendem léčby chronické HCV infekce je preference tzv. bezinterferonových režimů, ideálně i režimů bez podání RBV. Tyto režimy však v současné době představují ekonomicky nejnáročnější variantu terapie. Zástupci České hepatologické společnosti a Společnosti infekčního lékařství se ve spolupráci s účastníky každého jednotlivého správního řízení snaží o nalezení optimálního řešení této složité situace, které by zpřístupnilo moderní varianty léčby i pacientům v ČR.
10.2 Pegylované interferony, ribavirin
Účinnost kombinační terapie pegylovaných inteferonů s ribavirinem (SVR) u genotypu 1 je 40–60 %, u genotypu 2 a 3 kolem 80 %. Dávkování těchto preparátů ukazuje tab. 2.
10.3 Simeprevir
SMV je specifický inhibitor virové NS3/4A serinové proteázy. Někdy bývá označován jako virostatikum „druhé vlny první generace“ DAA. SMV je transformován pomocí systému CYP3A4, a proto může jeho podání podléhat interakcím s inhibitory či induktory tohoto systému. Inhibitory CYP3A4 hladinu SMV zvyšují, hrozí proto vzrůst jeho sérové hladiny, který vede k vyššímu výskytu závažnějších nežádoucích účinků. Podání induktorů CYP3A4 naopak zvyšuje odbourávání SMV, plazmatické hladiny klesají a důsledkem je ztráta protivirové účinnosti. Z důvodu tohoto potenciálu lékových interakcí je proto potřeba vždy zkontrolovat souběžně užívanou medikaci se seznamem kontraindikovaných a rizikových léčiv, který je součástí Souhrnu údajů o přípravku SMV.
SMV (Olysio, výrobce Janssen-Cilag, Belgie) je dostupný ve formě tobolky obsahující 150 mg účinné látky. Celková denní dávka je 150 mg, tj. 1 tobolka denně.
10.4 Sofosbuvir
Sofosbuvir (SOF) je syntetický nukleotidový inhibitor (analog uridinu) virové RNA dependentní RNA polymerázy (RdRp, produkt NS5B oblasti virové genomu). SOF je prodrug, který je intracelulárně trifosforylován a následně je pomocí RdRp inkorporován do HCV RNA. Mechanizmem účinku je tzv. ukončení řetězce, kdy po navázání aktivní látky (v našem případě SOF) nemůže pokračovat další řetězení dceřiné virové RNA. SOF je účinný u všech hlavních nejrozšířenějších genotypů HCV (1–6), neinterferuje se syntézou lidské DNA či RNA, neinhibuje ani mitochondriální RNA polymerázy.
SOF není metabolizován systémem cytochromu, potenciál lékových interakcí je tedy mnohem omezenější než u virostatik nižších generací. SOF je substrátem lékového transportéru P-gp a „breast cancer resistance protein“ (BCRP), jeho aktivní metabolit však nikoli. Potentní induktory P-gp ve střevě (rifampicin, karbamazepin a fenytoin) snižují plazmatickou hladinu SOF, snižuje se tedy i intracelulární přítomnost aktivního metabolitu a dochází ke snížení protivirové účinnosti SOF. Naopak inhibitory P-gp/BCRP zvyšují plazmatickou hladinu SOF, avšak nikoli aktivního metabolitu, takže SOF může být s inhibitory podáván současně.
SOF (Sovaldi, výrobce Gilead Sciences, USA) je dostupný ve formě potahované tablety obsahující 400 mg účinné látky. Celková denní dávka je 400 mg, tj. 1 tableta denně.
10.5 Fixní kombinace sofosbuviru a ledipasviru
Tato kombinace je dostupná ve formě jedné tablety obsahující 400 mg SOF a 90 mg ledipasviru (LDV). Celková denní dávka je 1 tableta denně.
LDV je transportován podobně jako SOF, tj. na jeho transportu se účastní P-gp a „breast cancer resistance protein“. Lékové interakce jsou proto velmi podobné. LDV je v nezměněné podobě vylučován žlučí, ledvinami je vyloučeno pouze 1 % celkového množství. V případě fixní kombinace SOF a LDV není třeba redukce dávky u pacientů s mírnou či středně závažnou renální insuficiencí. Bezpečnost podání nebyla dosud zkoumána u pacientů s poklesem eGFR < 30ml/min/1,73m2 a u pacientů se selháním ledvin vyžadujícím hemodialýzu.
10.6 Dasabuvir, ombitasvir, paritaprevir/ritonavir (kombinace 3D)
Dasabuvir je nenukleosidovým inhibitorem RdRp, produktu NS5B virového genomu. Není určen k podávání v monoterapii, striktně je třeba jej kombinovat s ombitasvirem/paritaprevirem/ritonavirem (viz dále). Kombinací dochází ke spojení tří přímo působících antivirotik s různými mechanizmy účinku, mezi nimiž není zkřížená rezistence. Dasabuvir je metabolizován systémem cytochromu, především pomocí CYP2C8 a CYP3A. Proto se při kombinaci dasabuviru s induktory těchto systémů očekává snížení jeho plazmatické koncentrace a snížení jeho protivirového účinku. Níže jsou uvedeny příklady induktorů, které jsou považovány z tohoto důvodu za kontraindikované k současnému podání s dasabuvirem. Naopak podání silných inhibitorů CYP2C8 může vést ke vzestupu plazmatické koncentrace dasabuviru a v důsledku toho ke zvýšení množství a závažnosti možných nežádoucích účinků.
Ombitasvir je inhibitorem NS5A proteázy, paritaprevir je inhibitorem NS3/4 proteázy viru. Ombitasvir i paritaprevir jsou metabolizovány přes složky cytochromu CYP3A. Další součást kombinace ritonavir není látkou s protivirovou účinností na HCV. Je silným inhibitorem CYP3A. Jeho zařazení do 3D kombinace umožnilo snížení použité dávky paritapreviru. Při současném zachování optimální protivirové účinnosti paritapreviru tak došlo ke snížení počtu a závažnosti nežádoucích účinků.
Dostupné preparáty: Exviera (výrobce AbbVie, USA) potahovaná tableta obsahující dasabuvir 250 mg. Preparát Viekirax (AbbVie, USA) obsahuje v potahované tabletě ombitasvir 12,5 mg, paritaprevir 75 mg a ritonavir 50 mg.
10.7 Daclatasvir
DCV je inhibitor replikačního komplexu NS5A. Blokuje dvě fáze virového replikačního cyklu, a to sice syntézu RNA, ale také kompletaci virionu a pravděpodobně i proces jeho uvolnění z hepatocytu. DCV je metabolizován pomocí CYP34A, je inhibitorem P-gp. Má proto rovněž potenciál lékových interakcí, i když významně nižší než např. proteázové inhibitory první generace.
DCV (Daklinza, výrobce BristolMyers--Squibb, USA) je dostupný ve formě tablety obsahující 60 nebo 30 mg účinné látky. Obvyklá denní dávka je 60 mg, tj. 1 tableta denně, dávka se upravuje při léčbě HIV koinfekce z důvodu lékových interakcí.
11. Terapie HCV infekce
V současné době je pro pacienty s chronickou HCV infekcí dostupná celá řada léčebných kombinací, ze kterých budou mít užitek jak pacienti dosud neléčení, tak osoby s neúspěšnou léčbou v minulosti. Indikace a podání jednotlivých léčebných variant jsou závislé na genotypu HCV, případně i subtypu HCV a na stupni pokročilosti jaterního postižení. Indikace jsou stejné pro HCV monoinfikované pacienty i pro pacienty s HCV/HIV koinfekcí.
Tabulky 4 a 5 ukazují přehledně dostupné možnosti protivirové léčby pro jednotlivé indikace. V dalším textu jsou popsány u každého genotypu všechny dostupné možnosti protivirové léčby se stručným přehledem dostupných klinických dat ke každé variantě.
Tab. 3. Dávkování pegylovaných interferonů a ribavirinu. Tab. 3. Pegylated interferon and ribavirin dosing. 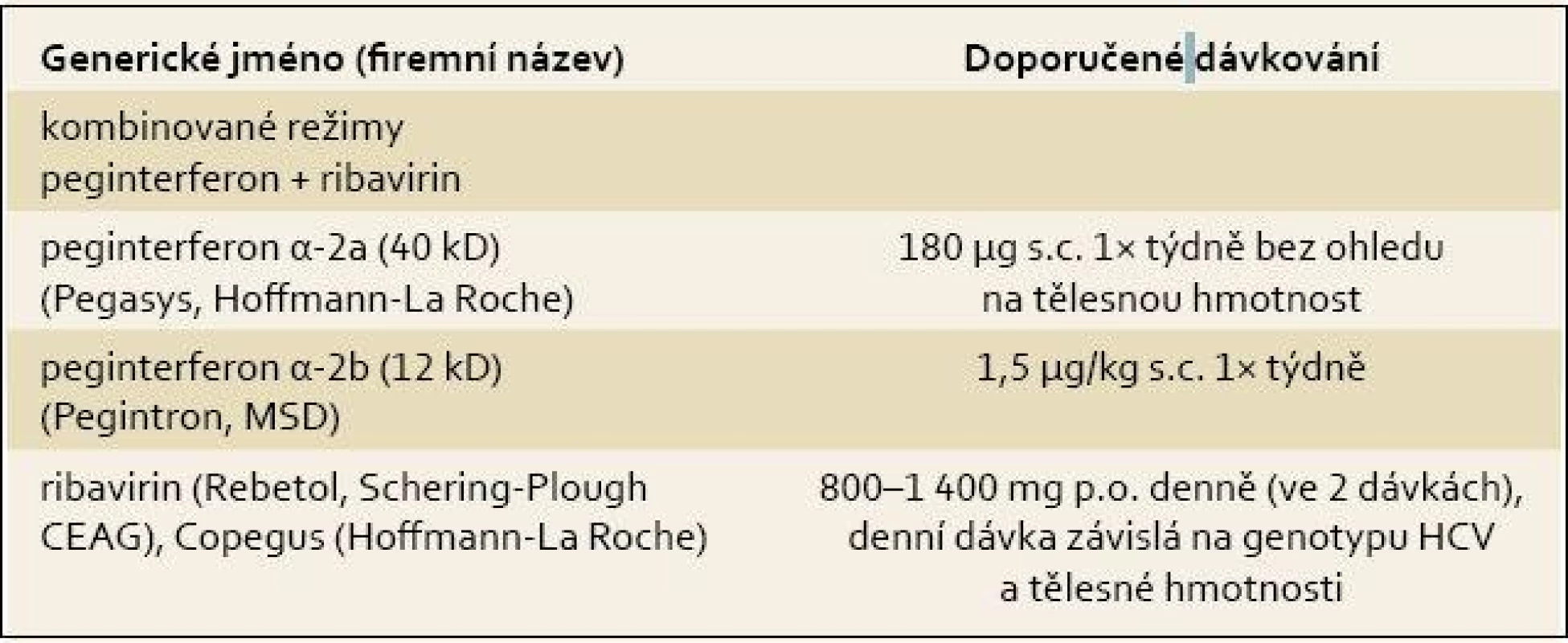
Tab. 4. Doporučené režimy léčby chronické HCV infekce a koinfekce HCV/HIV u pacientů bez jaterní cirhózy, pacienty dosud neléčené a pacienty s neúspěšnou léčbou PEG-IFN + RBV. Tab. 4. Treatment recommendations for HCV-mono-infected or HCV/HIV-co-infected patients with chronic hepatitis C without cirrhosis, patients untreated so far and patients who underwent unsuccessful treatment with PegIFN-α and ribavirin (RBV). 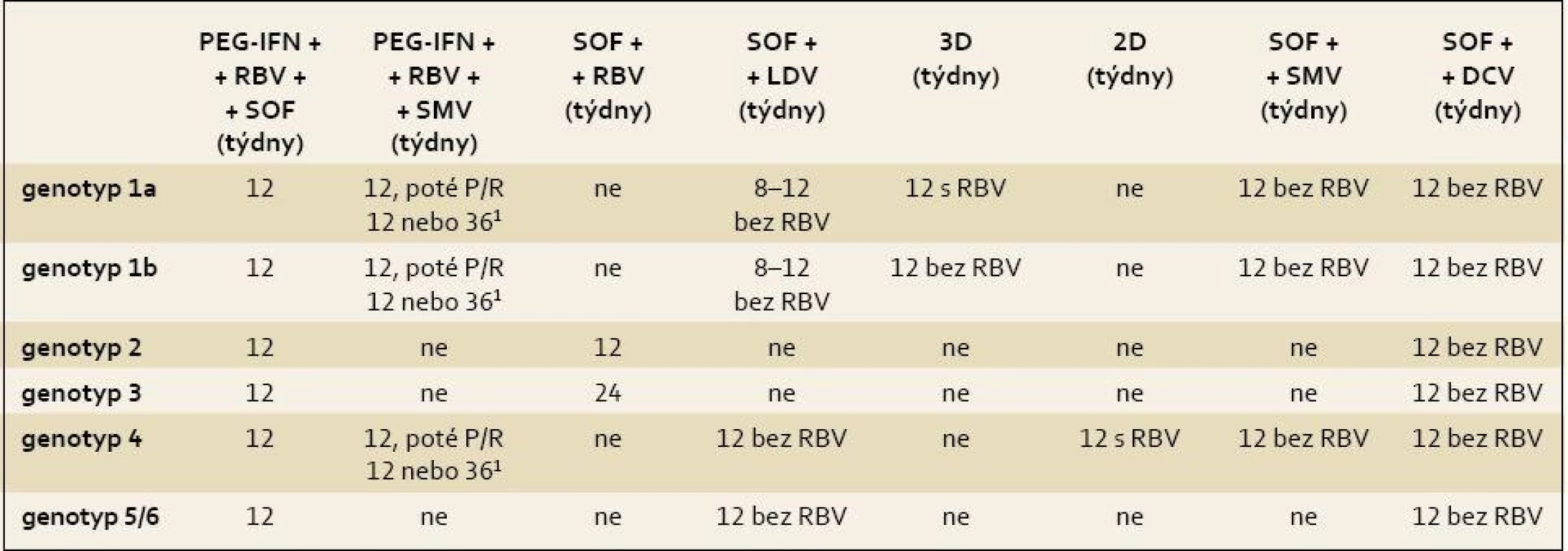
PEG-IFN – pegylovaný interferon α, RBV – ribavirin, P/R – kombinace PEG-IFN + RBV, SOF – sofosbuvir, LDV – ledipasvir, 3D – ombitasvir + paritaprevir/ritonavir + dasobuvir, 2D – paritaprevir/ritonavir + ombitasvir, SMV – simeprevir, DCV – daclatasvir. 1celková doba léčby 24 týdnů (12 + 12) je doporučována pro dosud neléčené osoby a pro pacienty s relapsem po předchozí kombinaci PEG-IFN + RBV. Celková doba 48 týdnů (12 + 36) je doporučována pro pacienty s částečnou odpovědí a s null response na předchozí protivirovou léčbu kombinací PEG-IFN + RBV (je nutno ale mít na paměti, že účinnost u těchto pacientů je velmi nízká i při prodloužení léčby). Tab. 5. Doporučené režimy léčby chronické HCV infekce a koinfekce HCV/HIV u pacientů s kompenzovanou jaterní cirhózou (Child-Pugh A), pacienty dosud neléčené a pacienty s neúspěšnou léčbou PEG-IFN + RBV. Tab. 5. Treatment recommendations for HCV-mono-infected or HCV/HIV-co-infected patients with chronic hepatitis C with compensated (Child-Pugh A) cirrhosis, patients who failed on a treatment based on PegIFN-α and ribavirin (RBV). 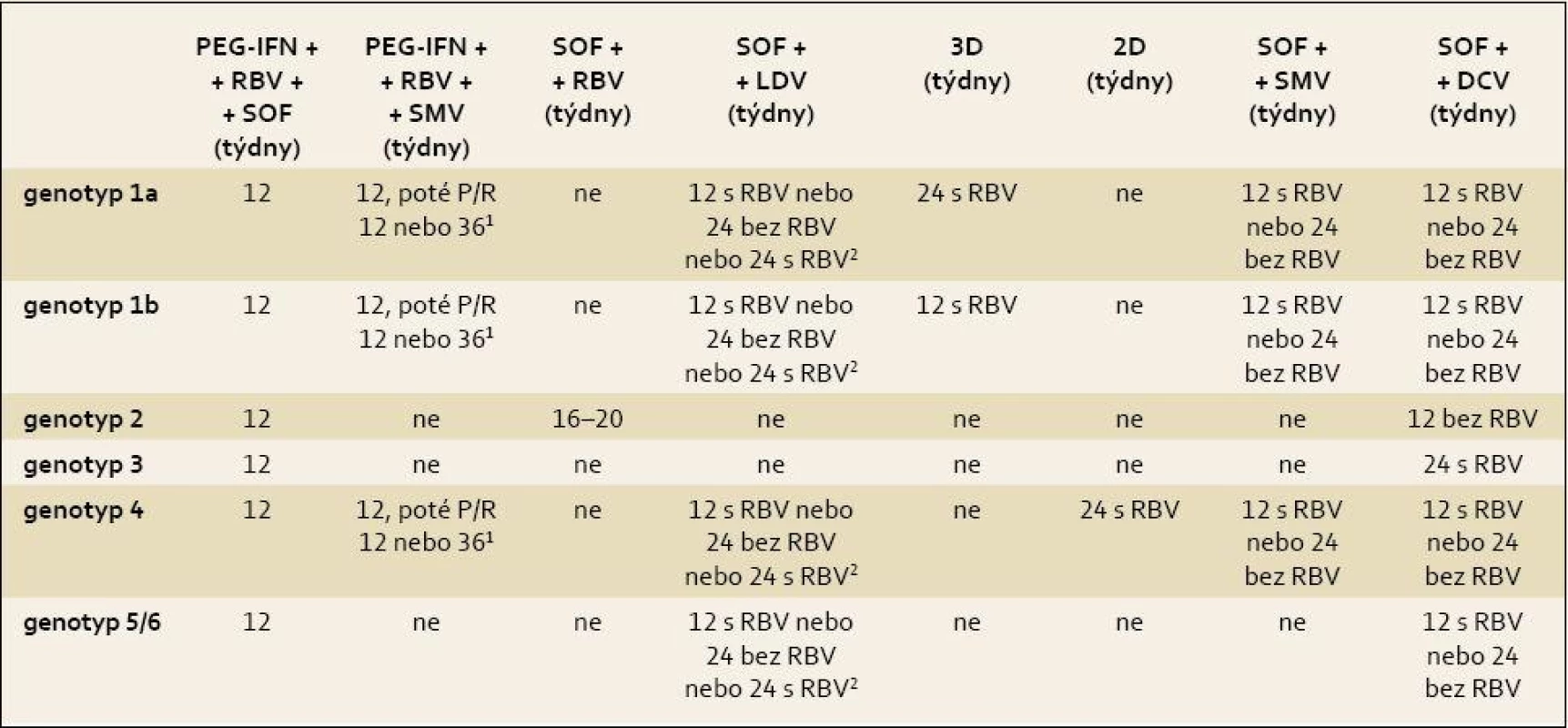
PEG-IFN – pegylovaný interferon α, RBV – ribavirin, SOF – sofosbuvir, LDV – ledipasvir, 3D – ombitasvir + paritaprevir/ritonavir + + dasobuvir, 2D – paritaprevir/ritonavir + ombitasvir, SMV – simeprevir, DCV – daclatasvir 1celková doba léčby 24 týdnů (12 + 12) je doporučována pro dosud neléčené osoby a pro pacienty s relapsem po předchozí kombinaci PEG-IFN + RBV. Celková doba 48 týdnů (12 + 36) je doporučována pro pacienty s částečnou odpovědí a s null response na předchozí protivirovou léčbu kombinací PEG-IFN + RBV (je nutno ale mít na paměti, že účinnost léčby je velmi nízká i při prodloužení léčby), 2 léčba by měla trvat 24 týdnů, pokud jsou přítomny tradiční negativní prediktory efektu léčby. 11.1 Genotyp HCV 1
11.1.1 Léčebná varianta 1: PEG-IFN + ribavirin + sofosbuvir
Dávkování PEG-IFN a RBV uvádí tab. 3. SOF je podáván v dávce 400 mg denně. Délka léčby je 12 týdnů.
Tato varianta se jeví jako nejúčinnější a nejjednodušší u pacientů, kteří mohou být léčeni režimem obsahujícím PEG-IFN. Tento postup nemá riziko selekce rezistentních variant viru. Účinnost kombinace zkoumala studie NEUTRINO. SVR bylo dosaženo celkem v 89 % případů – u subtypu 1a v 92 % a u subtypu 1b v 82 % případů. Pacienti s jaterní cirhózou měli SVR v 80 %, pacienti bez jaterní cirhózy v 92 % případů. Žádné selhání léčby nebylo spojeno se vznikem rezistence na SOF.
V posledním roce byla publikována data z běžné praxe („real life“) z USA (projekty Target a Trio). V projektu Target byla celková SVR4 85 %. Mezi pacienty bez jaterní cirhózy byla SVR4 90 %, mezi cirhotiky 70 %. V projektu Trio byla SVR12 81 % mezi dosud neléčenými pacienty bez cirhózy, 81 % mezi dosud neléčenými cirhotiky, 77 % mezi opakovaně léčenými pacienty bez cirhózy a 62 % mezi pacienty opakovaně léčenými s jaterní cirhózou.
11.1.2 Léčebná varianta 2: PEG-IFN + ribavirin + simeprevir
Dávkování PEG-IFN a RBV uvádí tab. 3. SMV je podáván v dávce 150 mg denně.
SMV v kombinaci s dalšími dvěma preparáty by měl být podáván po dobu 12 týdnů. Další pokračování léčby se liší podle stupně jaterního postižení a efektu případné předchozí léčby:
- Dosud neléčené osoby a osoby s relapsem po předchozí terapii (včetně kompenzovaných cirhotiků) by měly být léčeny kombinací PEG-IFN + RBV po dobu dalších 12 týdnů. Celková doba léčby je tedy 24 týdnů.
- Osoby s částečnou odpovědí a předchozí null-respondéři (včetně kompenzovaných cirhotiků) by měli být léčeni kombinací PEG-IFN + RBV po dobu dalších 36 týdnů. Celková doba léčby je tedy 48 týdnů.
Ve všech případech by měla být léčba ukončena, pokud v týdnech 4, 12 nebo 24 je HCV RNA ≥ 25 IU/ml. Pokud dojde k naplnění těchto pravidel předčasného ukončení, je třeba zvážit bezprostřední přechod na jiný režim obsahující IFN a přímo působící virostatikum nebo na režim léčby bez interferonu.
Kombinace PEG-IFN + RBV + SMV není doporučována u pacientů infikovaných subtypem HCV 1a s prokazatelnou rezistentní variantou Q80K oblasti NS3 proteázy před zahájením léčby. U pacientů s genotypem 1a s průkazem této varianty či v případech, kdy nelze z různých důvodů provést vyšetření přítomnosti této varianty, lze použít k terapii kombinaci PEG-IFN ++ RBV + boceprevir nebo telaprevir.
Kombinace se SMV byla u dosud neléčených pacientů zkoumána ve studiích QUEST-1 a QUEST-2, celková SVR byla 80 a 81 %. Kumulovaná data z obou studií ukázala, že u subtypu 1b byla SVR 85 %. U subtypu 1a bez varianty Q80K byla SVR 84 %, v případě pozitivního průkazu pouze 58 %. Při hodnocení podle stupně jaterního postižení bylo dosaženo těchto výsledků:
- METAVIR F0–F2, SVR 84 %,
- METAVIR F3, SVR 73 %,
- METAVIR F4 (cirhóza), SVR 60 %.
U dosud neléčených pacientů s koinfekcí HCV/HIV byla SVR 79 %. U pacientů s monoinfekcí HCV, kteří relabovali po předchozí léčbě IFN-α ++ RBV, bylo SVR dosaženo v 86 % případů u subtypu 1b a v 70 % u subtypu 1a (bez Q80K 78 %, při pozitivitě Q80K ve 47 %). Ve studii ATTAIN bylo SVR dosaženo u 70 % parciálních respondérů a u 43 % null-respondérů na předchozí terapii kombinací IFN-α ++ RBV. Tato úspěšnost byla v přímém srovnání významně vyšší než účinnost kombinace s telaprevirem ve stejných skupinách osob.
11.1.3 Léčebná varianta 3: sofosbuvir/ledipasvir
Kombinace SOF/LDV je dostupná jako fixní kombinace v jedné tabletě obsahující SOF 400 mg a LDV 90 mg. Standardní dávkování je 1 tableta denně.
Uvedená kombinace byla zkoumána v rozsáhlém programu fáze III. Ve studii ION-1 (dosud neléčené osoby, 16 % pacientů s kompenzovanou jaterní cirhózou) byla SVR12 99 % ve skupině pacientů bez RBV a 97 % ve skupině s RBV. Léčba byla stejně účinná při délce podávání 12 a 24 týdnů. Ve studii ION-3 mezi dosud neléčenými pacienty bez cirhózy byla SVR12 94 % bez RBV při délce podávání 8 týdnů, 93 % s RBV při stejné délce léčby. Při léčbě bez RBV po dobu 12 týdnů byla SVR12 95 %. V ramenech s osmitýdenní léčbou však bylo zaznamenáno větší množství relapsů. Bližší pozdější analýzy ukázaly, že faktorem negativně determinujícím efekt léčby trvající osm týdnů byla viremie ≥ 6 mil. IU/ml. Data však ani v tuto chvíli nelze hodnotit jako definitivní a je třeba vyčkat ověření, že tato kombinace podávaná u dosud neléčených osob po dobu osmi týdnů je dostatečně efektivní.
Studie ION-2 zkoumala účinek této kombinace u pacientů v minulosti neúspěšně léčených. Zahrnuti byli pacienti léčení kombinací PEG-IFN + RBV, ale i PEG-IFN + RBV + boceprevir nebo telaprevir. Jaterní cirhózu mělo 20 % pacientů. SVR12 byla ve skupině s kombinací s RBV 94 %, bez RBV 96 %. Po 24 týdnech byla SVR12 v obou případech 99 %. Ve studii SIRIUS byla zkoumána účinnost SOF/LDV s RBV po dobu 12 týdnů vs. SOF/LDV bez RBV po dobu 24 týdnů u pacientů s kompenzovanou jaterní cirhózou, kteří byli neúspěšně léčeni kombinací PEG-IFN ++ RBV + boceprevir nebo telaprevir. SVR12 byla 96 a 97 %.
11.1.4 Léčebná varianta 4: ombitasvir + paritaprevir/ritonavir + + dasabuvir (3D)
Tato léčebná kombinace se skládá z ombitasviru 12,5 mg, paritapreviru 75 mg a ritonaviru 50 mg v jedné tabletě (dávkování: 2 tablety 1× denně spolu s jídlem) a dasabuviru 250 mg (dávkování: 1 tableta 2× denně).
Pacienti infikovaní genotypem HCV 1b bez jaterní cirhózy by měli být léčeni touto kombinací po dobu 12 týdnů bez RBV.
Pacienti infikovaní genotypem HCV 1b s jaterní cirhózou by měli být léčeni touto kombinací po dobu 12 týdnů s RBV ve standardním váhově definovaném dávkování.
Pacienti infikovaní genotypem HCV 1a bez jaterní cirhózy by měli být léčeni touto kombinací po dobu 12 týdnů s RBV ve standardním váhově definovaném dávkování.
Pacienti infikovaní genotypem HCV 1a s jaterní cirhózou by měli být léčeni touto kombinací po dobu 24 týdnů s RBV ve standardním váhově definovaném dávkování.
Uvedená doporučení jsou opřena o výsledky sedmi studií fáze III.
Studie SAPHIRE-I zkoumala SVR u pacientů dosud neléčených bez jaterní cirhózy. Léčeni byli kombinací 3D s RBV po dobu 12 týdnů a SVR12 byla 95 % u genotypu 1a a 98 % u genotypu 1b. Ve studii PEARL-IV byla SVR12 bez RBV 90 % a 97 % s RBV. Ve studii PEARL-III u pacientů dosud neléčených bez jaterní cirhózy infikovaných genotypem 1b byla SVR12 bez RBV 99 % a s RBV rovněž 99 %. Ve studii TURQUOISE-1 u dosud neléčených osob bez jaterní cirhózy koinfikovaných HIV a stabilizovaných na režimech s atazanavirem nebo reltegavirem byla SVR12 po 12 týdnech 93 %, po 24 týdnech 91 %. U osob infikovaných genotypem 1a byla SVR12 91 % a u infekcí genotypem 1b byla SVR12 100 %.
U osob bez jaterní cirhózy v minulosti neúspěšně léčených PEG-IFN a RBV léčených kombinací 3D s RBV ve studii SAPHIRE-II byla SVR12 u genotypu 1a 96 % a u genotypu 1b 97 %. Souhrnně u relapserů byla SVR12 95 %, 100 % u pacientů s částečnou odpovědí a 95 % u předchozích null-respondérů. Ve studii PEARL-II byla SVR12 100 % u osob infikovaných genotypem 1b a léčených 3D bez RBV a 97 % u osob léčených 3D s RBV. U dosud neléčených osob a osob v minulosti neúspěšně léčených s kompenzovanou cirhózou byla SVR12 92 % po 12týdenní léčbě a 96 % po 24týdenní léčbě s RBV (studie TURQUOISE-II). U osob infikovaných genotypem 1a byla SVR12 92 % a u genotypu 1b byla SVR12 99 %. U osob s koncentrací AFP < 20 ng/ml, počtem trombocytů ≥ 90 × 109 /l a koncentrací albuminu ≥ 35 g/l bylo množství relapsu 1 % po 12 týdnech a 0 % po 24 týdnech léčby. U pokročilejších pacientů s hodnotami AFP > 20 ng/ml, množstvím trombocytů < 90 × 109 /l a koncentrací albuminu < 35 g/l bylo množství relapsů 21 % po 12týdenní léčbě a 2 % po 24týdenní léčbě.
11.1.5 Léčebná varianta 5: sofosbuvir + simeprevir
Dávkování: SOF 400 mg denně a SMV 150 mg denně po dobu 12 týdnů. U pacientů s jaterní cirhózou je doporučeno doplnit kombinaci o podání RBV ve standardním váhově definovaném dávkování. U pacientů s jaterní cirhózou s kontraindikací RBV musí být uváženo prodloužení této léčby na 24 týdnů.
Toto doporučení je založeno na výsledcích studie fáze IIb COSMOS. Studie měla dvě kohorty:
- Kohorta 1 byla tvořena osobami s null-response na předchozí léčbu PEG-IFN + RBV s Metavir skóre F0–F2. Tyto osoby byly léčeny 12 nebo 24 týdnů, s nebo bez RBV. SVR12 byla 93 % pro variantu bez RBV po dobu 12 týdnů, 96 % pro variantu s RBV po dobu 12 týdnů, 93 % pro variantu bez RBV po dobu 24 týdnů a 79 % pro variantu s RBV po dobu 24 týdnů.
- Kohorta 2 byla tvořena osobami dosud neléčeným a předchozími null-respondéry s Metavir skóre F3–F4 léčenými opět s RBV a bez RBV po dobu 12 nebo 24 týdnů. SVR12 byla 93 % pro variantu bez RBV po dobu 12 týdnů, 93 % pro variantu s RBV po dobu 12 týdnů, 100 % pro variantu bez RBV po dobu 24 týdnů a 93 % pro variantu s RBV po dobu 24 týdnů.
Předběžné výsledky dvou rozsáhlých „real life“ studií z USA svědčí pro skutečnost, že tato varianta je dobře tolerována, a že hodnoty SVR12 jsou sice vysoké, ale nižší než SVR12 dosažené ve studii COSMOS. Ze závěru těchto studií nelze učinit žádné terapeutické doporučení.
11.1.6 Léčebná varianta: sofosbuvir + daclatasvir
Dávkování: SOF 400 mg denně a DCV 60 mg denně po dobu 12 týdnů. Tato kombinace by měla být doplněna o RBV v obvyklém dávkování (1 000 nebo 1 200 mg denně) u pacientů s jaterní cirhózou. Pacienti s jaterní cirhózou, u kterých je kontraindikace podání RBV, by měli být léčeni po dobu 24 týdnů.
Uvedené doporučení se opírá o výsledky studií fáze IIb. K SVR vedla 24týdenní léčba ve 100 % případů bez i s RBV u dosud neléčených pacientů. U pacientů léčených neúspěšně kombinací PEG-IFN, RBV a bocepreviru nebo telapreviru byla SVR 100 % bez RBV a 95 % s RBV. Dosud neléčení pacienti, kteří byli léčeni 12 týdnů kombinací bez RBV, dosáhli SVR v 98 % případů. Jedná se o výsledky studií fáze IIb s malými počty pacientů v jednotlivých skupinách.
11.2 Genotyp HCV 2
Ideální léčebnou variantou se jeví kombinace SOF s RBV. Pokud není tato léčebná varianta dostupná, pacienti infikovaní genotypem HCV 2 mohou být léčeni kombinací PEG-IFN a RBV.
11.2.1 Léčebná varianta 1: sofosbuvir + ribavirin
SOF je podáván v dávce 400 mg denně a ribavirin ve standardním dávkování. Délka léčby je 12 týdnů.
Při použití této kombinace bylo dosaženo po 12 týdnech léčby SVR v 95 % případů. Léčba byla účinnější u pacientů bez jaterní cirhózy (97 vs. 83 %). Pacienti s jaterní cirhózou mohou dle dosavadních znalostí profitovat z léčby prodloužené na 16 týdnů (studie FISSION), zejména pokud jde o pacienty opakovaně léčené. Navýšení SVR při takto vedené léčbě bylo proti 12 týdnům o 18 % (60 vs. 78 %). Studie POSITRON měla léčenou skupinu osob tvořenou pacienty, kteří nebyli vhodní pro léčbu s podáním IFN nebo tuto léčbu netolerovali. Léčba v rámci studie POSITRON trvala 12 týdnů. SVR byla 93 %. Při srovnání 12 - a 16týdenní léčby byla SVR 82 a 89 %, mezi cirhotiky pak kratší režim vedl k SVR v 60 % případů a delší režim v 78 %. Pacienti s jaterní cirhózou mají proto větší přínos z léčby trvající 16 týdnů. Studie VALENCE dosáhla SVR po 12 týdnech léčby u dosud neléčených pacientů bez jaterní cirhózy v 97 % případů, 100 % u neléčených cirhotiků, 91 % u opakovaně léčených osob bez jaterní cirhózy a 88 % u opakovaně léčených cirhotiků. Kombinace SOF + RBV byla ve všech studiích dobře tolerována a nebyl zaznamenán žádný virologický breakthrough během léčby. Relapsy nebyly asociovány se vznikem rezistenčních variant.
11.2.2 Léčebná varianta 2: PEG-IFN + RBV + sofosbuvir
Dávkování PEG-IFN a RBV je obvyklé. SOF je podáván v dávce 400 mg denně. Délka léčby je 12 týdnů.
Tato varianta může být užita u pacientů s jaterní cirhózou a/nebo neúspěšnou léčbou v minulosti. Tato kombinace byla studována ve studii LONESTAR-2, kde ve skupině cirhotiků bylo dosaženo SVR v 96 % případů.
11.2.3 Léčebná varianta 3: sofosbuvir + daclatasvir
Tato kombinace podávaná po dobu 12 týdnů je indikována u pacientů s jaterní cirhózou nebo u opakovaně léčených pacientů.
Ve studii fáze II s podáváním této kombinace po dobu 24 týdnů byla SVR 92 %. V souvislosti s ostatními výsledky u genotypů obtížněji léčitelnými, než je genotyp 2, je pravděpodobné, že délka léčby 12 týdnů je v této indikaci dostatečná.
11.3 Genotyp HCV 3
Pro genotyp 3 jsou dostupné tři varianty léčby. Kombinace SOF a RBV se jeví jako suboptimální zejména u pacientů s jaterní cirhózou, kteří byli neúspěšně léčení kombinací PEG-IFN ++ RBV. Jako ideální se jeví kombinace PEG-IFN + RBV + SOF. LDV je ve studiích in vitro méně účinný proti genotypu 3 než DCV. Tato kombinace byla sice zkoumána, nicméně na malém počtu osob, a protože jsou výsledky větších studií dosud očekávány, není tato kombinace aktuálně doporučována. V oblastech, kde žádná z těchto léčebných kombinací není dostupná, zůstává akceptovatelnou variantou léčby PEG-IFN + RBV.
11.3.1 Léčebná varianta 1: PEG-IFN + RBV + SOF
Dávkování PEG-IFN a RBV je obvyklé. SOF je podáván v dávce 400 mg denně. Délka léčby je 12 týdnů.
Tato kombinace se jeví jako nejúčinnější varianta při nejkratší délce trvání terapie. Znalosti o účinnosti této léčby pocházejí ze studie fáze IIb LONESTAR-2, kde bylo dosaženo SVR u 83 % pacientů (20/24 pacientů). Do studie vstoupilo 12 cirhotiků a 10 z nich dosáhlo SVR. Touto léčebnou kombinací bylo také dosaženo SVR 91 % u pacientů neúspěšně léčených kombinací SOF + RBV.
11.3.2 Léčebná varianta 2: sofosbuvir + ribavirin
SOF je podáván v dávce 400 mg denně, RBV v obvyklém dávkování. Délka léčby je 24 týdnů.
Tato terapie je považována za suboptimální zejména u pacientů neúspěšně léčených v minulosti s jaterní cirhózou.
Účinnost této varianty léčby ve studii VALENCE (24 týdnů) byla následující:
- pacienti dosud neléčení bez jaterní cirhózy, SVR 94 %,
- pacienti dosud neléčení s jaterní cirhózou, SVR 92 %,
- pacienti opakovaně léčení bez jaterní cirhózy, SVR 87 %,
- pacienti opakovaně léčení s jaterní cirhózou, SVR 60 %.
Kombinace SOF + RBV podávaná po dobu 12 týdnů byla zkoumána ve studii FISSION. SVR byla 56 %. Lepší léčebná odpověď byla dosažena u pacientů bez jaterní cirhózy (61 vs. 34 % u cirhotiků). Kombinace SOF a RBV po dobu 24 týdnů byla zkoumána i u osob, které relabovaly po stejném režimu podávaném po dobu 12 týdnů. SVR v tomto případě byla pouze 63 %. Ve všech studiích byla léčba dobře tolerována a relapsy nebyly spojeny se vznikem rezistenčních variant.
11.3.3 Léčebná varianta 3: sofosbuvir + daclatasvir
SOF je podáván v dávce 400 mg denně, DCV 60 mg denně. Délka léčby pacientů bez jaterní cirhózy je 12 týdnů. Pacienti neúspěšně léčení v minulosti a pacienti s jaterní cirhózou by měli být léčeni 24 týdnů. Dosud nebyla zveřejněna data o významu doplnění RBV do tohoto léčebného režimu nebo o zkrácení léčby s RBV na 12 týdnů v případě pacientů s cirhózou či neúspěšně léčených v minulosti.
Ve studii fáze IIb s touto kombinací podávanou po 24 týdnů byla SVR 89 % u dosud neléčených pacientů bez jaterní cirhózy. Ve studii fáze III ALLY-3 byli pacienti léčeni touto kombinací po dobu 12 týdnů. SVR12 byla 97 % mezi dosud neléčenými necirhotiky a 58 % mezi dosud neléčenými cirhotiky. Mezi opakovaně léčenými necirhotiky byla SVR12 94 % a mezi opakovaně léčenými pacienty s jaterní cirhózou byla SVR12 69 %. Léčba byla dobře tolerována, nežádoucí účinky nikdy nevedly k ukončení léčby. Nejasný zůstává význam preexistujících rezistenčních variant oblasti NS5A vedoucích k rezistenci na DCV.
11.4 Genotypy HCV 4
11.4.1 Léčebná varianta 1: PEG-IFN + ribavirin + sofosbuvir
Dávkování PEG-IFN a RBV je obvyklé. SOF je podáván v dávce 400 mg denně. Délka léčby je 12 týdnů.
Léčba dosud neléčených pacientů infikovaných genotypem HCV 4 byla součástí studie fáze III NEUTRINO. SVR12 v této skupině byla 96 %. Jediný pacient, který relaboval, nevyvinul žádnou z možných rezistenčních variant. Žádná další data nejsou v tuto chvíli dostupná (opakovaně léčené osoby, HCV/HIV koinfekce apod.).
11.4.2 Léčebná varianta 2: PEG-IFN + ribavirin + simeprevir
Dávkování PEG-IFN a RBV uvádí tab. 3. SMV je podáván v dávce 150 mg denně. Délka podávání SMV v kombinaci s PEG-IFN a RBV je 12 týdnů. U dosud neléčených pacientů, relapsérů po předchozí léčbě (včetně cirhotiků), následuje dalších 12 týdnů léčby kombinací PEG-IFN + RBV. Celková doba léčby je tedy u dosud neléčených a u relapserů 24 týdnů. U pacientů hodnocených při předchozí léčbě jako „partial response“ a „null response“ (včetně cirhotiků) následuje po 12 týdnech léčby se SMV ještě 36 týdnů léčby kombinací PEG-IFN + RBV. Celková doba léčby je tedy 48 týdnů. Léčba by měla být ukončena, pokud je HCV RNA > 25 IU/ml v týdnech 4, 12 nebo 24.
Dosavadní výsledky studie fáze III na 107 pacientech infikovaných genotypem 4 jsou následující:
- dosud neléčení pacienti, SVR12 83 %,
- relapséři, SVR12 86 %,
- částečná odpověď, SVR12 60 %,
- null response, SVR12 40 %.
Žádný z léčených pacientů neměl před vstupem do léčby prokazatelnou mutaci NS3 Q80K, která je asociována s rezistencí na SMV.
11.4.3 Léčebná varianta 3: sofosbuvir/ledipasvir
Kombinace SOF/LDV je dostupná jako fixní kombinace v jedné tabletě obsahující SOF 400 mg a LDV 90 mg. Standardní dávkování je 1 tableta denně.
Pacienti bez jaterní cirhózy, dosud neléčení i opakovaně léčení, by měli být léčeni touto kombinací po dobu 12 týdnů bez RBV. RBV by měl být součástí léčby trvající 12 týdnů u pacientů dosud neléčených i opakovaně léčených, pokud mají jaterní cirhózu. RBV je v tomto případě podáván v obvyklém dávkování. Osoby mající kontraindikaci podání RBV by měly být léčeny fixní kombinací po dobu 24 týdnů. Léčba fixní kombinací s RBV by měla být prodloužena na 24 týdnů u pacientů opakovaně léčených s kompenzovanou jaterní cirhózou a negativními prediktory odpovědi, jako je např. počet krevních destiček ≤ 75 000/µl.
Doporučení se opírá především o výsledky studie SYNERGY. SVR12 byla 95 % (20/21 – jeden pacient ukončil studii předčasně). Nejasné zůstává, zda by u dosud neléčených osob mohla být léčba zkrácena na osm týdnů.
11.4.4 Léčebná varianta 4: ombitasvir + paritaprevir/ritonavir (2D)
Pacienti infikovaní genotypem HCV 4 bez jaterní cirhózy mohou být léčeni kombinací ombitasviru (12,5 mg), paritapreviru (75 mg) a ritonaviru (50 mg) v jedné tabletě (denní dávka je 2 tablety denně) po dobu 12 týdnů. Kombinace 2D je u genotypu HCV4 standardně doplněna o RBV v obvyklém dávkování. Součástí léčby není dasabuvir. Pacienti s jaterní cirhózou infikovaní gentoypem HCV 4 mají být léčeni stejnou kombinací po dobu 24 týdnů.
Tato doporučení se opírají o výsledky studie PEARL-I. Tato studie zahrnovala pacienty dosud neléčené i opakovaně léčené, bez jaterní cirhózy. Délka léčby s RBV byla 12 týdnů. SVR12 byla v obou skupinách 100 %. Studie s cirhotiky v tuto chvíli probíhá a dosud nebyly zveřejněny její výsledky.
11.4.5 Léčebná varianta 5: sofosbuvir + simeprevir
Dávkování: SOF 400 mg denně a SMV 150 mg denně po dobu 12 týdnů. Kombinace by u pacientů s jaterní cirhózou měla být doplněna o RBV ve standardním dávkování (tab. 3). Pokud je RBV kontraindikován, léčba by měla trvat 24 týdnů.
Tato kombinace nebyla dosud zkoumána v žádné klinické studii pokročilé fáze. Její doporučení se opírá o in vitro prokázanou účinnost obou složek kombinace u genotypu HCV 4 a o extrapolaci výsledků studie COSMOS.
11.4.6 Léčebná varianta 6: sofosbuvir + daclatasvir
SOF je podáván v dávce 400 mg denně, DCV 60 mg denně. Délka léčby je 12 týdnů. U pacientů s jaterní cirhózou by léčba měla být doplněna o podání RBV ve standardním dávkování (tab. 3). Pokud je RBV kontraindikován, léčba by měla trvat 24 týdnů.
Tato kombinace nebyla dosud zkoumána v žádné klinické studii pokročilé fáze. Její doporučení se opírá o in vitro prokázanou účinnost obou složek kombinace u genotypu HCV 4 a o extrapolaci výsledků dosažených u genotypu HCV 1.
11.5 Genotypy HCV 5 a 6
Tyto genotypy se v ČR prakticky nevyskytují, léčebné varianty proto nebudou rozebírány. V případě nutnosti lze všechny léčebné možnosti nalézt v textu standardních doporučení vydaných Evropskou asociací pro studium jater na www.easl.eu.
12. Monitorování léčby HCV infekce
12.1 Monitorování účinnosti léčby
Monitorování účinnosti léčby je založeno na opakovaném sledování koncentrace HCV RNA v krvi. K tomuto účelu je třeba užívat metody o standardní citlivosti ≤ 15 IU/ml. Nutné je dbát na to, aby při sledování jednoho konkrétního pacienta byla využívána stejná metoda, ideálně stejná laboratoř. Pro účely monitorování účinnosti léčby a pro kvalifikované rozhodování o pokračování či naopak o ukončení protivirové léčby je třeba respektovat definované časové body, kdy je vyšetření HCV RNA indikováno. Časové body, kdy je vhodné vyšetření HCV RNA, se mohou u jednotlivých léčebných variant lišit, vždy však byly určeny tak, aby znalost HCV RNA v daném okamžiku měla vliv na předepsaný léčebný režim. Obecně jde o tyto indikace:
- ověření adherence pacienta k léčbě (týden 2 léčby) – u bezinterferonových režimů,
- rozhodnutí o ukončení či pokračování léčby, „futility rules“,
- rozhodnutí o případném zkrácení protivirové léčby, tzv. léčba vedená podle odpovědi (response guided therapy – RGT),
- rozhodnutí o úspěchu léčby, tj. v okamžiku ukončení léčby a ve 12. a/nebo 24. týdnu po skončení léčby (SVR).
12.1.1 Monitorování účinnosti léčby u jednotlivých léčebných variant
PEG-IFN + RBV + SOF:
- zahájení léčby, týdny 4, 12 během léčby,
- týdny 12 a/nebo 24 po skončení léčby.
PEG-IFN + RBV + SMV:
- zahájení léčby, týdny 4, 12, 24 (konec léčby u dosud neléčených a předchozích relapsérů) + týden 48 (konec léčby u předchozích parciálních respondérů a null-respondérů),
- týdny 12 a/nebo 24 po skončení léčby,
- týdny 12 a/nebo 24 po skončení léčby.
Bezinterferonové režimy (SOF + + SMV +/ – RBV 12 týdnů, SOF + + DCV +/ – RBV 12/24 týdnů, SOF + RBV 12/24 týdnů):
- zahájení léčby, týdny 2, 4, 12, 24,
- týdny 12 a/nebo 24 po skončení léčby.
Pravidla předčasného ukončení (futility rules) z důvodu minimální/nulové pravděpodobnosti dosažení SVR byla definována pouze pro trojkombinaci PEG-IFN + RBV + SMV.
Léčba tímto režimem by měla být ukončena, pokud je HCV RNA ≥ 25 IU/mlv týdnu 4, 12 nebo 24.
Pro žádný jiný léčebný režim s novými DAA nebyla podobná pravidla definována.
12.2 Monitorování bezpečnosti léčby HCV infekce
Dosud nebyly definovány vhodné intervaly klinických kontrol z pohledu monitorování možných nežádoucích účinků léčby. Tyto je třeba individualizovat s ohledem na dostupná data o výskytu možných vážnějších nežádoucích reakcí.
Pacienti léčeni protivirovými režimy se SOF by měli mít pravidelně kontrolovány renální funkce. SMV může být příčinou zvýšení sérové koncentrace nepřímého bilirubinu a kožních reakcí. 3D kombinace může rovněž vést ke vzestupu koncentrace nepřímého bilirubinu. Dosud bylo prokázáno, že u pacientů s mírnou, střední a těžkou renální insuficiencí není třeba redukovat dávky SMV, LDV a DCV. Vhodná redukce SOF u pacientů s eGFR ≤ 30ml/min/1,73 m2 nebyla dosud stanovena. Redukce dávek není třeba u kombinace SOF/LDV ani u DCV u pacientů s jaterní cirhózou funkční klasifikace Child-Pugh C. Vyšší sérové hladiny účinných látek byly pozorovány u 3D kombinace u cirhózy s jaterní dysfunkcí, a proto je v této skupině potřeba získat další data před vydáním finálních doporučení.
12.3 Monitorování lékových interakcí během léčby HCV infekce
Dostupné nové protivirové léky často přinášejí množství lékových interakcí. Proto je třeba během podávání nových léčebných režimů opakovaně kontrolovat současné podávanou medikaci. V indikovaných případech je třeba konkomitantní léčbu přerušit (pokud lze) nebo zvolit alternativu s menším rizikem interakcí. Významnost interakcí si lze ověřit na www.hep-druginteractions.org.
13. Metody zvýšení adherence pacientů k léčbě
Plná adherence ke všem podávaným a výše diskutovaným preparátům je základní podmínkou dosažení vysoké úspěšnosti léčby, tj. vysoké SVR. Není-li tato podmínka splněna, je vysoké riziko selhání léčby ať už ve formě breakthrough fenoménu či relapsu HCV po skončení protivirové léčby, v případě podání DAA se dále zvyšuje také riziko vzniku virologické rezistence. Existuje několik základních opatření, jak adherenci zvýšit:
- Před zahájením léčby je nutno s pacienty diskutovat veškeré možné a očekávané vedlejší účinky léčby. Je potřeba pacientům vysvětlit, že řadě z nich lze účinně zabránit či je terapeuticky ovlivnit v případě jejich rozvoje během protivirové léčby.
- Klíčovým opatřením je přístup pacientů ke specialistům multidisciplinárního týmu s maximem zkušeností s terapií HCV infekce a se zvládáním všech nežádoucích účinků, s monitoringem účinnosti a bezpečnosti protivirové léčby.
- Alkohol negativně ovlivňuje výsledky protivirové léčby. Během léčby by proto měla být pacientům doporučována abstinence či maximální možná redukce jeho příjmu. Pacientům s pokračující konzumací alkoholu, kteří jinak dobře spolupracují, by protivirová léčba neměla být odmítnuta.
14. Péče o pacienty s dosaženou SVR
Pacienti bez jaterní cirhózy, kteří dosáhli SVR, by měli být znovu testováni ve 48. týdnu po skončení léčby. Pokud je v tomto okamžiku HCV RNA v krvi nedetekovatelná, je možno považovat HCV infekci za vyléčenou v daném případě a HCV RNA již dále nemusí být vyšetřována. V období jednoho a dvou let po skončení protivirové léčby s režimy obsahujícími PEG-IFN je třeba kontrolovat funkci štítné žlázy. Pacienti se SVR, u nichž ale byly před zahájením protivirové léčby přítomny ještě jiné možné příčiny jaterního onemocnění (DM, zvýšený příjem alkoholu), by měli být dále sledováni v odborných poradnách. Interval sledování nebyl stanoven.
Pacienti s jaterní cirhózou, kteří dosáhnou SVR, by měli být zařazeni do programů surveillance HCC a měla by být u nich monitorována možná progrese portální hypertenze. U této skupiny nemocných je proto indikována abdominální sonografie v intervalu šesti měsíců, a pokud byly přítomny jícnové varixy před zahájením léčby, je třeba provádět endoskopické vyšetření v intervalu jednoho roku. Další faktory, DM2 či anamnéza abúzu alkoholu, mohou tento navrhovaný postup modifikovat.
U osob s vysoce rizikovým chováním, jako jsou např. intravenózní uživatelé drog či homosexuálové, je třeba uvažovat i o riziku reinfekce. Riziko reinfekce je nicméně malé, publikovaná data se pohybují v rozmezí 1–5 % ročně. Reinfekci lze prokázat jen opakovaným vyšetřením HCV RNA v krvi.
15. Opakovaná léčba pacientů bez dosažení SVR
U pacientů infikovaných genotypem HCV 1, kteří byli léčeni kombinací PEG-IFN + RBV + telaprevir či boceprevir, lze zvážit podání kombinace SOF a SMV. Zkušenosti s touto léčebnou variantou jsou dané pouze „real-life“ programem TRIO. SVR12 v tomto programu byla 83 %, což jsou stejné výsledky jako pro pacienty s neúspěchem kombinace PEG-IFN + RBV. SVR12 ve stejném programu při užití režimu PEG-IFN + RBV + SOF po dobu 12 týdnů byla 73 %.
Další variantou postupu je kombinace SOF a DCV. Účinnost tohoto režimu byla 100 % s RBV a 95 % bez RBV. V této populaci dosud nebyla zkoušena kombinace PEG-IFN + SOF + RBV. Na základě předběžných výsledků lze považovat v této indikaci za slibnou i kombinaci SOF a LDV.
16. Léčba pacientů s hepatocelulárním karcinomem bez indikace k transplantaci jater
Pravidla léčby této skupiny pacientů se nijak neliší od pravidel probraných v předchozích kapitolách. U pacientů s možností jiné radikální léčby (resekce) je léčba jednoznačně indikovaná. U pacientů bez možnosti radikální léčby je nutno vždy individuálně zhodnotit prognózu pacienta a přínos léčby.
17. Léčba pacientů s pokročilým jaterním onemocněním
17.1 Kompenzovaná jaterní cirhóza
Pacienti s kompenzovanou jaterní cirhózou představují skupinu osob, u kterých by měla být protivirová léčba zahájena co nejdříve. Všechny komplikace jaterní cirhózy, dekompenzace, rozvoj HCC, se v této skupině může objevit v krátkém časovém horizontu. Snížení incidence dekompenzace a HCC v případech úspěšné léčby bylo prokázáno opakovaně metaanalýzami. Na druhou stranu je léčba těchto pokročilých stadií onemocnění spojena s nižší pravděpodobností dosažení SVR, a to i při použití režimů s DAA. Tito pokročilí pacienti rovněž vyžadují zvláštní péči ve smyslu prevence a včasné léčby závažných nebo potenciálně závažných nežádoucích účinků léčby. Jde většinou o pacienty, kteří jsou ve srovnání s pacienty bez cirhózy starší, mající řadu souběžné medikace, a tudíž také léčbu hůře snášejí. Preferovanými režimy v této skupině jsou v současné době bezinterferonové režimy. Použití režimů založených na interferonu se v současné době jeví jako racionální pouze v situaci, že bezinterferonové režimy nejsou dostupné.
17.2 Dekompenzovaná jaterní cirhóza
Pacienti s genotypem 1: jediným režimem s prokázanou účinností a bezpečností u pacientů s dekompenzovanou jaterní cirhózou je fixní kombinace SOF (400 mg denně) s LDV (90 mg denně) po dobu 12 týdnů.
Pacienti s genotypy 2 a 3: bezpečnost a účinnost byla prokázána pouze v menších studiích pro kombinaci SOF s ribavirinem po dobu 24 týdnů.
17.3 Pacienti indikovaní k transplantaci jater
Transplantace (Tx) jater je postupem volby u pacientů s konečným stadiem jaterního onemocnění. Rekurence HCV infekce s reinfekcí štěpu po Tx je prakticky 100 %, což negativně ovlivňuje přežití příjemců i štěpů. U pacientů, kteří se připravují na Tx jater, musí být vždy zvažována protivirová léčba. Dosažení SVR před transplantací spolehlivě zabrání rekurenci HCV po transplantaci. V současné době je ale k dispozici účinná léčba i pro pacienty po transplantaci. Zahájení léčby před transplantací je nutno zvažovat i s ohledem na předpokládanou dobu čekání na transplantaci a pokročilost cirhózy. Účinnost léčby po transplantaci je totiž vyšší ve srovnání s pokročilými cirhotiky klasifikace dle Child-Pugh C. Léčbu před transplantací je nutno časovat tak, aby ji pacient mohl absolvovat pokud možno celou, transplantaci při léčbě lze připustit nejdříve po 30 dnech negativní viremie (HCV RNA).
Pacienti před transplantací jater mohou být léčeni kombinacemi antivirotik, která jsou výše popsána v odstavcích týkajících se léčby pacientů s kompenzovanou a dekompenzovanou cirhózou jater. Většina pacientů, kteří se připravují k transplantaci jater, jsou pacienti s dekompenzovanou cirhózou, jen asi 20 % z nich jsou kompenzovaní cirhotici, kteří jsou k transplantaci indikováni pro malý HCC v cirhóze.
17.4 Pacienti po transplantaci jater
Rekurence HCV infekce po Tx jater postihuje téměř všechny pacienty. Průběh infekce po Tx je akcelerován a přibližně u třetiny pacientů se rozvine jaterní cirhóza během pěti let po Tx. V posledních letech se podařilo prokázat, že úspěšná protivirová léčba má velmi pozitivní vliv na přežití štěpu i pacienta.
Pacienti s potransplantační rekurencí infekce jsou proto kandidáty protivirové léčby. Dostupná data o účinnosti léčby v této skupině jsou omezená. Kombinace SOF + RBV po dobu 24 týdnů vedla k dosažení SVR12 u 70 % pacientů s lehkou formou rekurentní hepatitidy C (nebyli zařazováni pacienti s dekompenzovanou cirhózou stěpu a fibrotizující cholestatickou hepatitidou). Kombinace SOF a SMV byla účinná i u pacientů s těžkou rekurentní cholestatickou hepatitidou po Tx jater. Těžká forma rekurence byla úspěšně léčena i kombinací SOF s DCV.
17.4.1 Léčebné varianty po transplantaci jater
- Pacienti s infekcí vyvolanou HCV genotypem 2 musí být léčeni kombinací RBV ve standardním dávkování se SOF 400 mg denně po dobu 12–24 týdnů.
- Pacienti s infekcí vyvolanou HCV genotypem 1 mohou být léčeni fixní kombinací SOF 400 mg denně a LDV 90 mg denně po dobu 12–24 týdnů. K této kombinaci může být doplněn RBV v obvyklém dávkování. U této kombinace není třeba změna dávkování takrolimu a cyklosporinu.
- Pacienti s infekcí vyvolanou HCV genotypy 1 a 3–6 mohou být léčeni kombinací SOF 400 mg denně a DCV 60 mg denně po dobu 12–24 týdnů. K této kombinaci může být doplněn RBV v obvyklém dávkování. U této kombinace není třeba změna dávkování takrolimu a cyklosporinu.
- Pacienti s HCV genotypem 1 nebo 4 mohou být léčeni kombinací SOF 400 mg denně, SMV 150 mg denně po dobu 12–24 týdnů. K této kombinaci může být doplněn RBV v obvyklém dávkování. Kombinace se SMV se nedoporučuje u pacientů užívajících cyklosporin, dávkování takrolimu není třeba měnit.
- Pacienti s genotypem 1b mohou být léčeni kombinací paritapreviru, ombitasviru a dasabuviru s RBV 12 týdnů, u genotypu 1a u pacientů s cirhózou by měla být délka léčby prodloužena na 24 týdnů. Při užití této kombinace je třeba redukovat dávku takrolimu i cyklosporinu a respektovat i ostatní lékové interakce.
18. Léčba pacientů s komorbiditami
18.1 Koinfekce HBV/HCV
Neexistují zatím žádná obecně platná doporučení pro léčbu pacientů s koinfekcí HBV/HCV. Je nutný individuální přístup a postupné uplatňování nových zkušeností s léčbou těchto pacientů. U naprosté většiny těchto pacientů tlumí replikace HCV replikaci HBV, proto lze zpravidla v séru prokázat HCV RNA, zatímco sérová koncentrace HBV DNA je pod hranicí detekovatelnosti. HCV je pak hlavním nositelem a příčinou jaterního postižení. Z uvedeného vyplývá, že u těchto osob je zapotřebí stanovit replikační aktivitu obou virů, tj. stanovit sérové hladiny HBV DNA i HCV RNA. Indikováno je i vyšetření sérologie HDV (případně i HDV RNA). Pokud je hlavním patogenetickým činitelem HCV, je třeba v případech koinfekce postupovat stejně jako u monoinfekce HCV. Po dosažení eliminace HCV je určité riziko reaktivace HBV. Pokud k této situaci dojde a objeví se významná replikace HBV, je indikováno zahájení léčby nukleotidovými analogy. Nukleotidová analoga jsou indikována jako součást protivirové léčby i v případě, že významná replikace HBV je přítomna i před zahájením protivirové léčby HCV infekce.
18.2 Pacienti v pravidelném dialyzačním léčení
Pacienti zařazení do pravidelného dialyzačního léčení (PDL) představují velmi speciální skupinu nemocných s chronickou HCV infekcí. HCV infekce je u pacientů v PDL asociována s vyšší všeobecnou i jaterní mortalitou. Hlavním faktorem limitujícím přežití těchto nemocných však zůstává kardiovaskulární morbidita. Největším rizikem vyplývajícím z HCV infekce je reaktivace infekce po transplantaci ledviny při imunosupresivní léčbě. K protivirové léčbě by měli proto být indikováni zejména hemodialyzovaní pacienti, kteří jsou vhodnými kandidáty transplantace ledviny.
V ostatních případech je třeba zcela individuální přístup, zvážení závažnosti jaterního postižení, celkové prognózy nemocného a především možných rizik vyplývajících z podání protivirové léčby. Léčba pacientů v PDL by měla být vedena na pracovišti majícím s touto skupinou nemocných zkušenosti.
Použití RBV u této populace je limitováno, dávkování je třeba individualizovat. Zprávy jsou o podávání RBV 200 mg denně, 200 mg obden nebo 200 mg 3× týdně (vždy po hemodialýze). Z těchto důvodů by pacienti zařazení do PDL měli být léčeni preferenčně režimy bez INF a ideálně i bez RBV. U pacientů bez jaterní cirhózy by léčba měla trvat 12 týdnů, u pacientů s jaterní cirhózou pak 24 týdnů.
SMV, DCV a 3D kombinace jsou eliminovány především játry, a proto se jeví jako rozumná varianta léčby u pacientů v PDL. SOF by neměl být užit u pacientů s eGFR ≤ 30 ml/min/1,73 m2. Důvodem tohoto doporučení je absence dat u takto pokročilé renální insuficience. U většiny dosud registrovaných DAA nejsou dostupná data umožňující definovat potřebné redukce dávek u pacientů s renální insuficiencí. Tyto léky by proto měly být užívány pouze s velkou opatrností a léčba by měla být vedena ve specializovaných centrech s velkou zkušeností s touto specifickou podskupinou nemocných.
18.3 Příjemci orgánových štěpů (s výjimkou jater)
HCV infikovaní příjemci transplantované ledviny jsou ohroženi rychlým průběhem jaterní fibrózy. HCV přitom negativně ovlivňuje přežití štěpu i pacienta. Přežití pacienta je ovlivněno i dalšími faktory asociovanými s HCV (HCV asociovanou glomerulonefritidou), ale i faktory bez vztahu k HCV. I v této skupině nemocných je hlavním limitujícím faktorem kardiovaskulární morbidita. Přítomnost jaterní cirhózy v okamžiku Tx ledviny je jedním z nejvýznamnějších negativních faktorů asociovaných se špatnou prognózou po Tx. Z tohoto důvodu by u všech HCV RNA pozitivních kandidátů Tx ledviny měl být určen stupeň jaterní fibrózy před provedením Tx. U pacientů s jaterní cirhózou a portální hypertenzí, u kterých je léčba založená na podání PEG-IFN považována za kontraindikovanou, je možno považovat za kontraindikovanou i izolovanou Tx ledviny. Zvážena by měla být kombinovaná Tx jater a ledviny. Podání PEG-IFN po Tx ledviny je kontraindikováno pro riziko rejekce štěpu, proto existuje urgentní potřeba získat data o použití bezinterferonových režimů v této indikaci. Tato data nejsou dosud dostupná. Odmítnutí protivirové terapie pacientem není absolutní kontraindikací první transplantace ledviny. Podmínkou je nepřítomnost pokročilé fibrózy jater a nízká zánětlivá aktivita.
Data o HCV infekci u pacientů před transplantací srdce, nebo po ní jsou kontroverzní. Z možností protivirové léčby by měly být preferovány bezinterferonové režimy, zvážení rizik a přínosu je přísně individuální.
HCV infekce je považována v řadě center za kontraindikaci transplantace plic, perspektiva bezinterferonové léčby po transplantaci ale takovou kontraindikaci činí jen relativní.
18.4 Hemofilici
Charakteristiky HCV infekce u pacientů s různými typy hemofilií se nijak neliší od pacientů HCV pozitivních bez hemofilie. Metodou volby pro určení stadia jaterního postižení jsou v této skupině neinvazivní metody, v případech, kdy je indikováno měření portosystémového gradientu, lze provést současně i jaterní biopsii transjugulárním přístupem. Úmrtí z jaterních příčin patří v této skupině pacientů mezi nejčastější příčiny úmrtí. S výjimkou omezení pro jaterní biopsii je péče o HCV pozitivní hemofiliky stejná jako pro ostatní populaci. Nová DAA lze proto u této skupiny použít podle stejných pravidel.
18.5 Aktivní uživatelé drog
Drogová závislost je uvedena v Mezinárodní statistické klasifikaci nemocí a přidružených zdravotních problémů. Na pacienta drogově závislého je proto nutné pohlížet jako na člověka nemocného. Ani medicínsky ani eticky není tedy odůvodnitelné odmítnutí jakékoli léčby uživatelům drog. Rozhodující je vždy zvážení přínosu a rizika pro individuálního pacienta.
Aktivní abúzus alkoholu a drog negativně ovlivňuje adherenci k léčbě. Drogově závislí mají častější výskyt poruch mentálního zdraví, častější psychiatrické onemocnění. Obojí dále zhoršuje adherenci k terapii. Studie léčených pacientů s aktivní drogovou závislostí ukazují srovnatelný efekt terapie chronické HCV infekce s jinými skupinami infikovaných osob. Rychlá inhibice replikace viru hepatitidy C (již během osmi hodin po aplikaci interferonu) zabraňuje dalšímu šíření infekce.
Zcela zásadní podmínkou pro zahájení terapie je motivace pacienta a jeho adherence k terapii. Předčasné ukončení terapie na základě špatné adherence je častější v prvních 12 týdnech. Kontrolou pomůcek a další intervencí u uživatelů drog lze snížit riziko reinfekce.
K léčbě musí být pacient motivován a musí spolupracovat, aby bylo možno snížit riziko rozvoje závažných nežádoucích účinků terapie. Tyto často souvisejí se současným užíváním drog a kombinované protivirové terapie. Léčba drogově závislých je multifaktoriální a multioborová. Předpokládá zajištění psychiatrické intervence, sociálního šetření. Drogově závislý musí být před léčbou vyšetřen psychiatrem nebo lékařem pro léčbu závislostí. K uživatelům drog musí být vždy individuální přístup.
Pacienti na substituční léčbě jsou považováni za pacienty s kontrolovaným psychiatrickým onemocněním. Postup, diagnostika a terapie virové hepatitidy C u spolupracujícího pacienta, u pacienta s aktivní drogovou závislostí (nebo na substituční terapii), je shodný s doporučeným postupem u pacientů bez závislosti.
18.6 Akutní HCV infekce
Průběh akutní HCV infekce je ve většině případů asymptomatický, ale ke chronickému průběhu onemocnění dochází v 50–90 % případů. Symptomatický průběh, ženské pohlaví, nižší věk a genotyp IL28B CC jsou faktory asociované se spontánní eliminací viru. Žádný z těchto parametrů však nemá dostatečnou individuální prediktivní hodnotu. Pacienti s diagnostikovanou akutní hepatitidou C by měli být považováni za kandidáty protivirové léčby. V této skupině pacientů bylo dosaženo SVR > 90 % při podání monoterapie PEG-IFN-α. Doplnění RBV do kombinace v této indikaci nijak nenavyšuje SVR. Data s novými DAA v indikaci akutní HCV infekce nebyla dosud publikována.
Ideální okamžik zahájení protivirové léčby nebyl u akutní HCV infekce definován. Někteří autoři považují za ideální okamžik k zahájení léčby okamžik vzniku elevace ALT, a to bez ohledu na přítomnost či absenci dalších klinických příznaků. Alternativou postupu je vyčkat do 12. týdne od vzniku příznaků a léčbu zahájit pouze u osob, které jsou i v tomto okamžiku HCV RNA pozitivní. Tento postup se jeví racionální především v symptomatických případech u osob s genotypem CC lokusu rs12979860 genu IL28B.
19. Sledování pacientů neléčených a pacientů s neúspěšnou léčbou
Pacienti neléčení a pacienti s prodělanou neúspěšnou terapií (tj. bez SVR) by měli být dál pravidelně sledováni. Základním pravidlem má být zdokumentování důvodu nepodání protivirové léčby v daném okamžiku a případně typu odpovědi na předchozí protivirovou léčbu a pravděpodobného důvodu selhání předchozí léčby (zejména při suspekci na špatnou adherenci k léčbě). Neléčení pacienti by měli podstoupit kompletní vyšetření každých 12–24 měsíců, v intervalu dvou let může být provedeno i neinvazivní měření stadia jaterní fibrózy. Pacienti s jaterní cirhózou by měli absolvovat program surveillance HCC, tj. abdominální ultrasonografii každých šest měsíců.
20. Vakcinace proti ostatním virovým infekcím jater
Všichni pacienti s chronickou HCV infekcí by měli být očkováni proti virové hepatitidě A. Séronegativní pacienti (tj. HBsAg a anti-HBs negativní) by měli být očkováni i proti virové hepatitidě B.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Datum aktualizace: 16. 8. 2015
Datum schválení výborem ČHS ČLS JEP: 1. 10. 2015
prof. MUDr. Petr Urbánek, CSc.
Interní klinika 1. LF UK a ÚVN Praha
U Vojenské nemocnice 1200
169 02 Praha 6
petr.urbanek@uvn.cz
Zdroje
1. EASL Clinical Practice Guidelines: management of hepatitis C virus infection. J Hepatol 2014; 60(2): 392–420. doi: 10.1016/j.jhep.2013.11.003.
2. Jensen DM, O’Leary JG, Pockros PJ et al. Safety and efficacy of sofosbuvir-containing regimens for hepatitis C: realworld experience in a diverse, longitudinal observational cohort. Hepatology 2014; 60: 219A.
3. Dieterich D, Bacon BR, Flamm SL et al. Evaluation of sofosbuvir and simeprevir-based regimens in the TRIO network: academic and community treatment of a real-world, heterogeneous population. Hepatology 2014; 60: 220A.
4. Lawitz E, Sulkowski MS, Ghalib R et al. Simeprevir plus sofosbuvir, with or without ribavirin, to treat chronic infection with hepatitis C virus genotype 1 in non-responders to pegylated interferon and ribavirin and treatment-naive patients: the COSMOS randomised study. Lancet 2014; 384(9956): 1756–1765. doi: 10.1016/S0140-6736(14)61036-9.
5. Sulkowski MS, Gardiner DF, Rodriguez-Torres M et al. Daclatasvir plus sofosbuvir for previously treated or untreated chronic HCV infection. N Engl J Med 2014; 370(3): 211–221. doi: 10.1056/NEJMoa1306218.
6. Afdhal N, Zeuzem S, Kwo P et al. Ledipasvir and sofosbuvir for untreated HCV genotype 1 infection. N Engl J Med 2014; 370(20): 1889–1898. doi: 10.1056/NEJMoa1402454.
7. Bourlire M, Bronowicki JP, de Ledinghen V et al. Ledipasvir/sofosbuvir fixed dose combination is safe and efficacious in cirrhotic patients who have previously failed protease-inhibitor based triple therapy. Hepatology 2014; 60 : 1271A.
8. Feld JJ, Kowdley KV, Coakley E et al. Treatment of HCV with ABT-450/r-ombitasvir and dasabuvir with ribavirin. N Engl J Med 2014; 370(17): 1594–1603. doi: 10.1056/NEJMoa1315722.
9. Ferenci P, Bernstein D, Lalezari J et al. ABT-450/rombitasvir and dasabuvir with or without ribavirin for HCV. N Engl J Med 2014; 370(21): 1983–1992. doi: 10.1056/NEJMoa1402338.
10. Wyles DL, Sulkowski MS, Eron JJ et al. TURQUOISE-I: 94% SVR12 in HCV/HIV-1 coinfected patients treated with ABT-450/r/ombitasvir, dasabuvir and ribavirin. Hepatology 2014; 60 : 1136A.
11. Zeuzem S, Jacobson IM, Baykal T et al. Retreatment of HCV with ABT-450/r-ombitasvir and dasabuvir with ribavirin. N Engl J Med 2014; 370(17): 1604–1614. doi: 10.1056/NEJMoa1401561.
12. Andreone P, Colombo MG, Enejosa JV et al. ABT-450, ritonavir, ombitasvir, and dasabuvir achieves 97% and 100% sustained virologic response with or without ribavirin in treatment experienced patients with HCV genotype 1b infection. Gastroenterology 2014; 147(2): 359–365. doi: 10.1053/j.gastro.2014.04.045.
13. Poordad F, Hezode C, Trinh R et al. ABT-450/r-ombitasvir and dasabuvir with ribavirin for hepatitis C with cirrhosis. N Engl J Med 2014; 370(21): 1973–1982. doi: 10.1056/NEJMoa1402869.
14. Jacobson IM, Gordon SC, Kowdley KV et al. Sofosbuvir for hepatitis C genotype 2 or 3 in patients without treatment options. N Engl J Med 2013; 368(20): 1867–1877. doi: 10.1056/NEJMoa1214854.
15. Zeuzem S, Dusheiko GM, Salupere R et al. Sofosbuvir and ribavirin in HCV genotypes 2 and 3. N Engl J Med 2014; 370(21): 1993–2001. doi: 10.1056/NEJMoa1316145.
16. Esteban R, Nyberg L, Lalezari J et al. Successful retreatment with sofosbuvir-containing regimens for HCV genotype 2 or 3 infected patients who failed prior sofosbuvir plus ribavirin therapy. J Hepatol 2014; 60(1): S4–S5. doi:10.1016/S0168-8278(14)60010-6.
17. Lawitz E, Poordad F, Brainard DM et al. Sofosbuvir in combination with PegIFN and ribavirin for 12 weeks provides high SVR rates in HCV-infected genotype 2 or 3 treatment-experienced patients with and without compensated cirrhosis: results from the LONESTAR-2 study. Hepatology 2013; 58 : 1380A.
18. Lawitz E, Mangia A, Wyles D et al. Sofosbuvir for previously untreated chronic hepatitis C infection. N Engl J Med 2013; 368(20): 1878–1887. doi: 10.1056/NEJMoa1214853.
19. Nelson DR, Cooper JN, Lalezari JP et al. Alloral 12-week treatment with daclatasvir plus sofosbuvir in patients with hepatitis C virus genotype 3 infection: ALLY-3 phase 3 study. Hepatology 2015; 61(4): 1127–1135. doi: 10.1002/hep.27726.
20. Moreno C, Hezode C, Marcellin P et al. Efficacy and safety of simeprevir with PegIFN/ribavirin in naive or experienced patients infected with chronic HCV genotype 4. J Hepatol 2015; 62(5): 1047–1055. doi: 10.1016/j.jhep.2014.12.031.
21. Kapoor R, Kohli A, Sidharthan S et al. All-oral treatment for genotype 4 chronic hepatitis C infection with sofosbuvir and ledipasvir: interim results from the NIAID SYNERGY trial. Hepatology 2014; 60: 321A.
22. Pol S, Reddy KR, Baykal T et al. Interferon-free regimens of ombitasvir and ABT-450/r with or without ribavirin in patients with HCV genotype 4 infection: PEARL-I study results. Hepatology 2014; 60: 1129A.
23. Castera L, Sebastiani G, Le Bail B et al. Prospective comparison of two algorithms combining non-invasive methods for staging liver fibrosis in chronic hepatitis C. J Hepatol 2010; 52(2): 191–198. doi: 10.1016/j.jhep.2009.11.008.
24. Castéra L, Vergniol J, Foucher J et al. Prospective comparison of transient elastography, fibrotest, APRI, and liver biopsy for the assessment of fibrosis in chronic hepatitis C. Gastroenterology 2005; 128(2): 343–350.
25. Lawitz E, Forns X, Zeuzem S et al. Simeprevir (TMC435) with peginterferon//ribavirin for treatment of chronic HCV genotype 1 infection in patients who relapsed after previous interferonbased therapy: results from PROMISE, a Phase III trial. Gastroenterology 2013; 144(5): 151. doi: 10.1016/S0016-5085(13)60542-9.
26. Gane EJ, Stedman CA, Hyland RH et al. Nucleotide polymerase inhibitor sofosbuvir plus ribavirin for hepatitis C. N Engl J Med 2013; 368(1): 34–44. doi: 10.1056/NEJMoa1208953.
27. Sulkowski M, Rodriguez-Torres M, Lalezari J et al. All-Oral therapy with sofosbuvir plus ribavirin for the treatment of HCV genotype 1, 2, and 3 infection in patients co-infected with HIV (PHOTON-1). Hepatology 2013; 58 (Suppl 1): 313A–314A.
28. Fontana RJ, Hughes EA, Bifano M et al. Sofosbuvir and daclatasvir combination therapy in a liver transplant recipient with severe recurrent cholestatic hepatitis C. Am J Transplant 2013; 13(6): 1601–1605. doi: 10.1111/ajt.12209.
29. Zeuzem S, Dusheiko GM, Salupere R et al. Sofosbuvir plus ribavirin for 12 or 24 weeks for patients with HCV genotype 2 or 3: the VALENCE trial. Hepatology 2013; 58 (Suppl 1): 733A.
30. Recommendations for prevention and control of hepatitis C virus (HCV) infection and HCV-related chronic disease. Centers for Disease Control and Prevention. MMWR Recomm Rep 1998; 47(RR-19): 1–39.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2015 Číslo 5- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Odcházení
- Pneumoperitoneum
- Pilotní experimentální studie stenóz jícnu po ESD
- Variabilní endoskopický obraz časného dlaždicobuněčného karcinomu jícnu
- Prvé skúsenosti s digitálnym Spyglass™ DS na Slovensku z gastroenterologického pracoviska FN Trnava
- Endoskopická histologizace diminutivních polypů tračníku. Jsme připraveni na změnu?
- Kvalita biopsií u pacientů s Barrettovým jícnem – jumbo vs. large capacity kleště
- Screeningové kolonoskopie u seniorů starších 70 let
- Nové přístupy u pacientů trpících nespecifickými střevními záněty
- Domáca parenterálna výživa – význam a využitie v klinickej praxi
- Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C
- Ledipasvir/ sofosbuvir – rychlý vývoj poznatků vede ke zkrácení léčby u cirhotických pacientů s chronickou hepatitidou C
- Recenze knihy
- Hands-on trénink pokročilých endoskopických metod – mezinárodní workshop v Aténách
-
XXIX. Hildebrandovy Bardějovské gastroenterologické dny
Střevní záněty v kazuistických obrazech a přehledných přednáškách - Výběr z mezinárodních časopisů
- Správná odpověď na kvíz
- Autodidaktický test: klinická a experimentální gastroenterologie
- SOUTĚŽ O NEJLEPŠÍ KAZUISTIKU 2015
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Endoskopická histologizace diminutivních polypů tračníku. Jsme připraveni na změnu?
- Pneumoperitoneum
- Screeningové kolonoskopie u seniorů starších 70 let
- Domáca parenterálna výživa – význam a využitie v klinickej praxi
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



