-
Medical journals
- Career
Manažment stabilnej anginy pectoris a iných foriem chronickej kardiovaskulárnej artériovej choroby
Authors: P. Gavornik; A. Dukát; Ľ. Gašpar
Authors‘ workplace: II. interná klinika Lekárskej fakulty UK a UN Bratislava, Prvé angiologické pracovisko (PAP), Slovenská republika, prednosta prof. MUDr. Ľudovít Gašpar, CSc.
Published in: Vnitř Lék 2012; 58(7 a 8): 29-36
Category: 80th Birthday MUDr. Miroslav Mydlík, DrSc.
Overview
Úlohou tohto dokumentu Sekcie angiológov Slovenskej lekárskej komory (SA SLK) je zamerať sa na štúdie o stabilnej angine pectoris, publikované v posledných 5 rokoch s cieľom určiť ich príspevok k rozšíreniu našich vedomostí o chronických kardiovaskulárnych artériových chorobách. Prevalencia anginy pectoris je podľa Európskej kardiologickej spoločnosti od 2–5 % (muži 45–54-roční) do 10–20 % (muži 65–74-roční), od 0,1–1 % (ženy 45–54-ročné) do 10–15 % (ženy 65–74-ročné), pričom v poslednej dekáde badať jej posun do vyšších vekových skupín. V dôsledku predlžovania veku občanov v Európe výskyt anginy pectoris globálne narastá. Toto cievne ochorenie ovplyvňuje najmä kvalitu života, morbiditu, predčasnú invalidizáciu a mortalitu. Autori rozoberajú klinicko-etiologicko-anatomicko-patofyziologické problémy u pacientov s anginou pectoris, kam patria nedostatočnosť medikamentovej liečby, perzistencia anginových ťažkostí po revaskularizácii, nemožnosť revaskularizácie u niektorých pacientov, ako aj nedobrá tolerancia medikamentovej liečby u iných pacientov. Sústreďujú sa predovšetkým na liečebné prístupy, ktoré zlepšujú prognózu pacienta (antitrombotická liečba, beta-blokátory, statíny, ACE inhibítory) a prístupy zlepšujúce kvalitu života (kalciové blokátory, nitráty, nikorandil, trimetazidín, ranolazín, ivabradín a i.). Nemožno zabúdať na non-farmakoterapiu. Pri prevencii progresie chronickej kardiovaskulárnej artériovej choroby treba zavčasu diagnostikovať a primerane liečiť pacientov s anginou pectoris. Takýmto osobám zlepšujeme nielen ich prognózu, ale aj kvalitu života.
Kľúčové slová:
stabilná angina pectoris – chronické kardiovaskulárne artériové choroby – orgánovovaskulárne artériové choroby – manažmentÚvod
Stabilná angina pectoris (SAP) je bolestivý dyskomfort v hrudníku (stenokardia), ktorý vzniká pri rovnakej telesnej námahe a/alebo pri psychoemocionálnom strese, je retrosternálnej lokalizácie, zvieravého (tlakového, pálivého a i.) charakteru, často s vyžarovaním do ľavého ramena, po ulnárnej strane predlaktia až do 4. a 5. prstu ľavej ruky (krku, sánky a pod.), krátkeho trvania (do 5 min) a ustupuje v pokoji alebo po užití nitroglycerínu [1]. Je to typický manifestný klinický syndróm (C2) spôsobený ischémiou myokardu pri koronárnej chorobe srdca (ischemickej chorobe srdca; kardiovaskulárnej artériovej chorobe) [2,3]. Stabilná angina pectoris (SAP) je častou chorobou, ktorej prevalencia sa zvyšuje vekom u obidvoch pohlaví, z 0,1–1,0 % u žien vo veku 45–54 rokov na 10–15 % u žien vo veku 65–74 rokov; a z 2,0–5,0 % u mužov vo veku 45–54 rokov na 10–20 % u mužov vo veku 65–74 rokov. Výrazne ovplyvňuje kvalitu života, morbiditu, invalidizáciu a mortalitu populácie [1].
Komplexná klinicko-etiologicko-anatomicko-patofyziologická (CEAP) diagnóza chronickej kardiovaskulárnej artériovej choroby
Klinický obraz aterosklerózy a iných systémových artériových chorôb je mimoriadne mnohotvárny, čo súvisí najmä s funkčnými i štruktúrnymi zmenami samotných artérií a/alebo s funkčnými i štruktúrnymi ischemickými až nekrotickými následkami, ktoré môžu vzniknúť nielen v srdci, ale v takmer každom tkanive a orgáne ľudského organizmu (tab. 1 a 2).
Table 1. Klinicko-etiologicko-anatomicko-patofyziologická (CEAP) klasifikácia chronickej kardiovaskulárnej artériovej ischemickej choroby pri ateroskleróze a iných stenotizujúco-obliterujúcich cievnych chorobách. 
Table 2. Najčastejšie orgánovovaskulárne artériové ischemické choroby. 
Klinický komponent diagnózy (C)
C0 – žiadne príznaky a žiadne objektívne morfologické znaky organickej artériovej cievnej choroby (latentné, nulté štádium vaskulárnej choroby). Môže sa zistiť endotelová dysfunkcia a/alebo je prítomný aspoň jeden rizikový vaskulárny faktor (obr. 1). Každý človek s aterogénnou dyslipoproteinémiou, s diabetes mellitus, s artériovou hypertenziou alebo iným rizikovým faktorom, by mal byť dispenzarizovaný ako vysokorizikový primárnopreventívny srdcovocievny pacient (kardioangiak). Mal by byť aktívne informovaný minimálne o nutnosti nefajčenia, zdravo a menej jesť, viac sa pohybovať a o potrebe eliminácie každého rizikového vaskulárneho faktora [2,3].
Image 1. Dysfunkcia endotelu a zložité vzájomné vzťahy s vaskulárnymi rizikovými faktormi a patologickými mechanizmami v patogenéze cievnych artériových chorôb a orgánovovaskulárnych artériových chorôb. 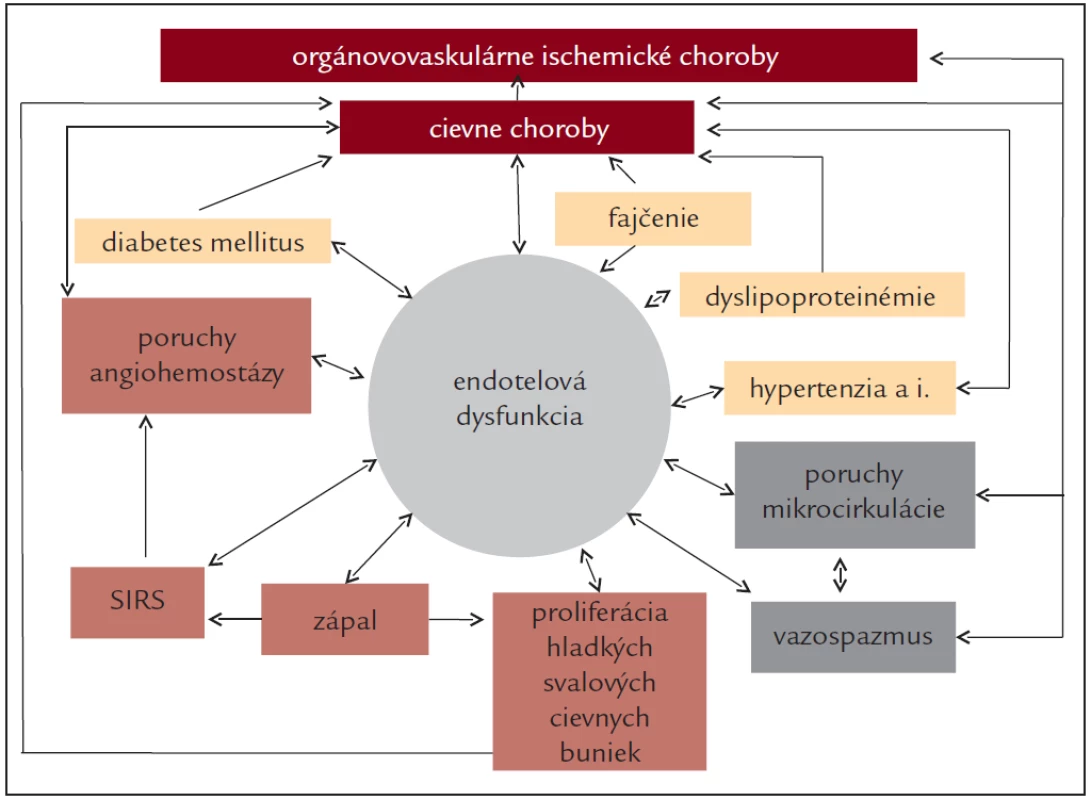
SIRS (systemic inflammatory response syndrome) – syndróm systémovej zápalovej odpovede. C1 – žiadne príznaky (asymptomatické manifestné štádium vaskulárnej choroby), ale objektívne prítomné znaky aterosklerózy alebo inej artériovej choroby (stenotické artériové šelesty, slabšie hmatné pulzácie, vír, pozitívne funkčné záťažové testy a iné znaky artériovej choroby, bez prejavov ischémie). Každý by mal byť dispenzarizovaný ako vysokorizikový sekundárnopreventívny srdcovocievny pacient (kardioangiak) [2,3].
C2 – symptomatické záťažové manifestné štádium (štádium stabilnej orgánovej ischémie), ktoré sa prejavuje námahovými stenokardiami (stabilná angina pectoris) pri srdcovocievnej ischemickej chorobe. Súčasne môže (ale nemusí) mať pacient poruchy novopamäti, závraty pri mozgovocievnej ischemickej chorobe, klaudikačné bolesti v končatinách pri končatinovocievnej ischemickej chorobe, erektilnú dysfunkciu a adekvátne libido pri pohlavnocievnej chorobe atď. [2,3].
C3 – symptomatické pokojové manifestné štádium (štádium instabilnej orgánovej ischémie). Pri srdcovocievnej ischemickej chorobe treba za prejav instability považovať akúkoľvek kvantitatívnu i kvalitatívnu zmenu stenokardie, vrátane jej prvej manifestácie (instabilná angina pectoris). Súčasne môže mať pacient aj bolesť v končatine, ktorá nezávisí od telesnej námahy. Objavuje sa najskôr v ležiacej horizontálnej polohe, najmä v noci a budí chorého zo spánku. Pacient ju pociťuje v prstoch alebo len v jednom prste a v nohe, zmierňuje sa pri posadení, pri zvesení končatín do zvislej polohy z postele, pri postavení alebo niekoľkých pomalých krokoch. Je príznakom ťažkej ischémie nielen svalového tkaniva, ale aj kožného a ďalších tkanív končatiny pri končatinovocievnej ischemickej chorobe. V oblasti mozgu je typický tranzitórny ischemický atak (TIA), fokálny výpad funkcie, trvajúci niekoľko sekúnd, minút až hodín, maximálne 24 hod. Neprítomnosť spontánnej nočnej erekcie pri pohlavnocievnej chorobe atď. [2,3].
C4 – štádium orgánových nekrotických komplikácií, napr. akútny infarkt myokardu, náhla koronárna smrť, mozgová porážka, mŕtvica (infarkt, iktus, apoplexia, stroke), gangréna končatiny atď. [2,3].
Variabilita klinického obrazu je určovaná predovšetkým rôznymi vzájomnými kombináciami artériových cievnych chorôb a rôznymi orgánovovaskulárnymi manifestáciami (tab. 2).
Etiologický komponent (E)
Takmer všetky medzinárodné dokumenty zdôrazňujú, že najčastejšou, ale nie jedinou, cievnou základnou chorobou (morbus principalis) je ateroskleróza (E1), avšak ostatnými chorobami artérií sa už obvykle nezaoberajú [1,4,5,8–10,12,13,15,17–30]. V praxi sa potom stáva, že niektorí lekári považujú aterosklerózu nesprávne za jedinú cievnu artériovú chorobu, ktorá spôsobuje kardiovaskulárne a iné orgánovovaskulárne artériové choroby (cerebrovaskulárne, extremitovaskulárne, renovaskulárne, genitovaskulárne, pulmovaskulárne, gastrointestinovaskulárne, okulovaskulárne, otovaskulárne, stomatovaskulárne a ďalšie) (tab. 2). Okrem aterosklerózy (E1) môže byť kauzálnou artériovou cievnou chorobou SAP a iných orgánovovaskulárnych ischemických chorôb (tab. 3): arterioloskleróza/arteriolonekróza (E2), diabetická makroangiopatia (E3a), diabetická mikroangiopatia (E3b), Mönckebergova medioskleróza/mediokalcinóza (E4), arteritídy – vaskulitídy (E5), kompresívne artériové syndrómy (E6), fibromuskulárna dysplázia artérií (E7), cystická degenerácia adventície artérií (E8), artériová trombóza (E9), artério-vá embólia, vrátane tromboembólie (E10), traumatické a posttraumatické arteriopatie (E11), fyzikálne arteriopatie (E12), chemické a toxické arteriopatie (E13), iatrogénne oklúzie artérií (E14), disekcia artérií (E15), anomálie priebehu artérií (E16), komplikovaná artériová aneuryzma (E17), artériovo-vénová fistula (E18), ojedinelé cievne choroby (E19), napr. amyloidová vaskulopatia, Fabryho choroba a ďalšie [2,3,6,11,14,16].
Table 3. Etiológia chronickej kardiovaskulárnej artériovej choroby (koronárnej choroby srdca; ischemickej choroby srdca; artériovej choroby srdca). 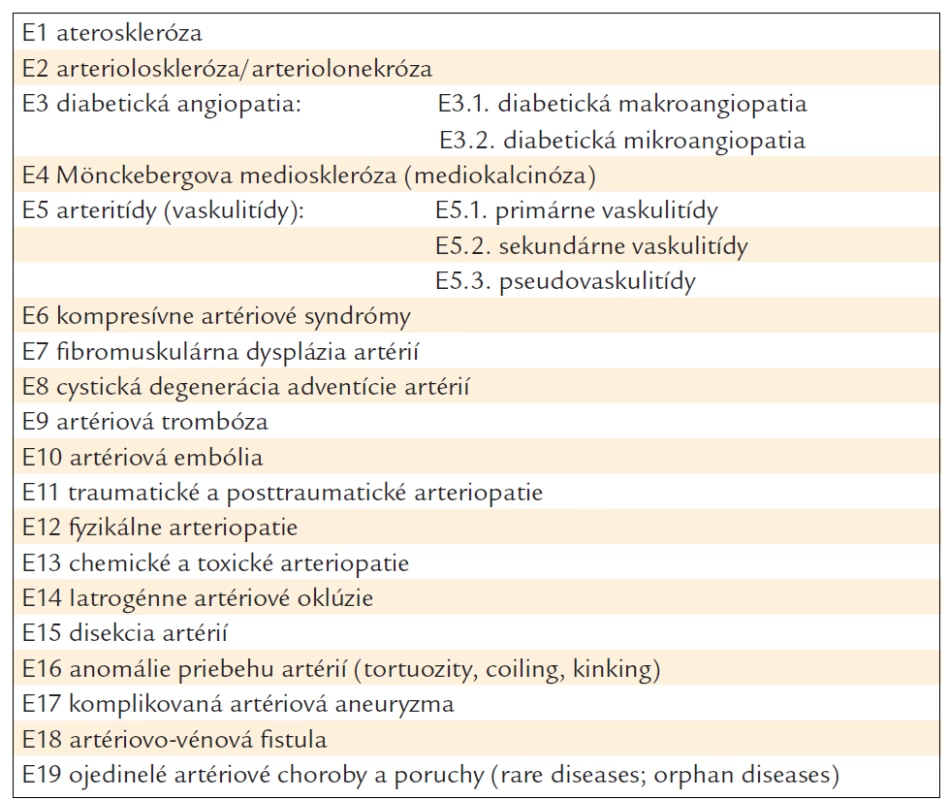
Ateroskleróza (E1), bez iných cievnych chorôb (E2 až E19), je zriedkavo osamotená (monovaskulárna choroba). Častejšie sa vyskytujú 2 a viac cievnych chorôb srdca (polyvaskulárna choroba), napr. ateroskleróza a arterioloskleróza pri artériovej hypertenzii [2,3,6]. Čím viac cievnych chorôb, tým horšia je prognóza. Nesprávna/chybná etiologická diagnóza nemôže mať iné, ako tragické následky.
Anatomický komponent (A)
Z anatomicko-morfologického hľadiska možno rozlišovať minimálne 3 typy SAP: makrovaskulárny (AAM), mikrovaskulárny (AAm) a kombinovaný (AAK). Pri oklúziách proximálnych častí koronárnych artérií – makrovaskulárny proximálny typ (AAMP) je obvykle chronická ischémia myokardu a pri priaznivom kolaterálnom cievnom systéme sa nemusia vyvíjať nekrotické zmeny. Pri oklúziách distálnych častí koronárnych artérií – makrovaskulárny distálny typ (AAMD) sú kompenzačné možnosti obmedzené. Pri mikrovaskulárnom type (AAm) je možnosť vzniku (mikro)nekróz aj bez predchádzajúcej ischémie. Pritom štandardné zobrazovacie inštrumentárne angiologické vyšetrovacie metódy, vrátane intravaskulárnej ultrasonografie (IVU) a artérioskopie môžu byť s negatívnym výsledkom. Prognosticky najhorší je kombinovaný typ (AAKMm). Pri radikálnej liečbe sa uvedie lokalizácia a spôsob (metóda), dátum. Okrem anatomickej klasifikácie artériovej choroby (AA) by sa malo čo najpresnejšie určiť štruktúrne a/alebo funkčné poškodenie srdca (AO). Kardiovaskulárna choroba je len zriedkavo osamotená (monoorgánovovaskulárna), častejšie sú postihnuté 2 orgány alebo viac orgánov (multiorgánovovaskulárna, polyorgánovaskulárna choroba). Čím viac orgánovovaskulárnych chorôb, tým horšia je prognóza [2,3,6,11,14,16].
Patofyziologický komponent (P)
Nemalo by sa zabúdať na určenie patofyziologického štádia vaskulárneho poškodenia (P1 – dysfunkcia endotelu, P2 – stabilné štruktúrne vaskulárne poškodenie, P3 – instabilné vaskulárne poškodenie) [30] a vaskulárnych rizikových faktorov [1,16]. Vždy by sa mali uviesť aj funkčné následky orgánového angiogénneho poškodenia a zlyhávania. K hodnoteniu závažnosti SAP sa používa funkčná klasifikácia podľa Kanadskej kardiovaskulárnej spoločnosti (Canadian Cardiovascular Society – CCS), ktorá je na rozdiel od klasifikácie New York Heart Association (NYHA) lepšie reprodukovateľná [1] (tab. 4).
Table 4. Funkčná klasifikácia anginy pectoris podľa Kanadskej kardiovaskulárnej spoločnosti (CCS). 
Klinické formy chronickej kardiovaskulárnej artériovej choroby
Klinická mnohotvárnosť je navyše umocnená aj rôznym klinickým priebehom akútnych a chronických foriem a rôznou časovou postupnosťou vývinu choroby, vrátane toho, že letálna komplikácia môže byť prvou manifestáciou artériovej cievnej choroby (tab. 5). Väčšina stenotizujúco-obliterujúcich artériových chorôb patrí medzi systémové, generalizované cievne choroby, takže izolovaná monoorgánová kardiovaskulárna artériová choroba je v skutočnosti zriedkavejšia ako multiorgánovovaskulárne choroby. Napríklad pre angiometabolický syndróm X je typické vaskulárne poškodenie artérií a tkanív 2 a viacerých orgánov (multiorgánovovaskulárne artériové choroby), čo niektorí autori nesprávne pomenovali ako „polyvaskulárna choroba (polyvascular disease)“. Typické je viacetážové vaskulárne postihnutie 2 i viacerými artériovými chorobnými jednotkami (multivaskulárne, polyvaskulárne artériové choroby). Pre angiometabolický syndróm X sú teda charakteristické multiorgánovo-multivaskulárne artériové choroby. Nie je potom prekvapením, že aj ischemické a nekrotické následky príslušných tkanív a orgánov sú závažnejšie a spojené s vyššou vaskulárnou morbiditou a mortalitou [2,3,6,11,14,16].
Table 5. Klinické formy kardiovaskulárnej artériovej choroby (koronárnej choroby srdca, ischemickej choroby srdca). 
Typická stabilná angina pectoris (SAP)
SAP má všetky prejavy typické v časovom období dlhšom než 4 týždne, vzniká počas rovnakej fyzickej námahy, najčastejšie pri chôdzi (angina pectoris ambulatoria, effort angina pectoris, námahová angina pectoris). Podľa provokujúceho faktora sa rozoznávajú aj ďalšie typy SAP. Angina pectoris decubitus (angine des décubitus, SAP ležiacich) sa prejavuje stenokardiou večer po uložení do postele. Na jej vzniku sa podieľa jednak zvýšený vénový návrat v horizontálnej polohe (preload), a jednak kontakt s chladnou posteľou (zvýšená vazokonstrikcia periférie, afterload). Angina pectoris postprandialis – bolesť na hrudníku vzniká po výdatnom jedle, keď nastáva distribúcia krvi do oblasti tráviacich orgánov a myokard je nedokrvený. Angina pectoris psychoemotionalis – stenokardia vzniká pri psychoemocionálnom strese atď. V niektorých prípadoch nemá bolesť charakteristické črty a je atypická (atypická SAP), čo ešte viac komplikuje diferenciálnu diagnostiku bolesti na hrudníku. Na EKG sú typické horizontálne alebo descendentné depresie segmentu ST ≥ 1 mm (0,1 mV) [1]. Efektívnou liečbou sa môže zmeniť na asymptomatickú formu (C1), alebo naopak, pri poruche integrity vaskulárneho poškodenia sa môže zhoršiť na instabilnú anginu pectoris (C3) až infarkt myokardu (C4) alebo náhlu smrť (mors subita) [2,3–5].
Variantná angina pectoris
Variantná angina pectoris, primárna vazospastická angina pectoris, angina pectoris inversa, Prinzmetalov variant anginy pectoris, Prinzmetalova angina pectoris sa prejavuje stenokardiami v pokoji, zatiaľ čo telesná námaha bolesti nevyvoláva. Počas záchvatu sa na EKG zjavuje vysoká elevácia ST segmentu. Mimo záchvatu nie sú na EKG žiadne patologické odchýlky. V patogenéze sa uplatňuje spazmus koronárnych artérií v ohraničenom hyperaktívnom segmente. Ukázalo sa, že v mieste dlhotrvajúceho spazmu môže dochádzať k poruche integrity endotelu a k artériovej trombóze, čo môže spôsobiť infarkt myokardu a malígne dysrytmie. Preto daktorí autori zaraďujú Prinzmetalovu anginu pectoris k nestabilnej angine pectoris (NAP). Časť chorých trpí súčasne aj námahovou SAP („variant variantu“). Pri priaznivom priebehu variantná angina pectoris spontánne ustupuje a epizodicky sa znovu objavuje [1–4].
Koronárny syndróm X („angina pectoris s normálnym koronarogramom“)
Koronárny syndróm X je heterogénny syndróm s viacerými podjednotkami s rôznou etiológiou [1]. Klinické prejavy sú prakticky rovnaké ako u typickej námahovej SAP, ale koronarografický nález je negatívny. Zisťuje sa znížená koronárna rezerva, väčšinou s ischémiou. Príčinou je buď funkčná porucha (dysfunkcia endotelu) s nedostatočnou vazodilatáciou koronárnych arteriol pri záťaži či s vazokonstrikciou arteriol (arteriolospazmom), alebo organické choroby malých ciev (small vessell disease, mikrovaskulárna angina pectoris – AAm), najmä arterioloskleróza (E2), diabetická mikroangiopatia (E3.1), mikrovaskulitídy (E5), mikrovaskulárna trombóza (E9), mikrovaskulárna tromboembólia (E10) a i. [1–3]. Prognóza závisí od etiológie. Koronárny syndróm X treba odlišovať od angiometabolického syndrómu X, ktorý však môže byť v kauzálnom vzťahu [2,3,6,11,14,16].
Nebolestivá asymptomatická (silent) ischémia („angina pectoris bez anginy“)
Asymptomatická (tichá, nemá, skrytá, „silent“) forma chronickej kardiovaskulárnej artériovej choroby sa definuje objektívne dokázateľnými epizódami ischémie myokardu, bez stenokardií a bez iných klinických prejavov. Je to heterogénny syndróm, v ktorom je niekoľko skupín chorých s tichou ischémiou:
- Úplná asymptomatická forma, pri ktorej majú pacienti objektívne dokázanú ischémiu myokardu, ale ani pri cielenej anamnéze nemajú žiadne príznaky. Napriek tomu, že nezhoršuje kvalitu života, má zlú prognózu.
- Parciálna (kombinovaná) asymptomatická forma. Do tejto skupiny patria pacienti, ktorí majú okrem tichej ischémie aj iné formy kardiovaskulárnej artériovej choroby. Najčastejšie sú tieto kombinácie:
- tichá ischémia a stabilná angina pectoris, najrizikovejšia je „choroba troch koronárnych artérií“;
- tichá ischémia u pacientov po infarkte myokardu;
- tichá ischémia u pacientov po revaskularizácii myokardu;
- tichá ischémia u pacientov po úspešnej kardiopulmonálnej resuscitácii.
Tichá ischémia vo všetkých prípadoch zhoršuje prognózu a nesmie sa podceňovať. Príčiny tichej ischémie sú tie isté ako u klinicky manifestnej ischémie (tab. 3). Nebolestivosť je podmienená vysokým prahom pre bolesť, napr. pri zvýšených hladinách β-endorfínov, pri diabetickej neuropatii a iných neuropatiách, pri cerebrovaskulárnych chorobách a i. K diagnóze tichej ischémie sú potrebné pozitívne výsledky viacerých neinvazívnych vyšetrení: záťažový EKG test, Holterovo longitudinálne monitorovanie EKG. Za jednu epizódu ischémie sa považuje depresia segmentu ST najmenej o 1 mm (0,1 mV), trvajúca najmenej 1 min, oddelená od ďalšej epizódy najmenej 1 min (pravidlo 3 × 1).Určuje sa aj celková ischemická záťaž (total ischemic burden), čo je súčet trvania všetkých manifestných aj asymptomatických ischémií počas 24 hod, záťažová echokardiografia s dôkazom porúch kinetiky, záťažová perfúzna táliová scintigrafia myokardu. Základným vyšetrením je anamnéza a fyzikálne vyšetrenie [1–3].
Nebolestivá symptomatická forma s ischemickou dysfunkciou ľavej komory
Nebolestivá symptomatická forma s dysfunkciou ľavej komory má niekoľko stupňov – od reverzibilnej tranzitórnej poruchy kontraktility pri ischémii myokardu, potom trvalú asymptomatickú dysfunkciu, až po príznaky a znaky chronického srdcového zlyhávania. Remodelácia srdca je nepriaznivým prognostickým znakom [1–3,12].
Nebolestivá dysrytmická forma
Nebolestivá dysrytmická forma sa prejavuje príznakmi a znakmi porúch srdcového rytmu. Treba zdôrazniť, že ischémia myokardu je v súčasnosti najčastejšou príčinou dysrytmií. Vzniknúť môžu prakticky všetky druhy dysrytmií, ale klinicky najčastejšia je fibrilácia predsiení. Tromboembolické komplikácie, najmä v cerebrovaskulárnej oblasti, sú vlastne bludným cievnym kruhom (circulus vitiosus vasorum) [1,2,11]. V klinickej praxi by sme pri každej dysrytmii mali myslieť na systémové stenotizujúco-obliterujúce cievne choroby.
Stavy po infarkte myokardu
Chronická kardiovaskulárna artériová choroba po infarkte myokardu vyžaduje dispenzarizáciu. Prognóza závisí predovšetkým od úspešnosti eliminácie všetkých rizikových vaskulárnych faktorov, od vývoja základnej artériovej choroby a závažnosti ischémie myokardu, od funkcií ľavej komory [1,2,5,25]. Prognózu zhoršujú multiorgánovo-multivaskulárne artériové choroby (tab. 2 a 3).
Je dobre známe, že včasná a presná diagnóza i stratifikácia globálneho rizika orgánovocievnych artériových chorôb, vrátane SAP, je možná iba vtedy, keď poznáme všetky nozologické jednotky, druhy a typy cievnych chorôb a keď vôbec na ne myslíme! Každá diagnóza musí byť komplexná – má 4 komponenty (klinický, etiologický, anatomický a patofyziologický, vrátane rizikových faktorov). Treba zdôrazniť, že komplexná „CEAP“ diagnóza vychádza z nevyhnutnosti vždy urobiť anamnestické a základné i funkčné fyzikálne interné vyšetrenie, vrátane vyšetrenia srdca a ciev u každého pacienta. Každý lekár, ktorý sa zaoberá klinickou problematikou ciev, by mal ovládať nielen echovaskulografiu (ECHOVG) a pletyzmografiu (PG), ale aj funduskopiu (FS), pomocou ktorej možno najjednoduchšie neinvazívne vyšetriť simultánne prakticky všetky hlavné druhy ciev (artérie, arterioly, kapiláry, venuly, vény) a ich choroby [2,3,6,14,16].
Každý chorý človek je postihnutý, vrátane každého cievneho pacienta (angiaka, kardioangiaka), ale pacienti s ojedinelými cievnymi chorobami (rare vascular diseases, orphan diseases – E19) sú postihnutí viacnásobne. Popri závažnej chorobe, ktorou trpia, ich postihujú aj mnohé ďalšie problémy súvisiace s jej oneskorenou diagnostikou, nedostatočnými vedomosťami o podstate chorobného procesu a nedostatočnou pripravenosťou na jej riešenie v bežnej klinickej praxi. Postihuje ich aj nedostupnosť špecializovanej zdravotnej starostlivosti a často chýba aj špecifická účinná liečba – čiastočne pre nízku motiváciu farmakopriemyslu na prípravu špecifických liekov pre choroby, ktoré vzhľadom na malý počet pacientov neprinášajú adekvátny zisk [2,3,6,11,16].
Diferenciálna diagnóza vaskulárnej hypoxie (ischémie) a nonvaskulárnej hypoxie
Diferenciálnodiagnosticky treba presne stanoviť správnu komplexnú klinicko-etiologicko-anatomicko-patofyziologickú (CEAP) diagnózu angiogénnej (vaskulárnej, artériovej, lokálnej, regionálnej, ischemickej) hypoxie, ktorú treba odlíšiť od nonangiogénnej (nonvaskulárnej, globálnej, nonischemickej) hypoxie. Táto sa rozdeľuje prinajmenšom na 5 podskupín: cirkulačná (hypoperfúzna, normoperfúzna až hyperperfúzna), hypoxemická, anemická, metabolická a histotoxická. Je samozrejmé, že všetky chorobné stavy s neischemickou hypoxiou zhoršujú výslednú hypoxiu tkanív, ale ich pomenovanie za „ischémiu“ je chybné a zavádzajúce [2,14]. Antiischemická liečba necievnej hypoxie nemôže byť efektívna. Jedinou racionálnou možnosťou je kauzálna liečba základného ochorenia.
Prevencia a liečba
Keďže etiopatogenéza artériových cievnych chorôb je multifaktoriálna a mimoriadne zložitá, aj prevencia a liečba týchto chorôb musí byť mimoriadne komplexná. Cieľom prevencie cievnych chorôb je nielen predĺženie života (zníženie mortality) a zníženie morbidity, ale aj zlepšenie kvality života. V ostatných medzinárodných odporúčaniach a podľa VAS (Vascular Independent Research and Education European Organization) sa rozlišujú 3 navzájom sa doplňujúce preventívne stratégie: populačná, vysokoriziková a sekundárna [1,2,23,24].
Populačná globálna stratégia primárnej prevencie
Populačná globálna stratégia má viesť k zmene životného štýlu a k zmene tých sociálnych a ekonomických determinantov životného prostredia, ktoré sú v príčinnej súvislosti s pandemickým výskytom cievnych chorôb (angiopandémia 3. milénia). Populačná stratégia má v primárnej prevencii rozhodujúci význam. Nefajčiť!; Menej a zdravo jesť!; Viac sa pohybovať! – sú 3 základné nonfarmakoprofylaktické vaskuloprotektívne piliere (imperatívy) zdravého životného štýlu a prevencie nielen orgánovocievnych artériových ischemických chorôb, ale všetkých cievnych chorôb. Je potrebné zmeniť myslenie a konanie nielen zdravotníkov, ale celej spoločnosti, vrátane všetkých štátnych a medzinárodných inštitúcií. Úspech primárnych preventívnych opatrení spočíva iba asi v 20 % v rezorte zdravotníctva, ale až asi v 80 % v racionálnych aktivitách nezdravotníckych zložiek spoločnosti [1,2,16,23–25].
Vysokoriziková individuálna stratégia primárnej prevencie
Vysokoriziková individuálna stratégia je preventívna starostlivosť zameraná na osoby, ktoré majú genetickú predispozíciu k cievnym chorobám a/alebo majú vaskulárne rizikové faktory (dyslipoproteinémie, artériová hypertenzia, fajčenie, metabolický syndróm, diabetes mellitus atď.), ktorá má viesť k ich eliminácii. Značnú časť rizikových faktorov nevieme adekvátne eliminovať, či aspoň redukovať nefarmakoprofylakticky, preto musíme použiť už v primárnej prevencii aj farmakoprofylaktické metódy. Ak má byť preventívna vaskulárna medicína (angioprevencia) efektívna, nemôže začínať až v dospelosti, ale musí začať pri narodení, resp. už v prenatálnom období. Ďalším imperatívom je zlepšiť spoluprácu angiológov a kardiológov s pediatrami, s inými špecialistami aj so širokou verejnosťou [2,16,23–25].
Sekundárna prevencia (liečba stabilnej anginy pectoris)
Etiopatogenetická (kauzálna) liečba
Sekundárna prevencia (liečba) by mala byť zásadne etiopatogenetická (kauzálna) s hlavným cieľom: zastaviť progresiu, či dosiahnuť regresiu základnej artériovej cievnej choroby a zlepšiť prognózu SAP. Pokroky v neinvazívnej, „konzervatívnej“ lekárskej starostlivosti, ktoré sa označujú ako optimálne lekárske ošetrovanie (OLO), sú veľmi nádejné [1,2,6,16–20]. Zásada eliminácie vaskulárnych rizikových faktorov je podobná ako v primárnej prevencii, musí však mať oveľa vyššiu mieru individualizácie. Vo farmakoterapii všetkých rizikových vaskulárnych faktorov uprednostňujeme tie liekové skupiny, ktoré majú dokázané aj endotelovoprotektívne a orgánovoprotektívne účinky. Antilipidogénna (antidyslipidemická) [8,9,15,16], antitrombotická (artériotromboprofylaktická) [7,16,25], a vazoaktívna terapia (ACEI) [1,16] – sú 3 základné farmakoprofylaktické angioprotektívne metódy všetkých orgánovovaskulárnych artériových chorôb. K tomu často v klinickej praxi pribúda problém redukcie reziduálneho rizika (3R), ktorý si bude vyžadovať aj nové liečebné prístupy [2,16]. Základné metódy OLO sme z didaktických dôvodov pomenovali „terapeutická zásada 3 × 3“. Liečebné postupy v určitých klinických situáciách (detský vek, staroba, diabetes mellitus [10], srdcové zlyhávanie [12], fibrilácia predsiení [11], SAP žien, gravidita [13], erektilná dysfunkcia [15,16,26] atď.) si vyžadujú niektoré špecifické liečebné postupy.
Symptomatická liečba
Symptomatickú liečbu ischémie myokardu možno uskutočniť 2 hlavnými spôsobmi. Prvým je antianginová, antiischemická farmakoterapia, pri ktorej sa používajú lieky zvyšujúce prietok krvi v ischemickej oblasti a/alebo lieky znižujúce požiadavky myokardu na kyslík. Používajú sa krátkotrvajúco účinkujúce nitráty, dlhotrvajúco pôsobiace nitráty, beta-blokátory, blokátory kalciových kanálov, inhibítory enzýmu konvertujúceho angiotenzín (ACEI), trimetazidín, ranolazín, nikorandil, modulátory angiogenézy a ďalšie [1–20]. Ivabradín (inhibítor pacemakerového If prúdu), ktorý optimálne znižuje frekvenciu srdca, má nové dôkazy o zlepšení kvality života, zníženia mortality a remodelácii i funkcie myokardu aj pri zlyhávaní srdca [27–29].
Druhým hlavným spôsobom je radikálna liečba – revaskularizácia myokardu, ktorá sa robí 2 postupmi: chirurgickou revaskularizáciou (CABS) a perkutánnou koronárnou intervenciou (PKI). Významným posunom v indikáciách v porovnaní s predchádzajúcimi odporúčaniami pre perkutánnu koronárnu intervenciu je používanie stentov uvoľňujúcich lieky (SUL, DES). Realitou už sú aj biodegradabilné stenty. Autori ostatných odporúčaní oživili pojmy „heart team” a „vascular team“ . Indikácia k revaskularizácii a výber najvhodnejšieho terapeutického postupu by nemali byť výsadou jednotlivca. Je výsledkom vzájomnej diskusie referujúceho (ošetrujúceho) kardiológa/angiológa, kardiochirurga/angiochirurga a intervenčného vaskulárného radiologa a podľa nášho názoru aj internistu, anesteziológa a podľa potreby príslušných ďalších orgánových špecialistov. Na jej konci by malo byť odporúčanie pre pacienta. Pacient ho môže, ale nemusí akceptovať. A tu je ďalší významný odkaz. Veľký dôraz sa kladie na práva pacienta, jeho poučenie o výhodách, ale aj možných komplikáciách každého postupu. Pacient má významnou mierou participovať na rozhodovaní. Len dobre poučený pacient sa môže správne rozhodnúť [21,22,25,26].
Záver
Doterajšie medzinárodné i národné odporúčania manažmentu stabilnej anginy pectoris a iných foriem chronickej kardiovaskulárnej artériovej choroby, ako aj ďalších orgánovovaskulárnych artériových ischemických chorôb, vychádzali iba z klinickej diagnózy a klasifikácie. Základným predpokladom kauzálnej racionálnej prevencie a liečby je rýchla a správna komplexná klinická (C0–C4), etiologická (E1–E19), anatomická (AM, Am, AkMm) a patofyziologická (P1–P3) diagnóza. Interná medicína je dobrým príkladom i dôkazom toho, že efektívny manažment cievnych chorôb, ktoré sa vyznačujú orgánovou a/alebo vaskulárnou polymorbiditou, sa nezaobíde bez jej významných generalizačných, integračných a koordinačných funkcií. V klinickej praxi nesmie byť stredobodom liečby len určitý systém, orgán či tkanivo, ale celý človek. Pacient so stabilnou anginou pectoris je nositeľom vysokého globálneho multiorgánového a multivaskulárneho rizika a opačne. Prognosticky sú najvážnejšie multiorgánovo-multivaskulárne choroby. Nelieči sa klinický nález, ani sa nelieči akýkoľvek prístrojový či laboratórny výsledok alebo diagnóza, ale človek – pacient.
doc. MUDr. Peter Gavorník, CSc., PhD., mim. prof.
www.fmed.uniba.sk
e-mail: peter.gavornik@sm.unb.sk
Doručeno do redakce: 28. 1. 2012
Sources
1. Fox K, Garcia MAA, Ardissino D et al. Guidelines on the management on stable angina pectoris: executive summary: The Task Force on the Management of Stable Angina Pectoris of the European Society of Cardiology. Eur Heart J 2006; 27 : 1341–1381.
2. Gavorník P. Manažment stabilnej anginy pectoris. Medikom/Medinews 2011; 1 : 12–14.
3. Gavorník P. Obliterujúce choroby artérií a končatinovocievna ischemická choroba. Nová klinicko-etiologicko-anatomicko-patofyziologická (CEAP) klasifikácia. Cardiology 2010; 19 : 201–213.
4. Hamm CW, Bassand JP, Agewall S et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. The Task Force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2011; 32(23): 2999–3054.
5. Van de Werf F, Bax J, Betriu A et al. Management of acute myocardial infarction in patients presenting with persistent ST-segment elevation: The Task Force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology. Eur Heart J 2008; 29 : 2909–2945.
6. Gavorník P. Nevyhnutnosť neustáleho prehodnocovania manažmentu artériovej hypertenzie ako cievnej choroby cievnych chorôb. Medikom/Medinews 2011; 1 : 12–13.
7. Gavorník P. Artériotromboprofylaxia v klinickej praxi. Cardiology 2010; 19 : 293–299.
8. Reiner Ž, Catapano AL, De Backer G et al. ESC/EAS Guidelines for the management of dyslipidaemias: The Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and the European Atherosclerosis Society (EAS). Eur Heart J 2011; 32 : 1769–1818.
9. Chapman MJ, Ginsberg NH, Amarenco P et al. Triglyceride-rich lipoproteins and high-density lipoprotein cholesterol in patients at high risk of cardiovascular disease: evidence and guidance for management. Eur Heart J 2011; 32 : 1345–1361.
10. Rydén L, Standl E, Bartnik M et al. Guidelines on diabetes, pre-diabetes, and cardiovascular diseases: executive summary: The Task Force on Diabetes and Cardiovascular Diseases of the European Society of Cardiology (ESC) and of the European Association for the Study of Diabetes (EASD). Eur Heart J 2007; 28 : 88–136.
11. Gavorník P. Aktuálne odporúčania pre manažment fibrilácie predsiení a jej systémových artériových tromboembolických komplikácií. Medikom/Medinews 2011; 1 : 12–14.
12. Diskstein K, Cohen-Solal A, Filippatos G et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2008: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM). Eur Heart J 2008; 29 : 2388–2442.
13. Regitz-Zagrosek V, Lundquist CB, Borghi C et al. ESC Guidelines on the management of cardiovascular diseases during pregnancy: The Task Force on the Management of Cardiovascular Diseases during Pregnancy of the European Society of Cardiology (ESC). Eur Heart 2011; 32(24): 3149–3197.
14. Gavorník P. Etiopatogenéza neurovaskulárnych ischemických chorôb (syndrómov). Neurológia 2010; 5 : 61–68.
15. Tendera M, Aboyans V, Bartelink ML et al. ESC Guidelines on the diagnosis and treatment of peripheral artery diseases: Document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity arteries. The Task Force on the Diagnosis and Treatment of Peripheral Artery Diseases of the European Society of Cardiology (ESC). Eur Heart J 2011; 32(22): 2851–2906.
16. Gavorník P. Končatinovocievne ischemické choroby. B 2.1 : 1–92. In: Gavorník P, Hrubiško M, Rozborilová E (eds). Diferenciálna diagnostika kardio-vaskulárnych, respiračných a hematologických ochorení. I. Bratislava: Dr. Josef Raabe 2010.
17. Kotík L. Snížení morbidity a mortality nemocných s chronickými formami ischemické choroby srdeční je výsledkem konzervativní léčby. Vnitř Lék 2011; 57 : 497–501.
18. Cífková R. Co způsobuje pokles úmrtnosti na ischemickou chorobu srdeční? – editorial. Vnitř Lék 2011; 57 : 435–436.
19. Groch L. Co způsobuje pokles úmrtnosti na ischemickou chorobu srdeční? – editorial. Vnitř Lék 2011; 57 : 437–438.
20. Špinar J, Vítovec J, Špinarová L. FARIM – FARmakoterapie po Infarktu Myokardu. Vnitř Lék 2011; 57 : 778–784.
21. Wijns W, Kolh Ph, Danchin N et al. Guidelines on myocardial revascularization: The Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2010; 31 : 2501–2555.
22. Mack MJ, Feldman TE, Kappetein AP et al. Comparison of coronary bypass surgery with drug-eluting stenting for the treatment of left main and/or three-vessel disease: 3-year follow-up of the SYNTAX trial. Eur Heart J 2011; 32 : 2125–2134.
23. Graham I, Atar D, Borch-Johnsen K et al. European guidelines on cardiovascular disease prevention in clinical practice: executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and by invited experts). Eur Heart J 2007; 28 : 2375–2414.
24. Banegas JR, López-Garcia E, Dallongeville J et al. Achievement of treatment goals for primary prevention of cardiovascular disease in clinical practice across Europe: the EURIKA study. Eur Heart J 2011; 32 : 2143–2152.
25. Smith jr. SC, Benjamin EJ, Bonow RO et al. AHA/ACCF Secondary Prevention and Risk Reduction Therapy for Patients With Coronary and Other Atherosclerotic Vascular Disease: 2011 Update. A Guideline From the American Heart Association and American College of Cardiology Foundation. J Am Coll Cardiol 2011; 58(23): 2432–2446.
26. Rooke TW, Hirsch AT, Misra S et al. 2011 ACCF/AHA Focused Update of the Guideline for the Management of Patients With Peripheral Artery Disease (Updating the 2005 Guideline). A Report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2011; 58 : 2020–2045.
27. Swedberg K, Komajda M, Böhm M et al. Rationale and design of a randomized, double-blind, placebo-controled outcome trial of ivabradine in chronic heart failure: the Systolic Heart Failure Treatment with the If Inhibitor Ivabradine Trial (SHIFT). Eur J Heart Fail 2010; 12 : 75–81.
28. Ekman I, Chassany O, Komajda M et al. Heart rate reduction with ivabradine and health related quality of life in patients with chronic heart failure: results from the SHIFT study. Eur Heart J 2011; 32 : 2395–2404.
29. Tardif JC, ÓMeara E, Komajda M et al. Effects of selective heart rate reduction with ivabradine on the left ventricular remodeling and function: results from the SHIFT echocardiographic substudy. Eur Heart J 2011; 32 : 2507–2515.
30. Ip JH, Fuster V, Badimon L et al. Syndromes of accelerated atherosclerosis: Role of vascular injury and smooth muscle cell proliferation. J Amer Coll Cardiol 1990; 15 : 1667–1687.
Labels
Diabetology Endocrinology Internal medicine
Article was published inInternal Medicine

2012 Issue 7 a 8-
All articles in this issue
- Syndróm nepokojných nôh u dialyzovaných pacientov
- Antagonisty aldosterónu v liečbe chronického srdcového zlyhávania
- Manažment stabilnej anginy pectoris a iných foriem chronickej kardiovaskulárnej artériovej choroby
- Antiaterogénny účinok HDL subpopulácií u jedincov s novodiagnostikovanou končatinovocievnou artériovou chorobou
- Koncentrace sodíku v dialyzačním roztoku – důležitý, ale opomíjený parametr hemodialýzy u nemocných s chronickým selháním ledvin
- Oxidačný stres a antioxidačné systémy u hemodialyzovaných chorých
- Farmakogenetické aspekty liečby orálnymi antidiabetikami
- Refeeding syndrom u mladého pacienta s anxiózně-depresivní poruchou
- Detekce KRAS a jeho mutace v biopsii pokročilého kolorektálního karcinomu při koloskopii
- Tuhosť aorty zvyšuje centrálny aortový tlak u pacientov s hypertenziou
- Jak definovat osoby s vysokým rizikem pankreatického karcinomu
- Veľkosť LDL lipoproteínových partikúl u pacientov s náhlou mozgovocievnou príhodou
- Chronický zánět a metabolický syndrom
- Profylaxe a léčba antifosfolipidového syndromu – současné možnosti, úskalí a perspektivy do budoucna
- Pokrok v oblasti mnohočetného myelomu a vývoj souvisejícího laboratorního zázemí
- Jak v ambulantní péči neprošvihnout rozvíjející se kritické poruchy hemostázy
- Frekvence nových trombofilních mutací antitrombinu (SERPINC1) (IVS +141G>A), glykoproteinu GPVI (Ser219Pro) a cytochromu CYP4V2 (Lys259Gln) u zdravých osob středního věku v oblasti středních Čech
- Megakaryopoéza a geneze destiček
- Současné možnosti diagnostiky a léčby myelomové kostní nemoci v klinické praxi
- Změny kalcium-fosfátového metabolizmu při chronických nefropatiích
- Konečné stadium chronického onemocnění ledvin a metabolická acidóza
- Chronické ochorenie obličiek a vápniková homeostáza bunky
- Solit nebo nesolit při ledvinových chorobách? Ne více než quantum satis!
- Infarkt myokardu v mladom veku – naše výsledky a skúsenosti
- Vzťah mikroalbuminúrie a obezity u zdravých mladistvých – predbežné výsledky štúdie „Rešpekt pre zdravie“
- Kontrastová nefropatie a možnosti její prevence
- Terapeutický přístup ke krvácení v souvislosti se „starými“ a „novými“ antikoagulans
- Možnosti diagnostiky heparinem indukované trombocytopenie v České republice
- Získaná hemofilie A
- Vysokodávková léčba a přípravné režimy před transplantací krvetvorných buněk
- Trojkombinační léčba chronické hepatitidy C
- Požadavky na předoperační vyšetření z pohledu anesteziologa
- Fixní kombinace v léčbě hypertenze
- Farmakoterapie hypertenze po transplantaci srdce
- Snížení srdeční frekvence u srdečního selhání: změny funkce levé komory a kvalita života v podstudiích SHIFT
- Ischemické a neischemické příčiny elevace ST segmentu u pacientů s bolestí na hrudi: Systematický přehled literatury
- Internal Medicine
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Infarkt myokardu v mladom veku – naše výsledky a skúsenosti
- Požadavky na předoperační vyšetření z pohledu anesteziologa
- Megakaryopoéza a geneze destiček
- Ischemické a neischemické příčiny elevace ST segmentu u pacientů s bolestí na hrudi: Systematický přehled literatury
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

