-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Volná místa
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaLaparoskopická cévní chirurgie
Autoři: L. Dvořáček; P. Štádler; P. Vitásek; P. Matouš; D. Pilous
Působiště autorů: Oddělení cévní chirurgie, Nemocnice Na Homolce, Praha, primář: Doc. MUDr. P. Štádler, Ph. D.
Vyšlo v časopise: Rozhl. Chir., 2012, roč. 91, č. 7, s. 406-409.
Kategorie: Postgraduální vzdělávání
Úvod
První laparoskopie provedená v roce 1901 na zvířeti znamenala začátek postupného rozvoje laparoskopické chirurgie, která se později nejprve uplatnila v gynekologii a všeobecné chirurgii. A až v r. 1993 byl pak Dionem laparoskopicky proveden aortobifemorální bypass [1]. V České republice jako první provedl laparoskopicky asistovaný ilikofemorální bypass Dostalík v r. 1997 [2].
V r. 1999 byl Dionem poprvé plně laparoskopicky operován pacient s výdutí břišní aorty (AAA) [3]. V České republice tuto operaci poprvé provedl Štádler [4] v roce 2005.
V současnosti jsou laparoskopické cévní operace prováděny ve specializovaných centrech po celém světě. Indikace k laparoskopické chirurgii se rozšiřují a kontraindikace snižují. Dokonce bylo operováno i torakoabdominální aneuryzma (TAAA) typu IV a juxtarenální aneuryzma [5–6].
Napříč všemi chirurgickými obory byly dokázané výhody laparoskopie oproti otevřené chirurgii – snížení mortality, zkrácení doby hospitalizace, zmenšení pooperačních bolestí, dřívější návrat k běžnému příjmu potravy, běžné činnosti a do ambulantní péče, snížení četnosti kýl v jizvě a konečně lepší kosmetický efekt.
Metodika
Laparoskopické cévní operace patří svými nároky na preciznost a detail provedení mezi nejobtížnější laparoskopické výkony. Technicky je možné provést operaci rukou asistovaně, laparoskopicky asistovaně nebo plně laparoskopicky.
1. Rukou asistovaná technika (hand assisted)
Rukou asistovaná laparoskopie spočívá v použití tzv. „handportu“. Přitom může nedominantní ruka chirurga v operačním poli pomoci najít optimální místo pro umístění cévních svorek nebo místo pro bezpečné našití cévní anastomózy a zjednodušit laparoskopické šití takové anastomózy.
2. Laparoskopicky asistovaná technika (laparoscopic-assisted)
Laparoskopicky asistovaná technika představuje kombinované použití laparoskopie a minilaparotomie, která bývá umístěna nejčastěji vlevo v mezogastriu. V první době je laparoskopicky vypreparována aorta nebo pánevní tepna. V další době je provedena minilaparotomie a cévní anastomóza je našita klasickou technikou. Někteří autoři upřednostňují tento přístup standardně z důvodu bezpečného šití cévní anastomózy, jiní ho považují jen jako mezistupeň v rámci přípravy k plné laparoskopické technice. Na druhou stranu lze v případě komplikací poměrně jednoduše konvertovat plně laparoskopický výkon na laparoskopicky asistovaný.
3. Plně laparoskopická technika (totally laparoscopic)
Plně laparoskopická technika spočívá v tom, že celá operace probíhá jen laparoskopickými nástroji zavedenými přes trokary bez použití dalších pomocných řezů. Tato metoda je v současnosti všeobecně preferována.
Stejně jako při otevřené operaci je možné i laparoskopicky zvolit několik možných cest k aortě a pánevním tepnám.
- a) Přímý transperitoneální přístup [7–9]
Při tomto přístupu jsou tenké střevní kličky umístěny směrem k žaludku a játrům a následně dočasně fixovány retraktory nebo síťkou, která je přes trokar umístěna do dutiny břišní. Retroperitoneum je otevřeno nad příslušnou tepnou, která je v potřebném rozsahu vypreparována.
- b) Retrokolický intraperitoneální přístup [10–13]
Retroperitoneum je otevřeno laterálně od colon descendens a vše je odtaženo přes střední čáru do pravé poloviny břicha.
- c) Retrorenální intraperitoneální přístup [14]
Mediálně od colon descendens je otevřeno peritoneum a Todtova fascie. V dalším průběhu je mobilizována ledvina, která je poté uložena mediálně.
- d) Retroperitoneální přístup [15]
Z drobné incise je přímo proniknuto do retroperitonea a pomocí insuflace CO2 nebo dilatačním balónem je v retroperitoneu vytvořen potřebný pracovní prostor v okolí příslušné tepny.
- e) Modifikovaný přímý transperitoneální přístup [16]
Retroperitoneum je otevřeno od bifurkace aorty případně levé pánevní tepny k levé renální žíle na levé straně aorty v místě levé gonadální žíly. Retroperitoneum je uvolněno v potřebném rozsahu až k pravému okraji aorty a dále je zavěšeno několika stehy ke stěně břišní (Obr. 1). Tímto způsobem vzniká dostatečná bariéra pro tenké střevní kličky a není třeba uvolňovat celý sestupný tračník.
Obr. 1. Vyvěšování zadního peritonea 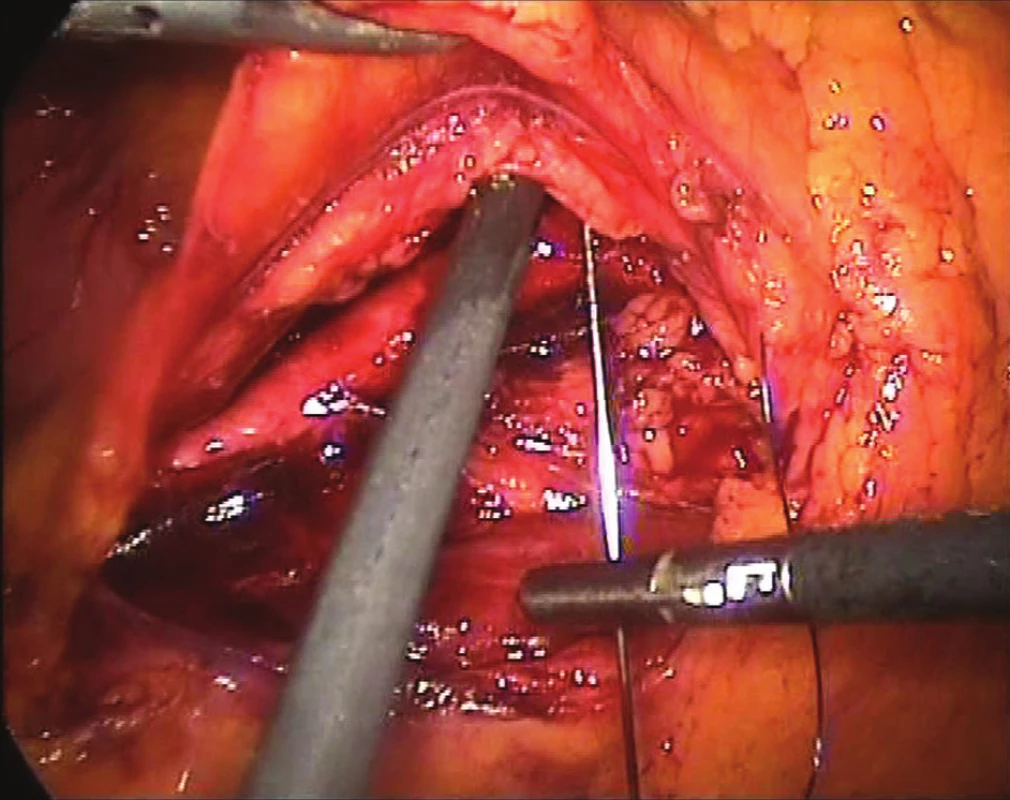
Všechny typy laparoskopických cévních rekonstrukcí – iliakofemorální (IF) a aortofemorální bypass (AF) pravostranný nebo levostranný, aortobifemorální (ABF) bypass a operace výdutě břišní aorty (AAA) – jsou prováděny v kapnoperitoneu s vyhřívaným do břicha proudícím CO2. Intraabdominální tlak je udržován na hodnotě 10–12 mm Hg. Poloha pacienta je na pravém boku v úhlu 45°, v mírné Trendelenburgově poloze, pravá horní končetina bývá upažena, levá u těla. Umístění a počet trokarů závisí na typu rekonstrukce. Obecně jsou trokary umístěny v levé polovině břicha v počtu 4–6. Základní rozmístění trokarů u laparoskopických cévních rekonstrukcí je znázorněno na schematickém nákresu (Obr. 2, 3). Kromě běžného laparoskopického istrumentária jsou použity i speciální cévní laparoskopické nástroje, mezi které patří cévní svorky, endobuldogy, háček na dotahování stehů anastomózy, endoskopický skalpel, endoskopické mikrojehelce a další.
Obr. 2. Schéma portů červeně – pravostranný IF bypass černě – levostranný IF bypass 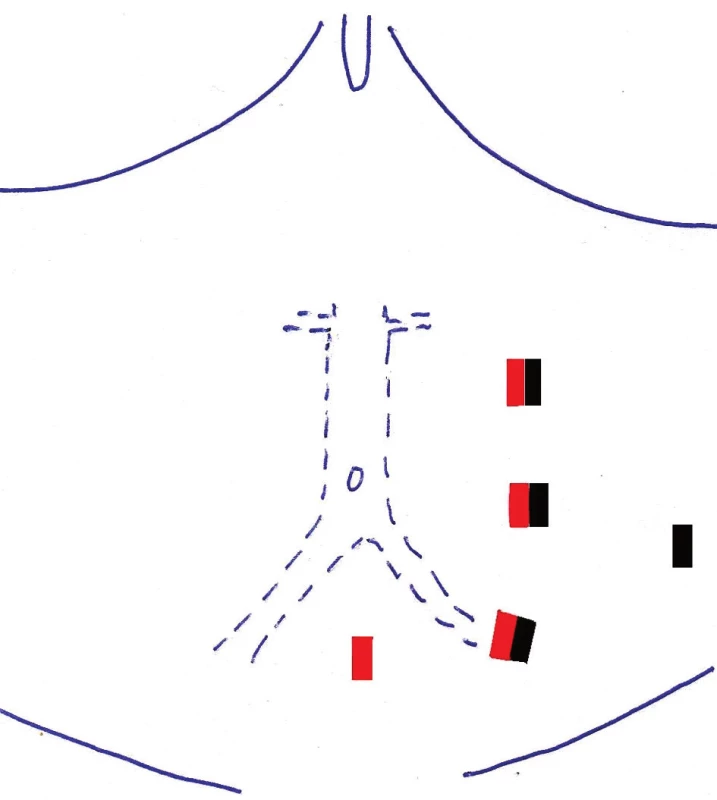
Obr. 3. Schéma portů pro ABF, AF bypass a resekci AAA 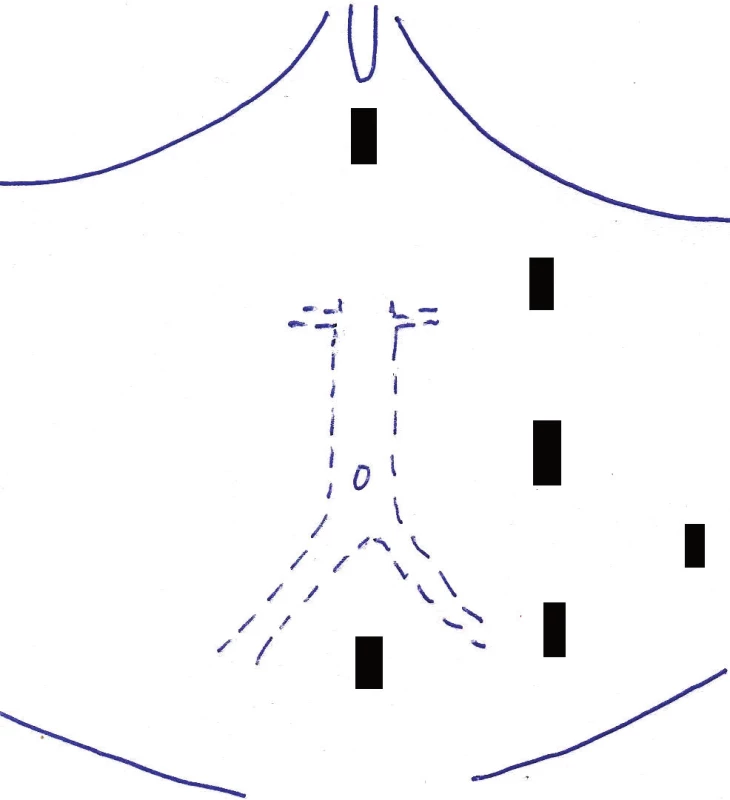
Cévní anastomózy u laparoskopických nebo torakoskopických rekonstrukčních výkonů jsou prováděny pomocí dvou endojehelců (Obr. 4). V případě IF, AF nebo ABF rekonstrukce bývá centrální anastomóza šita pokračujícím nevstřebatelným polytetrafluorethylenovým (PTFE) stehem koncem ke straně (Obr. 5) a při laparoskopické resekci AAA pak koncem ke konci (jedna anastomóza v případě ABF náhrady, dvě anastomózy u aorto-aortální náhrady nebo více anastomóz u aortobiiliacké náhrady či operace torakoabdominální výdutě).
Obr. 4. Šití proximální anastomózy 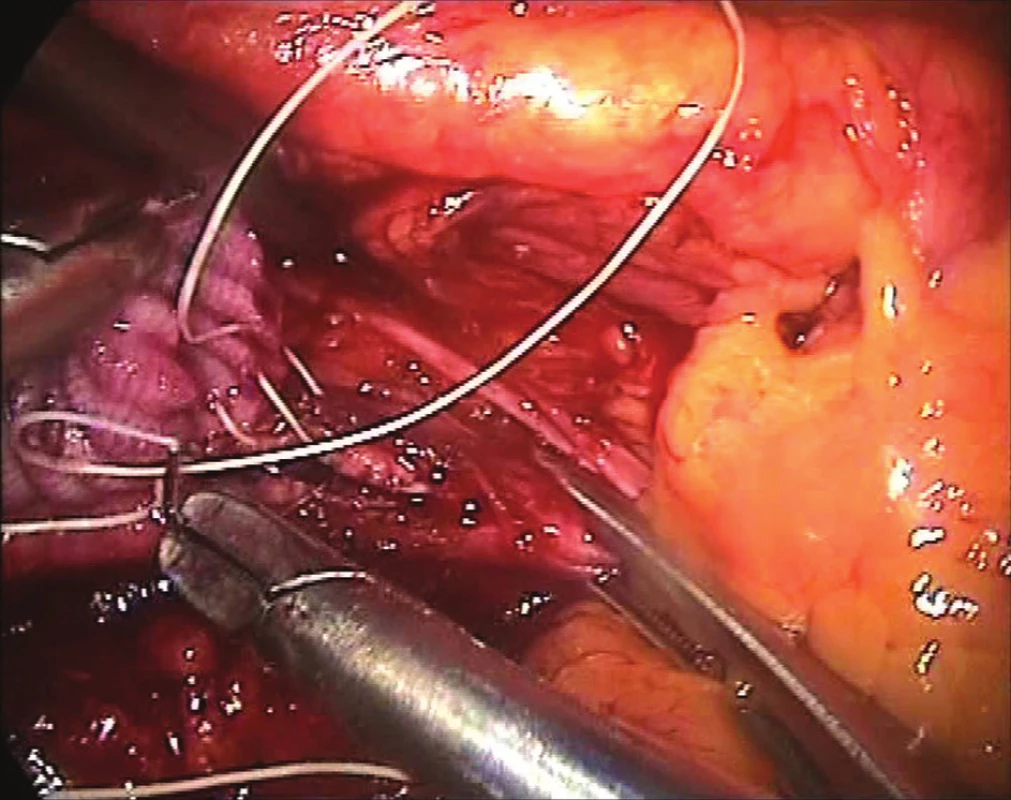
Obr. 5. Proximální anastomóza levostranného IF bypassu 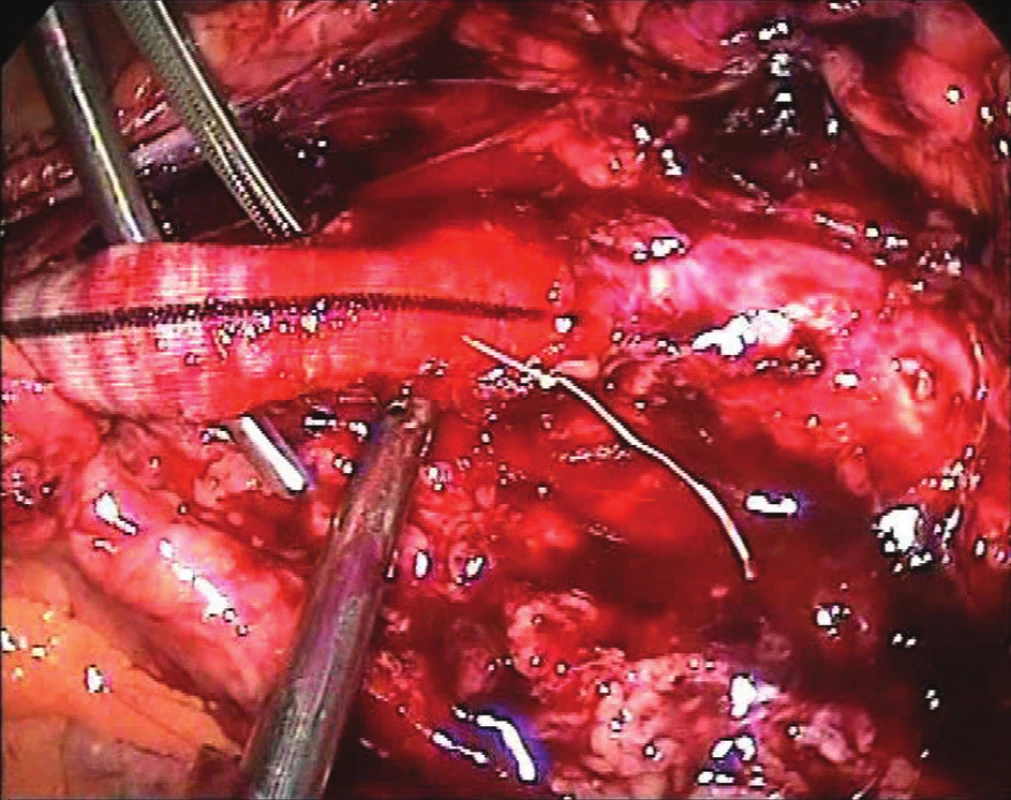
Při laparoskopické operaci výdutě břišní aorty je pro bezpečné našití anastomózy důležité úplné přerušení aorty s ponecháním dostatečně dlouhého krčku. Další odlišnost spočívá v nutnosti zaklipování lumbálních tepen před otevřením vaku výdutě aorty, což vyžaduje větší preparaci ve srovnání s klasickou operací AAA. K okluzi pánevních tepen lze použít Foleyovy katetry CH 12. Mezi další typy operací prováděných laparoskopicky patří bederní sympatektomie, dále operace odstraňující zdroje endoleaků po endovaskulárním řešení AAA – bandáže kotvicích zón nebo klipování lumbálních tepen či dolní mezenterické tepny.
Vzácně jsou prováděny operace hybridní, kdy je řešeno AAA či TAAA endovaskulárně stentgraftem a kvůli plánovanému překrytí viscerálních tepen tomu předchází aortomezenterická nebo aortohepatální cévní rekonstrukce [17–19].
Torakoskopické operace na hrudní aortě patří ve světě zatím stále ještě mezi ojedinělé výkony a jsou publikovány pouze jednotlivé případy. Někteří autoři popisují rekonstrukce mezi sestupnou hrudní aortou a femorální tepnou, operace TAAA nebo bypass mezi vzestupnou hrudní aortou a femorální tepnou, tzv. ventrální aorta.
V experimentální chirurgii jsou zkoušena i různá bezstehová spojení a staplery s prozatím nepříliš uspokojivými výsledky [20–30].
Indikace
Pro okluzivní aortoiliacké postižení jsou dány indikace dle TASC II (Trans-Atlantic inter-Society Consensus) guidelines [31]. Pro otevřenou a stejně i laparoskopickou léčbu jsou indikována postižení typu C a D. S přibývajícími zkušenostmi v laparoskopické chirurgii a s ohledem na dobré výsledky této metody je pravděpodobné, že některá postižení typu B budou v budoucnu řešena laparoskopicky.
Zlatým standardem léčby aortoiliackých aneuryzmat je stále otevřená resekce. Se zdokonalováním endovaskulární techniky (EVAR) dochází k jejímu užívání zejména u rizikových pacientů. Výsledky autorů u laparoskopických operací AAA odpovídají výsledkům EVAR se zachováním definitivního řešení bez nutnosti rehospitalizací stejně jako u otevřené operativy. U EVAR techniky totiž vidíme poměrně častou nutnost řešení komplikací ve smyslu tzv. endoleaků.
Ke kontraindikacím laparoskopické operace patří předchozí aortoiliacká operace, rozsáhlé kalcifikace aortoiliackého úseku, zánětlivá aneuryzmata. Dříve se jednalo i o výdutě aorty vyžadující suprarenální svorku, ovšem s přibývajícími zkušenostmi jsou chirurgové schopni operovat juxtarenální výdutě s dobrými výsledky [32]. Z přidružených onemocnění jsou kontraindikací ASA více než III a těžká obezita.
Komplikace a úskalí
K nevýhodám miniinvazivních výkonů v cévní chirurgii může patřit delší operační čas, který je závislý na zkušenostech chirurga. S narůstajícími zkušenostmi i zde dochází k významné redukci délky operace. Zvláště u laparoskopických a torakoskopických výkonů je důležitý nácvik cévní anastomózy na trenažéru a na zvířeti před zahájením vlastní klinické operativy. Nezanedbatelná není ani laparoskopická zkušenost v obecné chirurgii, která může významně urychlit zvládnutí techniky laparoskopie v cévní chirurgii.
Komplikace u minimálně invazivních cévních výkonů (zvláště laparoskopických nebo torakoskopických) mohou být obecné a specifické.
Mezi obecné patří komplikace v důsledku insuflace CO2 a zvýšeného tlaku v dutině břišní nebo hrudní. Při obvyklém intraabdominálním tlaku (10–12 mm Hg) používaném při laparoskopii vzniká jen mírná hyperkapnie a respirační acidóza, které jsou dobře tolerovány. Nároky kladené na respirační systém při laparoskopii jsou mnohem vyšší než při klasické operaci. Vysoký intraabdominální tlak může způsobit kolaps kapacitních cév, snížit cévní rezistenci a krevní tlak, zapříčinit těžkou hyperkapnii, která má kardiodepresivní efekt, popřípadě může být příčinou embolizace plynu.
V průběhu laparoskopických zákroků je třeba průběžně kontrolovat přístroj pro insuflaci CO2, zajistit dostatečnou relaxaci břišní stěny, intermitentní desuflaci dutiny břišní a úplnou desuflaci CO2 po operaci. Dalšími možnými komplikacemi může být poranění břišních nebo hrudních orgánů při zavádění trokarů. Instalace prvního trokaru musí být prováděna opatrně a v případě jizvy po předcházející operaci zcela mimo tuto oblast. Jizva po střední laparotomii a jizvy v pravé polovině břicha nejsou kontraindikací k laparoskopii. Další trokary jsou již striktně instalovány za přímé vizuální kontroly kamerou. Pohyby trokarů a nástrojů uvnitř dutiny břišní musejí být pečlivě sledovány.
Specifické komplikace jsou závislé na typu operace. V cévní chirurgii se jedná hlavně o krvácení, které může být jednak z oblasti anastomózy, z nedostatečně těsnících cévních svorek, neošetřených drobných větví aorty (např. lumbální tepny), poranění retroaortální levé renální žíly atd. Důležité je důkladné prostudování předoperačního CT se zaměřením na pozici levé renální žíly a odstupy lumbálních tepen. Při neztišitelném krvácení je nutná konverze na otevřený přístup. Na konci operace je také třeba pečlivě zkontrolovat a případně ošetřit krvácení po jednotlivých portech. Při disekci zadního listu peritonea je také určité riziko poranění či distenze ureteru.
Závěr
Laparoskopické cévní operace nejsou běžně prováděny, ale jsou zatím soustředěny jen na některá specializovaná centra. Zlepšující se technické podmínky a narůstající zkušenosti umožňují provádět stále složitější laparoskopické cévní výkony, mezi které patří například resekce juxtarenální výdutě břisní aorty, resekce výdutě břišní aorty s implantací dolní mezenterické tepny, aortomezenterický či aortohepatický bypass nebo reoperace laparoskopických cévních výkonů atd.
Minimálně invazivní výkony v cévní chirurgii splňují obecné výhody miniinvazivní chirurgie. Patří k nim především příznivý kosmetický efekt, snížení pooperační bolestivosti, redukce morbidity a mortality, snížení četnosti kýly v jizvě po laparotomii, dále zkrácení pooperační závislosti na ventilátoru i pobytu na JIP, zkrácení celkové doby hospitalizace, snížení nákladů na léčbu a časnější návrat pacienta k běžnému životu.
Zavedení pravidelného programu laparoskopické operativy zkracuje „learning curve“, přináší inovace postupů a snižuje četnost technických chyb a komplikací.
Seznam zkratek
IF – iliakofemorální rekonstrukce
AF – jednostranná aortofemorální rekonstrukce
ABF – oboustranná aortofemorální rekonstrukce
AAA – výduť břišní aorty
TAAA – výduť torakoabdominální aorty
EVAR – Endovascular Aneurysm/Aortic Repair
TASC II – Trans-Atlantic inter-Society Consensus
MUDr. Libor Dvořáček
Tajovského 1260/9
142 00 Praha 4
e-mail: libor.dvoracek@homolka.cz
Zdroje
1. Dion YM, Kathouda N, Rouleau C, Aucoin A. Laparoscopy-assisted aortobifemoral bypass. Surg Laparosc Endosc 1993;3 : 425–429.
2. Dostalík J. Laparoskopicky asistovaný ilikofemorální by-pass. Rozhl Chir 1997;76;4 : 187–189.
3. Dion YM, Gracia CR, Ben El Kadi HH. Totally laparoscopic abdominal aortic aneurysm repair. J Vasc Surg 2001;33 : 181–185.
4. Štádler P, Vitásek P, Matouš P, Špaček M. Laparoskopická resekce výdutě břišní aorty. Rozhl Chir 2005;84 : 443–447.
5. Coggia M, Javerliat I, Di Centa I, Royer B, Kitzis M, Goeau-Brissonniere OA. Total videoscopic treatment of a type IV thoracoabdominal aneurysm. J Vasc Surg 2005;41 : 141–145.
6. Coggia M, Cerceau P, Di Centa I, Javerliat I, Colacchio G, Goeau Brissonniere O. Total laparoscopic juxtarenal abdominal aortic aneurysm repair. J Vasc Surg 2008;48 : 37–42.
7. Alimi YS, Hartung O, Cavalero C et al. Intestinal retraktor for transperitoneal laparoscopic aortoiliac reconstruction: experimental study on human cadavers and initial clinical experience. Surg Endosc 2000;14 : 915–917.
8. Alimi YS, Hartung O, Valerio N et al. Laparoscopic aortoiliac surgery for aneurysm and occlusive disease: when should a minilaparotomy be performed? J Vasc Surg 2001;33 : 469–475.
9. Di Centa I, Coggia M, Javerliat I et al. Total laparoscopic aortic surgery: transperitoneal direct approach. Eur J Vasc Endovasc Surg 2005;30 : 494–496.
10. Dion YM, Gracia CR. A new technique for laparoscopic aortobifemoral graft inocclusive aortoiliac disease. J Vasc Surg 1997;26 : 685–692.
11. Dion YM, Gracia CR, El Kad i H. Totally laparoscopic abdominal aortic aneurysm repair. J Vasc Surg 2001;33 : 181–185.
12. Coggia M, Bourriez A, Javerliat I et al. Totally laparoscopic aortobifemoral bypass: a new and simplified approach. Eur J Vasc Endovasc Surg 2002;24 : 274–275.
13. Dion YM, Thaveau F, Fearn S. Current modifications to totally laparoscopic “apron technique”. J Vasc Surg 2003;38 : 403–406.
14. Coggia M, Di Centa I, Javerliat I et al.Total laparoscopic aortic surgery: transperitoneal left retrorenal approach. Eur J Vasc Endovasc Surg 2004;28 : 619–622.
15. Javerliat I, Coggia M, Di Centa I et al. Total videoscopic aortic surgery: left retroperitoneoscopic approach. Eur J Vasc Endovasc Surg 2005;29 : 244–246.
16. Štádler P, Šebesta P, Vitásek P, Matouš P, El Samman K. A Modified Technique of Transperitoneal Direct Approach for Totally Laparoscopic Aortoiliac Surgery. European Journal Of Vascular And Endovascular Surgery 2006;32;3 : 266–269.
17. Bakoyiannis CN, Cagiannos C, Wasilljew S et al. Laparoscopy-assisted hybrid technique for renal revascularization using an endovascular graft: report of three cases. Vascular 2007;15 : 154–157.
18. Bakoyiannis C, Cagiannos C, Wasilljew S et al. Totally laparoscopic aortohepatic bypass for aortic debranching during endovascular thoracoabdominal aneurysm repair. Eur J Vasc Endovasc Surg 2007;34 : 173–175.
19. Bakoyiannis C, Cagiannos C, Wasilljew S et al. Laparoscopic hybrid techniques for ectopic or accessory renal arteries debranching in complex endovascular aneurysm repair. J Cardiovasc Surg 2008;49 : 67–71.
20. Romachou F. Les appareils soviétiques chirurgicaux de suture. Presse Med 1964;72 : 277–282.
21. Nakayama K, Tamiya T, Yamamoto K. A simple new apparatus for small vessels anastomosis. Surgery 1962;52 : 918–922.
22. Zeebregts CJ, Heijmen RH, van den Dungen JJ, van Schilfgaarde R. Non-suture methods of vascular anastomosis. Br JSurg 2003; 90 : 261–271.
23. Millon A, Boufi M, Garitey V et al. Evaluation of a new vascular suture system for aortic laparoscopic surgery: an experimental study on pigs and cadavers. Eur J Vasc Endovasc Surg 2008;35 : 730–736.
24. Nakano Y, Hori Y, Sato A et al. Evaluation of a Poly(l-lactic acid) stent for sutureless vascular anastomosis. Ann Vasc Surg 2009;23(2):231–238.
25. Scarcello E, Triggiani G, Arispici M et al. Experimental study of a new vascular anastomotic technique in a swine model: short and mid-term results. Ann Vasc Surg 2007;21 : 346–331.
26. Yoffe B, Vaysbeyn I, Urin Y et al. Experimental study of a novel suture-less aortic anastomotic device. Eur J Vasc Endovasc Surg 2007;34(1):79–86.
27. Elkouri S, Noel AA, Gloviczki P et al. Stapled aortic anastomoses: a minimally invasive, feasible alternative to videoscopic aortic suturing? Vasc Endovasc Surg 2004;38(4):321–330.
28. Shifrin EG, Moore WS, Bell PR, Kolvenbach R, Daniline EI. Intravascular stapler for open aortic surgery: preliminary results. Eur J Vasc Endovasc Surg 2007;33(4):408–411.
29. Kolvenbach R, Shiffrin E, Schwierz E, Wassiljew S, Caggianos C. Evaluation of an aortic stapler for an open aortic anastomosis. J Cardiovasc Surg 2007;48(5):659–665.
30. Calles-Vazquez MC, Viguera FJ, Crisostomo V, Uson-Gargallo J. Vascular closure stapler clip anastomosis decreases aortic cross-clamping time compared to interrupted nonabsorbable and running absorbable sutures in growing pigs. Ann Vasc Surg 2006;20(1) :35–41.
31. Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). J Vasc Surg 2007;45Suppl S:S5–67.
32. Coggia M, Cerceau P, Di Centa I et al. Total laparoscopic juxtarenal abdominal aortic aneurysm repair. J Vasc Surg 2008;48 : 37–42.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2012 Číslo 7- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Trandolapril snižuje riziko rozvoje srdečního selhání i u pacientů se stabilní ICHS
- Stillova choroba: vzácné a závažné systémové onemocnění
- Cinitaprid – v Česku nová účinná látka nejen pro léčbu dysmotilitní dyspepsie
-
Všechny články tohoto čísla
- Interní grantová agentura MZČR a výzkum v chirurgii
- Endosonografie jícnu v diagnostice a léčbě tumorů jícnu
- Descendentní nekrotizující mediastinitida – chirurgická léčba
- Výsledky limitované resekce karcinomu gastroezofageální junkce
- Rekonstrukce prsů přenosem autologního tuku
- Perzistence foramen ovale patens a riziko paradoxní embolizace žilních bublin u potápěčů – cave pro sklerotizaci varixů pěnovou metodou
- Chirurgické řešení komplikované jaterní echinokokózy u dvou bulharských občanů na dvou pracovištích v České republice
- Segmentální duodenektomie (D3, D4) pro angiosarkom
- Specializační příprava v nástavbovém oboru onkochirurgie (Ve stejném znění platí i pro obor koloproktologie)
- Je prokletím lidské přirozenosti zapomínat
- Aktuální pohled na robotickou cévní chirurgii
- EVAR - jeho současné možnosti a role v cévní chirurgii
- Laparoskopická cévní chirurgie
- Radiofrekvenční ablace varixů dolních končetin pod ultrasonografickou kontrolou
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- EVAR - jeho současné možnosti a role v cévní chirurgii
- Chirurgické řešení komplikované jaterní echinokokózy u dvou bulharských občanů na dvou pracovištích v České republice
- Descendentní nekrotizující mediastinitida – chirurgická léčba
- Segmentální duodenektomie (D3, D4) pro angiosarkom
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



