-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Aktuální pohled na robotickou cévní chirurgii
Autoři: P. Štádler; L. Dvořáček; P. Vitásek; P. Matouš
Působiště autorů: Oddělení cévní chirurgie, Nemocnice Na Homolce Praha, primář: Doc. MUDr. P. Štádler, Ph. D.
Vyšlo v časopise: Rozhl. Chir., 2012, roč. 91, č. 7, s. 396-399.
Kategorie: Postgraduální vzdělávání
Vývoj lékařských robotů navazuje na rozvoj průmyslových robotických zařízení. V medicíně byly první roboty použity jako podpůrní a rehabilitační pomocníci a dále následovala chirurgie. Při rehabilitaci bylo typické použití robotického ramena u pacientů s pohybovým postižením. Tento typ robotů má asi pětiletý náskok proti robotům v chirurgii, kde byla postupně vyvinuta řada těchto zařízení s různými názvy (MAT 560, ROBODOC, PUMA 200, MINERVA, ZEUS, AESOP atd.), které si zkoušely najít využití v řadě chirurgických oborů. První klinické využití robota v urologii (Probot) proběhlo v roce 1989, a to konkrétně k transuretrální resekci prostaty. Další robotické systémy s označením Aesop a Zeus byly již počítačem řízené. Robotický systém da Vinci je jediným zařízením pro široké klinické využití, který byl schválen jako chirurgický pomocník v roce 2000 a stal se v chirurgii určitým mezníkem. Pomáhá hlavně v hůře přístupných oblastech a při zákrocích, které jsou prostou rukou chirurga obtížně proveditelné [9–16].
Robot da Vinci
Operační robot je založen na principu multimotorického víceramenného systému a je složen ze tří hlavních částí. První částí je ovládací konzola tzv. pracoviště operatéra, odkud se řídí ramena s nástroji a kde má operatér prostřednictvím 3D obrazu dokonalý přehled v operované oblasti. Druhou částí je pak operační konzola s robotickými rameny pro nástroje a třetí je přístrojová věž (Obr. 1). Chirurgické zákroky prováděné robotickým systémem da Vinci jsou často označovány jako da Vinci chirurgie. Pracovní konce robotických nástrojů jsou v podstatě pohyblivé jako ruka a dá se s nimi lépe manipulovat hlavně i v nepřístupných oblastech, tzv. „za rohem“, což je hlavní výhoda tohoto zařízení (Endo-Wrist technika). Všechny pohyby jsou zpracovány a interpretovány počítačem tak, aby zpřesnily a zabezpečily bezpečný pohyb chirurgických nástrojů v pacientově těle. To vše spolu s eliminací třesu rukou přispívá k významnému snížení operačních rizik a tím překonává ve všech směrech klasickou laparoskopii [9–13].
Obr. 1. Robotický systém da Vinci 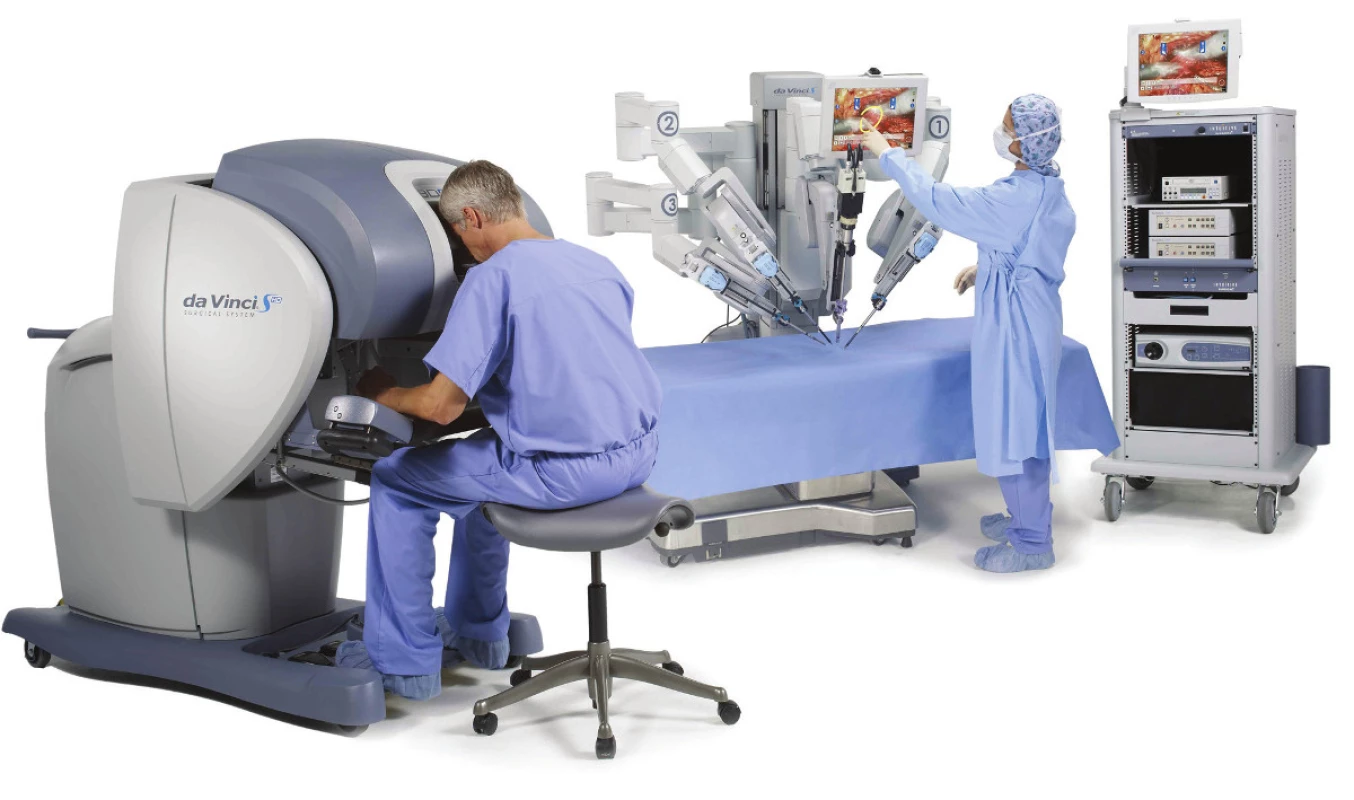
Ovládací konzola slouží operatérovi k ovládání robotického systému a operační pole sleduje prostřednictvím 3D obrazu v zobrazovacím zařízení. Trojrozměrný obraz je zprostředkován díky stereoskopické optice, která obsahuje dvě digitální kamery a osvětlení. Ovládací konzola nemusí být umístěna na operačním sále, ale většina robotických chirurgů v tom však nevidí zásadní výhodu, protože preferují přímou komunikaci s ostatními členy týmu a oční kontrolu situace na operačním sále.
Operační konzola podle konfigurace obsahuje dvě nebo tři pracovní ramena a jedno rameno kamerové a je během zákroku umístěna bezprostředně u operačního stolu. Během operace je kryta speciálními jednorázovými sterilními povlaky (Obr. 2). Vlastní robotické nástroje o průměru 8 nebo 5 mm jsou sterilizovatelné a k ramenům robota se připevňují prostřednictvím plastových destiček. Robotické nástroje mají svoji předem určenou životnost, tzn. s určitým nástrojem lze provést přesně daný počet operací.
Obr. 2. Umístění robotických ramen při operaci 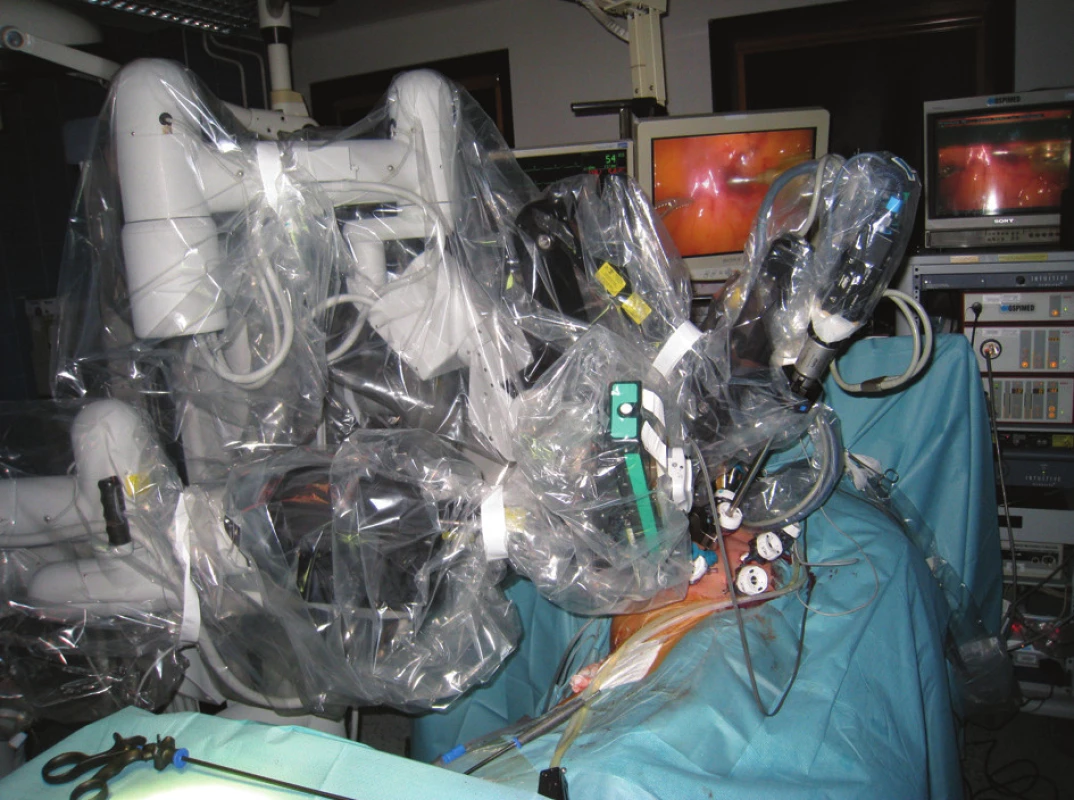
Přístrojová věž je základní součástí robotického systému a slouží pro zpracování obrazů ze stereoskopické kamery. Prostřednictvím asistentského monitoru je umožňován pohled na operovanou oblast pro asistenty i ostatní personál. Na videověži jsou umístěny i další přístroje, které jsou potřebné pro vlastní robotickou operaci, kam patří zdroj světla, koagulace, insuflace, odsávačka, zařízení pro ohřev CO2, který zajišťuje pneumoperitoneum, atd.
Využití robotického systému v cévní chirurgii
Na základě vlastních zkušeností s více než 250 operacemi můžeme konstatovat, že lze roboticky úspěšně provádět cévní anastomózu na aortě, pánevní i viscerální tepně, a to dokonce zásadně snadněji než při klasické laparoskopické operaci [14–16]. Další možností je odstranění aterosklerotických hmot z lumina aorty nebo pánevních tepen, které mohou způsobit jejich zúžení, a robotický systém je tedy možné využít k tromboendarterektomii velkých tepen a následně i pro uzávěr takto desobliterovaných tepen cévní záplatou. Neméně zajímavou oblastí pro robotickou cévní chirurgii jsou operace výdutě břišní aorty. Velice zajímavé je použití robotického systému při rekonstrukci viscerálních tepen, například při operaci výdutě slezinné tepny nebo rekonstrukce ledvinné tepny, ošetření endoleaku po endovaskulárních zákrocích či některé hybridní výkony, které patří také do spektra našich robotických cévních operací. Ojedinělým výkonem pak je i robotická intervence při řešení výdutě vnitřní prsní tepny (Tab. 1).
Tab. 1. Možnosti roboticky asistované cévní chirurgie 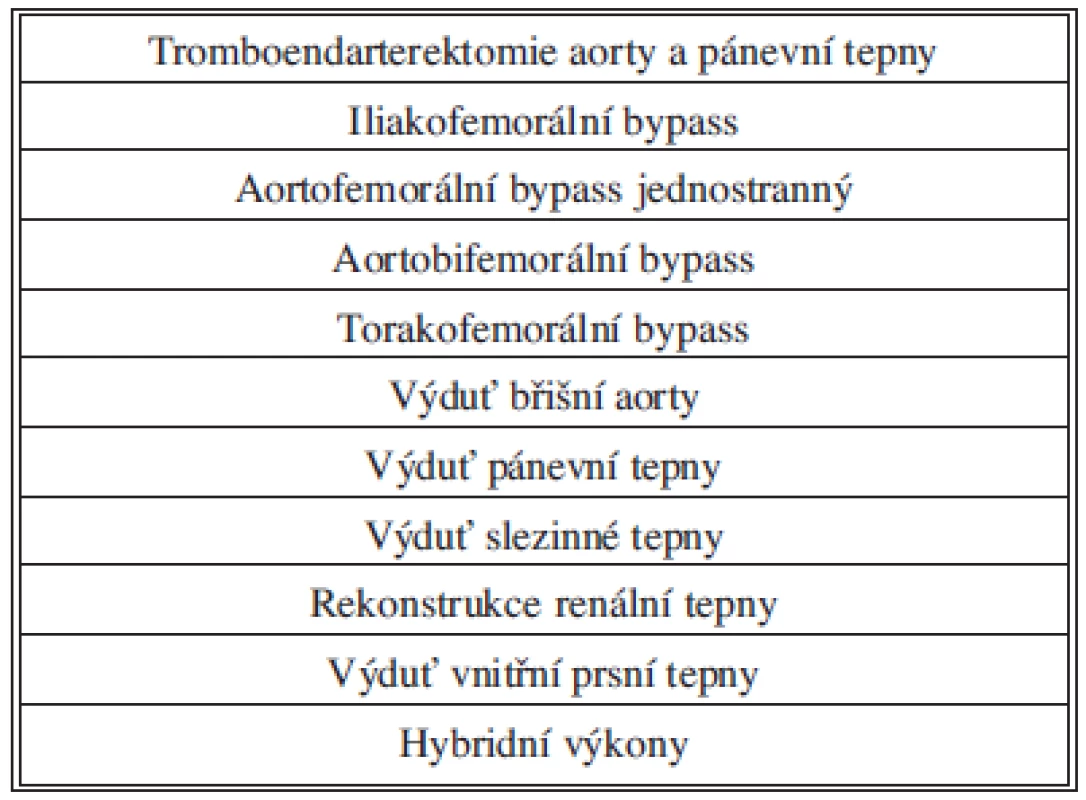
Podle typu onemocnění se může jednat o robotické operace v aortoiliacké oblasti z důvodu aterosklerotického obliterujícího nebo aneuryzmatického postižení. Obecně náročnější výkony na viscerálních tepnách, hybridní výkony v kombinaci s endovaskulárními technikami a robotické operace hrudní aorty zcela jistě patří jen do rukou zkušených vaskulárních chirurgů s dobrými laparoskopickými i robotickými zkušenostmi [17–20].
Základním přístupem k cévní problematice v aortoiliacké oblasti je modifikovaný transperitoneální přístup. Pro většinu robotických cévních rekonstrukcí jsou použita tři robotická ramena, jen v případě operace výdutě pánevní tepny nebo kombinovaného aneuryzmatického postižení aorty a pánevních tepen či operace renálních tepen bývá často čtvrté rameno s nástrojem využito jako tkáňový retraktor. Poloha pacienta je většinou na pravém boku, v úhlu 30–45°, levá horní končetina je uložena podél těla a dolní končetiny jsou mírně pokrčeny v kolenou. Poloha pacienta musí v případě aortobifemorální rekonstrukce zajišťovat dokonalý přístup i do třísel. Operační konzola je v naprosté většině případů umístěna na pravé straně pacientova těla. Roboticky asistované cévní operace je možné provádět kombinovaně za použití standardní laparoskopie a robotického systému Da Vinci anebo plně roboticky. Při kombinovaném postupu je laparoskopicky provedena preparace tepen a následně pak roboticky vlastní cévní anastomóza. V případě plně robotické operace jsou všechny kroky uskutečněny jen roboticky. Standardně používáme pro aterosklerotické stenozující postižení šest 10–12mm trokarů a pro aneuryzmatické postižení je jejich počet sedm.
Tromboendarterektomie aorty a pánevní tepny bývá obecně prováděna chirurgicky velice ojediněle. Stejná situace platí i pro robotickou chirurgii (Obr. 3). Naprostá většina izolovaných stenotických postižení v této oblasti je indikována k angioplastice, v našem souboru se jednalo o pět pacientů (2 %).
Obr. 3. Tromboendarterektomie aorty 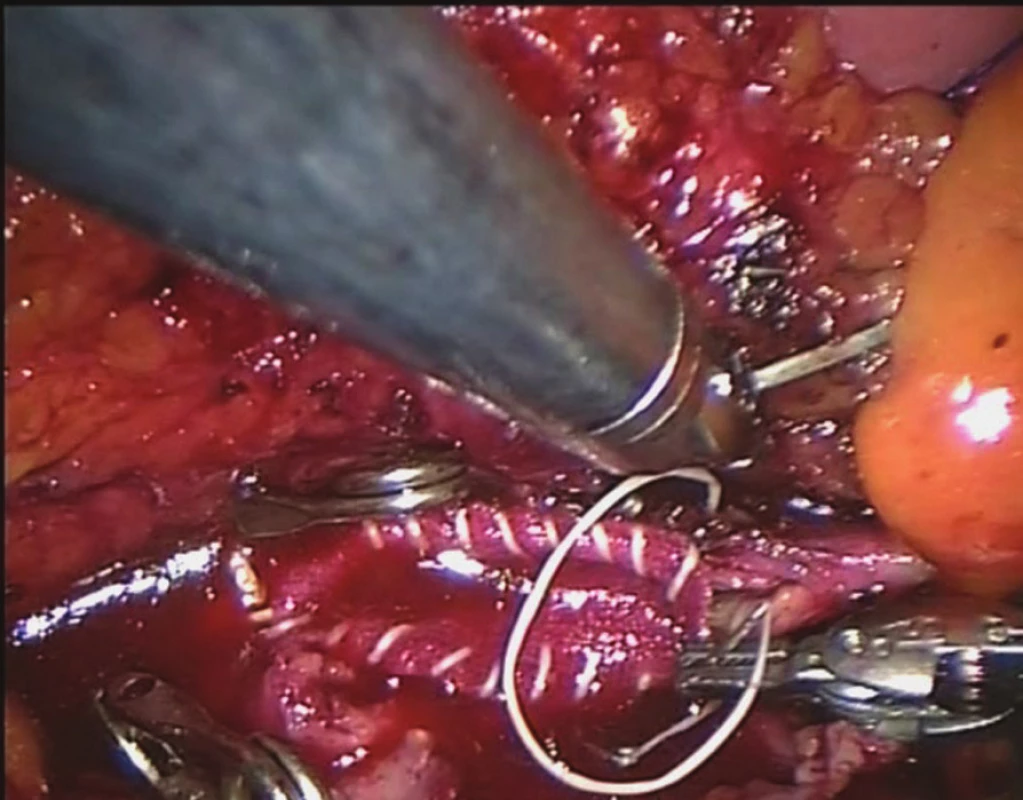
Iliakofemorální a aortofemorální bypassy představují nejčastější typ roboticky asistované cévní rekonstrukce a v našem souboru tvoří 76 %. Iliakofemorální rekonstrukce jsou indikovány při uzávěru zevní pánevní tepny a průchodné společné pánevní tepně, aortofemorální jednostranný pak při kompletním uzávěru příslušné pánevní tepny a oboustranný při postižení obou pánevních tepen (Obr. 4).
Obr. 4. Centrální „end to side“ anastomóza (ABF) 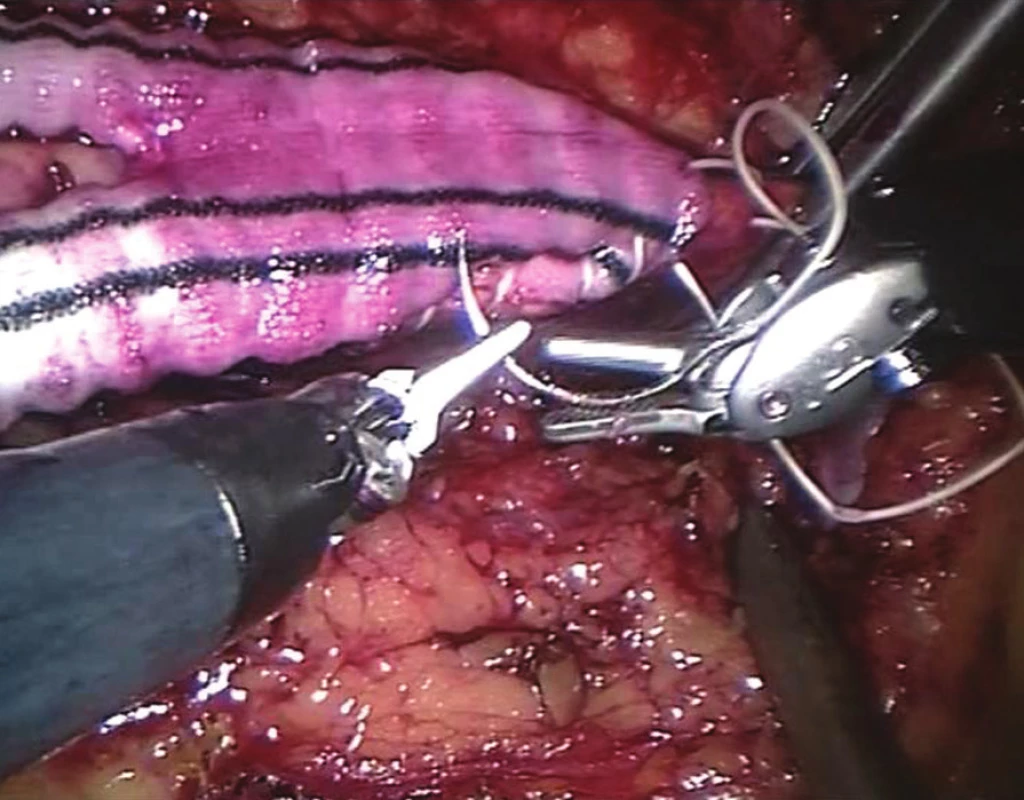
Na tomto místě je třeba zmínit, že roboticky asistované iliakofemorální rekonstrukce bývají uskutečňovány hlavně z důvodu tréninku a nácviku robotických cévních operací a v současné době jsou prováděny na našem pracovišti při indikaci mininvazivní strategie téměř výlučně laparoskopicky.
Výduť břišní aorty
Roboticky asistovaná náhrada výdutě břišní aorty již představuje náročnější operační výkon, který vyžaduje dostatečnou zkušenost operatéra jak v oblasti otevřené chirurgie, tak hlavně v chirurgii robotické (Obr. 5). Roboticky můžeme provést jak aorto-aortální náhradu, tak i náhradu aortoiliackou při postižení břišní aorty a pánevních tepen. Náš soubor obsahuje téměř 19 % těchto operací. Rozmístění trokarů je shodné s robotickými aortofemorálními rekonstrukcemi, jen počet je zvýšen na sedm.
Obr. 5. Centrální anastomóza „end to end“ (AAA) 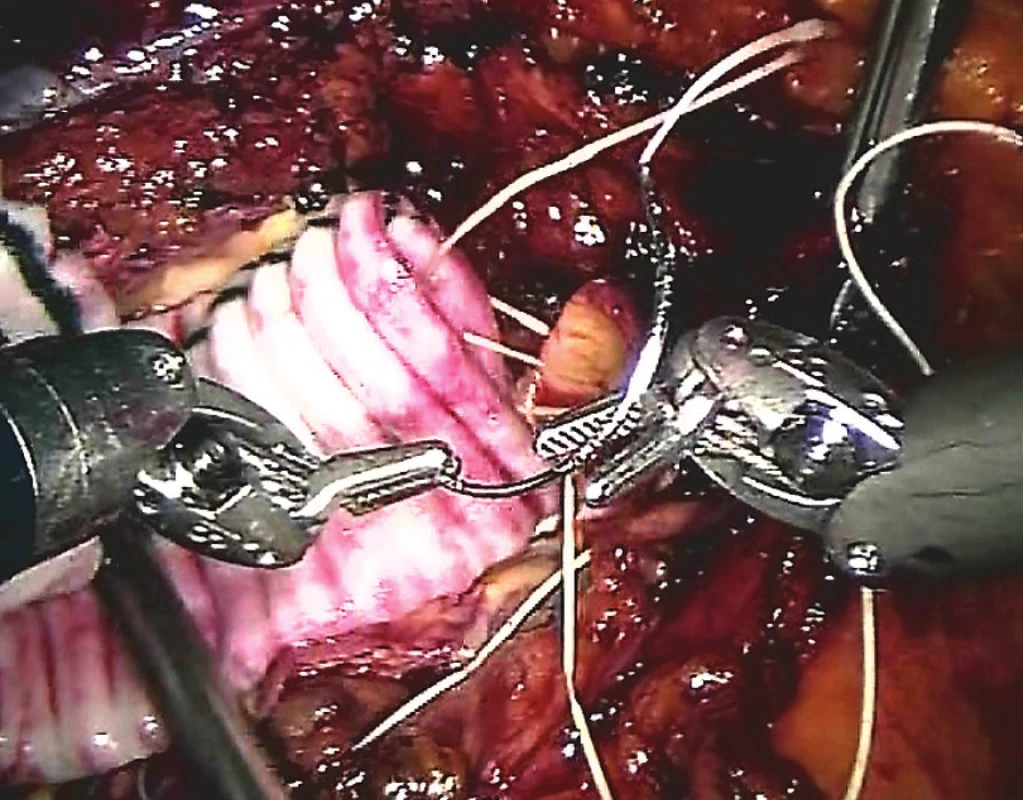
Výduť pánevní tepny
Izolovaná výduť pánevní tepny je poměrně vzácné onemocnění, které se v našem souboru vyskytovalo v necelém 1 % výkonů. Při robotické operaci používáme v tomto případě čtyři robotická ramena, z nichž nástroj jednoho z nich funguje jako retraktor v oblasti pánve.
Poloha pacienta i vlastní operační přístup je obdobný jako při operaci AAA, standardně je použito šest trokarů.
Výduť slezinné tepny
Představuje sice zajímavý, ale opět poměrně málo se vyskytující robotický zákrok. Naprostá většina výdutí menšího rozsahu je řešena v této oblasti endovaskulárně. Při nálezu velké výdutě však často není endovaskulární zákrok možný a většinou se nabízí jako řešení splenektomie. Pomocí robotického systému můžeme provést záchovnou operaci sleziny i při výduti, která dosahuje velikosti kolem 6 cm. Je nutno říci, že se musí jednat o nález, který není umístěn v hilu sleziny. V našem souboru se opět počet těchto zákroků pohybuje do 1 %.
Při této operaci je robotický systém umístěn atypicky šikmo za levým ramenem pacienta, ale poloha nemocného zůstává stejná jako při ostatních cévních výkonech, jen s menším podložením a počtem 4–5 trokarů.
Rekonstrukce renálních tepen
Rekonstrukce renálních tepen je v éře angioplastiky sice další možnou, ale jen málo se vyskytující robotickou operací. V uváděném souboru jsme zaznamenali výskyt v necelém 1 %. Tento zákrok je možno provést samostatně nebo jako součást dalšího cévního výkonu. K robotické operaci výdutě ledvinné tepny je zapotřebí uvolnit a mobilizovat příslušné ohbí tlustého střeva a v potřebném rozsahu vypreparovat aneuryzmatické rozšíření renální tepny. Většinou je zapotřebí k rekonstrukci této tepny interponovat žilní štěp, ve výjimečných případech při dostatečném uvolnění centrální i periferní části ledvinné tepny je možná po exkluzi výdutě její přímá sutura [21, 22].
Hybridní robotické výkony
V robotické cévní chirurgii se může jednat o kombinovaný výkon cévní a všeobecně chirurgický nebo čistě cévní zákrok. V kombinaci s všeobecnou chirurgií to může být robotická cévní operace, např. aortofemorální bypass nebo AAA a pupeční kýla nebo kýla v jizvě po předcházející laparotomii.
V případě hybridních čistě cévních výkonů je nejjednodušší kombinací angioplastika a cévní rekonstrukce nebo kombinace bederní sympatektomie a iliako nebo aortofemorálního bypassu. Dále připadá v úvahu kombinace endovaskulárního zákroku (např. stentgraft hrudní aorty) a revaskularizace viscerální tepny (např. renální) nebo kombinace aortofemorální rekonstrukce s endarterektomií renální tepny. K náročnějším výkonům pak patří hybridní operace výdutě torakoabdominální aorty u rizikových pacientů, kde by byl pro nemocného klasický otevřený přístup extrémně nebezpečný.
Ošetření endoleaku po implantaci stentgraftu
V úvahu připadá laparoskopické či robotické ošetření endoleaku prvního nebo druhého typu po endovaskulární léčbě AAA. Závažné jsou hlavně endoleaky, kdy dochází k dalšímu růstu vaku výdutě, tzv. „endotension“.
První typ endoleaku je charakterizován nedostatečnou těsností vlastního stentgraftu, nejčastěji centrální části. Druhý typ pak vzniká v důsledku zpětného toku tepen odstupujících z aorty. Endoleak II. typu po implantaci stentgraftu do subrenální aorty vzniká nejčastěji z průchodné arteria mesenterica inferior (IMA) nebo z lumbálních tepen. Průchodnou IMA lze ošetřit poměrně jednoduše laparoskopicky. Zvládnutí endoleaku z lumbálních tepen je složitější a zvláště pravostranné jsou pro laparoskopickou techniku těžko přístupné. Za těchto okolností lze k zrušení zpětného toku z lumbálních tepen úspěšně použít robotický systém a všechny jeho přednosti.
Výhody robotiky v cévní chirurgii
Nástup robotiky znamená zcela zásadní zlom pro laparoskopickou cévní chirurgii, která představovala obtížnou manipulaci s nástroji, dlouhé šití anastomózy a dlouhou dobu svorky na aortě. Robotický systém tyto zásadní nevýhody cévní laparoskopie zcela odstraňuje a otevírá možnosti pro rozšíření roboticky asistované laparoskopické chirurgie v tomto oboru (Tab. 2).
Tab. 2. Obecné výhody robotické chirurgie 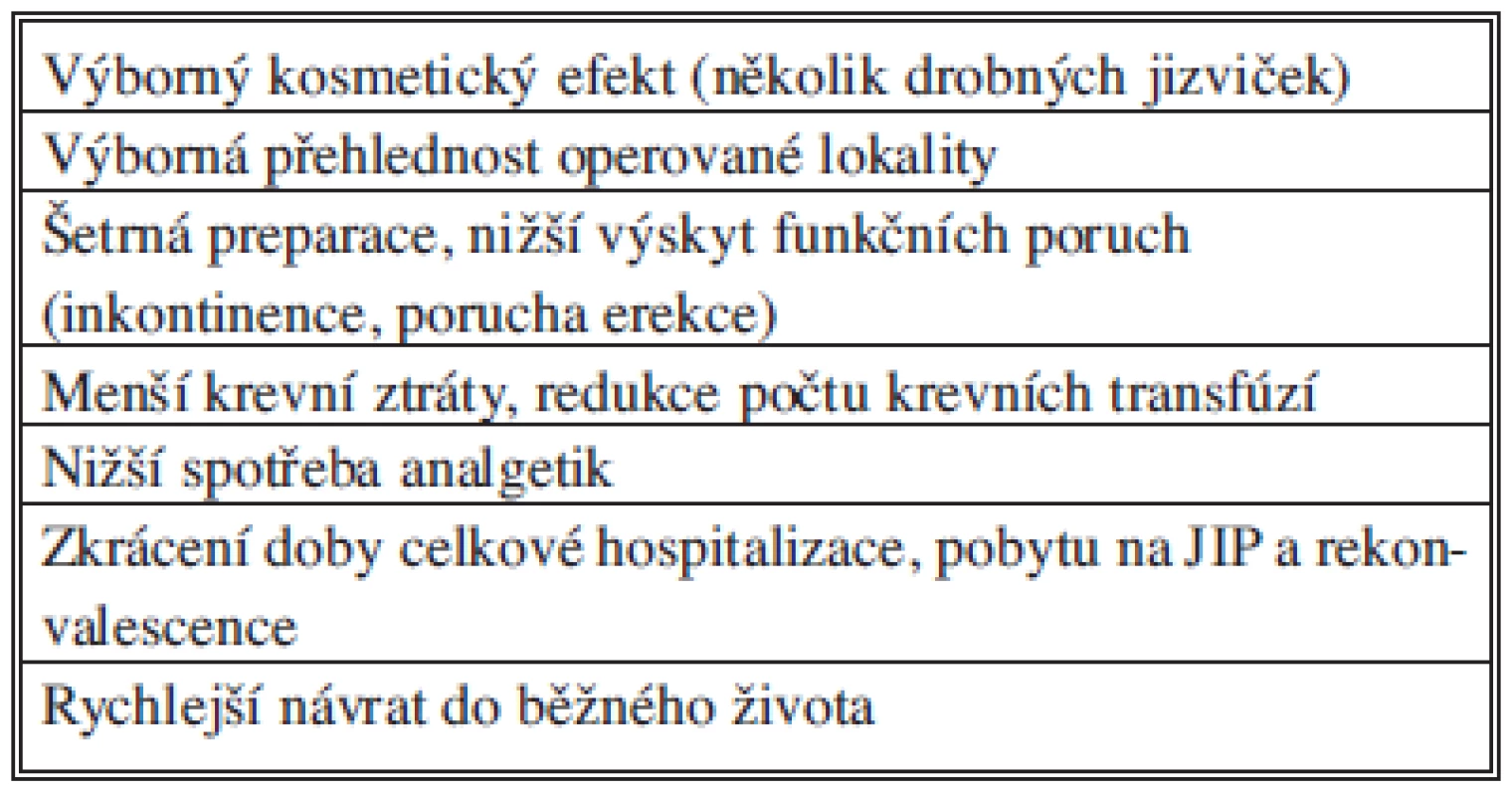
Z praktického hlediska je největším přínosem robotiky rychlost zhotovení cévní anastomózy. Tím byla odstraněna největší nevýhoda laparoskopických cévních rekonstrukcí – dlouhý čas naložené cévní svorky. Zkrácením času nutného ke zhotovení anastomózy se zkrátí i doba dočasné ischémie dolních končetin při naložené aortální svorce. Tyto časy jsou velice podstatné pro srdeční zátěž i reperfúzi svalů a zásadně ovlivňují pooperační průběh včetně morbidity a mortality. V současné době jsou tyto časy srovnatelné s klasickou cévní chirurgií a navíc právě s využitím všech výhod miniinvazivní chirurgie. Cévní pacient profituje hlavně z kratší doby hospitalizace a z možného brzkého návratu k běžným aktivitám i pracovní činnosti, kterou je prakticky možno provádět ve většině případů bez výraznějšího omezení. Nezanedbatelný je vynikající kosmetický efekt. S výhodou je možné používat tuto metodu i u obézních pacientů, kde je klasický výkon technicky náročný a často bývá porucha hojení rány po laparotomii.
Doc. MUDr. Petr Štádler, Ph.D.
Roentgenova 2
150 30 Praha 5
e-mail: petr.stadler@homolka.cz
Zdroje
1. Bonatti J, Schachner T, Bonaros N, Lehr EJ, Zimrin D, Griffith B. Robotically assisted totally endoscopic coronary bypass surgery. Circulation 2011;124(2):236–244.
2. Bokhari MB, Patel CB, Ramos-Valadez DI, Ragupathi M, Haas EM. Learning curve for robotic-assisted laparoscopic colorectal surgery. Surg Endosc 2011;25(3):855–860.
3. Park YM, Lee WJ, Lee JG, Lee WS, Choi EC, Chung SM, Kim SH. Transoral robotic surgery (TORS) in laryngeal and hypopharyngeal cancer. J. Laparoendosc. Adv Surg Tech 2009;19(3): 361–368.
4. Feuer G, Hernandez P, Barker J. Surgical technique enhances the efficiency of robotic hysterectomy. Int J Med Robot 2011;7(1): 1–6.
5. Patel VR, Abdul-Muhsin HM, Schatloff O, Coelho RF, Valero R, Ko YH, Sivaraman A, Palmer KJ, Chauhan S. Critical review of _ntafecta_utcomes after robot-assisted laparoscopic prostatectomy in high-volume centres. B J U Int 2011;108 : 1007–1017.
6. Lang JE, Mannava S, Floyd AJ, Goddard MS, Smith BP, Mofidi A, Seyler TM, Jinnah RH. Robotic systems in orthopaedic surgery. J Bone Joint Surg Br 2011;93(10):1296–1299.
7. Kaouk JH, Goel RK, Haber GP, Crouzet S, Stein RJ. Robotic single-port transumbilical surgery in humans: initial report. B J U Int 2009;103(3):366–369.
8. Marescaux J, Leroy J, Gagner M, Rubino F, Mutter D, Vix M, Butner SE, Smith MK. Transatlantic robot-assisted telesurgery. Nature 2001;27,413(6854):379–380.
9. Wisselink W, Cuesta MA, Gracia C, Rauwerda JA. Robot-assisted laparoscopic aortobifemoral bypass for aortoiliac occlusive disease: a report of two cases. J Vasc Surg 2002;36(5):1079–1082.
10. Ruurda JP, Wisselink W, Cuesta MA, et al. Robot-assisted versus standard videoscopic aortic replacement. A comparative study in pigs. Eur J Vasc Endovasc Surg 2004;27 : 501–506.
11. Martinez BD, Wiegand CS. Robotic in vascular surgery. Am J Surg 2004;188 : 57–62.
12. Cadiére GB, Himpens J, Germay O et al. Feasibility of robotic laparoscopic surgery: 146 Cases World J Surg 2001;25 : 1467–1477.
13. Bodner J, Wykypiel H, Wetscher G et al. First experiences with the da Vinci operating robot in thoracic surgery. Eur J Cardiothorac Surg 2004;25 : 844–851.
14. Štádler P, Matouš P, Vitásek P et al. Robot-assisted aortoiliac reconstruction: A review of 30 cases. J Vasc Surg 2006;5 : 915–919.
15. Štádler P, Dvořáček L, Vitásek P, Matouš P. Is Robotic Surgery Appropriate for Vascular Procedures? Report of 100 Aortoiliac Cases. Eur J Vasc Endovasc Surg 2008;36 : 401–404.
16. Štádler P, Dvořáček L, Vitásek P, Matouš P. Robotic vascular surgery, 150 cases. Int J Med Robot 2010; 6(4):394–398.
17. Fernandez JD, Garrett HE, Jr., Cal N. Robot-assisted minimally invasive procedure for descending aorta-bifemoral bypass: a case report. Vasc Endovasc Surg 2009;43(1):93–95.
18. Štádler P, Vitásek P, Matouš P, Dvořáček L. Hybridní roboticky asistovaná operace, aortobifemorální bypass s rekonstrukcí kýly v jizvě. Rozhl Chir 2008;11 : 590–592.
19. Ishikawa N, Sun YS, Nifong LW, Ohtake H, Watanabe G, Chitwood WR, Jr. Robotic replacement of the descending aorta in human cadaver. Artif Organs 2006;30 : 719–721.
20. Wahlgren CM, Skelly C, Shalhav A, Bassiouny H. Hybrid laparorobotic debranching and endovascular repair of thoracoabdominal aortic aneurysm. Ann Vasc Surg 2008;22 : 285–289.
21. Luke P, Knudsen BE, Nguan CY, Pautler SE, Swinnimer S, Kiaii R, Kapoor A. Robot-assisted laparoscopic renal artery aneurysm reconstruction. J Vasc Surg 2006;44 : 651–653.
22. Giulianotti PC, Bianco FM, Addeo P, Lombardi A, Coratti, A. Sbrana F. Robot-assisted laparoscopic repair of renal artery aneurysms. J Vasc Surg 2010;51 : 842–849.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2012 Číslo 7- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Interní grantová agentura MZČR a výzkum v chirurgii
- Endosonografie jícnu v diagnostice a léčbě tumorů jícnu
- Descendentní nekrotizující mediastinitida – chirurgická léčba
- Výsledky limitované resekce karcinomu gastroezofageální junkce
- Rekonstrukce prsů přenosem autologního tuku
- Perzistence foramen ovale patens a riziko paradoxní embolizace žilních bublin u potápěčů – cave pro sklerotizaci varixů pěnovou metodou
- Chirurgické řešení komplikované jaterní echinokokózy u dvou bulharských občanů na dvou pracovištích v České republice
- Segmentální duodenektomie (D3, D4) pro angiosarkom
- Specializační příprava v nástavbovém oboru onkochirurgie (Ve stejném znění platí i pro obor koloproktologie)
- Je prokletím lidské přirozenosti zapomínat
- Aktuální pohled na robotickou cévní chirurgii
- EVAR - jeho současné možnosti a role v cévní chirurgii
- Laparoskopická cévní chirurgie
- Radiofrekvenční ablace varixů dolních končetin pod ultrasonografickou kontrolou
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- EVAR - jeho současné možnosti a role v cévní chirurgii
- Chirurgické řešení komplikované jaterní echinokokózy u dvou bulharských občanů na dvou pracovištích v České republice
- Descendentní nekrotizující mediastinitida – chirurgická léčba
- Segmentální duodenektomie (D3, D4) pro angiosarkom
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



