-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Nanomedicínský přístup pro rychlou identifikaci virů za využití elektrochemických biosenzorů
A nanomedical approach for the rapid identification of viruses using electrochemical biosensors
Aim: The review provides basic practical information about the use of biosensors in the rapid diagnosis of viral pathogens. Results: Thanks to evolutionary changes in the genome, viruses jump into the human population, where they cause serious epidemics. Rapid POCT diagnostic tools based on biosensors will enable their use for clinical diagnosis needs outside of specialized laboratories. The combination of these devices with the techniques of 3D printing, microfluidic systems, nanotechnology and electrochemical detection significantly increases the usability of biosensors. Intensive research is carried out on a wide range of viruses, e.g. HIV, Ebola, influenza, hepatitis viruses. In connection with the global covid-19 pandemic, the development of nanobiosensors is currently focused primarily on the detection of SARS-CoV-2.
Conclusion: Available literature data suggest that fast sensors and biosensors have considerable clinical potential for the use in POCT.
Keywords:
nanomedicine – Nanotechnology – biosensor – medical applications – virus detection
Autoři: K. Dunovská 1; E. Klapková 1; M. Fořtová 1; J. Werle 1; J. Petrus 1; T. Grondžák 1; B. Hosnedlová 2; K. Kotaška 1
; J. Čepová 1; R. Průša 1; R. Kizek 1,2
Působiště autorů: 2. lékařská fakulta Univerzity Karlovy a Fakultní nemocnice Motol, Praha, Ústav lékařské chemie a klinické biochemie, Přednosta: prof. MUDr. Richard Průša, CSc. 1; 1. lékařská fakulta Univerzity Karlovy a Všeobecná fakultní nemocnice, Praha, Klinika pediatrie a dědičných poruch metabolismu, Přednosta: prof. MUDr. Tomáš Honzík, Ph. D. 2
Vyšlo v časopise: Prakt. Lék. 2022; 102(4): 171-176
Kategorie: Přehledy
Souhrn
Cíl: Přehledová práce poskytuje základní praktické informace o využití biosenzorů v rychlé diagnostice virových patogenů.
Výsledky: Viry díky evolučním změnám v genomu přeskakují do lidské populace, u níž vyvolávají závažné epidemie. Rychlé diagnostické nástroje POCT založené na biosenzorech umožní jejich rozpoznání pro potřeby klinické diagnostiky mimo specializované laboratoře. Kombinace těchto zařízení s technikami 3D tisku, mikrofluidních systémů, nanotechnologie a elektrochemické detekce výrazně zvyšuje využitelnost biosenzorů v laboratorní medicíně. Intenzivní nanomedicínský výzkum probíhá u celé řady virů, např. HIV, ebola, chřipka a viry hepatitid. V souvislosti s celosvětovou pandemií covid-19 se v současné době vývoj nanobiosenzorů ubírá především směrem k detekci SARS-CoV-2.
Závěr: Dostupná literární data naznačují, že rychlé senzory a biosenzory mají značný klinický potenciál pro využití v POCT.
Klíčová slova:
nanomedicína – biosenzor – lékařské aplikace – detekce virů – nanotechnologie
ÚVOD
Viry jako původci nebezpečných onemocnění představují hrozbu pro člověka i další druhy živočichů (1). Základní podmínkou pro úspěšné zastavení virové epidemie/epizoocie je identifikace nakažených jedinců a jejich následná izolace. U závažných a nově popsaných onemocnění mohou být léčebné strategie omezeny pro nedostatek vhodných analytických a diagnostických metod v dostupném biologickém materiálu. Z toho důvodu musí být hledány nové, rychlé a snadno aplikovatelné způsoby detekce patogenu, jak je známo u řady vážných virových onemocnění (obr. 1). Biodiverzita a evoluční změny virů vedou k přenosu virů ze zvířat na lidi s vysokou letalitou (jak dobře víme z epidemií viry ebola, marburg, chřipka, SARS, aj.). Nejvíce obávanými jsou onemocnění s vysokou letalitou dosahující až 100 % u vnímavých jedinců. Analyzátory POCT (point of care testing) jsou určeny pro rychlou analýzu. Způsoby detekce hledaného analytu mohou být různé, avšak řada z nich je založena na biosenzorech.
Obr. 1. Zdrojem biodiverzity jsou různá prostředí, především však tropické lesy. Identifikace nových druhů představuje výzvu. Pro rychlou identifikaci a roztřídění mohou být vhodné biosenzory. Takové postupy využívají metody molekulární biologie v jejich kombinaci s vhodnou bioanalytickou metodou. Získané informace jsou následně klíčové pro zastavení virové epidemie. 
BIOSENZORY
Biosenzor jako analytický nástroj je sestaven z rozpoznávací části, převodníku a vlastního detektoru s digitálním výstupem (2). Pro rozpoznání analytu se využívá specifických fyzikálních nebo chemických interakcí s biologickou složkou biosenzoru (3). Pomocí fyzikálně-chemického převodníku se molekulární signál změní na měřitelnou fyzikální veličinu (napětí, teplota, vodivost, fluorescence, absorbance a další). Biosenzory jsou díky svému uspořádání vhodné pro detekci biomolekul, zejména objektů o nano-/mikrovelikosti (jako proteinové biomarkery, případně celé bakterie a viry). Typické uspořádání biosenzoru s elektrochemickou detekcí je ukázáno na obrázku 2. Navíc v nanomedicínské aplikaci je vlastní biosenzor zakomponován do mikrofluidního zařízení, které může být vyrobeno technikami 3D tisku (4).
Obr. 2. Zjednodušené schéma biosenzoru s elektrochemickým detektorem. Analyt (virus) reaguje s povrchem senzoru (rozpoznávací část). Povrch senzoru je modifikován molekulami, které specificky reagují s analytem (nukleové kyseliny, protilátky, polymery apod.). Modifikace povrchu a následné reakce zodpovídají za vlastní průběh vazby. Povrch musí být upraven tak, aby se předcházelo nespecifické interakci nebo falešně pozitivním výsledkům. Po specifické interakci je fyzikálně-chemický signál přenesen přes převodník do detektoru. Dále je měřený signál matematicky zpracován. V případě elektrochemického biosenzoru probíhá na povrchu elektrody elektrochemická reakce. Ta je analyzována v detektoru pomocí různých metod. Získaný upravený signál odpovídá koncentraci analytu ve vzorku. V případě detekce viru je povrch modifikován např. molekulami DNA, RNA, PNA, LNA a dalších struktur nukleových kyselin, jako jsou aptamery, kvadruplexy. Tyto molekuly rozpoznají hledanou část viru (povrchový antigen, nukleovou kyselinu, virový protein). 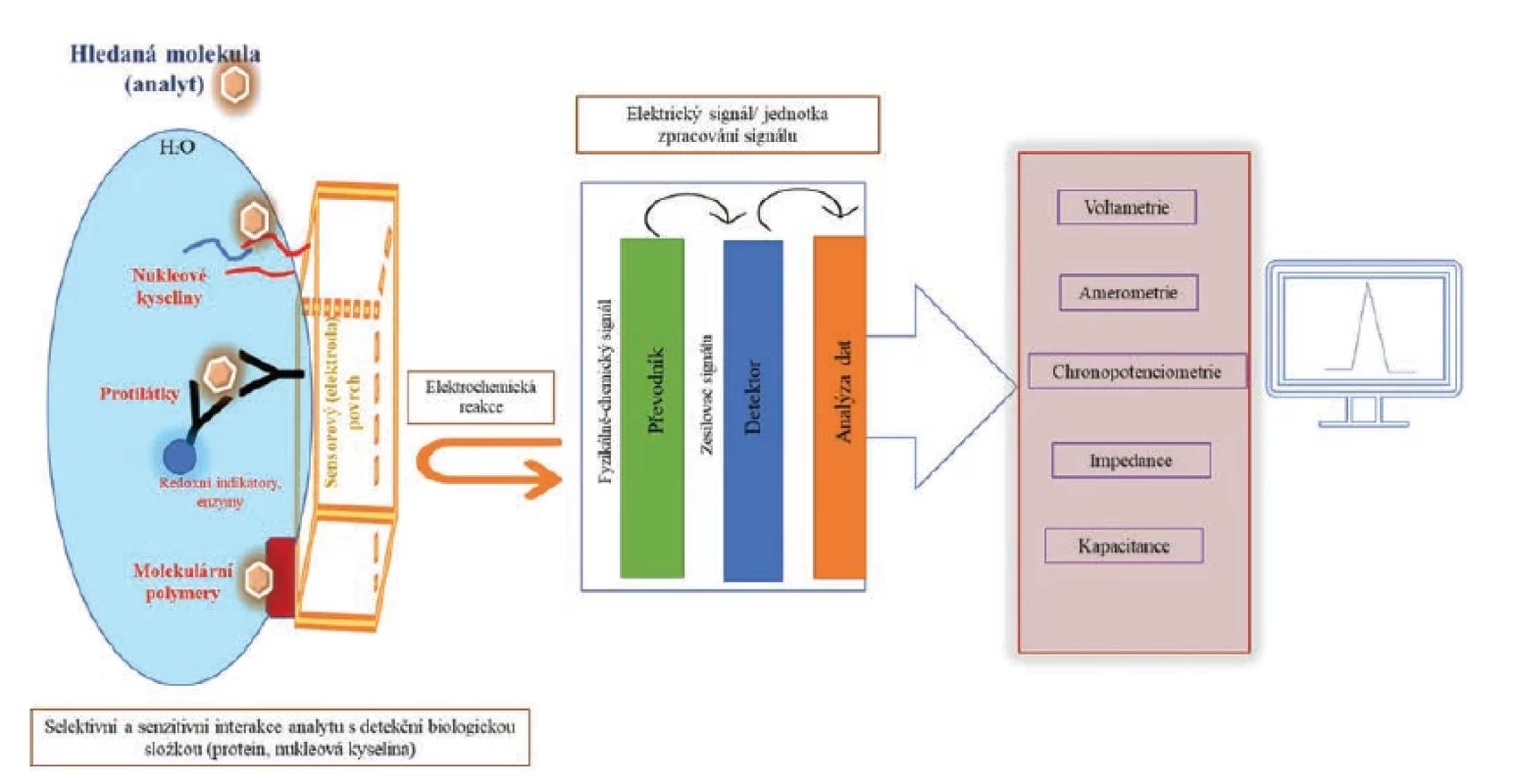
BIOSENZORY PRO VIRY
Vlastní bioanalytické způsoby detekce virů jsou trvalou výzvou. Biosenzor může detekovat virus buď přímo (jeho nukleovou kyselinu, povrchový či strukturní protein), nebo nepřímo na základě reakce hostitele na infekci (změny hladiny určitých biochemických markerů)(5). Takové výzvy detekce lze klasifikovat podle biologických vlastností analytu (nízký počet přítomného biologického činitele a biologické matrice), případně technologických omezení (specifičnost, mez detekce, lineární dynamický rozsah, stabilita a spolehlivost). Identifikace je možná jejich přímým pozorováním pod elektronovým mikroskopem, reakcemi se specifickou protilátkou, ale především potvrzením přítomnosti genomové nukleové kyseliny. K tomuto cíli je možné přistoupit nanomedicínsky, jak je ukázáno na obrázku 3. V literatuře je popsána řada návrhů biosenzorů pro rozpoznání přítomnosti virových patogenů. S ohledem na pandemii HIV jsou zkoumány biosenzory pro detekci přítomnosti virové nukleové kyseliny (6). Limity detekce HIV nukleové kyseliny se pohybují v jednotkách femtomolárních koncentrací (3). Mezi další pandemické virové patogeny se značným dopadem na veřejné zdraví jsou viry hepatitidy. Zde jsou zkoumány biosenzory jak nukleových kyselin, tak povrchové proteiny. Limity detekce sledované biomolekuly se opět pohybují v jednotkách femtomolárních koncentrací (3). Viry jako ebola, zika, noroviry, chřipka a dengue jsou se zájmem studovány s ohledem na jejich rychlé šíření v populaci a vysokou letalitu. Biosenzory jsou zaměřeny na potvrzení přítomnosti nukleové kyseliny nebo přítomnosti povrchového proteinu. Limity detekce virové nukleové kyseliny se pohybují v rozsahu jednotek nanomolárních až femtomolárních koncentrací (3). Izolace genomové nukleové kyseliny je kritickým bodem v následné identifikaci viru. Jsou hledány různé způsoby jak virovou částici rozvolnit, a uvolnit tak nukleovou kyselinu (7). Pro zkoncentrování nukleové kyseliny ze vzorku lze využívat modifikovaných magnetických nanočástic (SPION). Na obrázku 4 je ukázána SPION částice (nese na svém povrchu kladný náboj) pro vazbu virové genomové nukleové kyseliny. Množství přítomné nukleové kyseliny je pro další analýzy často velmi malé, proto je klíčové využít metodu polymerázové řetězové reakce (PCR) k jejímu namnožení. Při klasickém uspořádání je však nevýhodou nutnost využívat cyklické změny teploty. Tyto nevýhody mohou odstranit způsoby amplifikace založené na LAMP technice za mírně zvýšené nebo běžné laboratorní teploty (8). DNA jako elektroaktivní molekulu pak lze pomocí elektrochemie stanovit ve velmi nízkých koncentracích (9). Kromě toho lze určit sekvenci přímým sekvenováním, což není zatím vhodné pro POCT využití, ale otevírají se možnosti nanopórového sekvenování a sekvenování na čipech (10, 11). Pro účely prokázání přítomnosti virových proteinů je využíváno různě značených monoklonálních protilátek k těmto strukturám. Nejpoužívanější je systém avidin/streptavidin-enzym a následná barevná reakce po vygenerování peroxidu vodíku. Kromě toho jsou využívány další způsoby značení včetně fluorescenčního (kvantové tečky, europium apod.). Elektroaktivita značky může být využita pro elektrochemické rozpoznání přítomnosti antigenu (ruthenium, zinek, měď, kadmium, a případně další elektroaktivní molekuly) (2).
Obr. 3. Využití magnetických nanočástic pro identifikaci virového patogenu. Virová nukleová kyselina je za využití SPION (superparamagnetické nanočástice oxidů železa) s kladným nábojem zachycena z roztoku. V případě, že je zachycen celý virion (SPION částice lze modifikovat protilátkou k povrchovým strukturám viru), následuje uvolnění nukleové kyseliny. Nukleová kyselina může být detekována přímo (bez specifické amplifikace) nebo je dále amplifikována pomocí PCR. SPION mohou být využity jako polyfunkční struktury, tedy na povrchu je možné rozpoznat jak nukleovou kyselinu, tak přítomnost povrchových antigenů. Biobarkódování tak zvyšuje senzitivitu a selektivitu rozpoznání přítomnosti hledaného viru (28). 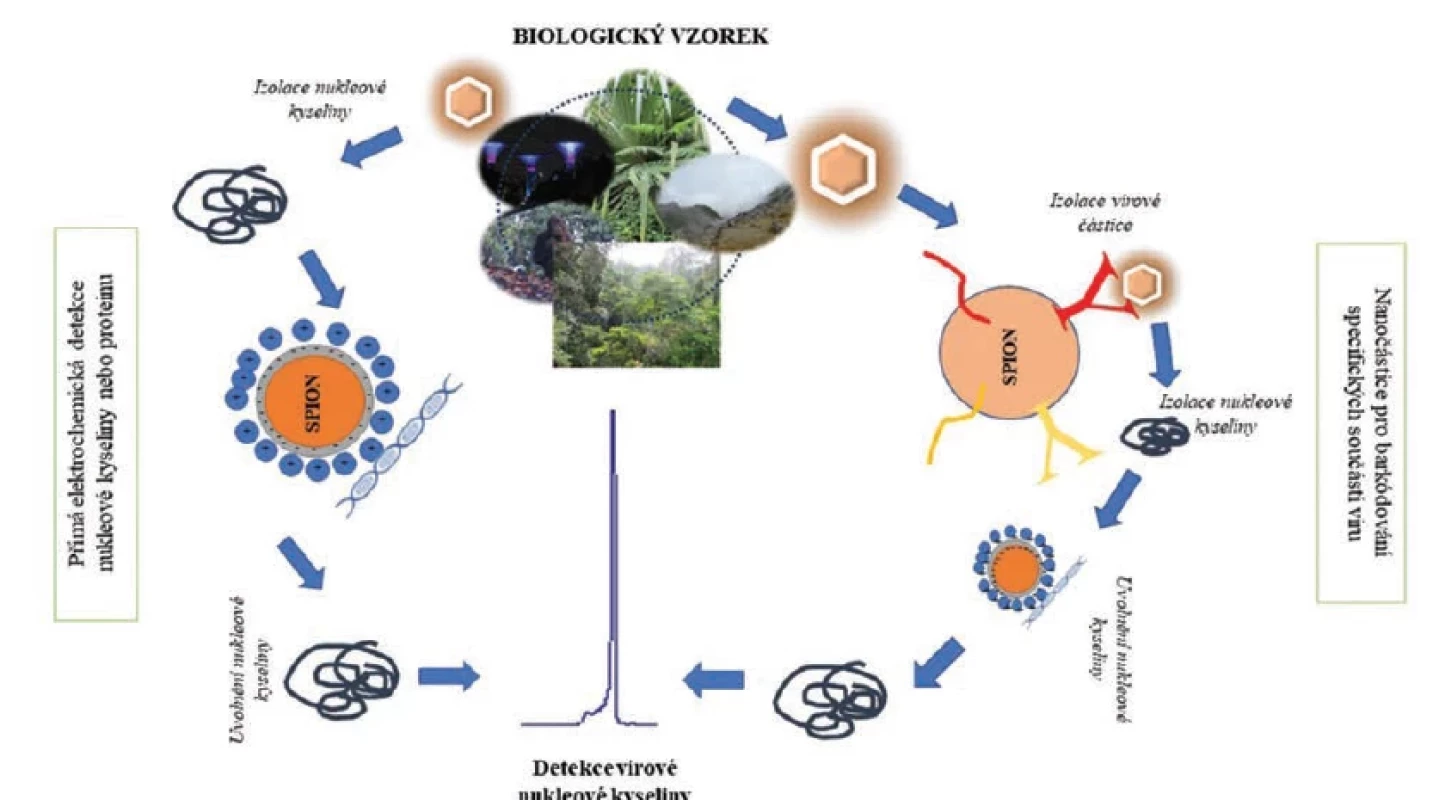
Obr. 4. SPION nanočástice pro zachycení nukleové kyseliny. SPION nanočástice nesou na svém povrchu kladný náboj, a tak mohou zachytit nukleovou kyselinu (nese záporný náboj) (7). Nukleové kyseliny jsou dobrými vodiči a jejich přítomnost lze určit za pomocí elektrochemického stanovení. 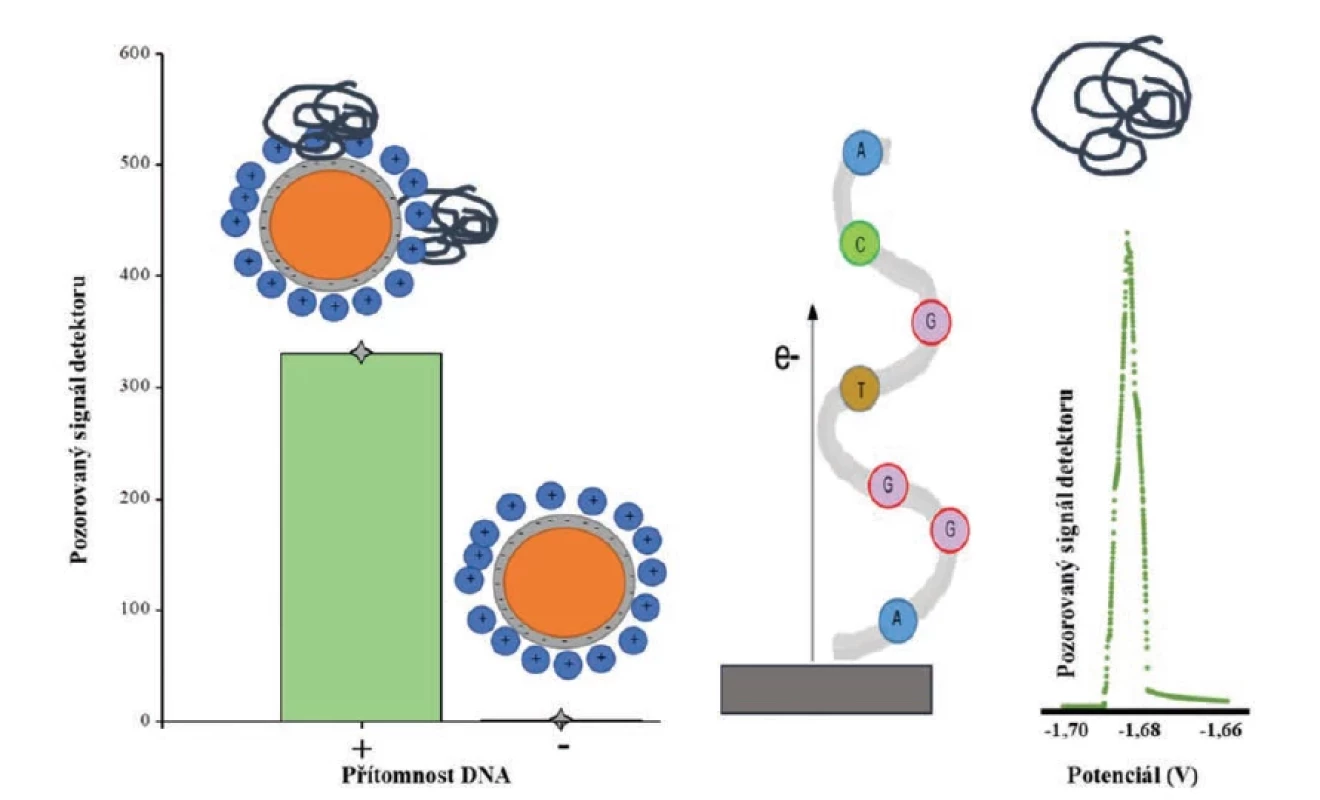
BIOSENZORY PRO KORONAVIRY
Nově popsaný virus (v roce 2019) ze skupiny koronavirů způsobil globální pandemii s vysokým počtem hospitalizovaných s těžkým akutním respiračním onemocněním a smrtností kolem 1–5 % (12, 13). SARS-CoV-2 je jednovláknový RNA ((+)ssRNA) virus, který je původcem již více než 2 roky trvající pandemie. Navzdory značnému úsilí zůstávají možnosti terapie onemocnění covid-19 poměrně limitované. Koronavirus SARS-CoV-2 (těžký akutní respirační syndrom koronavirus 2) se přenáší kapénkami. V respiračním traktu vstupuje do buněk přes ACE2 receptory se spoluúčastí (TLR)2 receptorů (14). Vzhledem k tomu, že se objevil tento nový koronavirus, výzkumné úsilí se zaměřilo na vývoj detekčních testů, včetně vývoje nanobiosenzorů, které by mohly být vysoce účinné při jeho detekci (15). Přístupy k detekci SARS - -CoV-2, včetně možného použití platformy smartphonu připojené k senzorům a použití protokolu RT-LAMP byly diskutovány v práci Laghrib et al. (16). Detekci je také možné zaměřit na protein S1 MERS-CoV na multiplexním poli elektrod (17). Intenzivně je rozvíjeno použití modifikovaných magnetických nanočástic s polyklonální a následně detekční monoklonální protilátkou. Nakonec je protilátka značena enzymem – alkalickou fosfatázou, která štěpí 1-naftyl fosfát na 1-naftol, který je elektrochemicky aktivní a poskytuje velmi dobrý voltametrický a/nebo amperometrický signál. Metoda má dobrou reprodukovatelnost a byla aplikována na skutečné vzorky slin (18). Elektrody mohou být modifikovány různými typy nanočástic, jako jsou oxidy grafenu nebo zlaté nanočástice a následně je virový glykoprotein analyzován na vhodném detektoru (19). Byl navržen čip se čtyřmi AuNP (zlaté nanočástice) modifikovanými specifickými oligonukleotidy pro virovou sekvenci. Tato sonda byla poté přenesena na papírovou elektrochemickou platformu (zlatá elektroda). Citlivost metody byla prokázána především na sekvenci SARS-CoV-2 v relativně krátkém časovém okně řádu minut (20). Zajímavý koncept návrhu biosenzoru představuje možnost, kdy je na povrch elektrody navázán N protein. K reakční směsi se následně přidá protilátka proti proteinu N. Pokud není přítomen virus SARS, protilátka se váže přímo na N protein. Pokud je do roztoku přidán vzorek se SARS, virový protein se naváže na protilátku. Protilátka se již tedy nemůže vázat na N protein. V případě konkurence s protilátkou odpovídá sledovaný signál nepřímo úměrně přítomnosti viru (21).
NANOTECHNOLOGIE NA VZESTUPU
Převedení biosenzorů z laboratoře do reálného klinického využití vykazuje některé potíže, které vedou k vlastní nespolehlivosti systému. To by mohly odstranit matematické a statistické postupy. Malá chytrá zařízení (POCT) jsou vhodná pro automatizaci detekce nebezpečného patogenu (22, 23). Kromě toho využití technologie 3D tisku výrazně zrychluje možnosti jejich praktického použití (24). To se ukazuje užitečné u vážných onemocnění jako chřipka, ebola, SARS či MERS. Technologie jsou potřebné pro naléhavé situace a prospěšné jak pro pacienty, tak pro poskytovatele zdravotní péče (25). SARS pandemie způsobila výrazné zrychlení alternativních způsobů léčby, diagnostiky a zabránění vstupu viru. Byla již připravena řada nanotechnologických produktů (roušky, dezinfekce, úpravy povrchů, čističe vzduchu a další). Využívá se polymerních, metalických, lipidových a magnetických nanočástic, liposomů, grafenu, nanovláken pro koncepty senzorů a biosenzorů (12). Velmi rozšířeným se staly jednoduché diagnostické testy. Test využívá typicky protilátky značené zlatými, uhlíkovými nebo barevnými latexovými částicemi na nitrocelulózové membráně. Přítomnost hledaného antigenu nebo nukleové kyseliny se projeví jako zóna agregace nanočástic (vzniká barevný proužek) (26, 27).
ZÁVĚRY PRO KLINICKOU PRAXI
Nanomedicína je rychle se rozvíjející biomedicínský obor. Automatizovaná, chytrá zařízení (POCT) umožní identifikaci patogenu v místě rozhodování. POCT systémy založené na elektrochemických biosenzorech takto mohou rychle reagovat na potřeby klinické diagnostiky přímo mimo specializované laboratoře (v ordinacích praktických lékařů, na urgentních příjmech, u záchranných složek apod.).
Práce byla řešena jako součást institucionální podpory MZ ČR – RVO, FN v Motole 00064203.
Konflikt zájmů: žádný.
adresa pro korespondenci:
prof. Ing. René Kizek, PhD., DrSc., MBA
Ústav lékařské chemie a klinické biochemie
2. LF UK a FN Motol
V Úvalu 84, 150 06 Praha 5
e-mail: kizekrene@gmail.com
Zdroje
1. Banas D, Aksu DA, Noguera MV, et al. Electrochemical study of quantum dots-labeled oligonucleotide probes for detecting nucleic acid of African swine fever virus. Chem Listy 2020; 114(11): 778–783.
2. Skládal P. Advances in electrochemical immunosensors for pathogens. Cur Opin Electrochem 2019; 1466–1470.
3. Saylan Y, Erdem Ö, Ünal S. et al. An alternative medical diagnosis method: biosensors for virus detection. Biosensors 2019; 9(2): 65.
4. Monia Kabandana GK, Zhang T, Chen C. Emerging 3D printing technologies and methodologies for microfluidic development. Anal Method 2022; 14(30): 2885–2906.
5. Hushegyi A, Pihikova D, Bertok T, et al. Ultrasensitive detection of influenza viruses with a glycan-based impedimetric biosensor. Biosens Bioelectron 2016; 79(5): 644–649.
6. Rodrigo MAM, Heger Z, Cernei N, et al. HIV biosensors - the potential of the electrochemical way. Int J Electrochem Sci 2014; 9(7): 3449–3457.
7. Banas D, Rychly O, Salmistraro S, et al. Optimization of nucleic acid binding to magnetic particles with the aim of detection of dangerous viruses. 12th International Conference on Nanomaterials – Research and Application (NANOCON) 2020; 324–329.
8. Parida M, Sannarangaiah S, Dash PK, et al. Loop mediated isothermal amplification (LAMP): a new generation of innovative gene amplification technique; perspectives in clinical diagnosis of infectious diseases. Rev Med Virol 2008; 18(6): 407–421.
9. Slinker JD, Muren NB, Renfrew SE, et al. DNA charge transport over 34 nm. Nat Chem 2011; 3(3): 228–233.
10. Wang YH, Zhao Y, Bollas A, et al. Nanopore sequencing technology, bioinformatics and applications. Nat Biotechnol 2021; 39(11): 1348–1365.
11. Lockhart DJ, Dong HL, Byrne MC, et al. Expression monitoring by hybridization to high-density oligonucleotide arrays. Nat Biotechnol 1996; 14(13): 1675–1680.
12. Tavares JL, Cavalcanti IDL, Santos Magalhães NS, et al. Nanotechnology and COVID-19: quo vadis? J Nanopart Res 2022; 24(3): 62.
13. Gorbalenya AE, Baker SC, Baric RS, et al. The species Severe acute respiratory syndrome-related coronavirus: classifying 2019-nCoV and naming it SARS-CoV-2. Nat Microbiol 2020; 5(4): 536–544.
14. Petrus J, Dunovska K, Klapkova E, et al. Infekce virem SARSCoV-2 u dětí se zhoubnými nádory: léčba remdesivirem. Prakt. Lék. 2022; 102(1): 6–12.15. Alhalaili B, Popescu IN, Kamoun O, et al. Nanobiosensors for the detection of novel coronavirus 2019-nCoV and other pandemic/epidemic respiratory viruses: a review. Sensors 2020; 20(22): 6591
16. Laghrib F, Saqrane S, El Bouabi Y, et al. Current progress on COVID-19 related to biosensing technologies: New opportunity for detection and monitoring of viruses. Microchem J 2021; 160 : 105606.
17. Layqah LA, Eissa S. An electrochemical immunosensor for the corona virus associated with the Middle East respiratory syndrome using an array of gold nanoparticle-modified carbon electrodes. Microchim Acta 2019; 186(4): 224.
18. Fabiani L, Saroglia M, Galata G, et al. Magnetic beads combined with carbon black-based screen-printed electrodes for COVID-19: A reliable and miniaturized electrochemical immunosensor for SARS-CoV-2 detection in saliva. Biosens Bioelectron 2021; 171(1): 112686.
19. Hashemi SA, Golab Behbahan NG, Bahrani S, et al. Ultrasensitive viral glycoprotein detection NanoSystem toward accurate tracing SARS-CoV-2 in biological/non-biological media. Biosens Bioelectronics 2021; 171(1): 112731.
20. Alafeef M, Dighe K, Moitra P, et al. Rapid, ultrasensitive, and quantitative detection of SARS-CoV-2 using antisense oligonucleotides directed electrochemical biosensor chip. ACS nano 2020; 14(12): 17028–17045.
21. Eissa S, Zourob M. Development of a low-cost cotton-tipped electrochemical immunosensor for the detection of SARS-CoV-2. Anal Chem 2020; 93(3): 1826–1833.22. Gargulak M, Docekalova M, Kepinska M, et al. 3D-printed CdTe QDs-based sensor for sensitive electrochemical detection of viral particles. IEEE Inter Conf Sens. Nanotechnol 2019; 125–128.
23. Krejcova L, Dospivova D, Ryvolova M, et al. Paramagnetic particles coupled with an automated flow injection analysis as a tool for influenza viral protein detection. Electrophoresis 2012; 33(21): 3195–3204.
24. Krejcova L, Nejdl L, Rodrigo MAM, et al. 3D printed chip for electrochemical detection of influenza virus labeled with CdS quantum dots. Biosens Bioelectron 2014; 54(4): 421–427.
25. Krejcova L, Hynek D, Adam V, et al. Electrochemical sensors and biosensors for influenza detection. Int J Electrochem Sci 2012; 7(11): 10779–10801.
26. Whitman JD, Hiatt J, Mowery CT, et al. Evaluation of SARSCoV-2 serology assays reveals a range of test performance. Nat Biotechnol 2020; 38(10): 1174–1178.
27. Turbe V, Herbst C, Mngomezulu T, et al. Deep learning of HIV field-based rapid tests. Nat Med 2021; 27(7): 1165–1168.
28. Krejcova L, Hynek D, Kopel P, et al. Development of a magnetic electrochemical bar code array for point mutation detection in the H5N1 neuraminidase gene. Viruses-Basel 2013; 5(7): 1719–1739.Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2022 Číslo 4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Nanomedicínský přístup pro rychlou identifikaci virů za využití elektrochemických biosenzorů
- Různorodost pohledů na problematiku dopravních úrazů
- Nižší náklady na péči u venkovských všeobecných praktických lékařů – známka efektivity nebo varování?
- Problematika ošetřovatelské péče u sester v první linii během pandemie covid-19
- Potápění na nádech: nutná velká ostražitost, může jít o život!
- K problematice povinného očkování v první Československé republice
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Potápění na nádech: nutná velká ostražitost, může jít o život!
- Problematika ošetřovatelské péče u sester v první linii během pandemie covid-19
- K problematice povinného očkování v první Československé republice
- Nižší náklady na péči u venkovských všeobecných praktických lékařů – známka efektivity nebo varování?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



