-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Současné možnosti diagnostiky a léčby ohraničených chrupavčitých lézí nosných kloubů
Current possibilities of diagnostics and treatment of cartilaginous lesions of weight-bearing joints
Hyaline articular cartilage injuries of weight-bearing joints present for the patient a serious condition, that if left undiagnosed and treated appropriately, can lead to premature development of arthritis and permanent functional limitations. Articular surface damage can be seen in patients of all ages and may be clinically silent for a long time or present with non-specific symptoms. A general practitioner is often the first who comes into contact with patients after a large joint injury. Therefore, in addition to the more frequent cases of common contusions, distortions, ligament or meniscus injuries, should also consider the possibility of joint cartilage damage. The following article gives an overview of current possibilities of diagnosis and treatment of this orthopaedic-traumatological problematics.
Keywords:
magnetic resonance – hyaline cartilage – chondral defect – knee – ankle
Autoři: T. Otaševič 1; A. Šprláková-Puková 2
Působiště autorů: Ortopedická klinika FN Brno a LF MU, Brno, Přednosta: prof. MUDr. Martin Repko, Ph. D. 1; Klinika radiologie a nukleární medicíny LF MU a FN, Brno, Přednosta: prof. MUDr. Vlastimil Válek, CSc., MBA 2
Vyšlo v časopise: Prakt. Lék. 2020; 100(3): 107-112
Kategorie: Přehledy
Souhrn
Poranění hyalinní kloubní chrupavky nosných kloubů představuje pro daného jedince závažný stav, který, pokud zůstane nediagnostikován a adekvátně léčen, může vést k rozvoji předčasné artrózy a trvalému funkčnímu omezení. S poškozením kloubního povrchu je možné se setkat u pacientů všech věkových kategorií, přičemž může být dlouho klinicky němé nebo se projevovat nespecifickými příznaky. Praktický lékař je často první, který s pacienty po úrazu velkých kloubů přijde do kontaktu. Měl by proto, kromě častějších případů běžných kontuzí, distorzí, poranění vazů nebo menisků, myslet také na možnost poškození kloubní chrupavky. Následující článek podává přehled o současných možnostech diagnostiky a léčby této ortopedicko-traumatologické problematiky.
Klíčová slova:
hyalinní chrupavka – chondrální defekt – magnetická rezonance – koleno – hlezno
ÚVOD
Hyalinní kloubní chrupavka je specializovaná pojivová tkáň kryjící v kloubech povrch kosti a vzhledem ke své struktuře slouží jako tlumič nárazů, zajišťuje rovnoměrnou distribuci námahy a umožňuje hladký bezbolestný pohyb (1). Kloubní chrupavka není, na rozdíl od jiných lokalit, kryta pevným vazivovým perichondriem, ze kterého probíhá výživa, což výrazně omezuje její regenerační schopnosti. Proto každé poranění či poškození hyalinní chrupavky nosných kloubů je nutné považovat za závažný stav, který může vést k předčasnému rozvoji artrózy a tím k významnému funkčnímu omezení a snížení kvality života daného jedince. V posledních třech dekádách došlo k velkému rozvoji technik umožňující jednak přesnější diagnostiku poškozeného kloubního povrchu pomocí magnetické rezonance, jednak technik k ošetření poškozeného kloubního povrchu. Na straně druhé, vzhledem ke zvyšující se aktivitě a věku populace roste výskyt úrazů i degenerativních změn nosných kloubů. Ke vzniku ohraničeného defektu kloubního povrchu může dojít na podkladě akutního traumatu – sportovní úrazy, autonehody, pracovní úrazy nebo vzniká následkem disekující osteochondronekrózy. U starších pacientů pak převládají defekty vznikající na podkladě degenerativního procesu.
DIAGNOSTIKA POŠKOZENÉ KLOUBNÍ CHRUPAVKY
Anamnéza a klinické vyšetření
V případě úrazového děje v anamnéze zjišťujeme okolnosti a mechanismus úrazu, přítomnost otoku, bolesti. U neúrazové anamnézy pátráme po době trvání potíží, charakteru bolestí, předchozích úrazech, pracovní a sportovní aktivitě. Klinickými projevy poškozené kloubní chrupavky mohou být bolesti, hlavně zátěžové, otoky, omezení hybnosti a funkce kloubu. Často však chondrální léze zůstávají dlouho klinicky němé a jsou pak náhodným nálezem na zobrazovacích metodách nebo při artroskopii kolene prováděné z důvodu poraněného menisku nebo vazů. Při klinickém vyšetření daného kloubu je vhodné posouzení tvarových abnormalit, osových úchylek na dolních končetinách, přítomnost výpotku, pohybu, lokalizujeme místa největší bolesti. Jednoznačné provokační manévry na zjištění chondrální patologie však neexistují.
Zobrazovací metody
Rentgenový snímek
Rentgenový snímek patří mezi základní zobrazovací metody při podezření na změny degenerativní. Vlastní chrupavku nemůžeme na snímku zobrazit, patrné jsou však jiné změny, které mohou provázet její případné poškození, např. zúžení kloubní štěrbiny, okrajové osteofyty či změny subchondrální kosti.
Snímek z takovéto indikace je vhodné provádět v zátěži, vstoje, důvodem je zejména skutečný stav šíře kloubní štěrbiny a přesnější detekce jejího zúžení. Rovněž se lépe detekuje skutečné osové postavení jednotlivých kloubních členů. Snímek se vždy provádí v předozadní a boční projekci. Pro zhodnocení stupně degenerativních změn se používá Lawrence-Kellgrenova klasifikace, které má pět stupňů – od normálního nálezu až po nejtěžší deformační změny.
Dalším patologickým stavem, který souvisí s poškozením chrupavky, je osteochondrální defekt. V tomto případě lze na rentgenovém snímku patologické kostní změny detekovat a popsat velikost defektu a rovněž uložení případného kostního fragmentu. Jiná situace může být u subchondrálních fraktur, kdy může být běžné rentgenové vyšetření zcela negativní a příčinu potíží neodhalí. V takovémto případě je vhodné zvolit jinou diagnostickou metodu, např. magnetickou rezonanci.
Magnetická rezonance
Magnetická rezonance (MR) je tomografická metoda, jejíž použití je v indikaci mnoha patologických stavů již velmi dobře známé. V obraze magnetické rezonance zobrazujeme přímo tkáň hyalinní chrupavky (2). Vhodně zvoleným způsobem vyšetření se tak můžeme, i při běžném vyšetření jakéhokoliv kloubu, vyjádřit k její morfologii.
Pro správné zobrazení je nutné příslušné vybavení pracoviště, povrchová cívka a správná volba vyšetřovacího protokolu. K zobrazení chrupavky jsou klíčové zejména sekvence protonové denzity či T2 vážení, nejlépe v kombinaci se saturací tukové tkáně. Vyšetření by mělo zahrnovat nejen 2D sekvence, ale i 3D sekvenci, nejlépe s izotropním rozlišením.
Velkou výhodou zobrazování chrupavky MR je právě nejen její přímé zhodnocení, ale i přehlednost změn subchondrálních, které nejsou při artroskopickém vyšetření patrné. Mezi subchondrální změny, které poškození chrupavky provázejí, patří zejména edém kostní dřeně, který je v MR obraze velmi dobře patrný a hodnotitelný. V současné době se navíc nabízí řada dalších možností jak neinvazivně hodnotit nejen morfologii, ale i biochemické složení chrupavky. K tomu je však nutné využít některé ze speciálních metod zobrazení, které nejsou součástí běžného vyšetření (3).
Nejvíce využívanou technikou je T2 mapování zejména v rámci různých studií. Další možností je vyšetření po aplikaci kontrastní látky – dGEMRIC (delayed Gadolinium-Enhanced MRI of Cartilage) sekvence, metoda náročná časově a rovněž se specifickými nároky na zpracování, nicméně bez nutnosti zvláštního vybavení (speciální cívky či přístroje s vyšším magnetickým polem). Ostatní možnosti – T1rho, zobrazení sodíku, gagCEST či difuzní vážení – nejsou běžně využívány, jsou vázány na specifické vybavení a jejich použití je součástí vědeckých projektů
Nevýhodou MR vyšetření je délka jejího trvání, nejčastěji kolem 30 minut. Po tuto dobu je nutná spolupráce pacienta, během vyšetření je nutné eliminovat pohyb vyšetřované části. Dále je nutné si uvědomit, že silnému magnetickému poli je vystaven celý pacient, nejen vyšetřovaná část. Musí být tak dodrženy bezpečnostní podmínky, z kterých vyplývají kontraindikace k vyšetření. Kontraindikace dělíme na absolutní, kdy pacienta vyšetřit bezpečně nelze, a relativní, kdy za určitých podmínek pacient vyšetření absolvovat může (tab. 1).
Tab. 1. Absolutní a relativní kontraindikace MR vyšetření 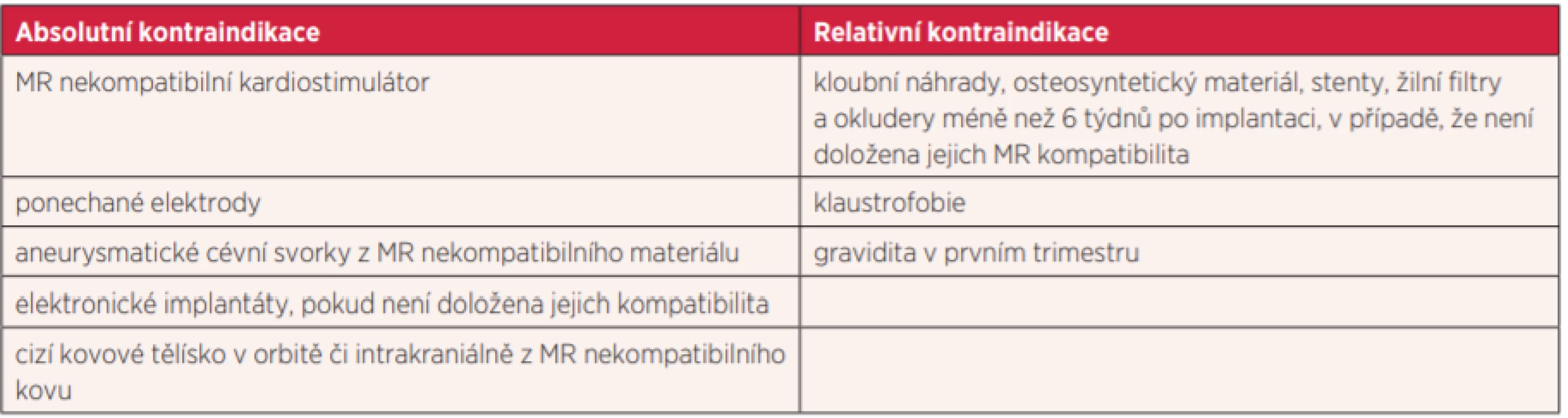
Odesílající lékař by rovněž měl mít na paměti, že pacient s MR kompatibilním kardiostimulátorem může být vyšetřen v případě, že je kardiostimulátor uveden do MR kompatibilního modu. Tento výkon provádí před vyšetřením kardiolog, který rovněž vystaví pacientovi potvrzení o tomto výkonu a po vyšetření jej opět uvede do původního nastavení.
Ultrazvukové vyšetření
I když je tato metoda velmi rozšířená a lehce dostupná, při detekci vlastních chondrálních změn nemá žádný přínos. Ultrazvukem není možné spolehlivě hodnotit kloubní povrch krytý hyalinní chrupavkou. V některých částech kloubu (např. oblast femorálního sulku) je sice přehlednost dobrá, nicméně k bezpečnému zhodnocení stavu chrupavky to nestačí. Ultrazvukem tak lze diagnostikovat např. zvýšený podíl tekutiny v kloubu, který může patologické stavy chrupavky provázet, zmnožení synoviální výstelky a případné osteoproduktivní změny při okrajích kloubních ploch. Nelze však provést žádnou spolehlivou klasifikaci, tak jako např. na RTG snímku.
Počítačová tomografie
Počítačová tomografie (CT) má v případě zobrazení hyalinní chrupavky okrajový význam. Přímo chrupavku zobrazit nelze. Na CT lze zobrazit některé subchondrální změny a změny při okrajích kloubních ploch. Výšku chrupavčité vrstvy a případný defekt lze zobrazit pomocí CT artrografie, nicméně tato metoda vzhledem k možnosti vyšetření magnetickou rezonancí ztrácí význam.
Artroskopie
Artroskopie (ASK) je mini invazivní operační technika, při které je do kloubu přes malé vstupy zaveden artroskop, který převádí obraz z kloubu na monitor, a nejrůznější operační endoskopické nástroje. Při artroskopii je možné přesně posoudit stav chrupavek, stupeň jejich opotřebení, velikost, lokalizaci a hloubku chondrálních defektů (obr. 1).
Obr. 1. ASK nález chondrálního defektu mediálního kondylu femuru pravého kolene 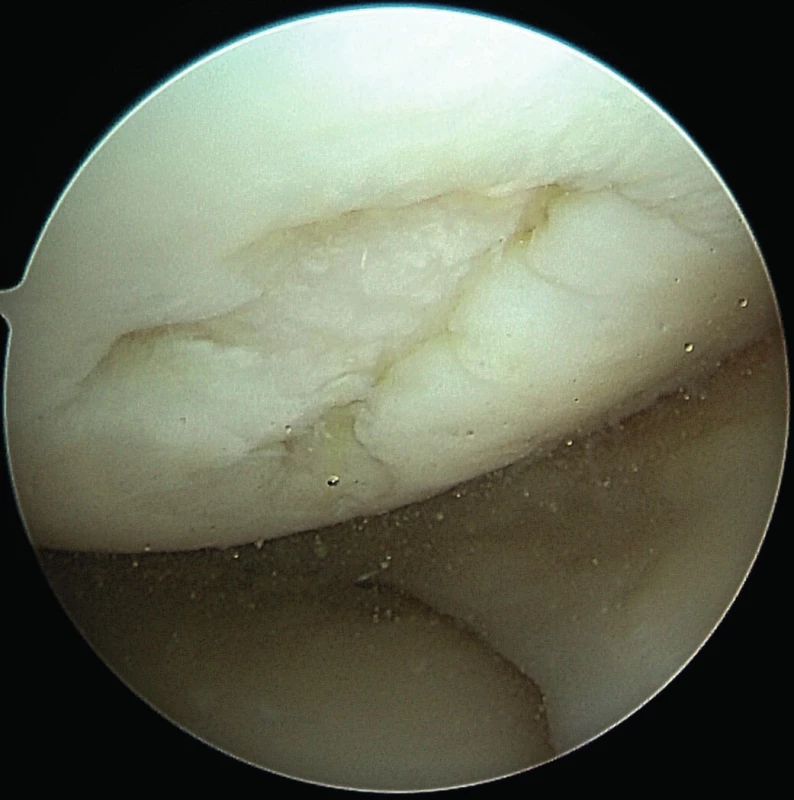
LÉČBA CHONDRÁLNÍCH DEFEKTŮ
Vzhledem k velmi omezené regenerační a reparační schopnosti hyalinní kloubní chrupavky představuje léčba chondrálních lézí jednu z obtížných oblastí ortopedie. Za obecný cíl všech léčebných postupů je možné považovat snahu, aby v místě chondrálního defektu došlo k vytvoření tkáně co nejvíce podobné původní hyalinní chrupavce (tzv. hyaline-like tissue) a tím došlo k obnovení hladkého kloubního povrchu, umožňující bezbolestný pohyb. Terapeutické postupy dělíme na konzervativní a operační.
Konzervativní léčba
Neoperační léčebné postupy mají efekt hlavně u povrchových chondrálních lézí a jako doplňková léčba chirurgických postupů u hlubokých defektů. Řadí se zde perorální přípravky ze skupiny tzv. SYSADOA (Symptomatic Slow Acting Drugs of Osteoarthritis), dříve označované jako chondroprotektiva – glukosamin sulfát, chondroitin sulfát, diacerein, ASU (Avocado and Soybean Unsaponifiables) – výtažky z avokáda a sóji. Dalším hojně využívaným přípravkem je intarartikulární aplikace kyseliny hyaluronové (HA), tzv. viskosuplementace. Novější metodou je intraartikulární aplikace autologní plazmy obohacené o trombocyty – A-PRP (Autologous-Platelet Rich Plasma).
Operační léčba
Chirurgické postupy se využívají v případě hlubokých chondrálních a osteochondrálních lézí. V současné době je využíváno několik technik, každá má své indikace i limity použití. U všech technik ošetření lokalizovaných chrupavčitých lézí je nutné dodržovat základní indikační kritéria – horní věková hranice 50–60 let, optimální je do 40 let, přítomnost nejvýše II. stupně artrózy na RTG dle Lawrence-Kellgrena a nejvýše II. stupně chondropatie na okolní chrupavce při artroskopickém vyšetření, nutnost ošetření dalších nitrokloubních patologií společně s ošetřením chrupavky, např. ošetření poraněných vazů, menisků, osových deformit atd.
Debridement
Debridement neboli očištění, zahlazení je nejjednodušší chirurgická metoda prováděná při artroskopii daného kloubu, spočívající v odstranění poškozených, odlučujících se nebo volných částí chrupavky. Provádí se mechanicky pomocí rotační frézy – shaveru nebo pomocí bipolárních radiofrekvenčních nástrojů. S debridementem souvisí také tzv. lavage kloubu – odstranění nitrokloubní tekutiny obsahující chrupavčitý detritus, tedy výplach kloubu. Použití těchto postupů má význam hlavně u povrchových lézí, eventuálně jako záchovný výkon u pokročilejších stupňů poškození kloubní chrupavky (4).
Metody stimulující kostní dřeň – návrty a mikrofraktury spodiny defektu
Principem těchto postupů je rozrušení subchondrální kosti na spodině defektu, ze které dojde ke krvácení a vyplavení pluripotentních kmenových buněk a dalších biologických faktorů z kostní dřeně (obr. 2). V místě defektu se vytvoří tzv. fibrinová zátka, ve které dochází k přeměně kmenových buněk v chondrocyty, které dále vytvářejí novou fibrokartilaginózní tkáň, obsahující směs hyalinní a vazivové chrupavky. Návrty a mikrofraktury se provádějí při artroskopii postiženého kloubu. Tyto metody jsou na většině pracovišť považovány za zlatý standard v léčbě ohraničených chondrálních lézí. Nejlepší výsledky mají u malých defektů do 2–2,5 cm2 a mladých pacientů do 40 let (5, 6). U velkých defektů a starších pacientů poskytují špatné výsledky.
Obr. 2. Mikrofraktury chondrálního defektu mediálního kondylu femuru levého kolene: a – stav po provedení debridementu spodiny a okrajů defektu, b – stav po provedení mikrofraktur spodiny pomocí šídla 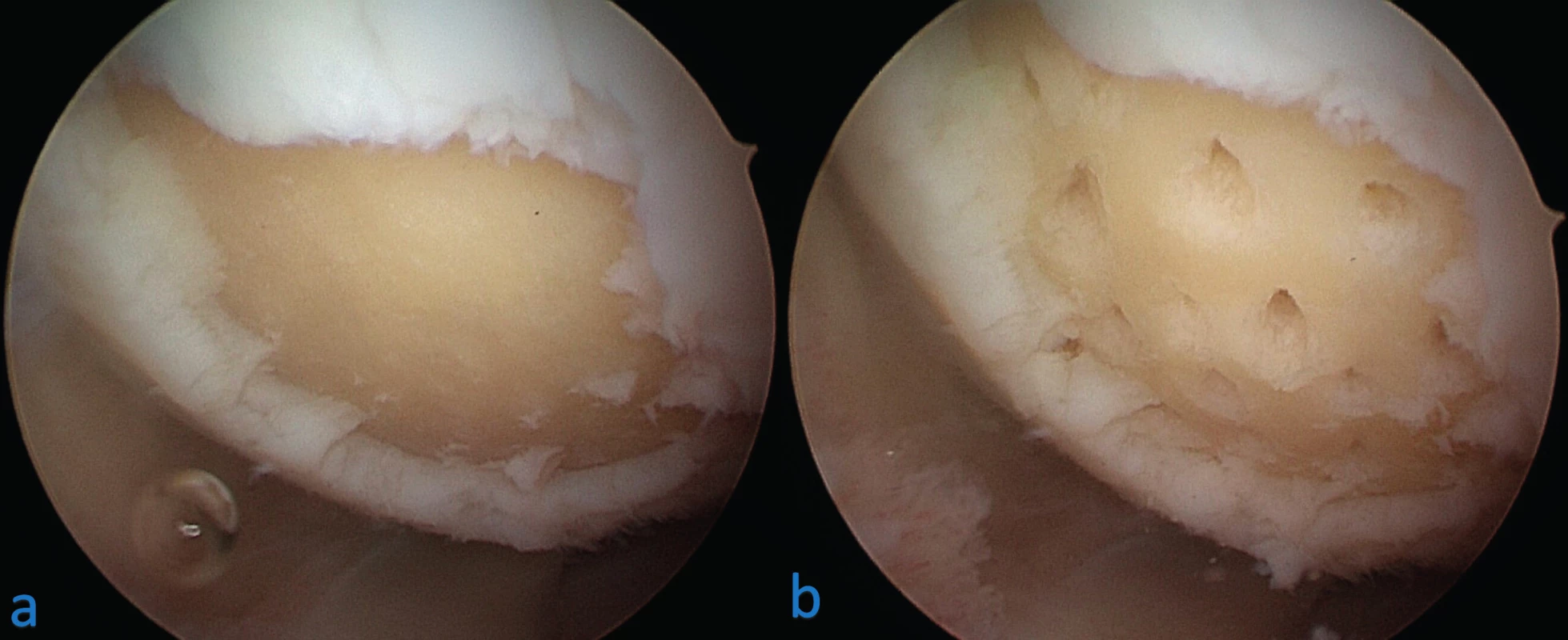
Autologní osteochondrální štěpy
Autologní ostechondrální štěpy se používají ve formě tzv. mozaikové plastiky, kdy se z nezátěžové plochy kloubu odebírají osteochondrální bločky, které se následně transplantují do místa chondrálního nebo osteochondrálního defektu (obr. 3). Poskytuje dobré výsledky u ohraničených lézí velikosti 2–4 cm2 (7).
Obr. 3. Mozaiková plastika mediálního kondylu femuru pravého kolene: a – místo odběrů ostechondrálních bločků z okraje kondylu, b – implantace bločků do místa defektu v zátěžové zóně kondylu 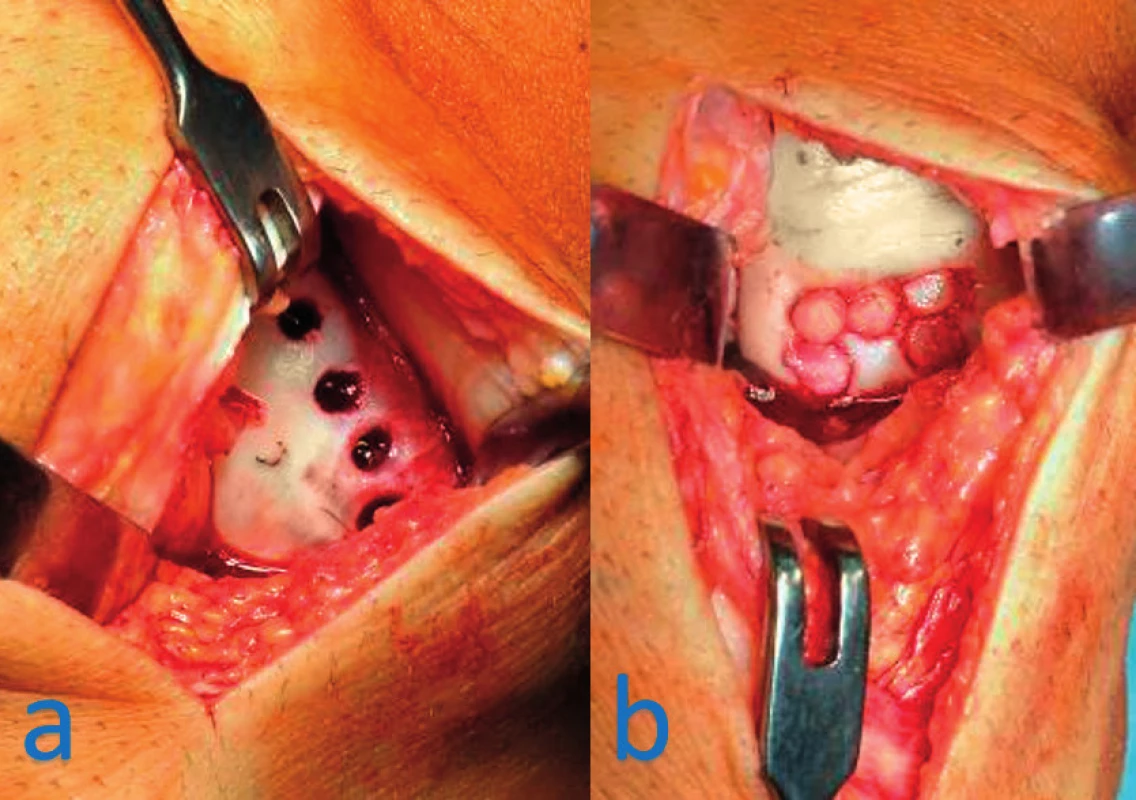
Alogenní osteochondrální štěpy
Použití alogenních štěpů od dárců má v současné době omezené použití, např. při revizních operacích po předchozím ošetření a selhání jiných metod nebo ve specifických traumatologických indikacích (8).
Implantace autologních kultivovaných chondrocytů
Implantace autologních chondrocytů v podobě solidního chondrograftu byla v minulých letech používána jako nejdokonalejší metoda a většinou vede v místě defektu k vytvoření „hyaline-like“ tkáně, blízce podobné původní chrupavce. Jedná se dvoufázové ošetření, kdy v prvním kroku je pa - cientovi provedena artroskopie, při které se po identifikaci defektu odebírá z nezátěžové oblasti kloubu malý vzorek chrupavky. Ten je za aseptických podmínek transportován do laboratoře, kde jsou ze vzorku izolovány chondrocyty. Ty jsou následně kultivovány a pomnoženy po dobu 3–5 týdnů, poté jsou umístěny do trojrozměrného nosiče, tzv. chondrograftu. Chondrograft je pak v druhé fázi implantován do místa defektu při otevřené operaci (obr. 4). Metoda poskytuje dlouhodobé dobré klinické výsledky a je možné ji použít i u velkých chondrálních a ostechondrálních lézí až do velikosti 8–10 cm2 (9, 10). Nevýhodou techniky je nutnost dvou operačních zákroků a vyšší cena implantátu.
Obr. 4. Implantace solidního chondrograftu na mediální kondyl levého kolene: a – chondrální defekt mediálního kondylu femuru, b – debridement chrupavky, zarovnání defektu na pravidelný tvar a provedení mikrofraktur spodiny šídlem, c – výsledný stav po vložení solidního chondrograftu do místa defektu 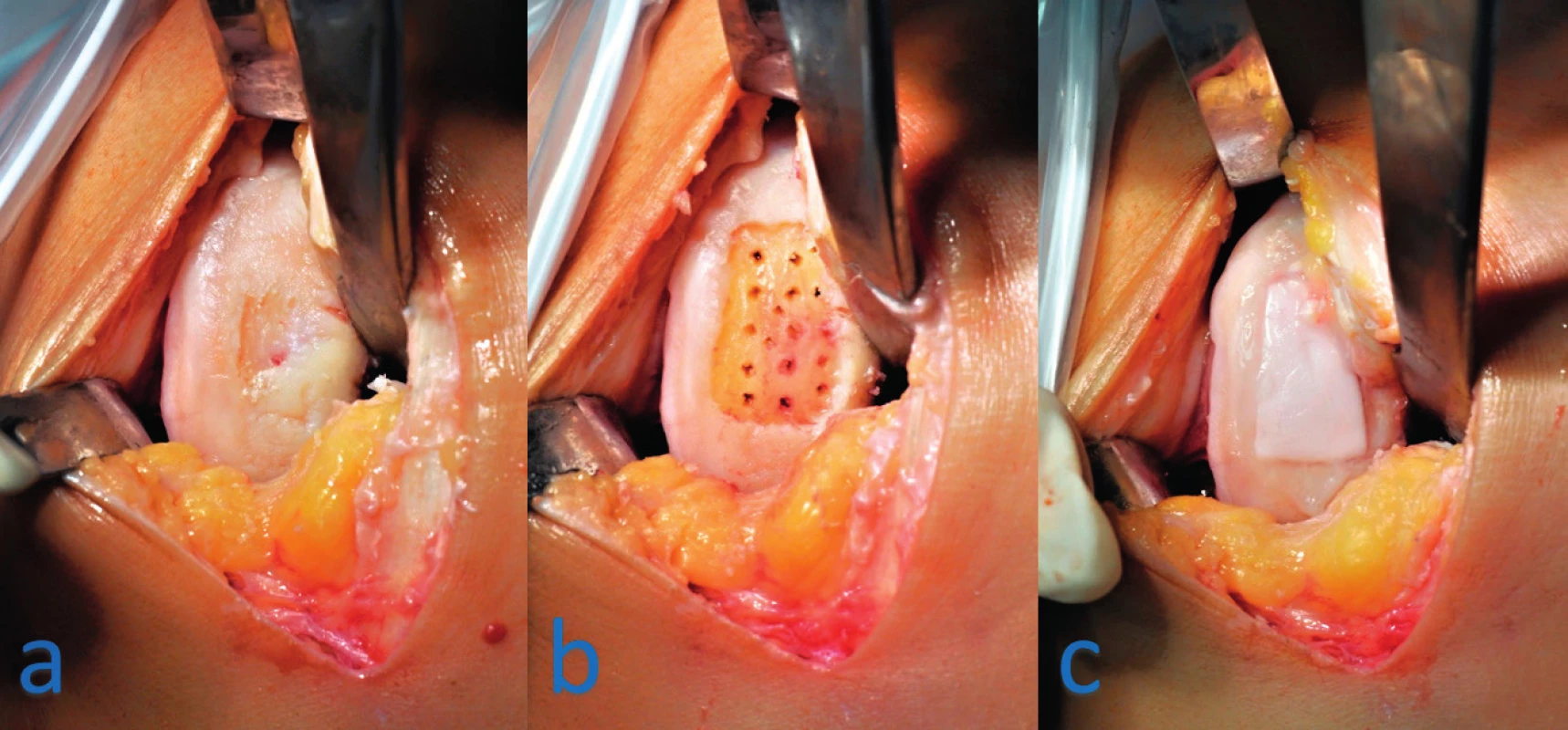
Implantace bezbuněčných nosičů (scaffoldy)
Bezbuněčné trojrozměrné nosiče jsou biokompatibilní a biodegradabilní implantáty, které po implantaci do místa defektu slouží jako nosná struktura neboli „lešení“ pro uchycení a pomnožení chondrocytů z okolní chrupavky. Scaffoldy mohou být připraveny z kolagenu I. typu, kyseliny hyaluronové, alginátu, kalcium sulfátu, polyglykolové kyseliny a jiných (11). Výhodou scaffoldů oproti implantaci autologních chondrocytů je především nutnost pouze jednoho operačního zákroku. Některé nosiče je možné implantovat artroskopicky. Nevýhodou je především chybění dlouhodobých klinických výsledků (12, 13).
AMIC (Autologous Matrix-Induced Chondrogenesis)
Jedná se o inovativní metodu ošetření lokalizovaných chondrálních defektů kombinující provedení klasických mikrofraktur spodiny defektu následované aplikací bezbuněčného implantátu (obr. 5). V originálním popisu metody je použita kolagenová membrána tvořena I. a III. typem kolagenu (14), je ale možné použít i jiný typ scaffoldu. Implantát v místě defektu zadržuje krevní zátku vytvořenou z krve unikající z rozrušené spodiny defektu a současně vytváří trojrozměrnou síť pro pluripotentní kmenové buňky kostní dřeně a napomáhá v jejich diferenciaci do chrupavčitých buněk. Jedná se o jednodobou operaci, která v sobě spojuje výhody mikrofraktur i použití bezbuněčných nosičů. Nověji ji provádíme artroskopicky bez nutnosti otevřené operace.
Obr. 5. Ošetření chondrálního defektu mediálního kondylu femuru pravého kolene modifikovanou AMIC technikou: a – ze spodiny a okrajů defektu odstraněna poškozená chrupavka, b – na spodině defektu provedeny mikrofraktury pomocí šídla, c – výsledný stav po implantaci scaffoldu a zalití okrajů tkáňovým lepidlem 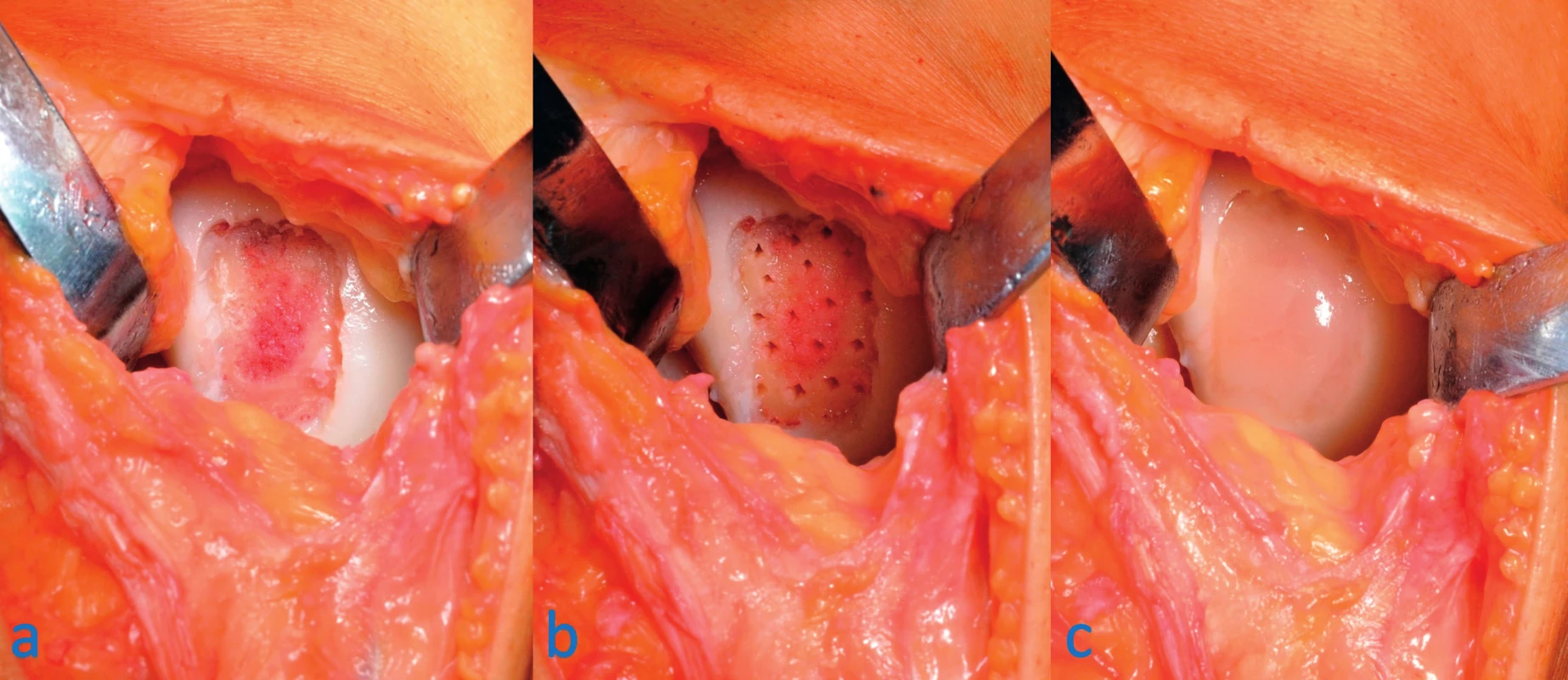
Pooperační režim
U všech výše uvedených technik je nutné dodržet podobný pooperační režim – odlehčení operované končetiny po dobu 6–8 týdnů, fixace operovaného kloubu – kolenní ortéza, eventuálně sádrová fixace hlezna až 6 týdnů po operaci dle velikosti defektu, následná dlouhodobá rehabilitace k obnovení plného pohybu a posílení svalstva. Regenerace chrupavky je dlouhotrvající proces, proto je potřeba pacienty poučit, že doba k návratu k plné sportovní nebo pracovní zátěži může trvat 6–12 měsíců.
Podpořeno grantem MZ ČR – RVO (FNBr, 16-30833A).
Konflikt zájmů: žádný.
ADRESA PRO KORESPONDENCI:
MUDr. Andrea Šprláková-Puková, Ph.D.
Klinika radiologie a nukleární medicíny LF MU a FN
Jihlavská 20, 625 00 Brno
Zdroje
1. Lüllmann-Rauch R. Histologie. Praha: Grada Publishing 2012.
2. Šprláková-Puková A, Vališ P, Mechl M. Zobrazování hyalinní chrupavky pomocí magnetické rezonance. Ces Radiol 2017; 71(4): 291–295.
3. Bekkers JEJ, Bartels LW, Benink RJ, et al. Delayed gadolinium enhanced MRI of cartilage (dGEMRIC) can be effectively applied for longitudinal cohort evaluation of articular cartilage regeneration. Osteoarthritis Cartilage 2013; 21(7): 943–949.
4. Voloshin I, Morse KR, Allred CD, et al. Arthroscopic evaluation of radiofrequency chondroplasty of the knee. Am J Sports Med 2007; 35(10): 1702–1707.
5. Erggelet C, Vavken P. Microfracture for the treatment of cartilage defects in the knee joint – a golden standard? J Clin Orthop Trauma 2016; 7(3): 145–152.
6. Steinwachs MR, Guggi T, Kreuz PC. Marrow stimulation techniques. Injury 2008; 39(Suppl 1): 26–31.
7. Hangody L, Füles P. Autologous osteochondral mosaicplasty for the treatment of full-thickness defects of weight-bearing joints: ten years of experimental and clinical experience. J Bone Joint Surg Am 2003; 85-A(Suppl 2): 25–32.
8. Fagan R, Furey AJ. Use of large osteochondral allografts in reconstruction of traumatic uncontained distal femoral defects. J Orthop 2014; 11(1): 43–47.
9. Brittberg M. Autologous chondrocyte implantation-technique and long-term follow-up. Injury 2008; 39(Suppl 1): 40–49.
10. Minas T, Peterson L. Autologous chondrocyte transplantation. Oper Tech Sports Med 2012; 20 : 72–86.
11. Irion VH, Flanigan DC. New and emerging techniques in cartilage repair: other scaffold-based cartilage treatment options. Oper Tech Sports Med 2013; 21(2): 125–137.
12. Filardo G, Kon E, Roffi A, et al. Scaffold-based repair for cartilage healing: a systematic review and technical note. Arthroscopy 2013; 29(1): 174–186.
13. Fischer S, Kisser A. Single-step scaffold-based cartilage repair in the knee: A systematic review. J Orthop 2016; 13(4): 246–253.
14. Benthien JP, Behrens P. The treatment of chondral and osteochondral defects of the knee with autologous matrix-induced chondrogenesis (AMIC): method description and recent developments. Knee Surg Sports Traumatol Arthrosc 2011; 19(8): 1316–1319.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2020 Číslo 3- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
-
Všechny články tohoto čísla
- Současné možnosti diagnostiky a léčby ohraničených chrupavčitých lézí nosných kloubů
- Sociodemografické charakteristiky seniorskej populácie a ich vplyv na úroveň zdravotnej gramotnosti: literárny prehľad
- Profesionální onemocnění hlášená v České republice v roce 2019
- Využití biochemických markerů v prenatálním screeningu chromozomových aberací v České republice
- Role sestry a sekundární prevence cévní mozkové příhody
- Metódy nefarmakologickej liečby pri reumatoidnej artritíde
- Diagnostika a léčba diabetu typu LADA v klinické praxi
- Zánětlivá bolest zad
- Parkinsonova choroba a jej vplyv na dôstojnosť pacienta: prípadová štúdia s využitím interpretatívno fenomenologickej analýzy
- Vzdělávací portál ČLK: Digitální revoluce v akreditovaném vzdělávání lékařů
- Digitální ordinace bez starostí
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Diagnostika a léčba diabetu typu LADA v klinické praxi
- Metódy nefarmakologickej liečby pri reumatoidnej artritíde
- Současné možnosti diagnostiky a léčby ohraničených chrupavčitých lézí nosných kloubů
- Role sestry a sekundární prevence cévní mozkové příhody
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



