-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Prediktory kognitívnych omylov u odliečených onkologických pacientov
Predictors of cognitive failures in cancer survivors
Background: Progress in cancer diagnostic and treatment increases the probability of survival and survival time in cancer patients. Current research focuses on the quality of life of cancer survivors and the late effects of treatment, which can take the form of cognitive failures in daily life. The aim of the presented research was to examine the relationships between subjectively-reported cognitive failures and selected socio-demographic, clinical, and psychological characteristics (age, hormonal treatment, depression, anxiety, fatigue, sleep satisfaction). Patients and methods: The research sample consisted of 102 cancer survivors aged 25–79 years and a mean time since the end of the last treatment was 17.4 months (standard deviation = 15.4). The largest part of the sample consisted of breast cancer survivors (62.4%). The level of cognitive errors and failures was measured by the Cognitive Failures Questionnaire. The PHQ-9 Patient Health Questionnaire, the GAD-7 General Anxiety Disorder Scale, and the WHOQOL-BREF Quality of Life Questionnaire were used to measure depression, anxiety, and selected aspects of quality of life. Results: An increased level of cognitive failures in daily life was found in approximately one-third of cancer survivors. The overall cognitive failures score is strongly related to the level of depression and anxiety. Decreasing levels of energy and sleep satisfaction are associated with increasing cognitive failures in everyday life. The age and hormonal therapy do not significantly differentiate the level of cognitive failures. In the regression model, which explained 34.4% of the variance of subjectively-reported cognitive functioning, depression was the only significant predictor. Conclusion: The study results mention relationship between subjective evaluation of cognitive functioning and emotional experience in cancer survivors. The administration of self-reported methods for measuring cognitive failures can be helpful in clinical practice in identifying psychological distress.
Keywords:
anxiety – Quality of life – Cognition – depression – cancer survivors – cognitive failures
Autoři: V. Boleková; V. Chlebcová
Působiště autorů: Fakulta psychológie, Paneurópska vysoká škola, Bratislava, Slovenská republika
Vyšlo v časopise: Klin Onkol 2023; 36(1): 45-53
Kategorie: Původní práce
doi: https://doi.org/10.48095/ccko202345Souhrn
Východiská: Pokroky v diagnostike a liečbe rakoviny umožňujú zvýšiť pravdepodobnosť a dĺžku prežitia onkologických pacientov. Súčasný výskum sa zameriava na kvalitu života odliečených onkologických pacientov a neskoré následky liečby, ktoré môžu mať podobu kognitívnych omylov v každodennom živote. Cieľom prezentovaného výskumu bolo skúmať vzťahy medzi subjektívne posúdenou mierou kognitívnych omylov a vybraných sociodemografických, klinických a psychologických charakteristík (vek, absolvovanie hormonálnej liečby, depresia, úzkosť, únava, spokojnosť so spánkom). Súbor pacientov a metódy: Výskumný výber tvorilo 102 odliečených pacientov vo veku 25–79 rokov a s priemernou dĺžkou od ukončenia poslednej liečby 17,4 mesiacov (štandardná odchýlka = 15,4). Najväčšiu časť výskumného súboru tvorili odliečené pacientky s rakovinou prsníka (62,4 %). Miera kognitívnych chýb a omylov bola meraná Dotazníkom kognitívnych zlyhaní. Na meranie úrovne depresie, úzkosti a vybraných aspektov kvality života boli použité Dotazník zdravia pacienta PHQ-9, Škála generalizovanej úzkostnej poruchy GAD-7 a dotazník kvality života WHOQOL-BREF. Výsledky: Zvýšená miera kognitívnych omylov v bežnom živote bola zistená približne u tretiny odliečených onkologických pacientov. Celkové skóre kognitívnych omylov je v silnom vzťahu s mierou depresie a úzkosti. S klesajúcou mierou energie a spokojnosti so spánkom je zároveň spätý nárast kognitívnych chýb v bežnom živote. Vek a absolvovanie hormonálnej terapie mieru kognitívnych omylov výrazne nediferencujú. V regresnom modeli, ktorý vysvetľoval 34,4 % variancie subjektívne hodnoteného kognitívneho fungovania, bola jediným signifikantným prediktorom depresia. Záver: Výsledky výskumu poukazujú na vzťah subjektívneho hodnotenia kognitívneho fungovania a emocionálneho prežívania odliečených onkologických pacientov. Administrácia sebaposudzovacích metód na meranie kognitívnych omylov môže byť v klinickej praxi nápomocná pri identifikácii psychologického distresu.
Klíčová slova:
kvalita života – úzkost – depresia – odliečení onkologickí pacienti – kognícia – kognitívne zlyhania
Úvod
V dôsledku zvyšujúceho sa počtu pacientov, ktorí v minulosti úspešne absolvovali liečbu onkologického ochorenia, sa v posledných dvoch desaťročiach venuje zvýšená pozornosť kvalite života odliečených pacientov [1]. Tá je v mnohých prípadoch narušená oslabením kognitívnych funkcií rôznej závažnosti, ktoré má výrazný vplyv na ich osobnú pohodu a funkčný stav [2].
U onkologických pacientov v predchorobí zrejme nedochádza k žiadnym špecifickým zmenám v kognitívnom fungovaní [3]. S nástupom ochorenia a jeho liečbou sú však spojené mnohé, stále nie dostatočne objasnené, patofyziologické mechanizmy zapríčiňujúce pokles kognitívnych schopností [4]. Kognitívny deficit sa môže rozvinúť napr. následkom priameho neurotoxického účinku liečby, spustenia zápalových kaskád, poškodenia progenitorových buniek, abnormalít v bielej hmote či zníženia funkčnej konektivity mozgu [2,3]. Závažnosť kognitívneho oslabenia zväčša variuje od mierneho až po stredne závažný deficit [2,5]. V najväčšej miere sa prejavuje v oblasti učenia, pamäti, rýchlosti spracovania informácií či exekutívnych funkcií [2, 6–9].
Prevalencia kognitívnej poruchy u onkologických pacientov po ukončení liečby je na úrovni 24 % a po jednom roku je stále prítomná u pomerne veľkého počtu pacientov (21 %) [5,8,10]. Na základe aktuálnej metaanalýzy výskumných štúdií realizovaných v populácii pacientiek s rakovinou prsníka možno konštatovať, že klinicky významné kognitívne oslabenie sa vyskytuje u 1 z 3 pacientiek. Skríningovým testom je zachytený nižší počet prípadov (16 %) ako komplexnou neuropsychologickou batériou (21–34 %). Prevalencia kognitívneho oslabenia je ešte vyššia, ak sa zohľadní subjektívne hodnotenie pacienta (44 %) [11]. Nesúlad v uvedených hodnotách poukazuje na skutočnosť, že subjektívne vnímaný deficit sa u odliečených pacientov vyskytuje častejšie ako deficit zistený objektívnymi výkonovými testami [12]. Závery viacerých štúdií poukazujú na zanedbateľný vzťah medzi objektívnym a subjektívnym posúdením kognitívneho výkonu [7,8,10,13–15]. Štandardné neuropsychologické testy často nie sú dostatočne senzitívne pre zachytenie kognitívnych symptómov v situáciách každodenného života. Je preto potrebné venovať pozornosť aj subjektívne hodnotenému stavu pacienta a skúmať faktory potenciálne predikujúce či mediujúce vnímaný pokles kognitívnych funkcií [1], ktorý po absolvovaní chemoterapie uvádza takmer 40 % onkologických pacientov [16]. Jean-Pierre et al konštatujú, že u pacientov s rakovinou je pravdepodobnosť výskytu subjektívne vnímaných problémov v oblasti mnestických funkcií vyššia o 40 % v porovnaní s ľuďmi bez onkologického ochorenia [17].
Na základe záverov výskumných štúdií možno predpokladať, že klinické a sociodemografické premenné predikujú úroveň objektívne hodnoteného kognitívneho fungovania, avšak subjektívne posúdenie ťažkostí je vo vzťahu najmä so psychologickými charakteristikami [18]. Subjektívne vnímané oslabenie kognície môže byť skôr indikátorom emocionálneho distresu ako prítomnosti kognitívneho deficitu [12]. Psychologické faktory, vrátane črtovej a aktuálne prežívanej úzkosti, depresie, únavy či vnímaného stresu, sú prediktormi frekvencie sťažností na kogníciu a spokojnosti s ňou [19].
Úzkosť a depresia sú najčastejšie sa vyskytujúcimi duševnými ochoreniami v populácii pacientov s rakovinou. Údaje o prevalencii depresie sa pohybujú na úrovni 28–38 % prípadov [8,20,21]. Zvýšenú mieru úzkosti možno konštatovať u približne tretiny onkologických pacientov [8,21]. Výskyt depresie (13,6 %) a úzkosti (24,6 %) nie je zanedbateľný ani rok po ukončení liečby [22].
Prežívanie depresie a úzkosti [8,10,14, 16,23], emočná vulnerabilita a miera symptómov posttraumatickej stresovej poruchy [23] či črtová negatívna afektivita [10] sú vo vzťahu so subjektívne vnímaným zhoršením kognitívneho fungovania. Výsledky v objektívnych testoch naopak s mierou úzkosti či depresie nesúvisia [10,14]. Prediktorom subjektívne zníženého výkonu po absolvovaní chemoterapie je tiež únava [14,16]. Po ukončení liečby onkologického ochorenia sa vyskytuje u 53–61 % pacientov a u 40 % pretrváva aj po jednom roku [24]. Stres a únava v nedávnom výskume Gutenkunstovej et al vysvetľovali 33 % variancie subjektívne vnímaných ťažkostí u pacientov v ranom štádiu ochorenia, po absolvovaní adjuvantnej chemoterapie [18]. O zníženej koncentrácii ďalej referujú pacienti, u ktorých sa vyskytli problémy so spánkom [25].
Vek ako prediktor kognitívneho výkonu je pomerne často predmetom záujmu výskumníkov. Empirická evidencia v tejto oblasti však nie je jednoznačná. Vek je prediktorom objektívneho výkonu v testoch rýchlosti spracovania informácií, exekutívnych funkcií, verbálnej epizodickej pamäti a sémantickej fluencie, v ktorých lepšie výkony dosahujú ľudia v mladšom veku [26]. V americkom výskume bol naopak nižší vek spätý s vyšším výskytom subjektívne vnímaných porúch pamäti [17]. O‘Farrellová et al zas konštatujú zanedbateľný vzťah medzi vekom a subjektívne vnímanými zmenami v kognícii [14].
Posúdiť špecifické účinky konkrétneho liečebného postupu je náročné, nakoľko pacienti mnohokrát absolvujú viacero druhov liečby. U pacientov, ktorí absolvovali chemoterapiu, však možno predpokladať vyššiu pravdepodobnosť vzniku kognitívneho oslabenia alebo deficitu ako u zdravých kontrol a pacientov, ktorí tento typ liečby neabsolvovali [5]. U pacientiek s rakovinou prsníka po ukončení chemoterapie bol zistený významný pokles v kognitívnom výkone, najmä v oblasti verbálneho učenia a pamäti, abstraktného uvažovania, distribúcie pozornosti, motorickej koordinácie a psychomotorického tempa [27–29]. Quesnelová et al uvádzajú, že znížená schopnosť vybavovania informácií z verbálnej pamäti bola identifikovaná v rovnakej miere u pacientov absolvujúcich chemoterapiu a rádioterapiu. U pacientov po liečbe chemoterapiou však bol naviac konštatovaný znížený výkon v oblasti verbálnej fluencie a nárast subjektívne vnímaných ťažkostí [30]. Hormonálna terapia u pacientiek s rakovinou prsníka má za následok deficit v oblasti verbálnej pamäti, verbálnej fluencie, pozornosti a pracovnej pamäti [31]. Závery štúdie zohľadňujúcej typ liečiva poukazujú na zhoršené verbálne funkcie u užívateľov tamoxifénu. Podanie exemestánu bolo asociované s pomalším psychomotorickým tempom [32].
Vzhľadom na zvyšujúci sa počet odliečených onkologických pacientov je potrebné skúmať vplyv dlhodobých následkov liečby na kvalitu života spojenú so zdravím a mať k dispozícii nástroje na meranie širokého spektra možných komplikácií po liečbe onkologického ochorenia, vrátane prejavov oslabenia kognitívnych funkcií. V zahraničných výskumných štúdiách je preferovaný špecifický nástroj na posúdenie zmien v kognícii a funkčného stavu pacienta po liečbe rakoviny FACT-Cog [7,14,18,23]. V našom výskume sme použili menej využívaný nástroj Dotazník kognitívnych zlyhaní, ktorý umožňuje subjektívne posúdenie kognitívneho oslabenia v podobe chýb a omylov objavujúcich sa počas vykonávania každodenných aktivít v dôsledku krátkodobého zlyhania mnestických funkcií, koncentrácie či distribúcie pozornosti, vnímania alebo dosahovania cieľa iniciovanej činnosti [33,34]. Kognitívne zlyhania sú prejavom obmedzenej kognitívnej kapacity pre vykonanie bežných úloh, nemusia byť nevyhnutne odrazom všeobecných kognitívnych schopností a intelektu [35,36]. Pravdepodobnosť ich výskytu sa zvyšuje v situáciách, v ktorých jednotlivec musí spracovať väčšie množstvo informácií [37]. Sú dôležitým predmetom výskumu, nakoľko výrazne ovplyvňujú kvalitu života odliečených pacientov [15].
Cieľom prezentovaného výskumu bolo skúmať vzťahy medzi subjektívne posúdenou mierou kognitívnych omylov a vybranými sociodemografickými, klinickými a psychologickými charakteristikami (vek, absolvovanie hormonálnej liečby, depresia, úzkosť, únava, spokojnosť so spánkom).
Výskumný súbor a metódy
Výskumný súbor
Výskumu sa zúčastnilo 200 odliečených onkologických pacientov, ktorí absolvovali liečbu vo vybraných kúpeľných zariadeniach (Bardejovské Kúpele, Kúpele Lúčky, Kúpele Bojnice), klientky pomáhajúcich organizácií a členky svojpomocných skupín (OZ Amazonky, OZ Venuše, Klub venuše, OZ Nie rakovine, OZ Noktua, Liga proti rakovine). Časť zberu dát prebiehala prostredníctvom online dotazníka. Z uvedeného počtu participantov bolo do analýzy zaradených 102 participantov, ktorí spĺňali stanovené inklúzne kritériá: 1) vek nad 18 rokov; 2) prekonané onkologické ochorenie; 3) liečba chemoterapiou; 4) doba od ukončenia liečby max. 60 mesiacov.
Výskumný výber tvorilo 9 mužov a 93 žien vo veku 25 až 79 rokov (M = 53,9; SD = 11,9), s priemernou dĺžkou od ukončenia poslednej liečby M = 17,4 mesiacov (SD = 15,4). Najväčšiu časť výskumného súboru tvorili odliečené pacientky s rakovinou prsníka (62,4 %). V súbore boli ďalej zastúpení pacienti, ktorí prekonali rakovinu hrubého čreva (7,7 %), lymfatických uzlín (7,7 %), vaječníkov (4,3 %), kože (3,4 %), prostaty (1,7 %) a leukémiu (1,7 %). Ostatné diagnózy (rakovina močového mechúra, konečníka, obličiek, štítnej žľazy, hlavy a krku, hrtana, krčka maternice a pľúc) boli prítomné ojedinele (0,9 %). Komorbidita viacerých onkologických ochorení bola zaznamenaná u 12 participantov. U 11 participantov bolo v anamnéze prítomné recidivujúce onkologické ochorenie. Všetci pacienti absolvovali chemoterapiu, príp. súbežne viacero druhov liečby. Informácie o druhoch liečby, vrátane podpornej psychologickej a psychoterapeutickej intervencie, uvádzame v tab 1.
Tab. 1. Distribúcia participantov z hľadiska absolvovanej liečby. 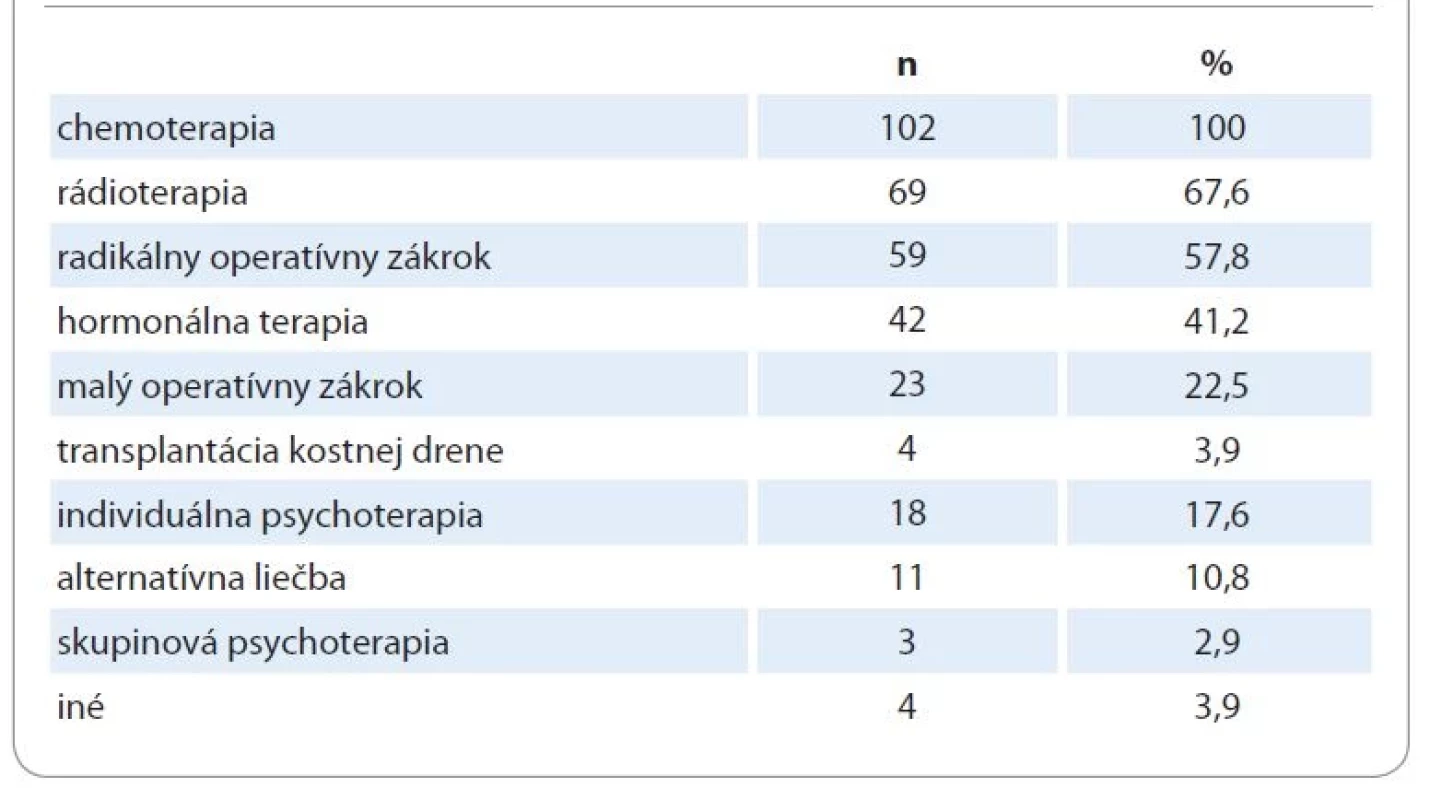
Nástroje merania
Mieru kognitívnych chýb a omylov v každodennom živote sme merali prostredníctvom 25 položiek Dotazníka kognitívnych zlyhaní [35]. Výskyt omylov prameniacich z vnímaného oslabenia pamäti, pozornosti či vnímania participanti hodnotili na škále 0–4 (nikdy až veľmi často). Jensen et al uvádzajú 41 bodov ako odporúčané „cut-off“ skóre pre konštatovanie zvýšenej miery kognitívnych zlyhaní [38]. Dotazník bol pôvodne navrhnutý ako jedno-dimenzionálna metóda na meranie všeobecného faktora kognitívneho zlyhania, avšak ďalšie výskumy poukazujú na možnosť vytvorenia viacerých faktorov. Wallace na základe konfirmačnej analýzy identifikoval štyri faktory: pamäť (zabúdanie v dôsledku nepozornosti v danom momente), roztržitosť, omyly a pamäť na mená [39]. V slovenskom výskume boli rozlíšené taktiež štyri faktory: problémy s pamäťou a pozornosťou, roztržitosť a zmätenosť, omyly pri zvládaní každodenných úloh v dôsledku neprítomnosti v aktuálnom okamihu a interpersonálna komunikácia [40]. V prezentovanom výskume sme zistili dobrú vnútornú konzistenciu položiek dotazníka (a = 0,93).
Miera depresie bola meraná Dotazníkom zdravia pacienta (Patient Health Questionnaire-9 – PHQ-9), ktorý obsahuje 9 položiek so štvorstupňovou odpoveďovou škálou [41]. Jednotlivé položky vyjadrujú symptómy depresie (napr. nezáujem, depresívne prežívanie, pocit zlyhania, samovražedné myšlienky, psychomotorický útlm a pod.). Na základe celkového skóre možno orientačne posúdiť závažnosť depresie (0–4 minimálna depresia, 5–9 ľahká depresia, 10–14 mierna depresia, 15–19 stredne ťažká depresia a 20–27 ťažká depresia). Škála generalizovanej úzkostnej poruchy (General Anxiety Disorder-7 – GAD-7) bola odliečeným onkologickým pacientom administrovaná s cieľom posúdiť mieru symptómov spojených s dlhodobo prítomnou úzkosťou, resp. úzkostlivosťou (napr. prehnané starosti o rôzne veci, nepokoj či ťažkosti s uvoľnením sa) [42]. Participant zaznamenáva frekvenciu prežívania siedmich symptómov úzkosti za posledné 2 týždne (na škále od 0 – vôbec nie po 3 – takmer každý deň). Na základe skóre možno odlíšiť miernu (5–9 bodov), strednú (10–14 bodov) a silnú úzkosť (15–21 bodov). Pre obidve metódy sme zistili dobré hodnoty Cronbachovej alfy (a = 0,87 pre PHQ-9 a a = 0,89 pre GAD-7).
Úroveň energie a spokojnosti so spánkom hodnotili participanti prostredníctvom dvoch položiek z dotazníka na meranie kvality života WHOQOL-BREF [43]. Teoretické rozpätie položiek bolo 1–5 bodov. Participanti tiež vyplnili dotazník zameraný na základné sociodemografické a klinické údaje, vrátane otvorenej otázky dopytujúcej sa na neskoré následky liečby.
Metódy analýzy dát
V príspevku sú prezentované výsledky frekvenčných analýz a základné deskriptívne štatistiky. Odhad reliability sme realizovali prostredníctvom analýzy vnútornej konzistencie (Cronbachova alfa). Ukazovateľom sily vzťahu medzi skóre z jednotlivých dotazníkov bol Spearmanov koeficient poradovej korelácie. Multivariačnú analýzu premenných sme realizovali prostredníctvom hierarchickej regresnej analýzy so závislou premennou kognitívne omyly. Výpočet koeficientu determinácie sme realizovali s cieľom zistiť percento variability vysvetlenej vzťahom so zaradenými prediktormi. Predpoklad o normalite distribúcie závislej premennej bol testovaný prostredníctvom Kolmogorov-Smirnovho testu. Pred realizáciou regresnej analýzy boli tiež zhodnotené hodnoty štandardizovaných reziduí a prítomnosť multikolinearity bola zisťovaná prostredníctvom korelačnej analýzy a výpočtu variačného inflačného faktora.
Etické aspekty výskumu
Výskum bol realizovaný v rámci grantovej úlohy GA/3/2019 Prediktory posttraumatického rozvoja u odliečených onkologických pacientov, ktorá bola schválená Etickou komisiou Paneurópskej vysokej školy. Participantom boli poskytnuté informácie o cieli výskumu a podstatných náležitostiach ich participácie.
Výsledky
Znížená kognitívna kapacita pre vykonanie bežných úloh sa u najväčšieho počtu participantov (43,1 %) prejavuje neschopnosťou sústrediť sa na mená ľudí, s ktorými sa zoznamujú. Až 38,6 % si nemôže na niečo spomenúť, napriek tomu, že to má na jazyku a 31,4 % si pri čítaní zrazu uvedomí, že textu nevenuje pozornosť a musí ho čítať odznovu. Kognitívne omyly sa u nezanedbateľnej časti odliečených onkologických pacientov prejavujú zabúdaním mien ľudí (29,2 %), dôvodu premiestnenia sa z jednej časti domu do druhej (28,7 %), neplánovaným prerušovaním vykonávanej činnosti iniciovaním inej aktivity (25,7 %) a tiež zabúdaním, kde bol odložený konkrétny predmet (25,5 %). Naopak, zabúdanie na dohodnuté stretnutia, vyhadzovanie vecí a vrážanie do ľudí v dôsledku roztržitosti sa vyskytuje u menej ako 5 % participantov. Zvýšenú mieru kognitívnych omylov (tj. skóre > 41 bodov) možno predpokladať u 33,3 % participantov.
Najvýraznejším indikátorom depresívneho prežívania bol pocit nedostatku energie. Až 54,7 % uviedlo prítomnosť symptómu počas viac ako polovice dní alebo takmer každého dňa v priebehu uplynulých 2 týždňov. Až 47,9 % referovalo o poruchách spánku a 23,2 % o ťažkostiach so sústredením sa. Pocity nešťastia, depresie a beznádeje aspoň raz počas posledných 14 dní boli prítomné u 50 % participantov a myšlienky, že by bolo lepšie umrieť alebo si ublížiť sa vyskytli u 18,8 % odliečených onkologických pacientov. Distribúcia z hľadiska závažnosti symptómov depresie bola nasledovná: 30,9 % minimálna depresia, 37,2 % ľahká depresia, 19,1 % mierna depresia, 6,4 % stredne ťažká depresia a 6,4 % ťažká depresia.
Prítomnosť úzkostnej symptomatiky môžeme konštatovať u približne polovice participantov: u 31,6 % participantov bola zistená mierna úzkosť, 9,5 % referovalo o stredne závažnej úzkosti, u 8,4 % bola skríningom zachytená silná úzkosť. Úzkosť sa u participantov prejavovala najmä prehnanými starosťami (25,0 %), ťažkosťami s uvoľnením sa (24,2 %) a neschopnosťou prestať si robiť starosti a dostať ich pod kontrolu (19,8 %).
Približne 16 % participantov nesúhlasilo s tvrdením, že má dosť energie na každodenný život a ďalších 34 % uviedlo strednú úroveň energie. Nespokojnosť so spánkom uviedlo 35 %. Deskriptívnu štatistku pre jednotlivé premenné uvádzame v tab. 2.
Tab. 2. Deskriptívna štatistika skúmaných premenných. 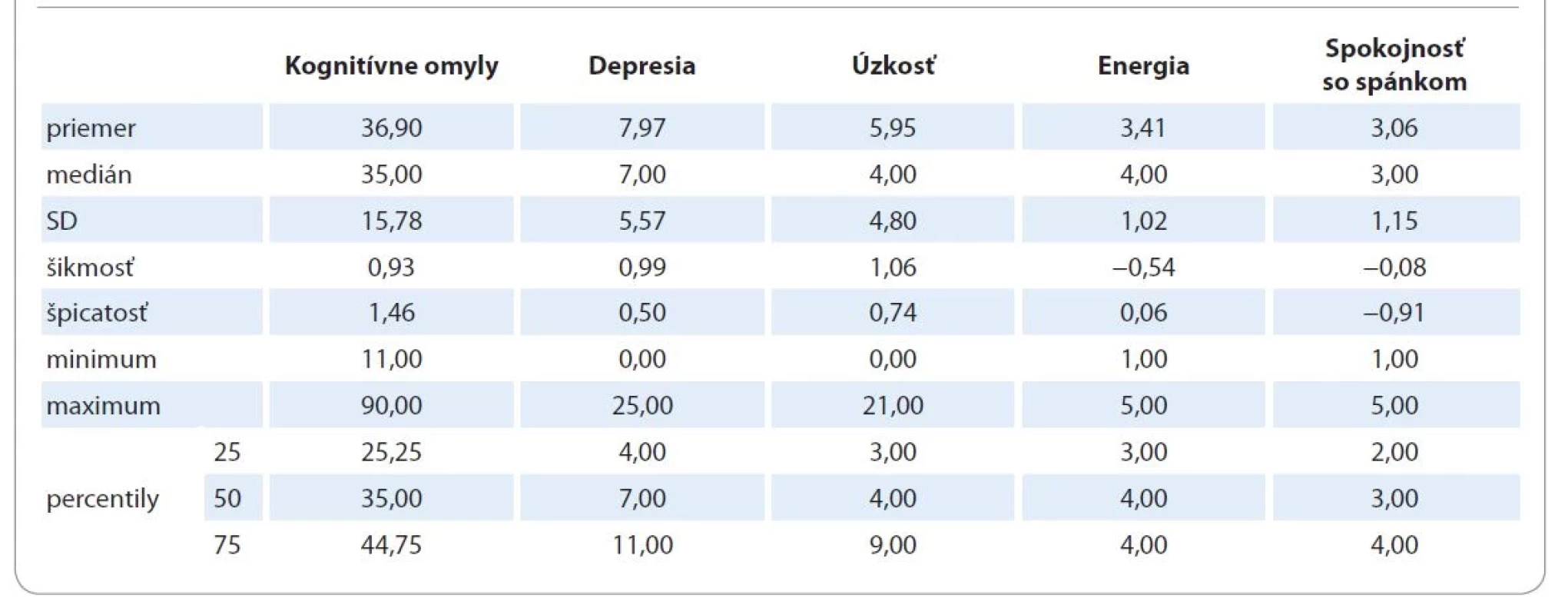
Viac ako polovica odliečených onkologických pacientov (56,9 %) uviedla, že sa u nich vyskytli neskoré následky liečby. Svoju odpoveď špecifikovalo 57 participantov, z ktorých 25 % prežíva zvýšenú únavu a slabosť, 11 % participantov explicitne uviedlo ako neskorý následok liečby nespavosť, 9 % referovalo o zhoršení pamäťových funkcií a nižšom výkone v oblasti kognitívnych funkcií a len 7 % označilo ako problém depresiu a psychické problémy.
Celkové skóre kognitívnych omylov je v silnom vzťahu s mierou depresie (rs = 0,55; p < 0,001) a úzkosti (rs = 0,54; p < 0,001). S klesajúcou mierou energie (rs = −0,41; p < 0,001) a spokojnosti so spánkom (rs = −0,40; p < 0,001) je spätý nárast kognitívnych chýb a omylov v bežnom živote. Vzťah medzi kognitívnymi omylmi a vekom je slabý (rs = −0,15; p = 0,16). Súvis s absolvovaním hormonálnej terapie bol slabý, avšak nie zanedbateľný (η = 0,13). Vyššie skóre získali pacienti, ktorí tento typ liečby absolvovali (M = 38,77; SD = 15,60 vs. M = 34,58; SD = 15,86). V tab. 3 uvádzame hodnoty korelačných koeficientov aj pre jednotlivé faktory kognitívnych omylov. Silný vzťah existuje medzi problémami s pamäťou a pozornosťou a depresiou (rs = 0,56; p < 0,001) a tiež medzi úzkosťou a problémami v interpersonálnej komunikácii v dôsledku subjektívne vnímaného kognitívneho oslabenia (rs = 0,57; p < 0,001).
Tab. 3. Vzťah kognitívnych omylov, veku a subjektívne vnímaných problémov. 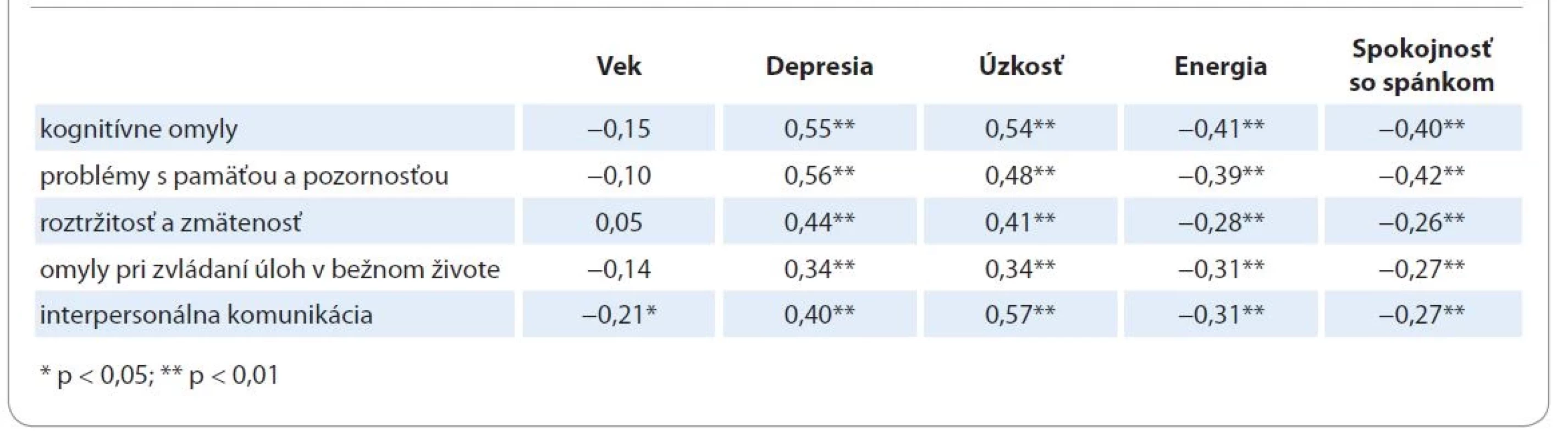
Prediktory kognitívnych omylov sme identifikovali prostredníctvom hierarchickej viacnásobnej regresnej analýzy, do ktorej sme v prvom kroku zaradili premenné vek a absolvovanie hormonálnej terapie a v druhom kroku boli do analýzy zaradené skúmané psychologické premenné (depresia, úzkosť, únava, spokojnosť so spánkom). Kategorizovaná premenná hormonálna terapia bola rekódovaná podľa kódovacej schémy 0 – neabsolvoval/a hormonálnu terapiu a 1 – absolvoval/a hormonálnu terapiu.
Predpoklad o normalite distribúcie závislej premennej nebol výrazne narušený (D (96) = 0,07; p = 0,20). V súbore sa nenachádzali žiadne extrémne hodnoty. Hodnoty štandardizovaných reziduí pochádzali z intervalu <−3; 3>. Prítomnosť multikolinearity bola zisťovaná prostredníctvom korelačnej analýzy. Na hranici akceptovateľnosti (rs = 0,70) bol zistený vzťah medzi úzkosťou a depresiou. VIF faktor pre jednotlivé premenné sa pohyboval v rozmedzí 1,08–3,79.
Vek a absolvovanie hormonálnej terapie vysvetľovali zanedbateľné percento (0,003 %) variancie kognitívnych omylov. Pridaním psychologických premenných do analýzy stúplo percento vysvetlenej variancie na 34,4 %. Nárast kognitívnych omylov je asociovaný s vyššou mierou depresie (b = 0,47; p = 0,01). Ostatné premenné neboli vo výslednom modeli signifikantnými prediktormi kognitívnych omylov (tab. 4).
Tab. 4. Hierarchická lineárna regresia so závislou premennou kognitívne omyly. 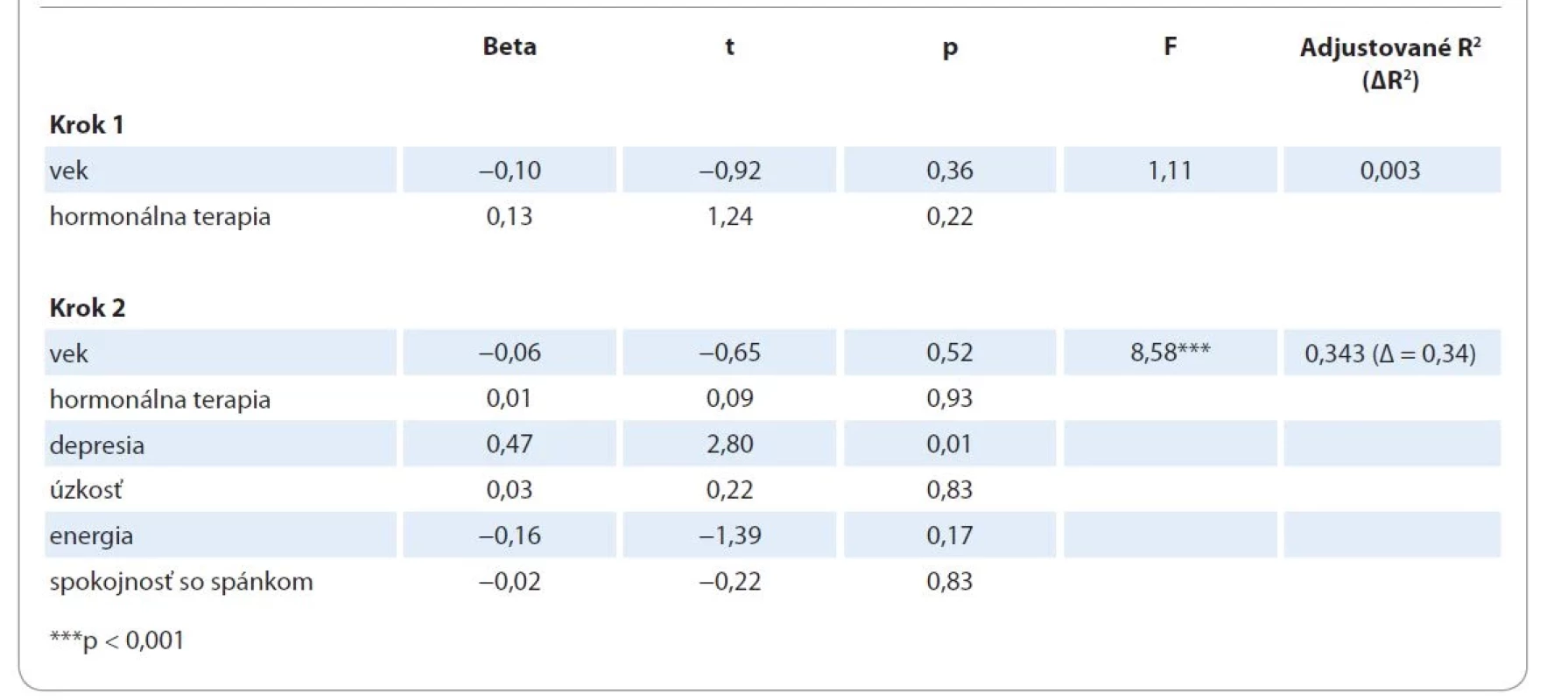
Diskusia
Rakovina a jej liečba sú u odbornej aj laickej verejnosti čoraz viac asociované s poklesom kognitívnych funkcií, ktorý je v literatúre označovaný ako kognitívne poškodenie súvisiace s rakovinou (cancer-related cognitive impairment) [2]. Nevyhnutnou súčasťou klinickej praxe a empirického skúmania je tiež mapovanie dopadu ochorenia a liečby na fungovanie pacienta [44]. Za dôležitý zdroj informácií sa považuje názor a hodnotenie samotného pacienta. V súlade s uvedeným trendom sme sa vo výskume zamerali na subjektívne hodnotené kognitívne omyly odliečených onkologických pacientov vyskytujúce sa v každodennom živote. Cieľom výskumu bolo skúmať vzťahy medzi mierou subjektívne hodnotených kognitívnych omylov a vybraných sociodemografických, klinických a psychologických charakteristík (vek, absolvovanie hormonálnej liečby, depresia, úzkosť, únava, spokojnosť so spánkom).
Zistené prejavy kognitívneho oslabenia čiastočne korešpondujú so závermi kvalitatívneho výskumu Shillingovej a Jenkinsovej, ktorý bol zameraný na identifikáciu špecifických problémov onkologických pacientov v oblasti pamäti a pozornosti [25]. V súlade s našimi zisteniami pacienti referovali o zabúdaní mien, zníženej schopnosti sústrediť sa na čítaný text, nájsť odložený predmet, či rozpamätať sa na konkrétne slovo alebo zamýšľanú činnosť. K ďalším problémom, ktoré v našom výskume Dotazníkom kognitívnych zlyhaní identifikované neboli, možno zaradiť zabúdanie na stretnutia, dôležité osobné udalosti, zabúdanie na položky nákupného zoznamu, neschopnosť udržať niť rozhovoru a roztržitosť pri šoférovaní. Uvedené kognitívne omyly môžu byť dôsledkom oslabenia mnestických a exekutívnych funkcií, ktoré sa u odliečených pacientov vyskytujú v najväčšej miere [2,6,7,45]. Subjektívne vnímané problémy s nájdením vhodných slov a vyjadrení sú zas v zhode so závermi objektívneho posúdenia kognície, ktoré poukazuje na zníženú schopnosť verbálnej fluencie u pacientov po absolvovaní chemoterapie [30].
Na základe odporúčaného cut-off skóre v Dotazníku kognitívnych zlyhaní možno zvýšenú mieru kognitívnych omylov predpokladať u približne 33 % odliečených pacientov. Údaj korešponduje so záverom o kognitívnom oslabení vyskytujúcom sa u 1 z 3 odliečených pacientov, avšak je nižší ako predpokladaná prevalencia subjektívne vnímaného oslabenia kognitívnych funkcií (44 %) [11]. Keďže do výskumu nebola zahrnutá kontrolná skupina, zistené priemerné hodnoty môžeme len orientačne porovnať s údajmi zo zahraničných štúdií. Odliečení pacienti v našom výskume získali vyššie skóre (M = 36,90) v porovnaní so zdravými kontrolami (M = 24,92; resp. M = 27,90) v dánskych výskumných štúdiách [46,47], avšak porovnateľné skóre s onkologickými pacientami v štúdii Quesnelovej et al, v ktorej boli kognitívne zlyhania merané po ukončení chemoterapie (M = 36,04) a vo follow-up meraní po 3 mesiacoch (M = 35,41) [30]. U pacientiek s rakovinou prsníka, ktoré po chemoterapii absolvovali hormonálnu terapiu, nebol zistený rozdiel medzi skupinou, v ktorej bol podávaný tamoxifén (M = 33,80) a exemestán (M = 36,70) [32].
Prítomnosť kognitívnych omylov však nemožno jednoznačne pripísať existencii kognitívneho deficitu. V našom výskume výkonové testy neboli administrované, no závery viacerých štúdií poukazujú na zanedbateľný vzťah medzi objektívnym a subjektívnym posúdením kognitívneho výkonu [7,8,10,13–15]. Následky liečby onkologického ochorenia v každodennom živote sa prejavujú výraznejšie ako v situácii neuropsychologického vyšetrenia kognície prostredníctvom testov objektívneho výkonu [30]. Neuropsychologické testy môžu mať nízku senzitivitu pre zachytenie drobných zmien v kognícii [18,25]. Zapojenie kompenzačných mechanizmov naviac pomáha pacientom podať relatívne dobrý výkon v štruktúrovanej situácii psychologického testovania bez vonkajších rušivých podnetov [45]. Identifikácia kognitívneho deficitu prostredníctvom neuropsychologických testov je u pacientov po ukončení liečby tiež vo veľkej miere závislá od veľkosti kognitívnej rezervy [6]. Je teda potrebné venovať pozornosť aj tým pacientom, u ktorých kognitívny deficit nebol potvrdený neuropsychologickým vyšetrením výkonovými testami, nakoľko subjektívne vnímané oslabenie môže spôsobovať alebo byť prejavom psychického utrpenia vyžadujúceho intervenciu [13]. Aj podľa našich zistení je úroveň kognitívnych omylov v silnom vzťahu s mierou depresie a úzkosti. Zároveň je asociovaná s úbytkom energie a vnímanými problémami so spánkom. Depresia bola tiež jediným signifikantným prediktorom kognitívnych chýb a omylov v každodennom živote.
Uvedené zistenia sú v zhode so závermi zahraničných štúdií, v ktorých bolo kognitívne fungovanie merané dotazníkom FACT-Cog. Únava, úzkosť, depresia a nižšia kvalita života boli asociované s horším subjektívne vnímaným výkonom u pacientov s kolorektálnym karcinómom [15]. Depresia bola prediktorom subjektívne vnímaného, avšak nie objektívne hodnoteného, kognitívneho oslabenia u pacientov po absolvovaní chemoterapie [16]. Vo výskume Pullensovej et al boli depresívne prežívanie a spokojnosť s kognitívnym fungovaním u pacientiek s rakovinou prsníka signifikantnými prediktormi skóre v Dotazníku kognitívnych zlyhaní [19]. Schilderová et al s použitím rovnakého nástroja merania v populácii pacientiek s rakovinou prsníka konštatuje vzťah kognitívnych omylov s úzkosťou, depresiou, únavou a výskytom symptómov menopauzy [32].
Závery výskumu tak korešpondujú s predpokladom, že subjektívne vnímaný pokles kognitívnych schopností môže byť odrazom psychických problémov. Neschopnosť premýšľať alebo sa sústrediť sú možné symptómy depresie. Sprievodným javom úzkosti zas často bývajú problémy s koncentráciou [48]. Negatívna afektivita a záťaž súvisiaca s liečbou môžu v priebehu prvého roka po liečbe spôsobovať pesimistické sebahodnotenie. Občasné kognitívne zlyhania sú súčasťou každodenného fungovania, avšak ľudia s vyššou mierou negatívnej afektivity a pesimistického myslenia problémom pripisujú väčšiu vážnosť a vo väčšej miere o nich referujú [13]. Keďže realizovaná štúdia nebola prospektívna, smer vzťahu medzi subjektívnym posúdením kognitívneho fungovania a emocionálnym prežívaním nevieme jednoznačne určiť. Depresia, úzkosť a únava môžu viesť ku kognitívnym omylom. Je však tiež možné, že kognitívne zlyhania sú zdrojom emocionálneho distresu [12].
Vzťah kognitívnych omylov s vekom bol slabý a záporný. Je pravdepodobné, že pacienti v mladšom veku majú vo väčšej miere zachovaný kritický náhľad na fungovanie kognitívnych funkcií. V dôsledku aktívneho spôsobu života (vykonávanie zamestnania, aktívny sociálny život) majú zároveň viac príležitostí pre uvedomenie si kognitívneho oslabenia [17]. Rozdiely medzi vekovými skupinami preto nemusia byť výrazné. Absolvovanie hormonálnej terapie vo veľkej miere úroveň kognitívnych omylov nediferencovalo.
Prezentované zistenia interpretujeme s ohľadom na viacero limitov realizovaného výskumu. Väčšinové zastúpenie vo výskumnom súbore mali pacientky s rakovinou prsníka, a preto nemožno zistenia zovšeobecňovať na pacientov s rôznymi onkologickými diagnózami. K ďalším metodologickým limitom možno zaradiť nedostatočnú štatistickú silu administrovaných nástrojov merania, meranie kvality spánku a úrovne energie jednou otázkou a absenciu kontrolnej skupiny participantov bez onkologického ochorenia. Vo výskume tiež neboli zohľadnené viaceré dôležité premenné, napr. užívanie antidepresív či nástup predčasnej menopauzy v dôsledku liečby. Do súboru boli zaradení pacienti po absolvovaní chemoterapie. Viacerí pacienti však podstúpili niekoľko druhov liečby, čo mohlo nepriaznivé efekty liečby zvýrazniť. Závery aktuálnych výskumov indikujú, že kognitívne oslabenie sa v pomerne veľkej časti populácie onkologických pacientov vyskytuje už pred zahájením liečby [5,10,30]. Z prierezovej štúdie nemožno túto skutočnosť vylúčiť, zároveň nie je možné identifikovať kauzálne vzťahy ani časovú následnosť javov.
V budúcnosti považujeme za prínosné realizovať longitudinálny výskum so zameraním na rôzne trajektórie kognitívneho fungovania odliečených pacientov. Aktuálna empirická evidencia naznačuje rozmanitý priebeh subjektívne vnímaného kognitívneho oslabenia. Časť pacientov po ukončení liečby referuje o pretrvávajúcom kognitívnom poškodení alebo občasnom zhoršení kognitívneho fungovania. U viacerých pacientov možno pozorovať oneskorený nástup ťažkostí, napr. v dôsledku adjuvantnej hormonálnej terapie. Opätovné zaradenie do bežného života tiež môže prispieť k uvedomeniu si kognitívneho oslabenia a zmien v životnom štýle [49]. Longitudinálny výskum, ale aj skríningové vyšetrenia či kontrolné komplexné neuropsychologické vyšetrenia považujeme za dôležité realizovať v dlhšom časovom úseku po ukončení liečby. V budúcom výskume je tiež potrebné v súlade s odporúčaniami Vlčkovej et al zohľadniť možnosť komorbidity kognitívneho deficitu a prítomnosť psychiatrických diagnóz, ktoré by mohli prispievať k väčšej miere a intenzite skúmaných problémov [50].
Záver
Počet vedeckých článkov, záujem o problematiku kognitívneho fungovania po liečbe rakoviny, ako aj povedomie o dôležitosti tejto témy v komunite onkologických pacientov sa v poslednom desaťročí neustále zvyšuje [5]. V kontexte onkológie sa tiež čoraz väčšia pozornosť venuje tzv. kvalite života súvisiacej s onkologickým ochorením, ktorá je definovaná ako individuálne zhodnotenie zvládania každodenných aktivít a osobnej pohody po diagnostikovaní rakoviny a po absolvovaní liečby [51]. Práve každodenné situácie sú často zdrojom uvedomenia si kognitívnych chýb a omylov, ktoré sa u pacientov vyskytujú v dôsledku oslabenia kognitívnych funkcií alebo obmedzenej kognitívnej kapacity pre vykonanie bežných úloh. Kognitívne omyly obmedzujú funkčnú nezávislosť pacientov a vykonávanie bežných povinností [52]. Zistenia prezentovaného výskumu poukazujú na zvýšenú mieru kognitívnych omylov u tretiny odliečených onkologických pacientov a tiež na súvis vnímaných ťažkostí s mierou depresie. Administrácia sebaposudzovacích metód zameraných na kognitívne fungovanie tak môže pomôcť lekárom identifikovať prítomnosť psychologického distresu [12]. Včasné sprostredkovanie informácií a odoslanie pacienta k psychológovi v rámci multidisciplinárnej spolupráce umožňuje nastavenie vhodného kognitívneho tréningu, zahájenie kognitívnej rehabilitácie či osvojenie si vhodných kompenzačných mechanizmov zmierňujúcich komplikácie prameniace z prejavov kognitívneho oslabenia v bežnom živote [4,45]. Psychológ tiež môže pomôcť pacientom akceptovať ochorenie a následky liečby, redukovať úzkosť a mieru depresívnych symptómov, čo môže prispieť k ich lepšiemu kognitívnemu fungovaniu [53].
PhDr. Veronika Boleková, PhD.
Fakulta psychológie
Paneurópska vysoká škola
Tomášikova 20
821 02 Bratislava
Slovenská republika
e-mail: veronika.bolekova@gmail.com
Obdržané/Submitted: 31. 5. 2022
Prijaté/Accepted: 30. 8. 2022
Zdroje
1. Hardy SJ, Krull KR, Wefel JS et al. Cognitive changes in cancer survivors. Am Soc Clin Oncol Educ Book 2018; 38 : 795–806. doi: 10.1200/EDBK_201179.
2. Wefel JS, Kesler SR, Noll KR et al. Clinical characteristics, pathophysiology, and management of noncentral nervous system cancer-related cognitive impairment in adults. CA Cancer J Clin 2015; 65 (2): 123–138. doi: 10.3322/caac.21258.
3. van der Willik KD, Hauptmann M, Jóźwiak K et al. Trajectories of cognitive function prior to cancer diagnosis: a population-based study. J Natl Cancer Inst 2020; 112 (5): 480–488. doi: 10.1093/jnci/djz178.
4. Fayette D, Gaherová Ľ, Kozák T et al. Chemotherapy-related cognitive impairment in patients with Hodgkin lymphoma – pathophysiology and risk factors. Klin Onkol 2017; 30 (2): 93–99. doi: 10.14735/amko201 793.
5. Dijkshoorn ABC, van Stralen HE, Sloots M et al. Prevalence of cognitive impairment and change in patients with breast cancer: a systematic review of longitudinal studies. Psychooncology 2021; 30 (5): 635–648. doi: 10.1002/pon.5623.
6. Wefel JS, Schagen SB. Chemotherapy-related cognitive dysfunction. Curr Neurol Neurosci Rep 2012; 12 (3): 267–275. doi: 10.1007/s11910-012-0264-9.
7. Vardy JL, Dhillon HM, Pond GR et al. Cognitive function in patients with colorectal cancer who do and do not receive chemotherapy: a prospective, longitudinal, controlled study. J Clin Oncol 2015; 33 (34): 4085–4092. doi: 10.1200/JCO.2015.63.0905.
8. Poppelreuter M, Weis J, Külz AK et al. Cognitive dysfunction and subjective complaints of cancer patients. A cross-sectional study in a cancer rehabilitation centre. Eur J Cancer 2004; 40 (1): 43–49. doi: 10.1016/ j.ejca.2003.08.001.
9. Vasiľková L. Impact of treatments to improve cognitive function and quality of life on cancer patients with carcinoma of the testes. Klin Onkol 2016; 29 (4): 267–273. doi: 10.14735/amko2016267.
10. Hermelink K, Untch M, Lux MP et al. Cognitive function during neoadjuvant chemotherapy for breast cancer: results of a prospective, multicenter, longitudinal study. Cancer 2007; 109 (9): 1905–1913. doi: 10.1002/cncr.22610.
11. Whittaker AL, George RP, O‘Malley L. Prevalence of cognitive impairment following chemotherapy treatment for breast cancer: a systematic review and meta--analysis. Sci Rep 2022; 12 (1): 2135. doi: 10.1038/s41598-022-05682-1.
12. Hutchinson AD, Hosking JR, Kichenadasse G et al. Objective and subjective cognitive impairment following chemotherapy for cancer: a systematic review. Cancer Treat Rev 2012; 38 (7): 926–934. doi: 10.1016/ j.ctrv.2012.05.002.
13. Hermelink K, Küchenhoff H, Untch M et al. Two different sides of ‚chemobrain‘: determinants and nondeterminants of self-perceived cognitive dysfunction in a prospective, randomized, multicenter study. Psychooncology 2010; 19 (12): 1321–1328. doi: 10.1002/pon.1695.
14. O‘Farrell E, Smith A, Collins B. Objective-subjective disparity in cancer-related cognitive impairment: does the use of change measures help reconcile the difference? Psychooncology 2017; 26 (10): 1667–1674. doi: 10.1002/pon.4190.
15. Dhillon HM, Tannock IF, Pond GR et al. Perceived cognitive impairment in people with colorectal cancer who do and do not receive chemotherapy. J Cancer Surviv 2018; 12 (2): 178–185. doi: 10.1007/s11764-017-0656-6.
16. Oh PJ. Predictors of cognitive decline in people with cancer undergoing chemotherapy. Eur J Oncol Nurs 2017; 27 : 53–59. doi: 10.1016/j.ejon.2016.12.007.
17. Jean-Pierre P, Winters PC, Ahles TA et al. Prevalence of self-reported memory problems in adult cancer survivors: a national cross-sectional study. J Oncol Pract 2012; 8 (1): 30–34. doi: 10.1200/JOP.2011.000231.
18. Gutenkunst SL, Vardy JL, Dhillon HM et al. Correlates of cognitive impairment in adult cancer survivors who have received chemotherapy and report cognitive problems. Support Care Cancer 2021; 29 (3): 1377–1386. doi: 10.1007/s00520-020-05616-5.
19. Pullens MJ, De Vries J, Van Warmerdam LJ et al. Chemotherapy and cognitive complaints in women with breast cancer. Psychooncology 2013; 22 (8): 1783–1789. doi: 10.1002/pon.3214.
20. Iconomou G, Mega V, Koutras A et al. Prospective assessment of emotional distress, cognitive function, and quality of life in patients with cancer treated with chemotherapy. Cancer 2004; 101 (2): 404–411. doi: 10.1002/cncr.20385.
21. Tsaras K, Papathanasiou IV, Mitsi D et al. Assessment of depression and anxiety in breast cancer patients: prevalence and associated factors. Asian Pac J Cancer Prev 2018; 19 (6): 1661–1669. doi: 10.22034/APJCP.2018.19.6. 1661.
22. Ramalho M, Fontes F, Ruano L et al. Cognitive impairment in the first year after breast cancer diagnosis: a prospective cohort study. Breast 2017; 32 : 173–178. doi: 10.1016/j.breast.2017.01.018.
23. Chapman B, Helmrath S, Derakshan N. Perceived cognitive functioning and its influence on emotional vulnerability in breast cancer. Health Psychol Open 2019; 6 (2): 2055102919871661. doi: 10.1177/2055102919871661.
24. Noal S, Levy C, Hardouin A et al. One-year longitudinal study of fatigue, cognitive functions, and quality of life after adjuvant radiotherapy for breast cancer. Int J Radiat Oncol Biol Phys 2011; 81 (3): 795–803. doi: 10.1016/j.ijrobp.2010.06.037.
25. Shilling V, Jenkins V. Self-reported cognitive problems in women receiving adjuvant therapy for breast cancer. Eur J Oncol Nurs 2007; 11 (1): 6–15. doi: 10.1016/j.ejon.2006.02.005.
26. Lycke M, Pottel L, Pottel H et al. Predictors of baseline cancer-related cognitive impairment in cancer patients scheduled for a curative treatment. Psychooncology 2017; 26 (5): 632–639. doi: 10.1002/pon.4200.
27. Vearncombe KJ, Rolfe M, Wright M et al. Predictors of cognitive decline after chemotherapy in breast cancer patients. J Int Neuropsychol Soc 2009; 15 (6): 951–962. doi: 10.1017/S1355617709990567.
28. Ahles TA, Saykin AJ, Furstenberg CT et al. Neuropsychologic impact of standard-dose systemic chemotherapy in long-term survivors of breast cancer and lymphoma. J Clin Oncol 2002; 20 (2): 485–493. doi: 10.1200/JCO.2002.20.2.485.
29. Wazqar DY. Cognitive dysfunction and its predictors in adult patients with cancer receiving chemotherapy: a cross-sectional correlational study. J Nurs Res 2019; 27 (6): e56. doi: 10.1097/jnr.0000000000000340.
30. Quesnel C, Savard J, Ivers H. Cognitive impairments associated with breast cancer treatments: results from a longitudinal study. Breast Cancer Res Treat 2009; 116 (1): 113–123. doi: 10.1007/s10549-008-0114-2.
31. Bakoyiannis I, Tsigka EA, Perrea D et al. The impact of endocrine therapy on cognitive functions of breast cancer patients: a systematic review. Clin Drug Investig 2016; 36 (2): 109–118. doi: 10.1007/s40261-015-0364-9.
32. Schilder CM, Eggens PC, Seynaeve C et al. Neuropsychological functioning in postmenopausal breast cancer patients treated with tamoxifen or exemestane after AC-chemotherapy: cross-sectional findings from the neuropsychological TEAM-side study. Acta Oncol 2009; 48 (1): 76–85. doi: 10.1080/02841860802314738.
33. Navarra-Ventura G, Fernandez-Gonzalo S, Serra-Blasco M et al. Cognitive failures in healthy middle-aged Spanish adults: a cross-sectional study describing magnitude categories of subjective cognitive deficits. Eur J Psychiatry 2019; 33 (3): 135–141. doi: 10.1016/j.ejpsy.2019.04.001.
34. Bridger RS, Johnsen SÅ, Brasher K. Psychometric properties of the cognitive failures questionnaire. Ergonomics 2013; 56 (10): 1515–1524. doi: 10.1080/001 40139.2013.821172.
35. Broadbent DE, Cooper PF, FitzGerald P et al. The cognitive failures questionnaire (CFQ) and its correlates. Br J Clin Psychol 1982; 21 (1): 1–16. doi: 10.1111/j.2044-8260.1982.tb01421.x.
36. Carrigan N, Barkus E. A systematic review of cognitive failures in daily life: healthy populations. Neurosci Biobehav Rev 2016; 63 : 29–42. doi: 10.1016/j.neubiorev.2016.01.010.
37. Paiva GC, Fialho MB, Costa DS et al. Ecological validity of the five digit test and the oral trails test. Arq Neuropsiquiatr 2016; 74 (1): 29–34. doi: 10.1590/0004-282X20150184.
38. Jensen JH, Miskowiak KW, Purdon S et al. Screening for cognitive impairment among patients with work-related stress complaints in Denmark: validation and evaluation of objective and self-report tools. Scand J Work Environ Health 2022; 48 (1): 71–80. doi: 10.5271/sjweh.3990.
39. Wallace CJ. Confirmatory factor analysis of the cognitive failures questionnaire: evidence for dimensionality and construct validity. Pers Individ Differ 2004; 37 (2): 307–324. doi: 10.1016/J.PAID.2003.09.005.
40. Boleková V, Chlebcová V. Overenie psychometrických charakteristík Dotazníka kognitívnych zlyhaní. In: Quaere. Recenzovaný sborník příspěvků interdisciplinární mezinárodní vědecké konference doktorandů a odborných asistentů. Hradec Králové, 2020.
41. Kroenke K, Spitzer RL, Williams JB. The PHQ-9: validity of a brief depression severity measure. J Gen Intern Med 2001; 16 (9): 606–613. doi: 10.1046/j.1525-1497.2001.01 6009606.x.
42. Spitzer RL, Kroenke K, Williams JB et al. A brief measure for assessing generalized anxiety disorder: the GAD-7. Arch Intern Med 2006; 166 (10): 1092–1097. doi: 10.1001/archinte.166.10.1092.
43. World Health Organization. Programme on mental health: WHOQOL user manual, 2012 revision. World Health Organization, 1998.
44. Aaronson NK, Bullinger M, Ahmedzai S. A modular approach to quality-of-life assessment in cancer clinical trials. Recent Results Cancer Res 1988; 111 : 231–249. doi: 10.1007/978-3-642-83419-6_27.
45. Lange M, Joly F, Vardy J et al. Cancer-related cognitive impairment: an update on state of the art, detection, and management strategies in cancer survivors. Ann Oncol 2019; 30 (12): 1925–1940. doi: 10.1093/annonc/mdz410.
46. Eskildsen A, Andersen LP, Pedersen AD et al. Cognitive impairments in former patients with work-related stress complaints – one year later. Stress 2016; 19 (6): 559–566. doi: 10.1080/10253890.2016.1222370.
47. Dalgaard VL, Hviid Andersen J, Pedersen AD et al. Cognitive impairments and recovery in patients with work-related stress complaints – four years later. Stress 2021; 24 (3): 294–302. doi: 10.1080/10253890.2020.1797 673.
48. Pullens MJ, De Vries J, Roukema JA. Subjective cognitive dysfunction in breast cancer patients: a systematic review. Psychooncology 2010; 19 (11): 1127–1138. doi: 10.1002/pon.1673.
49. Ng T, Dorajoo SR, Cheung YT et al. Distinct and heterogeneous trajectories of self-perceived cognitive impairment among Asian breast cancer survivors. Psychooncology 2018; 27 (4): 1185–1192. doi: 10.1002/pon.4635.
50. Vlčková I, Pavelková K, Kepák T et al. Changes of neurocognitive functions as result of cancer treatment in children and adolescents. Klin Onkol 2008; 21 (5): 294–302.
51. Derogar M, van der Schaaf M, Lagergren P. Reference values for the EORTC QLQ-C30 quality of life questionnaire in a random sample of the Swedish population. Acta Oncol 2012; 51 (1): 10–16. doi: 10.3109/0284186X.2011.614636.
52. Boykoff N, Moieni M, Subramanian SK. Confronting chemobrain: an in-depth look at survivors‘ reports of impact on work, social networks, and health care response. J Cancer Surviv 2009; 3 (4): 223–232. doi: 10.1007/s11764-009-0098-x.
53. Kuba K, Weißflog G, Götzea H et al. The relationship between acceptance, fatigue, and subjective cognitive impairment in hematologic cancer survivors. Int J Clin Health Psychol 2019; 19 (2): 97–106. doi: 10.1016/ j.ijchp.2018.12.001.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2023 Číslo 1- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
- Nejasný stín na plicích – kazuistika
-
Všechny články tohoto čísla
- Onkolytické viry a léčení nádorového bujení
- Prediktívne biomarkery v imunoterapii triple-negatívneho karcinómu prsníka – súčasné poznatky a perspektívy
- Editorial
- Kapacita pro výstavbu infrastruktury onkologické péče v oblasti Karnataka – současnost a budoucnost
- Prediktory kognitívnych omylov u odliečených onkologických pacientov
- Informace z České onkologické společnosti
- Perzistencia pri denosumabe u slovenských pacientov s kostnými metastázami – prospektívna observačná štúdia
- Lymfopenie způsobená radioterapií – možný kritický faktor v současné onkologické léčbě
- Raritný prípad obrovského mucinózneho cystadenómu vaječníka zapríčiňujúceho akútnu renálnu insuficienciu a kompartment syndróm
- Poděkování recenzentům
- Unikátní přirozená historie EGFR mutovaného adenokarcinomu
- Vzácné choroby provázené hypergamaglobulinemií a zánětlivými projevy
- Hereditární nádorová onemocnění v klinické praxi
- Komplikace onkologických pacientů a možnosti jejich řešení v primární péči
- Snížení rizika užívání tabáku – mýtus, nebo realita?
- prof. RNDr. PhMr. Jan Kovařík, DrSc.
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Onkolytické viry a léčení nádorového bujení
- Lymfopenie způsobená radioterapií – možný kritický faktor v současné onkologické léčbě
- Prediktívne biomarkery v imunoterapii triple-negatívneho karcinómu prsníka – súčasné poznatky a perspektívy
- Prediktory kognitívnych omylov u odliečených onkologických pacientov
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



