-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Inhibitory protonové pumpy – nové molekuly, nové poznatky
Proton pump inhibitors – new molecules, new knowledge
Proton pump inhibitors (PPI) are the primary medication in the treatment of acid-related diseases. All proton pump inhibitors are weak bases selectively metabolised in an acid environment which block the function of active proton pumps. Proton pump inhibitors provide efficient treatment for gastroesophageal reflux disease, Helicobacter pylori, functional dyspepsia and NSAID gastropathy. PPI may be helpful in patients with eosinophilic oesophagitis. PPI of the first generation comprise omeprazole, pantoprazole and lansoprazole, the second one is represented by esomeprazole and rabeprazole. Proton pump inhibitors differ in pharmacokinetic properties but these differences do not necessarily have clinically relevant consequences. Generally, second generation proton pump inhibitors provide a faster onset of effect, longer gastric secretion inhibition, and specifically the effect of rabeprazole is less dependent on the method of administration and has less influence on the function of cytochrome P450. The effect of proton pump inhibitors, particularly the first generation, is modified by the genetic variety of the CYP2C19 enzyme and is significantly lower in rapid metabolisers. Proton pump inhibitors are very safe and immediate complications are rare. They can cause progression of gastritis in Helicobacter infection. In spite of causing hypergastrinemia, they do not have malignant potential. Their long-term administration is associated with an increased risk of pelvis and hip fractures, community-acquired pneumonia, and clostridium infection. They decrease the effect of antiaggregant therapy with clopidogrel, and increase the risk of recurrent cardiovascular events. This effect is not proven in prasugrel. We cannot expect any potential progression in developing new molecules or PPI formulas. The instructions for patients are usually not clearly presented and often lack important information.
Keywords:
proton pump inhibitors – omeprazole – lansoprazole – pantoprazole – rabeprazole – esomeprazole – side effects – interactions
Autoři: J. Špičák; K. Chmelová
Působiště autorů: Klinika hepatogastroenterologie, Transplantcentrum, IKEM, Praha
Vyšlo v časopise: Kardiol Rev Int Med 2016, 18(1): 67-75
Kategorie: Kardiologická revue
Souhrn
Hlavními medikamenty v léčbě acidopeptických onemocnění jsou inhibitory protonové pumpy (IPP). Všechny IPP jsou slabé zásady selektivně se metabolizující v kyselém prostředí a blokující funkci aktivní protonové pumpy. IPP poskytují účinnou léčbu u refluxní nemoci jícnu, eradikace Helicobacter pylori, funkční dyspepsie a gastropatie z nesteroidních antirevmatik. Jsou také součástí léčby u eozinofilní ezofagitidy. IPP první generace zahrnují omeprazol, pantoprazol a lansoprazol, druhé generace esomeprazol a rabeprazol. IPP se liší ve farmakokinetických charakteristikách, tyto rozdíly však nemusí mít klinicky relevantní důsledky. Obecně IPP druhé generace zajišťují rychlejší nástup účinku, protrahovanější inhibici žaludeční sekrece a zejména účinek rabeprazolu je méně závislý na způsobu podávání a méně ovlivňuje funkce cytochromu P450. Účinnost IPP zejména první generace ovlivňuje genetická variabilita enzymu CYP2C19 a je významně nižší u rychlých metabolizátorů. IPP jsou velmi bezpečné a bezprostřední komplikace jsou výjimečné. U helikobakterové infekce vedou k progresi gastrititidy. Přestože způsobují hypergastrinemii, nevykazují IPP maligní potenciál. Jejich dlouhodobé podávání je spojeno s vyšším rizikem fraktur páteře a kyčlí, komunitních pneumonií a klostridiové střevní infekce. Mohou vést ke snížení účinnosti antiagregační léčby s klopidogrelem se zvýšeným rizikem recidivujících kardiovaskulárních příhod, což neplatí pro prasugrel. V nejbližší době nelze očekávat v jiných molekulách či lékových úpravách zásadní pokrok. Příbalové letáky jsou vesměs nevhodně konstruovány a chybí v nich často zásadní informace.
Klíčová slova:
inhibitory protonové pumpy – omeprazol – lansoprazol – pantoprazol – rabeprazol – esomeprazol – vedlejší účinky – interakceÚvod
Žaludeční acidita a její fyziologické a patologické souvislosti přitahují pozornost od počátku civilizace. Léky ovlivňující acidopeptická onemocnění jsou jedny z nejužívanějších vůbec a jejich účinnost a bezpečnost jsou trvale významnými tématy. V současné době máme k dispozici léky vysoce účinné, přesto však populační zatížení těmito chorobami neklesá. Při často celoživotní potřebě této farmakoterapie nabývají významu interakce s léky podávanými u jiných indikací a komplikace vyplývající z jejich dlouhodobého užívání. Objevují se stále nové poznatky, které by měla zohlednit klinická praxe. Cílem tohoto přehledu je podat informaci o nových poznatcích získaných v posledních letech.
Inhibitory protonové pumpy (IPP) zůstávají hlavními léky snižujícími žaludeční sekreci a na této skutečnosti se patrně v dohledné době nic nezmění. Jsou podstatně účinnější než antagonisté H (histamin) 2 receptorů (AH2R) a zatlačily všechny jiné léky ovlivňující žaludeční sekreci do pozadí. Jako první byl zaregistrován omeprazol v roce 1989 a následovaly jej lansoprazol (1995), pantoprazol (1997), rabeprazol (1999) a S-enantiomer omeprazolu v roce 2001.
IPP jsou různě substituované benzimidazoly a slabé zásady, které se proto jako primárně neúčinné pro-léky téměř výlučně akumulují v kyselém prostředí parietálních buněk žaludku. Jejich disociační konstanta (pKa) je přibližně 4 u omeprazolu a lansoprazolu, 3,9 u pantoprazolu a 5 u rabeprazolu. V opačném poměru probíhá jejich konverze: rabeprazol 4,71 > omeprazol 4,09 > lansoprazol 3,92 > pantoprazol 3,89. Zde dochází k jejich přeměně na kyselinu sulfonovou a deriváty sulfenamidů, které se váží na SH skupiny cysteinových reziduí na α-podjednotce protonové pumpy, tj. H + K + ATP. Vazebná místa jednotlivých prazolů, a tedy typy cysteinových podjednotek, jsou různá. Kovalentní inhibice enzymu H + K + ATP vede ke specifickému a dlouhodobému zablokování této jedinečné pumpy, která pracuje proti iontovému gradientu 1 : 1 000 000 s výsledkem pH 0,8 – 1,0 uvnitř kanalikulu parietální buňky. IPP jsou nejaktivnější při plné sekreci HCl postprandiálně, což má bezprostřední klinický důsledek. Protože protonová pumpa je nejaktivnější po dlouhodobém lačnění, IPP by se měly s výjimkou rabeprazolu podávat před prvním denním jídlem. Bylo prokázáno, že při požití omeprazolu 30 min před snídaní byla doba pH < 4,0, a tedy pro hojení slizničních lézí nedostatečná, pouhých 17,2 % z 24 hod oproti 42,0 %, pokud jídlo nenásledovalo. Během jednoho jídla nejsou aktivní ani všechny parietální buňky ani všechny protonové pumpy. Protože IPP blokují pouze aktivní protonové pumpy, pokles sekrece po jednorázovém podání není optimální, a stane se tak až po několika dnech. Tento interval může být zkrácen při více denních dávkách. Z těchto důvodů nelze od příležitostného podávání on-demand očekávat dostatečný efekt na rozdíl od AH2R, které působí bezprostředně. Plné účinnosti IPP také brání současné podávání s jinými léky snižujícími sekreci. Poločas existence bílkoviny protonové pumpy je 54 hod u krys a snad i u člověka, takže denně je syntetizováno přibližně 20 % nových pump. Po přerušení léčby nastává obnovení žaludeční sekrece za 24 – 48 hod [1].
Omeprazol
Racemická směs dvou enantiomerů je acidolabilní a vyžaduje acidorezistentní úpravu. Rychle se vstřebává a jeho metabolity se vylučují převážně močí. Je metabolizován játry enzymy cytochromu P450, zejména CYP2C19 na hydroxyl a desmetylmetabolity a CYP3A4 na sulfony. Polymorfizmus CYP2C19 významně ovlivňuje jeho metabolizmus (méně esomeprazolu – viz dále). Podle metabolické účinnosti enzymu lze klasifikovat jedince na homozygotní rychlé metabolizátory, heterozygotní rychlé metabolizátory a pomalé metabolizátory, jejichž prevalence činí do 3,8 % v euroatlantické populaci a až 23 % v populaci asijské. Pomalá metabolizace vyúsťuje ve větší účinnost s násobně větší plochou pod křivkou (area under the curve – AUC) sledovaných funkčních parametrů. Podle recentní studie byla expozice omeprazolu vyjádřena AUC po perorálním podání 40 mg 1 : 2,7 : 9,0 u homozygotních rychlých metabolizátorů, heterozygotních metabolizátorů a pomalých metabolizátorů. Rozdíly se poněkud smazávají ve stáří. Objevují se stále nové varianty alel kódujících nefunkční protein.
Lansoprazol
Rychle se vstřebává a jeho farmakokinetika po opakovaném podávání je stejná jako po jednorázové aplikaci. Metabolizuje se enzymy CYP3A4 a CYP2C19, z čehož plyne problém interakcí např. s klaritromycinem, který zvyšuje jeho účinnost.
Pantoprazol
Také pantoprazol se po orální aplikaci enterosolventních tablet rychle vstřebává. Jeho vysoká biologická dostupnost není ovlivněna výší dávky ani příjmem jídla. Je metabolizován méně CYP2C19 a více CYP3A4 a nevykazuje interakce kromě těch, které vyplývají z potlačení kyselé žaludeční sekrece. Jeho hladinu klaritromycin nezvyšuje [2].
Esomeprazol
Většina léků se podává ve formě racemických směsí. Řada biologických procesů je ovšem prostorově selektivních, z čehož vyplývá, že prostorově opačně orientovaná „dvojčata“ mohou mít různou účinnost. Např. receptory metabolizujících enzymů mohou preferenčně vázat jednu z obou prostorových variant (enantiomerů). Poměrně nedávno s velkým odstupem proti jiným zemím byl na náš trh uveden S-enanthiomer omeprazolu esomeprazol. Jeho specifickými vlastnostmi jsou vyšší biologická dostupnost, menší interindividuální variabilita a relativně odlišná metabolizace v játrech: jestliže racemická směs omeprazol je z 90 % metabolizován CYP2C19, u esomeprazolu je to jen 70 %. Esomeprazol je relativně více metabolizován CYP3A4 a je tedy méně závislý na geneticky podmíněné variabilitě prvního z enzymů s možným důsledkem méně významné interakce např. s klopidogrelem. Podobně se zkoumají prostorově selektivní enantiomery ostatních prazolů, ale zdá se, že žádný z nich nevykazuje komplexně příznivější předpoklady než užívané racemické směsi [3].
Rabeprazol
Rabeprazol je spolu s esomeprazolem představitel tzv. druhé generace IPP. Jeho pKa1 je nejvyšší, tudíž je nejvyšší také jeho aktivace v sekrečním kanálku parietální buňky, a to i v méně kyselém prostředí. Parietální buňky vznikají na povrchu indických žlázek a stárnutím migrují k jejich dnu, kde je acidita slabší. Rabeprazol se proto aktivuje v relativně větším počtu parietálních buněk než ostatní IPP. Neovlivňuje také negativně recyklaci jejich tubulovezikulárního aparátu. Inhibice protonových pump je při podávání rabeprazolu tedy prakticky konzistentně 100% ve srovnání s lansoprazolem (66 – 100 %), omeprazolem (47 – 83 %) a pantoprazolem (20 – 49 %). Rychle se vstřebává a jeho biologická dostupnost se s dalšími dávkami nezvyšuje. Jeho farmakokinetické parametry se nemění u specifických věkových skupin jako jsou malé děti a senioři a neovlivňuje je renální a jaterní dysfunkce. Současné podávání s jídlem zpomaluje jeho vstřebávání, ale neovlivňuje biologickou dostupnost tak výrazně jako ostatní IPP. V poslední době byla vyvinuta nová formule obsahující specifickou úpravu umožňující uvolňování rabeprazolu bez ohledu na pH v celém průběhu tenkého i tlustého střeva, což zvyšuje dobu účinné koncentrace v plazmě. Bylo prokázáno, že nová formule poskytuje protrahovanější vzestup pH žaludku ve srovnání s esomeprazolem i běžnou úpravou rabeprazolu. Metabolizmus rabeprazolu je jedinečný, protože se na inaktivní thioeter nemetabolizuje cytochromem P450. Účast CYP2C19 a CYP3A4 v jeho metabolizaci je menší než u ostatních IPP, takže jeho účinnost i interakce vykazují minimální ovlivnění polymorfizmem těchto enzymů. AUC hodnoty u jednotlivých metabolizátorů byly 1,0 : 1,3 : 1,8, a tedy daleko méně rozdílné, než je tomu u omeprazolu [4].
Refluxní nemoc jícnu
Cílem léčby obecně je zhojení slizničních lézí, prevence rekurence a komplikací a úleva od obtíží a zlepšení kvality života. Poslední cíle jsou více zvažovány v posledních letech s narůstajícím zájmem o neerozivní refluxní ezofagititidu a extraezofageální symptomatologii refluxu. Nejčastějším kritériem je žaludeční pH v důsledku nestandardizovaného hodnocení pH jícnového refluxátu. Nejčastějším zástupným markerem účinnosti jednotlivých farmak je doba, během které je pH žaludku > 4. Objevují se názory, že vhodnějším parametrem by bylo pH > 3 nebo dokonce > 2. Refluxní nemoc jícnu (GERD) je primárně multifaktoriální motorická porucha, v jejímž důsledku se zjednodušeně řečeno obsah žaludku ve zvýšené míře dostává do oblasti jícnu. Abnormální expozice jícnu žaludečnímu obsahu, a tedy HCl, není obvykle spojena s její hypersekrecí. Protože léky upravující dostatečně a specificky poruchu motility při GERD chybí, léčba spočívá v aplikaci antisekreční léčby, přičemž klinická účinnost IPP převažující účinek AH2R byla prokázána jednoznačně v mnoha srovnávacích studiích. Podle již historické metaanalýzy Chiby et al dosáhla léčba IPP vyhojení slizničních lézí u 85 % ve srovnání s 52% úspěšností u AH2R [5], což je v přímé souvislosti s delším a hlubším útlumem sekrece HCl. Existuje řada studií srovnávajících jednotlivá IPP. Podle jedné z nich obsahující deset studií poskytuje esomeprazol přibližně o 5 % vyšší úspěšnost než ostatní bez přímého srovnání s rabeprazolem [6]. Protože jen 30 % nemocných s GERD vykazuje slizniční erozivní změny, je úleva od obtíží hlavním cílem u zbývajících 70 % nemocných. Podle již citované studie Chiby et al udávalo 77 % nemocných při IPP úlevu po osmi týdnech léčby ve srovnání s 48 % uživatelů AH2R.
Srovnáním rabeprazolu s esomeprazolem se zabývá studie zaměřená na mírnou a střední formu erozivní ezofagititidy. Na rozdíl od většiny jiných studií se u obou skupin podával IPP v dávce 40 mg. Ve všech zkoumaných parametrech (symptomy, endoskopický nález, kvalita života) předčil rabeprazol statisticky významně esomeprazol. U endoskopického nálezu byl rozdíl v normalizaci 30 % a zlepšení 55 % ve prospěch rabeprazolu [7]. V roce 2015 byla publikována švédsko-britská metaanalýza srovnávající IPP s chirurgickým řešením GERD zahrnující čtyři randomizované studie. Vysokou účinnost vykázaly oba postupy, i když celkové zlepšení kvality života bylo poněkud vyšší u pacientů, kteří podstoupili operaci [8]. De Jonge et al nezaznamenali významný rozdíl mezi těmito léčebnými přístupy s ohledem na riziko vzniku adenokarcinomu v terénu Barrettova jícnu [9]. V jiné studii byli prospektivně monitorováni nemocní s Barrettovým jícnem, kteří byli léčeni rabeprazolem v dávce 20 mg 2× denně. Normalizace refluxu byla zaznamenána po jednom měsíci léčby v 79 % případů a u zbylých pacientů mělo pozitivní účinek zdvojnásobení denní dávky [10].
Ve Spojených státech amerických jsou všechny účinné lékové skupiny volně dostupné bez nutnosti preskripce. V této souvislosti byla publikována práce, která monitorovala symptomatickou úlevu a správné užívání IPP u pacientů, kteří si léky volně kupovali, ve srovnání s pacienty, kterým byly IPP předepisovány praktickým lékařem (PL) a gastroenterologem. Výzkum prokázal 2,86× vyšší účinnost léčby ve skupině, která měla léčbu indikovanou PL, a dokonce 3,77× vyšší úspěšnost, pokud léčbu vedl gastroenterolog. Příčinou neúspěchu byla obvykle nesprávná indikace, špatné dávkování a nedostatečná délka léčby nebo nevhodná denní doba požití léků, což také často vedlo k jejich nadbytečnému užívání [11].
Eradikace Helicobacter pylori
IPP v násobné dávce jsou nedílnou součástí jakéhokoli eradikačního schématu. Eradikaci hypoteticky ovlivňuje genotyp CYP2C19, protože u rychlých metabolizátorů omeprazolu a lansoprazolu lze očekávat sníženou účinnost inhibice žaludeční sekrece. Zcela recentně byla publikována metaanalýza studií zaměřených na účinnost eradikace v souvislosti s variantami CYP2C19 zahrnující 16 studií. Byly zjištěny významné rozdíly mezi homozygotními a heretozygotními rychlými metabolizátory (OR 0,724), mezi homozygotními rychlými a pomalými metabolizátory (OR 0,507) i mezi heterozygotními rychlými a pomalými metabolizátory (OR 0,688). Subanalýza prokázala rozdíly mezi jednotlivými IPP: u omeprazolu byl rozdíl mezi homozygotními a heterozygotními metabolizátory OR 0,329, zatímco u lansoprazolu OR 0,692. Mezi homozygotními rychlými a pomalými metabolizátory byl u omeprazolu rozdíl OR 0,232 a u lansoprazolu OR 0,441. U esomeprazolu a rabeprazolu nebyla účinnost eradikace genetickými variantami ovlivněna. Rozdíl mezi generacemi v dosažení očekávaných výsledků vyznívá jednoznačně ve prospěch druhé generace a genetickou variabilitou je nejvíce zatížen omeprazol [12].
Prevence gastropatie a jejích důsledků
Aspirin a další nesteroidní antirevmatika (NSAID) jsou vůbec nejužívanější léky v populaci, ať už z indikace antiagregace či pro antirevmatické a analgetické působení. Jejich gastrotoxicita je různá, nicméně vychází z inhibice syntézy prostaglandinů a do určité míry z přímého poškození sliznice žaludku. Snižuje se angiogeneze, průtok kapilárami, produkce bikarbonátu a hlenu, agregace trombocytů, zvyšuje se adherence leukocytů a zpětná difuze kyseliny.
Ulcerózní léze se u aspirinu nejčastěji vyskytují v těle žaludku, na angulární řase a v bulbu duodena a jsou často mnohočetné. Podle studie na dobrovolnících vznikají často již během prvních 24 hod. Riziko lézí závisí na dávce a do určité míry také projektivně působí enterosolventní úprava medikamentu.
V prevenci a léčbě gastropatie a jejích důsledků a komplikací připadá v úvahu podávání gastrotoxických COX-2 inhibitorů a simultánní podávání gastroprotektivních léků.
Odůvodnění podávání prostaglandinů spočívá v substituci jejich deplece způsobené NSAID. Misoprostol (u nás není dostupný) redukuje žaludeční léze, avšak nemá vliv na případné dyspeptické obtíže a další vedlejší gastrointestinální vedlejší účinky. V současné době se zkouší kombinace misoprostolu s diklofenacem v jedné tabletě. Na poškození žaludku při NSAID se podílí kyselý obsah a zásadní význam hraje v prevenci a léčbě gastropatie – zvýšení pH . AH2R jsou účinné v hojení slizničních lézí, mají však malý vliv na doprovodné krvácení. IPP jsou účinnější, nejpřesvědčivější výsledky dosáhly esomeprazol a rabeprazol podobně jako v jiných indikacích. Zkouší se kombinace omeprazol a ketoprofen v jedné tabletě. Nevýhodou PPI je, že dostatečně nepůsobí na další komplikace NSAIDs jako kolopatie a enteropatie a v případě helikobakterové toxicity negativně ovlivňují vývoj gastrititidy.
Další možností je podávání COX-2 inhibitorů, nevýhodou je kardiotoxicita v důsledku inhibice syntézy prostacyklinu. Řada prací se zabývá mírou rizika gastrointestinálních změn u uživatelů aspirinu a dalších NSAID. Evropská metaanalýza kvalifikuje rizikové faktory na jednoznačné (vysoký věk nad 65 – 70 let, vřed v anamnéze, současné užívání antikoagulancií, kortikosteroidů, aspirinu a více druhů NSAID), kontraverzní (vysoké dávky NSAID, současné užívání klopidogrelu či SSRI – selective serotonin reuptake inhibitor, gastrointestinální symptomy v anamnéze, obtěžující revmatoidní artritida a choroby kardiovaskulární) a additivní, kterým je helikobakterová infekce [13]. Eradikace je tedy žádoucí, nicméně stran další gastroprotekce se výsledky studií různí a spíše se zdá, že je nutná [14]. Vzhledem ke komplexnosti problému není reálné odůvodněné upřednostnění jednotlivého IPP. V prevenci se uplatňují AH2R i IPP a přirozeně existují i studie srovnávací jednotlivé medikamenty. Problematiku konečně shrnuje podrobný doporučený postup Americal College of Gastroenterology: Konstatuje se, že u 25 uživatelů NSAID vzniká vřed, gastrotoxicita zapříčiňuje ročně v USA 100 000 hospitalizací a až 10 000 úmrtí. Rizikové faktory přibližně odpovídají evropské metaanalýze, zdůrazňuje se potřeba eradikace H. pylori. U AH2R se soudí, že zabrání vzniku vředu duodenálního, nikoli však žaludečního, a účinnější jsou ve vysokých dávkách. Podle jednotlivých srovnávacích studií byly IPP účinnější než AH2R i misoprostol, rozdíly mezi esomeprazolem 20 a 40 mg byly bezvýznamné. Léčba AH2R je levnější. COX-2 inhibitory snižují významně riziko gastropatie, ale tento efekt mizí při společném užívání aspirinu. Vždy se individuálně zvažují kardiovaskulární a gastrointestinální rizika (tab. 1) [15].
Tab. 1. Kardiovaskulární vs. gastrotoxické riziko. 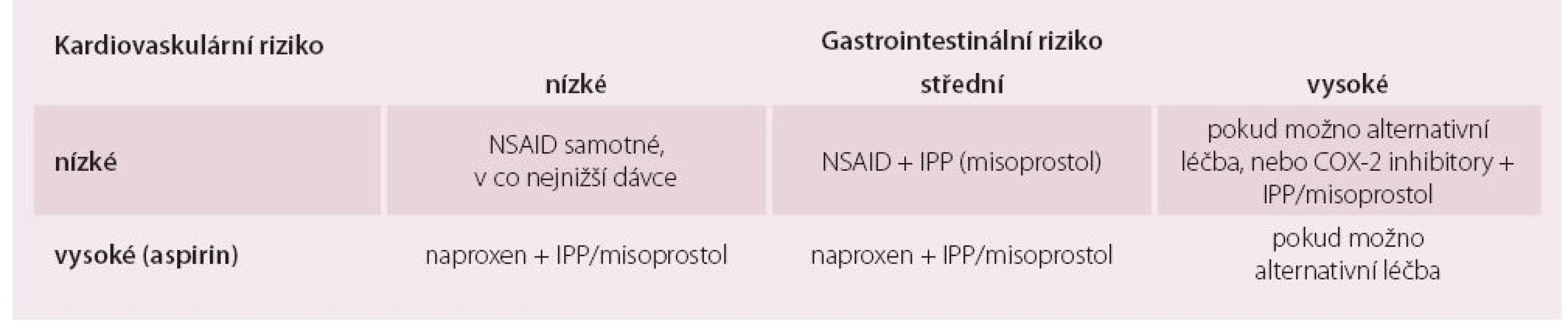
Střední gastrointestinální riziko – jeden nebo dva rizikové faktory; vysoké riziko – předchozí vřed, současné užívání kortikoidů či antikoagulancií nebo dva a více dalších rizikových faktorů. Naproxen vykazuje kardioprotektivní a nikoli kardiotoxické vlastnosti.
Pozoruhodným fenoménem je NSAID enteropatie. Vzniká s odstupem, podílí se na ní enterohepatální oběh NSAID, změny v metabolizmu prostaglandinů a gramnegativní bakterie. IPP enteropatii zhoršují (výskyt vředů) v důsledku snížení acidity žaludku a změn bakteriálního složení. Pomoci může misoprostol. Japonská randomizovaná studie prokázala, že celecoxib v kombinaci s rabeprazolem může způsobit také časný vznik erozí jejuna (RR 2,67) [16].
Stresový vřed, krvácení
Problémem neurologických, kriticky nemocných pacientů je vznik stresového vředu a až 15% riziko krvácení. Metaanalýza osmi randomizovaných studií jasně prokázala snížené riziko krvácení u nemocných léčených IPP ve srovnání s placebem (RR 0,31; p ≤ 0,00001), a antisekreční léčba by proto měla být nedílnou součástí komplexní léčby [17]. Pozornost si zaslouží současný trend preferovat orální formu IPP před intravenózní, výsledky srovnávacích studií jsou totiž prakticky totožné [18].
Funkční dyspepsie
Vzhledem k nejasné patogenezi a variabilitě dyspepsie ve všech ohledech je nutné brát výsledky studií obecně s nadhledem. Některé prokázaly účinnost IPP, v jiných se výsledek nelišil od placeba. Několik doporučených postupů vyznívá v souhrnu přibližně takto:
IPP jsou indikovány jako lék první volby v oblastech s nízkou prevalencí helikobakterové infekce a dále tam, kde příznaky přetrvávají po její eradikaci. Dávka má být standardní, ale v případě úspěchu má být držena na co nejnižší úrovni, naopak v případě snížení účinnosti může být zdvojnásobena. IPP jsou vhodné zejména u pseudoulcerózní dyspepsie a pyrózy. V případě pozitivního účinku lze po 4 – 8 týdnech zvážit převedení na AH2R [19].
Eozinofilní ezofagitida
Eozinofilní ezofagitida (EoE) je chronické zánětlivé imunitní onemocnění jícnu se stále se zvyšující prevalencí. Klinicky se toto onemocnění projevuje nespecifickými příznaky (dysfagie, atypické bolesti na hrudi, zvracení, uvíznutí potravy, pyróza aj.) a současně se vyskytují polyvalentní nebo potravinové alergie. Příznačnými endoskopickými rysy jsou distální zúžení jícnu, cirkulární zvrásnění tzv. tracheizace, podélné slizniční defekty a bělavý exsudát. Histologicky je přítomen zánětlivý infiltrát s predominancí eozinofilů (> 15 eozinofilů/ zorné pole). Terapeuticky se zavádějí dietní opatření, IPP, topická léčba kortikosteroidy a v indikovaných případech se provádí endoskopická dilatace jícnu. Výzkum u této nozologické jednotky je dynamický proces s rychle se objevujícími novými poznatky. Recentně publikované doporučené postupy zavedly nový pojem „PPI-responsive esophageal eosinophilia“ (PPI-REE), která se svým průběhem a léčbou od EoE liší.
Doporučení z roku 2011 zahrnují v rámci diagnostiky nejprve vyloučení GERD jako potenciální příčiny ezofageální eozinofilie, a to podáváním antisekreční léčby a provedením pH-metrie. Z klinického hlediska je toto rozlišení nutné vzhledem k odlišnému přístupu k léčbě [20].
Zatímco u PPI-REE je přítomen abnormální pH-metrický nález a dobrá klinická i histologická odpověď na léčbu IPP, u EoE je typická normální pH-metrie a absence klinické odpovědi na osmitýdenní terapii IPP. Výsledky jednotlivých studií jsou příznačně kontraverzní, a tak Vazquez-Elizondo et al publikovali pokus o léčbu pacientů s EoE omeprazolem v dávce 40 mg na den rozdělené do dvou denních dávek po dobu osmi týdnů se zlepšením histologického nálezu ve více než 50 % případů a s kompletní klinicko-patologickou remisí u třetiny pacientů [21].
Následně Lucendo et al shrnuli úspěšnost léčby IPP u EoE v metaanalýze celkem 33 studií. Účinnost této léčby v navození remise byla v průměru 50,5 %. Nejlepší účinek byl zaznamenán u lansoprazolu a rabeprazolu s účinností 70,2 %, resp. 72,3 %, horší výsledky prokázal omeprazol (53,5 %), nejméně účinný byl esomeprazol (46,8 %) [22]. Přestože kritériem EoE je absence klinicko-patologické odpovědi na terapii IPP, jsou doporučovány jako lék volby v rámci komplexní léčby. Důvodem je doposud neuspokojivě popsaný vztah mezi PPI-REE, EoE a GERD a fakt, že mechanizmy působení IPP jsou komplexnější, než se dříve předpokládalo. Kromě antisekrečního účinku je dokumentována také protizánětlivá a antieozinofilní aktivita způsobená snížením Th2 mediované chemoatrakce eozinofilů. Podle jiných prací IPP přímo inhibují neutrofily a monocyty, snižují expresi zánětlivých cytokinů a zároveň snižují expozici alergenu obnovením slizniční integrity v jícnu. Blokují také interleukin (IL) IL-4 - a IL-13-stimulovanou sekreci eotaxinu-3 ovlivněním STAT-6 signalizační dráhy a následným snížením jeho exprese. Udržení dlouhodobé remise u PPI-REE je signifikantně snížené u rychlých metabolizátorů CYP2C19 a u pacientů s rinokonjunktivitidou. IPP mají také přímý baktericidní a fungicidní efekt. Z těchto důvodů je predikce odpovědi na léčbu IPP obtížná a je nutno se řídit individuálně klinickým stavem pacienta [23].
Komplikace
Vzhledem k objemu veškeré medikace jsou IPP léky neobyčejně bezpečné. Vážné bezprostřední komplikace jsou mimořádně vzácné a zahrnují ojedinělé případy intersticiální nefrititidy po omeprazolu, hepatitidy po omeprazolu a lansoprazolu a poruch vidění po pantoprazolu a omeprazolu. Nicméně dlouhodobé podávání je zvažováno v souvislosti se zvýšeným rizikem řady vážných onemocnění.
Obvyklé nezávažné komplikace se vyskytují u maximálně 5 % uživatelů IPP. Podle dat z více počátečních studií s omeprazolem se bolest hlavy vyskytla u 2,4 %, průjem u 1,4 %, nauzea u 0,9 % a urtika u 1,1 %, což přibližně odpovídá údajům při podávání AH2R. Podobný profil vedlejších účinků byl zaznamenán u pantoprazolu a rabeprazolu a v podstatě se nelišil od placeba v kontrolních skupinách.
Předpokládaný a sám o sobě fyziologický důsledek dlouhodobého podávání IPP je zvýšená hladina gastrinu. Je relativně vyšší při podávání rabeprazolu a lansoprazolu a relativně nižší při podávání pantoprazolu, rozdíly však nejsou významné [24].
Gastritida a neoplazie žaludku
U osob bez helikobakterové infekce IPP nevyvolávají gastrititidu a případný preexistující zánět mohou dokonce zmírnit. U osob Helicobacter pylori pozitivních může podávání IPP vést k progresi zánětu a ke změně antrum-predominantní gastrititidy na gastrititidu převážně lokalizovanou v oblasti těla žaludku. Eradikace Helicobacter pylori může vést k regresi zánětlivých změn, výsledky jednotlivých studií však nejsou zcela jednoznačné. Nicméně konsenzuální konference eradikaci u nemocných s předpokládanou dlouhodobou léčbou IPP doporučují.
Bylo zmíněno, že podávání IPP vede k hypergastrinemii nezávisle na infekci Hylicobacter pylori. Zvýšení koncentrace enterochromafiních-like buněk (ECL) není v jednotlivých studiích jednoznačné. Významnou informaci poskytuje LOTUS trial srovnávající vliv dlouhodobé medikace esomeprazolem a fundoplikace. U esomeprazolu došlo u helikobakter pozitivní podskupiny během pěti let k poklesu zánětlivé aktivity v antru a snížení koncentrace bakteriálního osídlení. Změny v těle žaludku nebyly analyzovány. Ač došlo ke zvýšení koncentrace ECL buněk, nebyly zaznamenány dysplastické změny [25]. Gastrin vykazuje trofický vliv na gastrointestinální sliznici obecně a u perniciózní anémie je vyšší riziko rakoviny žaludku. Je třeba zmínit, že hypergastrinemie při Zollinger-Ellisonově syndromu obvykle nevede ke zvýšení počtu ECL a karcinom žaludku byl u tohoto onemocnění popsán zcela ojediněle. V souvislosti s hypergastrinemií také nebyl zaznamenán nárůst výskytu karcinoidu. V důsledku užívání IPP se objevuje hyperplazie parietálních buněk a zvýšený výskyt polypů z fundických žlázek. Podobně je tomu u helikobakterové infekce. Po eradikaci a vyloučení IPP dochází k regresi. Polypy z fundických žlázek nevykazují dysplastické změny a adenomy vznikají jen vzácně u familiární adenomové polypózy.
Deficience železa a vitaminu B12
Vzhledem ke snížené žaludeční sekreci může dojít ke snížení intestinální absorpce organického i anorganického železa, nicméně hyposideremie a sideropenická anémie nevzniká. Důsledkem snížené kyselé sekrece dochází ke snížení aktivace pepsinogenu, čehož důsledkem je snížení uvolňování vitaminu B12 vázaného na složky potravy. U starších osob s gastritidou může dojít ke snížené koncentraci B12. Ta bývá také redukována u Zollinger-Ellisonova syndromu léčeného vysokými dávkami IPP. U mladších, jinak zdravých osob ke snížení koncentrace vitaminu B12 nedochází [26].
Osteoporóza, osteopenie, fraktury
V důsledku léčby IPP nedochází ke změnám metabolizmu vitaminu D a vliv na absorpci kalcia je velmi variabilní. Mechanizmus zvýšené lomivosti kostí není plně objasněn. Zvažuje se působení kyseliny chlorovodíkové na rozpustnost a následné vstřebání kalciových solí. Předpokládá se také vliv malabsorbce kalcia na rozvoj sekundární hyperparatyreózy a následné redukci kostní denzity. Podle recentní metaanalýzy 11 studií bylo riziko fraktur kyčle u uživatelů IPP (RR) 1,30, riziko fraktury páteře RR 1,56 a riziko fraktur obecně RR 1,16 bez ohledu na pohlaví. Užívání AH2R bylo zatíženo rizikem fraktur nesignifikantně (RR 1,12). Nicméně do statistik mohou zasahovat další faktory a specifická opatření se u uživatelů IPP nedoporučují [27].
Recentně publikovaná metaanalýza 18 observačních studií s celkem 244 109 frakturami u pacientů užívajících PPI prokázala středně zvýšené riziko fraktury kyčle (RR = 1,26; 95% CI 1,16 – 1,36). Zvýšené riziko provázelo užívání krátkodobě (méně než jeden rok) i dlouhodobě (více než jeden rok). Stejně tak bylo prokázáno středně zvýšené riziko fraktur obratlů (RR = 1,58; 95% CI 1,38 – 1,82) a fraktur všeobecně (RR = 1,33; 95% CI 1,15 – 1,54) [28]. V roce 2010 proto Food and Drug Association (FDA) vydala příslušné varovné prohlášení.
Jiná metaanalýza čtyř velkých studií prokázala významně vyšší riziko fraktur u pacientů užívajících terapii bisfosfonáty v kombinaci s IPP oproti pacientům léčených pouze bisfosfonáty (OR = 1,52; p = 0,025) [29].
Hypomagnezemie
Přibližně u více než 20 nemocných byla publikována hypomagnezemie obvykle také s hypokalemií a hypokalcemií manifestující se tetanickými křečemi. Je ovšem možné, že je výskyt hypomagnezemie podceněn, protože se hladina magnezia ne vždy stanovuje. Přesná příčina není jasná, pravděpodobně dochází u disponovaných jedinců ke snížení absorpce magnezia. Komplikace není závislá na výši dávky IPP. Na výskyt hypomagnezemie zareagovala ve Spojených státech amerických FDA varovným prohlášením.
Diskutuje se také vliv hypomagnezemie na výše popsanou zvýšenou náchylnost k frakturám. Ta je patrně způsobena blokádou absorpce pomocí TRPM 6/ 7 transportního kanálu. Podle recentní nizozemské populační studie je riziko zvýšené zejména u dlouhodobého užívání IPP (více než jeden rok; OR 2,99) a efekt je navíc významně vyšší při užívání kličkových diuretik OR 7,22 [30]. Hypomagnezemie přesto zůstává kontroverzním tématem. Sharara et al ve své metaanalýze spojitost mezi hypomagnezemií a užíváním IPP neprokázali, pokud měli pacienti normální renální funkce a neužívali diuretika [31].
Nozokomiální a komunitní pneumonie
Hypoacidita žaludku znamená snížení přirozené funkce baktericidního filtru. Dochází ke kolonizaci žaludku aerobními bakteriemi, jejich mikroaspiraci a následné kolonizaci dýchacích cest, nevyjasněně ovšem i bakteriemi v žaludku se nevyskytujícími. Další možností je vliv IPP na aktivaci protonové pumpy v hrtanu a v plicích s následnou kolonizací dýchacích cest, takže zánět je způsoben přímo atypickým osídlením respiračního aparátu. Pravděpodobně se však jedná o kombinaci obou hypotéz.
Podle první metaanalýzy respiračních infekcí nedosáhlo relativní riziko OR 1,42 statistické významnosti. Běžné riziko komunitní pneumonie je přibližně 0,6 na 100 paciento-roků a užívání IPP je zvyšuje 1,89×. IPP obecně nezvyšuje riziko nozokomiální pneumonie vyjma nemocných s nazogastrickou sondou. Podle recentní metaanalýzy zvyšovalo riziko současného podávání IPP riziko komunitní pneumonie 1,39×, podávání vysoké dávky 1,50× a podávání nízké dávky 1,17× a tyto rozdíly byly statisticky významné. Konstatuje se, že lékaři by si měli být vědomi tohoto rizika a v případě hrozby komunitní pneumonie zvážit namísto IPP alternativní léčbu [32].
Recentní metaanalýza 26 studií prokázala na skupině 226 769 pacientů užívajících IPP 1,5násobné riziko onemocnění komunitní pneumonií a 1,6× zvýšený počet hospitalizací RR 1,49 (95% CI 1,16; 1,92; p < 0,001). Největší riziko hrozí v prvních 30 dnech léčby PPI. Užívání H2RA nemělo na vznik komunitních pneumonií vliv [33].
Střevní infekce
IPP nevykazují konzistentní vliv na střevní mikrobiot, nicméně průjmy jsou nejčastější komplikací užívání IPP a také nejčastějším důvodem přerušení léčby. Mikrobiot u uživatelů IPP se liší ve více než 20 %, a to zejména ve prospěch Enterokoka, Sterptokoka, Stafylokoka a některých potenciálně patogenních kmenů E. Coli, nicméně klinické důsledky jsou neurčité. Zvyšuje se riziko infekce salmonellou 2,6 – 11,2×, Campylobacterem 1,7 – 11,7× a netyfoidní salmonelózy (OR 8,8; 95% CI 2,0 – 38,3) [34]. Vztah mezi antisekreční léčbou a infekcí Clostridium difficile byl poprvé zmíněn v roce 1993. Clostridium difficile je nejčastější příčinou střevní infekce u hospitalizovaných pacientů. Riziko zvyšuje věk a užívání širokospektrých antibiotik. Důležitá vlastnost spor Clostridium difficile je acidorezistence, naopak vegetativní fáze je na kyselinu velmi senzitivní. Recentně publikovaná metaanalýza zahrnula 30 studií a zjistila riziko klostridiové infekce zvýšené 2,15×. Mechanizmus je nejasný [35].
Lékové interakce
Značná pozornost se v poslední době obrací k lékovým interakcím. IPP jako běžně dlouhodobě podávané léky se nevyhnutelně kombinují s jinými medikamenty, s nimiž se dostávají do interakce v důsledku styčných metabolických procesů.
Farmakokinetické mechanizmy interakcí se různí. Vyšší pH v trávicí trubici může vést k poruše absorpce. IPP vedou k snížení absorpce ketoconazolu a itraconazolu, nikoli však fluconazolu. Pantoprazol snížil hladinu mykofenolát-mofetilu (AUC) až o 30 %. Naopak omeprazol zvyšuje absorpci bismutu při podávání dicitrát bismutát tripotassia. IPP zasahují do metabolizmu inhibitorů proteáz podávaných u AIDs. Lansoprazol vedl ke snížení AUC atazanaviru o 90 %, omeprazol snižuje AUC indinaviru, nalfinaviru, darunaviru a fosamprenaviru. Naopak se zvyšuje biologická dostupnost bismutu a penicilinů. Omeprazol, nikoli pantoprazol, také zvyšuje biologickou dostupnost digoxinu o 10 % interakcí s cytochromem P450. Vliv (snížení clearance) na digoxin je podmíněn etnickou genetickou výbavou. Alterací renální eliminace mohou IPP zpomalit vylučování metotrexátu. Omeprazol zvyšuje AUC phenytoinu, nifedipinu a carbamazepinu o 26 – 89 %. Lansoprazol zvyšuje AUC takrolimu. Zvýšenou afinitou k CYP2C19 jsou více zatíženy interakcemi omeprazol a lansoprazol než pantoprazol a rabeprazol. Opatrnost je na místě při současném podávání diazepamu, imipraminu a citalopramu, jejichž hladiny mohou být zvýšené. V případě užívání kumarinových preparátů se doporučuje monitorovat koagulační parametry. K vzájemnému zvýšení AUC může dojít při současném podávání omeprazolu a klaritromycinu [36].
Velmi významná je interakce s antiagregancii klopidogrelem a aspirinem. Klopidogrel se užívá jako alternativa či v kombinaci s aspirinem k redukci kardiovaskulárních příhod, zejména při akutním koronárním syndromu a po zavedení koronárního stentu. Klopidogrel není primárně ulcerogenní, zvyšuje však riziko krvácení s preexistujících lézí. Riziko krvácení při léčbě klopidogrelem je dvojnásobné proti běžné populaci a dvojnásobně také zvyšuje riziko dané podáváním aspirinu. Klopidogrel se ve dvou oxidativních krocích aktivuje v játrech cytochromem P450, jehož součástí je CYP2C19, a v účinné formě se ireverzibilně váže k destičkovému receptoru P2Y12. Kompeticí na CYP2C19 s IPP může dojít ke snížení účinku antiagregační léčby a ke zvýšení rizika kardiovaskulárních příhod. Největším inhibitorem CYP2C19 je lansoprazol s inhibiční konstantou Ki 0,4 – 1,5 µmol/ l, následují omeprazol Ki 2 – 6 µmol/ l, esomeprazol Ki 8 µmol/ l, pantoprazol Ki 14 – 69 µmol/ l a rabeprazol Ki 17 – 29 µmol/ l. Pantoprazol je ovšem největším inhibitorem CYP3A4. CYP2C19 je značně variabilní a ohroženi jsou zejména nositelé afunkčních alel. Interakce zkoumaly desítky studií a metaanalýz, z nichž některé jsou zaměřeny na agregační vlastnosti trombocytů, jiné na genetiku a další na klinické důsledky. Agregometrii (index vazoaktivně stimulovaného fosfoproteinu nebo agregometrie stimulovaná adenozin difosfátem) zkoumalo na více než 20 studií, 19 prokázalo statisticky významné snížení antiagregační aktivity, zatímco čtyři nikoli. Nebyl zaznamenán vliv separovaného podávání farmak a ve třech srovnávacích studiích nebyly zaznamenány rozdíly mezi jednotlivými IPP (omeprazol, lansoprazol, pantoprazol a rabeprazol), jejich výsledky však byly různé. Z klinických studií 20 shledalo častější výskyt kardiovaskulárních příhod u IPP, zatímco 14 nikoli. Tři metaanalýzy shledaly častější výskyt infarktu myokardu i závažných kardiovaskulárních příhod obecně, nedošlo však ke zvýšení mortality, v jedné byla mortalita u IPP častější. Dvě metaanalýzy se zabývaly jednotlivými IPP. Hulot shledal častější výskyt závažných kardiovaskulárních příhod u omeprazolu (RR 1,37), zatímco v metaanalýze Sillera-Matuly zaměřené na omeprazol a pantoprazol byly rozdíly nesignifikantní. Tři metaanalýzy zaznamenaly opačnou souvislost s výskytem interakcí a kvalitou metodiky studií [37].
Podávání IPP s prasugrelem, který je aktivován jinými izoenzymy než CYP2C19, není výše popsanou interakcí zatíženo. Studie Trilogy prokázala významně nižší výskyt koronárních příhod u pacientů s nestabilní anginou pectoris nebo infarktem myokardu bez ST elevací (NSTEMI) užívajících kombinaci prasugrel s IPP než ve skupině užívající s IPP klopidogrel (14,6 vs. 23,8 %; p < 0,02) [38]. Obdobné výsledky byly zaznamenány u diabetických pacientů po revaskularizaci věnčitých tepen užívajících IPP (HR = 1,63) [39].
Randomizovaná studie DOSAPI (Double the Dose of Clopidogrel or Switch to Prasugrel to Antagonize Proton Pump Inhibitor Interaction) srovnává reziduální destičkovou aktivitu (residual platelet aktivity – RPA) u pacientů užívajících dvojnásobnou dávku klopidogrelu (150 mg) či prasugrel (10 mg) za současného podávání lansoprazolu. Výsledek potvrdil nižší RPA v rameni s prasugrelem, a to i přesto, že lansoprazol snižuje jeho absorpci o 25 % a vrchol koncentrace v plazmě o 52 % [40].
Řada studií se naopak zabývala krvácením do gastrointestinálního traktu a vředovou nemocí v souvislosti s užíváním antiagregační léčby a IPP, pouze dvě však byly randomizované. U šesti byla zjištěna významná redukce krvácivých příhod, u sedmi nikoli a u tří byly výsledky s IPP horší. Obě metaanalýzy prokázaly významný protektivní účinek IPP [41]. Recentní metaanalýza osmi randomizovaných studií zjistila u 23 552 pacientů protektivní vliv IPP při konkomitantní duální antiagregaci (OR 0,24; p < 0,003), celková mortalita ani akutní koronární příhody nebyly IPP ovlivněny [42].
Jediná dvojslepá randomizovaná studie byla ukončena předčasně pro finanční problémy sponzora. Zkoumala obvyklou duální antiagregaci v aktivní skupině v kombinaci s omeprazolem a zahrnula 3 873 nemocných. Ve skupině s omeprazolem byl menší výskyt krvácivých příhod, v kardiovaskulárních parametrech (smrt, infarkt myokardu, ischemická cévní mozková příhoda a koronární revaskularizace) nebyly mezi skupinami statisticky významné rozdíly [43].
Metabolická aktivita CYP2C19 je značně interindividuálně variabilní, což může vést k závažným klinickým důsledkům. Byla popsána řada genetických variant, z nichž alela CYP2C19*2 (nebo polymorfizmus G681A) určuje 90 % pomalých metabolizátorů. Jejich nositelé (až 30 % Evropanů) vykazují sníženou účinnost klopidogrelu a zvýšený výskyt rekurujících kardiovaskulárních příhod ve srovnání s rychlými metabolizátory. CYP2C19 je také inhibován IPP, zejména omeprazolem a lansoprazolem. Vlivem genetických variant na účinek klopidogrelu se zabývala řada studií a jedna recentně publikovaná metaanalýza zahrnující 23 studií a 11 959 nemocných. Nositelé alely CYP2C19*2 (28 %, n = 3 418) vykázali 30% nárůst závažných kardiovaskulárních příhod ve srovnání s ostatními (9,7 vs. 7,8 %; OR 1,29). Ještě vyšší rozdíl byl v mortalitě (1,8 vs. 1 %) a trombóze stentů (2,9 vs. 0,9 %). Riziko bylo stejné u homozygotů i heterozygotů a bylo nezávislé na výši kardiovaskulárního rizika. Uživatelé IPP (42 %) byli zatíženi větším rizikem závažných kardiovaskulárních příhod (21,8 vs. 16,7 %; OR 1,41) a mortalitou (12,7 vs. 4,4 %; OR 1,18). Tento rozdíl byl však ovlivněn mírou kardiovaskulárního rizika [44].
Byla publikována řada prací zkoumající předpokládané odlišné riziko interakcí mezi jednotlivými IPP a klopidogrelem. Japonští dobrovolníci užívali ve třech skupinách aspirin (A), klopidogrel (C), oba medikamenty (AC) a konečně obě látky s rabeprazolem (ACR) a prováděla se endoskopie, stanovení acidity a vyšetření aktivity trombocytů. Bylo zjištěno, že poškození žaludeční sliznice bylo podobné u A, C i AC skupin. Rabeprazol zvyšoval průměrné pH účinněji u Helicobacter pozitivních než Helicobacter negativních jedinců. Různým genotypům CYP2C19 odpovídalo u Helicobacter pozitivních jedinců různé poškození žaludeční sliznice, výdej kyseliny i funkce trombocytů a rabeprazol neměl na tyto výsledky vliv. Rabeprazol účinně snižoval slizniční poškození indukované duální terapií zejména u Helicobacter negativních intermediálních a pomalých metabolizátorů bez ovlivnění protisrážlivého účinku. Nebyl však dostatečně účinný u rychlých metabolizátorů. V budoucnu by měli kandidáti kombinované antiagregační léčby a IPP se zvýšeným rizikem krvácení podstoupit vyšetření genetiky CYP2C19 a u rychlých metabolizátorů by se dávka IPP měla zdvojnásobit [45]. Jiná studie zkoumala vliv esomeprazolu a rabeprazolu na antiagregační aktivitu klopidogrelu. U 239 nemocných se provedla genotypizace CYP2C19 a stanovila se agregace trombocytů při léčbě klopidogrelem (skupina C) a v kombinaci s esomeprazolem (CE) a rabeprazolem (CR). Index reaktivity trombocytů byl 20,7 ve skupině C, 19,1 ve skupině CR a 24,5 ve skupině CE. Výsledky nebyly ovlivněny genotypem CYP2C19 [46].
Na interakci IPP s antiagregancii reagují v doporučených postupech profesionální organizace a regulační úřady. American College of Gastroenterology a American Heart Association publikovali konsenzus v roce 2010. Instituce konstatují, že vliv IPP na antiagregační působení klopidogrelu je v jednotlivých studiích inkonzistentní a doporučují přístup podle individuálního gastroenterologického a kardiovaskulárního rizika. FDA varuje před užíváním omeprazolu (i esomeprazolu) společně s klopidogrelem. Výslovně se udává, že varování neplatí pro ostatní IPP. Podobně se vyjadřuje European Medicines Agency. Nabádá, že v případě nutnosti u rizikových pacientů by se mělo IPP podávat v nejmenší účinné dávce. Toto doporučení poněkud postrádá logiku, uvědomíme-li si, že u rychlých metabolizátorů (genetické vyšetření se běžně neprovádí) je účinnost IPP snížena, a navíc krvácení u nemocných na antiagregační léčbě se obvykle objevuje bez varovných příznaků [41]. Evropská kardiologická společnost (ESC) doporučuje u pacientů po STEMI i NSTEMI spolu s duální antiagregací současné podávání IPP, a to zejména u pacientů, kteří v minulosti krváceli do zažívacího traktu či mají anamnézu peptického vředu (doporučení IA) [47].
Budoucnost inhibice žaludeční sekrece
Přes spektakulární úspěch kontroly žaludeční sekrece IPP se přibližně u 20 – 30 nemocných očekávaný výsledek nedostavuje nebo je úspěch jen částečný za cenu zvýšení doporučené dávky. Je tomu tak zejména u GERD a gastropatie z užívání nesteroidních antirevmatik. U řady nemocných je doba redukce žaludeční sekrece běžnou dávkou IPP nedostatečná, často v důsledku genetické predispozice (rychlí metabolizátoři). Dalším snad i nejčastějším faktorem je nedostatečná compliance nemocných. Ideální preparát by měl dostatečně snižovat žaludeční sekreci v průběhu alespoň 20 hod, užíval by se v jedné dávce, byl by prost vedlejších účinků a interakcí a jeho účinek by nebyl závislý na konzumaci potravy. Je zjevné, že jako všechny ideály je nedosažitelný, protože čím účinnější sekrece, tím nevyhnutelně větší riziko některých komplikací. Nadto neúspěch standardní léčbou IPP mívá různou příčinu, což prosté zvýšení inhibice sekrece nevyřeší.
Tenatoprazol je imidazol-pyridin. Aktivuje se pomaleji než schválená IPP a jeho vazba je ireverzibilní. Jeho plazmatický poločas činí 6 hod. Podobně působí ilaprazol.
Dex-lansoprazol je R-enantiomer lansoprazolu, který v důsledku prostorové orientace působí více protrahovaně než běžný lansoprazol. Příznivěji také vyznívají klinické studie s až 95% hojením erozivní refluxní ezofagititidy. Dex-lansoprazol byl již schválen FDA, avšak počet srovnávacích studií ve všech souvislostech je dosud nedostatečný.
Alevium je opět proléková forma omeprazolu, nicméně tento sulfonamidový derivát omeprazolu je acidorezistentní, pomalu se vstřebává v průběhu celého tenkého střeva, takže jeho poločas v plazmě je ve srovnání s omeprazolem podstatně delší.
Potassium-kompetitivní blokátory sekrece jsou imidazol pyridiny, které nevyžadují aktivaci kyselinou a jejich antisekreční působení je rychlé a dlouhodobé, nicméně výsledky klinických studií jsou dosud nepřesvědčivé.
Přes dobře zdůvodněné antagonistické působení různých principů inhibice sekrece vývoj spočívá i v jejich kombinování. Immediate-release (IR) omeprazol kombinuje zmíněnou molekulu s bikarbonátem, který stimuluje protonovou pumpu. Zkouší se v podobě žvýkačky.
Objevují se nové kombinace AH2R, např. emodin-kalcium karbonát a magnezium hydroxid. Ebrotidin vedle antisekrečního účinku chrání žaludeční epitel. Latifudin je dostupný v Japonsku a jeho účinek nastupuje velmi rychle, takže jej lze užívat on-demand.
Spiroglumid a itriglumid jsou antagonisté gastrinových a CCK receptorů, které lze využívat v kombinaci s prazoly [48,49].
Informace nemocným
Pro účinnou léčbu má vždy informovanost nemocných zásadní význam. Obecně optimalizuje spolupráci a správné užívání medikamentů, umožňuje předejít, případně včas zareagovat na nežádoucí účinky a vyhnout se interakcím. U IPP je tato informovanost důležitá mimořádně, neboť správné podání léku ovlivňuje jeho účinnost zásadním způsobem. Je známo, že informace od lékařů je často nedostatečná, a autorům tak přišlo na mysl přehlédnout doporučené postupy IPP, které jsou v ČR na trhu. Celkem prohlédli 17 příbalových letáků všech obvyklých molekul. Letáky se často od sebe významně liší, kupodivu velmi často bývají popsány jevy zcela podružné, jako nevýznamné komplikace a irelevantní interakce. Běžně se používají bez bližšího vysvětlení termíny jako AUC či CYP všeho druhu, kterým běžný uživatel a čtenář nemůže rozumět. Naopak z informací důležitých byla jen u šesti zmínka o nutnosti podání před jídlem, nikoli však před snídaní. Z významných interakcí a komplikací chyběla zmínka o klopidogrelu 7×, metabolizmu kostí 6×, gastrointestinálních infekcích 7× (a clostridium difficile bylo zmíněno jen jednou), hypomagnezemii 6× a informace o vhodné eradikaci Helicobacter pylori při dlouhodobém podávání IPP chybí úplně.
Závěr
Závěrem lze shrnout, že IPP poskytují účinnou léčbu u GERD, eradikace Helicobacter pylori, funkční dyspepsie a gastropatie z nesteroidních antirevmatik u 70 – 80 % nemocných. Jsou též významnou součástí léčby u EoE. Jejich farmakokinetické parametry se někdy výrazně liší, nicméně klinický efekt jednotlivých IPP je velmi podobný. Velmi zjednodušeně a přibližně lze soudit, že IPP nové generace, tj. rabeprazol a esomeprazol, zvyšují úspěšnost léčby přibližně o 5 %, což vzhledem k šíři problému není rozdíl zanedbatelný. IPP jsou celkově léky velmi bezpečné, jejich přímá toxicita je výjimečná. Závažné mohou být jejich interakce s podáváním antiagregační léčby, kdy může dojít ke zvýšení rizika závažných kardiovaskulárních příhod. Toto riziko je významné při podávání klopidogrelu, nikoli prasugrelu. Vliv jednotlivých IPP se liší, nejnižší je patrně u rabeprazolu. Zvyšují také riziko clostridiové infekce, komunitních pneumonií a fraktur. Účinnost IPP je významně ovlivněna polymorfizmem cytochromu P450 a genetické vyšetření se bude v budoucnu využívat ve zvýšené míře. Od nových IPP lze očekávat menší závislost na příjmu potravy a i větší účinnost v inhibici sekrece, což se ovšem nemůže neprojevit na některých vedlejších účincích. Vždy je třeba mít na paměti, že žaludeční sekrece a vysoká acidita žaludku jsou primárně fyziologické fenomény. Přes zvýšenou pozornost věnovanou vedlejším účinkům IPP je lze obecně označit za léky velmi bezpečné, nicméně i zde platí univerzální pravidlo – podávat je jen ve zřejmých indikacích, po dobu danou indikací a cílem léčby a v nejnižší účinné dávce.
prof. MU Dr. Julius Špičák, CSc.
www.ikem.cz
julius.spicak@ikem.cz
Doručeno do redakce 28. 1. 2016
Přijato po recenzi 15. 2. 2016
www.csgh.info
Zdroje
1. Huang JQ, Hunt RH. Pharmacological and pharmacodynamic essentials of H2-receptor antagonists and proton pump inhibitors for the practicing physicians. Best Practis Res Clin Gastroenterol 2001; 15 : 355 – 370.
2. Martínek J, Lukáš M. Inhibitory protonové pumpy – up to date. Gastroent Hepatol 2011; 65 : 231 – 242.
3. Andersson T, Weidolf L. Stereoselective disposition of proton pump inhibitors. Clin Drug Investig 2008; 28 : 263 – 279.
4. Morelli G, Chen H, Rossiter B et al. An open-label, parallel, multiple-dose study comparing the pharmacokinetics and gastrin acid suppression of rabeprazole extended-realise with omeprazole 40 mg and rabeprazole delayed-release 20 mg in healthy volunteers. Aliment Pharmacol Ther 2011; 33 : 845 – 854. doi: 10.1111/ j.1365-2036.2011.04580.x.
5. Chiba N, De Gara CJ, Wilkinson JM et al. Speed of healing and symptom relief in grade II to IV gastroesopohageal reflux disease: a metaanalysis. Gastroenterology 1997; 112 : 1798 – 1810.
6. Vakil N, Fennerty MB. Direct comparative trials of the efficacy of proton pump inhibitors in the management of gastro-oesophageal reflux disease and peptic ulcer disease. Aliment Pharmacol Ther 2003; 18 : 559 – 568.
7. Maiti R, Jaida J, Israel J et al. Rabeprazole and esomeprazole in mild-to-moderate erosive gastroesophageal reflux disease: a comparative study of efficacy and safety. J Pharmacol Pharmacother 2011; 2 : 150 – 157. doi: 10.4103/ 0976-500X.83278.
8. Maret-Ouda J, Brusselaers N, Lagergren J. What is the most effective treatment for severe gastro-oesophageal reflux disease? BMJ 2015; 350 : 3169. doi: 10.1136/ bmj.h3169.
9. de Jonge PJ, Spaander MC, Bruna MJ et al. Acid suppression and surgical therapy for Barrett's oesophagus. Best Pract Res Clin Gastroenterol 2015; 29 : 139 – 150. doi: 10.1016/ j.bpg.2014.11.005.
10. Jachimski P, Maqbool S, Bhat YM et al. Control of acid and duodenogastroesophageal reflux (DGER) in patients with Barrett's esofagus. Am J Gastroenterol 2015; 110 : 1143 – 1148. doi: 10.1038/ ajg.2015.161.
11. Sheikh I, Waghray A, Waghray N et al. Consumer use of over-the-counter proton pump inhibitors in patients with gastroesophageal reflux disease. Am J Gastroenterol 2014; 109 : 789 – 794. doi: 10.1038/ ajg.2013.421.
12. Tang HL, Li Y, Hu YF et al. Effects of CYP2C19 loss--of-function variants on the eradication of H. pylori infection in patients treated with proton pump inhibitor-based triple therapy regimens: A meta-analysis of randomized clinical trials. PLoS One 2013; 8: e62162. doi: 10.1371/ journal.pone.0062162.
13. Tielemans MM, Eikendal T, Jansen JB et al. Identification of NSAID users at risk for gastrointestinal complications. Drug Saf 2010; 33 : 443 – 453. doi: 10.2165/ 11534590-000000000-00000
14. Iwamoto J, Saito Y, Honda A et al. Clinical features of gastroduodenal injury associated with long-term low dose aspirin therapy. World J Gastroenterol 2013; 19 : 1673 – 1682. doi: 10.3748/ wjg.v19.i11.1673.
15. Lanza FI, Chan FK, Quigley EM et al. Guidelines for prevention of NSAID-related ulcer complications. Am J Gastroenterol 2009; 104 : 728 – 738. doi: 10.1038/ ajg.2009.
16. Washio E, Esaki M, Maehata Y et al. Proton pump inhibitors increase incidence od nonsteroidal anti--inflammatory drug-induced small bowel injury: A randomized, placebo-controlled trial. Clin Gastroenterol Hepatol 2015; S1542-3565(15)01489-5. doi: 10.1016/ j.cgh.2015.10.022.
17. Liu B, Liu S, Yin A et al. Risks and benefits of stress ulcer prophylaxis in adult neurocritical care patients: a systematic review and metaanalysis of randomized controlled trials. Critical Care 2015; 19 : 409. doi: 10.1186/ s13054-015-1107-2.
18. Jian Z, Li H, Race NS et al. Is the Era of intravenous proton pump inhibitors coming to an end in patients with bleeding peptic ulcers? Meta-analysis of the published literature. Br J Clin Pharmacol 2015. [Ahead of print]. doi: 10.1111/ bcp.12866.
19. Fords A, Moayyedi P. Current guidelines for dyspepsia management. Dig Dis 2008; 26 : 225 – 230. doi: 10.1159/ 000121351.
20. Liacouras CA, Furuta GT, Hirano et al. Eosinophilic esophagitis: updated konsensus recommendations for children and adults. J Allergy Clin Immunol 2011; 128 : 3 – 20. doi: 10.1016/ j.jaci.2011.02.040.
21. Vazquez-Elizondo G, Ngamruengphong S, Khrisna M et al. The outcome of patients with oesophageal eosinophilic infiltration after an eight-week trial of a proton pump inhibitor. Aliment Pharmacol Ther 2013; 38 : 1312 – 1319. doi: 10.1111/ apt.12513.
22. Lucendo AJ, Arias A, Molina-Infante J. Efficacy of Proton pump inhibitor drugs for inducing clinical and histologic remission in patients with symptomatic esophageal eosinophilia: a systematic review and meta-analysis. Clin Gastroenterol Hepatol 2016; 14 : 13 – 22. doi: 10.1016/ j.cgh.2015.07.041.
23. Molina-Infante J, Rodriguez-Sanchez J, Martinek J et al. Long-term loss of response in proton pump inhibitor-responsive esophageal eosinophilia is uncommon and influenced by cyp2c19 genotype and rhinoconjunctivitis. Am J Gastroenterol 2015; 11 : 1567 – 1575. doi: 10.1038/ ajg.2015.314.
24. Lodato F, Azzyaroli F, Turco L et al. Adverse effects of proton pump inhibitors. Best Pract Res Clin Gastroenterol 2010; 24 : 193 – 201. doi: 10.1016/ j.bpg.2009.11.004.
25. Fiocca R, Mastracci L, Attwood SE et al. Gastric exocrine and endocrine cell morfology under prolonged acid inhibition therapy: results of 5-year follow-up in the LOTUS trial. Aliment Pharmacol Ther 2012; 36 : 959 – 971. doi: 10.1111/ apt.12052.
26. Thomson AB, Sauve MD, Kassam N et al. Safety of long-term use of proton pump inhibitors. World J Gastroenterol 2010; 16 : 2323 – 2330.
27. Yu EW, Bauer SR, Bain PA et al. Proton pump inhibitors and risk of fractures: a meta-analylsis of 11 internbational studies. Am J Med 2011; 124 : 519 – 526. doi: 10.1016/ j.amjmed.2011.01.007.
28. Zhou B, Huang Y, Li H et al. Proton-pump inhibitors and risk of fractures: an update meta-analysis. Osteoporos Int 2015. In press.
29. Yang SD, Chen Q, Wei HK et al. Bone fracture and the interaction between bisphosphonates and proton pump inhibitors: a meta-analysis. Int J Clin Exp Med 2015; 8 : 4899 – 4910.
30. Kieboom BC, Kiefte - de Jong JC, Eijgelsheim M et al. Proton pump inhibitors and hypomagnesemia in the general population: a population-based cohort study. Am J Kidney Dis 2015; 66 : 775 – 782. doi: 10.1053/ j.ajkd.2015.05.012.
31. Sharara Al, Chalhoub JM, Hammoud N et al. Low prevalence of hypomagnesemia in long-term recipients of proton pump inhibitors in a manage care cohort. Clin Gastroenterol Hepatol 2016; 14 : 317 – 321. doi: 10.1016/ j.cgh.2015.10.012.
32. Giuliano C, Wilhem SM, Kale-Pradhan PB. Are proton pump inhibitors associated with the development of community-acquired pneumonia? A meta-analysis. Expert Rev Clin Pharmacol 2012; 5 : 337 – 344. doi: 10.1586/ ecp.12.20.
33. Lambert AA, Lam JO, Paik JJ. Risk of community--acquired pneumonia with outpatient proton-pump inhibitor therapy: a systematic review and meta-analysis. PLoS One 2015; 10: e0128004. doi: 10.1371/ journal.pone.0128004.
34. Freeman R, Dabrera G, Lane C et al. Association between use of proton pump inhibitors and non-typhoidal salmonellosis identified following investigation into an outbreak of Salmonella Mikawasima in the UK, 2013. Epidemiol Infect 2015; 1 : 1 – 8.
35. Deshpande A, Pant Ch, Pasupuleti V et al. Association between proton pump inhibitor therapy and clostridium difficile in a meta-analysis. Clin Gast-roenterol Hepatol 2012; 10 : 225 – 233. doi: 10.1016/ j.cgh.2011.09.030.
36. Ogawa R, Echizen H. Drug-drug interactions profiles of proton pump inhibitors. Clin Pharmacokinet 2010; 8 : 509 – 533. doi: 10.2165/ 11531320-000000000-00000.
37. Drepper MD, Spahr L, Frossard JL.Clopidogrel and proton pumpo inhibitors – where do we stand in 2012? World J Gastroenterol 2012; 18 : 2161 – 2171. doi: 10.3748/ wjg.v18.i18.2161.
38. Roe MT, Armstrong PW, Fox KA et al. Prasugrel versus clopidogrel for acute coronary syndromes without revascularization N Engl J Med 2012; 367 : 1297 – 1309. doi: 10.1056/ NEJMoa1205512.
39. Hsieh CF, Huang WF, Chiang YT et al. Effects of clopidogrel and proton pump inhibitors on cardiovascular events in patients with type 2 diabetes mellitus after drug-eluting stent implantation: a nationwide cohort study. PLoS One 2015; 10: e0135915. doi: 10.1371/ journal.pone.0135915.
40. Collet JP, Hulot JS, Abtan J et al. Prasugrel but not high dose clopidogrel overcomes the lansoprazole neutralizing effect of P2Y12 inhibition: Results of the randomized DOSAPI study. Eur J Clin Pharmacol 2014; 70 : 1049 – 1057. doi: 10.1007/ s00228-014-1710-1.
41. Chen J, Yuan YC, Leontiadis GI et al. Recent safety concerns with proton pump inhibitors. J Clin Gastroenterol 2012; 46 : 93 – 114. doi: 10.1097/ MCG. 0b013e3182333820.
42. Cardoso RN, Benjo AM, DiNicolantonio JJ et al. Incidence of cardiovascular events and gastrointestinal bleeding in patients receiving clopidogrel with and without proton pump inhibitors: an updated meta-analysis. Open Heart 2015; 2: e000248. doi: 10.1136/ openhrt-2015-000248.
43. Bhatt DL, Cryer BL, Contant CF et al. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med 2010; 363 : 1909 – 1917. doi: 10.1056/ NEJMoa1007964.
44. Hulot JS, Collet JP, Silvain J et al. Cardiovascular risk in clopidogrel-treated patients according to cytochrome P450 2C19*2 loss-of-function allele or proton pump inhibitor coadministration. J Am Coll Cardiol 2010; 56 : 134 – 143. doi: 10.1016/ j.jacc.2009.12.071.
45. Uotani T, Sugimoto M, Nishino M et al. Ability of rabeprazole to prevent gastrin mucosal damage from clopidogrel and low doses of aspirin depends on CYP2C19. Clin Gasteroenterol Hepatol 2012; 10 : 879 – 885. doi: 10.1016/ j.cgh.2012.04.016.
46. El-Halabi MM, Zgheuib N, Mansour NM et al. CYP2C19 genetic polymorphism, rabeprazole and esomeprazole have no effect on the anti-platelet action of clopidogrel. J Cardiovasc Pharmacol 2013; 62 : 41 – 49. doi: 10.1097/ FJC.0b013e31828ecf44.
47. Agewall S, Cattaneo M, Collet JP et al. Expert position paper on the use of proton pump inhibitors in patients with cardiovascular disease and antithrombotic therapy. Eur Heart J 2013; 34 : 1708 – 1713. doi: 10.1093/ eurheartj/ eht042.
48. DeVault KR, Talley NJ. Insights into the future of gastric acid suppression. Nat Rev Gastroenterol Hepatol 2009; 6 : 524 – 532. doi: 10.1038/ nrgastro.2009.125.
49. Sachs G, Shin JM, Hunt R et al. Novel approaches to inhibition of gastrin acid secretion. Curr Gastroenterol Rep 2010; 12 : 437 – 447. doi: 10.1007/ s11894-010-0149-5.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2016 Číslo 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Jak nejlépe blokovat renin-angiotenzinový systém u nemocných s hypertenzí a diabetes mellitus?
- Infekční komplikace u pacientů s akutním srdečním selháním – přehled
- Přidružená onemocnění a jejich význam pro prognózu akutního srdečního selhání – AHEAD score
- Kardiálna kachexia
- Tělesný trénink a rehabilitace u srdečního selhání
- Kvalita života pacientů s akutní dekompenzací chronického systolického srdečního selhání hodnocená pomocí standardizovaných dotazníků
- Hyperurikémia, kardiovaskulárne choroby a srdcové zlyhávanie
- Antikoagulace, antiagregace nebo obojí u pacientů s ischemickou chorobou srdeční a fibrilací síní
- Místo sitagliptinu v léčbě pacientů s diabetem 2. typu po studii TECOS
- Na jaké hodnoty snižovat systolický krevní tlak? Studie SPRINT
- prof. MUDr. Jiří Vítovec, CSc., FESC (*25. 2. 1951)
- Evropský konsenzus k otázkám aterogenní dyslipidemie a kombinační léčbě statinem a fibrátem
- Inhibitory protonové pumpy – nové molekuly, nové poznatky
- Nové pohledy na patofyziologii, diagnostiku a léčbu srdečního selhání se zachovanou ejekční frakcí
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Inhibitory protonové pumpy – nové molekuly, nové poznatky
- Antikoagulace, antiagregace nebo obojí u pacientů s ischemickou chorobou srdeční a fibrilací síní
- Kardiálna kachexia
- Hyperurikémia, kardiovaskulárne choroby a srdcové zlyhávanie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



