-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
Pegasus study – long‑term dual antiaggregation therapy (ASA + ticagrelor) following myocardial infarction
Background:
Ticagrelor is a P2Y12 receptor antagonist that has been shown to reduce the incidence of ischemic events for up to a year after an myocardial infarction acute coronary syndrome. The efficacy and safety of long‑term ticagrelor therapy beyond 1 year after a myocardial infarction is was unknown.Methods:
We randomized 21,162 patients with a history of myocardial infarction within the previous 1 – 3 years on a double‑blind basis 1 : 1 : 1 fashion to ticagrelor 90 mg twice daily, ticagrelor 60 mg twice daily, or placebo, all treated with low‑dose aspirin, and followed them up for a median of 33 months. The primary efficacy endpoint was the composite of cardiovascular death, myocardial infarction, or stroke. The primary safety endpoint was TIMI major bleeding.Results:
Both doses of ticagrelor significantly reduced the primary efficacy endpoint at 3 years compared to placebo, with Kaplan ‑ Meier rates at 3 years of 7.85% with ticagrelor 90 mg, 7.77% with ticagrelor 60 mg, and 9.04% with placebo (HR for ticagrelor 90 mg vs. placebo was 0.85, 95% CI 0.75 – 0.96, p = 0.0080; HR for ticagrelor 60 mg vs. placebo was 0.84, 95% CI 0.74 – 0.95, p = 0.0043). The rates of TIMI major bleeding were higher with ticagrelor (2.60% for 90 mg, 2.30% for 60 mg and 1.06% for placebo, p < 0.001 for each dose against placebo); the rates of fatal intracranial hemorrhage or fatal bleeding were 0.63%, 0.71%, and 0.60% in the 3 arms, respectively.Conclusions:
Treatment with ticagrelor of patients more than 1 year after a myocardial infarction with ticagrelor reduces the risk of cardiovascular death, myocardial infarction, or stroke, and slightly increases the risk of major bleeding.Keywords:
ticagrelor – myocardial infarction – secondary prevention
Autoři: J. Špinar 1; L. Špinarová 2; J. Vítovec 2
Působiště autorů: Interní kardiologická klinika LF MU a FN Brno 1; I. interní kardioangiologická klinika LF MU a FN u sv. Anny v Brně 2
Vyšlo v časopise: Kardiol Rev Int Med 2015, 17(1): 41-45
Kategorie: Kardiologická revue
Souhrn
Předpoklad:
Ticagrelor je inhibitor receptoru P2Y12 a má prokázaný účinek na snížení ischemických příhod jeden rok po akutním infarktu myokardu. Jeho efekt v delším časovém období nebyl znám.Metodika:
Zařazeno bylo 21 162 nemocných s anamnézou infarktu myokardu 1 – 3 roky před randomizací, kteří byli dvojitě zaslepeně randomizováni v poměru 1 : 1 : 1 na ticagrelor 2 × 90 mg : 2 × 60 mg : placebo. Všichni nemocní museli být léčeni malou dávkou kyseliny acetylsalicylové. Pacienti byli sledováni v mediánu 33 měsíců. Primární souhrnný cíl účinnosti byl kardiovaskulární úmrtí, infarkt myokardu nebo cévní mozková příhoda. Primární bezpečnostní cíl bylo TIMI velké krvácení.Výsledky:
Obě dávky ticagreloru signifikantně snížily primární cíl za 3 roky: 7,85 % ticagrelor 2 × 90 mg, 7,77 % ticagrelor 2 × 60 mg a 9,04 % placebo (HR pro ticagrelor 2 × 90 mg vs placebo 0,85, 95% CI 0,75 – 0,96; p = 0,0080; HR pro ticagrelor 2 × 60 mg vs placebo 0,84, 95% CI 0,74 – 0,95; p = 0,0043). TIMI velké krvácení bylo vyšší na ticagreloru (2,60 % pro 2 × 90 mg, 2,30 % pro 2 × 60 mg a 1,06 % pro placebo; p < 0,001 pro obě dávky; fatální intrakraniální krvácení se vyskytlo v 0,63 %, 0,71 % a 0,60 % (NS).Závěr:
Léčba ticagrelorem více než jeden rok po infarktu myokardu snižuje riziko úmrtí, infarktu myokardu, cévní mozkové příhody s mírným zvýšením velkých krvácení.Klíčová slova:
ticagrelor – infarkt myokardu – sekundární prevence
Infarkt myokardu je stále jednou z velmi závažných diagnóz, díky systému primární péče ale stále více lidí přežívá a jsou ve významném ohrožení recidivy. Proto je na tyto nemocné cíleně zaměřena intenzivní sekundární prevence. Jedním ze základních mechanizmů další ischemické příhody je aktivace destiček – tvorba trombu. Kyselina acetylsalicylová má prokázanou účinnost na snížení trombotických příhod, proto je doporučována po infarktu myokardu do dlouhodobé léčby. Přidání ticagreloru – inhibitoru P2Y12 receptoru – vedlo ke snížení trombotických příhod do jednoho roku po akutním infarktu myokardu např. ve studii PLATO [1 – 3]. Na základě těchto výsledků jsou inhibitory P2Y12 receptoru doporučovány po dobu 12 měsíců po akutním koronárním syndromu jak v amerických, tak v evropských doporučených postupech [4 – 7].
Na základě těchto údajů byla naplánována studie PEGASUS-TIMI 54, která testovala hypotézu, zda přidání ticagreloru k malé dávce kyseliny acetylsalicylové sníží výskyt kardiovaskulárních příhod u stabilních pacientů po infarktu myokardu. Testovány byly dvě dávky, a to 2 × 60 mg a 2 × 90 mg (obr. 1) [8 – 10].
Obr. 1. PEGASUS-TIMI 54 – design studie. 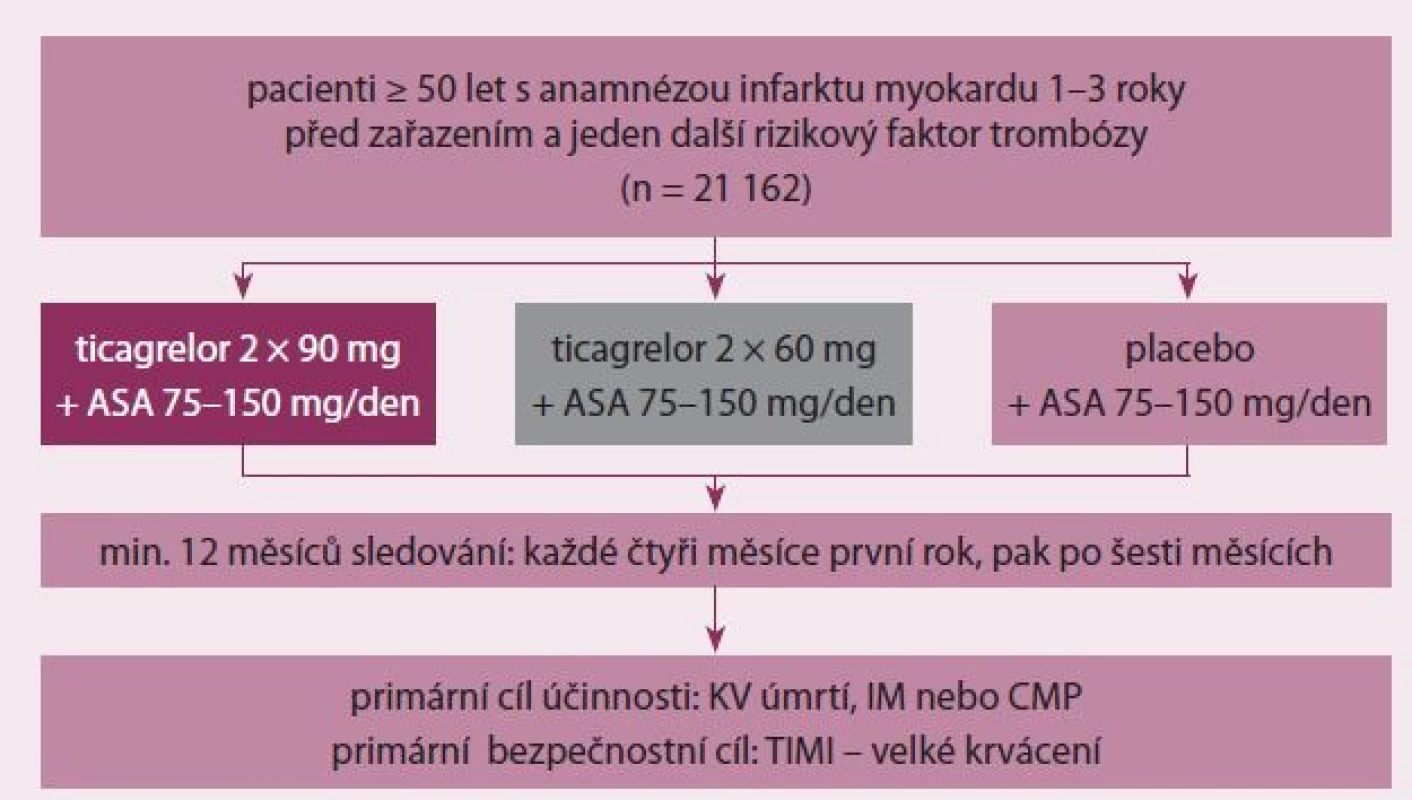
Metodika
Studie PEGASUS ‑ TIMI 54 byla dvojitě slepá, randomizovaná mezinárodní studie prováděná v 1 161 centrech v 31 zemích, včetně České republiky. Zařazeni mohli být nemocní 1 – 3 roky po infarktu myokardu s dalším kardiovaskulárním rizikovým faktorem, jako je věk na 65 let, diabetes mellitus na medikaci, předchozí infarkt myokardu, vícečetné postižení dokumentované koronarografií či kreatinová clearance pod 60 ml/ min. Mezi nepovolenou medikaci patřily jiné inhibitory P2Y12 receptoru, antikoagulační léčba, dipyridamol a další. Kontraindikací byla též nutnost dialýzy či předchozí ischemická cévní mozková příhoda. Kontraindikací bylo také závažné krvácení v anamnéze. Doprovodnou medikací byla kyselina acetylsalicylová v dávce 75 – 150 mg. Pokud pacient během studie musel podstoupit chirurgický nekardiální výkon, byla medikace pět dnů před zákrokem vysazena a nasazena co nejdříve po zákroku.
Primárním cílem byla kombinace kardiovaskulárního úmrtí, infarktu myokardu a cévní mozkové příhody. Sekundárním cílem byla celková mortalita. Primárním bezpečnostním cílem bylo krvácení hodnocené TIMI klasifikací jako velké [9,10].
Výsledky
Randomizováno bylo 21 162 nemocných v době od října 2010 do března 2013. Základní charakteristiku nemocných ukazuje tab. 1.
Tab. 1. Základní charakteristika nemocných. 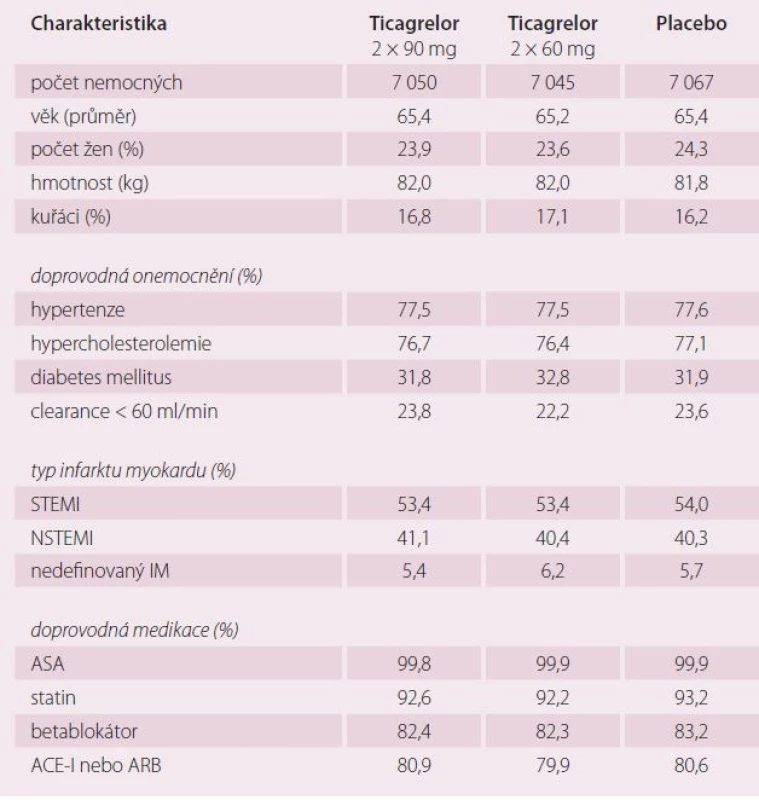
Průměrná doba od posledního infarktu byla 1,7 let; infarkty myokardu s elevací ST úseku tvořily nadpoloviční většinu. Většina pacientů (83 %) byla léčena primární angioplastikou, u 59 % bylo postižení více tepen. Tab. 1 ukazuje velmi kvalitní farmakologickou léčbu splňující současná doporučení.
Alespoň jednu dávku studijního léku dostalo 20 942 nemocných (99,0 %), během studie ukončilo léčbu 32,0 % na 2 × 90 mg, 28,7 % na 2 × 60 mg a 21,4 % na placebu (p < 0,001 pro obě dávky vs placebo). Medián sledování byl 33 měsíců, což v součtu dělá 56 004 pacientských roků.
Obě dávky ticagreloru statisticky významně snížily primární kombinovaný cíl – kardiovaskulární úmrtí, infarkt myokardu a ischemickou mozkovou příhodu (graf 1). Účinek ticagreloru byl konzistentní na každý z primárních podcílů, kdy na obou dávkách byl výskyt primárního cíle 7,81 %, výskyt kardiovaskulárního úmrtí 2,90 % vs 3,39 % na placebu (p = 0,57), infarkt myokardu 4,47 % vs 5,25 % (p = 0,0055) a výskyt cévní mozkové příhody 1,54 % vs 1,94 % (p = 0,034) (tab. 2).
Graf 1. PEGASUS-TIMI 54 – primární cíl. 
Tab. 2. PEGASUS-TIMI 54 – primární účinnostní cíle. 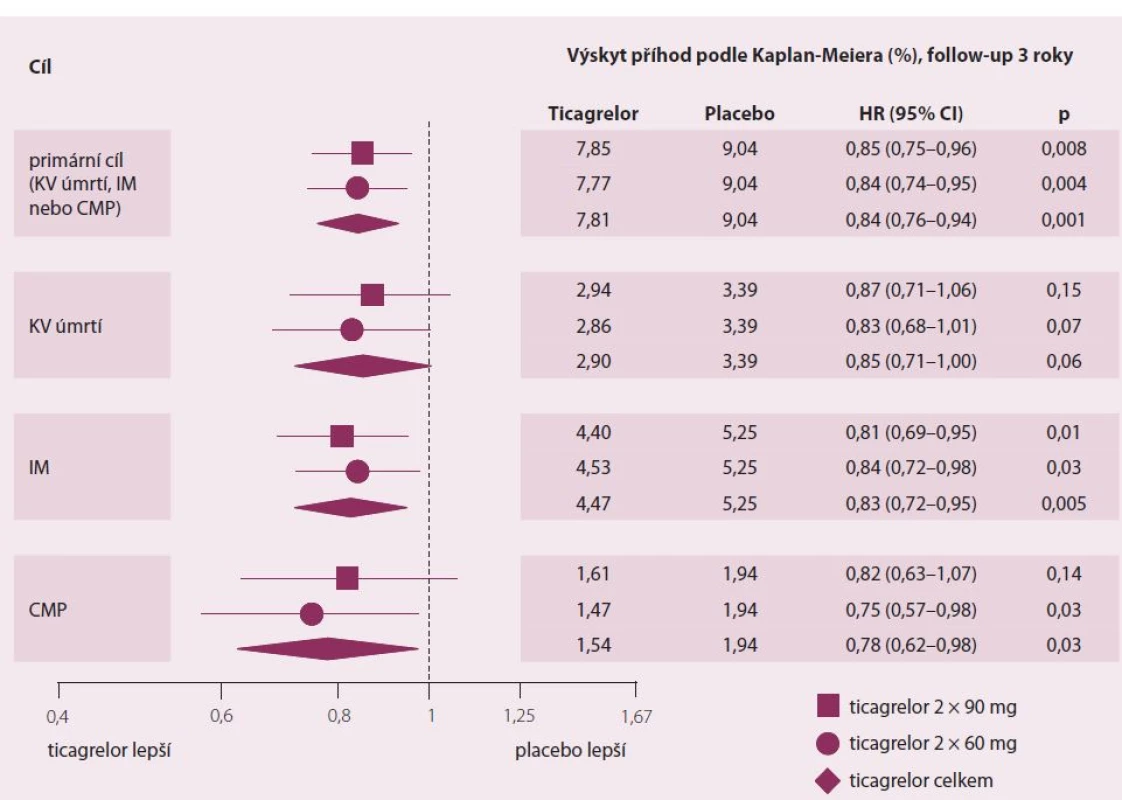
Nebyl pozorován žádný rozdíl podle věku, pohlaví, typu infarktu myokardu či dávce kyseliny acetylsalicylové.
Primární bezpečnostní cíl – TIMI velké krvácení – byl vyšší na obou dávkách ticagreloru s výskytem po třech letech 2,60 % na 2 × 90 mg, 2,30 % na 2 × 60 mg a 1,06 % na placebu (p < 0,001 pro obě dávky vs placebo). TIMI malé krvácení bylo podobné na obou dávkách i na placebu (tab. 3). Výskyt fatálního krvácení byl pod 1 % a nelišil se mezi skupinami. Předčasné ukončení pro krvácení bylo častější na aktivní léčbě 7,8 % pro 2 × 90 mg, 6,2 % pro 2 × 60 mg a 1,5 % pro placebo.
Tab. 3. PEGASUS-TIMI 54 – bezpečnostní cíl. 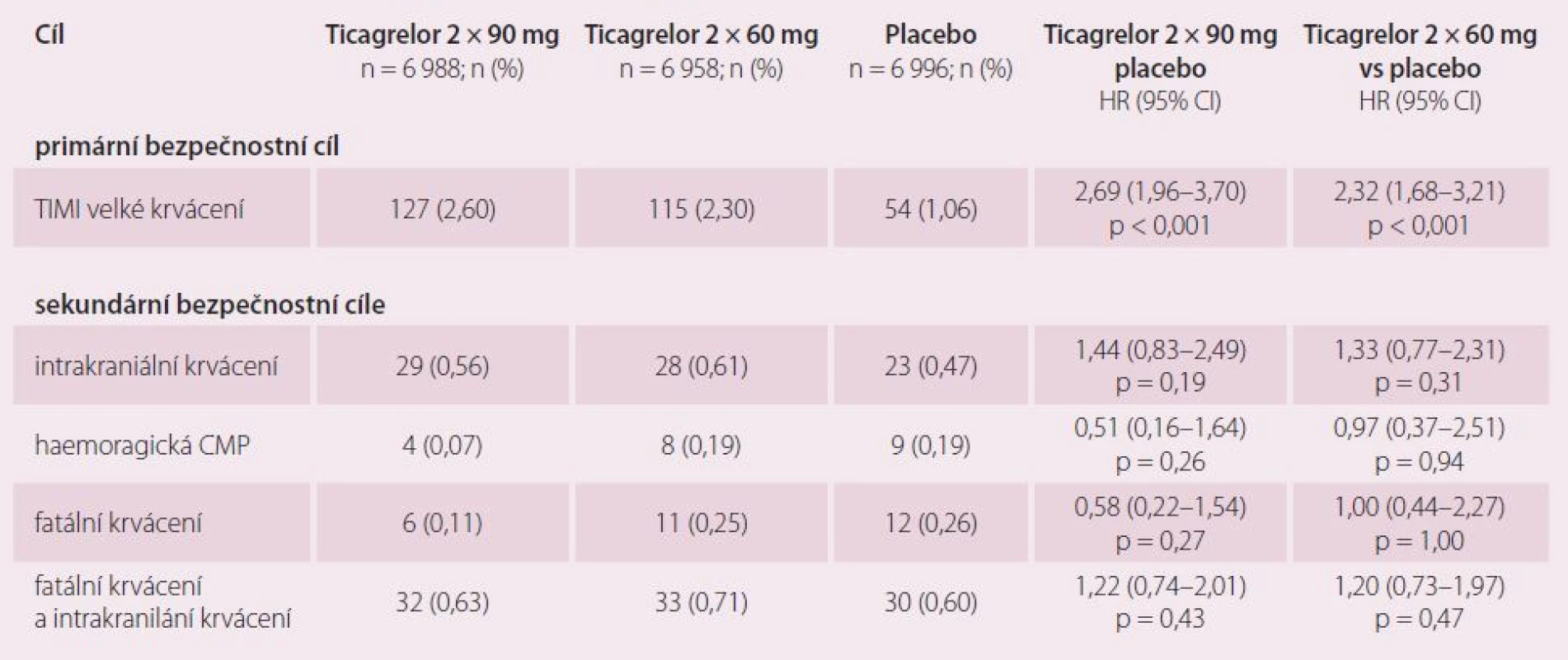
Dušnost byla častější na obou dávkách a pro dušnost byla významně častěji léčba ukončena na obou dávkách 6,5 % vs 4,5 % vs 0,8 % (p < 0,001 pro obě dávky). Celkový výskyt dušnosti za tři roky byl 18,9 % na 2 × 90 mg, 15,8 % na 2 × 60 mg a 6,4 % v placebové větvi (p < 0,001 pro obě dávky vs placebo). Většina dušností byla charakterizována jako lehká (59 %) nebo střední (37 %). Závažná dyspnoe byla udána jen v 0,4 % za tři roky. Nebyly pozorovány žádné nežádoucí účinky hepatotoxické, nefrotoxické ani bradyarytmické (tab. 4).
Tab. 4. Krvácení a nežádoucí účinky. 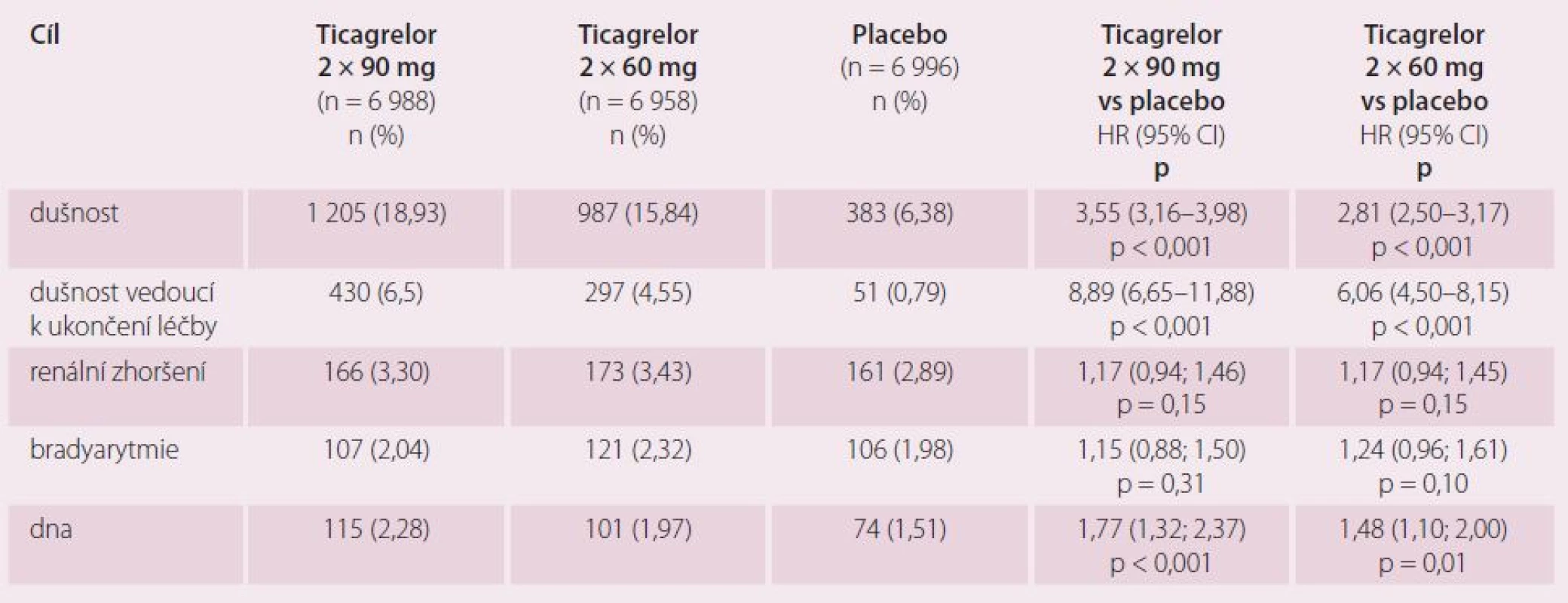
Diskuze
Pacienti po srdečním infarktu zůstávají ve velkém riziku další koronární příhody po dlouhou dobu. Studie PEGASUS prokázala, že P2Y12 inhibitor ticagrelor přidaný k malé dávce kyseliny acteylsalicylové snižuje signifikantně kardiovaskulární úmrtí, infarkt myokardu a cévní mozkovou příhodu. Účinek ticagreloru je konzistentní u všech podskupin.
Ohledně délky antiagregační terapie se vedou dlouhé diskuze. Některé zpětné analýzy ukazují, že prodloužení duální antiagregace by mohlo být prospěšné, a to přesto, že studie s klopidogrelem toto nepotvrdila [11 – 13]. Krátce po této práci byla publikována analýza studie CHARISMA prokazující efekt na snížení ischemických příhod, přesto ale současná doporučení udávají doporučenou délku podávání pro P2Y12 receptorové antagonisty jeden rok po akutním infarktu myokardu [4 – 6]. Výsledky studie PEGASUS ‑ TIMI 54 nyní přinášejí jasný průkaz prospěchu z dlouhodobého podávání ticagreloru u pacientů s předchozím akutním koronárním syndromem, a to na kardiovaskulární mortalitu. Podobné výsledky přinesla i studie DAPT u pacientů po implantaci koronárního stentu, kde byl P2Y12 blokátor podáván 12 – 30 měsíců po implantaci stentu společně s malou dávkou kyseliny acetylsalicylové. Po ukončení léčby ve studii DAPT se ale brzy ukázaly nežádoucí účinky potvrzující, že nemocní by neměli přerušovat duální antiagregační léčbu a měli by v ní pokračovat i po 12 měsících. Obě studie – PEGASUS ‑ TIMI 54 i DAPT potvrdily, že prodloužené podávání inhibitoru P2Y12 receptoru vede ke snížení ischemických příhod, ale za cenu zvýšeného rizika krvácení u nemocných s koronárním onemocněním.
Ticagrelor zvyšuje TIMI velké krvácení, krvácení vyžadující transfuzi i krvácení vedoucí k ukončení léčby. Výskyt závažných krvácení, ireverzibilních či smrtelných, je ale < 1 % za tři roky ve všech třech větvích studie. Je třeba připomenout, že protokol vyloučil nemocné s recentním krvácením, předchozí cévní mozkovou příhodou či na perorální antikoagulaci. Proto by bezpečnostní hledisko nemělo být aplikováno na celou populaci.
Obě dávky ticagreloru způsobovaly dušnost, většinou krátce po zahájení léčby, ale tato dušnost nebyla natolik závažná, aby vedla k ukončení léčby ve srovnání s placebem. Tento výskyt ve studii PEGASUS ‑ TIMI 54 byl ale vyšší než ve studii PLATO, možná proto, že investigátoři již cíleně dušnost sledovali [3]. Jiným vysvětlením je, že v akutní fázi je dušnost považována za přirozenou součást zdravotního stavu, zatímco u stabilních nemocných se již očekává méně.
Obě dávky ticagreloru – 2 × 60 mg i 2 × 90 mg byly stejně účinné na primární cíl účinnosti, avšak menší počet ukončení a lepší tolerance byla pozorována po nižší dávce. Obě dávky byly testovány jako přidání k malé dávce kyseliny acetylsalicylové, což je plně v souladu s doporučeními pro stabilní ischemickou chorobu srdeční [14,15].
Závěr
Přidání 2 × 90 mg ticagreloru nebo 2 × 60 mg ticagreloru k malé dávce kyseliny acetylsalicylové snižovalo riziko kardiovaskulárního úmrtí, srdečního infarktu či cévní mozkové příhody u nemocných s infarktem myokardu před 1 – 3 lety. Počet TIMI velkých krvácení byl vyšší při léčbě ticagrelorem [8]. Když dáme dohromady tato data s daty o použití ticagreloru v akutní fázi infarktu myokardu a následných 12 měsíců, můžeme vyslovit doporučení pro dlouhodobé užívání ticagreloru u nemocných s vysokým rizikem po infarktu myokardu, kteří ale nemají vysoké riziko krvácení.
Studie PEGASUS pravděpodobně přepíše doporučení pro antiagregační terapii po infarktu myokardu. Do budoucnosti můžeme očekávat především diskuzi, jak s duální antiagregací po roce od infarktu myokardu – bude doživotně? Velká diskuze bude pravděpodobně vedena i o doporučené dávce ticagreloru, protože dávka 2 × 60 mg se ukázala minimálně rovnocenná (ne‑li lepší) dávce 2 × 90 mg.
Doručeno po recenzi: 17. 3. 2015
Přijato do redakce: 19. 3. 2015
prof. MU Dr. Jindřich Špinar, CSc., FESC
www.fnbrno.cz
jspinar@fnbrno.cz
Zdroje
1. Scirica BM, Vannon CH, Emanuelsson H et al. The incidence or arrhytmias and clinical arrhytmias events in patients with acute coronary syndromes treated with ticagrelor or clopidogrel in the PLATO trial. J Am Coll Cardiol 2010; 55 (10s1). doi:10.1016/ S0735 – 1097(10)61007 – 8.
2. Špinar J, Vítovec J. Ticagrelor a studie PLATO. Kardiol Rev Int Med 2011; 13(4): 254 – 257.
3. Wallentin L, Becker RC, Budaj A et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009; 361 : 1045 – 1057. doi: 10.1056/ NEJMoa0904327.
4. Amsterdam EA, Wenger NK, Brindis RG et al. 2014 AHA/ ACC Guideline for the management of patients with non‑ST‑elevation acute coronary syndromes: executive summary: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines. Circulation 2014; 130 : 2354 – 2394. doi: 10.1161/ CIR.0000000000000133.
5. Hamm CW, Bassand JP, Agewall S et al. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST‑segment elevation: The Task Force for the management of acute coronary syndromes (ACS) in patients presenting without persistent ST‑segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2011; 32 : 2999 – 3054. doi: 10.1093/ eurheartj/ ehr236.
6. O'Gara PT, Kushner FG, Ascheim DD et al. 2013 ACCF/ AHA guideline for the management of ST‑elevation myocardial infarction: a report of the American College of Cardiology Foundation/ American Heart Association Task Force on Practice Guidelines. Circulation 2013; 127: e362 – e425.
7. Steg PG, James SK, Atar D et al. ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST‑segment elevation. Eur Heart J 2012; 33 : 2569 – 2619. doi: 10.1093/ eurheartj/ ehs215.
8. Bonaca MP, Bhatt DL, Cohen M for the PEGASUS investigators: Ticagrelor for long‑term secondary prevention of atherothrombotic events in patients with prior myocardial Infarctio. N Engl J Med 2015. Epub ahead of print. doi: 10.1056/ NEJMoa1500857.
9. Bonaca MP, Bhatt DL, Braunwald E et al. Design and rationale for the prevention of cardiovascular events in patients with prior heart attack using ticagrelor compared to placebo on a background of aspirin‑thrombolysis in myocardial infarction 54 (PEGASUS ‑ TIMI 54) trial. Am Heart J 2014; 167 : 437 – 444. doi: 10.1016/ j.ahj.2013.12.020.
10. Mehran R, Rao SV, Bhatt DL et al: Standardized bleeding definitions for cardiovascular clinical trial. A consensus report from the bleeding academic research consortium. Circulation 2011; 123 : 2736 – 2747. doi: 10.1161/ CIRCULATIONAHA.110.009449.
11. Bhatt DL, Fox KA, Hacke W et al. Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events. N Engl J Med 2006; 354 : 1706 – 1717.
12. Bhatt DL, Flather MD, Hacke W et al. Patients with prior myocardial infarction, stroke, or symptomatic peripheral arterial disease in the CHARISMA trial. J Am Coll Cardiol 2007; 49 : 1982 – 1988.
13. Mauri L, Kereiakes DJ, Yeh RW et al. Twelve or 30 months of dual antiplatelet therapy after drug‑eluting stents. N Engl J Med 2014; 371(23): 2155 – 2166. doi: 10.1056/ NEJMoa1409312.
14. Fihn SD, Gardin JM, Abrams J et al. 2012 ACCF/ AHA/ ACP/ AATS/ PCNA/ SCAI/ STS guideline for the diagnosis and management of patients with stable ischemic heart disease: a report of the American College of Cardiology Foundation/ American Heart Association task force on practice guidelines, and the American College of Physicians, American Association for Thoracic Surgery, Preventive Cardiovascular Nurses Association, Society for Cardiovascular Angiography and Interventions, and Society of Thoracic Surgeons. Circulation 2012; 126: e354 – e471. doi: 10.1161/ CIR.0b013e318277d6a0.
15. Montalescot G, Sechtem U, Achenbach S et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J 2013; 34 : 2949 – 3003. doi: 10.1093/ eurheartj/ eht296.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek Genetika kardiomyopatií
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2015 Číslo 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Vyšetření cerebrovaskulární rezervy u asymptomatických pacientů s významnou stenózou vnitřní karotické tepny
- Genetika kardiomyopatií
- Katetrizační léčba chronické stabilní ischemické choroby srdeční v současnosti
- Katetrizační uzávěr foramen ovale patens u potápěčů
- Katetrizační léčba fibrilace síní
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- Není perikarditida jako perikarditida – kazuistika
- Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
- Nové studie dávají naději na zlepšení terapie aterosklerózy
-
Hlavolamy 2015
Propojení kardiologie a diabetologie - Vyhlášení výsledků autorské soutěže O nejlepší kazuistiku v roce 2014
- Vývoj a úkoly klinické farmakologie ve zdravotnické péči v ČR
- TDM antibiotik v klinické praxi
- prof. MUDr. Josef Veselka, CSc., FESC, FSCAI, FICA (*23. 3. 1965)
- TDM digoxinu v klinické praxi
- Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
- Lékové interakce a současná klinická praxe
- Přímá perorální antikoagulancia – perspektivy terapeutického monitorování
- Klinická farmakologie antirevmatik
- Specifika klinických hodnocení léčiv časných fází I a II
- Význam TDM metotrexátu při terapii psoriázy
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



