-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Katetrizační uzávěr foramen ovale patens u potápěčů
Catheter‑based patent foramen ovale closure in divers
Patent foramen ovale (PFO) is associated with increased risk of decompression sickness (DCS) in divers due to paradoxical embolization of nitrogen bubbles from venous blood to systemic circulation. Despite the high prevalence of PFO, many important questions, including optimal screening, risk stratification and management strategy, remain unanswered. Recently published data suggest possible effectiveness of PFO closure as well as conservative diving measures in preventing arterial gas embolization. This review aims to introduce the basic principles of physiology and pathophysiology of bubble formation and to summarize current literature on PFO and diving and review the possibilities of management of symptomatic divers.
Keywords:
patent foramen ovale – catheter‑based closure – decompression sickness
Autoři: J. Honěk
Působiště autorů: Kardiologická klinika 2. LF UK a FN v Motole, Praha
Vyšlo v časopise: Kardiol Rev Int Med 2015, 17(1): 25-27
Kategorie: Kardiologická revue
Souhrn
Foramen ovale patens (PFO) je asociováno se zvýšeným rizikem vzniku dekompresní choroby potápěčů (DCS). Mechanizmem je paradoxní embolizace dusíkových bublin z žilní krve do systémového oběhu skrze PFO. Recentně publikovaná data poukazují na možnou efektivitu jak katetrizačního uzávěru, tak konzervativních profilů ponoru v prevenci paradoxní embolizace bublin. Tento přehledový článek si klade za cíl uvést základní fyziologické a patofyziologické principy tvorby bublin a vzniku DCS a shrnout současné poznatky o vztahu PFO a DCS a možnostech léčby symptomatických potápěčů.
Klíčová slova:
foramen ovale patens – katetrizační uzávěr – dekompresní choroba
Potápěč je při pobytu pod vodní hladinou vystaven zvýšenému tlaku okolního prostředí. Tato okolnost je spojena s řadou fyziologických, ale i patofyziologických změn, a také se specifickými zdravotními riziky, zejména dekompresní chorobou potápěčů (DCS). V posledních letech byla intenzivně studována souvislost foramen ovale patens (PFO) s různými chorobnými stavy. U potápěčů je PFO spojeno se zvýšeným rizikem vzniku DCS [1]. I přes vysokou prevalenci PFO v dospělém věku (~27 %) [2] však zůstávají nezodpovězeny základní otázky screeningové strategie, rizikové stratifikace i léčby symptomatických potápěčů. Tento přehledový článek si klade za cíl uvést základní fyziologické a patofyziologické principy tvorby bublin a vzniku DCS a shrnout současné poznatky k tématu PFO a DCS včetně možnosti katetrizačního uzávěru PFO u symptomatických potápěčů.
Dekompresní choroba potápěčů – fyziologie a patofyziologie
Dýchací směs (vzduch, případně jiná směs obsahující kyslík) je potápěči dodávána z přístroje (SCUBA – self contained underwater breathing apparatus) pod okolním tlakem zvyšujícím se s hloubkou ponoru. Podle Henryho zákona jsou plyny rozpouštěny v tkáních v množství úměrném jejich parciálnímu tlaku. V hloubce tedy dochází k sycení tkání dusíkem, který se nezúčastní metabolizmu. Rychlost saturace se liší mezi tkáněmi a je závislá na jejich kapilaritě a chemickém složení [3]. Při výstupu potápěče k hladině se tlakový gradient obrací, dýchaná směs obsahuje nižší parciální tlak dusíku a ten je postupně vysycován z tkání a vydýcháván. Pokud okolní tlak poklesne příliš rychle, dojde k přesycení (supersaturaci) tkání a ke vzniku plynné fáze (bublin) [4].
Proces vzniku bublin je zkoumán již přes 100 let a stále zůstává mnoho aspektů nejasných. Předpokládá se apriorní přítomnost určité formy mikrojader, přestože jejich přesná povaha stále není známa [4]. Z praktického hlediska je významné, že rychlost saturace a desaturace je odlišná v různých tkáních. K popisu celotělové kinetiky dusíku se používají multikompartmentové matematické modely [5]. Na těchto modelech jsou založeny potápěčské tabulky a počítače používané při plánování a v průběhu ponoru. Pomocí správného plánování lze teoreticky předejít přesycení tkání a tvorbě bublin.
Dekompresní choroba je způsobena vznikem a růstem bublin v přesycených tkáních při výstupu na hladinu. Tyto bubliny mohou působit buď lokálně v místě vzniku, nebo embolizovat krevním řečištěm [6]. Malé množství bublin v žilní krvi lze sonograficky detekovat i po běžných ponorech [7,8] (obr. 1). Většina potápěčů však zůstává asymptomatická, protože bubliny jsou efektivně filtrovány v plicním řečišti. Symptomy mohou vzniknout buď při masivní embolizaci (plicní forma DCS při závažném porušení dekompresních pravidel – např. nekontrolovaný výstup k hladině), nebo při paradoxní embolizaci bublin do systémového oběhu u potápěče s permanentním či tranzientním pravo ‑ levým zkratem. U potápěčů s PFO způsobují arteriální plynové emboly (bubliny) obturací kapilár lokální ischemii. V periferii je navíc stále zvýšený parciální tlak dusíku, proto nedochází k rozpouštění bublin, ale naopak k jejich dalšímu růstu [6].
Obr. 1. Echokardiografický obraz dusíkových bublin v pravostranných srdečních oddílech. 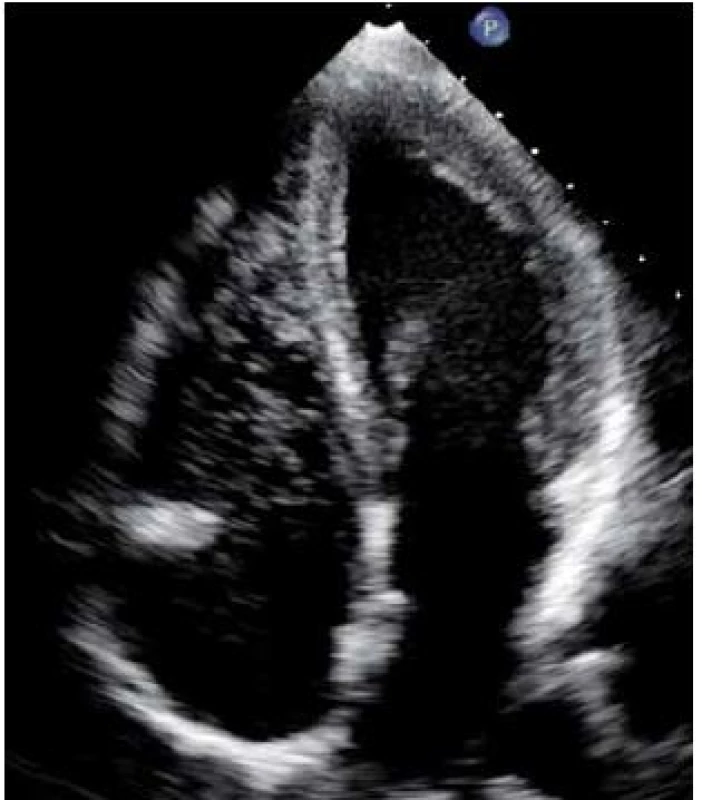
Klinický obraz DCS je velice heterogenní, odpovídá množství, velikosti a distribuci bublin. Podle symptomatologie rozlišujeme formu kožní, muskuloskeletální, neurologickou a plicní. Muskuloskeletální forma se projevuje krutou bolestí velkých kloubů a předpokládá se, že je způsobena lokální tvorbou bublin v avaskulární kloubní chrupavce [9]. Naopak PFO je spojováno zejména s formou neurologickou, ale i kožní. Zdá se, že paradoxní embolizace bublin skrze PFO by mohla hrát významnou roli u těchto forem DCS [5].
Dekompresní choroba potápěčů – role foramen ovale patens
Souvislost mezi PFO a DCS byla poprvé popsána v 80. letech 20. století [10,11]. Od té doby byla opakovaně zaznamenána vyšší prevalence PFO u potápěčů s neurologickou a kožní formou DCS [12 – 15]. Současně bylo dokumentováno, že riziko vzniku DCS roste s velikostí pravo ‑ levého zkratu [15]. Mimo tyto akutní projevy byly popsány také možné chronické následky opakovaných asymptomatických embolizací do centrálního nervového systému (CNS) v podobě mnohočetných lézí detekovatelných na magnetické rezonanci mozku [16].
Patofyziologickým podkladem vzniku DCS u potápěčů s PFO je paradoxní embolizace bublin. Při pobytu pod vodou dochází k nárůstu tlaku v pravé síni v důsledku redistribuce krve z periferie do hrudníku [17], potápěči navíc v průběhu ponoru často opakovaně provádějí Valsalvův manévr (k vyrovnání tlaku ve středouší), v důsledku toho může dojít k intermitentnímu pravo ‑ levému zkratu skrze PFO. Výskyt určitého množství žilních bublin je přitom častý i po běžném rekreačním ponoru [8]. Proto se můžeme setkat u potápěčů s PFO s projevy DCS i v případě, že nedošlo k porušení dekompresních pravidel [14]. Tuto nepredikovatelnou událost nazýváme nevyprovokovanou dekompresní příhodou. Potápěči s PFO navíc častěji trpí recidivující DCS [18].
Na druhou stranu je také diskutována možnost paradoxní embolizace transpulmonální cestou [19]. Vzhledem k nízké prevalenci významných plicních arteriovenózních malformací [20] a naopak k vysoké prevalenci PFO [2] a výše zmíněným klinickým studiím [12 – 16,18] se však zdá, že PFO hraje v paradoxní embolizaci bublin u potápěčů významnější roli. Přesto zůstává v péči o potápěče s PFO řada nezodpovězených otázek. U symptomatických potápěčů se nabízejí tři možnosti dalšího postupu – ukončení činnosti, konzervativní přístup k potápění a katetrizační uzávěr PFO.
Katetrizační uzávěr foramen ovale patens
Řada autorů již formulovala hypotézu, že katetrizační uzávěr PFO by mohl vést k prevenci paradoxní embolizace bublin u potápěčů a snížit riziko vzniku DCS [21 – 23]. K dispozici je však doposud pouze jediná studie, ve které bylo prokázáno, že katetrizační uzávěr vedl k eliminaci arteriálních bublin po ponoru [24]. V této studii byl sonograficky srovnán výskyt venózních a arteriálních bublin u potápěčů po katetrizačním uzávěru PFO (n = 20) a s PFO (n = 27). Intervence byly prováděny okludery Amplatzer septal occluder (AGA Medical Corporation, Golden Valley, USA) a Occlutech Figulla PFO Occluder N (Occlutech GmbH, Jena, Německo). Ve studii nebyly detekovány žádné arteriální bubliny u potápěčů po katetrizačním uzávěru PFO, současně se u žádného z těchto potápěčů nevyskytly symptomy DCS (tento trend nedosáhl statistické významnosti). Limitací studie je její experimentální charakter (ponory byly simulovány v hyperbarické komoře), nízký počet pacientů a absence klinického primárního cíle (primárním cílem byla sonograficky ověřená přítomnost arteriálních bublin). Přestože jsou tyto výsledky velice povzbudivé, definitivní odpověď na to, jakou úlohu bude mít katetrizační uzávěr PFO u potápěčů, by měly přinést zejména longitudinální klinické studie.
Konzervativní postup
Za konzervativní postup u potápěčů, kterým bylo zjištěno PFO, lze označit buď zákaz další činnosti, nebo doporučení konzervativního způsobu potápění. Tento soubor opatření má za cíl snížení rizika vzniku dusíkových bublin, a tím i výskytu DCS. Prevence vzniku bublin můžeme dosáhnout jak omezením saturace tkání (zkrácená expozice, mělčí ponor, snížený obsah dusíku v dýchané směsi), tak zpomalením jejich desaturace (pomalejší rychlost výstupu). Doposud je však málo důkazů o efektivitě těchto postupů u potápěčů s PFO [25,26]. Obecně lze také snížit riziko vzniku bublin správnou přípravou na ponor (preconditioning) pomocí hydratace a lehké fyzické zátěže bezprostředně před ponorem [27].
Závěr
Foramen ovale patens je spojeno se zvýšeným rizikem vzniku DCS u potápěčů. I přes vysokou prevalenci PFO však stále zůstává v této problematice řada otázek a chybí doporučené postupy. Některé recentní studie naznačují možnou efektivitu katetrizačního uzávěru PFO v prevenci DCS. Pokud bude tato hypotéza potvrzena v longitudinálních klinických studiích, mohl by být katetrizační uzávěr PFO efektivní metodou v sekundární prevenci DCS v situacích, kdy nelze dostatečně přizpůsobit potápěčskou praxi přítomnosti PFO, tedy zejména u profesionálních potápěčů.
Podpořeno MZ ČR – RVO, FN v Motole 00064203.
Doručeno do redakce: 4. 1. 2015
Přijato po recenzi: 15. 1. 2015
MU Dr. Jakub Honěk
www.fnmotol.cz
jakub.honek@gmail.com
Zdroje
1. Bove AA. The PFO gets blamed again…perhaps this time it is real. JACC Cardiovasc Interv 2014; 7 : 409 – 410. doi: 10.1016/ j.jcin.2014.01.152.
2. Hagen PT, Scholz DG, Edwards WD. Incidence and size of patent foramen ovale during the first 10 decades of life: an autopsy study of 965 normal hearts. Mayo Clin Proc 1984; 59 : 17 – 20.
3. Doolette DJ, Mitchell SJ. The physiological kinetics of nitrogen and the prevention of decompression sickness. Clin Pharmacokinet 2001; 40 : 1 – 14.
4. Papadopoulou V, Eckersley RJ, Balestra C et al. A critical review of physiological bubble formation in hyperbaric decompression. Adv Colloid Interface Sci 2013; 191 – 192 : 22 – 30. doi: 10.1016/ j.cis.2013.02.002.
5. Bove AA. Diving medicine. Am J Respir Crit Care Med 2014; 189 : 1479 – 1486. doi: 10.1164/ rccm.201309 ‑ 1662CI.
6. Vann RD, Butler FK, Mitchell SJ et al. Decompression Illness. Lancet 2011; 377 : 153 – 164. doi: 10.1016/ S0140 ‑ 6736(10)61085 ‑ 9.
7. Dunford RG, Vann RD, Gerth WA et al. The incidence of venous gas emboli in recreational diving. Undersea Hyperb Med 2002; 29 : 247 – 259.
8. Ljubkovic M, Dujic Z, Møllerløkken A et al. Venous and arterial bubbles at rest after no ‑ decompression air dives. Med Sci Sports Exerc 2011; 43 : 990 – 995. doi: 10.1249/ MSS.0b013e31820618d3.
9. Gempp E, Blatteau JE, Simon O et al. Musculoskeletal decompression sickness and risk of dysbaric osteonecrosis in recreational divers. Diving Hyperb Med 2009; 39 : 200 – 204.
10. Wilmshurst PT, Ellis PT, Jenkins BS. Paradoxical gas embolism in a scuba diver with an atrial septal defect. Br Med J 1986; 293 : 1277.
11. Moon RE, Camporesi EM, Kisslo JA. Patent foramen ovale and decompression sickness in divers. Lancet 1989; 1 : 513 – 514.
12. Cantais E, Louge P, Suppini A et al. Right ‑ to ‑ left shunt and risk of decompression illness with cochleovestibular and cerebral symptoms in divers: case control study in 101 consecutive dive accidents. Crit Care Med 2003; 31 : 84 – 88.
13. Wilmshurst PT, Pearson MJ, Walsh KP et al. Relationship between right ‑ to ‑ left shunts and cutaneous decompression illness. Clin Sci 2001; 100 : 539 – 542.
14. Germonpré P, Dendale P, Unger P et al. Patent foramen ovale and decompression sickness in sports divers. J Appl Physiol 1998; 84 : 1622 – 1626.
15. Torti SR, Billinger M, Schwerzmann M et al. Risk of decompression illness among 230 divers in relation to the presence and size of patent foramen ovale. Eur Heart J 2004; 25 : 1014 – 1020.
16. Knauth M, Ries S, Pohimann S et al. Cohort study of multiple brain lesions in sport divers: role of a patent foramen ovale. BMJ 1997; 314 : 701 – 705.
17. Marabotti C, Scalzini A, Menicucci D et al. Cardiovascular changes during SCUBA diving: an underwater Doppler echocardiographic study. Acta Physiol 2013. doi: 10.1111/ apha.12112.
18. Gempp E, Louge P, Blatteau JE et al. Risks factors for recurrent neurological decompression sickness in recreational divers: a case ‑ control study. J Sports Med Phys Fitness 2012; 52 : 530 – 536.
19. Ljubkovic M, Zanchi J, Breskovic T et al. Determinants of arterial gas embolism after scuba diving. J Appl Physiol 2012; 112 : 91 – 95. doi: 10.1152/ japplphysiol.00943.2011.
20. Cartin‑Ceba R, Swanson KL, Krowka MJ. Pulmonary arteriovenous malformations. Chest 2013; 144 : 1033 – 1044. doi: 10.1378/ chest.12 ‑ 0924.
21. Billinger M, Zbinden R, Mordasini R et al. Patent foramen ovale closure in recreational divers: effect on decompression illness and ischaemic brain lesions during long‑term follow‑up. Heart 2011; 97 : 1932 – 1937. doi: 10.1136/ heartjnl ‑ 2011 ‑ 300436.
22. Walsh KP, Wilmshurst PT, Morrison WL. Transcatheter closure of patent foramen ovale using the Amplatzer septal occluder to prevent recurrence of neurological decompression illness in divers. Heart 1999; 81 : 257 – 261.
23. Lairez O, Cournot M, Minville V et al. Risk of neurological decompression sickness in the diver with right ‑ to ‑ left shunt: literature review and meta‑analysis. Clin J Sport Med 2009; 19 : 231 – 235. doi: 10.1097/ JSM.0b013e31819b0fa2.
24. Honěk J, Šrámek M, Šefc L et al. Effect of catheter‑based patent foramen ovale closure on the occurrence of arterial bubbles in scuba divers. JACC Cardivasc Interv 2014; 7 : 403 – 408. doi: 10.1016/ j.jcin.2013.12.199.
25. Honěk J, Šrámek M, Šefc L et al. Effect of conservative dive profiles on the occurrence of venous and arterial bubbles in divers with a patent foramen ovale: a pilot study. Int J Cardiol 2014; 176 : 1001 – 1002. doi: 10.1016/ j.ijcard.2014.04.218.
26. Klingmann C, Rathmann N, Hausmann D et al. Lower risk of decompression sickness after recommendation of conservative decompression practices in divers with and without vascular right ‑ to ‑ left shunt. Diving Hyperb Med 2012; 42 : 146 – 150.
27. Gempp E, Blatteau JE. Preconditioning methods and mechanisms for preventing the risk of decompression sickness in scuba divers: a review. Res Sports Med 2010; 18 : 205 – 218. doi: 10.1080/ 15438627.2010.490189.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek Genetika kardiomyopatií
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2015 Číslo 1- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Vyšetření cerebrovaskulární rezervy u asymptomatických pacientů s významnou stenózou vnitřní karotické tepny
- Genetika kardiomyopatií
- Katetrizační léčba chronické stabilní ischemické choroby srdeční v současnosti
- Katetrizační uzávěr foramen ovale patens u potápěčů
- Katetrizační léčba fibrilace síní
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- Není perikarditida jako perikarditida – kazuistika
- Studie Pegasus – duální antiagregace (ASA + ticagrelor) dlouhodobě po infarktu myokardu
- Nové studie dávají naději na zlepšení terapie aterosklerózy
-
Hlavolamy 2015
Propojení kardiologie a diabetologie - Vyhlášení výsledků autorské soutěže O nejlepší kazuistiku v roce 2014
- Vývoj a úkoly klinické farmakologie ve zdravotnické péči v ČR
- TDM antibiotik v klinické praxi
- prof. MUDr. Josef Veselka, CSc., FESC, FSCAI, FICA (*23. 3. 1965)
- TDM digoxinu v klinické praxi
- Patofyziologie a diagnóza obstrukce u hypertrofické kardiomyopatie
- Lékové interakce a současná klinická praxe
- Přímá perorální antikoagulancia – perspektivy terapeutického monitorování
- Klinická farmakologie antirevmatik
- Specifika klinických hodnocení léčiv časných fází I a II
- Význam TDM metotrexátu při terapii psoriázy
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- TDM digoxinu v klinické praxi
- Lékové interakce a současná klinická praxe
- Srdeční resynchronizační terapie – kdy a u koho ji v současnosti indikovat?
- TDM antibiotik v klinické praxi
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



