-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Krční uzlinový syndrom z pohledu otorinolaryngologa
Cervical lymphadenopathy from the perspective of an otolaryngologist
By using the term cervical lymphadenopathy (CL) we describe the pathological changes in terms of size, shape, structure, or clustering of lymph nodes in the neck region. These changes may or may not be accompanied by further symptoms. Inflammatory and malignant lesions in the area of head and neck are the most common causes of CL. In children, infectious causes by far prevail over other etiology and and they are also a very frequent reason for pediatricians' visits.
Although the region of neck is a matter of otorhinolaryngology (ENT), primary care of a child's patient with CL is work for pediatrician. This one should be able to perform a basic diagnostic-therapeutic procedures.
The correct diagnostics and subsequently an adequately chosen therapy requires basic conditions.1) The basic knowledge of clinical anatomy, physiology, pathophysiology of lymphatic system. 2) Doctor's general knowledge in differential diagnostics, for one thing within the illness of lymph nodes but also concerning other diseases, which can be presented as swelling in the neck region. 3) The knowledge of diagnostic-therapeutic possibilities and procedures.Key words:
cervical lymphadenopathy, lymph node, children, differential diagnostics, diagnostic-therapeutic procedures
Autoři: K. Sobotková
Působiště autorů: Klinika dětské otorinolaryngologie LF MU a FN Brno, Lékařská fakulta Masarykovy univerzity, Brno přednosta prof. MUDr. I. Šlapák, CSc.
Vyšlo v časopise: Čes-slov Pediat 2015; 70 (3): 166-173.
Kategorie: Přehledové články
Souhrn
Termínem krční uzlinový syndrom (KUS) se označují patologické změny ve velikosti, tvaru, struktuře ev. seskupení lymfatických uzlin v oblasti zevního krku. Tyto změny mohou nebo nemusí být doprovázeny dalšími symptomy. Nejčastějšími příčinami KUS jsou bezesporu zánětlivá onemocnění a nádorové procesy probíhající v oblasti hlavy a krku. V dětském věku infekční příčiny výrazně převažují nad ostatní etiologií a jsou zároveň velmi častým důvodem návštěvy dětských lékařů.
Ačkoliv je zevní krk oblastí náležící oboru ORL, primární péče o dětského pacienta s krční lymfadenopatií spadá do rukou praktického lékaře pro dítě a dorost (PLDD). Ten by měl být schopen provést základní diagnosticko-terapeutický postup.
Správná diagnóza a následně adekvátně zvolená terapie vyžaduje základní předpoklady. 1) Znalost základů klinické anatomie, fyziologie a patofyziologie lymfatického systému. 2) Orientaci lékaře v základní diferenciální diagnostice, jednak v rámci onemocnění uzlinového systému, ale také v rámci dalších chorob, které se mohou prezentovat jako zduření v oblasti krku a imitovat tak KUS. 3) Znalost diagnostických a terapeutických možností a postupů.Klíčová slova:
krční uzlinový syndrom, lymfatická uzlina, děti, diferenciální diagnostika, diagnosticko-terapeutický postupZÁKLADY ANATOMIE LYMFATICKÉHO SYSTÉMU
Zdravá, „normální“ lymfatická uzlina (LU) je ledvinovitého tvaru, uváděné jsou velikosti do 1 cm v longitudinálním rozměru v oblasti krku a axilách, do 1,5 cm v oblasti třísel. V praxi však u zdravých dětí nalézáme fyziologické LU velikosti 1,5 cm také v oblasti submandibulární. U velkého počtu dětí jsou i „normální“ LU palpovatelné, při určitých pozicích hlavy i viditelné.
K usnadnění komunikace mezi lékaři je v současné době mezinárodně užívána modifikovaná klasifikace dle Robbinse (Ferlito, 2009) [1], rozdělující krk na 6 základních oblastí, kterým odpovídá lokalizace jednotlivých skupin krčních LU (obr. 1). U dětských pacientů však stále používáme starší dělení (tab. 1). Jednotlivé skupiny LU charakteristicky drénují určitou oblast hlavy a krku, čehož lze s výhodou využít při pátrání po příčině lymfadenopatie [2].
Obr. 1. Schéma mezinárodní klasifikace krčních oblastí. 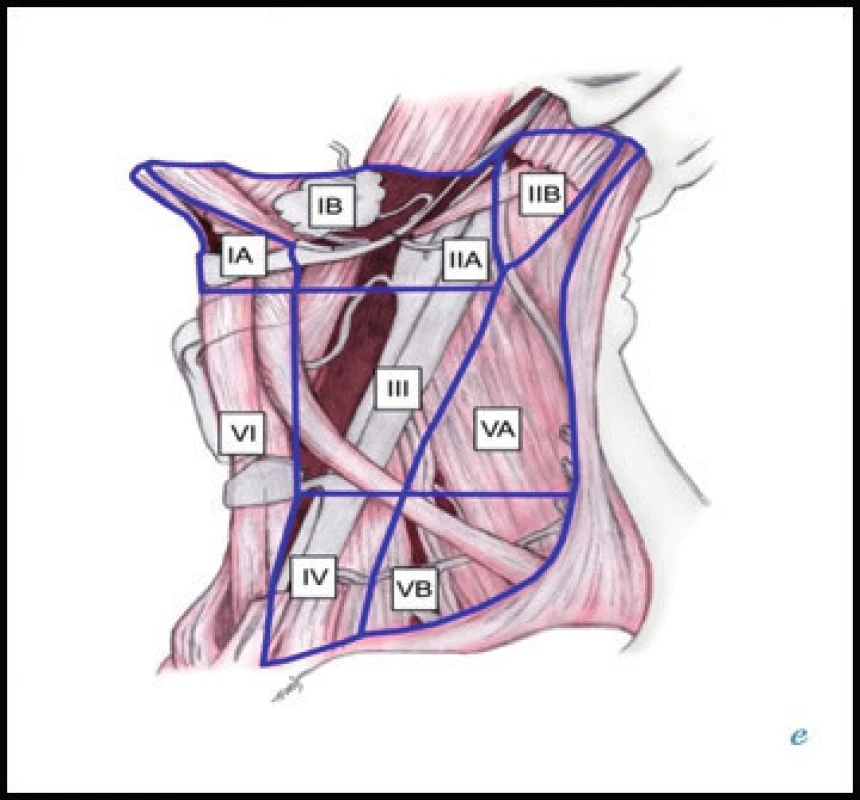
Vysvětlivky I až VI – rozdělení krku na 6 základních oblastí, kterým odpovídá lokalizace jednotlivých skupin krčních LU (pro srovnání viz také tab. 1) IA, IB – rozdělení oblasti I předním bříškem musculus digastricus na 2 podoblasti IIA, IIB – rozdělení oblasti II průběhem nervus accessorius na 2 podoblasti VA, VB – rozdělení oblasti V rovinou proloženou dolním okrajem chrupavky prstencové na 2 podoblasti Tab. 1. Skupiny uzlin a oblasti, které drénují. 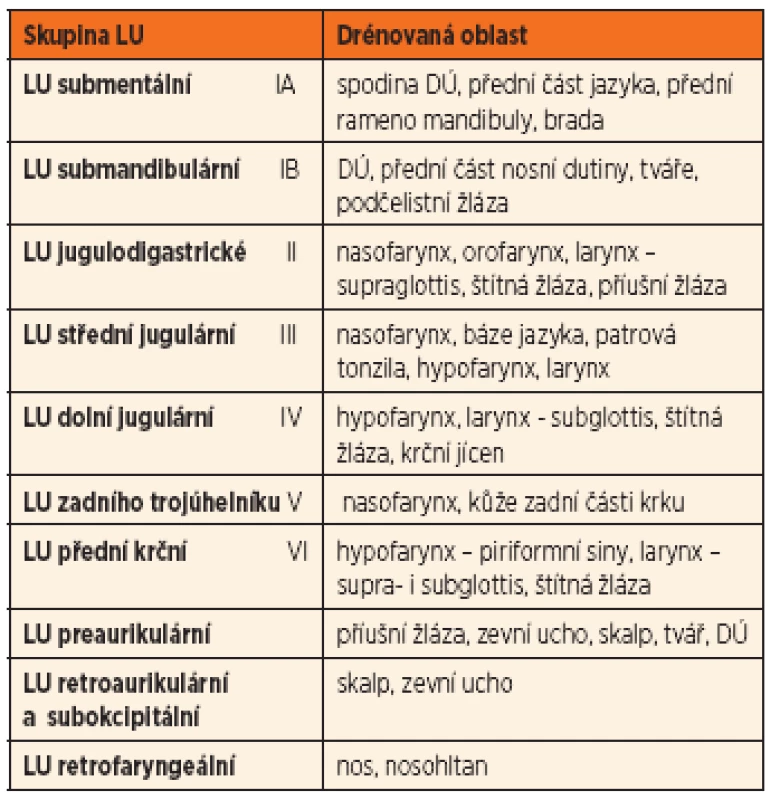
LU – lymfatická uzlina, DÚ – dutina ústní PŘÍČINY LYMFADENOPATIE
Termínem lymfadenopatie označujeme patologické zvětšení LU. Při jasné infekční příčině lymfadenopatie používáme termín lymfadenitida.
Lymfadenopatie podle doby trvání rozdělujeme na akutní (do 3 týdnů) a chronické (nad 6 týdnů), podle etiologie na infekční, zánětlivé neinfekční, nádorové [3].
Někteří autoři zdůrazňují tzv. pravidlo sedmi:
- 7 dnů trvající zduření – pravděpodobně zánětlivá etiologie,
- 7 týdnů trvající zduření – pravděpodobně nádorový proces,
- 7 roků trvající zduření – pravděpodobně vrozená vada nebo benigní léze [4].
Podle našeho názoru je uvedené pravidlo, zvláště u dětí, opravdu jen velmi orientační. Není naprosto žádnou výjimkou, že infekční příčiny mohou v dětském věku vést k lymfadenopatii, která přetrvává týdny, měsíce i roky.
Zánětlivá infekční onemocnění LU (lymfadenitidy) jsou v dětském věku jednoznačně nejčastější příčinou lymfadenopatie.
Virové infekty vyvolávají vznik akutních katarálních nebo také tzv. reaktivních lymfadenitid. Dochází k vyplavení mikroorganismů z primárního zánětlivého ložiska do lymfatických cest a jejich zanesení do spádových LU, kde jsou fagocytovány a ničeny. Hlavní charakteristikou virových infektů je generalizovaný průběh, který se klinicky projeví celkovými symptomy (teploty, únava, bolesti svalů, kloubů a mnohdy generalizovanou lymfadenopatií). Nejvýraznější potíže jsou však patrné v místě vstupu infekce, tj. v podobě kataru horních cest dýchacích (HCD) s regionální lymfadenitidou. LU jsou zvětšené bilaterálně, v různém rozsahu submandibulárně a na laterální straně krku. Pohmatově bývají elastické, bolestivé (v důsledku aktivace a edému uzliny a napnutí jejího pouzdra), volně pohyblivé, kůže nad nimi není zánětlivě změněná, není hmatná fluktuace. Katarální krční lymfadenitidu způsobují rhinoviry, adenoviry, enteroviry, viry chřipky a viry vyvolávající dětské exantémové infekce (zarděnky, spalničky) nebo příušnice. S reakcí lymfatických uzlin se často setkáváme také v průběhu herpetických infekcí – virus herpes simplex (HSV – herpes simplex virus), virus varicely a zosteru (VZV – varicella-zoster virus), lidský herpetický virus 6 (HHV6 – human herpesvirus 6), který je příčinou šesté nemoci (exanthema subitum) u kojenců a batolat. Krční lymfadenitidu charakteristicky nacházíme u infekční mononukleózy způsobené primoinfekcí virem Epsteina a Barrové (EBV – Epstein Barr virus, HHV4), ev. cytomegalovirem (CMV – cytomegalovirus, HHV5).
Bakterie fungují jako více virulentní mikroorganismy schopné po vyplavení z primárního ložiska množit se i v lymfatických cestách. V LU tak vzniká zánětlivá reakce podobná jako v původním místě infekce. Akutní bakteriální (supurativní) lymfadenitidy se vyznačují svou jednostranností, postižená je LU spádová pro mikrobem primárně napadenou oblast. Může také dojít k přestupu infekce do okolí za vzniku perilymfadenitidy. Zánět pak přechází i na ostatní uzliny za vzniku paketů. Postižená oblast je bolestivá, tuhá, postupně může dojít ke kolikvaci, pohmatově zjistitelnou jako tzv. fluktuaci (změknutí v místě nejpovrchovějšího rozpadu LU). Takto změněné LU jsou hůře pohyblivé vůči okolí, velmi bolestivé, tudíž mnohdy obtížně vyšetřitelné, kůže je zarudlá až nafialovělá, teplá, okolí uzliny edematózně prosáklé. Původcem těchto lymfadenitid jsou v naprosté většině grampozitivní bakterie Streptococcus pyogenes a Staphylococcus aureus. S lymfadenitidami způsobenými gramnegativními bakteriemi se setkáváme v daleko menší míře, příkladem jsou klíšťaty přenášené ricketsiové (Rickettsia slovaca vyvolávající klíšťovou lymfadenopatii, tzv. TIBOLA) nebo spirochetové infekce (Borrelia burgdorferi způsobující lymeskou boreliózu s nálezem erythema migrans nebo boreliovým lymfocytomem a regionální lymfadenitidou). Anaerobní bakterie rodu Fusobacterium, Prevotella nebo Bacteroides jsou nejčastějšími původci odontogenních zánětů, ran po kousnutí zvířaty atd. Mykotické infekce společně s regionální lymfadenitidou vídáme u dětí velmi zřídka, nejznámějším zástupcem je Candida albicans (orofaryn-geální kandidóza, tzv. soor novorozenců a kojenců), ev. Aspergillus niger (sinusitidy u imunokompromitovaných).
Chronické lymfadenitidy jsou charakteristické pro granulomatózní nebo granulomatózně-nekrotické záněty, vznikají při nákaze mikroorganismy se schopností přežívat v makrofázích. Ve spádové LU dochází k jejich největšímu pomnožení za vzniku tzv. granulomů. Klinicky je uzlina výrazně zvětšená, svou velikostí neodpovídá charakteru infekce v primárním ložisku. Granulomy přetrvávají několik týdnů až let, mohou podlehnout postupné resorpci ev. s následnou fibrotizací tkáně, nebo působením toxinů dojde k jejich kolikvační nebo kaseifikační nekróze. Nekrotické hmoty se mohou vyprázdnit píštělí. Tento typ je charakteristický pro felinózu neboli nemoc z kočičího škrábnutí (původcem onemocnění je Bartonella henselae, méně často B. clarridgeiae či Afipia felis) a oroglandulární,ev. okuloglandulární formu tularémie (kolikvační nekróza) [5], tuberkulózní mykobakterie (kaseifikační nekróza) a larvální toxokarózu (Toxocara cati, T. canis).
Chronické lymfadenitidy způsobuje také intracelulární prvok Toxoplasma gondii spadající do skupiny tzv. lymfotropních agens, mikroorganismů adaptovaných na parazitismus s následným postižením anatomicky nesouvisejících oblastí (LU různé lokalizace, tonzily, slezina, játra ad.). Podobnou afinitu k lymfatické tkáni má již zmíněný EBV nebo CMV.
Symptomy u granulomatózních onemocnění jsou většinou velmi nespecifické. Mohou být asymptomatické nebo s příznaky typu chřipkového onemocnění. Stejně tak nález a charakter postižených LU je nespecifický. LU mohou být solitární, různé velikosti, konzistence, lokalizace, někdy tvoří pakety, relativně často dochází ke kolikvaci. Možné odhalení umožní až sérologické vyšetření. Histologické vyšetření bioptického materiálu (LU) potvrdí granulomatózní typ zánětu, většinou bez další specifikace. Granulomatózní typy krčních lymfadenitid v dětském věku vídáme zřídka, většinou se jedná o felinózu, toxoplazmózu, ev. tularémii, méně často infekce atypickými (non-tuberkulózními) mykobakteriemi [6].
Zánětlivá neinfekční onemocnění LU tvoří velkou heterogenní skupinu chorob (tab. 2). Krční lymfadenopatie je u těchto chorob velmi často jedním z mnoha klinických příznaků, mnohdy ne tím nejvýraznějším. Diagnostika a terapie těchto onemocnění vyžaduje vždy multioborovou spolupráci. Základním krokem je vyloučení infekčních příčin a nádorového procesu.
Tab. 2. Základní přehled neinfekčních příčin lymfadenopatie. 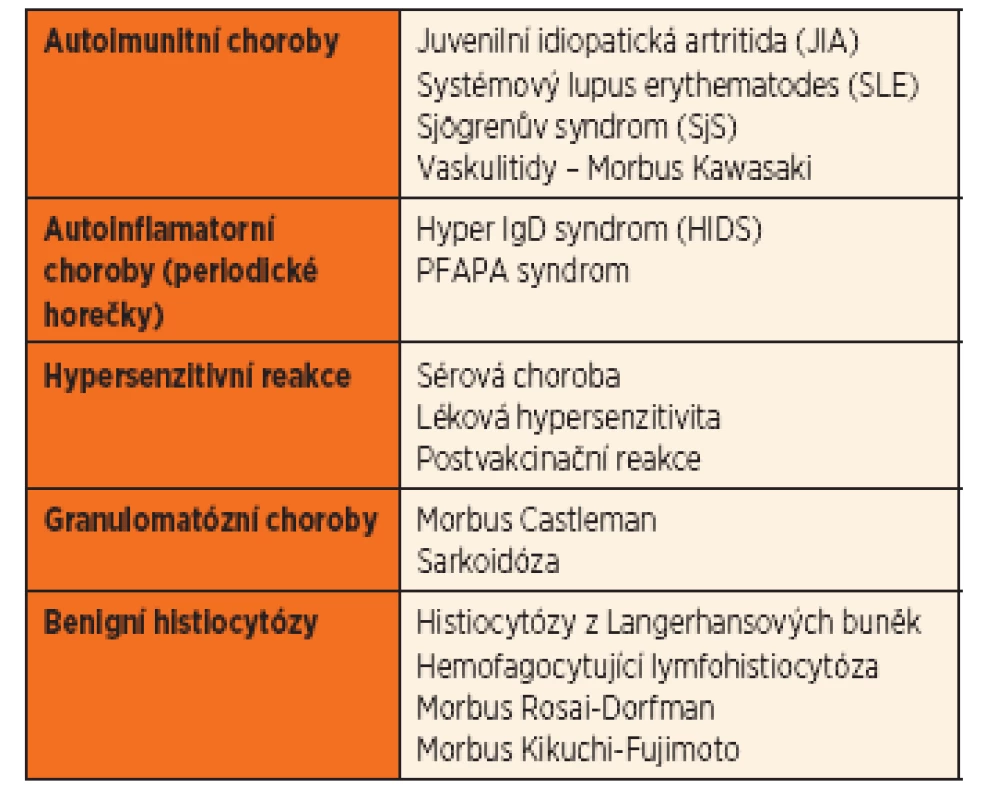
Za bližší zmínku stojí tzv. PFAPA syndrom (Periodic Fever, Aphthous stomatitis, Pharyngitis, and cervical Adenitis), idiopatické autoinflamatorní onemocnění charakterizované periodickými atakami horečky (nad 39 °C, periody průměrně 3 až 6 týdnů), aftózní stomatitidou, faryngitidou nebo tonzilitidou a cervikální lymfadenopatií, popřípadě i vedlejšími příznaky (bolest břicha, zvracení, průjmy, kožní vyrážky apod.), přičemž ne všechny příznaky musí být současně vyjádřeny [7, 8]. Laboratorní nálezy mohou být chudé, nespecifické nebo imitovat bakteriální příčinu (zvýšené zánětlivé parametry, kultivační nález) [8]. Onemocnění se manifestuje zpravidla před 5. rokem věku dítěte, spontánně vymizí kolem 10. roku, zaznamenána je predominance mužského pohlaví (55 až 71 %). Ataky bývají velmi často považovány za recidivující tonzilitidy a zbytečně opakovaně léčeny ATB. Diagnosticko-terapeutickým testem je podání Prednisonu per os v dávce 1 mg/kg, po němž následuje rychlý ústup potíží (v řádech několika hodin). Kauzální léčba zatím neexistuje, k remisi onemocnění může vést tonzilektomie, ev. včetně adenotomie. Histologické nálezy u tonzil nesou charakteristické rysy chronické tonzilitidy [7]. Mezi jednotlivými atakami je zcela asymptomatické období, onemocnění nemá vliv na růst a vývoj dítěte [9].
Nádorová onemocnění krčního uzlinového systému společně s měkkými tkáněmi krku jsou u dětí onkologicky nejfrekventovanějším úsekem v ORL oblasti (asi 70 % všech dětských ORL nádorů). Větší polovinu těchto malignit tvoří lymfomy [10].
Jako krční uzlinový syndrom se charakteristicky manifestuje Hodgkinův lymfom (HL), kdy až v 80 % případů bývá prvním příznakem většinou jednostranná krční lymfadenopatie v oblasti supraklavikulární nebo zadního krčního trojúhelníku (jedno - nebo víceložisková), postupně se zvětšující, nereagující na léčbu. Uzliny jsou nebolestivé, tuhé, konzistence gumy, mohou tvořit pakety s fixací k okolí, kůže nad nimi je nezměněna. Chybí nález zánětlivého procesu v oblasti, kterou uzliny fyziologicky drénují. Současně jsou postiženy LU v mediastinu, klinicky se projevující kašlem až dušností. Přibližně třetina nemocných má nespecifické celkové příznaky, tzv. B-symptomy: kolísající febrilie, noční pocení a ztráta hmotnosti o >10 % během 6 měsíců.
Non-Hodgkinovy lymfomy (NHL) naproti tomu časně leukemizují (meningy, CNS a jiné extranodální tkáně), jsou proto častěji diagnostikovány již v generalizované formě. Téměř u třetiny dětí se NHL onemocnění manifestuje pod obrazem život ohrožující příhody. Asi v 10 % případů je patrná krční lymfadenopatie jako jeden z příznaků onemocnění, uzliny tvoří nebolestivé pakety za kývačem nebo v nadklíčku, jejich růst je velmi rychlý.
U leukemií jsou nádorovými buňkami v různé míře prostoupeny všechny orgány, krční lymfadenopatie je u tohoto onemocnění obvykle nahodilým nálezem, ne příznakem onemocnění. V popředí je spíše únava, malátnost, nechutenství, váhový úbytek atd.
Metastázy do krčních lymfatických uzlin se projevují jako velmi tuhé, nebolestivé, málo pohyblivé nebo nepohyblivé infiltráty, mohou se vyskytovat homolaterálně i bilaterálně. V dětském věku se vyskytují výjimečně (karcinom štítné žlázy, nazofaryngeální ca, melanom, neuroblastom).
ZÁKLADY DIFERENCIÁLNÍ DIAGNOSTIKY
Pohledů na diferenciální diagnostiku krčního uzlinového syndromu je několik. V užším pojetí se zabývá pouze patologiemi v rámci lymfatického systému, v širším pak musíme rozlišit další procesy způsobující zduření na krku a imitující patologii uzlinového systému (tab. 3).
Tab. 3. Krční rezistence nelymfatického původu. 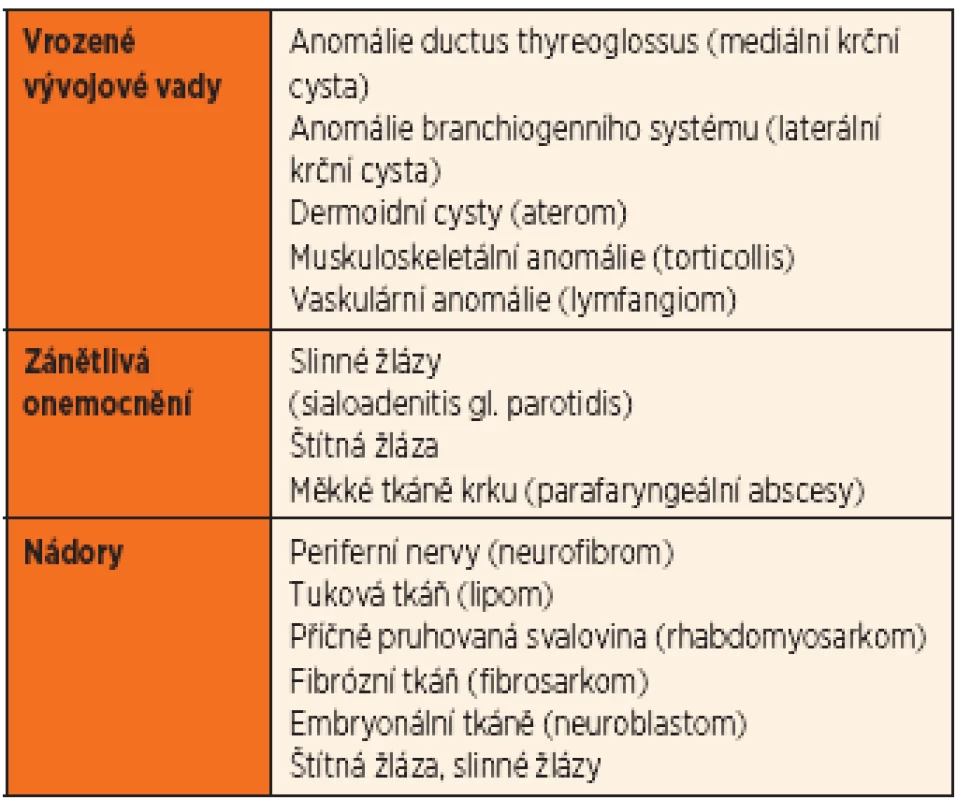
gl. – glandulae V rámci diferenciální diagnostiky z pohledu ORL lé-kaře je velmi praktické rozdělení podle lokalizace rezistence.
Ve střední čáře krku se s lymfadenitidou setkáme jen výjimečně, a to v oblasti submentální při akné, furunklech v oblasti brady, kariézní dentici, ev. při poranění, přítomnosti cizího tělesa v oblasti předního dolního vestibula nebo jazyka (piercing!!). Charakteristickou pro střední oblast krku je spíše mediální krční cysta (obr. 2) jako pozůstatek vývoje štítné žlázy (porucha při obliteraci ductus thyreoglossus). Bývá diagnostikována většinou v předškolním věku jako elastické nebo tuhé kulovité zduření v blízkosti jazylky, přibližně 1 až 2 cm v průměru, patrné nejlépe při záklonu hlavy. Relativně často dochází k zánětlivým změnám. Pacienti s thyreoglosální cystou jsou dispenzarizováni na ORL, důležitým vyšetřením je ultrazvukové vyšetření (UZ) včetně popisu štítné žlázy (v cystě může být uložena jediná funkční štítná žláza!!!). Jedinou možnou terapií je exstirpace cysty, nejlépe do 6. až 8. roku věku, v případě zánětlivých změn co nejdříve po přeléčení. Další charakteristickou strukturou pro tuto oblast je aterom (dermoidní cysta), často velmi obtížně odlišitelný od cysty mediální. Aterom bývá lokalizován kdekoliv od submentální oblasti po jugulum, výjimkou nejsou ani laterálnější oblasti krku. Diagnostikován bývá často u starších dětí, pacient je sledován na ORL, kde je provedena včasná exstirpace, nejlépe před případnými zánětlivými změnami.
Obr. 2. Mediální krční cysta (thyreoglosální). Fig. 2. Cystis ductus thyreoglossus 
Laterálně na krku rozeznáváme několik oblastí se svými specifiky. V oblasti submandibulární se nejčastěji setkáme s rezistencemi lymfatického původu v rámci infektu HCD (tab. 1), výjimkou nejsou ani odontogenní příčiny. Méně obvyklé v této oblasti jsou u dětí záněty submandibulární slinné žlázy (větší děti), lymfangiomy nebo kongenitální mucinózní cysty (kojenci), což jednoznačně rozliší UZ.
Podél předního okraje kývače v celém jeho průběhu se kromě patologií LU můžeme setkat s tzv. laterální krční cystou. Tato vrozená vývojová vada je pozůstatkem embryonálního branchiogenního systému. Častěji je diagnostikována v období adolescence jako jednostranná, solitární, elastická rezistence oválného tvaru při předním okraji musculus sternocleidomastoideus (m. scm.), při zánětlivých změnách na UZ někdy velmi špatně odlišitelná od abscedované LU. Dispenzarizace a terapie spadá do rukou ORL lékaře. Cystu exstirpujeme in toto, často s nutností odstranit vazivový pruh táhnoucí se k tonzilárnímu lůžku (v tomto případě doplňujeme jednostrannou tonzilektomii). Další možnou patologií v této oblasti je kongenitální tortikolis, zde diagnostika většinou nečiní potíže: velmi tuhá rezistence hmatatelná přímo v průběhu kývače u novorozence nebo malého kojence s hlavou natočenou na stranu nepostiženou v důsledku kontrakce svalu. Ultrazvuk diagnózu potvrdí téměř se 100% jistotou. Dalším charakteristickým nálezem u kojenců v této oblasti je lymfangiom (ev. lymfangiohemangiom). Pohmatově se jedná o měkký, fluktuující nebolestivý útvar, někdy modravě prosvítající, často lze skutečně rozpoznat přelévající se obsah při palpaci. Lymfangiomy (obr. 3) se vyznačují nepředvídatelným růstem, mohou svou velikostí způsobovat útlak okolních struktur, často jsou anatomicky úzce spojeny s hlavními neurovaskulárními strukturami hlavy a krku. Terapie je obtížnou, multioborovou záležitostí, exstirpaci in toto velmi často nelze provést vzhledem ke členitosti útvaru. Slibnou alternativou chirurgického zákroku se v posledních několika letech ukázala být perkutánní skleroterapie lymfatických malformací (nejlepší výsledky jsou dosaženy za použití doxycyklinu, ev. sklerotizační látky OK432) [11, 12, 13].
Obr. 3. Lymfangiom krku (cystis hygroma). Fig. 3. Lymphangioma colli (cystis hygroma). 
LU oblasti zadního krčního trojúhelníku sbírají lymfu z nosohltanu (zduření např. při katarech HCD, při zánětlivých komplikacích po adenotomii…) a kůže zadní části krku, ev. vlasaté části hlavy (furunkly, poranění, vši…). Výskyt lymfadenopatie v této oblasti vždy musí vést k myšlence možného výskytu lymfomu, stejně tak jako v oblasti supraklavikulární. Často jsou v těchto oblastech zvětšené LU při granulomatózních zánětech, supraklavikulárně v blízkosti jugula může být nalezen aterom.
DIAGNOSTICKÝ POSTUP
V optimálním případě je vstupní, primární vyšetření provedeno dětským lékařem.
Praktický lékař (PLDD) by měl provést:
- odběr anamnézy,
- fyzikální vyšetření.
A dále podle charakteru potíží:
- základní zobrazovací vyšetření,
- základní laboratorní vyšetření.
Na základě výsledků je ve většině případů schopen určit diagnózu a stanovit odpovídající terapeutický postup. V případě nejasných nálezů, potížích s interpretací výsledků, případů nereagujících na běžné terapeutické postupy nebo progredujících při zavedené léčbě, odesílá PLDD pacienta na specializovaná pracoviště (tab. 4).
Tab. 4. Přehled indikací k odeslání pacienta na specializované pracoviště. 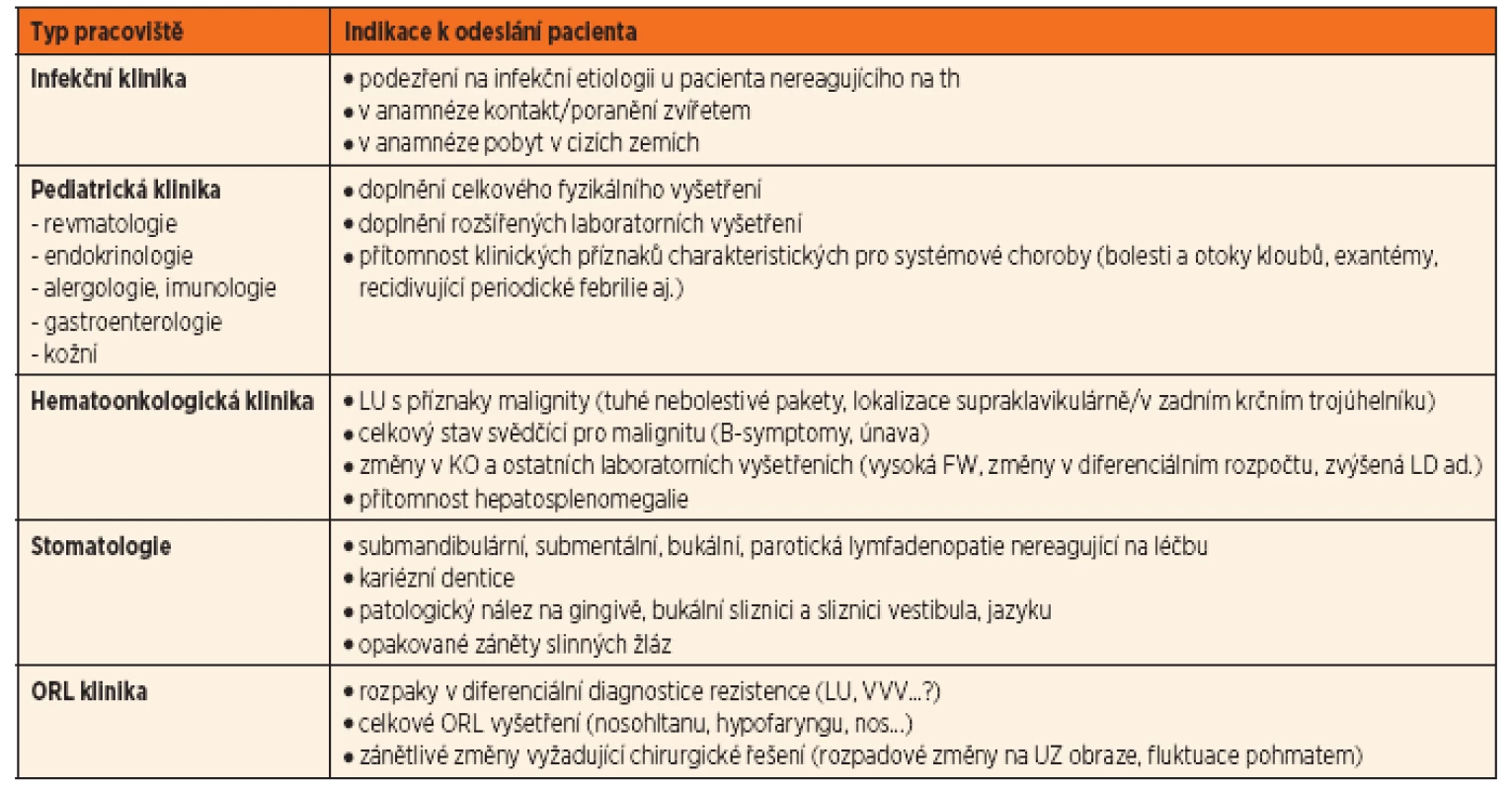
th – terapie, KO – krevní obraz, FW – sedimentace, LD – laktátdehydrogenáza, LU – lymfatická uzlina, VVV – vrozená vývojová vada, ORL – otorinolaryngologie Anamnéza je prvním krokem vyšetřovacího postupu. Podrobný anamnestický rozbor může zamezit rozsáhlému a někdy zbytečnému algoritmu vyšetření a časovému prodlení adekvátní léčby.
V rámci nynějšího onemocnění zjišťujeme dobu počátku příznaků, jejich trvání, měnlivost, charakter obtíží, spontánní a palpační bolestivost. Zda nález provázejí celkové příznaky či lokální změny ve sběrné oblasti uzliny (tonzilitida, pyodermie kůže včetně kštice, poranění kůže při kontaktu se zvířetem).
Věk pacienta není pro konečnou diagnózu rozhodující. Obecně lze však říci, že u dětí předškolního a mladšího školního věku je častější benigní zvětšení lymfatické tkáně, nejčastěji na podkladu opakovaných respiračních infektů. Největší uzliny lze pozorovat ve věku 4 až 8 let, jejich involuce začíná v adolescenci.
Zjišťujeme, jaké onemocnění prodělalo dítě v minulosti (opakované infekty HCD, opakované tonzilitidy, kariézní dentice atd.), zda je sledované na nějakém specializovaném pracovišti. Zaznamenáme také podstoupené operace (adenotomie, tonzilektomie aj.) nebo úrazy (především v oblasti hlavy a krku). U adolescentů pátráme po rizikovém životním stylu (sexuální anamnéza, abúzus drog apod.).
Epidemiologicky jsou významné údaje o přisátí klíštěte, výskytu vší v kolektivu a manipulaci se zvířaty, event. požívání syrového masa a mléčných výrobků. Cenný údaj je též o kontaktu s osobou postiženou infekčním onemocněním. Ptáme se na cestování (klinický obraz importovaných infekcí může být v našich podmínkách neobvyklý) a prodělaná očkování, sociální situaci. Důležitý je také údaj o současném nebo předchozím podání léčivých přípravků a o existujících alergiích.
Při fyzikálním vyšetření začínáme pohledem, všímáme si držení hlavy, lokalizace a velikosti rezistence, charakteru kůže. Lokalizace zduření může při diagnostice částečně napomoci. Akutní bilaterální lymfadenitida je většinou způsobena virovým zánětem HCD, akutní jednostranné postižení krčních LU velmi často způsobují streptokokové nebo stafylokokové infekce.
Palpací posuzujeme tvar, charakter povrchu, mobilitu, konzistenci, tuhost a bolestivost rezistence. Palpační nález u uzlin s akutní infekcí je charakteristický. Uzliny bývají elastické, pohmatově citlivé, často s periglandulárním edémem. Výrazně zvětšená uzlina způsobuje vyklenutí kůže, která je u hnisavých zánětů zarudlá, teplá. Chronicky změněné uzliny nebývají tolik výrazné jako u akutních zánětů. Maligně infiltrované LU jsou většinou nebolestivé, tužší konzistence, někdy nehomogenní, asymetricky zvětšené, bez edému okolních struktur, mohou být fixovány k okolí, beze změny kožního krytu.
Součástí klinického vyšetření je palpace uzlin ve všech dostupných lokalizacích hlavy, krku, trupu. Všímáme si také výrazu dítěte (otevřená ústa při dýchání), hlasu (huhňavost), zhoršeného polykání, zvýšeného slinění, ale také patologií mimo oblast ORL, např. typické exantémy (dětská infekční onemocnění, Kawasakiho syndrom, polékové lymfadenitidy, systémová onemocnění), hepatosplenomegalie (primoinfekce EBV, CMV, toxoplazmóza, lymfoproliferativní onemocnění, systémová onemocnění pojiva), kloubní projevy (rubeola, polékové lymfadenitidy). Některé choroby mají své specifické projevy, jako Lischovy noduly na rohovce, axilární freckling u neurofibromatózy I. typu, konjunktivitidu, změny sliznic rtů a dutiny ústní, palmární a plantární erytém a exantém u Kawasakiho choroby aj. Z tohoto důvodu je více než vhodné provést vstupní a prvotní vyšetření u praktického lékaře.
Za použití ústní lopatky nejprve přehlédneme oblast orofaryngu. Všímáme si změn na zadní stěně (granulace, zduření postranních lymfatických provazců, zatékání patologického sekretu z nosohltanu, vyklenutí), na tonzilách (velikost, asymetrie, charakter tkáně, patologický obsah nebo přítomnost povlaků, fixace k lůžku), na patrových obloucích (zánětlivé změny, asymetrie, tuhost či vyklenutí). Při otevřených ústech sledujeme také event. přítomnost trismu, který se vyskytuje u patologických pochodů v peritonzilárním prostoru. Dále vyšetříme sliznice tváří, vývody velkých slinných žláz, charakter dentice a vestibulum. Všímáme si možné přítomnosti cizích těles, poranění, aftů nebo slizničních ulcerací (poranění při kousání, útlak sliznic při erupci zadních molárů), petechií na měkkém patře (Holzelovo znamení) u infekční mononukleózy, Koplikových skvrn (tečkovité, bělavé skvrnky na zarudlém okolí v oblasti bukální sliznice, tzv. „rozsypaná sůl“) u spalniček aj.
V případě nespolupráce dítěte, nejasného nálezu nebo nutnosti došetření ostatních oblastí dýchacích a polykacích cest odesílá pediatr pacienta k ORL specialistovi (otoskopie, vyšetření nosních dutin, nosohltanu, hypofaryngu).
Základní laboratorní vyšetření může provést PLDD ambulantně. Rozsah volí individuálně podle povahy onemocnění a potíží pacienta. Cílem je získat další informace v rámci diferenciální diagnostiky lymfadenopatie.
Ve většině případů lze ambulantně velmi rychle zjistit hodnotu CRP, FW k vyloučení nebo potvrzení bakteriální etiologie onemocnění. V případě potřeby je možné doplnit vyšetření hematologické (krevní obraz s diferenciálním rozpočtem leukocytů) a biochemické, nejčastěji jaterní testy (celkový bilirubin, ALT, AST, GMT, ALP, LD, albumin), dále ev. ionty, ferritin, kyselinu močovou, glukózu.
Při kultivačním vyšetření odesíláme vzorky stěrů ze sliznic dutiny ústní a nosní. Vzorek by měl být co nejrychleji zpracován, doporučuje se do 2 hod při skladování v pokojové teplotě, do 24 hod při skladování v chladu. Předběžné výsledky kultivace je možno získat u aerobů již za 24 hod (citlivost bakterie na antibiotika za 48 hod), u anaerobů za 48 hod.
Sérologické vyšetření je indikováno v některých případech ihned při vstupním vyšetření pacienta, většinou při podezření na infekční mononukleózu, nebo pokud je v anamnéze uveden kontakt a poranění zvířetem. V běžné praxi do základních sérologických odběrů u dětí spadá EBV, CMV, felinóza, toxoplazmóza, tularémie, toxokaróza. Vyšetření může provést PLDD nebo podle svého uvážení odeslat pacienta na nejbližší specializované pracoviště. Základní spektrum lze samozřejmě rozšířit o další odběry podle charakteru postižených uzlin a vývoje onemocnění (mykobakterie, chlamydie, mykoplazmata, yersinie, salmonely aj.). Problémem u sérologických vyšetření bývá pozdní interpretace výsledků, navíc sérologie bývají v době nasazení léčby často negativní, protože protilátky jsou ve většině případů detekovatelné až ve 3.–4. týdnu onemocnění. Dalším úskalím je interpretace pozitivních sérologických výsledků vlivem polyklonální tvorby protilátek při akutní EBV infekci.
Základní zobrazovací metodou v diagnostickém algoritmu rezistencí na krku je sonografické vyšetření. UZ umožní vyhodnotit počet a velikost lymfatických uzlin, jejich lokalizaci, strukturu, ohraničení, krevní zásobení a prokrvení parenchymu uzliny, známky kolikvace a vztah k okolním strukturám. Při popisu velikosti a tvaru lymfatické uzliny se hodnotí tzv. LT index (poměr longitudinální/transverzální délky, někdy též označován jako L/S, čili délka/šířka, tab. 5). Ve většině případů odliší lymfatický původ rezistence na krku od jiných možných příčin (cysty, hemangiomy, lymfangiomy aj.). Velkou výhodou UZ je možnost častého opakování vyšetření, které je mnohdy potřebné pro sledování vývoje krční patologie.
Tab. 5. Základní popis UZ obrazu u jednotlivých typů lymfadenopatií. 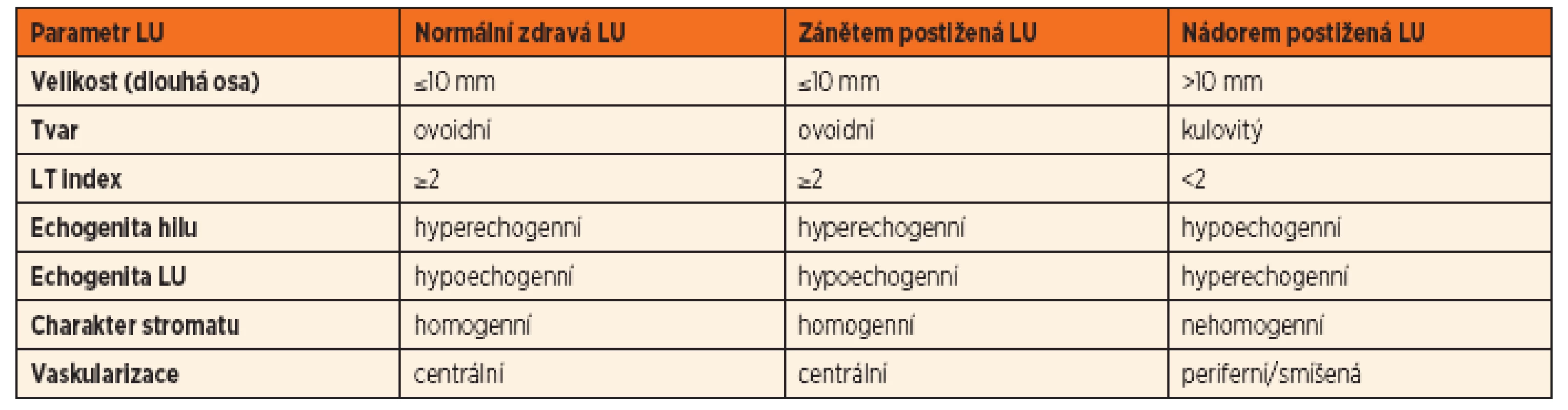
LU – lymfatická uzlina, LT index – poměr longitudinální a transverzální délky LU, hyperechogenní – na UZ světlejší, hypoechogenní – na UZ tmavší Další zobrazovací metody, počítačová tomografie (CT) a magnetická rezonance (MRI), jsou využívány v podstatně menší míře, při diagnostických rozpacích, ke zjištění rozsahu onemocnění atd., a to na specializovaných pracovištích.
TERAPEUTICKÝ POSTUP
Terapie KUS se odvíjí od základní příčiny onemocnění a klinických příznaků. Většina lymfadenopatií v dětském věku je virového původu a vzniká jako reakce lymfatické tkáně na probíhající katar HCD. V těchto případech postačí symptomatická terapie, ev. lokální ve formě alkoholových obkladů aplikovaných několikrát denně na oblast postižených LU. Ke spontánní regresi lymfadenitidy dochází většinou v rozmezí 2 až 4 týdnů.
Terapie bakteriálních lymfadenitid bez známého původce infekce by měla zajistit pokrytí obou nejčastějších, tj. S. aureus a S. pyogenes.
Protistafylokokovým antibiotikem první volby je oxacilin, odolný proti β-laktamázám stafylokoků. S. aureus je dále běžně citlivý na klindamycin, cefuroxim, gentamicin, ev. ciprofloxacin. Volba správného preparátu je však obtížná vzhledem k nedostupnosti léků v perorální formě (oxacilin a gentamicin jsou momentálně dostupné pouze ve formě injekční), nežádoucím účinkům, jež jsou kontraindikací pro podávání menším dětem (rozvoj pseudomembranózní kolitidy u ciprofloxacinu, klindamycinu) nebo nevhodné aplikační formě (velké tablety u klindamycinu). U stafylokoků citlivých na oxacilin by mohlo být alternativou použití širokospektrých aminopenicilinů (ampicilin, amoxicilin) v kombinaci s inhibitorem β-laktamáz. Podání těchto preparátů u krčního uzlinového syndromu je však kontraindikováno před vyloučením infekční mononukleózy. V praxi nejčastěji používáme linkosamidy (uváděné nežádoucí účinky jsme nezaznamenali), u menších dětí, které nespolknou tablety, pak cefalosporiny II. generace, potencované aminopeniciliny, méně často makrolidy.
S. pyogenes je charakteristicky citlivý na penicilin, který je zároveň lékem první volby, dále cefazolin (cefalosporin I. generace – nyní dostupný pouze v tabletách ve vyšších gramážích), ev. erytromycin, klindamycin. Při alergiích na penicilin proto volíme nejčastěji linkosamidy, makrolidy výjimečně.
Antimikrobiální terapii lze upravit v případě zjištění původce onemocnění (stěr ze sliznic, z rány) a jeho citlivosti na ATB, samozřejmě v závislosti na klinické odpovědi na stávající léčbu. Relativně častým problémem u dětských pacientů je jejich nesnášenlivost některých lékových forem, ať už ve formě nežádoucích účinků (nauzea, průjmy, zvracení aj.) nebo odmítání daného preparátu (velké tablety…). Pokud má lékař pochyby o výběru vhodného ATB, je možné se s dotazem obrátit na antibiotické středisko nebo infekční kliniku.
Účinek terapie antibiotiky by měl být zaznamenán do 48 až 72 hod od podání první dávky. Pokud se stav pacienta po uplynutí uvedené doby nelepší nebo dojde ke zhoršení klinického nebo laboratorního nálezu, je vhodné dítě odeslat na specializované pracoviště.
Úloha ORL lékaře v algoritmu diagnostiky a terapie KUS by měla být především „terapeutická invazivní“ (schéma 1). Jeho úkolem je zvážit, zda a kdy provést chirurgické ošetření LU a to buď formou punkce, ev. incize zkolikvované LU nebo biopsie patologicky změněné LU za účelem histologické verifikace. Tyto výkony mohou být ve své podstatě chápány jako diagnosticko-terapeutický postup.
Schéma 1. Diagnostický algoritmus u krčního uzlinového syndromu 
Punkce s následnou incizí a drénováním obsahu postižené LU indikujeme při známkách kolikvace. Sonografické vyšetření je schopné odhalit i malé, počínající okrsky rozpadových změn v LU, s výkonem však vyčkáváme až do doby jednoznačně palpovatelné fluktuace (čekáme, až uzlina tzv. uzraje). Punkci a incizi LU lze provést ambulantně v lokální anestezii, limitací je věk, spolupráce pacienta a umístění zánětlivého ložiska. Celkovou anestezii volíme u menších, hůře spolupracujících dětí a u uzlin uložených v hloubce, kde fluktuaci nelze spolehlivě nahmatat (lze provést pod sonografickou kontrolou). Punktujeme silnější jehlou v místě nejvýraznější fluktuace, v případě incize je nejvýhodnější vést čepel skalpelu podél zavedené jehly. Do rány zavádíme rukavicový nebo trubicový drén, který odstraňujeme za 2 až 4 dny. Aspirovaný materiál odesíláme na kultivační vyšetření.
Biopsie LU, čili exstirpace patologicky změněné LU, je v dětském věku stále považována za zlatý standard (základní indikace k odběru patologicky změněné LU jsou uvedeny v tab. 6).
Tab. 6. Základní indikace k biopsii lymfatických uzlin při krční lymdadenopatii. 
LU – lymfatická uzlina, FW – sedimentace erytrocytů, Hb – hemoglobin Exstirpovaná LU je dále zpracována histopatologem, při podezření na malignitu je kontaktován onkologický tým a materiál odevzdán přímo tzv. zákrokovým sestrám onkologické kliniky a podroben celé řadě speciálních vyšetření. Z tohoto důvodu by měl být pacient odeslán do specializovaného centra dětské onkologie, které je schopno všechna tato vyšetření zajistit.
ZÁVĚR
Krční lymfadenopatie je v ordinaci dětského lékaře běžnou diagnózou. Ve většině případů se jedná o reakci lymfatického systému na virovou nebo bakteriální infekci probíhající v oblasti horních cest dýchacích.
Ke stanovení diagnózy je obvykle dostačující správně odebraná anamnéza a pečlivé fyzikální vyšetření. Onemocnění většinou nevyžaduje specifickou terapii, symptomatická léčba bývá plně dostačující. Při podezření na bakteriální infekci volíme v první řadě antibiotické preparáty s prokázanou účinností proti S. pyogenes a S. aureus.
Kontrolní vyšetření, přinejmenším v počátcích léčby, jsou nutná ke sledování vývoje lymfadenopatie. Průměrná doba sledování pacienta s reaktivní lymfadenitidou je 2 až 4 týdny.
Nekomplikované formy lymfadenopatií by měl být schopen vyřešit dětský praktický lékař ve své ambulanci, tj. stanovit diagnózu a adekvátní terapii, podle potřeby zajistit základní laboratorní a sonografické vyšetření. Na specializovaná pracoviště odesílá ty případy, které nereagují na zvolenou léčbu, nebo když i během ní dochází k progresi příznaků (schéma 1).
Podpora FN Brno, podpořeno MZ ČR – RVO (FNB, 65269705).
Došlo: 2. 12. 2014
Přijato: 8. 1. 2015
MUDr. Kateřina Sobotková
Klinika dětské otorinolaryngologie FN
Černopolní 9
613 00 Brno
e-mail: k.sobotkova@email.cz
Zdroje
1. Ferlito A. Classification of neck dissections: An evolving system. Auris Nasus Larynx 2009; 36 (2): 127–134.
2. Čelakovský P, Plzák J, Betka J, et al. Krční metastázy. Anatomie krku ve vztahu k blokovým krčním disekcím. 1. vyd. Havlíčkův Brod: Tobiáš, 2012 : 18–37.
3. Vyhnánková L. Diferenciální diagnostika krčních lymfadenitid u dětí. Pediatr pro Praxi 2009; 10 (6): 361–363.
4. Čelakovský P, Plzák J, Betka J, et al. Krční metastázy. Klinické vyšetření při podezření na nádorové postižení krčních uzlin. 1. vyd. Havlíčkův Brod: Tobiáš, 2012 : 58.
5. Hozáková L, Rožnovský L, Bílková Fránková H. Felinóza – stále aktuální zoonóza. Klin Mikrobiol Inf Lék 2014; 20 (1): 4–10.
6. Carvalho A, Codecasa L, Pinsi G, et al. Differential diagnosis of cervical mycobacterial lymphadenitis in children. Pediatr Infect Dis J 2010; 29 (7): 629–633.
7. Peridis S, Koudoumnakis E, Theodoridis A, et al. Surgical outcomes and histology findings after tonsillectomy in children with periodic fever, aphthous stomatitis, pharyngitis, and cervical adenitis syndrome. Am J Otolaryngol 2010; 31 : 472–475.
8. Valenzuela PM, Araya A, Pérez CI, et al. Profile of inflammatory mediators in tonsils of patients with periodic fever, aphthous stomatitis, pharyngitis, and cervical adenitis (PFAPA) syndrome. Clin Rheumatol 2013; 32 : 1743–1749.
9. Galanakis E, Papadakis CE, Giannoussi E, et al. PFAPA syndrome in children evaluated for tonsillectomy. Arch Dis Child 2002; 86 : 434–435.
10. Roh JL, Huh J, Moon HN. Lymphomas of the head and neck in the pediatric population. Int J Pediatr Otorhinolaryngol 2007; 71 : 1471–1477.
11. Jamal N, Ahmed S, Miller T, et al. Doxycycline sclerotherapy for pediatric head and neck macrocystic lymphatic malformations: A case series and rewiev of the literature. Int J Pediatr Otorhinolaryngol 2012; 76 : 1127–1131.
12. Burrows PE, Mitri RK, Alomari A, et al. Percutaneous sclerotherapy of lymphatic malformations with doxycycline. Lymphat Res Biol 2008; 6 (3–4): 209–216.
13. Motz KM, Nickley KB, Bedwell JR, et al. OK432 versus doxycycline for treatment of macrocystic lymphatic malformations. Ann Otol Rhinol Laryngol 2014; 123 (2): 81–88.
Štítky
Neonatologie Pediatrie Praktické lékařství pro děti a dorost
Článek vyšel v časopiseČesko-slovenská pediatrie
Nejčtenější tento týden
2015 Číslo 3- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
- Syndrom Noonanové: etiologie, diagnostika a terapie
-
Všechny články tohoto čísla
- Přínos sonografického vyšetření v diagnostice akutní apendicitidy
- Segmentální dilatace střeva – prezentace souboru novorozenců se segmentální dilatací tenkého střeva a přehled literatury
- Primárny imunodeficit v praxi pediatrického pneumológa
- Lehká mentální retardace v ambulanci dětského lékaře – poznáte ji?
- Pozdní záchyt syndromu kaudální regrese u dítěte s extrémně nízkou porodní hmotností
- Preventivní vyšetření sportovců se zaměřením na klidové EKG
- Krční uzlinový syndrom z pohledu otorinolaryngologa
- Současné možnosti terapie juvenilní recidivující respirační papilomatózy
- Jednofotonová emisní tomografie při diagnostice lingvální ektopie štítné žlázy. Užití u novorozence s kongenitální hypotyreózou
- Diferenciální diagnostika proteinurie
- Diferenciální diagnostika hematurie
- Cushingův syndrom v dětském věku
- Česko-slovenská pediatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Krční uzlinový syndrom z pohledu otorinolaryngologa
- Diferenciální diagnostika proteinurie
- Diferenciální diagnostika hematurie
- Lehká mentální retardace v ambulanci dětského lékaře – poznáte ji?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



