-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Možnosti intervenční radiologie při léčbě nádorů ledvin
Possibilities of interventional radiology for treatment of renal tumors
Aim:
Th is article presentats the potential uses of interventional radiology in the treatment of renal tumors. It provides a review of indications and the outcomes of specifi c interventions in a single department.Methods:
From October 2008 to October 2011 7 patients with kidney cancer underwent renal artery embolization at the University Hospital Pilsen. The group included 1 man (14%) and 6 women (86%) at the average age of 52.6 ± 15.6 years (range 19–66).Results:
In one case, the total embolization was performed in a patient with inoperable kidney tumor. In 4 cases embolization was used to treat complications following resection (in one case following laparoscopic resection and in 3 cases following translumbal resection). In 2 cases embolization of angiomyolipoma was performed. In all cases, the embolization resulted in good clinical eff ect and no serious complications appeared.Conclusion:
Embolization is utilized for palliative treatment of inoperable tumors, in coping with complications following resection and for embolization of angiomyolipomas. Preoperative superselective embolization before laparoscopic resection has not been used. Embolization interventions are highly eff ective with good effi ciency and low risk of complications. Patients have benefi ted from the low invasivenness of this procedure. Th ese interventions require appropriate technical equipment and experienced staff , therefore concentration in large centers is necessary. Interdisciplinary cooperation between urologist and interventional radiologist is essential.Key words:
embolization, renal artery, kidney cancer, resection of the kidney, angiomyolipoma.
Autoři: Petr Stránský 1; Zdeněk Chudáček 2; Václav Havel 2; Viktor Eret 1; Jiří Klečka 1; Tomáš Ürge 1; Milan Hora 1
Působiště autorů: Urologická klinika LF UK a FN Plzeň 1; Radiodiagnostické oddělení FN Plzeň 2
Vyšlo v časopise: Ces Urol 2012; 16(1): 50-57
Kategorie: Původní práce
Souhrn
Cíl:
Cílem článku je prezentovat možnosti intervenční radiologie při léčbě nádorů ledvin. Seznamuje s indikacemi a výsledky výkonů jednoho pracoviště.Metoda:
V období od října 2008 do října 2011 bylo ve FN Plzeň v souvislosti s nádory ledvin ošetřeno embolizací renální tepny sedm pacientů. Jednalo se o jednoho muže (14 %) a šest žen (86 %), průměrný věk v době výkonu 52,6 ±15,6 let (rozmezí 19–66 let).Výsledky:
V jednom případě byla provedena embolizace u pacientky s inoperabilním tumorem ledviny. Ve čtyřech případech šlo o řešení komplikací po resekci (v jednom případě po laparoskopické resekci a ve třech případech po translumbální resekci). U dvou pacientů byla provedena embolizace angiomyolipomu. Ve všech případech měla embolizace dobrý klinický efekt a nebyly závažnější komplikace.Závěr:
Embolizaci využíváme k paliativní léčbě inoperabilních tumorů, k řešení komplikací po resekcích, k embolizaci angiomyolipomů. Předoperační superselektivní embolizaci před laparoskopickou resekcí jsme nepoužili. Embolizační výkony jsou velice efektivní, s dobrou účinností a mají nízké riziko komplikací. Pacient profi tuje z miniinvazivity zákroku. Tyto výkony vyžadují odpovídající technické vybavení a zkušený personál, je nutná koncentrace těchto výkonů do větších center. Velice důležitá je mezioborová spolupráce urolog – intervenční radiolog.Klíčová slova:
embolizace, ledvinná tepna, nádor ledviny, resekce ledviny, angiomyolipom.ÚVOD
Zobrazení renální arterie u člověka bylo poprvé prezentováno využitím techniky translumbální aortografie již v roce 1929 (1). Výrazné vylepšení renální arteriografie zavedl do praxe Seldinger vývojem metody perkutánní transfemorální arteriální katetrizace (2). Metodika se dále rozvíjela především dalším vývojem méně toxických kontrastních látek. V minulosti se selektivní renální arteriografie používala v diagnostice hlavně chirurgických onemocnění ledvin – nádorů, cyst, traumat a lézí renální tepny.
Význam renální arteriografie v diagnostice nádorů ledvin postupně klesal s vývojem neinvazivních zobrazovacích metod, hlavně CT a nově i MRI angiografie (3, 4). Dnes již nemá DSA (digitální subtrakční angiografie) význam v diagnostice onemocnění ledvin, nezastupitelnou roli má však dodnes v léčbě řady onemocnění.
V článku jsme chtěli ukázat na možnosti intervenční radiologie při léčbě nádorů ledvin, seznámit s touto ne příliš častou problematikou a prezentovat výsledky jednoho klinického pracoviště. Nejedná se o čistě urologickou problematiku, urolog se podílí ve většině případů pouze na indikaci výkonu, který provádí zkušený intervenční radiolog. Velice důležitá je tedy mezioborová spolupráce.
MATERIÁL A METODA
V období od října 2008 do října 2011 bylo na Radiodiagnostickém oddělení FN Plzeň ošetřeno embolizací renální tepny sedm pacientů, kteří byli hospitalizováni na Urologické klinice FN Plzeň. Jednalo se o jednoho muže (14 %) a šest žen (86 %), průměrný věk v době výkonu 52,6 ± 15,6 let (rozmezí 19–66 let).
Technické aspekty embolizace
Před vlastním zákrokem je doporučovaná ATB profylaxe širokospektrým antibiotikem v jedné nebo dvou dávkách. Používá se lokální anestezie před vpichem do femorální tepny, někdy i v kombinaci s analgosedací, někteří autoři doporučují zákrok v celkové anestezii (5). Celková anestezie je nutná u dětí. Cévní přístup je veden nejčastěji přes ipsilaterální (méně kontralaterální) společnou femorální arterii. Pokud jsou femorální arterie uzavřené, je možné použít přístup přes axilární nebo brachiální arterii. Následně je zavedeno 5 Fr zaváděcí pouzdro (sheath). Větší průměr pouzdra je někdy nutný pro některé složitější postupy – například použití balonkových katétrů. Balonkové katétry se někdy používají při ochraně druhé renální tepny balonem, který zabrání zpětné embolizaci do druhé renální tepny.
V první fázi výkonu se provádí přehledná diagnostická angiografi e abdominální aorty a selektivní nástřik renální tepny k posouzení cévního zásobení postižené ledviny. Následuje selektivní zavedení katétru a aplikace embolizačního materiálu.
Zvláště u rozsáhlých tumorů ledvin je nutné provést arteriografii i jiného povodí, které může souviset s ledvinou a ozřejmí nám eventuální cévní zkraty (např. rozsáhlé tumory ledvin prorůstající do jater). Při embolizaci se nejdříve embolizují drobné cévy, poté postupně cévy většího průměru.
Po výkonu je důležité hodnocení stavu pacienta. Možné jsou komplikace plynoucí z úniku embolizačních částic do plic, mozku, dolních končetin, které se projeví různým stupněm dechové nedostatečnosti, centrální mozkovou příhodou, bolestmi dolních končetin. Pokud je výkon prováděn správně, nemělo by ale k embolizaci necílové oblasti docházet. Použitá technika a embolizační materiál závisejí na zkušenostech a zvyklostech pracoviště.
Embolizační agens
Volba typu embolizačního materiálu závisí na cévní anatomii, hemodynamice a druhu patologického procesu. Používají se kovové spirály, embolizační částice nebo kapalné sklerotizační látky.
Kovové spirály mohou být složeny z nerezové oceli, platiny nebo nitinolu, některé obsahují syntetická vlákna pro podporu agregace trombocytů. Na našem pracovišti používáme hlavně mikroembolizační spirály Tornado®, Cook Medical, což jsou speciální měkké platinové spirálky se syntetickými vlákny.
Embolizační částice mohou být biologicky rozložitelné (Gelfoam®) nebo nerozložitelné – např. polyvinylalkohol (PVA). Biodegradabilní látky jsou vhodné například k minimalizaci ztrát krve před následnou laparoskopickou resekcí ledviny. Embolizační efekt těchto látek trvá většinou 2–3 týdny. Mezi nejčastěji používané embolizační částice na našem pracovišti patří polyvinylalkoholová pěna s různou velikostí embolizačních partikulí – preparát PVA Foam, Cook Medical nebo preparát Embosphere®, BioSphere Medical, což jsou biokompatibilní, hydrofilní, neresorbovatelné a kalibrované mikrokuličky z akrylpolymeru impregnované želatinou. Opět dostupné v různých velikostech a koncentracích.
Kapalné sklerotizační látky zahrnují N-butyl-2-cyanoakrylátové lepidlo, 98–99% etanol, ethibloc, akrylát nebo lipiodol (6, 7). Na našem pracovišti používáme například preparát Histoacryl®, B. Braun Medical v kombinaci s emulzí olejové kontrastní látky Lipiodol Ultra-Fluide®, Guerbet. Obrázek 1 zobrazuje některé typy embolizačního materiálu.
Obr. 1. Embolizační agens – nahoře Embosphere<sup>®</sup>, uprostřed Histoacryl<sup>®</sup> a preparát PVA Foam, dole mikroembolizační spirála Tornado<sup>®</sup> s detailem spirály v levém dolním rohu Fig. 1. Embolization agents – at the top Embosphere<sup>®</sup>, in the middle Histoacryl<sup>®</sup> and PVA Foam, at the bottom Tornado <sup>®</sup> embolization microcoil with the detail of the coil in the bottom left corner 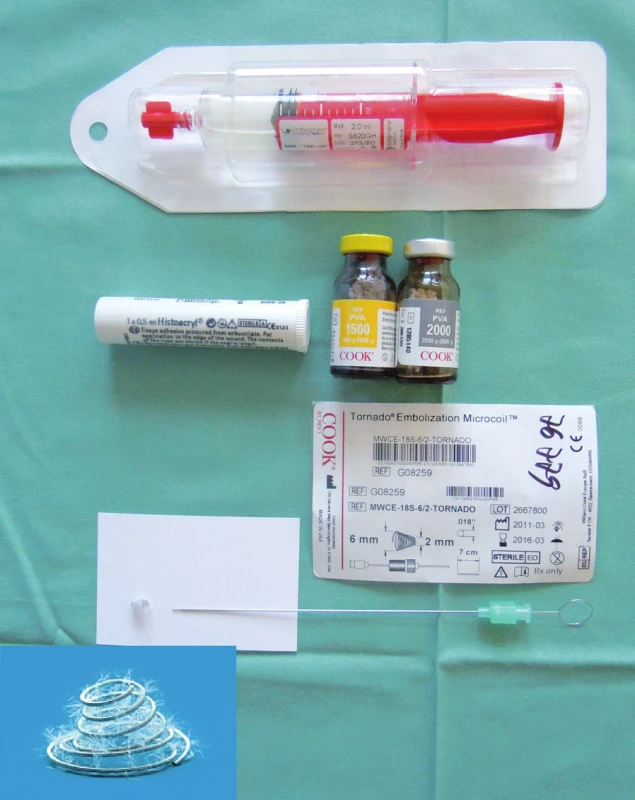
Selektivní a superselektivní embolizace
Cílem selektivní embolizace je odstranit část cévního zásobení ledviny s cílem minimalizovat funkční poškození ledviny. Selektivní embolizace je provedena selektivní katetrizací větví renální tepny. Superselektivní embolizace se vyznačuje okluzí konkrétních drobných větví renální tepny, které přímo vyživují lézi s minimálním dopadem na okolní tkáň. Superselektivní embolizace vede k infarktu méně než 10 % necílového parenchymu ledviny, která není spojena s klinicky významným snížením funkce ledviny (8).
Totální (celková) embolizace
Cílem celkové embolizace je kompletní okluze renální tepny vedoucí k afunkci ledviny a k odstranění krevního zásobení ledviny.
VÝSLEDKY
V jednom případě šlo o paliativní léčbu nádoru ledviny. Jednalo se o embolizaci u pacientky s inoperabilním 12cm tumorem pravé ledviny s metastatickým postižením uzlin retroperitonea. Nejprve byla provedena biopsie nádoru s nálezem granulární varianty světlobuněčného renálního karcinomu. Vzhledem k trvající makroskopické hematurii indikována k embolizaci renální tepny (obr. 2) a následně k ozáření pravé ledviny dávkou 52 Gy. Pacientka rok po zákroku exitovala na generalizaci onemocnění.
Obr. 2. Embolizace inoperabilního tumoru pravé ledviny Tumor je zásoben kromě renální tepny další kaudální arterií. Pomocí přípravku Embosphere<sup>®</sup>, spirál Tornado<sup>®</sup> a přípravku Histoacryl<sup>®</sup> uzavřena postupně dolní pólová arterie a poté i hlavní renální tepna. Fig. 2. Embolization of an inoperable tumor of the right kidney In addition to a renal artery the tumor is also supplied by another caudal artery. With the use of Embosphere <sup>®</sup>, Tornado<sup>®</sup> microcoils and Histoacryl<sup>®</sup> the lower pole artery and then also the general artery gradually closed. 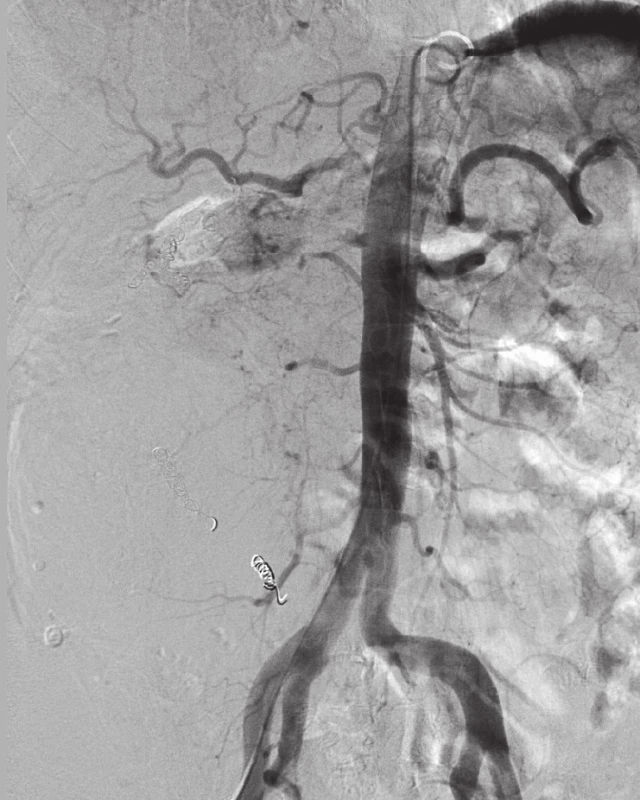
Ve čtyřech případech šlo o řešení komplikací po resekci, v jednom případě po laparoskopické resekci a ve třech případech po translumbální resekci. V uvedených případech vzniklo pseudoaneuryzma renální tepny, které se projevilo makroskopickou hematurií průměrně 19 dní od výkonu (rozmezí 9 až 25 dní). Ve všech čtyřech případech měla selektivní embolizace výborný efekt a došlo k zástavě krvácení.
Obrázek 3 zobrazuje úspěšnou selektivní embolizaci pro krvácení 9. den po laparoskopické resekci tumoru dolního pólu pravé ledviny.
Obr. 3. Selektivní embolizace dolní pólové větve pomocí spirál, větev pro pars intermedia je zachovaná Fig. 3. Selective embolization of the lower pole branch with the use of coils, the branch for pars intermedia is preserved 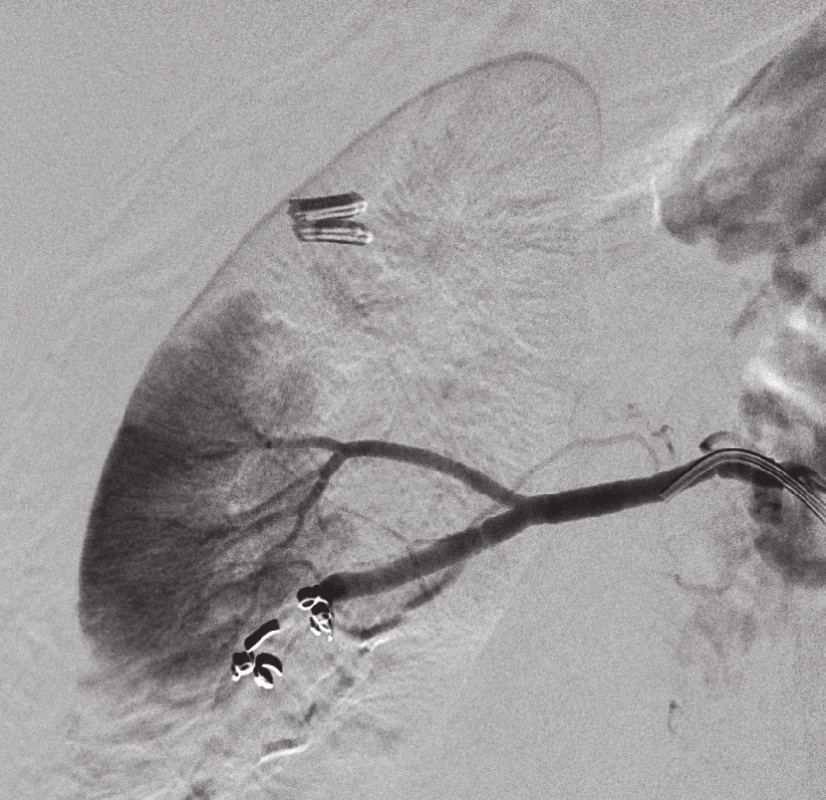
Obrázky 4 a 5 prezentují arteriografi i 20. den po translumbální resekci tumoru pravé ledviny a následnou embolizací krčku pseudoaneuryzmatu a přívodné arterie embolizačními spirálami s výborným klinickým efektem.
Obr. 4. Arteriografi e po translumbální resekci tumoru pravé ledviny Zobrazena mohutná větev pro kaudální renální segmenty, na kterou navazuje asi 2,5 cm pseudoaneuryzma a AV píštěl. Fig. 4. Arteriography after a translumbal tumor resection of the right kidney Image of a massive branch for caudal renal segments, which continues with approximately 2,5 cm long pseudoaneurysm and AV fi stula. 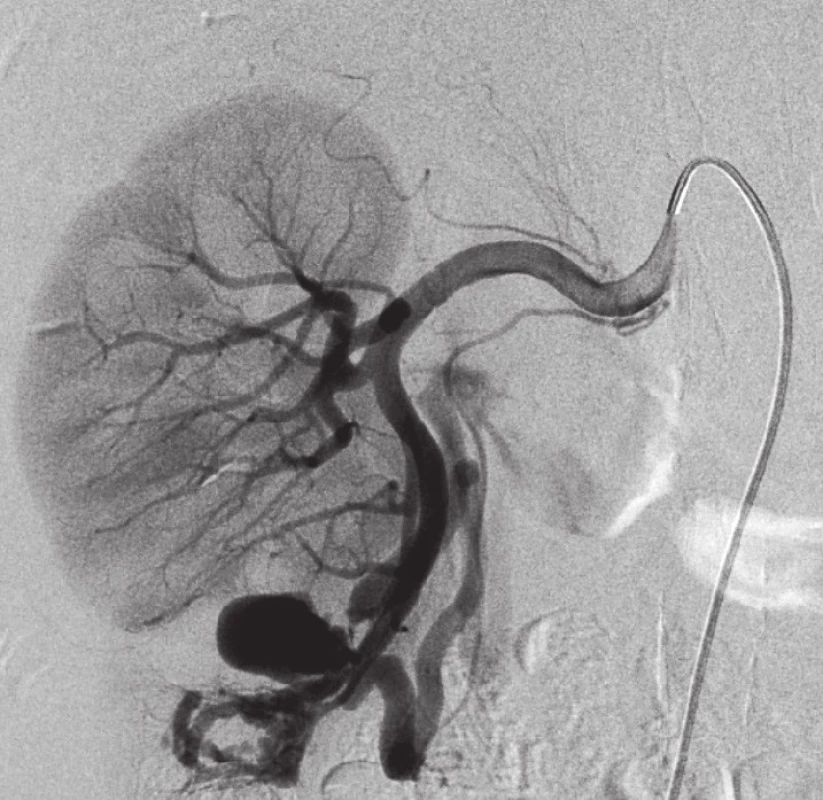
Obr. 5. Následná embolizace krčku pseudoaneuryzmatu a přívodné arterie embolizačními spirálami Tornado <sup>®</sup> Fig. 5. Subsequent embolization of the pseudoaneurysm neck and the aff erent artery with Tornado<sup>®</sup> embolization microcoils 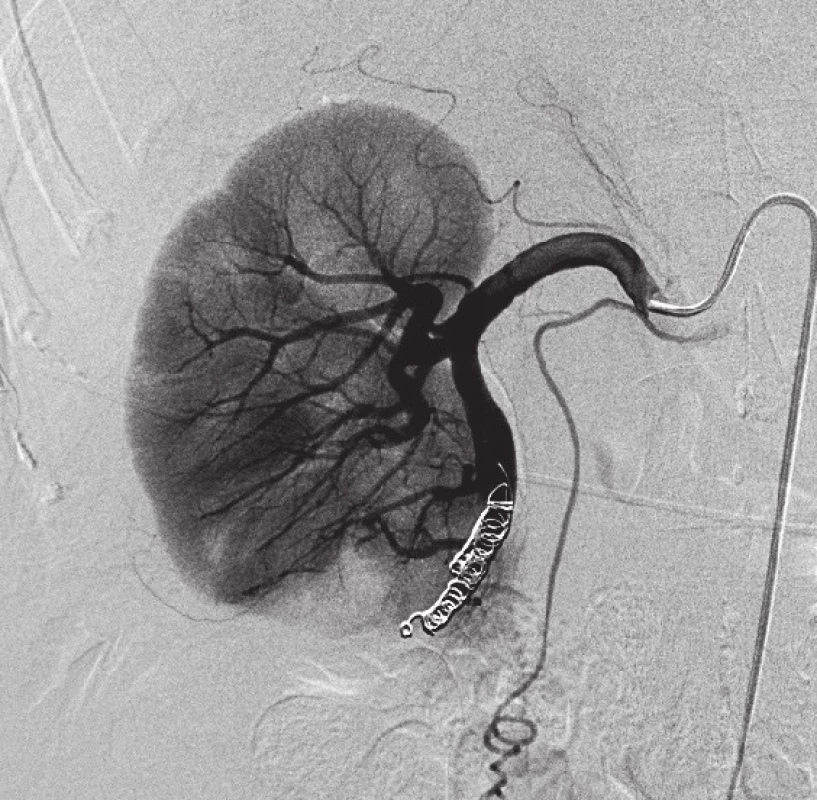
Ve dvou případech byla provedena embolizace angiomyolipomu (AML). U jedné pacientky (19 let) se jednalo o tuberózní sklerózu. Tato pacientka byla původně přijata na spádové chirurgické oddělení pro cefaleu a bolesti pravé poloviny břicha. Provedeno sonografické a CT vyšetření, které prokazuje polycystózu ledvin a 8cm AML pravé ledviny. Doplněno genetické, echokardiografické, neurologické a kožní vyšetření, MR mozku. Vzhledem k velikosti AML indikována embolizace, provedena superselektivní embolizace tří segmentárních tepen a vyřazení cévního zásobení tumoru. Arteriografi i se superselektivní embolizací zobrazuje obrázek 6.
Obr. 6. Superselektivní embolizace tří segmentárních tepen a vyřazení cévního zásobení AML Embolizováno PVA částicemi, absolutním alkoholem a spirálami. Fig. 6. Superselective embolization of three segmental arteries and elimination of the vascular supply of an angiomyolipoma Embolized with the use of PVA particles, absolute alcohol and coils. 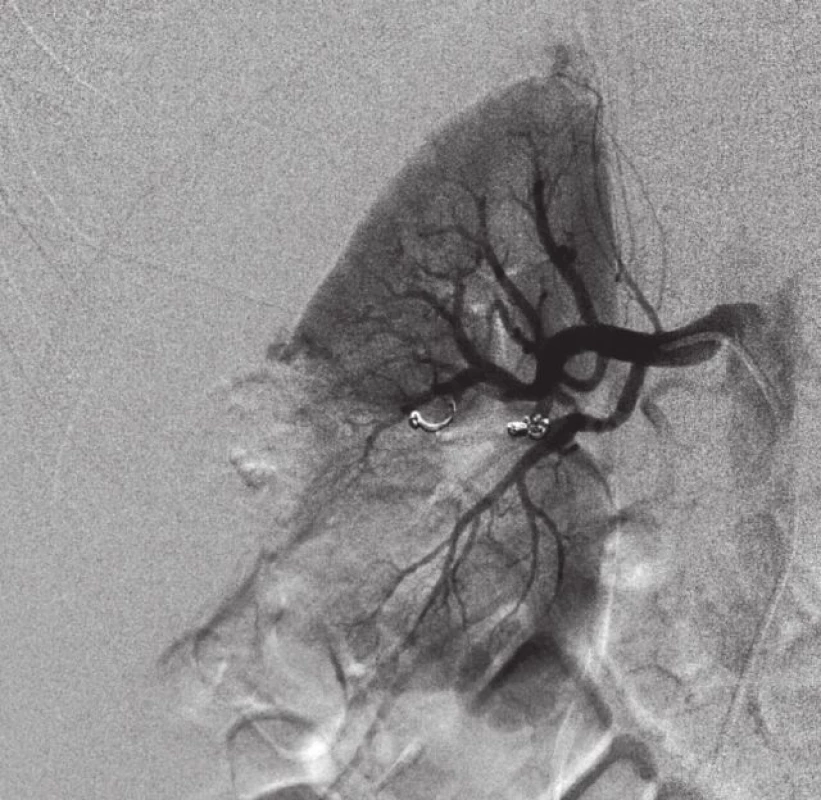
Tři měsíce po embolizaci došlo dle CT k regresi tumoru na průměr 5 cm, po dalším roce dle kontrolního sonografického vyšetření opět mírná regrese na maximální průměr 4,5 cm.
Komplikace arteriografie jsme v našem souboru neměli. Předoperační arteriografi i se selektivní embolizací ani s chlazením během resekce jsme u našeho souboru nepoužili.
DISKUSE
Embolizace inoperabilních tumorů
Dle doporučených postupů EAU (European Association of Urology) je embolizace indikována u pacientů s makroskopickou hematurií a lokální bolestivostí, kteří nejsou indikováni k chirurgické intervenci (9). Embolizace není přínosem před rutinní radikální nefrektomií (10).
Embolizace inoperabilních tumorů je více než v 90 % spojena s tzv. postembolizačním syndromem. Tento syndrom zahrnuje těžké lumbalgie na postižené straně, febrilie, nauzeu a zvracení, leukocytózu. Mohou se vyskytnout až příznaky peritoneálního dráždění a náhlé příhody břišní. Syndrom se vyskytuje 1–3 dny po embolizaci ledvinné tepny. Léčba je symptomatická a skládá se z analgetik, antipyretik a antiemetik (11).
Využití embolizace u resekcí ledvin
Vzhledem ke stále se rozšiřující a přesnější sonografi cké diagnostice z nejrůznějších indikací se zvyšuje procento incidentálních nádorů ledvin vhodných k záchovným výkonům. V souvislosti s rozvojem laparoskopie dochází i k většímu rozšíření laparoskopické resekce. Jejímu výraznějšímu rozšíření brání zatím technická náročnost operativy – hlavně kontrola krvácení a omezení dobou teplé ischémie při uzávěru hilu. Proto jsou laparoskopické resekce soustřeďovány jen do větších center a zatím nejde o standardní výkon (12).
O zjednodušení technické náročnosti laparoskopické resekce se snaží některá pracoviště předoperační superselektivní embolizací (SEA). Indikací pro předoperační SEA pak ve většině případů jsou nádory o průměru > 4 cm nebo nádory ≤ 4 cm s hloubkou intraparenchymové invaze > 1,5 cm. Pacienti s malými exofytickými nádory jsou léčeni laparoskopickou resekcí bez SEA. Pacienti s nádory > 4 cm v blízkosti hilových struktur nebo s hloubkou intraparenchymové invaze > 2 cm jsou léčeni otevřenou resekcí. Předoperační SEA umožní provádět laparoskopickou resekci bez klampování hilu a zabraňuje ischemickému poškození ledviny, které je hlavním omezujícím faktorem. Onkologické a funkční výsledky jsou srovnatelné s otevřeným přístupem (13).
Kromě kontroly hemostázy je neméně důležitý i interval teplé ischémie. Maximálně tolerovaný čas teplé ischémie je udáván 30 minut (14). Dobu teplé ischémie může prodloužit chlazení ledviny během výkonu. Jednou z možností chlazení je studená perfuze cestou renální arterie. Tato technika byla popsaná u lidí již více než před 20 lety pro otevřenou chirurgii (15, 16). Chlazení pomocí perfuze renální tepny je možné využít u laparoskopických výkonů, pokud předpokládáme delší dobu ischémie – centrální tumory, blízkost hilových struktur, větší nádor.
Pracoviště v Linci (G. Janetschek) popisuje svoje zkušenosti se souborem 28 pacientů, kterým byla provedena katetrizace renální tepny s následnou perfuzí 4 oC teplým roztokem Ringer-laktátu a následně provedena laparoskopická resekce (u tří pacientů konverze výkonu). Průměrná doba ischémie byla 42 minut – rozmezí 25–101 minut (14).
Metoda superselektivní embolizace je dále využitelná i před radiofrekvenční ablací nádoru (RFA), kde předchozí devaskularizace nádoru může údajně optimalizovat výsledek RFA snížením tepelných ztrát (7).
Řešení komplikací po resekcích
Nejčastější pooperační komplikací resekce ledviny je časné pooperační krvácení s výskytem kolem 5 % (17). Embolizaci lze dobře využít u krvácení po resekcích ledvin. Jedná o efektivní a možnou léčebnou metodu. Embolizace je méně invazivní než operační revize nebo nefrektomie, má nižší riziko komplikací a dobrou účinnost (18).
Méně častou komplikací po resekcích ledvin je AV píštěl a pseudoaneuryzma renální tepny. Incidence pseudoaneuryzmatu renální tepny po otevřené resekci se udává nižší než 0,5 % a po laparoskopické resekci 1–2 % (19–21). Nejvýznamnějším příznakem je makroskopická hematurie a lumbalgie nejčastěji v odstupu 3 týdnů po operaci. Albani a Novick (19) poukazují na možnost konzervativní léčby, jiné studie ukazují, že selektivní embolizace spirálou je ideální metoda s vysokou mírou úspěšnosti a malými komplikacemi (22, 23).
Existuje jen několik málo zpráv o AV píštěli po laparoskopické resekci, které byly řešeny pomocí selektivní embolizace (24, 25).
Angiomyolipomy
Angiomyolipomy jsou nádory benigní povahy, které obsahují cévy, tukovou a svalovou tkáň. Nádory průměru většího než 4 cm mají až 50% riziko ruptury a retroperitoneálního krvácení (26). Selektivní embolizace je metodou volby pro prevenci krvácení a dalšího růstu nebo má akutní využití v případě krvácení. Klinický úspěch je dosažen v 80–90 % případů superselektivní embolizace bez ztráty funkce ledviny, nicméně dlouhodobé sledování odhalí recidivy ve více než 30 % (7, 27). Kromě toho pacienti s tuberózní sklerózou mají větší riziko recidivy AML po embolizaci než pacienti se sporadickou formou AML (28).
Vzhledem k charakteru cévního zásobení AML, které připomíná cévní malformaci, je jako embolizační agens preferováno využití kapalin (alkohol, lepidlo) než použití embolizačních částic nebo spirál.
ZÁVĚR
Embolizace renální tepny je využitelná k paliativní léčbě inoperabilních tumorů, k řešení komplikací po resekcích, k léčbě angiomyolipomů a k předoperační superselektivní embolizaci před laparoskopickou resekcí.
Tyto výkony vyžadují odpovídající technické vybavení a zkušený personál, z tohoto důvodu je nutná koncentrace těchto výkonů do větších center. Velice důležitá je mezioborová spolupráce urolog – intervenční radiolog.
Embolizační výkony jsou velice efektivní, s dobrou účinností a mají nízké riziko komplikací. Pacient profituje z miniinvazivity zákroku.
Práce byla podpořena výzkumným záměrem MSM 0021620819 a grantem IGA NT 12010-5/2011.
Došlo: 5. 12. 2011.
Přijato: 22. 3. 2012.
Kontaktní adresa:
MUDr. Petr Stránský
Urologická klinika LF UK a FN
Dr. Edvarda Beneše 13,
305 99 Plzeň
e-mail: stranskyp@fnplzen.cz
Zdroje
1. Dos Santos R, Lamas A, Pereira Caldas J. L’arteriographie des membres de l’aorte et de ses branches abdominales. Bull et mem Soc Nat Chir 1929; 55 : 587–601.
2. Seldinger SI. Catheter replacement of needle in percutaneous arteriography: new technique. Acta radiol 1953; 39 : 368–376.
3. Hora M, Ferda J, Kreuzberg B, Klečka J, Hes O, Chudáček Z. Využití dvoufázové CT-angiografie při chirurgické léčbě nádorů ledvin. Ces Urol 2005; 9(1): 14–19.
4. Hora M, Ferda J, Kreuzberg B, Mírka H, Stránský P, Ürge T, Eret V, Hes O. Možnosti využití dvoufázové angiografie (2F AG) renálních cév u magnetické rezonance silou magnetického pole 3 Tesla (3T MRI). Ces Urol 2011; 15(Suppl 2): 71.
5. Abath C, Andrade G, Cavalcanti D, et al. Complex renal artery aneurysms: Liquids or coils? Tech Vasc Interv Radiol 2007; 10 : 299–307.
6. Ginat DT, Saad WE, Turba UC. Transcatheter renal artery embolization: Clinical applications and techniques. Tech Vasc Interv Radiol 2009; 12 : 224–239.
7. Ginat DT, Saad WE, Turba UC. Transcatheter Renal Artery Embolization for Management of Renal and Adrenal Tumors. Tech Vasc Interventional Rad 2010; 13 : 75–88.
8. Takebayashi S, Hosaka M, Kubota Y, et al. Transarterial embolization and ablation of renal arteriovenous malformations: Effi cacy and damages in 30 patients with long-term follow-up. J Urol 1998; 159 : 696–701.
9. Ljungberg B, Cowan NC, Hanbury DC, Hora M, Kuczyk MA, Merseburger AS, Patard JJ, Mulders PF, Sinescu IC. EAU Guidelines on Renal Cell Carcinoma: Th e 2010 Update. Eur Urol 2010; 58(3): 398–403.
10. Zielinski H, Szmigielski S, Petrovich Z. Comparison of preoperative embolization followed by radical nephrectomy with radical nephrectomy alone for renal cell carcinoma. Am J Clin Oncol 2000; 23(1): 6–12.
11. Cox GG, Lee KR, Price HI, et al. Colonic infarction following etanol embolization of renal-cell carcinoma. Radiology 1982; 145 : 343–345.
12. Hora M, Eret V, Ürge T, Stránský P, Klečka J jr, Hes O, Michal M, Chudáček Z, Ferda J. Results of laparoscopic resection of kidney tumour in everyday clinical practice. CEJU (Central European Journal of Urology) 2009; 62(3): 160–166.
13. Simone G, Papalia R,Guaglianone S, et al. Preoperative Superselective Transarterial Embolization in Laparoscopic Partial Nephrectomy: Technique, Oncologic, and Functional Outcomes. J Endourol 2009; 9(23): 1473–1478.
14. Beri A, Lattouf JB, Deambros O, et al. Partial Nephrectomy Using Renal Artery Perfusion for Cold Ischemia: Functional and Oncologic Outcomes. J Endourology 2008; 6(22): 1285–1290.
15. Marberger M, Georgi M, Guenther R, Hohenfellner R. Simultaneous balloon occlusion of the renal artery and hypothermic perfusion in situ surgery of the kidney. J Urol 1978; 119 : 463–467.
16. Farcon EM, Morales P, al-Askari S. In vivo hypothermic perfusion during renal surgery. Urology 1974; 3 : 414–420.
17. Van Poppel H, Bamelis B, Oyen R, Baert L. Partial nephrectomy for renal cell carcinoma can achieve long-term tumor control. J Urol 1998; 160(3 Pt 1): 674–678.
18. Baumann C, Westphalen K, Fuchs H, Oesterwitz H, Hierholzer J. Interventional managment of bleeding aft er partial nephrectomy. Cardiovasc Intervent Radiol 2007; 30(5): 828–832.
19. Albani JM, Novick AC. Renal artery pseudoaneurysm aft er partial nephrectomy: three case reports and a literature review. Urology 2003; 62 : 227–231.
20. Cohenpour M, Strauss S, Gottlieb P, et al. Pseudoaneurysm of the renal artery following partial nephrectomy: imaging fi ndings and coil embolization. Clin Radiol 2007; 62 : 1104–1109.
21. Singh D, Gill IS. Renal artery pseudoaneurysm following laparoscopic partial nephrectomy. J Urol 2005; 174 : 2256–2259.
22. Heyns CF, van Vollenhoven P. Increasing role of angiography and segmental artery embolization in the management of renal stab wounds. J Urol 1992; 147 : 1231–1234.
23. Huppert PE, Duda SH, Erley CM, et al. Embolization of renal vascular lesions: clinical experience with microcoils and tracker catheters. Cardiovasc Intervent Radiol 1993; 16 : 361–367.
24. Negoro H, Kawakita M, Koda Y. Renal artery pseudoaneurysm aft er laparoscopic partial nephrectomy for renal cell carcinoma in a solitary kidney. Int J Urol 2005; 12 : 683–685.
25. Wright JL, Porter JR. Renal artery pseudoaneurysm aft er laparoscopic partial nephrectomy. Urology 2005; 66 : 1109.
26. Rimon U, Duvdevani M, Garniek A, et al. Large renal angiomyolipomas: Digital subtraction angiographic grading and presentation with bleeding. Clin Radiol 2006; 61 : 520–526. 27. Kothary N, Soulen MC, Clark TW, et al. Renal angiomyolipoma: Longterm results aft er arterial embolization. J Vasc Interv Radiol 2005; 16 : 45–50.
28. Ewalt DH, Diamond N, Rees C, et al. Long-term outcome of transcatheter embolization of renal angiomyolipomas due to tuberous sclerosis complex. J Urol 2005; 174 : 1764–1766.
Štítky
Dětská urologie Nefrologie Urologie
Článek vyšel v časopiseČeská urologie
Nejčtenější tento týden
2012 Číslo 1- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Kterým pacientům se SLE nasadit biologickou léčbu?
- Nostiriazyn – spolehlivá 1. volba u nekomplikovaných infekcí močových cest
- Nitrofurantoin s řízeným uvolňováním: osvědčená účinnost, lepší snášenlivost a méně tablet při akutní cystitidě
- Jak souvisí časné zahájení biologické léčby SLE/LN s prevencí nevratného poškození?
-
Všechny články tohoto čísla
- Do akej miery je aktívne sledovanie malých nádorov obličiek bezpečná stratégia?
- Srovnání výsledků miniinvazivní léčby ženské stresové inkontinence metodou AjustTM a MiniArcTM
- Urologické komplikace po zavedení močového katétru po náhradách velkých kloubů u mužů
- Editorial
- Matematické modelování deformace penisu při induratio penis plastica po terapii rázovými vlnami (SWT)
- Korelace výsledku pozitronové emisní tomografie a nálezu při resekci reziduálních lézí po chemoterapii neseminomových germinálních nádorů
- Využití neuromodulace v léčbě dysfunkcí dolních močových cest
- Možnosti intervenční radiologie při léčbě nádorů ledvin
- Stanovení exprese SHB v tkáni karcinomu prostaty: využití v diagnostice a prognostice
- Oboustranná adrenalektomie – u pacientů s Cushingovým syndromem při ektopické sekreci ACTH
- Vzpomínka na pana docentra MUDr. Jaroslava Nováka, CSc.
- Výbor ČUS vyhlašuje soutěž o nejlepší vědecké publikace za rok 2011
- Výsledek losování o účast na ESOU
- Výbor ČUS společně se sponzory odměnili původní práce rezidentů v české urologii za rok 2011
- Česká urologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Urologické komplikace po zavedení močového katétru po náhradách velkých kloubů u mužů
- Do akej miery je aktívne sledovanie malých nádorov obličiek bezpečná stratégia?
- Využití neuromodulace v léčbě dysfunkcí dolních močových cest
- Oboustranná adrenalektomie – u pacientů s Cushingovým syndromem při ektopické sekreci ACTH
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



