-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Neurorehabilitace poruch chůze s využitím funkční elektrické stimulace – aktuální poznatky z randomizovaných klinických studií
Neurorehabilitation of gait impairment using functional electrical stimulation – current findings from randomized clinical trials
The review article summarizes results from studies with functional electrical stimulation (FES) in neurorehabilitation. In neurorehabilitation, FES is used mostly for therapeutic improvement of the swing phase of the gait cycle by stimulation of dorsal flexor muscles. For this review article, 510 papers were screened and 42 papers were eligible for a more detailed analysis. Based on the available studies, it seems that FES may constitute an enrichment of traditional therapeutic practice (such as exercise based on neurophysiological principles, gait and balance training). In some patients, FES may result in improved functional status rather than conventional therapy.
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE “uniform requirements” for biomedical papers.
Keywords:
Multiple sclerosis – stroke – neurorehabilitation – Functional electrical stimulation – gait
Autoři: K. Novotná 1,2; J. Jeníček 3; M. Janatová 3,4; E. Kubala; Havrdová 1; Y. Angerová 3
Působiště autorů: Neurologická klinika a Centrum klinických neurověd, 1. LF UK a VFN v Praze 1; MS rehab z. s. 3 Klinika rehabilitačního lékařství 1. LF UK a VFN v Praze 2; Společné pracoviště biomedicínského inženýrství FBMI a ČVUT a 1. LF UK, Praha 4
Vyšlo v časopise: Cesk Slov Neurol N 2019; 82(6): 621-626
Kategorie: Přehledný referát
doi: https://doi.org/10.14735/amcsnn2019621Souhrn
Systematický rešeršní článek popisuje zkušenosti s využitím funkční elektrické stimulace (FES) v neurorehabilitaci. V rámci neurorehabilitace se FES využívá především k terapeutickému ovlivnění poruch chůze pomocí stimulace dorzálních flexorů hlezna. Pro účely rešerše bylo vyhledáno 510 článků, z nichž 42 bylo podrobněji analyzováno. Na základě dostupných studií využívajících FES pro zlepšení funkce dolních končetin se zdá, že FES může představovat obohacení tradičních terapeutických postupů (jako jsou cvičení na neurofyziologickém podkladě, trénink chůze a stability). V některých případech pak může FES vést k výraznějšímu zlepšení funkčního stavu než tradiční terapie.
Klíčová slova:
funkční elektrická stimulace – chůze – neurorehabilitace – cévní mozková příhoda – roztroušená skleróza
Úvod
Metoda funkční elektrostimulace (FES) pro podporu nebo nahrazení ztracené pohybové funkce byla poprvé navržena Libersonem v roce 1961. Ten popsal stimulaci peroneálního nervu elektrickými impulzy jako podporu chybějící dorzální flexe hlezna (tzv. drop foot syndrom) u pacienta s hemiplegií po CMP. Stimulace byla aplikována povrchovými elektrodami a byla synchronizována se švihovou fází kroku díky patnímu tlakovému spínači v botě [1]. Termín „funkční elektrická stimulace“ uvedli v roce 1962 Moe a Post a brzy se objevily i první komerční přístroje [2]. Metoda byla v 70. a 80. letech díky elektrostimulátorům Tesla LSN (Tesla, Hloubětín, Česká republika) dostupná i v ČR. Přístroj se však v 90. letech přestal vyrábět a zkušenosti s FES se tak u nás dále příliš nerozvíjely [3]. V zahraničí byla metoda používána dál, k masivnímu rozšíření ale ještě řadu let nedošlo. S její aplikací byla spojena řada problémů technického a praktického charakteru, především složitost upevnění elektrod a propojovacích kabelů, dále spolehlivost, správné načasování a dyskomfort uložení patního snímače, často nedostatečný iniciální kontakt paty pacienta s podložkou, velikost, váha a uložení elektrostimulátoru apod.
S vývojem miniaturizovaných a ergonomických funkčních elektrostimulátorů se však rozšiřují možnosti jejich klinického použití. Byly vyvinuty přístroje s vícekanálovou stimulací, které umožňují kombinovat stimulaci peroneálního nervu se stimulací dalších svalů (plantárních flexorů hlezna, flexorů nebo extenzorů kolenního kloubu, flexorů nebo abduktorů kyčle). Tyto přístroje mohou pomoci při tréninku chůze u pacientů s poškozením horního motoneuronu. Ale i původní jednokanálový stimulátor peroneálního nervu byl dále rozvíjen a funkce patního snímače byla u některých typů nahrazena nebo doplněna o sofistikovaný systém akcelerometru a inklinometru/ gyroskopu, který optimalizuje načasování kontrakce a dekontrakce svalů v průběhu kroku [4]. Kromě FES dolní končetiny se také rozvíjí možnosti FES v oblasti horní končetiny, konkrétně stimulace úchopové funkce ruky [5].
Funkční elektrostimulace je považována za technicky pokročilejší a aktivnější variantu běžně užívané peroneální ortézy (ankle foot orthosis; AFO), která se používá s cílem mechanicky udržet nohu v neutrálním nebo mírně dorzálně flekčním postavení v hlezenním kloubu a zabezpečit tak hladký průběh švihové fáze kroku, ať již se jedná o poruchu postavení a hybnosti akrální části dolní končetiny vlivem poškození CNS nebo periferního nervového systému. Na rozdíl od jednodušších peroneálních pásek poskytují dlahy noze pevnější oporu a mohou tak pomoci i pacientům se spasticitou lýtkových svalů, pro které je podpora pouze peroneální páskou nedostatečná. Je možné rozlišit 3 typy těchto ortéz: pasivní AFO, semi-aktivní AFO a aktivní AFO. Pasivní AFO ortézy jsou v klinické praxi nejrozšířenější. Jedná se o rigidní ortézy vyrobené většinou z polypropylenu nebo z karbonu. Ortézy mohou být sériově vyráběné nebo individuálně zhotovené.
Možnosti využití FES v rámci neurorehabilitace se v ČR stále více rozvíjí a v současnosti jsou na českém trhu 2 přístroje pro elektrostimulaci chůze, proto bychom v tomto článku chtěli představit a porovnat výsledky randomizovaných klinických studií hodnotících efekt FES k ovlivnění chůze.
Metodika
Cílem tohoto článku bylo na základě analýzy dostupných randomizovaných studií zhodnotit možnost zlepšení chůze u dospělých neurologických pacientů se získaným poškozením CNS pomocí FES. Pro účely tohoto článku byla prohledána databáze medicínské literatury PubMed za pomoci kombinace těchto klíčových slov: functional electrostimulation, gait, walk, stroke, multiple sclerosis, traumatic brain injury, central paresis, hemiparesis, drop foot. Vyhledávání bylo omezeno pouze na období od roku 2000 až do září 2018. Do analýzy byly zařazeny pouze: 1. randomizované studie porovnávající efekt terapie u experimentální skupiny s FES oproti kontrolní skupině; 2. studie zahrnující dospělé neurologické pacienty starší 18 let; 3. studie publikované v anglickém jazyce.
Kvalita vyhledaných studií byla hodnocena pomocí škály PEDro. Jedná se o 11bodovou škálu, která hodnotí metodologickou kvalitu randomizovaných studií. V rámci této škály jsou hodnoceny kvalita randomizace, zaslepenost probandů a vyšetřujících a popis a porovnání výsledků mezi hodnocenými skupinami. Čím vyšší bodové hodnocení, tím vyšší metodologická kvalita článku [6]. Do článku nebyly zařazeny studie s příliš nízkou metodologickou kvalitou (škála PEDro < 4).
Výsledky
Na základě zadané kombinace klíčových slov bylo nalezeno 510 článků. Při kontrole abstraktů (v případě nejasnosti celých článků) bylo identifikováno 50 potencionálně vhodných článků za určené období. Po přečtení abstraktů byla část studií vyřazena pro nesplnění podmínek (účastníci nebyli neurologičtí pacienti, chyběla kontrolní skupina, nejednalo se o randomizovanou kontrolovanou studii) a pro finální analýzu tak zůstalo 42 studií. Průběh vyhledávání je zobrazen na obr. 1. Největší množství studií porovnávalo efekt FES v rámci neurorehabilitace u osob po CMP, celkem 38 publikací randomizovaných kontrolovaných studií, přičemž u 10 publikací se jednalo u osoby po CMP v akutním nebo subakutním stadiu. Dále byly zařazeny 4 studie sledující efekt FES u osob s roztroušenou sklerózou, 1 studie sledovala efekt u osob po úrazovém poškození CNS (kraniotraumatu). Průměrná kvalita studií byla 7,3 bodů podle škály PEDro.
Tab. 1. Schéma třídění vyhledaných článků do systematické rešerše. FES – funkční elektrická stimulace; n – počet
Fig. 1. The process of searching articles into the systematic review. FES – functional electrical stimulation; n – number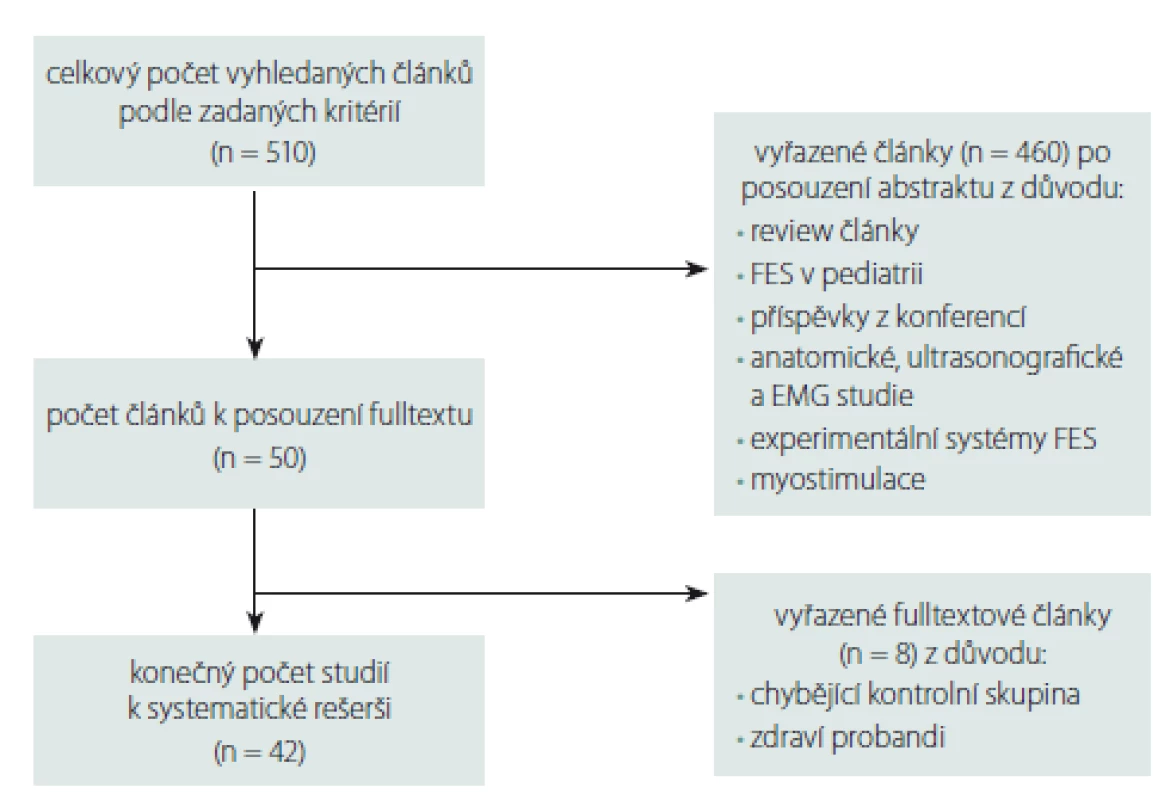
Využití FES u CMP
Celkem 31 studií (z některých studií bylo více publikací) hodnotilo u 1 512 osob po CMP v akutním až chronickém stadiu efekt FES oproti kontrolní skupině podstupující jiný typ intervence.
Ve dvou studiích zahrnujících 37 pacientů nedošlo k signifikantnímu zlepšení ve vyšetřovaných parametrech v kontrolní ani ve výzkumné skupině. Kontrolní skupina ve studii s 21 probandy podstoupila balanční trénink nebo běžnou péči, intervence trvala 2 týdny [7]. Kontrolní skupina ve studii s 16 probandy podstoupila terapii s využitím AFO ortézy, intervence trvala 12 týdnů [8].
U sedmi studií, do kterých bylo zařazeno celkem 699 pacientů, byl prokázán pozitivní efekt u kontrolní i výzkumné skupiny, přičemž u výzkumné skupiny nebyl efekt statisticky významně vyšší než u kontrolní skupiny. Délka intervence se pohybovala od 3 týdnů do 12 měsíců. Dvě ze studií byly zaměřeny na pacienty v chronickém stadiu po CMP [9,10]. Ve studii zahrnující nejvyšší počet probandů v počtu 384 pacientů a nejdelší dobu intervence v délce 12 měsíců byla u kontrolní skupiny aplikována AFO ortéza. V obou skupinách došlo k signifikantnímu zlepšení v rychlosti chůze na 10 m bez statisticky významného rozdílu mezi kontrolní a výzkumnou skupinou [2].
Ve 22 studiích zahrnujících celkem 774 pacientů došlo k signifikantně vyššímu zlepšení u pacientů ve výzkumné skupině (s FES) oproti kontrolní skupině. Kontrolní skupiny v těchto studiích podstoupily trénink chůze bez pomůcky, chůze na treadmillu, chůzi s AFO ortézou, stoj na úseči, nebo v metodice blíže nespecifikovanou rehabilitační intervenci (o frekvenci cvičení 3 – 5× týdně). Ke zlepšení došlo v kvalitě chůze i ve standardizovaných testech chůze a rovnováhy (Tinetti test, Fugl-Meyer Test, Šestiminutový test chůze, Desetiminutový test chůze, Berg Balance Scale a další). Dále došlo ke zlepšení v soběstačnosti, která byla hodnocena pomocí testu Functional Independence Measure (FIM) nebo Indexu Barthelové. V jedné ze studií bylo pozorováno signifikantní snížení spasticity (hodnocené modifikovanou Ashworthovou škálou) a zvýšení svalové síly u pacientů ve výzkumné skupině [11].
Využití FES u roztroušené sklerózy
Do naší analýzy byly zahrnuty 3 studie hodnotící u 144 osob s RS (z toho u 108 osob se jednalo o progresivní stadium RS) efekt FES oproti běžnému posilování svalů nebo žádné intervenci. Délka intervence se pohybovala od 18 do 24 týdnů. Pouze u 1 studie [12] došlo u skupiny s FES k významnějšímu zlepšení zapojení do denních aktivit a snížení počtu pádů oproti kontrolní skupině s běžným cvičením. V dalších studiích při srovnání efektu FES oproti posilování svalů dolních končetin nebo trupu nebylo zaznamenáno u skupiny s FES ani v kontrolní významnější zlepšení výkonu v testech chůze. Tento výsledek může být ovlivněn progresivním charakterem onemocnění RS. V jedné ze studií však bylo zaznamenáno snížení energetické náročnosti chůze při FES, což může být klinicky významné.
Využití FES u jiných dospělých pacientů se získaným neurologickým poškozením
Pouze 1 studie hodnotila efekt FES u pacientů s traumatickým poškozením mozku [13], další 2 studie pak zahrnovaly skupinu pacientů s hemiparetickým poškozením (po CMP nebo kraniotraumatu). Celkem se jednalo o 90 probandů, u kterých se porovnával efekt FES oproti jiné terapeutické intervenci (chůze na páse, stoj ve vertikalizačním stojanu nebo standardní fyzioterapeutické cvičení). Terapeutická intervence se lišila od velmi intenzivní v délce 1 týdne až po 12 týdnů. Trénink chůze na páse v kombinaci s FES hodinu denně v délce trvání 12 týdnů prokázal u skupiny osob s hemiparetickým postižením chůze se syndromem foot drop významné zlepšení vytrvalosti a kvality chůze oproti běžnému tréninku chůze. Při porovnání standardní fyzioterapie vs. fyzioterapie doplněné FES došlo k mírnému zlepšení v obou porovnávaných skupinách.
Diskuze
V rehabilitační praxi může být FES užívána při tréninku chůze na páse, v kombinaci s posilovacím cvičením nebo jako kompenzační pomůcka při běžné chůzi pacienta v prostředí rehabilitačního zařízení i v domácím prostředí.
Většina námi analyzovaných studií popisuje pozitivní tzv. ortotický efekt FES (tedy zlepšení při používání stimulátoru). Některé studie však zaznamenávají také pozitivní terapeutický efekt (tedy přetrvávající zlepšení i po vypnutí stimulace) na zlepšení funkční mobility [14,15], zlepšení výkonu v dlouhých testech chůze [16,17] a snížení energetické náročnosti chůze [18,19].
Všechny analyzované studie využívaly FES n. peroneus (n. fibularis), některé také v kombinaci se stimulací flexorů nebo extenzorů kolenního kloubu nebo m. gluteus medius. Stimulace byla využívána pouze pro intenzivní trénink chůze nebo byla běžně používána během všedních denních aktivit.
Nejvíce nalezených studií se zabývalo možnostmi využití FES u osob s CMP. U osob s hemiparetickým postižením chůze po CMP se v klinické praxi běžně využívá AFO ortéza. Také dosud největší realizovaná randomizovaná studie, která porovnávala efekt FES i AFO na chůzi, prokázala, že obě tyto kompenzační pomůcky mají dlouhodobě významně pozitivní vliv na parametry chůze [20]. Tomu odpovídají také závěry metaanalýzy z roku 2018, která potvrzuje, že obě tyto pomůcky mají pozitivní vliv na rychlost chůze a FES není v tomto směru nadřazena konvenčně používané terapii pro kompenzaci poruch chůze [21]. Některé studie však naznačují, že FES díky aktivnímu zapojení svalů může pomáhat fyziologičtějšímu zapojení svalů dolní končetiny během krokového cyklu, zvyšovat svalovou sílu [7,11,15 – 17,19,22 – 29] a snižovat spasticitu lýtkových svalů i v chronické fázi [9,11,22,23,27,30,31]. V literatuře jsou u některých pacientů po elektrostimulaci popisovány i neuroplastické změny [8,32,33] (zaznamenané pomocí funkční MR), a to zvýšení excitability a konektivity nepoškozených kortikálních motorických oblastí a reziduálních kortikospinálních drah. Za podklad této indukované restituce motorických funkcí jsou označovány především kortikální reorganizace (a to i v senzorických a kontralaterálních motorických oblastech), axonální sprouting a synaptogeneze, zvýšená aktivace sekundárních motorických oblastí a přesun řízení na extrapyramidové dráhy [10,34,35]. Zvýšení aktivity motorické oblasti je při FES připisováno zvýšené proprioceptivní stimulaci nebo zaměření pozornosti. Za nezbytnou podmínku indukce neuroplastických změn a obnovu řízené hybnosti je obecně považována vysoká intenzita tréninku (počtem opakování pohybu nebo jeho náročností – maximální rychlostí a maximálním rozsahem pohybu), vysoká frekvence terapií, specificita pohybu a jeho vazba na smysluplnou funkci a subjektivní motivace pacienta [10,36]. Gandolla et al uvádějí, že podmínkou pro vznik přetrvávajícího terapeutického efektu je schopnost pacienta pohyb akra dolní končetiny při FES předvídat a plánovat a vnímat jeho provedení jako součást vlastní zpětnovazebné smyčky [37]. Z animálních studií víme, že nezbytný počet opakování pohybu horní končetinou k podpoře neuroplastických změn je 400 – 600 opakování denně [38,39]. Při běžné neurorehabilitaci je však průměrný počet pohybů dolní končetinou během jedné terapie pouze 60 opakování [40]. Chůze s využitím FES také může pomáhat procesu motorického učení, protože zvyšuje průměrné množství vykonaných kroků [17]. Pro podporu motorického učení je nezbytná motivace pacienta a jeho aktivní zapojení. Vzhledem k tomu, že většina pacientů preferuje FES před peroneální ortézou zejména proto, že chůze se stimulací působí i vypadá „normálněji“ [41,42], může být právě trénink chůze s FES pro některé pacienty vhodným prostředkem na podporu motorického učení.
Většina analyzovaných studií hodnotí efekt stimulace u pacientů po CMP v chronickém stadiu. Některé studie také naznačují možnosti využití v časné terapii (v subakutní fázi po CMP). Po krátkém 1 – 2 týdny trvajícím rehabilitačním programu doplněném o FES n. peroneus došlo ke zlepšení EMG aktivity svalů dolní končetiny, časoprostorových parametrů chůze i funkční mobility [28,43]. Naopak studie hodnotící 2týdenní efekt balančního tréninku u subakutních pacientů neprokázala zlepšení rychlosti chůze [44], což však může být ovlivněno malou intenzitou terapie (celkem pouze 7 terapií). U 54 osob po CMP v subakutní fázi se prokázal pozitivní vliv tréninku chůze na páse (ať již se jednalo o chůzi s FES nebo bez ní) oproti konvenčnímu tréninku chůze. Další možností využití FES pro pacienty, kteří nejsou schopni delší chůze, nabízí FES kombinovaná se šlapáním na motomedu [45,46]. Celkem ve 30 studiích byl porovnáván efekt FES oproti běžně dostupné fyzioterapii nebo kinezioterapii. Až na studii Wilkinsona et al [47], která detailně popisuje využité fyzioterapeutické techniky a postupy, není obsah terapeutických jednotek ve studiích blíže specifikován a většinou je uváděn jen obecně jako „konvenční rehabilitace po CMP“, „rutinní reedukace chůze a stability“, „protahovací a posilovací cvičení“ nebo „fyzioterapie s využitím neurovývojových technik“ [11,19]. Sabut et al mezi terapeutické jednotky zařadili i ergoterapeutické postupy [11,19]. Běžná klinická praxe a využití FES se může v různých zemích lišit v závislosti na kulturních zvyklostech a zejména na ekonomických možnostech (FES představuje nákladnější variantu terapie a zpravidla nebývá hrazena ze zdravotního pojištění). V praxi také bývá tato možnost častěji předepisována pacientům s neprogresivní diagnózou (častěji u CMP, dětské mozkové obrny nebo nekompletních míšních lézí). Vždy však záleží na individuálním posouzení funkčního stavu a možností pacienta.
Uvádí se, že v praxi se vyskytují pacienti, kteří dobře profitují z terapie s využitím FES (tzv. respondéři), a pacienti, kteří i při dodržení podobných podmínek stimulace zůstávají bez efektu (tzv. non-respondéři). Předmětem některých prací je tedy snaha o stanovení prediktorů efektu FES [48]. Sota et al uvádějí, že jedním z těchto prediktorů může být rozsah aktivní dorzální flexe v hlezenním kloubu při úvodním vyšetření před intervencí FES [49]. Dalším prediktorem může být pacientova schopnost vnímání pohybu vyvolaného FES [37]. V řadě studií, které neprokázaly lepší efekt FES oproti peroneálnímu ortézování, je nicméně popisována významně vyšší preference uživatelů k FES. Nejčastěji uváděnými důvody této preference jsou větší sebejistota a pocit bezpečnosti při chůzi (nižší obava z pádu), vyšší komfort použití, snadné nasazování a sundávání pomůcky, estetický vzhled pomůcky, vliv na kvalitu chůze, nižší úsilí a únavu a neomezování volného pohybu hlezna [17,18,50,51]. Podobný přínos FES naznačují i práce Bulleyho et al [42] a Wilkieho et al [52] vedené formou semistrukturovaných rozhovorů, které u chronických pacientů po CMP a jejich terapeutů analyzovaly subjektivní vnímání a hodnocení efektu FES na chůzi, náladu, psychický stav, celkovou aktivitu v rámci aktivit denního života a participaci v rámci komunity. V retrospektivní studii [53] bylo u pacientů používajících FES v období 2 let popsáno jen 8 % přerušení nebo ukončení používání stimulátoru, což je významně nižší než přibližně čtvrtinové ukončení používání, které se uvádí v případě AFO [54]. Vyšší pocit sebejistoty a/ nebo bezpečí a současný významný terapeutický efekt FES na zvýšení aktivace a svalové síly dorzálních flexorů nohy a celkového aktivního rozsahu hlezna do dorzální flexe, který byl prokázán ve studiích [11,19,30], může mít oproti AFO vliv na snížení rizika pádů v situacích, kdy pacienti obvykle žádnou pomůcku pro chůzi nepoužijí, např. při dojití na toaletu nebo do koupelny v průběhu noci [18].
Tab. 1. Přehled zařazených studií
Publikace
Účastníci
Design studie
Vyšetřované testy
Výsledky
1
Barrett et al 2009: A randomized trial to investigate the effects of functional electrical stimulation and therapeutic exercise on walking performance for people with multiple sclerosis.
Multiple Sclerosis
44 osob s RS –sekundární progrese
18 týdnů rozdělení na: 1. experimentální skupinu s FES n.peroneus a 2. kontrolní skupinu s domácím posilovacím cvičením svalů DKK a trupu
10 metrový test rychlosti chůze, energetická náročnost chůze na 10 m, ušlá vzdálenost za 3 min
kontrolní skupina: snížení rychlosti chůze na 10 m, zvýšení vzdálenosti za 3 min, v experimentální skupině došlo pouze ke snížení náročnosti chůze s FES oproti vypnuté stimulaci
2
Bethoux et al 2015: Long-term follow-up to a randomized controlled trial comparing peroneal nerve functional electrical stimulation to an ankle foot orthosis for patients with chronic stroke. Neurorehabilitation and Neuroal Repair
384 osob po CMP –chronická faze
12 měsíců užívala 1. experimentální skupina FES n. peroneus a 2. kontrolní skupina AFO
10m test rychlosti chůze, 6min test, aktivity denního života, funkční ambulantní profil vyšetřen na GAITRite, modifikovaný Emory ambulation profile, Berg Balance test, Timed Up and Go
u obou skupin došlo ke signif. zlepšení v rychlosti chůze na 10 m
3
Bethoux et al 2014: The effects of peroneal nerve functional electrical stimulation versus ankle-foot orthosis in patients with chronic stroke: a randomized controlled trial.
Neurorehabilitation and Neuroal Repair
399 osob po CMP –chronická faze
6 měsíců: experimentální užívala FES n. peroneus, kontrolní AFO
10m test rychlosti chůze, 6min test, aktivity denního života, funkční ambulantní profil vyšetřen na GAITRite, modifikovaný Emory ambulation profile, Berg Balance test, Timed Up and Go
obě skupiny se signifikantně zlepšily v rychlosti chůze na 10 m
4
Broekmans et al 2011: Effects of long-term resistance training and simultaneous electro-stimulation on muscle strength and functional mobility in multiple sclerosis.
Multiple Sclerosis
36 osob s RS
20 týdnů rozděleni na 1. experimentální FES + posilování DK; 2. pouze posilování DK; 3. kontrolní
svalová síla flexorů a extenzorů kolenních kloubů, funkční testy: chůze na 25 stop, Timed Up and Go test, Functional reach, 2min test chůze
u obou skupin s posilovacím cvičením došlo ke zvýšení sval. síly
5
Daly et al 2006: A randomized controlled trial of functional neuromuscular stimulation in chronic stroke subjects.
Stroke
32 osob po CMP (déle než 1 rok)
12 týdnů: 4× týdně trénink chůze na treadmill (30 min) chůze na treadmill s podporou váhy těla (30 min) v obou skupinách + experimentální skupina navíc při chůzi funkční elektromuskulární stimulaci nejen dorzálních flexorů, ale také flexorů kolene, extenzorů kolena a gluteus medius
vyšetření chůze dle Tinetti (12bodová škála kvality chůze), Fugl-Meyer test koordinace flexe kolene, Tinetti balanční test, 6min test chůze
při funkční stimulaci zlepšení v testu chůze Tinetti a zlepšení koordinace flexe kolene
6
Daly et al 2004: Response of sagittal plane gait kinematics to weight-supported treadmill training and functional neuromuscular stimulation following stroke.
Journal of Rehabilitation Research and Development
16 osob po CMP (déle než 1 rok)
12 týdnů: 4× týdně trénink chůze na treadmill (30 min) chůze na treadmill s podporou váhy těla (30 min) v obou skupinách + experimentální skupina navíc při chůzi funkční elektromuskulární stimulaci nejen dorzálních flexorů, ale také flexorů kolene, extenzorů kolena a gluteus medius
3D kinematická analýza chůze
během švihové fáze kroku zlepšení flexe kolene a zvýšení dorzální flexe při střední švihové fázi u skupiny s FNS
7
Daly et al 2011: Recovery of coordinated gait: randomized controlled stroke trial of functional electrical stimulation (FES) versus no FES, with weight-supported treadmill and over-ground training.
Neurorehabiitation and Neural Repair
53 osob po CMP
12 týdnů: 4× týdně trénink chůze na treadmill (30 min) chůze na treadmill s podporou váhy těla (30 min) v obou skupinách + experimentální skupina navíc při chůzi funkční elektromuskulární stimulaci
Gait Assessment and Intervention Tool, Fugl-Meyer test, 6min test chůze, FIM test
ve skupině se stimulací zlepšení Gait Assessment and Intervention test-koordinace chůze
8
Dujovic et al 2017: Novel multi-pad functional electrical stimulation in stroke patients: A single-blind randomized study.
Neurorehabilitation
16 osob po CMP
4 týdny: 5× 60 min fyzioterapie v obou skupinách + experimentální skupina navíc FES n. peroneus
10m test rychlosti chůze, Fugl-Meyer vyšetření, Berg Balance Scale a Barthel Index
zlepšení rychlostí chůze na 10 m v experimentální skupině
9
Embrey et al 2010:
Functional electrical stimulation to dorsiflexors and plantar flexors during gait to improve walking in adults with chronic hemiplegia.
Archives of Physical Medicine and Rehabilitation
28 osob s hemiplegií (po CMP nebo kraniotraumatu)
12 týdnů: experimentální skupina chodila s FES n. peroneus každý den, kontrolní skupina trénink běžné chůze 1 h denně, 6 dní v týdnu
6min test chůze, Emory Ambulation Profile, svalová síla a spasticita
v experimentální skupině došlo ke zlepšení v testu chůze na 6 min a Emory Ambulation Profile
10
Esnouf et al 2010: Impact on activities of daily living using a functional electrical stimulation device to improve dropped foot in people with multiple sclerosis, measured by the Canadian Occupational Performance Measure.
Multiple Sclerosis
64 osob s progresivní RS
18 týdnů rozdělení na 1. experimentální skupinu s FES n.peroneus po celý den a 2. kontrolní skupinu instruktáž fyzioterapeutických cvičení 30 min 1–2× denně
Canadian occupational performance measure, deník pádů
skupina FES se výrazně zlepšila v canadian occupationa performance a došlo u ní ke snížení počtu pádů
11
Everaert et al 2013: Effect of a foot-drop stimulator and ankle-foot orthosis on walking performance after stroke: a multicenter randomized controlled trial.
Neurorehabiitation and Neural Repair
93 osob po CMP
12 týdnů: 1. prvních 6 týdnů chůze s FES n. peroneus, dalších 6 týdnů chůze s AFO; 2. prvních 6 týdnů chůze s AFO, dalších 6 týdnů chůze s FES; 3. celých 12 týdnů s AFO
10m test rychlosti chůze, fyziologická náročnost chůze
obě pomůcky FES stimulátor i AFO měly výrazný ortotický efekt i terapeutický efekt na rychlost chůze, AFO ortéza měla i signifikantní ortotický efekt na fyziologickou náročnost chůze
12
Ghédira et al 2017: Wireless, accelerometry-triggered functional electrical stimulation of the peroneal nerve in spastic paresis: A randomized, controlled pilot study.
Assistive technology
20 osob po CMP
10 týdnů: experimentální každý 45 min FES n. peroneus, kontrolní skupina běžná fyzioterapie 3× týdně 45 min
časoprostorové parametry chůze, kinematická analýza chůze, svalová síla, spasticita a rozsah pohybu v kloubech
ve skupině s FES došlo ke zlepšení hybnosti hlezna a kolene a snížení spasticity plantárních flexorů
13
Hsiao et al 2016: Mechanisms used to increase peak propulsive force following 12-weeks of gait training in individuals poststroke.
Journal of Biomechanics
45 osob po CMP
12 týdnů: 3× týdně trénink chůze na treadmil v délce 36 min, 3 skupiny: 1. trénink chůze běžnou rychlostí; 2. trénink rychlé chůze; 3. trénink rychlé chůze v kombinaci s FES n. peroneus
kinematická analýza chůze
ve všech skupinách došlo ke zlepšení parametrů chůze díky zlepšení odrazu, u skupiny s FES výraznější zvýšení momentu pohybu v kotníku
14
Hwang et al 2015: Treadmill training with tilt sensor functional electrical stimulation for improving balance, gait, and muscle architecture of tibialis anterior of survivors with chronic stroke: A randomized controlled trial.
Technology and Health Care
30 osob po CMP (déle než 1 rok)
4 týdny: standardní fyzioterapie a trénink chůze na traedmil 30 min každý den, experimentální skupina při chůzi FES n. peroneus, kontrolní skupina placebo stimulace
10m test rychlosti chůze, Timed Up and Go test, Berg Balance test
v obou skupinách došlo po 4 týdnech ke zlepšení ve vyšetřovaných parametrech, po dalších 4 týdnech při follow-up v experimentální skupině významně lepší výsledky v Timed Up and Go, Berg Balance testu a 10m testu chůze
15
Cheng et al 2010: Effects of combining electric stimulation with active ankle dorsiflexion while standing on a rocker board: a pilot study for subjects with spastic foot after stroke.
Archives of Physical Medicine and Rehabilitation
15 osob po CMP
4 týdny: obě skupiny 3× týdně 30 trénink stoje na úseči a 15 min trénink chůze, v experimentální navíc FES n. peroneus
svalová síla dorzálních flexorů, spasticita plantárních flexorů, časoprostorové parametry chůze, vyšetření rovnováhy na Balance Masteru, modifkovaný Emory Ambulation Profile
v experimentální skupině významné zvýšení rychlosti chůze, zvýšení symetrie kroku, zlepšení v Emory Ambulation Profile, snížení spasticity
16
Cho et al 2015: Treadmill gait training combined with functional electrical stimulation on hip abductor and ankle dorsiflexor muscles for chronic hemiparesis.
Gait and Posture
36 osob po CMP-chronická faze
4 týdny: 20 tréninků chůze na traedmill v závěsu, 1. trénink na traedmilu s FES m. tibialis anterior a m. gluteus medius; 2. trénink na traedmil s FES m.tibialis anterior; 3. pouze chůze na traedmill
rychlost chůze, kadence, délka kroku, svalová síla, Berg Balance test
ve skupině s FES m.tibialis anterior a m. gluteus medius dosáhla nejvýznamnějšího zlepšení rychlosti chůze, kadence, sval. síly a v Berg Balance testu
17
Chung et al 2014: Therapeutic effect of functional electrical stimulation-triggered gait training corresponding gait cycle for stroke.
Gait and Posture
18 osob po CMP
6 týdnů: obě skupiny trénink chůze 5× týdně 30 min, v experimentální navíc FES m. tibialis anterior a m. gluteus medius, kontrolní pouze trénink chůze
rychlost chůze, kadence, délka kroku, svalová síla, Berg Balance test
v experimentální skupině došlo ke zlepšení všech vyšetřovaných parametrů
18
Kluding et al 2013: Foot drop stimulation versus ankle foot orthosis after stroke: 30-week outcomes.
Stroke
196 osob po CMP
30 týdnů: během prvních 6 týdnů 8× individuální trénink chůze, experimentální skupina užívala FES n. peroneus, kontrolní skupina AFO
10m test rychlosti chůze, Timed Up and Go test, 6min test chůze, Fugl-Meyer test, Functional Reach, Berg Balance test
u obou skupin došlo ke zvýšení rychlosti chůze a v testu Timed Up and Go
19
Knutson et al 2013: Contralaterally controlled neuromuscular electrical stimulation for recovery of ankle dorsiflexion: a pilot randomized controlled trial in patients with chronic post-stroke hemiplegia.
American Journal of Physical Medicine and Rehabilitation
26 osob po CMP-chronická faze
6 týdnů: trénink chůze na treadmill + domácí stimulace 10× týdně, experimentální skupina FES n. peroneus spouštěná volním pohybem kontralaterální DKK, kontrolní skupina běžná FES n. peroneus
rychlost chůze, Fugl-Meyer test, modifikovaný Emory Ambulation Profile
v obou skupinách došlo ke zlepšení Fugl-Meyer testu a modifikovaný Emory Ambulation Profile
20
Kottink et al 2008: Therapeutic effect of an implantable peroneal nerve stimulator in subjects with chronic stroke and footdrop: a randomized controlled trial. Physical Therapy
29 osob po CMP-chronická faze
26 týdnů: experimentální skupina implentovaná FES stimulace n. peroneus vs. kontrolní běžná AFO ortéza nebo pomůcky pro chůzi
EMG aktivita svalů DKK, rychlost chůze
zlepšení sval aktivity m. tibialis anterior m. gastrocnemius ve skupině s FES, rychlost chůze bez významnější změny
21
Kottink et al 2007: A randomized controlled trial of an implantable 2-channel peroneal nerve stimulator on walking speed and activity in poststroke hemiplegia.
Archives of Physical Medicine and Rehabilitation
29 osob po CMP-chronická faze
26 týdnů: experimentální skupina implentovaná FES stimulace n. peroneus versus kontrolní běžná AFO ortéza nebo pomůcky pro chůzi
10m test rychlosti chůze, 6min test, kinematická analýza chůze
zlepšení rychlosti v 6min i 10m testu chůze s FES
22
Kunkel et al 2013: Functional electrical stimulation with exercises for standing balance and weight transfer in acute stroke patients: a feasibility randomized controlled trial. Neuromodulation Technology at Neural Interface
21 osob po CMP v subakutní fázi
2 týdny (celkem 7 terapií): experimentální skupina balanční trénink s FES m. gluteus maximus a m. quadriceps femoris, kontrolní skupina balanční trénink samotný nebo běžnou péči
10m test rychlosti chůze, symetrie stoje, schopnost přenášet váhu
nedošlo ke zlepšení ve vyšetřovaných parametrech
23
Lairamore et al 2014: Effects of functional electrical stimulation on gait recovery post-neurological injury during inpatient rehabilitation.
Perceptual and Motor Skills
26 osob s foot drop po CMP nebo kraniotraumatu v subakutní fázi (do 30 dnů)
1 týden: standardní rehabilitační program 1,5 h denně 5 dní v týdnu, experimentální skupina navíc 4× týdně 45 min FES n. peroneus, kontrolní skupina placebo stimulace
časoprostorové parametry chůze a EMG aktivita DKK, FIM test
v obou skupinách došlo ke zvýšení rychlosti chůze, zlepšení v testu FIM, zvýšení EMG aktivity dorzálních flexorů během švihové fáze kroku
24
Leung et al 2014: Standing with electrical stimulation and splinting is no better than standing alone for management of ankle plantarflexion contractures in people with traumatic brain injury: a randomised trial. Journal of Physiotherapy
36 osob po traumatickém poškození mozku
6 týdnů: experimentální skupina stoj ve vertikalizačním stojanu s FES dorzálních flexorů 30 min 5× týdně, plus dlahování 12 h denně, kontrolní skupina pouze stoj ve vertikalizačním stojanu
pasivní rozsah dorzální flexe hlezna, spasticita plantárních flexorů, FIM test, rychlost chůze
u obou skupin došlo k nesignifikantnímu zlepšení
25
Mesci et al 2009: The effects of neuromuscular electrical stimulation on clinical improvement in hemiplegic lower extremity rehabilitation in chronic stroke: a single-blind, randomised, controlled trial.
Disability and Rehabilitation
40 osob po CMP v chronickém stadiu
4 týdenní rehabilitační program, experimentální skupina navíc FES dorzálních flexorů 5 dní v týdnů
FIM test, funkční ambulantní profil, Rivermead skore pro DK a trup, Brunnstrom status
v experimentální skupině došlo ke zlepšení dorzální flexe a snížení spasticity, funkční mobilita se zlepšila v obou skupinách
26
Morone et al 2012: Walking training with foot drop stimulator controlled by a tilt sensor to improve walking outcomes: a randomized controlled pilot study in patients with stroke in subacute phase. Stroke Research and Treatment
20 osob po CMP
4 týdny: 20 terapií, 5× týdně v délce 40 min, experimentální skupina trénink chůze s FES n. peroneus, kontrolní skupina trénink chůze s AFO
10m test rychlosti chůze, Rivermead mobility index, svalová síla, ashwortova škála, funkční ambulanční skóre
v experimentální skupině došlo ke zvýšení rychlosti chůze a zlepšení funkční mobility
27
Ng et al 2008: A pilot study of randomized clinical controlled trial of gait training in subacute stroke patients with partial body-weight support electromechanical gait trainer and functional electrical stimulation: six-month follow-up.
Stroke
54 osob po CMP-subakutní fáze
4 týdny: účastníci měli každý den komplexní rehabilitační léčbu po CMP v kombinaci s tréninkem chůze 5 dní v týdnu 20 min denně 1. běžný trénink chůze; 2. chůze na treadmill s podporou váhy těla a podporou symetrie kroku; 3. chůze na traedmil s FES n. peroneus a podporou váhy těla
FIM test, Barthel test, Motricity index, Elderly mobility scale, Berg Balance test, rychlost chůze na 5 m, kategorie funkční mobility
trénink chůze na traedmil bez i s FES byl efektivnější pro zvýšení rychlosti chůze a zlepšení funkční mobility než běžný trénink chůze
28
Peurala et al 2005: The effectiveness of body weight-supported gait training and floor walking in patients with chronic stroke.
Archives of Physical Medicine and Rehabilitation
45 osob po CMP-chronická
3 týdny: účastníci měli každý den komplexní rehabilitační léčbu v kombinaci s tréninkem chůze 5 dní v týdnu 20 min denně 1. běžný trénink chůze na treadmill; 2. chůze na treadmill s podporou váhy těla a podporou symetrie kroku; 3. chůze na traedmil s FES n.peroneus a podporou váhy těla
10m test rychlosti chůze, svalová síla a spasticita DKK, test posturálních výchylek, modifikovaný Motor Assessment Scale, FIM test
ke zlepšení chůze v 10m testu, 6min testu, modifikovaný Motor Assessment, testu posturálních výchylek došlo ve všech 3 skupinách, bez signifkantního rozdílu mezi jednotlivými skupinami
29
Sabut et al 2010: Restoration of gait and motor recovery by functional electrical stimulation therapy in persons with stroke.
Disability and Rehabilitation
30 osob nejméně 3 měsíce po CMP
12 týdnů: běžná rehabilitace a v experimentální skupině plus 60 min FES m. tibialis anterior 5 dní v týdnu
rychlost chůze, kadence, délka kroku a fyziologické náročnost chůze, EMG aktivita m. tibialis anterior, rozsah pohybu kotníku, Fugl-Meyer test
FES skupina dosáhla většího zlepšení rychlosti chůze, zvýšení kadence a délky kroku, snížení fyziologické náročnosti chůze, zvýšení rozsahu pohybu v kotníku a zlepšení Fugl-Meyer test
30
Sabut et al 2011: Functional electrical stimulation of dorsiflexor muscle: effects on dorsiflexor strength, plantarflexor spasticity, and motor recovery in stroke patients.
Neurorehabilitation
51 osob po CMP
12 týdnů: běžná fyzioterapie 1 h denně, 5 dnů v týdnu + v experimentální skupině FES n. peroneus
modifikovaná ashworthova škála, svalová síla dorzálních flexorů, aktivní a pasivní rozsah pohybu, Fugl-Meyer test
snížení spasticity plantárních flexorů v obou skupinách, zvýšení svalové síly a rozsahu pohybu
v experimentální skupině bylo zlepšení ve všech parametrech výraznější
31
Salisbury et al 2013: A feasibility study to investigate the clinical application of functional electrical stimulation (FES), for dropped foot, during the sub-acute phase of stroke - A randomized controlled trial. Physiotherapy Theory and Practice
16 osob po CMP-subakutní stadium
12 týdnů: reedukace chůze, experimentální skupina s FES n. peroenus, kontrolní s AFO
rychlost chůze, kadence, funkční ambulatní klasifikace, subjektivní hodnocení chůze-vizuální analogová škála
neprokázaly se signif.změny, studie potvrdila proveditelnost studie s oběmi typy pomůcek
32
Sharif et al 2017: Effectiveness of Functional Electrical Stimulation (FES) versus Conventional Electrical Stimulation in Gait Rehabilitation of Patients with Stroke. Journal of the College of Physicians and Surgeon Pakistan
38 osob po CMP
6 týdnů: obě skupiny standartní rehabilitace 5 dnů v týdnu-experimenátlní FES n. peroneus, kontrolní skupina TENS stimulace
modifikovaná ashworthova škála, Fugl-Meyer test, Berg Balance test, Dynamic Gait Index, Timed Up and Go test
ve skupině FES sifnifikantní zlepšení ve všech vyšetřovaných testech
33
Sheffeler et al 2013: Randomized controlled trial of surface peroneal nerve stimulation for motor relearning in lower limb hemiparesis.
Archives of Physical Medicine and Rehabilitation
110 osob po CMP –déle než 12 měsíců
12 týdnů: experimentální skupina chodila FES n. peroneus versus a kontrolní s běžnou AFO ortézou
Fugl-Meyer test, modifikovaný Emory funkční ambulantní profil a kvalita života
obě skupiny se signifikantně zlepšily ve funkční mobilitě a kvalitě života během terapie, zlepšení přetrvalo i po 6 měsících follow-up
34
Sheffeler et al 2015: Surface peroneal nerve stimulation in lower limb hemiparesis: effect on quantitative gait parameters. American Journal of Physical Medicine and Rehabilitation
110 osob po CMP –déle než 12 měsíců
12 týdnů: experimentální skupina chodila FES n. peroneus versus a kontrolní s běžnou AFO ortézou
kinetické, kinematické a časoprostorové parametry chůze
v obou skupinách dožlo ke zlepšení síly kyčelního kloubu v předšvihové fázi kroku a síly kotníku při odrazu, které se projevilo jako zlepšení kadence, délky kroku a rychlosti chůze
35
Solopova et al 2011: Assisted leg displacements and progressive loading by a tilt table combined with FES promote gait recovery in acute stroke.
Neurorehabilitation
61 osob po subakutní CMP
2 týdny: obě skupiny konvenční rehabilitace po CMP, experimentální-FES 30 min denně 5 dní v týdnu spojené s robotickým tréninkem kroku
Fugl-Meyer test, 10m test rychlosti chůze, maximální izometrická svalová kontrakce, EMG aktivita svalů DKK
v experimentální skupině došlo k výraznějšímu zlepšení max. svalové kontrakce, EMG aktivity svalů DKK a funkční mobility
36
Tan et al 2014: The effectiveness of functional electrical stimulation based on a normal gait pattern on subjects with early stroke: a randomized controlled trial.
BioMed Research International
45 osob po CMP
3 týdny: konveční rehabilitace po CMP plus stimulace denně 30 min, 5 dní v týdnu, srovnání 3 skupin: skupina 4 kanálové FES stimulace-n. peroneus a svaly stehna, skupina 2 kanálové FES stimulace n. peroneus a kontrolní placebo skupina
Fugl-Meyer test, Berg Balance test, modifikovaný Barthel Index, posturální vyšetření a funkční ambulanční kategorie
ve všech 3 skupinách došlo ke signif.zlepšení ve všech testech, přičemž ve skupině 4 kanálové stimulace bylo zlepšení nejvyšší
37
Tanovic et al 2009: Effects of functional electrical stimulation in rehabilitation with hemiparesis patients.
Bosnian Journal of Basic Medical Science
40 osob s hemiparézou po 4–8 týdnů CMP
4 týdny: obě skupiny kinezioterapie, v experimentální navíc FES n.p eroneus 15 min denně 5 dní v týdnu
BI index, RAP index
v experimentální skupině výraznější zlepšení funkční mobiity
38
Taylor et al 2014: A feasibility study to investigate the effect of functional electrical stimulation and physiotherapy exercise on the quality of gait of people with multiple sclerosis.
Neuromodulation Technology at the Neural Interface
28 osob s progresivní RS
24 týdnů: experimentální skupina FES n. peroneus – první 6 týdnů pouze FES n. pereoneus; týden 6–12 přidána stimulace m. gluteus maximus; týden 12–24 přidáno cvičení na stabilitu trupu; kontrolní skupina pouze cvičení, FES n. peroneus přidána od 12. týdne, stimulace m. gluteus přidána od 18. týdne
Rivermead Observational Gait Analysis, 10m test chůze, deník pádů, MSIS-29
po FES došlo ke zlepšení chůze a kvality života (měřené MSIS 29), také došlo ke snížení počtu pádů, přidáním fyzioterapeutických cvičení se zvýšil efekt i když efekt FES byl významnější
39
Tong et al 2006: Effectiveness of gait training using an electromechanical gait trainer, with and without functional electric stimulation, in subacute stroke: a randomized controlled trial.
Archives of Physical Medicine and Rehabilitation
46 osob po CMP-subakutní
4 týdny: účastníci měli každý den komplexní rehabilitační léčbu po CMP v kombinaci s tréninkem chůze 5 dní v týdnu 20 min denně 1. běžný trénink chůze na treadmill; 2. chůze na treadmill s podporou váhy těla a podporou symetrie kroku; 3. chůze na traedmil s FES n.peroneus a podporou váhy těla
5m test chůze, motricity index
signifikantní zlepšení u obou skupin s podporou váhy těla bez FES i s FES
40
Wilkinson et al 2014: A randomised controlled trial of integrated electrical stimulation and physiotherapy to improve mobility for people less than 6 months post stroke.
Disability and Rehabilitation
20 osob po CMP
12 týdnů: experimentální skupina fyzioterapie a FES n. peroneus, kontrolní skupina pouze fyzioterapie
Rivermead Mobility index, Canadian Occupational Performance measure, 10m test chůze
u skupiny s FES došlo k signif. zvýšení rychlosti chůze
41
Yan et al 2005: Functional electrical stimulation improves motor recovery of the lower extremity and walking ability of subjects with first acute stroke: a randomized placebo-controlled trial.
Stroke
46 osob po akutní CMP (do 14 týdnů)
3 týdny: standardní rehabilitace po CMP 1. plus FES n. peroneus; 2. plus placebo stimulace; 3. pouze rehabilitace
kompozitní spasticity skóre, maximální izometrická volní kontrakce svalů dorzálních a plantárních flexorů, Timed Up and Go test
skupina FES se standardní rehabilitací se výrazně zlepšila v chůzi a více probandů z této skupiny mohlo být propuštěno domů, došlo ke zvýšení síly dorzálních flexorů, snížení kompozitního spasticity skóre
42
You et al 2014: Functional electrical stimulation early after stroke improves lower limb motor function and ability in activities of daily living.
Neurorehabilitation
37 osob po akutní CMP
3 týdny: obě skupiny konvenční fyzioterapie a ergoterapie po CMP, experimentální plus FES n. peroneus 30 min denně 5 dní v týdnů
kompozitní spasticity skóre, Fulg-Meyer test, posturální vyšetření, Berg Balance test a modifikovaný Barthel Index
FES skupina dosáhla sig.snížení kompozitního spasticity skóre a zlepšení ve Fugl-Meyer testu, Barther Index a testu posturální stability
Limity naší analýzy
Vzhledem k tomu, že se jednotlivé analyzované studie velmi lišily svou délkou i intenzitou terapie, je obtížné vyvozovat obecné závěry. Přesto jsme přesvědčeni, že tento přehled může pomoci rehabilitačním lékařům a fyzioterapeutům v klinické praxi. Z metodologického hlediska je limitem většiny studií nedostatečné zaslepení, ať již se jednalo o pacienty zapojené do studie nebo rehabilitační pracovníky provádějící terapii nebo vyšetření. Zaslepení není proveditelné vzhledem k povaze intervence – v zásadě není možné uspokojivě maskovat senzitivní vjem průchodu elektrického proudu s vyvoláním kontrakce svalů anterolaterální skupiny bérce, který se má při chůzi manifestovat zjevným pohybem v hlezenním kloubu. Některé ze studií uvádějí alespoň částečné zaslepení, kdy pacienti ani vyšetřující v okamžiku vstupního vyšetření neznali přiřazení do skupin [47] nebo kdy vyšetřující při výstupním vyšetření neznali přiřazení pacienta do skupiny [17,19].
Závěr
Na základě dostupných studií využívajících FES pro zlepšení funkce dolních končetin se zdá, že FES může představovat obohacení tradičních terapeutických postupů (jako jsou cvičení na neurofyziologickém podkladě, trénink chůze a stability). V některých případech pak může vést k výraznějšímu zlepšení funkčního stavu než tradiční terapie s využitím peroneálního ortézování. I v řadě studií, které neprokázaly lepší efekt FES oproti peroneálnímu ortézování, je nicméně popisována významně vyšší preference uživatelů k FES. Proto je důležité, aby byl efekt pomůcky objektivně dokumentován a individuální přínos této dražší pomůcky zvážen vzhledem k funkčnímu stavu pacienta. FES je pak možné aplikovat v rámci pobytové rehabilitační léčby (krátkodobě) nebo jako indivuální kompenzační pomůcku (dlouhodobě).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Studie byla podpořena z grantu Progress Q2/ LF 1.
Mgr. Klára Novotná
Neurologická klinika
a Centrum klinických neurověd
1. LF UK a VFN
Kateřinská 468/30
120 00 Praha Nové Město
e-mail: novotna.klara.k@gmail.com
Přijato k recenzi: 5. 6. 2019
Přijato do tisku: 13. 9. 2019
Zdroje
1. Liberson WT, Holmquest HJ, Scot D et al. Functional electrotherapy: stimulation of the peroneal nerve synchronized with the swing phase of the gait of hemiplegic patients. Arch Phys Med Rehab 1961; 42 : 101 – 105.
2. Peckham PH, Knutson JS. Functional electrical stimulation for neuromuscular applications. Annu Rev Biomed Eng 2005; 7 : 327 – 360. doi: 10.1146/ annurev.bioeng.6.040803.140103.
3. Votava J. Rehabilitace osob po cévní mozkové příhodě. Neurol praxi 2001; 4 : 184 – 189.
4. Cameron MH. The walkaide® functional electrical stimulation system – a novel therapeutic approach for foot drop in central nervous system disorders. Europ Nerologic Rev 2010; 5(2): 18 – 20. doi: http:/ / doi.org/ 10.17925/ ENR.2010.05.02.18.
5. Knutson JS, Harley MY, Hisel TZ et al. Contralaterally controlled functional electrical stimulation for recovery of elbow extension and hand opening after stroke: a pilot case series study. Am J Phys Med Rehab 2014; 93(6): 528 – 539. doi: 10.1097/ PHM.0000000000000066.
6. Maher CG, Sherrington C, Herbert RD et al. Reliability of the PEDro scale for rating quality of randomized controlled trials. Phys Ther 2003; 83(8): 713 – 721.
7. Chung Y, Kim JH, Cha Y et al. Therapeutic effect of functional electrical stimulation-triggered gait training corresponding gait cycle for stroke. Gait Posture 2014; 40(3): 471 – 475. doi: 10.1016/ j.gaitpost.2014.06.002.
8. Rosenkranz K, Rothwell JC. The effect of sensory input and attention on the sensorimotor organization of the hand area of the human motor cortex. J Physiol 2004; 561(Pt 1): 307 – 320. doi: 10.1113/ jphysiol.2004.069328.
9. Cheng JS, Yang YR, Cheng SJ et al. Effects of combining electric stimulation with active ankle dorsiflexion while standing on a rocker board: a pilot study for subjects with spastic foot after stroke. Arch Phys Med Rehab 2010; 91(4): 505 – 512. doi: 10.1016/ j.apmr.2009.11.022.
10. Gál O, Hoskovcová M, Jech R. Neuroplasticita, restituce motorických funkcí a možnosti rehabilitace spastické parézy. Rehab fyz Lék 2015; 22(3): 101 – 127.
11. Sabut SK, Sikdar C, Kumar R et al. Functional electrical stimulation of dorsiflexor muscle: effects on dorsiflexor strength, plantarflexor spasticity, and motor recovery in stroke patients. NeuroRehabilitation 2011; 29(4): 393 – 400. doi: 10.3233/ NRE-2011-0717.
12. Esnouf JE, Taylor PN, Mann GE et al. Impact on activities of daily living using a functional electrical stimulation device to improve dropped foot in people with multiple sclerosis, measured by the Canadian Occupational Performance Measure. Mult Scler 2010; 16(9): 1141 – 1147. doi: 10.1177/ 1352458510366013.
13. Leung J, Harvey LA, Moseley AM et al. Standing with electrical stimulation and splinting is no better than standing alone for management of ankle plantarflexion contractures in people with traumatic brain injury: a randomised trial. J Physiother 2014; 60(4): 201 – 208. doi: 10.1016/ j.jphys.2014.09.007.
14. Tong RK, Ng MF, Li LS et al. Gait training of patients after stroke using an electromechanical gait trainer combined with simultaneous functional electrical stimulation. Phys Ther 2006; 86(9): 1282 – 1294. doi: 10.2522/ ptj.20050183.
15. Ng MF, Tong RK, Li LS. A pilot study of randomized clinical controlled trial of gait training in subacute stroke patients with partial body-weight support electromechanical gait trainer and functional electrical stimulation: six-month follow-up. Stroke 2008; 39(1): 154 – 160. doi: 10.1161/ STROKEAHA.107.495705.
16. Daly JJ, Zimbelman J, Roenigk KL et al. Recovery of coordinated gait: randomized controlled stroke trial of functional electrical stimulation (FES) versus no FES, with weight-supported treadmill and over-ground training. Neurorehabil Neural Repair 2011; 25(7): 588 – 596. doi: 10.1177/ 1545968311400092.
17. Kluding PM, Dunning K, O’Dell MW et al. Foot drop stimulation versus ankle foot orthosis after stroke: 30-week outcomes. Stroke 2013; 44(6): 1660 – 1669. doi: 10.1161/ STROKEAHA.111.000334.
18. Everaert DG, Stein RB, Abrams GM et al. Effect of a foot-drop stimulator and ankle-foot orthosis on walking performance after stroke: a multicenter randomized controlled trial. Neurorehabil Neural Repair 2013; 27(7): 579 – 591. doi: 10.1177/ 1545968313481278.
19. Sabut SK, Sikdar C, Mondal R et al. Restoration of gait and motor recovery by functional electrical stimulation therapy in persons with stroke. Disabil Rehabil 2010; 32(19): 1594 – 1603. doi: 10.3109/ 09638281003599596.
20. Bethoux F, Rogers HL, Nolan KJ et al. Long-term follow-up to a randomized controlled trial comparing peroneal nerve functional electrical stimulation to an ankle foot orthosis for patients with chronic stroke. Neurorehabil Neural Repair 2015; 29(10): 911 – 922. doi: 10.1177/ 1545968315570325.
21. Prenton S, Hollands KL, Kenney LP et al. Functional electrical stimulation and ankle foot orthoses provide equivalent therapeutic effects on foot drop: a meta--analysis providing direction for future research. J Rehabil Med 2018; 50(2): 129 – 139. doi: 10.2340/ 16501977-2289.
22. Embrey DG, Holtz SL, Alon G et al. Functional electrical stimulation to dorsiflexors and plantar flexors during gait to improve walking in adults with chronic hemiplegia. Arch Phys Med Rehabil 2010; 91(5): 687 – 696. doi: 10.1016/ j.apmr.2009.12.024.
23. Peurala SH, Tarkka IM, Pitkanen K et al. The effectiveness of body weight-supported gait training and floor walking in patients with chronic stroke. Arch Phys Med Rehabil 2005; 86(8): 1557 – 1564. doi: 10.1016/ j.apmr.2005.02.005.
24. Sheffler LR, Bailey SN, Wilson RD et al. Spatiotemporal, kinematic, and kinetic effects of a peroneal nerve stimulator versus an ankle foot orthosis in hemiparetic gait. Neurorehabil Neural Repair 2013; 27(5): 403 – 410. doi: 10.1177/ 1545968312465897.
25. Cho MK, Kim JH, Chung Y et al. Treadmill gait training combined with functional electrical stimulation on hip abductor and ankle dorsiflexor muscles for chronic hemiparesis. Gait Posture 2015; 42(1): 73 – 78. doi: 10.1016/ j.gaitpost.2015.04.009.
26. Kottink AI, Hermens HJ, Nene AV et al. Therapeutic effect of an implantable peroneal nerve stimulator in subjects with chronic stroke and footdrop: a randomized controlled trial. Phys Ther 2008; 88(4): 437 – 448. doi: 10.2522/ ptj.20070035.
27. Mesci N, Ozdemir F, Kabayel DD et al. The effects of neuromuscular electrical stimulation on clinical improvement in hemiplegic lower extremity rehabilitation in chronic stroke: a single-blind, randomised, controlled trial. Disabil Rehabil 2009; 31(24): 2047 – 2054. doi: 10.3109/ 09638280902893626.
28. Solopova I, Tihonova D, Grishin A et al. Assisted leg displacements and progressive loading by a tilt table combined with FES promote gait recovery in acute stroke. NeuroRehabilitation 2011; 29(1): 67 – 77. doi: 10.3233/ NRE-2011-0679.
29. Yan T, Hui-Chan CW, Li LS. Functional electrical stimulation improves motor recovery of the lower extremity and walking ability of subjects with first acute stroke: a randomized placebo-controlled trial. Stroke 2005; 36(1): 80 – 85. doi: 10.1161/ 01.STR.0000149623.24906.63.
30. Ghédira M, Albertsen IM, Mardale V et al. Wireless, accelerometry-triggered functional electrical stimulation of the peroneal nerve in spastic paresis: a randomized, controlled pilot study. Assist Technol 2017; 29(2): 99 – 105. doi: 10.1080/ 10400435.2016.1214933.
31. Sharif F, Ghulam S, Malik AN et al. Effectiveness of functional electrical stimulation (FES) versus conventional electrical stimulation in gait rehabilitation of patients with stroke. J Coll Physicians Surg Pak 2017; 27(11): 703 – 706. doi: 2747.
32. Charlton CS, Ridding MC, Thompson PD et al. Prolonged peripheral nerve stimulation induces persistent changes in excitability of human motor cortex. J Neurol Sci 2003; 208(1 – 2): 79 – 85. doi: 10.1016/ s0022-510x(02)00443-4.
33. Meesen RL, Cuypers K, Rothwell JC et al. The effect of long-term TENS on persistent neuroplastic changes in the human cerebral cortex. Hum Brain Mapp 2011; 32(6): 872 – 882. doi: 10.1002/ hbm.21075.
34. Hara Y. Brain plasticity and rehabilitation in stroke patients. J Nippon Med Sch 2015; 82(1): 4 – 13. doi: 10.1272/ jnms.82.4.
35. Merkel C, Hausmann J, Hopf JM et al. Active prosthesis dependent functional cortical reorganization following stroke. Sci Rep 2017; 7(1): 8680. doi: 10.1038/ s41598-017-09325-8.
36. Meimoun M, Bayle N, Baude M et al. Intensity in the neurorehabilitation of spastic paresis. Rev Neurol (Paris) 2015; 171(2): 130 – 140. doi: 10.1016/ j.neurol.2014.09.011.
37. Gandolla M, Ward NS, Molteni F et al. The neural correlates of long-term carryover following functional electrical stimulation for stroke. Neural Plast 2016; 2016 : 4192718. doi: 10.1155/ 2016/ 4192718.
38. Plautz EJ, Milliken GW, Nudo RJ. Effects of repetitive motor training on movement representations in adult squirrel monkeys: role of use versus learning. Neurobiol Learn Mem 2000; 74(1): 27 – 55. doi: 10.1006/ nlme.1999.3934.
39. Nudo RJ, Milliken GW, Jenkins WM et al. Use-dependent alterations of movement representations in primary motor cortex of adult squirrel monkeys. J Neurosci 1996; 16(2): 785 – 807.
40. Kimberley TJ, Samargia S, Moore LG et al. Comparison of amounts and types of practice during rehabilitation for traumatic brain injury and stroke. J Rehabil Res Dev 2010; 47(9): 851 – 862.
41. Bulley C, Mercer TH, Hooper JE et al. Experiences of functional electrical stimulation (FES) and ankle foot orthoses (AFOs) for foot-drop in people with multiple sclerosis. Disabil Rehabil Assist Technol 2015; 10(6): 458 – 467. doi: 10.3109/ 17483107.2014.913713.
42. Bulley C, Shiels J, Wilkie K et al. User experiences, preferences and choices relating to functional electrical stimulation and ankle foot orthoses for foot-drop after stroke. Physiotherapy 2011; 97(3): 226 – 233. doi: 10.1016/ j.physio.2010.11.001.
43. Lairamore CI, Garrison MK, Bourgeon L et al. Lower Extremity functional electrical stimulation during inpatient rehabilitation: a pilot study investigating gait and muscle activity in persons with stroke or brain injury. Percept Mot Skills 2014; 119(2): 591 – 608. doi: 10.2466/ 15.25.PMS.119c19z5.
44. Kunkel D, Pickering RM, Burnett M et al. Functional electrical stimulation with exercises for standing balance and weight transfer in acute stroke patients: a feasibility randomized controlled trial. Neuromodulation 2013; 16(2): 168 – 177. doi: 10.1111/ j.1525-1403.2012.00488.x.
45. Aaron SE, Vanderwerker CJ, Embry AE et al. FES-assisted cycling improves aerobic capacity and locomotor function postcerebrovascular accident. Med Sci Sports Exerc 2018; 50(3): 400 – 406. doi: 10.1249/ MSS.0000000000001457.
46. Peri E, Ambrosini E, Pedrocchi A et al. Can FES-augmented active cycling training improve locomotion in post-acute elderly stroke patients? Eur J Transl Myol 2016; 26(3): 6063. doi: 10.4081/ ejtm.2016.6063.
47. Wilkinson IA, Burridge J, Strike P et al. A randomised controlled trial of integrated electrical stimulation and physiotherapy to improve mobility for people less than 6 months post stroke. Disabil Rehabil Assist Technol 2015; 10(6): 468 – 474. doi: 10.3109/ 17483107.2014.917125.
48. O‘Dell MW, Dunning K, Kluding P et al. Response and prediction of improvement in gait speed from functional electrical stimulation in persons with poststroke drop foot. PM R 2014; 6(7): 587 – 601. doi: 10.1016/ j.pmrj.2014.01.001.
49. Sota K, Uchiyama Y, Ochi M et al. Examination of factors related to the effect of improving gait speed with functional electrical stimulation intervention for stroke patients. PM R 2018; 10(8): 798 – 805. doi: 10.1016/ j.pmrj.2018.02.012.
50. Taylor PN, Burridge JH, Dunkerley AL et al. Clinical use of the Odstock dropped foot stimulator: its effect on the speed and effort of walking. Arch Phys Med Rehabil 1999; 80(12): 1577 – 1583. doi: 10.1016/ s0003-9993(99)90333-7.
51. van Swigchem R, van Duijnhoven HJ, den Boer J et al. Effect of peroneal electrical stimulation versus an ankle-foot orthosis on obstacle avoidance ability in people with stroke-related foot drop. Phys Ther 2012; 92(3): 398 – 406. doi: 10.2522/ ptj.20100405.
52. Wilkie KM, Shiels JE, Bulley C et al. „Functional electrical stimulation (FES) impacted on important aspects of my life“: a qualitative exploration of chronic stroke patients‘ and carers‘ perceptions of FES in the management of dropped foot. Physiother Theory Pract 2012; 28(1): 1 – 9. doi: 10.3109/ 09593985.2011.563775.
53. Taylor P, Humphreys L, Swain I. The long-term cost-effectiveness of the use of Functional Electrical Stimulation for the correction of dropped foot due to upper motor neuron lesion. J Rehabil Med 2013; 45(2): 154 – 160. doi: 10.2340/ 16501977-1090.
54. Barrett C, Taylor P. The effects of the odstock drop foot stimulator on perceived quality of life for people with stroke and multiple sclerosis. Neuromodulation 2010; 13(1): 58 – 64. doi: 10.1111/ j.1525-1403.2009.00250.x.
Štítky
Dětská neurologie Neurochirurgie Neurologie
Článek vyšel v časopiseČeská a slovenská neurologie a neurochirurgie
Nejčtenější tento týden
2019 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Magnosolv a jeho využití v neurologii
- Zolpidem může mít širší spektrum účinků, než jsme se doposud domnívali, a mnohdy i překvapivé
- Nejčastější nežádoucí účinky venlafaxinu během terapie odeznívají
-
Všechny články tohoto čísla
- Střelná poranění mozku
- Predstavujú ticagrelor a prasugrel alternatívu v protidoštičkovej liečbe ischemických CMP? ANO
- Představují tikagrelor a prasugrel alternativu v protidestičkové léčbě ischemických CMP? NE
- Predstavujú ticagrelor a prasugrel alternatívu v protidoštičkovej liečbe ischemických CMP?
- Klinické syndromy z oblasti cervikálního plexu
- Neurorehabilitace poruch chůze s využitím funkční elektrické stimulace – aktuální poznatky z randomizovaných klinických studií
- Úskalí při respektování autonomie u pacientů s Parkinsonovou nemocí
- Současný management pacientů s degenerativní kompresí krční míchy
- Krvácení do aterosklerotického plátu u symptomatické a asymptomatické progredující stenózy vnitřní karotidy – pilotní studie
- Porovnání perioperačního měření tlaku ve vaku aneuryzmatu a v mateřské tepně u prasklých a neprasklých aneuryzmat
- Významné rizikové faktory pádu v osobnej anamnéze u hospitalizovaných pacientov s neurologickým ochorením
- Systematická analýza klinické efektivity stabilizace sakroiliakálního skloubení v rámci terapie bolestí zad
- Spinální meningiomy – 92 pacientů operovaných na našem pracovišti
- Civilní a válečná střelná poranění hlavy
- Mění se při Parkinsonově nemoci tloušťka cévnatky?
- Epidurální aplikace kortikoidů Část 1 – Profil pacientů před aplikací
- Chirurgická terapie oboustranné farmakorezistentní Menièrovy choroby
- Mechanická trombektómia v liečbe akútnej ischemickej cievnej mozgovej príhody v detskom veku
- Konzervativní management prasklé Galassi III arachnoideální cysty střední jámy lební
- Rekonstrukce lícního nervu štěpem z nervus auricularis magnus při resekci recidivujícího bazaliomu parotideomasseterické krajiny
- Doporučení pro mechanickou trombektomii akutního mozkového infarktu – verze 2019
- Analýza dat v neurologii LXXVIII. Směsné míry korelace u vícerozměrných souborů kvantitativních a kvalitativních dat
- Osmdesátiny doc. MU Dr. Jiřího Bauera, CSc.
- Doc. MU Dr. Eugen Eiben, CSc.
- Recenze knih
- Česká a slovenská neurologie a neurochirurgie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Klinické syndromy z oblasti cervikálního plexu
- Doporučení pro mechanickou trombektomii akutního mozkového infarktu – verze 2019
- Mechanická trombektómia v liečbe akútnej ischemickej cievnej mozgovej príhody v detskom veku
- Střelná poranění mozku
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



