-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Vývoj postupů v léčbě akutního selhání jater
Development of procedures for the treatment of acute liver failure
During the last decade there have been many changes in how we care for patients with acute liver failure which provides them with a better chance of survival. With improved diagnostic capacities the cause of disease can be diagnosed more frequently than previously. It is important to determine the prognosis and to implement a specific therapy. Improvement in the overall management of patients in intensive care (intracranial pressure monitoring, prevention and treatment of early signs of intracranial hypertension, therapeutic hypothermia, microbiological monitoring and prophylaxis, modalities of renal replacement therapy), development of surgical techniques and perioperative care are the factors that have led to improved survival after an urgent liver transplantation for acute liver failure. Despite many improvements in the care of the patients with acute liver failure, mortality without liver transplantation is still high. Therefore, better understanding of the pathogenesis of acute liver failure and providing effective supportive therapy remains a core issue.
Key words:
acute liver failure – liver transplantation – intensive care
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
4. 9. 2013Accepted:
2. 10. 2013
Autoři: E. Kieslichová 1
; M. Ročeň 1; S. Fraňková 2
Působiště autorů: Klinika anesteziologie, resuscitace a intenzivní péče, IKEM, Praha 1; Klinika hepatogastroenterologie, IKEM, Praha 2
Vyšlo v časopise: Gastroent Hepatol 2013; 67(5): 426-430
Kategorie: Hepatologie: přehledová práce
Souhrn
V průběhu posledních desetiletí došlo k řadě změn v péči o pacienty s akutním selháním jater (ASJ), které jim dávají větší šanci na přežití. Díky lepším diagnostickým možnostem je častěji než dříve diagnostikována příčina onemocnění, což je důležité při určování prognózy i pro zavedení specifické terapie. Zlepšení celkového managementu pacientů v intenzivní péči (monitorace nitrolebního tlaku, prevence a léčba časných známek intrakraniální hypertenze, terapeutická hypotermie, mikrobiologické sledování a profylaxe, modality náhrady funkce ledvin), vývoj chirurgických technik a perioperační péče, jsou faktory, které vedly ke zlepšenému přežívání pacientů s urgentní transplantací jater pro akutní selhání. Přes pokroky v péči o pacienty s ASJ je míra přežití bez transplantace jater nízká. Nadále tak zůstává středem zájmu snaha o lepší porozumění patogeneze akutního selhání jater a vytvoření protokolu účinné podpůrné terapie.
Klíčová slova:
akutní selhání jater – transplantace jater – intenzivní péčeAkutní selhání jater (ASJ) je rychle progredující, život ohrožující onemocnění s vysokou mortalitou, provázené encefalopatií, koagulopatií a ikterem. Vyskytuje se řídce s incidencí cca šest případů na milion obyvatel ročně. Rozvíjí se během dnů až týdnů u jedinců bez předchozího onemocnění jater. Ztráta jaterních funkcí je spouštěcím impulzem multiorgánového selhání. Pacienti s ASJ umírají v důsledku nitrolební hypertenze nebo multiorgánové dysfunkce. ASJ je spojeno s masivní nekrózou hepatocytů, k níž dochází působením řady hepatotropních i extrahepatálních inzultů. Infekce viry hepatitid, intoxikace paracetamolem a idiosynkratické lékové reakce patří k nejčastějším příčinám ASJ. Pro většinu pacientů s ASJ představuje jedinou šanci na přežití urgentně provedená transplantace jater. Mnozí pacienti však zemřou dříve, než se transplantace dočkají.
V současnosti jsou k dispozici komplexní protokoly pro jednotky intenzivní péče (JIP) a urgentní transplantace jater, nicméně vzhledem k vzácnosti a závažnosti tohoto onemocnění je jeho komplexní studium obtížné a možnosti doporučení založených na důkazech omezené [1,2]. V rámci kontrolovaných klinických studií bylo hodnoceno pouze málo specifických intervencí, přičemž podpůrné intervence a strategie rozhodování vycházely z analýzy anamnestických údajů spolu s extrapolací z jiných kritických onemocnění [3].
Příčiny ASJ
Profil ASJ se postupem času měnil. Vliv měly iniciativy v oblasti péče o zdraví veřejnosti, díky nimž došlo k omezení incidence akutní virové hepatitidy, a také určitá omezení dostupnosti hepatotoxické medikace, např. omezení dostupnosti paracetamolu ve Velké Británii.
V posledních letech zůstávají celosvětově nejčastější příčinou ASJ virové hepatitidy, v USA a Evropě je dominující příčinou intoxikace paracetamolem a idiosynkratické lékové reakce. Díky zlepšení diagnostiky je postupně zaznamenáván snižující se podíl ASJ s nevyjasněnou etiologií [4].
Vývoj péče o pacienty s ASJ
V průběhu uplynulých čtyř desetiletí došlo k významným změnám v přístupu k péči o pacienty s ASJ. Jedná se o zavedení urgentní transplantace jater do terapie ASJ, vývoj postupů komplexní intenzivní a perioperační péče a moderní imunosupresivní protokoly.
Je-li diagnostikováno ASJ, je třeba neprodleně zahájit podpůrnou, v některých případech i specifickou terapii (tab. 1) a zvažovat transplantaci jater.
Tab. 1. Specifická terapie ASJ. Tab. 1. Specific therapy for ALF. 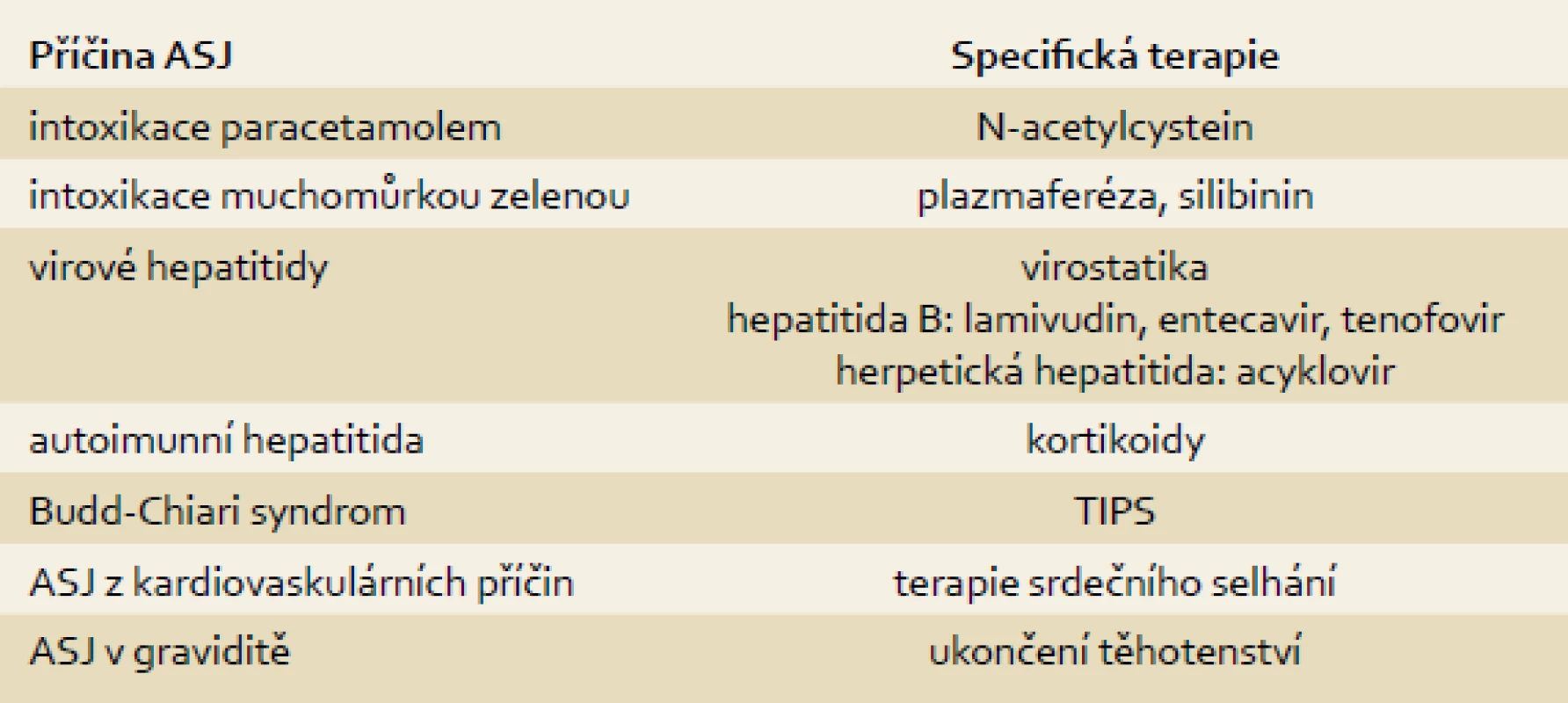
Podpůrná terapie zahrnuje resuscitaci oběhu, péči zaměřenou na respirační systém, podporu/náhradu funkce ledvin, prevenci a terapii nitrolební hypertenze, výživu, profylaxi infekce a profylaxi stresového vředu. Dříve často paušálně prováděná korekce koagulopatie je v současnosti indikována pouze výběrově jako příprava před invazivními procedurami nebo při krvácení.
Součástí podpůrné terapie ASJ se stalo podávání N-acetylcysteinu, a to pro jeho antioxidační účinky, které mohou bránit zánětlivé reakci na oxidativní poškození, což má příznivý vliv na mikrocirkulaci [5].
Prevence a terapie nitrolební hypertenze
Nejdůležitějším projevem ASJ, spojeným s nepříznivou prognózou, je encefalopatie a nitrolební hypertenze. Cílem terapie je udržování cerebrálního perfuzního tlaku (CPP) nad 50 mmHg a nitrolebního tlaku (ICP) pod 20 mmHg.
Nitrolební hypertenze byla dlouhou dobu nejobávanější komplikací ASJ a hlavní příčinou úmrtí. Její incidence v čase významně poklesla. Jde zřejmě o následek časnější diagnostiky a prezentace pacientů, aplikace N-acetylcysteinu, managementu tekutin, antibiotické terapie a náhrady funkce ledvin.
Všichni pacienti, u nichž došlo k rozvoji ASJ se zjevnou encefalopatií, by měli být intubováni a napojeni na umělou plicní ventilaci. V průběhu posledních 10 let je podávána pacientům s ASJ infuze roztoku hypertonického natria (10% NaCl) jako prevence a terapie edému mozku. Terapeutická hypotermie (32–34 °C) snižuje metabolický obrat v mozku (tab. 2).
Tab. 2. Prevence a terapie nitrolební hypertenze při ASJ. Tab. 2. Prevention and treatment of intracranial hypertension in ALF. 
Od hyperventilace se až na výjimečné případy prakticky upustilo, hyperventilace je dnes pouze rescue postupem při nárůstu nitrolební hypertenze, ovšem jen krátce a za monitorace nitrolebního tlaku.
Resuscitace oběhu
Základním a časným terapeutickým opatřením u pacientů s ASJ je adekvátní a časná tekutinová resuscitace. Protože funkce selhávajících jater se rapidně zhoršuje při tekutinovém přetížení, je třeba podávání tekutin řídit dle hemodynamických cílů. Od invazivní hemodynamické monitorace s měřením tlaků v plicnici se postupně upustilo. Nyní se za přínosnější považuje hodnocení dynamických parametrů preloadu. Monitorace odvozená od analýzy tepové vlny (LiDCO, PiCCO) poskytuje u ventilovaných pacientů informace o aktuálních hemodynamických parametrech, jejich trendech a o potřebě tekutin.
Samotná dodávka tekutin u pacientů s ASJ obvykle nepostačuje a k udržení dostatečného perfuzního tlaku (střední arteriální tlak > 65 mmHg) je nutné užití vazopresorů. Na prvním místě je noradrenalin, při nutnosti inotropní popory dobutamin. Dříve užívaný dopamin nyní doporučován není, zejména pro vysoké riziko arytmií při vyšších dávkách.
Je také možné užití vazopresinu, který potencuje vazokonstrikční efekt noradrenalinu. Dřívější studie poukazovaly na možnost vzestupu nitrolebního tlaku podmíněného cerebrální vazodilatací při podání vazopresinu [6]. Tyto skutečnosti ale nebyly jednoznačně potvrzeny.
Akutní selhání jater je provázeno adrenokortikální insuficiencí, proto je při progresi hemodynamické nestability doporučováno podání hydrokortizonu.
Ventilace
Dříve nebyla u pacientů s ASJ zaváděna sedace a umělá plicní ventilace byla oddalovaná co nejvíce, aby bylo možno hodnotit vývoj encefalopatie a progresi nebo reparaci onemocnění. V posledních letech je u pacientů s ASJ při dosažení 3. stupně encefalopatie doporučeno zajištění dýchacích cest a zavedení umělé plicní ventilace. Je užívána protektivní ventilace s nízkými dechovými objemy (6 ml/kg) s hodnotami PEEP (pozitivní end-expirační tlak) nepřesahujícími 10 cm H2O, aby nedocházelo k městnání v játrech a dalšímu zhoršení jaterních funkcí.
Náhrada funkce ledvin
Zpočátku byla k náhradě funkce levin při ASJ užívána intermitentní dialýza a antikoagulace heparinem. To vedlo ke zvýraznění oběhové nestability a progresi nitrolební hypertenze. Heparinová antikoagulace pak často spustila manifestaci krvácivých komplikací. Nyní jsou u pacientů s ASJ intermitentní metody nahrazeny kontinuálními, které hemodynamiku nekompromitují a nepodílí se na kolísání nitrolebního tlaku [7].
Nejčastěji se užívá kontinuální venovenózní hemodialýza (CVVHD) a kontinuální venovenózní hemodiafiltrace (CVVHDF).
Prahové hodnoty pro zavedení eliminačních metod postupně progresivně klesaly. Indikací je v současnosti nejen akutní poškození ledvin s anurií a vzestupem dusíkatých katabolitů, ale i tekutinové přetížení a metabolický rozvrat s acidózou a hyperlaktatemií a kontrola hyperamonemie, která je dávána do souvislosti s rozvojem edému mozku a herniacemi mozkové tkáně u pacientů s ASJ [8].
K antikoagulaci při kontinuálních metodách lze užít regionální heparinizaci, prostaglandiny nebo citrát. Ačkoli je dle KDIGO doporučení citrátová antikoagulace u pacientů s jaterním selháním kontraindikována, přibývá v poslední době důkazů, že regionální citrátová antikoagulace při selhání jater je bezpečná a účinná, podmínkou je ale vzdělaný tým na pracovišti s dostatečnými zkušenostmi s touto metodou [9,10].
Výživa
Nutriční intervence při ASJ vycházejí z limitovaných dat experimentálních studií a z klinických pozorování (tab. 3). Přístup k nutriční podpoře se neliší od zvyklých postupů u jiných populací pacientů na JIP. Pokud není možná enterální nutrice, je zahájena výživa parenterální. Důležité je při jaterním selhání udržení normoglykemie a podpora regenerace jater. V klinické praxi by měly být glukóza a lipidy podávány současně, užití lipidů je obzvláště výhodné při přítomné inzulinové rezistenci typické pro selhání jater [11].
Tab. 3. Doporučený přívod nutrientů. Tab. 3. Recommended intake of nutrients. 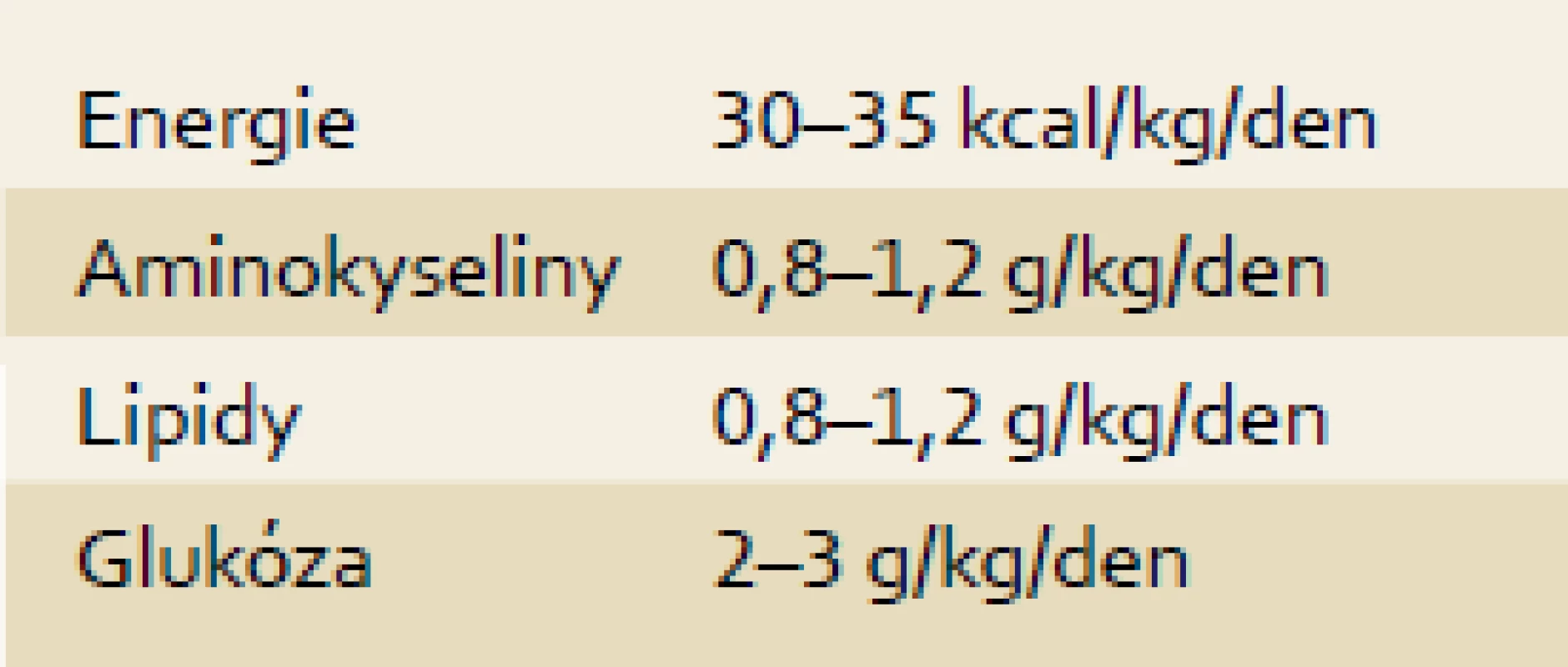
Antimikrobní profylaxe, profylaxe stresového vředu
Mikrobiologické sledování prokázalo změny v epidemiologii a načasování infekcí, přičemž dnes dochází k bakteremii mnohem později v průběhu ASJ [12]. Antibiotická profylaxe je užívána u pacientů s ASJ s rozvojem encefalopatie, jinou orgánovou dysfunkcí a u těch, kteří splňují nebo budou pravděpodobně splňovat kritéria pro transplantaci, a u pacientů s klinickými známkami významného systémového zánětu. Profylaxe stresového vředu je standardním opatřením u pacientů na JIP.
Korekce koagulopatie
Navzdory přítomným těžkým abnormalitám v parametrech koagulace u pacientů s ASJ je spontánní krvácení pozorováno velmi zřídka. Rutinní podávání transfuzních přípravků a krevních derivátů není indikováno. Výjimkou je příprava před invazivními procedurami a existence krvácivých projevů. Podávání čerstvě zmrazené plazmy nezvyšuje přežívání pacientů s ASJ, naopak může vést k tekutinovému přetížení, srdečnímu selhání a zhoršení funkce dalších orgánů i samotných jater. Nezanedbatelné je i riziko nežádoucích vedlejších účinků plazmy včetně s transfuzí spojeného akutního poškození plic.
Transplantace jater pro ASJ
Před nástupem transplantace jater se celková mortalita pacientů s akutním jaterním selháním pohybovala mezi 80 a 85 %. Transplantace jater představovala výrazné zlepšení a stala se standardním managementem u těchto pacientů od konce 80. let [13]. V současnosti představuje transplantace z důvodu ASJ 8–11 % transplantací jater v Evropě a USA.
Urgentně provedená transplantace jater představuje jedinou šanci na přežití pro většinu pacientů s ASJ, proto platí, že každý pacient s ASJ by měl být zvažován k transplantaci jater. Rozhodnutí o transplantaci je prováděno multidisciplinárním týmem na základě etiologie, klinické prezentace a hodnocení prognostických kritérií. Zbytečně provedená transplantace znamená nejen zatížení pacienta operací a celoživotní imunosupresivní terapií, ale i ztrátu štěpu pro někoho jiného, komu mohla transplantace zachránit život. Na druhou stranu její neprovedení nebo pozdní rozhodnutí má za následek úmrtí pacienta s pokročilým ASJ na čekací listině nebo závažné perioperační komplikace.
Kontraindikaci k transplantaci představuje nekontrolovaná sepse, progredující nitrolební hypertenze a extrahepatální malignity. Jsou zvažovány i faktory psychosociální.
K hodnocení prognózy jsou stále užívána King´s College kritéria (tab. 4), jejichž platnost byla opakovaně validována pro euroatlantickou populaci [14]. Jejich splnění znamená méně než 20% pravděpodobnost přežití bez transplantace jater. Clichy kritéria (tab. 5) jsou založena na hodnocení věku, faktoru V a stupně encefalopatie u pacientů s akutním jaterním selháním u hepatitidy B. Problémem obou těchto systémů je vysoká specificita a nízká senzitivita, což znamená, že někteří pacienti s ASJ zemřou, aniž tato kritéria splní.
Tab. 4. King’s College kritéria. Tab. 4. King’s College criteria. 
Tab. 5. Clichy kritéria. Tab. 5. Clichy criteria. 
Jiná kritéria, jako procento nekrózy jaterních buněk a hyperlaktatemie, jsou sice přijímána jako ukazatelé nepříznivé prognózy, ale k zařazení k transplantaci užívána nejsou.
Pokroky v chirurgických technikách
Nově užívané techniky umožňují transplantaci redukovaných štěpů jater a splitování jater pro jednoho nebo pro dva příjemce. Namísto cross clampu dolní duté žíly při hepatektomii provázeného hemodynamicky závažnými projevy se užívá ve většině případů techniky „piggy back“ s naložením nástěnné svorky na dolní dutou žílu. Výhodou je vyšší hemodynamická stabilita během anhepatické fáze bez nutnosti podávání velkého objemu tekutin. Technický pokrok a dokonalejší možnosti imunosuprese umožnily i provádění transplantací ABO inkompatibilním štěpem.
Přežití po transplantaci jater bylo nedávno hodnoceno u 4 903 pacientů s ASJ hlášených v Evropském registru transplantace jater (ELTR). Míra přežití pacientů po jednom roce, pěti a deseti letech a přežití štěpů byly udávány jako 74 %, 68 %, 63 %, resp. 63 %, 57 % a 50 %. Ke zlepšení přežití došlo v období 2004–2009 v porovnání s předchozími pětiletými obdobími (p < 0,001), přestože podíl dárců ve věku nad 60 let vzrostl z 1,8 % na 21 %. Z dat ELRT vyplývá konstantní a progresivní zlepšování přežití v čase [12].
Přístrojová podpora selhávajících jater
Racionálním podkladem užití podpůrné přístrojové terapie při ASJ je předpoklad, že projevy jaterního selhání jsou způsobeny akumulací toxinů z důvodu váznoucí detoxikace v selhávajících játrech. Hlavním cílem je překlenout dobu potřebnou k přežití do transplantace jater nebo spontánního zotavení. Nejčastěji užívanými podpůrnými systémy v Evropě jsou Molecular Adsorbent Recirculating Systém (MARS) a systém frakcionované plazmatické separace a adsorpce (FPSA, přístroj Prometheus).
Opakovaně byla prokázána biochemická účinnost obou systémů v odstraňování toxinů z krve, přičemž účinnost Promethea se zdá být lepší než MARS. Jen málo informací je však k dispozici ohledně dopadu těchto systémů na přežití pacientů s ASJ. Je to dáno nízkou incidencí ASJ v populaci a rozdílným designem jednotlivých studií. Randomizované kontrolované studie, které by přinášely jednoznačná doporučení, zatím k dispozici nejsou [15].
Vlastní zkušenosti s pacienty s ASJ v IKEM
Od zahájení programu transplantace jater v IKEM se zde provádějí i transplantace pro ASJ. Postupně byla do intenzivní péče o tyto pacienty implementována všechna výše zmíněná doporučení.
Management nitrolební hypertenze zahrnuje i zavedení čidla k měření nitrolebního tlaku, které je užíváno u všech pacientů s encefalopatií 3. stupně s umělou plicní ventilací a sedací. Před intervencí je korigována koagulopatie (INR pod 1,5, počet trombocytů nad 50 × 109/l). Závažné komplikace nebyly v průběhu let zaznamenány.
Náhrada funkce ledvin je v současnosti ve shodě se zkušenostmi evropských center indikována dříve před dosažením anurie, při známkách hrozící hyperhydratace, metabolickém rozvratu a hyperamonemii. Standardně je pro náhradní metody užívána citrátová antikoagulace.
Od roku 2005 je na Klinice anesteziologie, resuscitace a intenzivní péče u pacientů s ASJ prováděna podpůrná přístrojová terapie přístrojem Prometheus (obr. 1). Kromě potvrzení biochemické účinnosti metody v odstraňování ve vodě i na albumin vázaných toxinů bylo dokumentováno významné snížení prozánětlivých cytokinů [16]. Ve srovnání s historickou skupinou pacientů se standardní terapií bez přístrojové podpory bylo zaznamenáno prodloužení tzv. terapeutického okna, tedy doby stabilního stavu, kdy lze transplantaci provést. V provedené studii byla průměrná doba na čekací listině k urgentní transplantaci jater u pacientů se standardní terapií 2,5 dne, zatímco ve skupině pacientů se standardní terapií a frakcionovanou plazmatickou separací a adsorpcí 7,5 dne (p < 0,01) [17].
Obr. 1. Přístroj Prometheus (Fresenius Medical Care). Fig. 1. The device Prometheus (Fresenius Medical Care). 
Postupně došlo k vývoji chirurgických technik (redukce, split), což vedlo ke zvýšení dostupnosti transplantace jater, včetně transplantace dětských příjemců. Od roku 2008 je v IKEM prováděna rovněž ABO inkompatibilní transplantace jater.
Závěr
V průběhu posledních desetiletí došlo k řadě změn v péči o pacienty s ASJ. Zlepšení celkového managementu pacientů s ASJ přijatých na JIP, pokroky v chirurgických technikách, imunosupresi a vývoj perioperační péče vedly ke zlepšenému přežívání pacientů s urgentní transplantací jater pro ASJ. Přes dokumentované pokroky v podpůrné i transplantační terapii pacientů s ASJ zůstává toto onemocnění vysoce devastujícím s vysokou mortalitou. Šanci na přežití zvyšuje časná identifikace pacientů s ASJ, rozpoznání etiologie, včasná specifická a podpůrná terapie, včasný transport do transplantačního centra a v indikovaných případech urgentní transplantace jater.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 4. 9. 2013
Přijato: 2. 10. 2013
MUDr. Eva Kieslichová, Ph.D.
Klinika anesteziologie, resuscitace
a intenzivní péče, IKEM
Vídeňská 1958/9, 140 21 Praha 4
evki@ikem.cz
Zdroje
1. Lee WM, Stravitz RT, Larson AM. Introduction to the revised American Association for the Study of Liver Diseases Position Paper on acute liver failure 2011. Hepatology 2012; 55(3): 965–967.
2. Bernal W, Auzinger G, Dhawan A et al. Acute liver failure. Lancet 2010; 376(9736): 190–201.
3. Bernal W, Auzinger G, Sizer E et al. Intensive care management of acute liver failure. Semin Liver Dis 2008; 28(2): 188–200.
4. Bernal W, Hyyrylainen A, Gera A et al. Lessons from look-back in acute liver failure? A single centre experience of 3300 patients. J Hepatol 2013; 59(1): 74–80.
5. Lee WM, Hynan LS, Rossaro L el al. Intravenous N-acetylcysteine improves transplant-free survival in early stage non-acetaminophen acute liver failure. Gastroenterology 2009; 137(3): 856–864.
6. Shawcross DL, Davies NA, Mookerjee RP et al. Worsening of cerebral hyperemia by the administration of terlipressin in acute liver failure with severe encephalopathy. Hepatology 2004; 39(2): 471–475.
7. KDIGO Clinical Practice Guideline for Acute Kidney Injury. Kidney International Supplements 2012; 2(1): 124–138.
8. Bernal W, Hall C, Karvellas CJ et al. Arterial ammonia and clinical risk factors for encephalopathy and intracranial hypertension in acute liver failure. Hepatology 2007; 46(6): 1844–1852.
9. Faybik P, Hetz H, Mitterer G et al. Regional citrate anticoagulation in patients with liver failure supported by a molecular adsorbent recirculating system. Crit Care Med 2011; 39(2): 273–279.
10. Patel S, Wendon J. Regional citrate anticoagulation in patients with liver failure – time for a rethink? Crit Care 2012; 16(5): 153.
11. Plauth M, Cabré E, Campillo B et al. ESPEN Guidelines on Parenteral Nutrition: hepatology. Clin Nutr 2009; 28(4): 436–444.
12. Germani G, Theocharidou E, Adam R et al. Liver transplantation for acute liver failure in Europe: outcomes over 20 years from the ELTR database. J Hepatol 2012; 57(2): 288–296.
13. McPhail MJ, Wendon JA, Bernal W. Meta-analysis of performance of Kings's College Hospital Criteria in prediction of outcome in non-paracetamol-induced acute liver failure. J Hepatol 2010; 53(3): 492–499.
14. Faybik P, Krenn CG. Extracorporeal liver support. Curr Opin Crit Care 2013; 19(2): 149–153.
15. Rocen M, Kieslichova E, Merta D et al. The effect of Prometheus device on laboratory markers of inflammation and tissue regeneration in acute liver failure management. Transplant Proc 2010; 42(9): 3606–3611.
16. Ročeň M, Kieslichová E, Merta D et al. Terapie přístrojem Prometheus u pacientů s akutním jaterním selháním – vliv terapie na markery zánětu a regenerace. Anest Intenziv Med 2010; 21(4): 199–205.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2013 Číslo 5- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Gastrointestinální onkologie
- Kvíz – postižení jater s normálními jaterními testy
- Metodika adresného zvaní občanů do českého programu screeningu nádorů tlustého střeva a konečníku
- Vliv klinických a molekulárních faktorů na odhad rekurence kolorektálních adenomů u dlouhodobě sledovaných pacientů
- Postavenie neoadjuvantnej terapie v multimodálnej liečbe karcinómu rekta – klinické výsledky
- Hereditárny difúzny karcinóm žalúdka
- Cílená léčba karcinomu pankreatu – minulost či budoucnost?
- Lymfomy tenkého střeva
- Stav onkochirurgické péče a vzdělávání v onkochirurgii v České republice
- Multidisciplinární přístup v diagnostice a léčbě karcinomu žaludku
- 1 000 transplantací jater v IKEM
- Prvních 1 000 transplantací jater v IKEM
- Transplantace jater pro chronickou hepatitidu C, význam protivirové léčby
- Transplantace jater pro primární sklerozující cholangitidu
- Méně časté indikace k ortotopické transplantaci jater
- Vývoj postupů v léčbě akutního selhání jater
- Endosonograficky navigovaná tenkoihlová aspiračná biopsia zo solídnych pankreatických más – presnosť a impakt na liečbu u 358 pacientov
- Správná odpověď na kvíz
- Příprava tlustého střeva u pacientů s idiopatickými střevními záněty před endoskopickými nebo kolografickými (CT/MR) vyšetřeními – stanovisko IBD pracovní skupiny
-
XXII. jarní setkání Loket 2013 – Neoplazie žaludku
3. postgraduální kurz společnosti pro gastrointestinální onkologii - Životní jubileum prof. Miroslava Zavorala
- Picoprep – očistný prostředek s dvojím účinkem
- Autodidaktický test: gastrointestinální onkologie
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Picoprep – očistný prostředek s dvojím účinkem
- Lymfomy tenkého střeva
- Transplantace jater pro primární sklerozující cholangitidu
- Hereditárny difúzny karcinóm žalúdka
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



