-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaVzácné kožní změny asociované s monoklonální gamapatií: skleredém, skleromyxedém a IgA pemfigus – popis pěti případů a přehled léčebných možností
Rare dermatological entities associated with monoclonal gammopathy: sclerodema, scleromyxedema and IgA pemphigus – overview of 5 cases and therapeutic modalities
Scleroderma adultorum and scleromyxedema are rare scleromucinous diseases that characteristically lead to wooden induration located on the neck and upper trunk. Three types of scleroderma and scleromyxedema can be distinguished according to their association with pre-existing or underlying disease: association with infections (mostly streptococcal infections of the upper respiratory tract), association with monoclonal gammopathy and association with diabetes mellitus. The clinical findings, disease extent and course differ substantially depending on the subtype of scleroderma. Spontaneous regression often occurs in infection-associated scleroderma or scleromyxedema, whereas patients with diabetes or monoclonal gammopathy usually have a chronic progressive course. In cases with monoclonal gammopathy treatment leading to suppression of monoclonal gammopathy may alleviate the dermatologic symptoms. Intravenous immunoglobulins at a dose of 2g/kg can help in cases resistant to chemotherapy. Immunoglobulin (Ig)A pemphigus is a rare disease characterised by a vesiculopustular eruption with intercellular IgA deposition in the epidermis. In this article, we report our experience with 5 cases of rare skin diseases associated with monoclonal gammopathy and present an overview of treatment possibilities.
Keywords:
scleroderma adultorum – scleromyxedema – monoclonal gammopathy – IgA pemphigus
Autoři: Z. Král 1; M. Krejčí 1; L. Pour 1; S. Ševčíková 2; Z. Čermáková 3; Z. Adam 1
Působiště autorů: Interní hematologická a onkologická klinika LF MU a FN Brno 1; Ústav patologické fyziologie LF MU a FN Brno 2; Oddělení klinické biochemie FN Brno 3
Vyšlo v časopise: Transfuze Hematol. dnes,26, 2020, No. 3, p. 226-235.
Kategorie: Kazuistika
Souhrn
Skleredém dospělých a skleromyxedém jsou vzácná mucinózní onemocnění, charakterizovaná tuhou indurací kůže a podkoží. Podle souvislosti s dalšími chorobami se rozlišují tři typy: asociace s proběhlou infekcí (nejčastěji respirační streptokokový infekt), asociace s monoklonální gamapatií a asociace s diabetem. Při asociaci skleredému s proběhlou infekcí může dojít ke spontánní regresi. V případě asociace s monoklonální gamapatií či diabetes mellitus je průběh nemoci obvykle chronický s tendencí k progresi. V případě skleredému s přítomností monoklonální gamapatie může vést léčba eliminující monoklonální imunoglobulin (MIg) k ústupu potíží a kožních projevů. V případě chemorezistence mohou pomoci nitrožilní imunoglobuliny v imunomodulační dávce 2 g/kg. IgA pemfigus je vzácná nemoc s vezikopustulárními kožními erupcemi, asociovaná s MIg typu IgA. V článku je popsáno 5 případů těchto vzácných kožních onemocnění asociovaných s přítomností MIg, se kterými jsme se setkali za 20 let klinické praxe. Je připojen přehled léčebných možností.
Klíčová slova:
skleredém – skleromyxedém – monoklonální gamapatie – IgA pemfigus
ÚVOD
Mucinózy je termín pro skupinu velmi vzácných chorob, které jsou charakterizovány hromaděním mucinu, tedy mukopolysacharidů (glukosaminoglykanů) v kůži a v podkoží, ale i v jiných orgánech a tkáních. Skleredém a skleromyxedém jsou názvy pro velmi podobné nemoci s postižením kůže a podkoží. Jejich společným projevem je zesílení kůže a podkoží způsobené akumulací mucinu až do té míry, že kůže představuje krunýř omezující pohyb, například úst či končetin. U skleromyxedému se mohou vytvářet skupiny kožních papul a mění se i barva kůže. Přítomnost monoklonálního imunoglobulinu (MIg) je v některých případech společná jak pro skleredém, tak pro skleromyxedém. Obě tyto nemoci potom postihují obvykle nejen kůži, ale také vnitřní orgány a tkáně a rovněž centrální nervový systém [1–8]. Dalším kožním onemocněním, kde etiologickým faktorem je MIg typu IgA, je takzvaný IgA pemfigus.
Cílem následujícího textu je poukázat na tyto vzácné nemoci, které svojí etiopatogenezí, přítomností MIg i způsobem léčby patří jak do oblasti dermatologie, tak i do oblasti hematologie. Klinické příznaky způsobené přítomností MIg mohou být velmi pestré a zahrnují mimo jiné i kožní projevy.
V textu jsou popsány typické klinické projevy kožní i mimokožní, možné akutní komplikace, etiologie i diferenciální diagnostika. Dále uvádíme vlastní zkušenosti s léčbou 5 nemocných s monoklonální gamapatií a kožním postižením a obecné terapeutické možnosti u skleredému a skleromyxedému asociovaného s MIg.
KOŽNÍ PROJEVY SKLEROMYXEDÉMU A SKLEREDÉMU
Jsou to vzácná onemocnění ze skupiny mucinóz, s výsevem papilomatózních projevů podmíněných depozity mucinu v koriu a fibroprodukcí. Typické jsou bělavé, drobné, ploché, lesklé a tuhé, často lineárně uspořádané nahloučené papuly barvy kůže, často charakteru vosku, někdy se sklonem ke splývání do ložisek. Papuly velikosti 2–3 mm se nacházejí na rukou, předloktích, tváři, krku a horní části trupu. Současně dochází ke ztluštění kůže prakticky celého těla. Generalizované projevy s výrazným zmnožením vaziva a se vznikem tuhé kůže omezující hybnost, připomínající systémovou sklerodermii či skleredém, bývají označeny jako skleromyxedém. Ztuhlá kůže může být mramorovaná, někde bledá, jinde lividní, podobně jako bylo popsáno v české odborné literatuře a také u jedné naší pacientky [1–8].
Histopatologicky je typické nahromadění hlenu (chemicky glykosaminoglykanů) v dermis kůže, které je doprovázeno proliferací fibroblastů a zmnožením kolagenu v horní a střední dermis. Fibroblasty jsou nepravidelně uspořádané a kolagen má vágně vírovité řazení. Kolem cév jsou často řídké lymfocytární infiltráty [1–9].
Skleredém (scleroedema adultorum Buschke) je charakterizován indurací kůže s predilekcí pro tvář, šíji, ramena a horní část trupu. Postihuje osoby v každém věku. Skleredém je vzácné onemocnění s depozity mucinu v rozsahu celého koria. Dochází k postupnému vzniku tuhé, nezřasitelné kůže, postihující hlavu, krk, horní partie trupu a někdy i končetiny. Proces přechází i do podkoží a do podkožního tuku. U osob s klinicky manifestním skleredémem může dojít k poškození trávicího ústrojí, srdce, plic a svalů, stejně jak je popsáno u osob se skleromyxedémem. V případně skleredému se literární prameny shodují na dvou klinických formách [1–9].
Dlouhodobé mimokožní projevy skleromyxedému
Nemocní se skleromyxedémem mohou mít postiženy a poškozeny i další orgány. Postižení zažívacího traktu touto mucinózou způsobuje poruchu pasáže jícnem, žaludkem i tlustým střevem, častým projevem je obstipace.
Postižení svalů se projevuje svalovou slabostí, mohou být přítomny zvýšené hodnoty myoglobinu a kreatinkinázy [1–9].
Poškození plic se může manifestovat restrikční, méně často obstrukční ventilační poruchou. Skleredém, skleromyxedém a nakonec i jiné monoklonální gamapatie mohou být vzácně asociovány s plicní hypertenzí. Zda jde o kauzální souvislost či koincidenci, nebylo zatím definitivně objasněno, ale některé publikace popisují možný kauzální vztah [10–12]. V našem souboru 4 pacientů byla v jednom případě diagnostikována primární plicní hypertenze.
Literatura popisuje u osob se skleredémem také kardiomyopatii, nefropatii a artritidu. Při echokardiografickém vyšetření byla u jednoho z našich pacientů zjištěna srdeční hypokontraktilita. Kloubní postižení bývá někdy dokumentováno scintigrafickými metodami [13]. V patogenezi orgánového poškození, které může postihnout kterýkoliv orgán, mají významnou roli mucinová depozita v medii a adventicii cév těchto orgánů.
Akutní komplikace mucinóz – dermatoneurosyndrom
Jedná se o akutní, život ohrožující komplikaci, která způsobuje poškození mozkových cév a mozku při tomto onemocnění. Neurologické komplikace mucinóz jsou velmi pestré, od nejlehčích, které se manifestují jako nevýrazné závratě či změny kognitivních funkcí, až po závažné neurologické symptomy s poruchami vědomí typu somnolence, soporu a kómatu a dále křečové stavy. Pro závažnou neurologickou poruchu u osob s mucinózou se používá označení dermatoneurosyndrom. Jedná se o kritickou, život ohrožující poruchu vědomí až úrovně kómatu, často komplikovanou záchvaty generalizovaných tonicko-klonických křečí.
Dermatoneurosyndrom může následovat v intervalu několika týdnů po prodělaném horečnatém onemocnění, které vzácně může být spouštěčem této komplikace.
Zobrazení mozku metodou CT vyšetření (computer tomography, CT) v průběhu této ataky bývá zpravidla normální a ve vyšetření mozkomíšního moku v průběhu dermatoneurosyndromu nebyly popsány žádné typické patologické změny. A stejně tomu tak bylo i u našeho pacienta s dermatoneurosyndromem, jak je popsáno v dalším textu. Při adekvátní léčbě, zahrnující plazmaferézu a nitrožilní podání imunoglobulinů ve vysokých dávkách, se popisuje úprava této dramatické ataky.
Příčina dermatoneurosyndromu není jasná. Obvyklé bývá sice přítomný monoklonální imunoglobulin, ale v nízké koncentraci, takže není možné se domnívat, že by dermatoneurosyndrom byl projev hyperviskozity [14]. Nitrožilní podání vysokých dávek imunoglobulinů (IVIG) má výrazný imunomodulační efekt, a proto se používá při zvládání některých život ohrožujících projevů autoimunitních onemocnění, například vzestupná polyradikuloneuritida, závažná imunitní trombocytopenie a jiné. Pozitivní účinek IVIG svědčí pro autoimunitní mechanismus popisovaného dermatoneurosyndromu.
DIFERENCIÁLNÍ DIAGNÓZA SKLEREDÉMU
Skleredém a skleromyxedém mají společnou charakteristiku – patologické zesílení, respektive ztluštění kůže. Skleredém postihuje obvykle hlavu, krk, šíji a hrudník, tedy jedná se obvykle o celkové postižení, zatímco skleromyxedém může být lokalizovaný a mimo zesílení kůže jsou na kůži viditelné papuly barvy včelího vosku. V některých případech nemusí být zcela zřejmé, zda postižení nazvat skleredémem či skleromyxedémem.
Zásadní rozdíl obvykle je, že skleromyxedém na rozdíl od skleredému má navíc papulární formace. Některé učebnice dermatologie uvádějí, že při skleredému není možné posunout kůži oproti spodině, zatímco u skleromyxedému to možné je. V případně skleromyxedému se častěji popisují generalizovaná orgánová poškození než u skleredému, ale zřejmě u obou těchto jednotek je nutno počítat s tím, že patologické projevy postihují a poškozují i další orgány a tkáně. U obou jednotek, skleredému a skleromyxedému, je velmi často prokazatelný MIg.
V rámci diferenciální diagnózy jsou uváděny následující jednotky: systémová sklerodermie, eozinofilní fascitiida a hlavně skleromyxedém. Od systémové sklerózy se pacienti se skleredémem liší nepřítomností Raynaudova fenoménu, nepřítomností akrální sklerózy a nepřítomností antinukleárních protilátek (ANA a další) [9].
ETIOLOGIE MUCINÓZ TYP MYXEDÉMU, SKLEROMYXEDÉMU A SKLEREDÉMU
Etiologie u těchto vzácných onemocnění není zcela objasněna, předpokládá se především autoimunitní mechanismus. Všeobecně známé jsou například projevy hypotyreózy při Gravesově-Basedowově chorobě, spojené se zvýšenou tvorbou a akumulací mucinu v určitých oblastech, Gravesova orbitopatie se vyskytuje u 25 % nemocných s autoimunitní hypotyreózou, tyreoidní dermopatie (zvaná též pretibiální myxedém) u 1,5 % nemocných, kožní změny zvané acropachy jen u 0,3 % pacientů s Gravesovou hypotyreózou. Uvedené kožní extratyreoideální projevy hypotyreózy mají autoimunitní příčinu, zřejmě zprostředkovanou protilátkami proti TSH receptoru, které stimulující také fibrocyty v určité lokalizaci ke tvorbě mucinu.
Asi u 80 % osob se skleromyxedémem je přítomný MIg. Nicméně diagnózu symptomatického mnohočetného myelomu splní snad jen 10 % nemocných. U většiny osob se skleromyxedémem odpovídá plazmocelulární proliferace v kostní dřeni low-grade plazmocelulární gamapatii, neboli monoklonální gamapatii nejistého významu (monoclonal gammopathy of unknown signifikance, MGUS) [15].
Rongioletti a spol. popisují soubor 30 osob se skleromyxedémem [15]. U 27 z nich byl v séru detekován MIg, ale u žádného nebyla splněna diagnóza mnohočetného myelomu (MM). U 30 % z nich bylo zjištěno orgánové poškození [15].
Monoklonální imunoglobulin v nízké koncentraci většinu svých nositelů nepoškozuje, nicméně v menšině případů je popisováno zaměření antigenní determinanty MIg proti některému z autoantigenů, se vznikem závažných klinických příznaků. Nicméně je otázka, zda je kauzální souvislost mezi MIg a kožními změnami při skleromyxedému, nebo zda oba tyto jevy mají stejnou vyvolávající příčinu, takže spolu koexistují. Dosažení kompletní hematologické remise u MM a vymizení skleromyxedému či skleredému se dají vysvětlit jako průkaz možné příčinné souvislosti mezi MIg a těmito mucinózami. Monoklonální imunoglobulin v těchto případech zřejmě stimuluje fibroblasty v kůži a v podkoží k nadměrné tvorbě mucinu. Úplné vymizení skleredému i obstipace, která provázela skleredém, jsme pozorovali u druhého popsaného pacienta, u něhož vysokodávkovaná chemoterapie vedla k dlouhodobému vymizení MIg.
Nicméně je fakt, že existují i případy skleredému a skleromyxedému bez průkazu MIg. V těchto případech jsou buď fibroblasty stimulovány imunoglobulinem v tak nízké koncentraci, že monoklonalita imunoglobulinu není prokazatelná, nebo bude existovat ještě jiný spouštěcí mechanismus. Také účinnost imunosupresivní léčby svědčí pro autoimunitní mechanismus vzniku mucinóz.
VLASTNÍ ZKUŠENOSTI – POPIS ČTYŘ PŘÍPADŮ MUCINÓZ A JEDNOHO PŘÍPADU IgA PEMFIGU
V období 2000–2020 jsme na našem pracovišti léčili celkem čtyři pacienty s depozity mucinu v podkoží a monoklonální gamapatií a jednu pacientku s IgA pemfigem. Z komplikací typických pro mucinózy jsme se u všech pacientů setkali s poruchou pasáže a s obstipací, v jednom případně s primární plicní hypertenzí a v jednom případě s akutní komplikací – dermatoneurosyndromem. Kazuistiky těchto pacientů zveřejňujeme s jejich souhlasem, v případě dvou zemřelých pacientů byl souhlas s publikací případů získán ještě v době jejich života.
Žena narozená v roce 1949
Žena se systémovými projevy mucinózy typu skleromyxedému a současně s přítomností MIg přišla na naše pracoviště poprvé v prosinci 2009, tedy ve věku 60 let. Tato pacientka měla povšechně zesílenou kůži a podkoží a dále měla v oblasti předloktí, na rukou a na obličeji papulózní kožní projevy béžové barvy a voskového lesku. Kůže zesílená mucinovými hmotami měla střídavě bledou a lividní barvu (obr. 1–3).
Obr. 1. Fotografie kůže pacientky se skleromyxedémem: zřetelná lineární konfigurace papul 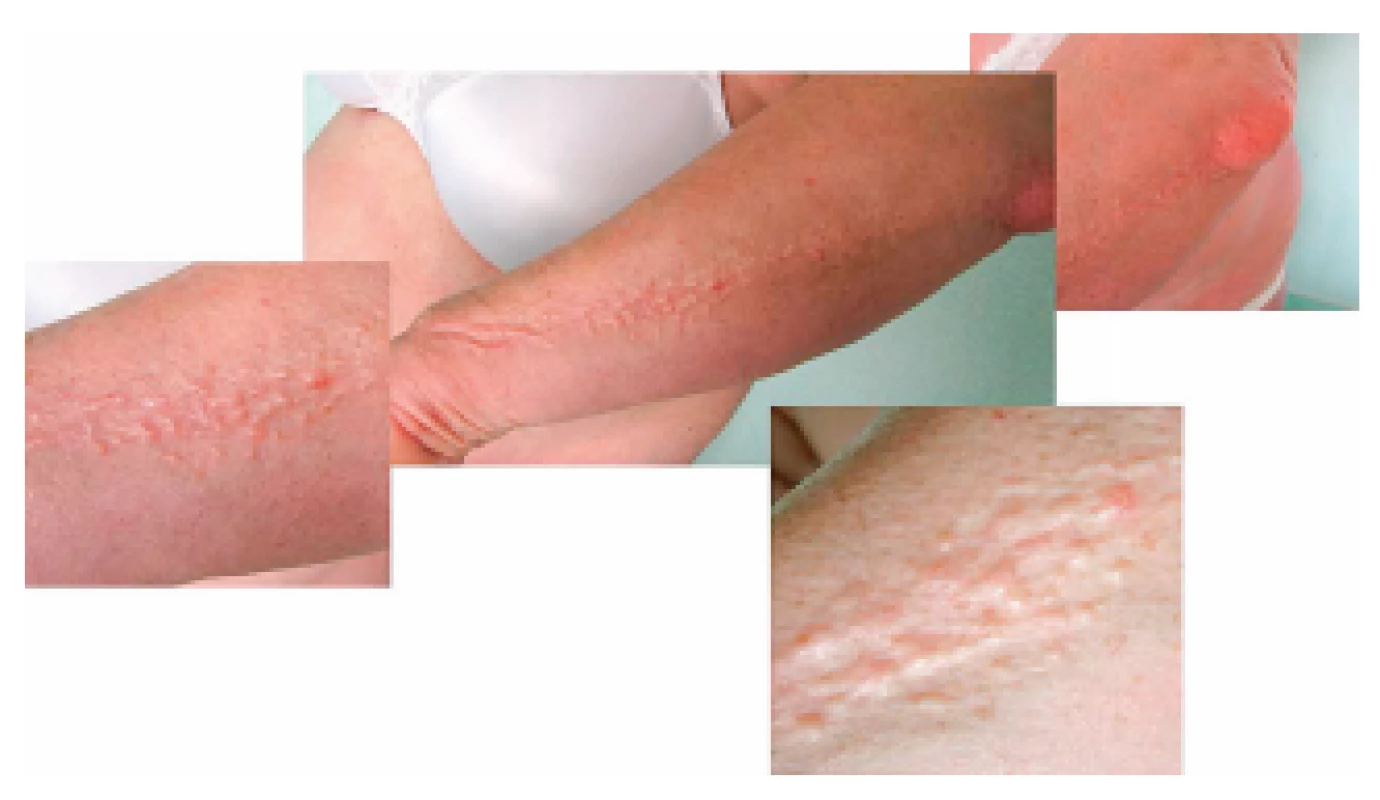
Obr. 2. Mramorovaná kůže pacientky se skleromyxedémem: místy bledá, místy lividní 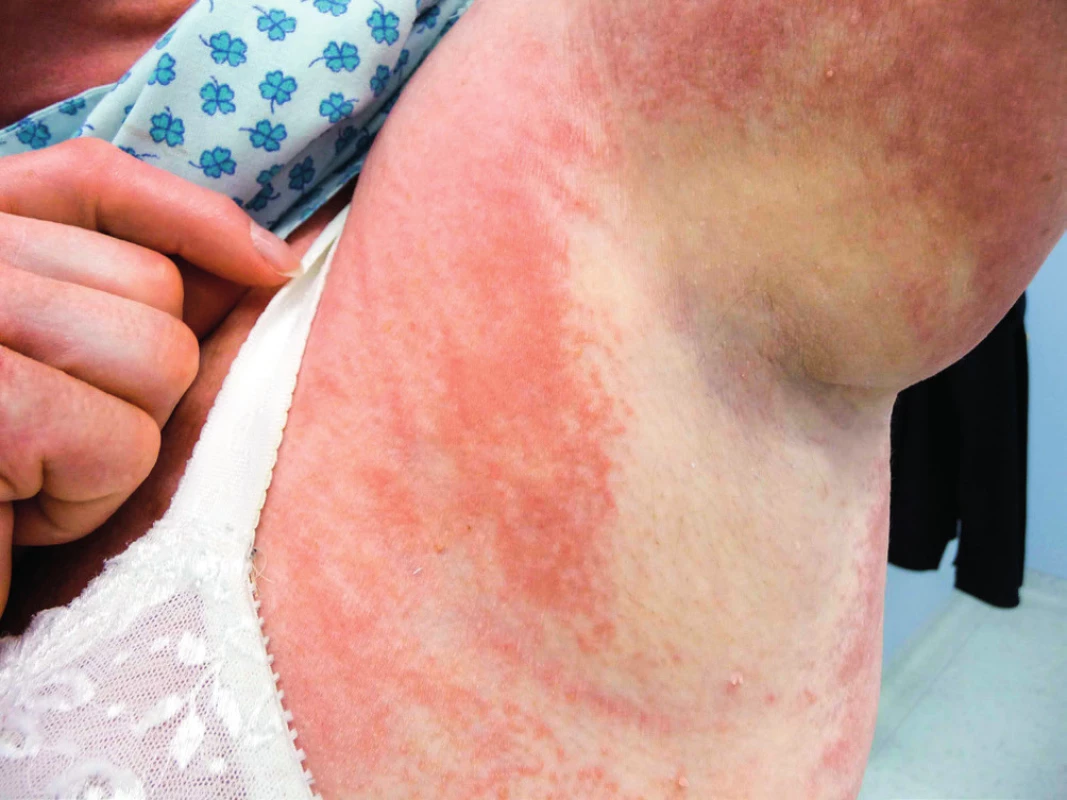
Obr. 3. Struktura ztluštělé kůže pacientky se skleromyxedémem 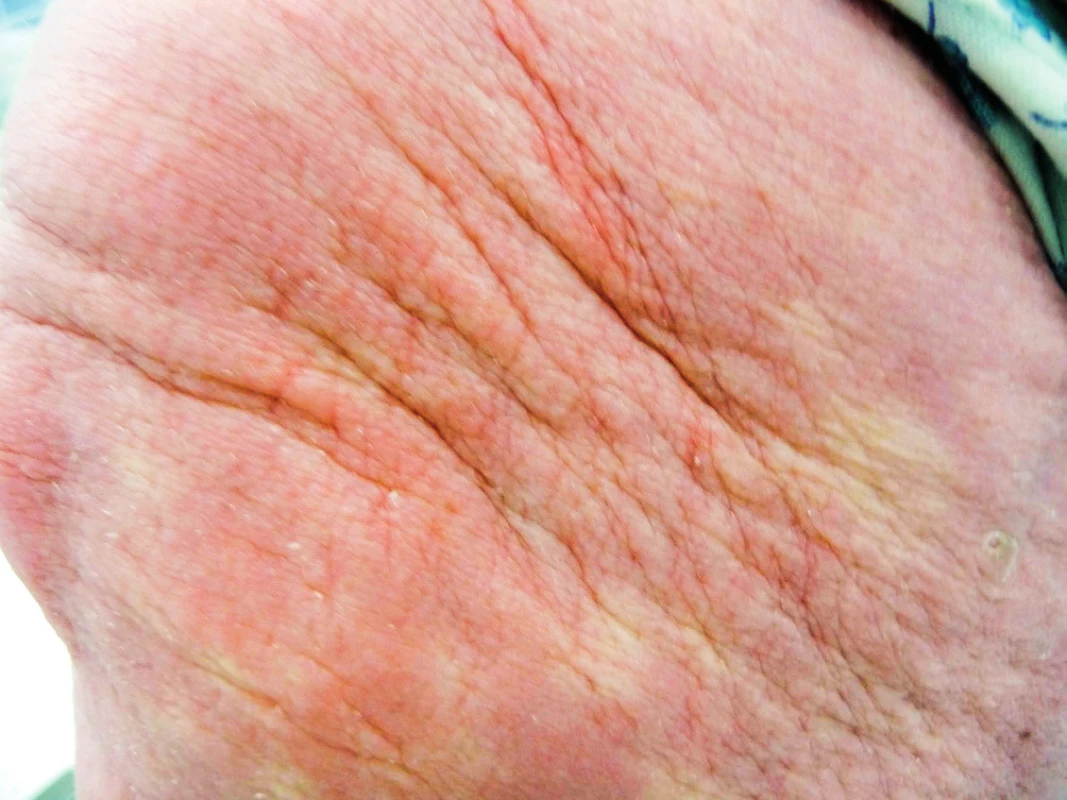
Histopatologické vyšetření válečku kostní dřeně prokázalo 2–4 % klonálních plazmocytů. Monoklonální imunoglobulin IgG kappa vstupně dosahoval koncentrace 9,0 g/l. Literatura popisuje souvislost skleromyxedému s MIg, proto byla indikována léčba vedoucí k potlačení tvorby MIg, i když diagnóza odpovídala monoklonální gamapatii nejasného významu (MGUS). Byla zvolena terapie pomocí kombinace cyklofosfamidu, bortezomibu a dexametazonu. Ta dosáhla poklesu MIg z 9,0 g/l na 3,9 g/l. V průběhu léčby se dočasně zmenšily i kožní projevy. Pacientka uvedla, že pociťovala částečné změknutí kůže a podkoží, ale změny na kůži odpovídající skleromyxedému byly stále patrné. V roce 2010 proběhlo poslední kontrolní histopatologické vyšetření kůže. Patolog popsal rozšíření dermis pod úroveň potních žláz, hrubé snopce kolagenu byly odděleny množstvím mucinu. Na zvýšené celularitě dermis se podílely fibroblasty. Zánětlivý infiltrát byl velmi mírný. Nález hodnocen jako skleromyxedém s počínající sklerotizací. Ve srovnání s předchozí histologií bylo vazivo nyní vyzrálejší a množství hlenu (mucinu) nižší. Průběh léčby byl komplikován pravostrannou srdeční slabostí s retencí tekutin. Příčinou byla posléze prokázaná plicní hypertenze, na jejíž důsledky pacientka zemřela. Uvedený případ dokumentoval částečné zlepšení kožních projevů při postupném poklesu MIg a opětovné zhoršení kožních projevů při vzestupu koncentrace MIg a dále rozvoj plicní hypertenze v průběhu této formy mucinózy typu skleromyxedému.
Muž narozený v roce 1953
Muž měl v anamnéze diabetes mellitus léčený perorálními antidiabetiky již od roku 2003. Na naše pracoviště poprvé přišel v listopadu roku 2011. Při přijetí bylo nápadné difuzní tuhé zesílení kůže a podkoží. Pacient měl maskovitý výraz obličeje bez možnosti mimiky. Ztuhlost kůže a podkoží v obličeji byla tak velká, že nemocný měl potíže s příjmem potravy, protože ztuhlost postihovala i pohyby úst. Trpěl urputnou obstipací, stolice byla za pomocí projímadel maximálně 1× za týden. V tomto případě dosáhla hodnota koncentrace MIg typu IgG kappa 36 g/l a na rentgenových snímcích skeletu byla zřetelná mnohočetná osteolytická ložiska a kompresivní fraktury obratlů. Histopatologie kostního válečku odebraného při trepanobiopsii prokázala přes 10 % plazmocytů. Morfologické vyšetření kůže prokázalo malé lymfocytární perivaskulární infiltráty a hlavně zmožení mucinu (hlenu), takže společný závěr dermatologa a patologa byl skleredém (skleroedema adultorum Buschke). Jednalo se tedy o pacienta se symptomatickým mnohočetným myelomem a současně s přítommností skleredému. Vzhledem k celkově špatnému vstupnímu klinickému stavu a k omezením plynoucím ze skleredému byla zahájena standardní chemoterapie cyklofosfamid, bortezomib a redukovaná dávka dexametazonu vzhledem k současné přítomnosti diabetes mellitus. Léčebný efekt byl excelentní, pokles MIg byl neobvykle rychlý, po dvou cyklech léčby poklesla koncentrace MIg z 36,7 g/l na 3,2 g/l a po třetím cyklu již MIg nebyl detekovatelný a pacient splňoval kritéria kompletní remise (CR). Po dvou měsících léčby začal zřetelně ustupovat také kožní nález, kůže změkla, stala se zřasitelnou. Tím se výrazně zlepšila i mimika obličeje a také hybnost nemocného. Ústup skleredému a návrat struktury kůže do původního stavu vedl k zásadnímu zlepšení klinického stavu, a tak byla provedena i vysokodávkovaná chemoterapie v červenci 2012 (melfalan 200 mg/m2 s následnou transplantací autologních periferních buněk). Kompletní remise trvala 5 let, v roce 2017 začal recidivovat jak myelom, tak i kožní projevy. Pacient odmítl další léčbu a v září 2018 zemřel. Uvedený případ dokumentuje, že léčba (klasická chemoterapie zakončená vysokodávkovanou chemoterapií) vedoucí k úplnému vymizení MIg vedla i k úplnému a dlouhodobému vymizení kožních i mimokožních projevů skleredému, jak dokumentují obrázky 4 a 5.
Obr. 4. Čelo pacienta se skleredémem 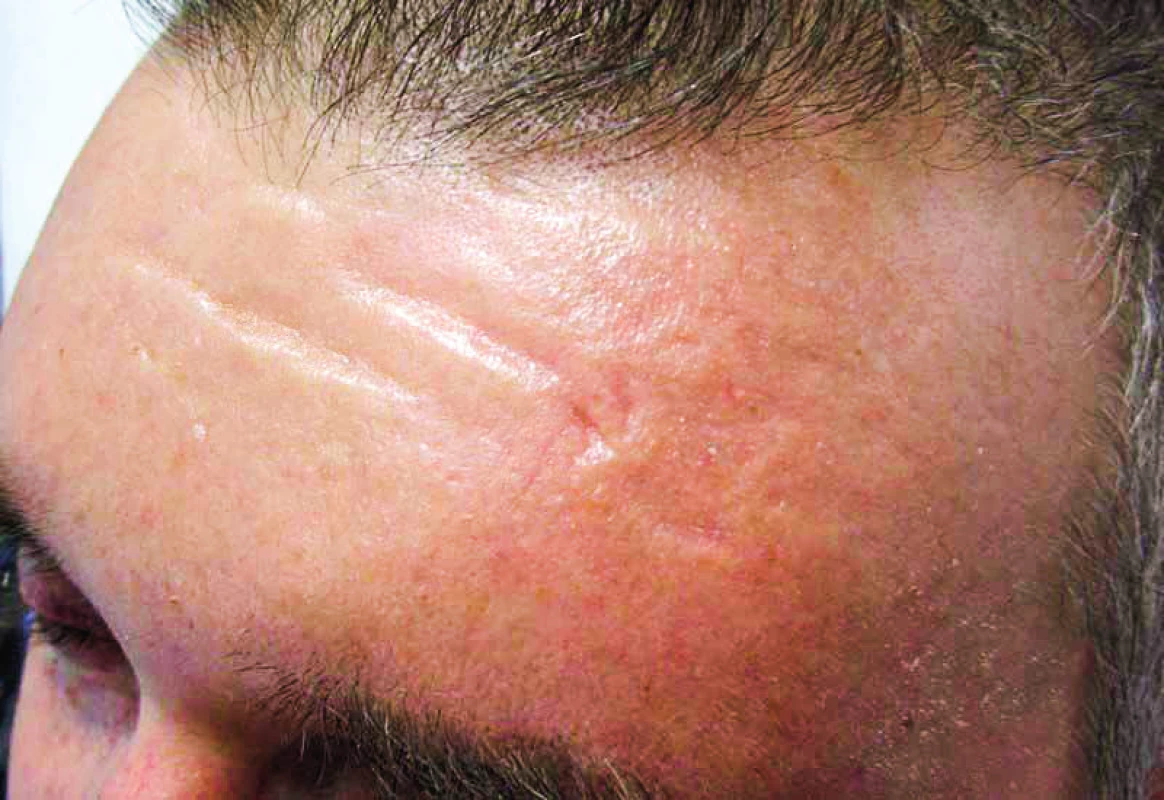
Obr. 5. Vlevo: Obličej pacienta se skleredémem: mucinózní infiltrace kůže a podkoží způsobila zesílení kůže a podkoží a omezení hybnosti Vpravo: Obličej pacienta se skleredémem: zlepšení po léčbě 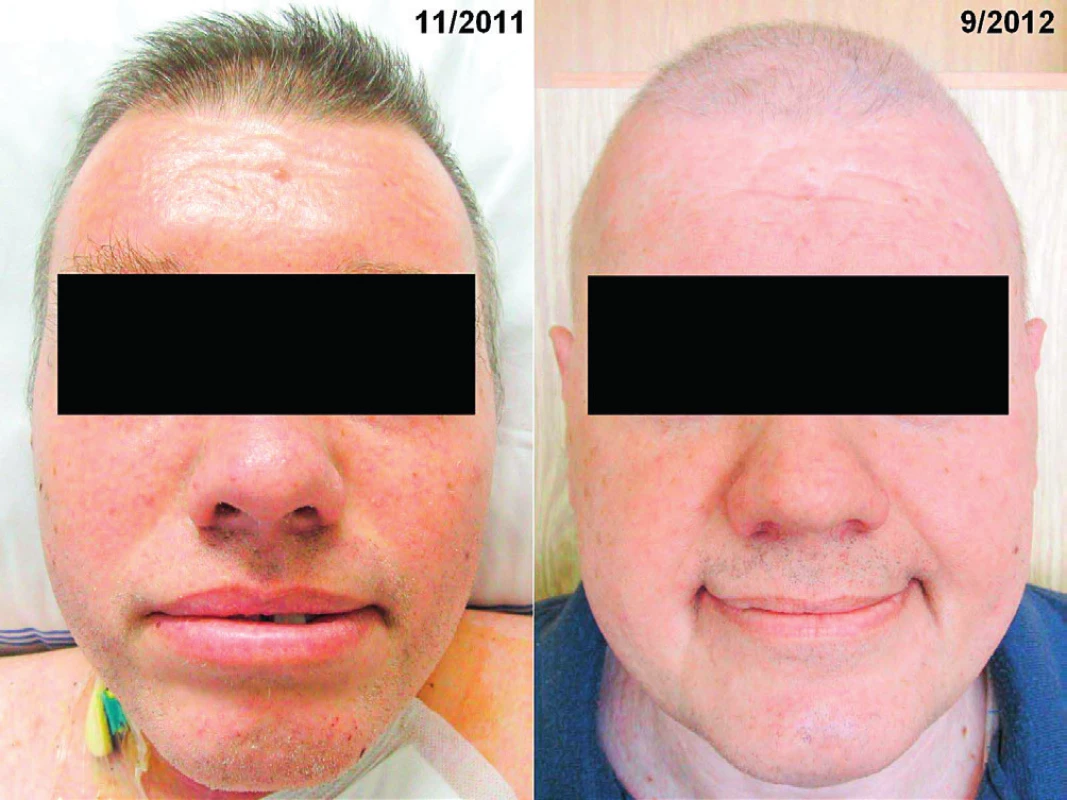
Muž narozený v roce 1956
Muž byl vyšetřován od konce roku 2012 pro vznik svědivých zatuhlých ložisek na kůži trupu, šíje i hlavy.
V březnu 2013 byla provedena biopsie kůže se závěrem skleromyxedém.
V dubnu 2013 byla již kůže celého těla ložiskově tuhá a mramorovitě fialovočerveně zbarvená. V dubnu 2013, po předchozím horečnatém onemocnění, byl pacient přijat do nemocnice pro epileptické paroxysmy. Křeče progredovaly do epileptického záchvatu typu grand mal s kvalitativní poruchou vědomí a zmateností, která posléze přešla ze somnolence až do kómatu, následně došlo k rozvoji ventilačního selhání s nutností řízené plicní ventilace. Vše bylo komplikováno sepsí a multiorgánovým selháním (selhávající funkce plic, ledvin a jater s nutností dočasných hemodialýz a umělé plicní ventilace). Tato krize byla zvládnuta specialisty na intenzivní medicínu standardními postupy používanými v intenzivní medicíně. Protože typ krize odpovídal dermatoneurosyndromu, tak ještě v rámci léčby multiorgánového selhání na jednotce intenzivní péče byly v dubnu 2013 podány nitrožilně imunoglobuliny v dávce 2 g/kg tělesné hmotnosti pacienta. Po nitrožilní aplikaci imunoglobulinů se stav pacienta výrazně zlepšil, postupně se dostal do plného vědomí a obnovily se funkce ledvin, plic a jater. Pacient měl vstupně v kostní dřeni 5–10 % klonálních plazmocytů a biochemické vyšetření prokázalo MIg typu IgG kappa ve velmi nízké koncentraci 1,9 g/l v séru. Po překonání kritického stavu se koncentrace MIg zvýšila a trvale se pohybuje na hodnotách 3–6 g/l.
V průběhu dalších let zůstává koncentrace MIg stabilní, nebyla tedy naplněna diagnostická kritéria pro mnohočetný myelom a již nejsou žádné známky kožní mucinózy. Vzhledem k obavám z recidivy dermatoneurosyndromu dostává tento pacient nitrožilní imunoglobuliny v uvedené dávce 2 g/kg 1× měsíčně.
Uvedený případ dokumentuje, že léčba IVIG v dávce 2 g/kg 1× měsíčně má zásadní vliv na kožní projevy, ale nemá žádný vliv na koncentraci MIg. Dále tento případ ilustruje, že IVIG mají léčebný potenciál i při tak závažné akutní komplikaci, jako je dermatoneurosyndrom.
Muž narozený v roce 1959
Pacient je na našem pracovišti sledován od března roku 2012. V té době udával, že nejméně tři roky si uvědomuje, že mu tuhne kůže a podkoží. Pacient má od roku 2009 diabetes mellitus léčený perorálními antidiabetiky. Diagnostika diabetu následovala po pokusu o ovlivnění skleredému glukokokortikoidy. Pacient má ztuhnutí a zesílení kůže v oblasti šíje, zad, s progresí na horní polovinu trupu, obličej a horní končetiny s výraznou omezenou hybností krku ale i omezení hybnosti paží (obr. 6). Z dalších projevů provázejících mucinózu byla přítomna urputná obstipace, s pomocí projímadel byla stolice maximálně 1× týdně. Byla provedena biopsie a histologické hodnocení kůže a podkoží. Jak histologický nález zmnoženého mucinu v celé retikulární dermis, tak klinický nález odpovídaly diagnóze skleredém (skleroedema adultorum Buschke). Vzhledem k současnému průkazu nálezu MIg typu IgG kappa byl pacient dále směřován na hematologii. Histopatologické vyšetření válečku kostní dřeně prokázalo 5 % klonálních plazmocytů. Zobrazovací vyšetření neprokázalo žádné postižení skeletu, diagnostická kritéria pro mnohočetný myelom nebyla naplněna.
Obr. 6. Kůže v oblasti krku u pacienta se skleredémem 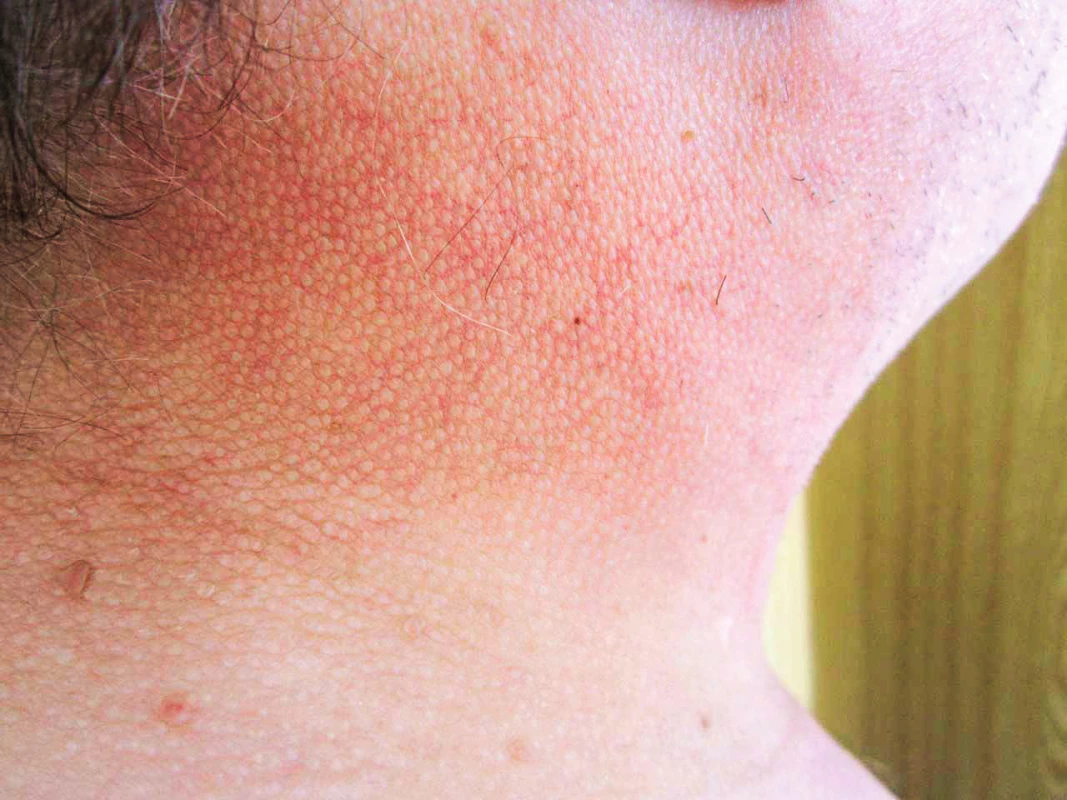
Testovali jsme možnost eliminace MIg standardní léčbou (cyklofosfamid, bortezomib, dexametazon), ale bez efektu na vývoj MIg i na kožní projevy.
Od roku 2016 doposud je pacient léčen nitrožilně podávanými imunoglobuliny. Koncentrace MIg je stabilní, ale kožní projevy nemoci se přestaly zhoršovat a pacient sám popisuje zhoršování tuhosti kůže, pokud se interval mezi aplikacemi imunoglobulinů prodlouží nad jeden měsíc. V tomto případě aplikace nitrožilních imunoglobulinů vede ke stabilizaci kožních projevů a pozastavení progrese kožních změn.
Žena narozená v roce 1949
Pemfigus je puchýřnaté onemocnění kůže. Za posledních 20 let jsme se setkali pouze s jednou pacientkou, která měla pemfigus a souběžně s ním diagnostikovanou monoklonální gamapatii nejistého významu (MGUS) typu IgA. Morfy pemfigu se prakticky nedaly ovlivnit žádnou dermatologickou léčbou. V průběhu sledování po 6 letech přešel MGUS do symptomatického mnohočetného myelomu s četnými osteolytickými ložisky. Léčba založená na bortezomibovém režimu (kombinace bortezomib, cyklofosfamid, dexametazon) dovedla pacientku do kompletní remise mnohočetného myelomu, došlo k vymizení MIg. Pararelně s vymizením MIg vymizely i kožní morfy pemfigu. Kompletní remise trvala 3 roky a po tuto dobu byla pacientka bez kožních morf. Recidiva nemoci byla spojená s obnovením kožních morf, čím vyšší koncentrace MIg typu IgA, tím více kožních morf. Léčba recidivy byla neúspěšná a pacientka nemoci nakonec podlehla. Tento případ demostruje možnost, že MIg může být také etiologickou příčinou pemfigu. Kožní změny dokumentují obrázky 7 a 8.
Obr. 7. Kožní puchýřnaté onemocnění IgA pemfigus u pacientky s mnohočetným myelomem 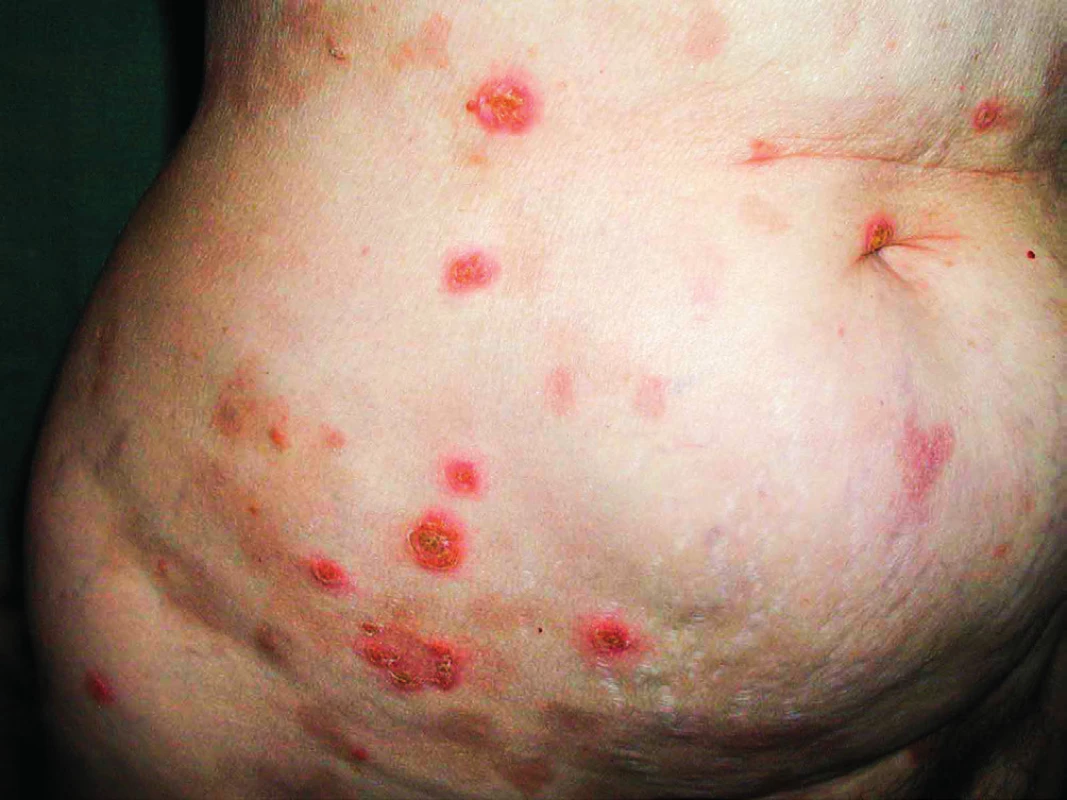
Obr. 8. Histologický obraz IgA pemfigu. Při použití imunohistochemického barvení byla v kožní morfě prokázána depozita imunoglobulinu typu IgA. 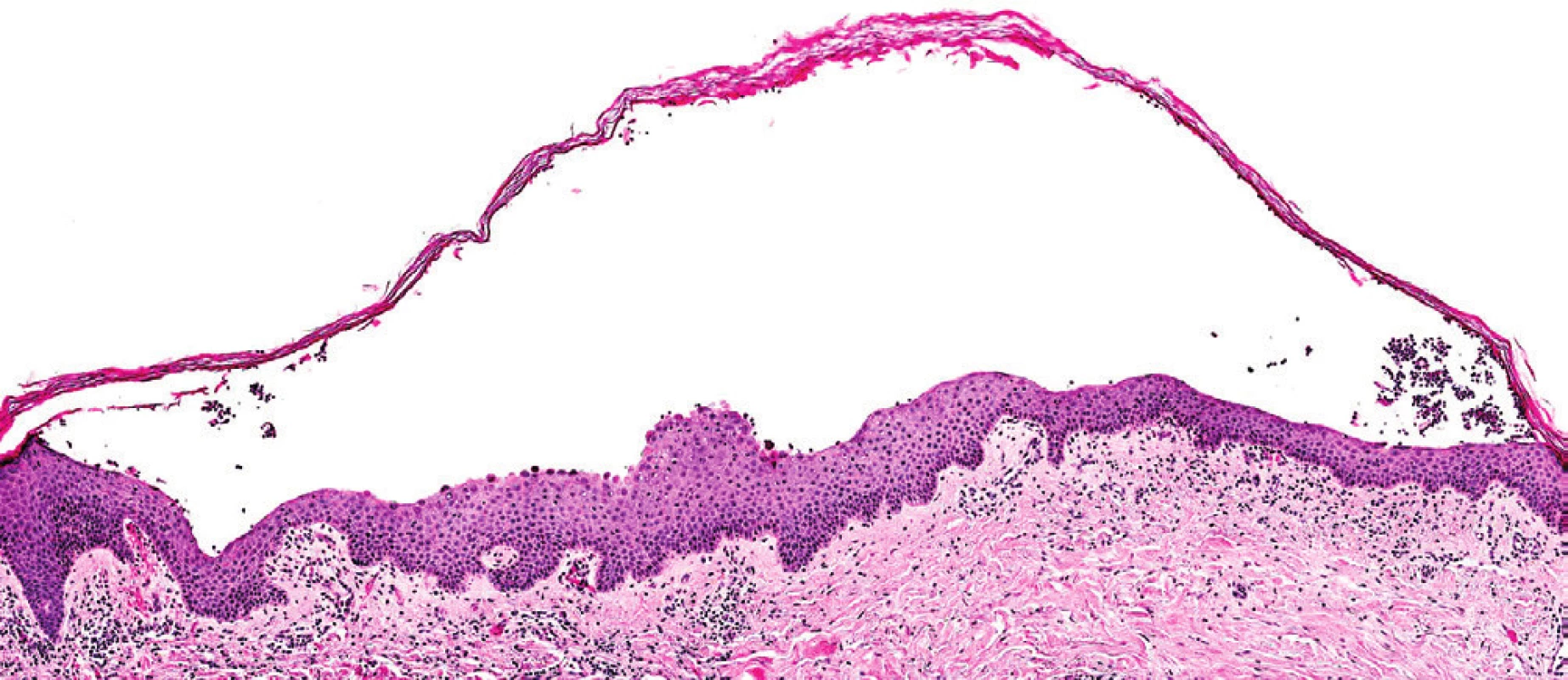
PŘEHLED LÉČEBNÝCH MOŽNOSTÍ U SKLEREDÉMU A SKLEROMYXEDÉMU SDRUŽENÉHO S PRODUKCÍ MONOKLONÁLNÍHO IMUNOGLOBULINU
V literatuře lze najít velmi různorodé léčebné postupy, které dosahovaly většího či menšího efektu. Uvedeme přehled informací o léčbě z literatury, které jsou základem pro rozhodování o léčbě.
Kortikoidy
Kortikoidy jsou často používány s ideou zamezit proliferaci vaziva a zastavit zánětlivé změny. V případě skleredému a skleromyxedému se v literatuře objevily ojedinělé pozitivní zprávy o efektu terapie kortikoidy [16, 17]. Většina autorů se však shoduje na tom, že efekt monoterapie kortikoidy byl malý, ne-li žádný. Rongioletti a spol., kteří zveřejnili hodnocení největšího souboru 30 nemocných, uvádí, že monoterapie glukokortikoidy neměla žádný klinicky významný přínos [15]. Podobně je tomu také u Gravesovy orbitopatie, kdy léčba glukokortikoidy většinou také nepřináší zásadní zlepšení.
Léčba nitrožilními imunoglobuliny
Preparáty nitrožilních imunoglobulinů IgG obsahují polyklonální imunoglobulin typu IgG od tisíců dárců. Nitrožilní léčba vysokými dávkami imunoglobulinů vede k rychlému poklesu prozánětlivých cytokinů a projevů zánětu, a to i u autoimunitních procesů zcela rezistentních na léčbu glukokortikoidy. Přesný mechanismus účinku nebyl zatím vysvětlen, i když tato léčba je používána již více než 30 let. Předpokládá se, že při terapii IVIG obsazení všech receptorů pro Fc fragment imunoglobulinů potlačí autoimunitní a autoinflamatorní reakce.
Literatura pojednávající o léčbě skleromyxedému a skleredému popisuje velmi často klinicky signifikantní léčebný efekt IVIG ve vysokých dávkách, který však nebyl vždy trvalý. Někdy po ukončení léčby postižení recidivovalo, a proto je doporučována udržovací léčba. Nejčastěji byla podána klasická dávka 2 g/kg 1× za měsíc opakovaně, méně často byly použity dávky nižší. V publikované literatuře se nacházejí velmi četná hodnocení této léčebné metody, popisující klinicky významný přínos pro nemocné, a to jak u pacientů se skleromyxedémem, tak se skleredémem [18–24].
Léčba cyklosporinem
Pro léčbu skleredému a skleromyxedému byla testována také léčba cyklosporinem. V literatuře lze nalézt jen ojedinělé případy s pozitivním hodnocením.
Vzhledem k tomu, že počet publikací s pozitivním hodnocením léčby cyklosporinem je malý, podstatně menší než počet publikací pozitivně hodnotících nitrožilní imunoglobuliny, je zřejmé, že imunosupresivní léčba cyklosporinem nebude zdaleka tak účinná, jako imunosupresivní léčba nitrožilními imunoglobuliny [25].
Thalidomid
Thalidomid má své místo při léčbě mnohočetného myelomu a v literatuře lze nalézt také publikované zprávy o přínosu pro pacienty se skleromyxedémem i skleredémem. V několika publikacích je popsána léčba 17 pacientů thalidomidem a ve většině případů je popisováno zlepšení kožních příznaků, nikoliv však úplné vymizení. Thalidomid zpomaluje pasáž trávicím traktem a má prokoagulační vliv, což limituje jeho použití u skupiny nemocných často trpících obstipací [25–27].
Radioterapie
Přínos radioterapie je popisován jen u skleredému adultorum Buschke. Obvykle se používá radioterapie nízce energetickými elektrony. V literatuře lze najít publikace s pozitivním hodnocením této léčebné modality. Němečtí autoři použili metodu nízce energetických elektronů (9 MeV v celkové dávce 20 Gy a denní dávce 2 Gy) pro léčbu pacienta, u něhož nebyla fototerapie účinná. Autoři popisují efekt této léčby jako drobné zlepšení, vymizení pruritu, ale nedošlo k signifikantní změně kožní tloušťky. Autoři této publikace jsou k možnosti přínosu radioterapie v této indikaci kritičtější než dřívější publikace [28].
Vysokodávkovaná chemoterapie
Vysokodávkovaná chemoterapie s transplantací autologních kmenových buněk je standardní léčebný postup pro symptomatický mnohočetný myelom. Je však účinným léčebným postupem i při nízce agresivních (low-grade) plazmocelulárních proliferacích, jako je primární systémová AL-amyloidóza a POEMS syndrom, tedy jednotky, u nichž je pouze malý počet klonálních plazmocytů v kostní dřeni a není dynamický vzestup MIg. Vyšší počet léčebných odpovědí u osob s nízkou koncentrací MIg než u osob s vyšší koncentrací MIg popsal již v roce 1995 Singhal. V roce 2001 byla poprvé popsána kompletní remise skleromyxedému po vysokodávkované chemoterapii s autologní transplantací kostní dřeně. Následně bylo popsáno více než 20 případů, kdy byl skleromyxedém úspěšně a dlouhodobě vyléčen pomocí tohoto postupu [29–30]. Léčba vysokodávkovanou chemoterapií s autologní transplantací krvetvorných buněk představuje pro pacienty s mucinózou a monoklonální gamapatií efektivní léčebnou možnost. Její použití je však limitováno věkem nemocného a současnými komorbiditami, případně poškozením vnitřních orgánů mucinózou.
Léčebné postupy používané též u mnohočetného myelomu
V literatuře lze najít zprávy popisující pacienty s mnohočetným myelomem, u nichž chemoterapie dosáhla hematologické kompletní remise a zároveň došlo k zásadnímu ústupu či totálnímu vymizení projevů skleredému. Klasickým cytostatikem pro myelom je melfalan, a proto byl použit také při léčbě mucinózy s přítomností MIg. Vpřípadech, kdy melfalan vedl k vymizení MIg (s dosažením negativní imunofixace), došlo i k vymizení projevů mucinózy. Následně byly používány i další léčebné postupy klasicky používané pro mnohočetný myelom, například cyklofosfamid a dexametazon. A samozřejmě lze najít i popisy úspěšné léčby mucinóz novými léky registrovanými pro mnohočetný myelom, jako jsou thalidomid, bortezomib a lenalidomid [31–38].
IgA pemfigus a léčebné možnosti
Monoklonální imunoglobulin typu IgA se může vázat na antigenní determinanty kůže, a způsobovat tak puchýřnaté onemocnění kůže. Je to další kožní projev, který může provázet lymfoproliferativní a také plazmocelulární onemocnění. V našem případě se podařilo prokázat depozita imunoglobulinu typu IgA v kožních ložiscích a dosažení kompletní remise vedlo k úplnému vymizení kožních projevů. To považujeme jako důkaz, že vyvolávajícím činitelem puchýřnatého onemocnění byl MIg IgA [39–42]. Cílem léčby je tedy dosáhnout vymizení monoklonálního imunoglobulinu. Tato komplikace monoklonální gamapatie je ještě vzácnější než mucinózy.
ZÁVĚRY PRO PRAXI
- Monoklonální imunoglobulin se v ojedinělých případech váže na autoantigeny, a to může vést k pestrým klinickým projevům.
- Monoklonální imuglobulin může stimulovat tvorbu mucinu, a způsobit tak ve vzácných a ojedinělých případech onemocnění zvané skleredém a skleromyxedém s viditelným a hmatatelným ztluštěním kůže a podkoží, limitující postupně pohyb a polykání.
- Vazba monoklonálního imunoglobulinu typu IgA na antigeny epidermis může velmi vzácně indukovat puchýřnaté onemocnění typu pemfigus.
- U těchto vzácných kožních onemocnění sdružených s přítomností MIg jsme pozorovali vymizení kožních projevů v případě vymizení MIg (negativní imunofixace) a obnovení kožního onemocnění při recidivě monoklonální gamapatie.
- Při diagnóze těchto vzácných kožních onemocnění je vhodné vyšetřit také monoklonální imunoglobulin. Pokud jej prokážeme, jde o monoclonal immunoglobulin releated disease a je vhodné zahájit léčbu této monoklonální gamapatie sdružené se závažnými kožními projevy, i když nejsou vždy naplněna kritéria symptomatického mnohočetného myelomu.
Podíl autorů na přípravě rukopisu
KZ, AZ – příprava rukopisu
KM, LP, ŠS, ČZ – korekce a revize rukopisu
Čestné prohlášení autorů
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Do redakce doručeno dne 17. 2. 2020.
Přijato po recenzi dne 15. 4. 2020.
prof. MUDr. Zdeněk Adam, CSc.
Interní hematologická a onkologická klinika LF MU a FN Brno
Jihlavská 20,
625 00 Brno
e-mail: adam.zdenek@fnbrno.cz
Zdroje
1. Pock L. Kožní mucinózy. Českoslov Dermatol. 2006;81 : 313–325.
2. Žamboch K, Ščudla V, Pika T, et al. Vzácná koincidence papulární mucinózy s primární systémovou AL-amyloidózou. Intern Med Praxi. 2008;10 : 248–250.
3. Žamboch K, Tichá V, Pika T, et al. Vzácná koincidence papulární mucinózy (lichen myxedematosus) s primární AL-amyloidózou. Vnitř Lék. 2007;53 : 591–592.
4. Drlík L, Pock L, Paťavová V, et al. Retikulární erytematózní mucinóza. Dermatol Praxi. 2011;5 : 150–151.
5. Sainerová A, Vencovský J. Skleromyxedém. Čes Revmatol. 1998;6 : 90–91.
6. Pock L, Abrahámová S. Retikulární erytematózní mucinóza. Českoslov Dermatol. 2000;72 : 117–119.
7. Štork J, Vosmík F. Klinický případ: erytémy trupu. Českoslov Dermatol. 1997;72 : 205–206.
8. Štítná M, Rasochová E. Diseminované voskové papuly a facies leontina. Českoslov Dermatol. 2012;87 : 57–59.
9. Štork J. Kožní fibróza u systémové sklerodermie a její diferenciální diagnóza. Postgrad Med. 2014;14 : 212–218.
10. Kreidy M, Al-Hilli A, Yachoui R, et al. Severe but reversible pulmonary hypertension in scleromyxedema and multiple myeloma: a case report. BMC Pulm Med. 2020; publikováno elektronicky 9. ledna 2020. DOI 10.1186/s12890-019-1020-6.
11. Feyereisn WL, Fenstad ER, McCully RB, et al. Severe reversible pulmonary hypertension in smoldering multiple myeloma: two cases and review of the literature. Pulm Circ. 2015;5 : 211–216.
12. Rostagno C, Ciolli S. Transient severe symptomatic pulmonary hypertension as onset symptom in multiple myeloma. Ann Hematol. 2006;85 : 627–628.
13. De Simone C, Castriota M, Carbone A, et al. Cardiomyopathy in scleromyxedema: report of a fatal case. Eur J Dermatol. 2010;20 : 852 – 853.
14. Fleming KE, Virmani D, Sutton E, et al. Scleromyxedema and the dermato-neuro syndrome: case report and review of the literature. J Cutan Pathol. 2012;39 : 508–517.
15. Rongioletti F, Merlo G, Cinotti E, et al. Scleromyxedema: a multicenter study of characteristics, comorbidities, course, and therapy in 30 patients. J Am Acad Dermatol. 2013;69 : 66–72.
16. Dogra S, Handa S, Kanwar AJ. Dexamethasone pulse therapy for scleredema. Pediatr Dermatol. 2004;21 : 280–281.
17. Kurtoğlu S, Yüksel S, Gündüz Z, et al. Use of high-dose intravenous corticosteroid treatment in a child with scleredema. J Emerg Med. 2004;26 : 245–246.
18. Lister RK, Whittaker JS, Blafl C, et al. Scleredema: response to high dose intravenous imunoglobulin J Amer Acad Dermatol. 2000;43 : 403–408.
19. Caudill L, Howell E. Scleromyxedema: a case clinically and histologically responsive to intravenous immunoglobulin. J Clin Aesthet Dermatol. 2014;7 : 45–47.
20. Macnab M, Kenny P. Successful intravenous immunoglobulin treatment of atypical lichen myxedematosus associated with hypothyroidism and central nervous system involvement: case report and discussion of the literature. J Cutan Med Surg. 2013;17 : 69–73.
21. Majeski C, Taher M, Grewal P, et al. Combination oral prednisone and intravenous immunoglobulin in the treatment of scleromyxedema. J Cutan Med Surg. 2005;9 : 99–104.
22. Wojas-Pelc A, Błaszczyk M, Glińska M, et al. Tumorous variant of scleromyxedema. Successful therapy with intravenous immunoglobulins. J Eur Acad Dermatol Venereol. 2005;9 : 462–565.
23. Bidier M, Zschoche C, Gholam P, et al. Scleromyxoedema: clinical follow-up after successful treatment with high-dose immunoglobulins reveals different long-term outcomes. Acta Derm Venereol. 2012;92 : 408–409.
24. Sroa N, Campbell S, Bechtel M. Intravenous immunoglobulin therapy for scleromyxedema: a case report and review of literature. J Drugs Dermatol. 2010;9 : 263–265.
25. Açikgöz G, Özmen I, Hüseynov S, et al. A case of atypical scleromyxedema without gammopathy treated with cyclosporine. Indian J Dermatol Venereol Leprol. 2014;80 : 278–279.
26. Guarenti I, Sebastiani V, Pinto G, et al. Successful treatment of scleromyxedema with oral thalidomide. Int J Dermatol. 2013;52 : 631–632.
27. Amini-Adle M, Thieulent N, Dalle S, et al. Scleromyxedema: Successful treatment with thalidomide in two patients. Dermatol. 2007;214 : 58–60.
28. Könemann S, Hesselmann S, Bölling T, et al. Radiotherapy of benign diseases-scleredema adultorum Buschke. Strahlenther Onkol. 2004;180 : 811–814.
29. Devos T, Thiessen S, Cuyle PJ, et al. Long-term follow-up in a patient with the dermato-neuro syndrome treated with high-dose melphalan, thalidomide, and intravenous immunoglobulins for more than 7 years. Ann Hematol. 2014;93 : 1927–1928.
30. Braue A, Dolianitis C, Varigos G. Spontaneous resolution of facial popular mucinosis in a transplant patient. Australas J Dermatol. 2008;49 : 164–166.
31. Szturz P, Adam Z, Vašků V, et al. Complete remission of multiple myeloma associated scleredema after bortezomib-based treatment. Leuk Lymphoma 2013;54 : 1324–1326.
32. Santos-Juanes J, Osuna CG, Iglesias JR, et a. Treatment with chemotherapy of scleredema associated with Ig A myeloma. Int J Dermatol. 2001;40 : 720–721.
33. Schubert K, Stein A, Meurer M. Initial scleromyxedema. Successful treatment with melphalan. Hautarzt. 2002;53 : 478–482.
34. Kuldeep CM, Mittal AK, Gupta LK, et al. Successful treatment of scleromyxedema with dexamethasone cyclophosphamide pulse therapy. Indian J Dermatol Venereol Leprol. 2005;71 : 44–45.
35. Yeung CK, Loong F, Kwong YL. Scleromyxoedema due to a plasma cell neoplasm: rapid remission with bortezomib, thalidomide and dexamethasone. Br J Haematol. 2012;157 : 411–412.
36. Hájek R. Vývoj diagnostiky a léčby mnohočetného myelomu v průběhu posledních 25 let. Transfuze Hematol Dnes. 2019; 25 : 96–106.
37. Krejčí M, Vacková B, Krejčová H., et al. Autologní transplantace u 495 pacientů s mnohočetným myelomem – analýza dat z Národního registru transplantací krvetvorných buněk České republiky. Transfuze Hematol Dnes 2007;13 : 56–62.
38. Zemanová M, Ščudla V, Pour, L, et al. Režim CTD (cyklofosfamid, thalidomid, dexametazon) v léčbě relabujících a refrakterních forem mnohočetného myelomu. Transfuze Hematol Dnes 2007;13 : 126–132.
39. von dem Borne PA, Jonkman MF, van Doorn R. Complete remission of skin lesions in a patient with subcorneal pustular dermatosis (Sneddon-Wilkinson disease) treated with antimyeloma therapy: association with disappearance of M-protein. Br J Dermatol. 2017;176 : 1341–1344.
40. España A, Gimenez-Azcarate A, Ishii N, et al. Antidesmocollin 1 autoantibody negative subcorneal pustular dermatosis-type IgA pemphigus associated with multiple myeloma. Br J Dermatol. 2015;172 : 296–298.
41. Cetkovská P, Komorousová M, Lomicová I. Management of a pemphigus with IgA and IgG antibodies and coexistent lung cancer. Dermatol Ther. 2014;27 : 236–269.
42. Aste N, Fumo G, Pinna AL, et al. IgA pemphigus of the subcorneal pustular dermatosis type associated with monoclonal IgA gammopathy. J Eur Acad Dermatol Venereol. 2003;17 : 725–727.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2020 Číslo 3- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Definice a klasifikace chronického onemocnění ledvin dle KDIGO
-
Všechny články tohoto čísla
- COVID-19 a transfuzní služba v ČR
- Regenerující krvetvorba se podobá embryonální krvetvorbě nezávislé na kmenových buňkách
- Příznaky a projevy Erdheimovy-Chesterovy choroby
- Aktuální pohled na léčbu nově diagnostikovaných nemocných s periferními T-lymfomy a novinky v této oblasti s důrazem na využití brentuximab vedotinu
- Léčba multicentrické a unicentrické formy Castlemanovy nemoci
- Tematizace problémů komplexní péče z perspektivy osob s hemofilií
- Hodnocení znalosti transfuzního lékařství u lékařů po promoci v Turecku
- Charakteristika a výsledky léčby mladších nemocných s akutní myeloidní leukemií pod 60 let: Analýza reálných dat z české databáze DATOOL-AML
- Vzácné kožní změny asociované s monoklonální gamapatií: skleredém, skleromyxedém a IgA pemfigus – popis pěti případů a přehled léčebných možností
- Doporučený postup pro použití rekonvalescentní plazmy v léčbě dospělých pacientů s COVID-19
- Doporučený postup při řešení a vyšetřování potransfuzních reakcí
- Konsenzuální doporučení Českého národního hemofilického programu (ČNHP) pro zajištění chirurgických a invazivních výkonů u pacientů s hemofilií, vydání 2., rok 2020
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Příznaky a projevy Erdheimovy-Chesterovy choroby
- Doporučený postup při řešení a vyšetřování potransfuzních reakcí
- Charakteristika a výsledky léčby mladších nemocných s akutní myeloidní leukemií pod 60 let: Analýza reálných dat z české databáze DATOOL-AML
- Aktuální pohled na léčbu nově diagnostikovaných nemocných s periferními T-lymfomy a novinky v této oblasti s důrazem na využití brentuximab vedotinu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



