-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Vplyv pooperačných komplikácií na prežívanie pacientov s karcinómom pankreasu
Impact of Postoperative Complications on Survival of Patients with Pancreatic Carcinoma
Introduction:
In spite of radical pancreatic resection and adjuvant therapy, the overall 5-year survival rate for patients with pancreatic cancer remains poor, ranging between 5% and 15%, with a median survival of 13 to 17 months.Material and Methods:
Between January 2000 and December 2009, the prospective study was performed to indentify the presence of postoperative complications and to find their influence on survival rate in pancreatic cancer patients.Results:
Between January 2000 and December 2009, the radical pancreatic resection was performed for 102 patients suffer from pancreatic cancer, at the I. Department of Surgery University Hospital in Košice.
Pancreatoduodenectomies were performed in Child-Stulhofer modification in 59 patients, Whipple modification was performed in 31 patients, Waugh-Clagett in 2 patients, Traverso-Longmire in 2 patients, distal resection of pancreas was performed in 7 patients and one patient had made total pancreatectomy.
The overall morbidity rate was 30.2% (31 patients) and mortality rate was 3.9% (4 patients). Specific (for pancreatic resection) complications were indentified in 26 patients, 25.3%. Non-specific complications were presented in 5 patients, 4.9%.
Two intraoperative risk factors were found to be significantly associated with pancreatic leakage, small pancreatic duct size and soft texture of the remnant pancreas.
The 5-years survival rate for patients with pancreatic cancer was in 5 patients, 4.9 %, with median survival rate 15 months. In group of patients with postoperative complications median survival rate was 13 months, in group of patients without postoperative complications median survival time was 18 months.Conclusion:
Long-term survival rate for pancreatic cancer patients is still low. The presence of postoperative complications had negative influence to survival rate in pancreatic cancer patients. Pancreatic leakage is the most afraid complications. Patients with a small pancreatic duct size or a soft pancreatic remnant were at high risk of pancreatic leakage.Key words:
pancreatic cancer – postoperative complications – pancreatic leakage – survival rate
Autoři: J. Kaťuchová; J. Bober; J. Radoňak
Působiště autorů: I. chirurgická klinika LF UPJŠ a UNLP Košice, Slovenská republika, prednosta: prof. MUDr. J. Radoňak, CSc
Vyšlo v časopise: Rozhl. Chir., 2011, roč. 90, č. 3, s. 174-181.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Úvod:
Napriek radikálnej chirurgickej a adjuvatnej onkologickej liečbe je päťročné prežívanie pacientov s karcinómom pankreasu naďalej alarmujúce, 5–15 %, s mediánom 13–17 mesiacov.Materiál a metódy:
Na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach bola od 1. 1. 2000 do 31. 12. 2009 vykonaná prospektívna štúdia na sledovanie vplyvu pooperačných komplikácií na prežívanie pacientov s karcinómom pankreasu.Výsledky:
Na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach bola od 1. 1. 2000 do 31. 12. 2009 vykonaná radikálna resekcia pankreasu pre duktálny pankreatický adenokarcinóm u 102 pacientov.
Duodenohemipankreatektómia bola vykonaná v modifikácii Child-Stulhofer 59x, Whipple 31x, Waugh-Clagett 2x, Traverso-Longmire 2x, 7x distálna hemipankreatektómia a u jedného pacienta bola vykonaná totálna pankreatektómia.
Pri hodnotení pooperačných komplikácií bola zaznamenaná 30,2% morbidita (31 pacientov) a 3,9% mortalita (4 pacienti). Komplikácie špecifické pre resekciu pankreasu boli u 26 pacientov, 25,3 %. Komplikácie nie špecifické pre resekčné výkony pankreasu boli u 5 pacientov, 4,7 %.
Pri sledovaní rizikových faktorov vzniku pankreatickej fistuly, bola zaznamenaná štatistická významnosť medzi vznikom pankreatickej fistuly a úzkym pankreatickým vývodom ako aj mäkkým tkanivom pankreasu.
V sledovanom súbore bolo zaznamenané 5-ročné prežívanie u piatich pacientov, 4,9 %, medián prežívania bol 15 mesiacov. U pacientov s prítomnými pooperačnými komplikáciami bol zistený medián prežívania 13 mesiacov, u pacientov bez prítomných pooperačných komplikácií bol medián prežívania 18 mesiacov.Záver:
Prežívanie pacientov s karcinómom pankreasu je naďalej nízke. Vplyv na jeho dĺžku majú aj prítomné pooperačné komplikácie. Najčastejšou a najobávanejšou pooperačnou komplikáciou je pankreatická fistula, ktorej rizikové faktory sú úzky pankreatický vývod a soft pankreas.Kľúčové slová:
karcinóm pankreasu – pooperačné komplikácie – pankreatická fistula – prežívanieÚVOD
Karcinóm pankreasu je na Slovensku šiestym najčastejším nádorovým ochorením, v USA štvrtým a vo Veľkej Británii šiestym, je to druhý najčastejší nádor tráviaceho traktu. Najviac je pozorovaný v populácii 65–75-ročných [1, 2, 3, 4]. Väčšina pacientov prichádza v pokročilom štádiu ochorenia, kde je možnosť resekčných výkonov nízka [5, 6, 7, 8].
Vznik špecializovaných centier je pravdepodobne hlavný dôvod zníženia pooperačných komplikácií a úmrtí po resekciách pankreasu [3, 9, 10, 11]. Jednoznačne bolo potvrdené, že táto oblasť chirurgie vyžaduje skúseného operatéra a je dokázaný vzťah medzi počtom operácií vykonaných na danom pracovisku a počtom pooperačných komplikácií a úmrtnosťou [12, 13, 14].
Na dlhodobé prežívanie pacientov s karcinómom pankreasu majú vplyv aj pooperačné komplikácie [12]. Medzi najobávanejšie patrí pankreatická fistula.
PACIENTI A METÓDY
Na I. chirurgickej klinike LF UJPŠ a UNLP v Košiciach bola v období od 1. 1. 2000 do 31. 12. 2009 vykonaná prospektívna štúdia zameraná na sledovanie vplyvu pooperačných komplikácií na prežívania pacientov s karcinómom pankreasu.
U pacientov boli sledované bezprostredné pooperačné komplikácie v období počas hospitalizácie a pri prvej pooperačnej kontrole tridsať dní po operácii. Pooperačné komplikácie boli rozdelené na komplikácie špecifické pre operačný výkon a komplikácie, ktoré sa vyskytujú aj pri iných typoch brušných operačných výkonov. Ku špecifickým komplikáciám boli zaradené pooperačné krvácanie, prítomnosť dehiscencií (leaku) vykonaných anastomóz, spomalené vyprázdňovanie žalúdka, prítomnosť pooperačného abscesu v brušnej dutine.
Z pooperačných komplikácií bola podrobnejšie sledovaná pankreatická fistula. V súbore bola na definíciu pankreatickej fistuly použitá definícia podľa Baltimorskej skupiny, kde je pankreatická fistula určená „ako odtok tekutín v dréne v množstve viac ako 50 ml/24 hod s hodnotou amyláz viac ako trojnásobok sérovej hodnoty v priebehu viac ako 10 dní“ [15].
Medzinárodná študijná komisia pre pankreatickú fistulu (International Study Group of Pancreatic Fistula ISGPF) vypracovala novú definíciu pankreatickej fistuly, ktorá rozdeľuje pankreatické fistuly podľa závažnosti na tri skupiny A, B, C [16]. Pankreatická fistula v sledovanom súbore bola rozdelená aj podľa klasifikácie ISGPF na typy A, B, C.
Medzi pooperačné komplikácie, ktoré nesúvisia bezprostredne s daným typom operačného výkonu boli zaradené infarkt myokardu, pľúcna embólia, cievna mozgová príhoda, pneumónia a uroinfekcia.
Podrobnejšie boli sledované rizikové faktory vzniku najobávanejšej komplikácie pri resekciách pankreasu, ktorou je pankreatická fistula. Pri hodnotení všeobecných rizikových faktorov vzniku pankreatickej fistuly boli zo súboru vylúčení pacienti s distálnou hemipankreatektómiou a pacient po totálnej pankreatektómii, kde pankreatická anastomóza nebola vykonávaná. Pri sledovaní peroperačných rizikových faktorov boli vylúčení dvaja pacienti s pankreatogastroanastomózou, porovnávaný bol súbor pacientov s vykonanou pankreatojejunoanastomózou, pričom bola sledovaná modifikácia anastomózy end-to-side a end-to-end.
Medzi všeobecnými rizikovými faktormi vzniku pankreatickej fistuly boli sledované vek pacientov, pohlavie, prítomnosť žltačky a podávanie Oktreotidu. Oktreotid v sledovanom súbore bol podávaný ako prevencia vzniku pankreatickej fistuly. Prvá dávka bola podávaná pred operáciou jednu hodinu 0,1mg subkutánne, celkovo boli denne podávané tri dávky a liečba pokračovala sedem dní. Medzi peroperačné rizikové faktory boli zaradené spôsob rekonštrukcie pankreatickej anastomózy (end-to-end a end-to-side), šírka pankreatického vývodu (< 3 mm a ≥ 3 mm), kvalita ponechaného tkaniva pankreasu (mäkké tkanivo pankreasu, soft pankreas a tuhý, fibrotický pankreas, hard pankreas), peroperačná strata krvi ako aj dĺžka samotnej operácie.
Zaznamenávané a vyhodnotené bolo prežívanie pacientov s karcinómom pankreasu a sledovaný bol vplyv prítomných pooperačných komplikácií na dlhodobé prežívanie.
Na porovnanie výskytu sledovaného znaku medzi skupinami bol použitý 2test, resp. Fisherov exaktný test, na vyjadrenie miery významnosti rozdielov stredných hodnôt vybraných ukazovateľov medzi jednotlivými skupinami sme použili nepárový t-test u parametrických dát, resp. neparametrický Mannov-Whitneyho test. Analýza prežívania sledovaných parametrov bola vyhodnotená Kaplanovou-Meierovou metódou. U všetkých testov bola hladina štatistickej významnosti zvolená p = 0,05
VÝSLEDKY
Sledovaný súbor hodnotí 102 pacientov operovaných na I. chirurgickej klinike LF UPJŠ a UNLP v Košiciach v období od 1. 1. 2000 do 31. 12. 2009, ktorým bola vykonaná resekcia pankreasu pre duktálny pankreatický karcinóm.
V súbore bolo 57 mužov a 45 žien, vekové rozmedzie zastúpených pacientov bolo 32–85 rokov, priemerný vek pacientov 60,86 rokov. Rozdelenie súboru pacientov popisujú tabuľka 1 a graf 1. Nebol zaznamenaný štatisticky významný rozdiel medzi vekovým zastúpením v skupine mužov a žien.
Tab. 1. Pacienti s resekčným výkonom pankreasu pre karcinóm pankreasu 2000–2009 Tab. 1. Group of pancreatic cancer patients after radical pancreatic resection 2000–2009 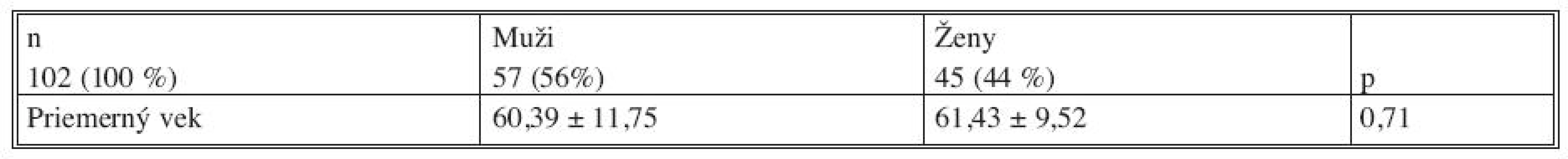
Graf 1. Súbor všetkých pacientov s resekčným výkonom pankreasu pre karcinóm pankreasu 2000–2009 Graph 1. Group of pancreatic cancer patients after radical pancreatic resection 2000–2009 
V sledovanom súbore bola cefalická duodenohemipankreatektómia 94krát, v modifikácii Child-Stulhofer 59krát, Whipple 31krát, Waugh-Clagett 2krát, so zachovaním pyloru – Traverso-Longmire 2krát. Distálna (ľavostranná) hemipankreatektómia bola vykonaná 7 pacientom. U jedného pacienta bola vykonaná totálna pankreatektómia. Zastúpenie jednotlivých operačných výkonov popisuje tabuľka 2 a graf 2.
Tab. 2. Vykonané operačné resekčné výkony pre karcinóm pankreasu 2000–2009 Tab. 2. Type of radical resection performed for pancreatic cancer 2000–2009 
Graf 2. Resekčné výkony pre karcinóm pankreasu 2000– –2009 Graph 2. Type of radical resection performed for pancreatic cancer 2000–2009 
V predloženom súbore bola zaznamenaná 30,2% morbidita (31 pacientov) a 3,9% mortalita (4 pacienti). Podrobné rozdelenie pooperačných komplikácií zaznamenávajú tabuľky 3, 4, 5. Najčastejšie bola prítomná pankreatická fistula u 13 pacientov (12,8 %), dehiscencia biliárnej anastomózy bola prítomná u 4 pacientov (3,9 %), dehiscencia gastroenteroanastomózy nebola v súbore zaznamenaná. Krvácanie do brušnej dutiny bolo pozorované u jedného pacienta (0,9 %), išlo o krvácanie z okolia ligamenta hepatoduodenálneho, pri reoperácii bolo krvácanie ošetrené, krvácanie do GIT bolo sledované u dvoch pacientov (1,9 %), išlo o krvácanie z gastroenteroanastomózy, ktoré bolo ošetrené endoskopicky. Spomalené vyprázdňovanie žalúdka bolo prítomné u dvoch pacientov (1,9 %), stav pacientov sa po konzervatívnej liečbe upravil a nevyžadoval operačnú revíziu.
Tab. 3. Pooperačné komplikácie – špecifické Tab. 3. Postoperative complications – specific 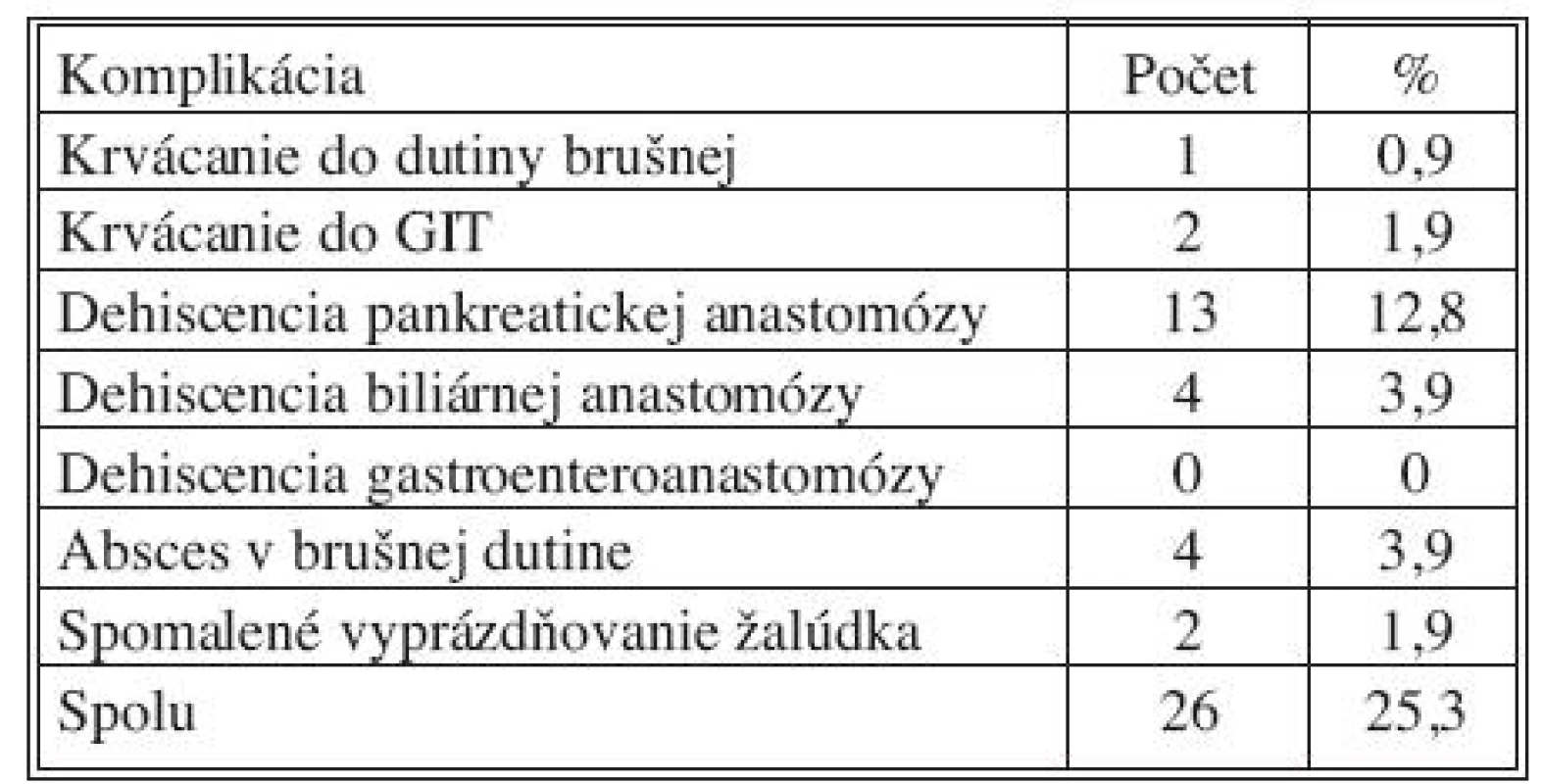
Tab. 4. Pooperačné komplikácie – nešpecifické Tab. 4. Postoperative complications – non specific 
Tab. 5. Pooperačná úmrtnosť pacientov po radikálnej resekcii pre karcinóm pankreasu Tab. 5. Mortality rate of pancreatic cancer patients after radical pancreatic resection 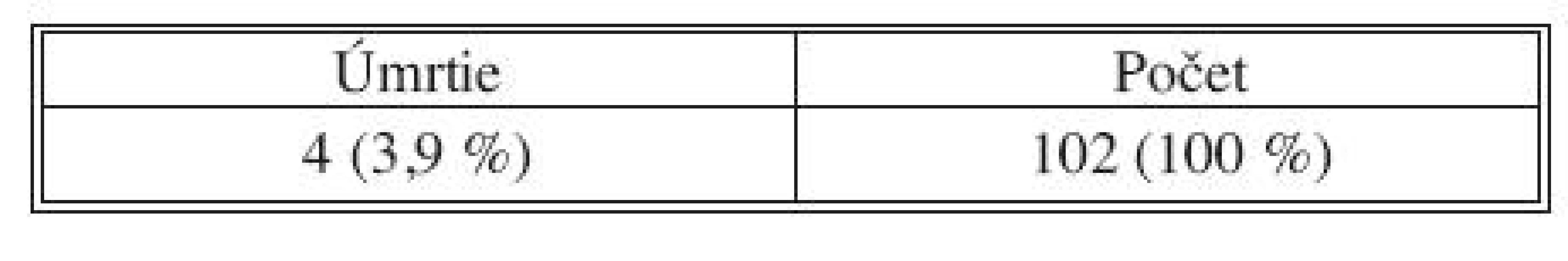
Tab. 6. Všeobecné rizikové faktory vzniku pankreatickej fistuly Tab. 6. General risk factors for pancreatic leakage 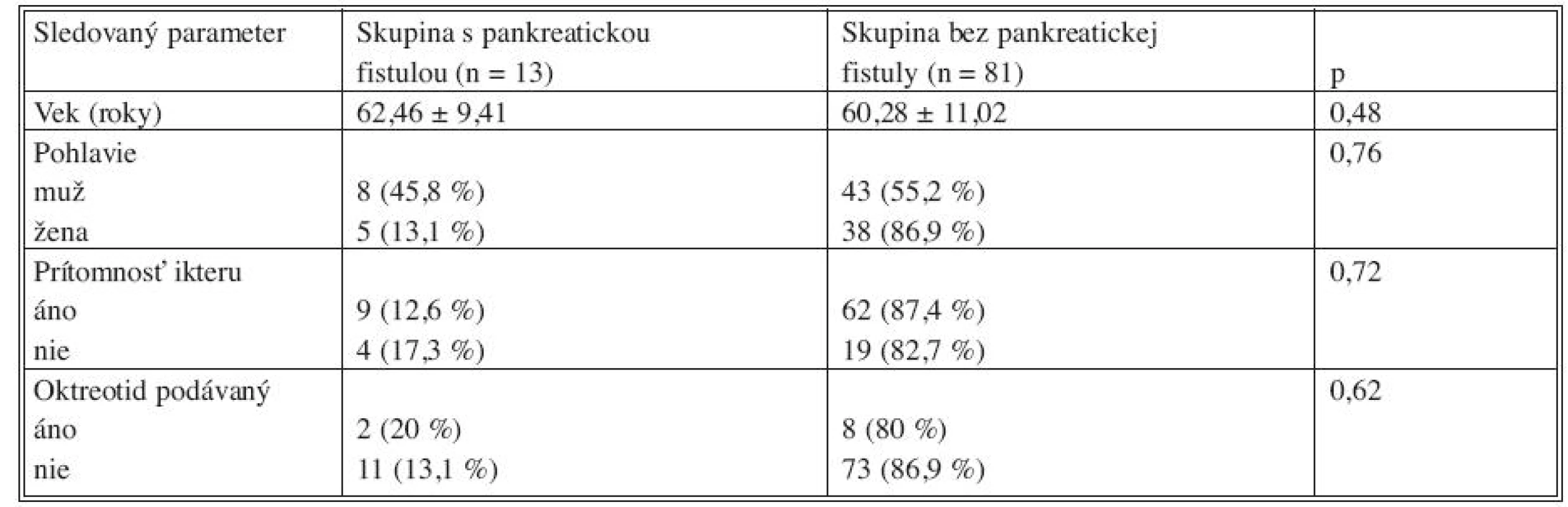
Tab. 7. Peroperačné rizikové faktory vzniku pankreatickej fistuly Tab. 7. Intraoperative risk factors for pancreatic leakage 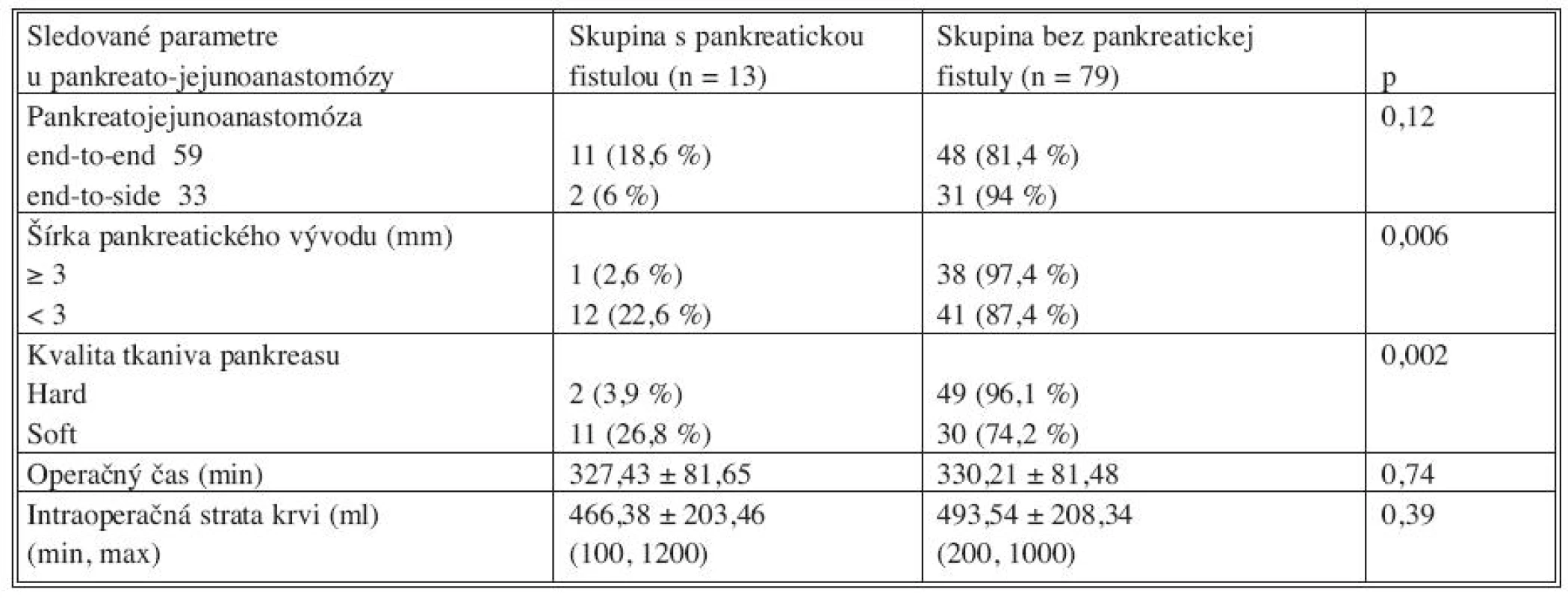
Z pooperačných komplikácií bola podrobnejšie sledovaná pankreatická fistula. V sledovanom súbore bola zaznamenaná pankreatická fistula typ A u 10 pacientov, typ B u 2 pacientov a najzávažnejší typ C u 1 pacienta. Pankreatická fistula typ A a typ B bola riešená konzervatívne. Pankreatická fistula typ C bola riešená reoperáciou a opakovanou drenážou. Celkový stav pacienta bol komplikovaný sepsou, následkom ktorej pacient exitoval.
Mortalita v sledovanom súbore bola 3,9 %, štyria pacienti exitovali, jeden pacient s pankreatickou fistulou typu C a traja pacienti na komplikácie nešpecifické: infarkt myokardu, pľúcnu embóliu a pneumóniu.
Podrobnejšie boli sledované rizikové faktory vzniku najobávanejšej komplikácie pri resekciách pankreasu, ktorou je pankreatická fistula. Pri vyhodnotení všeobecných rizikových faktorov vzniku pankreatickej fistuly boli zo súboru boli vylúčení pacienti s distálnou hemipankreatektómiou, ako aj pacient po totálnej pankreatektómii, kde pankreatická anastomóza nebola vykonávaná. Medzi všeobecné rizikové faktory vzniku pankreatickej fistuly boli zaradené vek pacientov, pohlavie, prítomnosť žltačky a podávanie Oktreotidu. Pri vyhodnotení všeobecných rizikových faktorov bolo zistené, že na vznik pankreatickej fistuly nemajú vplyv: vek pacienta, pohlavie, prítomnosť žltačky ani podávanie Oktreotidu. Medzi peroperačné rizikové faktory boli zaradené spôsob rekonštrukcie pankreatickej anastomózy, šírka pankreatického vývodu, kvalita ponechaného tkaniva pankreasu, peroperačná strata krvi ako aj dĺžka samotnej operácie. Na vznik pankreatickej fistuly nemali vplyv spôsob rekonštrukcie pankreatickej anastomózy, peroperačná strata krvi ani dĺžka samotnej operácie. Bolo dokázané, že úzky pankreatický vývod < 3 mm a mäkké tkanivo v ponechanom zvyšku pankreasu sú hlavné rizikové faktory vzniku pankreatickej fistuly. Štatistická významnosť rizika vzniku pankreatickej fistuly pri úzkom pankreatickom vývode bola dokázaná p = 0,006, v prípade mäkkého tkaniva pankreasu p = 0,002.
V predloženom súbore 102 pacientov s duktálnym pankreatickým karcinómom pankreasu bolo vyhodnotené pooperačné prežívanie po radikálnej resekcii pankreasu, pričom bol sledovaný vplyv pooperačných komplikácií na prežívanie. V celom súbore 102 pacientov bol medián prežívania 15 mesiacov, v skupine pacientov s prítomnými pooperačnými komplikáciami bol medián prežívania 13 mesiacov, v skupine pacientov bez pooperačných komplikácií bol medián prežívania 18 mesiacov (Tab. 8, Graf 3, 4, 5). Päťročné prežívanie bolo zaznamenané u piatich pacientov 4,9 % (Tab. 8, Graf 3). V štádiu IA bolo 5 pacientov s mediánom prežívania 25 mesiacov, v štádiu IB bolo 12 pacientov s mediánom prežívania 18 mesiacov, v štádiu IIA bolo prítomných 35 pacientov s mediánom prežívania 14 mesiacov, v štádiu IIB bolo prítomných 45 pacientov s mediánom prežívania 15 mesiacov, v štádiu III boli prítomní 3 pacientov s mediánom prežívania 8 mesiacov a v štádiu IV boli zaznamenaní 2 pacientov s mediánom prežívania 2 mesiace.
Tab. 8. Prežívanie pacientov s karcinóm pankreasu po radikálnej resekcii Tab. 8. Survival pancreatic cancer patients post pancreatic resection 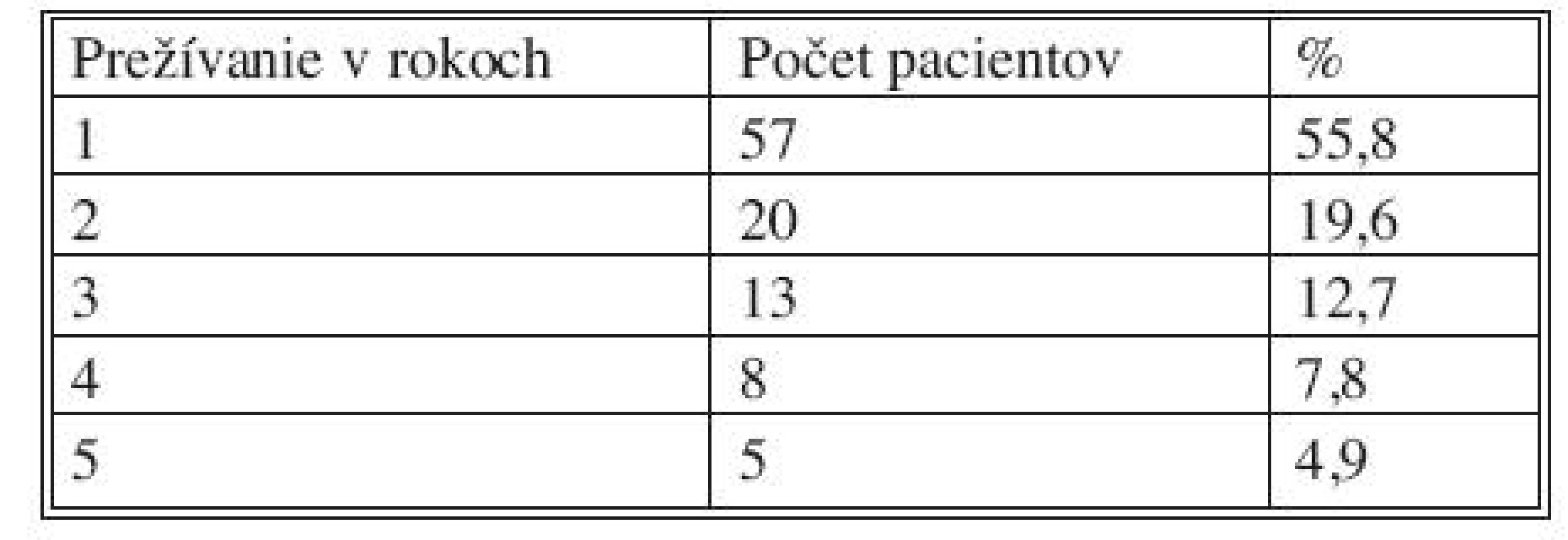
Tab. 9. Medián prežívania pacientov s karcinómom pankreasu po radikálnej resekcii, zaznamenané podľa štádia ochorenia Tab. 9. Median survival pancreatic cancer patients after pancreatic resection according to staging of disease 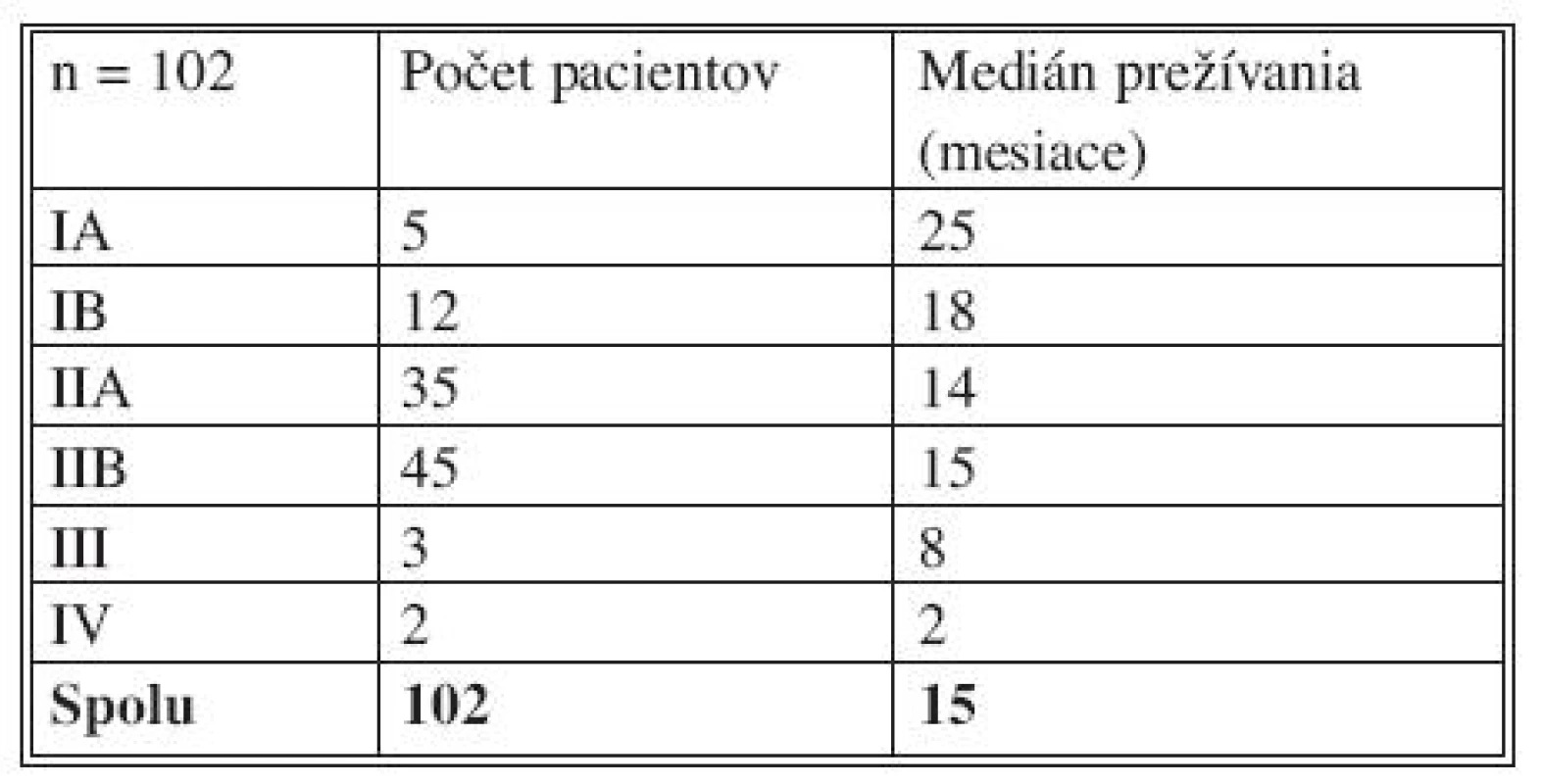
Graf 3. Prežívanie pacientov s karcinómom pankreasu po radikálnej resekcii Graph 3. Survival pancreatic cancer patients post pancreatic resection 
Graf 4. Prežívania pacientov s karcinómom pankreasu po radikálnej resekcii, zaznamenané podľa štádia ochorenia Graph 4. Survival pancreatic cancer patients after pancreatic resection according to staging disease 
Graf 5. Prežívanie v celom súbore pacientov s karcinómom pankreasu po radikálnej resekcii Graph 5. Survival pancreatic cancer patients in whole group of patients after radical resection 
Graf 6. Prežívanie pacientov s karcinómom pankreasu v skupinách s a bez prítomných pooperačných komplikácií, group 1 bez prítomných pooperačných group 2 s prítomnými pooperačnými komplikáciami Graph 6. Survival rate in patients with pancreatic cancer and presence of postoperative complications, group 1 without postoperative complications, group 2 with postoperative complications. Group 1 Median survival time (95,% CI) = 18, (13, to 20,) Group 2 Median survival time (95,% CI) = 13, (5, to 15,) 
DISKUSIA
Resekcie pankreasu sa v špecializovaných centrách stávajú bežným operačným výkonom. Operačný čas, peroperačná strata krvi ako aj dĺžka pooperačnej hospitalizácie dramaticky poklesli. Resekčné výkony pankreasu sú bezpečné operácie s pomerne nízkou mortalitou [10].
Napriek výraznému poklesu úmrtnosti po týchto operáciách (3–8 %), počet pooperačných komplikácií ostáva pomerne vysoký (20–70 %). Koncentrácia pacientov v špecializovaných centrách znižuje úmrtnosť aj pooperačnú chorobnosť [3, 9, 10].
V sledovanom celom súbore pacientov boli vyhodnotení pacienti I. chirurgickej kliniky LF UPJŠ a UNLP, Tr. SNP 1 v Košiciach operovaní od 1. 1. 2000 do 31. 12. 2009 pre karcinóm pankreasu, ktorým bola vykonaná radikálna resekcia. V súbore 102 pacientov bola zaznamenaná morbidita 30,2 %, perioperačná mortalita predstavovala 3,9 %.
Najrizikovejšiu z vykonaných anastomóz udávajú viacerí autori pankreatickú anastomózu. Referovaný počet pankreatických fistúl alebo leaku pankreatickej anastomózy je po duodenohemipankreatektómii od 2 do 24 % [12, 17, 18, 19]. Donedávna nebola jednoznačne určená štandardná definícia pankreatickej fistuly. Bassi a kol. zozbieral v literatúre 26 rôznych klasifikácií pankreatickej fistuly, z ktorých určil štyri základné skupiny, pričom podľa týchto klasifikácií určil percento fistúl vo vlastnom súbore 242 pacientov po duodenohemipankreatektómii, čím zaznamenal fistuly od 9,9 po 28,5 % [20].
Medzinárodná študijná komisia pre pankreatickú fistulu (International Study Group of Pancreatic Fistula ISGPF) vypracovala novú definíciu pankreatickej fistuly, ktorá rozdeľuje pankreatické fistuly na tri skupiny A, B, C. Pankreatická fistula skupiny A je najčastejšia, označovaná ako prechodná, zvyčajne bez klinických prejavov u pacientov. Tento typ fistuly si nevyžaduje antibiotickú liečbu, totálnu parenterálnu výživu, ani liečbu Oktreotidom. Pankreatická fistula skupiny A nepredlžuje dobu hospitalizácie u pacientov, v mnohých prípadoch je nutné ponechať poistné drény dlhšiu dobu. Pankreatická fistula skupiny B je klinicky závažná fistula. Môže byť spojená s bolesťami brucha, zvýšenou telesnou teplotou a leukocytózou. V mnohých prípadoch pacient neprijíma potravu per os, vyžaduje totálnu parenterálnu výživu, alebo enterálnu výživu. Poistné drény musia byť ponechané alebo znovu umiestnené do miesta intraabdominálnych tekutinových kolekcií pod USG alebo CT kontrolou. Pankreatická fistula skupiny B si vyžaduje antibiotickú liečbu a liečbu Oktreotidom, zvyčajne predlžuje dobu hospitalizácie u pacientov a zvyšuje náklady na liečbu. V niektorých prípadoch je možné ponechať poistné drény u pacientov a ich sledovanie ambulantne. Prítomnosť pankreatickej fistuly skupiny C je najzávažnejšou a môže byť potenciálne život ohrozujúcou situáciou. Pacienti musia mať zabezpečenú totálnu parenterálnu výživu, alebo enterálnu výživu, bez príjmu potravy per os, vyžadujú antibiotickú liečbu a liečbu Oktreotidom, zvyčajne sú umiestnení na jednotkách intenzívnej starostlivosti. CT snímky zobrazujú závažné tekutinové kolekcie, ktoré musia byť perkutánne drénované. Ak sa vyskytne sepsa alebo orgánové zlyhávanie je nevyhnutná reoperácia. Pankreatická fistula typu C výrazne predlžuje dobu hospitalizácie, zvyšuje výskyt ďalších pooperačných komplikácií, ako aj riziko pooperačného úmrtia [16]. V sledovanom súbore bola zaznamenaná pankreatická fistula u 13 pacientov, typ A u 10 pacientov, typ B u 2 pacientov a najzávažnejší typ C u 1 pacienta.
Poon a kol. zozbierali literárne údaje za obdobie desať rokov, ktoré potvrdili vlastnými výsledkami, pričom zistili, že na vznik pankreatickej fistuly po duodenohemipankreatektómii nemá vplyv technika anastomózy duct-to-mucosa oproti end-to-side, prípadne invaginačnej anastomózy, ani implantácia kýpťa pankreasu do žalúdka, či podávanie Oktreotidu, ale precíznosť a skúsenosť operatéra [21].
V sledovanom súbore boli u pacientov s vykonanou pankreatojejunoanastomózou porovnávané spôsoby rekonštrukcie, end-to-end anastomóza a end-to side anastomóza. Rozdiely vo výskyte pankreatickej fistuly neboli štatisticky významné.
Podávanie somatostatínových analógov za účelom prevencie pankreatickej fistuly a iných komplikácií nebolo celkom jasne potvrdené. Bolo vykonaných šesť randomizovaných štúdií v Európe, ktoré ukázali zníženie celkových komplikácií, tri z nich taktiež zníženie výskytu pankreatickej fistuly. Skupina v Uhlme v roku 1992 randomizovala 246 pacientov po rozsiahlych pankreatických výkonoch, z toho 200 po resekcii hlavy pankreasu, 31 po resekcii chvosta a v 15 prípadoch iný výkon. Celkovo bol signifikantne nižší výskyt komplikácií v skupine podávaného Oktreotidu ako v kontrolnej skupine s placebom 32 % oproti 55 %. Tento efekt bol ešte výraznejší v skupine pacientov s periampulárnymi tumormi. V roku 1995 Bernská skupina sledovala 247 pacientov najmä pri resekciách pre chronickú pankreatitídu. Celkovo bolo 124 resekcií hlavy pankreasu, 55 ľavostranných hemipankreatektómií, 61krát bola vykonaná pankreatojejunoanastomóza a sedemkrát iný výkon. Prvá dávka bola podaná jednu hodinu pred operáciou. Pooperačné komplikácie boli pri podávaní Oktreotidu signifikantne nižšie ako v skupine s podávaným placebom 16,4 % oproti 29,6 %, výskyt pankreatickej fistuly takisto klesol pri podávaní Oktreotidu na 9,8 % oproti skupine kde nebol podávaný 22,4 %. Podobné výsledky dosiahli dve štúdie z Talianska v rokoch 1994 a 1995, ako aj štúdia z Francúzka z roku 2001 [1].
Štúdia z roku 2004 ktorú vykonal Suc celkovo na skupine 230 pacientov zaznamenala odlišné výsledky. 122 pacientov dostávalo Oktreotid a 108 pacientov placebo. Bolo vykonaných 177 duodenohemipankreatektómií a 53 distálnych hemipankreatektómií. Pacienti dostávali prvú dávku Oktreotidu počas operácie. Nebol zaznamenaný signifikantný rozdiel v počte intraabdominálnych komplikácií oboch skupín. V skupine s podávaným Oktreotidom ich bolo 22 % a v placebo skupine 32 %. Podobne aj výskyt pankreatickej fistuly bol 17 % v skupine pacientov s Oktreotidom oproti 19 % v skupine bez neho [22]. Tri štúdie z USA nezaznamenali žiadny prínos v podávaní somatostatinových derivátov. Štúdia z nemocnice Johns Hopkins z Baltimore pri sledovaní 211 pacientov, zistila pankreatickú fistulu v 9 % v kontrolnej skupine a v 11 % pri podávaní Oktreotidu po duodenohemipankreatektómii, podobne ako aj výskyt komplikácií 34 % v kontrolnej skupine oproti 40 % v sledovanej skupine s Oktreotidom. Pacienti dostávali prvú dávku dve hodiny pred začiatkom operačného výkonu [23].
V sledovanom súbore bolo porovnávané podávanie Oktreotidu ako prevencia vzniku fistuly, nebol zaznamenaný štatisticky významný rozdiel v prítomnosti pankreatickej fistuly.
Bolo zistené, že na vznik pankreatickej fistuly má vplyv kvalita tkaniva pankreasu [24]. Ako soft pankreas, alebo vysoko rizikový bol hodnotený taký, ktorý bol mäkký, krehký, fragilný s úzkym pankreatickým vývodom. Hard pankreas, menej rizikový pre vznik pankreatickej fistuly bol tuhý, fibroticky zmenený, s úzkym alebo dilatovaným pankreatickým vývodom [25, 26]. Leffler udáva v prípadoch soft pankreasu prítomnosť pankreatickej fistuly v 30% a v prípadoch hard pankreasu 3 %, Hashimoto v podobnom sledovaní udáva u soft pankreasu fistulu v 15 % a v prípadoch hard pankreasu žiadnu [25, 26]. Suzuki a kol. vyhodnotili súbor 50 pacientov, pričom v skupine pacientov s ponechaným zvyškom tkaniva hodnoteným ako soft pankreas, 29 pacientov, zaznamenali 4 krát pankreatickú fistulu, v súbore pacientov s hard pankreasom, 21 pacientov, pankreatickú fistulu nezaznamenali [27].
V sledovanom súbore sa vyskytoval soft pankreas 41krát, pričom fistula vznikla u 11 pacientov, hard pankreas bol zaznamenaný u 51 pacientov, pankreatická fistula vznikla u 2 pacientov. Bola potvrdená štatistická významnosť medzi vznikom pankreatickej fistuly a mäkkým tkanivom v ponechanom zvyšku pankreasu p = 0,002.
Na zníženie výskytu pankreatickej fistuly odporúčajú japonskí autori používať typ pankreatickej anastomózy v závislosti od kvality tkaniva pankreasu a od šírky pankreatického vývodu. V prípade soft pankreasu a užšieho pankreatického vývodu ako 3 mm používajú invaginačnú anastomózu a v prípadoch širšieho pankreatického vývodu klasickú duct-to-mucosa techniku anastomózy [27, 28]. V sledovanom súbore bola zistená prítomnosť pankreatickej fistuly v súbore 43 pacientov s užším pankreatickým vývodom ako 3mm u 12 pacientov 22,6 %, oproti súboru 39 pacientov s vývodom rovným a širším ako 3 mm, kde sa vyskytla pankreatická fistula iba u jedného pacienta 2,6 %. Bola potvrdená štatistická významnosť medzi úzkym pankreatickým vývodom, užším ako 3 mm a vznikom pankreatickej fistuly p = 0,006.
Prežívanie pacientov s nádorom pankreasu je napriek radikálnej chirurgickej liečbe a adjuvantnej onkologickej liečbe stále alarmujúce. Autori viacerých pracovísk udávajú päťročné prežívanie len 5–15 % s mediánom 13–17 mesiacov. Yeo a kol. zistili bezprostredný vplyv pooperačných komplikácií na dlhodobé prežívanie po radikálnej resekcii pankreasu pre karcinóm [12].
V sledovanom súbore bol medián prežívania 15 mesiacov, v skupine pacientov s prítomnými pooperačnými komplikáciami bol medián prežívania 13 mesiacov, v skupine pacientov bez pooperačných komplikácií bol medián prežívania 18 mesiacov. Päťročné prežívanie bolo zaznamenané u 5 pacientov 4,9 %.
Koncentráciou pacientov v špecializovaných centrách je možné znížiť pooperačné komplikácie po resekciách pankreasu [3, 9, 10, 11]. Adam a kol. zaznamenali počas siedmych rokov aj na vlastnom pracovisku pokles pooperačných komplikácií, dĺžky trvania operačného výkonu, nutnosti podávania krvných transfúzií a pokles dĺžky pooperačnej hospitalizácie [13]. Americkí autori z Johns Hopkins Hospital v Baltimore dokázali, že nádor pôvodne označený za neresekabilný v nemocnici s menším počtom radikálnych výkonov na pankrease, bol neskôr v špecializovanom pracovisku radikálne operovaný bez nárastu pooperačných komplikácií [14].
ZÁVER
Pri sledovaní pooperačných komplikácií bolo zistené, že prítomnosť najobávanejšej komplikácie, ktorou je pankreatická fistula, neovplyvňuje vek pacientov, pohlavie, prítomnosť žltačky, spôsob rekonštrukcie pankreatickej anastomózy, podávanie somatostatínových derivátov ani peroperačná strata krvi a dĺžka samotnej operácie. Na jej vznik má vplyv kvalita samotného tkaniva pankreasu, rizikovejší pre vznik pankreatickej fistuly je soft pankreas a úzky pankreatický vývod, užší ako 3 mm.
Vyhodnotením dlhodobého prežívania pacientov po radikálnej resekcii pankreasu pre karcinóm bolo potvrdené, že prítomnosť pooperačných komplikácií znižuje prežívanie pacientov. Koncentráciou pacientov s nádorovým ochorením pankreasu v špecializovaných centrách je možné znížiť výskyt pooperačných komplikácií ako aj ich vplyv na dlhodobé prežívanie.
MUDr. Jana Kaťuchová, Ph.D.
I. chirurgická klinika LF UPJŠ a UNLP
Tr. SNP l
040 01 Košice
Slovenská republika
e-mail: jana.katuchova@upjs.sk
Zdroje
1. Alexalis, N., Halloran, C., Raraty, M., et al. Current standards of surgery for pancreatic cancer. Br. J. Surg., 2004; 91 : 1410–1427.
2. Beger, H. G., Matsuno, S., Cameron, J. L. Diseases of the pancreas. Current surgical therapy. 1st edition, Berlin Heidelberg New-York, Springer, 2008.
3. Neoptolemos, J. P., Russell, R. C., Bramhall, S., et al: Low mortality following resection for pancreatic and periampullary tumours in 1026 patients: UK survey of specialist pancreatic units. UK Pancreatic cancer group. Br. J. Surg., 1997; 84 : 1370–1376.
4. Šácha, M., Sákra, L., Havlíček, F. Současný pohled na problematiku karcinomu pankreatu. Rozhl. Chir., 2000; 79 : 123–127.
5. Benassai, G., Mastrorilli, M., Quarto, G., et al. Factors influencing survival after resection for ductal adenocarcinoma of the head of the pancreas. J. Surg. Oncol., 2000; 73 : 212–218.
6. Brennan, M. F., Kattan, M. W., Klimstra, D., et al. Prognostic nomogram for patients undergoing resection for adenocarcinoma of the pancreas. Ann. Surg., 2004; 240 : 293–298.
7. Cameron, J. L. Current surgical therapy. 8th edition, St. Loius, Mosby, 2004.
8. Bober, J., Blažej, I., Sabo-Nácko, J., et al. Karcinóm pankreasu-diagnostika, chirurgická liečba, výsledky. Folia Medica Cassoviensia Universitas Šafarikiana, 1996; 53 : 84–89.
9. Gordon, T. A., Bowmanm, H. M., Tielsch, J. M., et al. Statewide regionalization of pancreaticoduodenectomy and its effect on in-hospital mortality. Ann. Surg., 1998; 228 : 71–78.
10. Gouma, D. J., Greenen R. I., Gulik, T., et al. Rates of complications and death after pancreaticoduodenectomy: Risk factors and the impact of hospital volume. Ann. Surg., 2000; 232 : 786–795.
11. Ho, W., Heslin, M. J. Effect of hospital volume and experience on in-hospital mortality for pancreaticoduodenectomy. Ann. Surg., 2003; 237 : 509–514.
12. Yeo, C. J., Cameron, J. L., Lillemoe, K. D., et al. Pancreaticoduodenectomy with or without distal gastrectomy and extended retroperitoneal lymphadenectomy for periampullary adenocarcinoma, part 2. Randomized control trial evaluating survival, mortality and morbidity. Ann. Surg., 2002; 236 : 355–368.
13. Adam, U., Makowiec, F., Riediger, H., et al. Risk factors for complications after panceratic head rescetion. Am. J. Surg., 2004; 187 : 201–208.
14. Sohn, T. A., Lillemoe, K. D., Cameron, J. L., et al. Reexploration for periampullary carcinoma. Ann. Surg., 1999; 229 : 293–400.
15. Yeo, Ch. J., Cameron, J. L., Maher, M. M., et al. A prospective randomized trial of pancreaticogastrostomy versus pancreaticojejunostomy after pancreaticoduodenectomy. Ann. Surg., 1995; 222 : 580–592.
16. Butturini, G., Daskalaki, D., Molinari, E., et al. Pancreatic fistula: definition and current problems. J. Hepatobiliary. Pancreat. Surg., 2008; 15 : 247–251.
17. Büchler, M. W., Friess, H., Wagner, M., et al. Pancreatic fistula after panceratic head resection. Br. J. Surg., 2000; 87 : 883–889.
18. Büchler, M. W., Wagner, M., Schmied, B., et al. Changes in morbidity after pancreatic resection. Arch. Surg., 2003; 138 : 1310–1314.
19. Conlon, K. C., Labow, D., Leung, D., et al. Prospective randomized clinical trial of the value of intraperitoneal drainage after pancreatic rescetion. Ann. Surg., 2001; 234 : 487–494.
20. Bassi, C., Butturuni, G., Molinari, E., et al. Pancreatic fistula rate after pancreatic resection. The importance of definitions. Dig. Surg., 2004; 21 : 54–59.
21. Poon, R. T., Lo, S. H., Fong, D., et al. Prevention of pancreatic anastomotic leakage after pancreaticoduodenectomy. Am. J. Surg., 2002; 183 : 42–52.
22. Suc, B., Msika, S., Piccinini, M., et al. Octreotide in prevention of intra-abdominal complications following elective pancreatic resection. A prospective, multicenter randomized controlled trial. Arch. Surg., 2004; 139 : 288–294.
23. Yeo, C. J., Cameron, J. L., Lillemoe, K. D., et al. Does prophylactic octreotide decrease the rates of pancreatic fistula and other complications after pancreaticoduodenectomy? Ann. Surg., 2000; 232 : 419–429.
24. Marcus, S. G., Cohen, H., Ranson, J. H. Optimal management of the pancreatic remnant after pancreaticoduodenectomy. Ann. Surg., 1995; 221 : 635–648.
25. Hashimoto, N., Ohyanagi, H. Pancreatic juice output and amylase level in the drainage fluid after pancreatoduodenectomy in relation to leakage. Hepato-Gastroenterology, 2002; 49 : 553–555.
26. Leffler, J., Polouček, P. Poruchy hojení anastomóz na pankreatu. Rozhl. Chir., 2001; 80 : 432–436.
27. Suzuki, Y., Fujino, Y., Tanioka, Y., et al. Selection of pancreaticojejunostomy techniquea according to pancreatic texture and duct size. Arch. Surg., 2002;137 : 1044–1047.
28. Tani, M., Onishi, H., Kinoshita, H., et al. The evaluation of duct-to-mucosal pancreaticojejunostomy in pancreaticoduodenectomy. World J. Surg., 2005; 29 : 76–79.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2011 Číslo 3- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Role VATS v léčení empyému hrudníku
- Vzdálený syndrom zraněného gliomu po stereotaktické biopsii – kazuistika
- Biliární komplikace po velkých resekcích jater
- Jednotná klasifikace plicních lymfatik. Cesta ke status quo
- Přednosti klasického operačního přístupu v chirurgické léčbě plicních metastáz
- Kvalita života po laparoskopické fundoplikaci v závislosti na předoperační symptomatologii
- Program C34 CIS v praxi MMX. Předběžná zpráva
- Vplyv pooperačných komplikácií na prežívanie pacientov s karcinómom pankreasu
- Laparoskopické ošetření poranění tlustého střeva při kolonoskopii
- Nové možnosti diagnostiky karcinómu pankreasu
- Metastáza světlobuněčného renálního karcinomu do ductus choledochus
- Laparoskopická resekce pankreatu v experimentu a klinické praxi
- Laparoskopická distálna pankreatektómia pre neuroendokrinné nádory pankreasu – prvé skúsenosti
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Kvalita života po laparoskopické fundoplikaci v závislosti na předoperační symptomatologii
- Laparoskopická distálna pankreatektómia pre neuroendokrinné nádory pankreasu – prvé skúsenosti
- Laparoskopické ošetření poranění tlustého střeva při kolonoskopii
- Vplyv pooperačných komplikácií na prežívanie pacientov s karcinómom pankreasu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



