-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Intrahepatálna cholestáza gravidných – vybrané perinatologické ukazovatele
Intrahepatic cholestasis of pregnancy – selected perinatal outcomes.
Study aim:
To compare management, treatment and perinatologic outcomes in patients with intrahepatic cholestasis of pregnancy (ICP) before and after the introduction of ursodeoxycholic acid (UDCA) into the clinical practice at the Department of Obstetrics and Gynecology of the General Hospital Trencin, Slovakia. Patient sample and methodology: Retrospective analysis of 79 deliveries by women with ICP between 1992 – 1996 when the patients were not treated with UDCA (group 1) and between 1997 – 2004 when UDCA at the dose of 500 – 750 mg per day orally was used as the first‑line ICP therapy (group 2). The presence of pruritus made the basis for the diagnosis of ICP, together with elevated ALT or ALP levels. Collected for the analysis was the week of gestation at the disease diagnosis, the week of delivery, newborn‘s birth weight, Apgar score at 1st and 5th minute, ALT and bilirubin levels at the diagnosis and during delivery, the type of delivery and the presence of multiple pregnancies in the affected women. Results: The prevalence of ICP was the same in both groups. Treatment with UDCA significantly decreased ALT (p = 0.013) and bilirubin levels (p = 0.008), improved significantly the subjective well‑being of the affected women, delayed delivery, increased birth weight (p = 0.005) and reduced the use of the Caesarean section. No increase in congenital developmental disorders and treatment‑related adverse effects was detected in either group of women with ICP. Conclusion: UDCA may be considered as a safe first‑line treatment in women with ICP with a positive effect on the mother’s subjective well‑being and some of the perinatologic parameters.Key words:
intrahepatic cholestasis of pregnancy – ursodeoxycholic acid – pregnancy
Autoři: P. Kaščák
; M. Hlaváčik; M. Korbeľ
Působiště autorů: Gynekologicko-pôrodnícka klinika, FN Trenčín, I. gynekologicko-pôrodnícka klinika, LF UK a FNsP Bratislava
Vyšlo v časopise: Prakt Gyn 2010; 14(1): 36-41
Kategorie: Původní práce
Souhrn
Cieľ štúdie:
Porovnanie manažmentu, liečby a perinatálnych výsledkov pacientiek s intrahepatálnou cholestázou gravidných (ICP) pred zavedením kyseliny ursodeoxycholovej (UDCA) do liečby a po ňom v intermediárnom centre NsP Trenčín. Klinický súbor a metodika: Retrospektívna analýza 79 pôrodov žien s ICP v rokoch 1992 – 1996, kedy pacientky neboli liečené UDCA (skupina 1) a v rokoch 1997 – 2004, kedy bola UDCA v dávke 500 – 750 mg denne per os liekom prvej voľby (skupina 2). Diagnóza ICP bola stanovená na základe prítomnosti pruritu a podporená eleváciou hladiny ALT alebo ALP. Analyzovaný bol týždeň záchytu ochorenia, pôrodu, pôrodná hmotnosť novorodenca, Apgarovej skóre v 1. a 5. minúte, hladina ALT a bilirubínu v čase stanovenia diagnózy a počas pôrodu, spôsob pôrodu a výskyt viacplodovej tehotnosti u postihnutých žien. Výsledky: Frekvencia ICP bola rovnaká v oboch skupinách. Liečba UDCA signifikantne znižovala hladiny ALT (p = 0,013), bilirubínu (p = 0,008), zlepšila subjektívny stav postihnutých žien, predĺžila sa tehotnosť, zvýšila pôrodná hmotnosť novorodencov (p = 0,005) a znížila frekvenciu cisárskeho rezu. V žiadnej skupine žien s ICP nebol zaznamenaný zvýšený výskyt vrodených vývojových chýb a nežiadúcich účinkov liečby. Záver: UDCA možno považovať za bezpečný liek prvej voľby u žien s ICP s pozitívnym vplyvom na subjektívne ťažkosti matky a niektoré perinatologické ukazovatele.Kľúčové slová:
intrahepatálna cholestáza gravidných – ursodeoxycholová kyselina – tehotnosťÚvod
Po vírusových hepatitídach druhou najčastejšou príčinou žltačky u tehotných je intrahepatálna cholestáza gravidných (ICP). Ochorenie zvyčajne začína v III., zriedkavo už v II. trimestri tehotnosti. Typickým príznakom je svrbenie kože. Niektoré prípady sa manifestujú až krátko pred pôrodom. Mnohé ľahšie formy sa pravdepodobne nezistia vôbec [1–2]. Diagnózu ICP možno postaviť po vylúčení iných príčin vzniku pruritu, ikteru, prípadne zvýšených hladín hepatálnych enzýmov v tehotnosti, pretože neexistuje špecifický test na jej odhalenie. ICP sa všeobecne považuje za benígne ochorenie s dobrou prognózou pre matku, i keď ťažkosti pacientky počas gravidity bývajú často veľmi výrazné [3–5]. Perinatálna morbidita i mortalita sú však signifikantne zvýšené. Akútna anoxia plodu je výraznou hrozbou, pretože nekoreluje so stupňom postihnutia ženy a je ťažko predvídateľná konvenčným antepartálnym monitorovaním [6]. Nedávno boli publikované dva kazuistické prípady pacientiek s ICP, kde napriek adekvátnej liečbe a monitoringu došlo k intrauterinnému odumretiu dieťaťa [7]. Nezistená a neliečená ICP môže byť príčinou až polovice nevyjasnených intrauterinných odumretí plodov vo Veľkej Británii [8].
Najčastejšie používanými preparátmi v liečbe ICP sú S-adenosyl-L-methionín (SAMe) a ursodeoxycholová kyselina (UDCA). Nevýhodou liečby SAMe je limitovaná účinnosť na ľahké formy ICP a dlhodobé parenterálne podávanie. Perorálna liečba je považovaná za neúčinnú [9]. Zatiaľ najvyššiu účinnosť v liečbe pacientiek s ICP má UDCA, a to bez nežiadúcich účinkov na matku a plod. UDCA normalizuje, resp. znižuje hladiny hepatálnych enzýmov, priaznivo ovplyvňuje subjektívne ťažkosti pacientky a znižuje riziko postihnutia plodu. Znižuje hladiny žlčových kyselín v pupočníkovej krvi, plodovej vode i v kolostre [10–14]. UDCA chráni kardiomyocyty pred arytmiou spôsobenou zvýšenými hladinami žlčových kyselín [15].
Aj keď je liečba ICP relatívne účinná a vedie k zníženiu rizika intrauterinnej smrti plodu, nemala by sa u postihnutých žien pripustiť postmaturita. Vzhľadom k riziku postihnutia plodu je odporúčané prísne monitorovanie plodu a funkcie fetoplacentárnej jednotky, ktoré ale nemusí signalizovať ohrozenie plodu [16]. Po dosiahnutí pľúcnej zrelosti sa preto niektorí autori prikláňajú k indukciu pôrodu [4,17–18]. Pôrod by mal byť indukovaný v 38.–39. týždni tehotnosti [4,18].
Materiál a metodika
Retrospektívne bola analyzovaná populácia žien s diagnózou ICP v dvoch časových obdobiach. Rozčlenenie súboru bolo limitované modernými možnosťami sledovania intrauterinného stavu plodu, ktoré sa stali dostupnými v Trenčíne od roku 1992 a zavedením UDCA do liečby ICP v roku 1997.
V skupine 1 (bez liečby UDCA) boli pacientky liečené hepatoprotektívami, diétnymi a režimovými opatreniami, antihistaminikami (obdobie rokov 1992–1996).
V skupine 2 boli pacientky liečené UDCA – hepatoprotektíva a antihistaminiká neboli podávané (obdobie rokov 1997–2004). UDCA bola podávaná v dávke 500–750mg denne per os podľa hmotnosti pacientky a odozvy na liečbu. Vyššia dávka ako 750mg denne nebola aplikovaná u žiadnej pacientky.
Diagnózu ICP stanovoval hepatológ. Za hodnotiace kritérium ochorenia bola považovaná prítomnosť pruritu podporená eleváciou hladiny alanín aminotransferázy (ALT) alebo alkalickej fosfatázy (ALP). V sledovanom časovom období nebolo možné u nás vyšetrovať sérové hladiny žlčových kyselín. Do súboru boli zaradené len ženy s aktívnou liečbou ICP a kontrolovanými hladinami hepatálnych enzýmov. Do súboru neboli zaradené pacientky, u ktorých mohla byť suponovaná ICP, ale porodili bez diagnostického a liečebného procesu. Všetky pacientky boli vyšetrené gastroenterológom, resp. hepatológom a u väčšiny z nich bolo realizované ultrazvukové vyšetrenie heparu a cholecysty. Takisto bola vykonaná diferenciálna diagnostika prípadných iných ochorení so zvýšeným ALT. U žiadnej ženy nebola dokázaná vírusová hepatitída. Pacientky boli poučené hepatológom i pôrodníkom o povahe a prognóze ochorenia. Z biochemických parametrov bola sledovaná hladina ALT a bilirubínu na prístrojoch firmy Abbott v čase diagnostikovania ochorenia a v čase pôrodu. Intervaly krvných odberov na jednotlivé vyšetrenia hepatálnych enzýmov, ale i ostatných sledovaných parametrov u postihnutých žien boli vždy individuálne prispôsobené dynamike ochorenia. Stav plodu všetkých tehotných bol intenzívne sledovaný pomocou ultrazvukového vyšetrenia (Toshiba – Sonolayer-U-SAL-38D s 3,75 MHz konvexnou abdominálnou sondou a ATL-HDI 3 500 s multifrekvenčnou konvexnou abdominálnou sondou), vo vyšších gestačných týždňoch i kardiotokografickým vyšetrením (CTG) podľa kritérií FIGO z roku 1986 prístrojmi firmy Hewlett Packard a Philips – series 50A a sledovaním prietoku krvi v umbilikálnej artérii, prípadne v ďalších cievach plodu. Predčasný pôrod bol hodnotený podľa kritérií Svetovej zdravotníckej organizácie ako pôrod pred ukončeným 37. gestačným týždňom.
V oboch skupinách bol analyzovaný týždeň záchytu ochorenia, týždeň pôrodu, pôrodná hmotnosť novorodenca, Apgarovej skóre (AS) v 1. a 5. minúte, hladina ALT v čase stanovenia diagnózy a počas pôrodu, hladina bilirubínu v čase stanovenia diagnózy a počas pôrodu, spôsob pôrodu a výskyt viacplodovej tehotnosti u postihnutých žien.
V súbore sa pracovalo vždy s celou populáciou žien postihnutých ICP, preto bolo potrebné z matematického hľadiska vykonať tzv. cenzus a populáciu spracovať vo vyjadrení percentuálnom s analýzou priemeru, mediánu a štandardnej odchýlky. Každý rozdiel v uvedených výsledkoch je potom považovaný za významný. To platí aj v prípade porovnania spôsobu pôrodu žien s ICP s celkovým vývojom incidencie cisárskeho rezu a porovnania výskytu ICP u gemín s celkovou incidenciou gemín v sledovanom období v našej nemocnici. Súbor bol podrobený i štatistickej analýze významnosti vzťahu dvoch kategorických premenných chí-kvadrát testom nezávislosti. Vzťah medzi číselnou a kategorickou premennou bol analyzovaný testom ANOVA.
Výsledky
Retrospektívny súbor pacientiek s ICP v sledovanom časovom období zahŕňa spolu 79 gravidít, u ktorých bola stanovená diagnóza ICP. V 1. skupine bolo analyzovaných 36 gravidít v časovom období rokov 1992–1996 a v 2. skupine 43 gravidít v časovom období rokov 1997–2004. V prvej skupine sa gemini vyskytli 3× a v druhej skupine 2×. Základné charakteristiky súboru v zmysle výskytu ochorenia a výskytu viacplodovej tehotnosti sú uvedené v tab. 1.
Tab. 1. Charakteristika súboru s ICP. 
Tab. 2 zobrazuje týždeň tehotnosti v čase diagnostiky ochorenia. Do roku 1996 bola ICP diagnostikovaná priemerne v 35. týždni tehotnosti, od roku 1997 to bolo o 2 týždne skôr – v 33. týždni.
Tab. 2. Týždeň tehotnosti v čase diagnózy ICP. 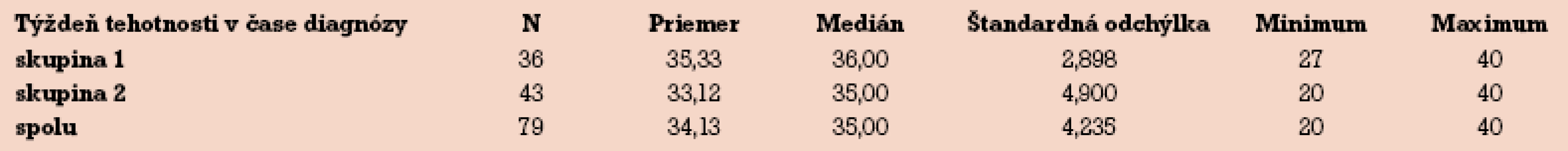
Tab. 3 zobrazuje týždeň tehotnosti v čase pôrodu. V prvom aj druhom období bola gravidita v priemere ukončovaná v 39. gestačnom týždni s rozdielom len niekoľkých dní. Medián pôrodu je však o týždeň vyšší v druhej skupine analyzovaného súboru.
Tab. 3. Týždeň tehotnosti v čase pôrodu. 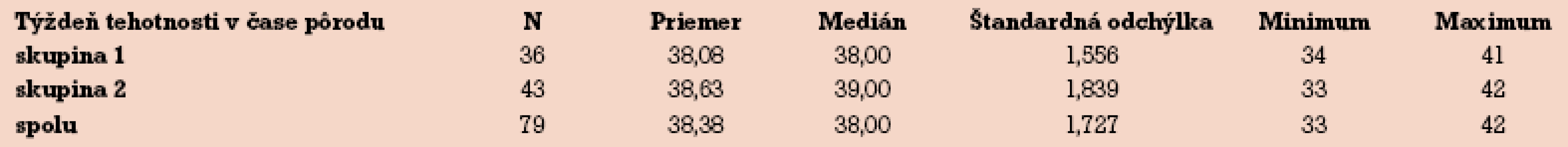
Hmotnosť plodu pri narodení je uvedená v tab. 4. Kým do roku 1996 bola priemerná hmotnosť novorodenca približne 3 000g, od roku 1997 sa zvýšila o viac ako 300g. Rozdiel je ešte výraznejší v prípade mediánu.
Tab. 4. Pôrodná hmotnosť plodu. 
Priemerné Apgarovej skóre (AS) v 1. minúte bolo do r. 1996 o 0,57 bodu nižšie ako v skupine od r. 1997. V 5. minúte bol rozdiel v AS už menší – len 0,23 bodu (tab. 5).
Tab. 5. Apgarovej skóre v 1. a 5. minúte. 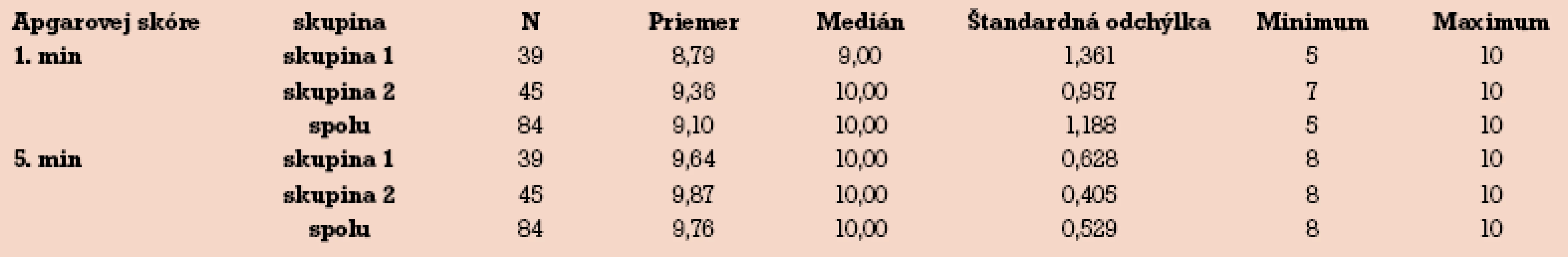
Priemerné hodnoty ALT v čase stanovenia diagnózy ICP v súbore neliečenom UDCA boli 2,5 µkat/l. V súbore liečenom UDCA boli podstatne vyššie – v priemere 4,2 µkat/l. V prípade mediánu rozdiel nie je natoľko významný (tab. 6).
Tab. 6. ALT v čase stanovenia diagnózy. 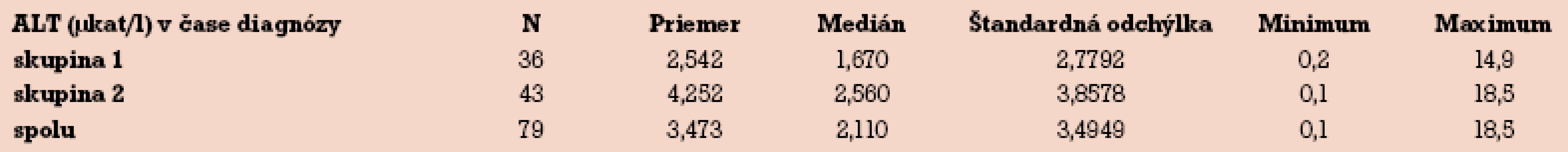
Priemerné hodnoty ALT v čase pôrodu v skupine neliečenej UDCA boli okolo 4 µkat/l. V skupine liečenej UDCA nedosahovalo ALT v priemere ani polovičnú hodnotu (1,8 µkat/l). Rovnaká situácia platí aj pre medián hladín ALT (tab. 7).
Dynamika ALT (graf 1) v skupine neliečenej UDCA vykazovala progresívne zvyšovanie od diagnózy k pôrodu, zatiaľ čo v skupine liečenej UDCA sa hladiny ALT od stanovenia diagnózy k pôrodu progresívne znižovali.
Graf 1. Zmena hladín ALT (μkat/l) od stanovenia diagnózy po pôrod. 
V skupine neliečenej UDCA sú priemerné hodnoty bilirubínu v čase stanovenia diagnózy ICP nižšie ako v skupine liečenej UDCA. V čase pôrodu sú hladiny bilirubínu v oboch skupinách v opačnom pomere. Kým pri liečbe hepatoprotektívami hladina bilirubínu k pôrodu stúpa, v skupine liečenej UDCA hladina bilirubínu v čase pôrodu výrazne klesá (tab. 8).
Tab. 8. Hladina bilirubínu v čase diagnózy a v čase pôrodu. 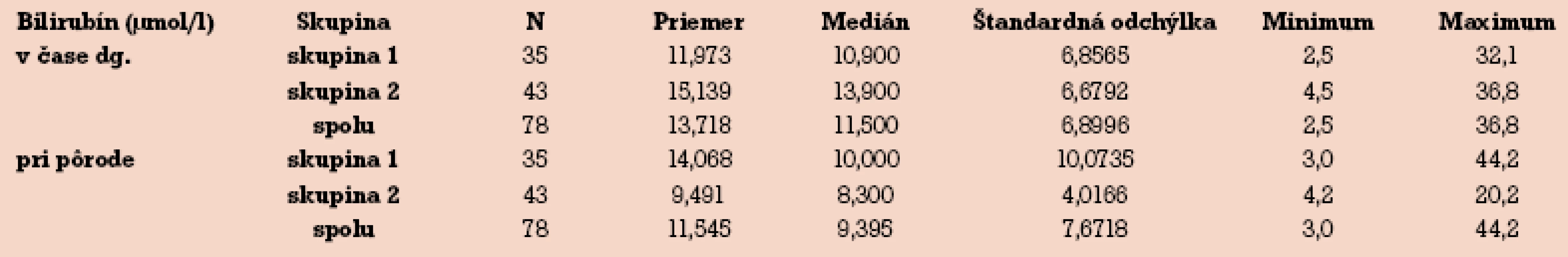
V skupine liečenej hepatoprotektívami bolo 50% pôrodov vedených spontánne, v skupine liečenej UDCA to bolo len 37% (tab. 9). V tejto skupine však stúpla frekvencia indukovaných pôrodov na 35% oproti 25% v skupine neliečenej UDCA. Významný je takmer štvornásobný pokles frekvencie cisárskeho rezu v skupine liečenej UDCA (2,3%) oproti liečenej hepatoprotektívami (8,3%). Naproti tomu však stúpa frekvencia cisárskeho rezu v skupine liečenej UDCA z inej indikácie ako je ICP takmer o 9 percent oproti skupine neliečenej UDCA. Kým frekvencia cisárskeho rezu v sledovanom období vo všeobecnej populácii stúpla o 6% (z 8% na 14%), u žien s ICP bol tento vzostup len o 3% (z 25% na 28%). Frekvencia predčasného pôrodu je podľa očakávania vyššia o 7% v skupine žien neliečených UDCA (27,8%) oproti skupine liečených UDCA (20,9%).
Diskusia
Frekvencia ICP v našom súbore je identická s literárnymi údajmi pre strednú Európu. V zhode s literárnymi údajmi sa v našom súbore vyskytuje takmer 6× častejšie viacplodová tehotnosť v porovnaní s celou populáciou rodiacich žien v uvedenom časovom období [4,6,19].
Očakávali sme približne rovnaký týždeň záchytu ochorenia. Zistili sme však štatistickú významnosť v týždni diagnostiky ochorenia (p = 0,019). Pri analýze (tab. 2) je zrejmé, že i keď priemer záchytu ICP sa líši až o dva týždne, je ovplyvnený extrémnymi hodnotami záchytu v 2. skupine. O skoršom záchyte, a teda možnej lepšej informovanosti a skoršom odoslaní pacientky k diagnostike a liečbe však svedčí medián, kedy boli pacientky v druhej skupine diagnostikované o týždeň skôr. Možným vysvetlením je zlepšené povedomie o ochorení v primárnej gynekologickej starostlivosti nášho regiónu. Pacientky s pruritom bez kožných eflorescencií sú už odoslané priamo k hepatológovi alebo na konziliárnu ambulanciu oddelenia.
Pri adekvátnom sledovaní plodu je nižšie riziko ohrozenia dieťaťa a gravidita môže často pokračovať do vyšších gestačných týždňov [20]. Pri ukončovaní tehotnosti (tab. 3) sme očakávali rozdiely, lebo úspešná liečba pomocou UDCA vedie k ústupu subjektívnych ťažkostí a objektívnemu poklesu hodnôt pečeňových testov. Nami predpokladané pokračovanie do vyšších gestačných týždňov sa tak naplnilo – priemer i medián pôrodu sú v skupine 2 vyššie (rozdiel je však štatisticky nevýznamný – p = 0,164). Niektoré ženy pri dobrom subjektívnom stave, zlepšených laboratórnych parametroch a ambulantnom manažmente sa k odporučenej indukcii pôrodu nedostavili a rodili aj po vypočítanom termíne. Vzhľadom na súčasné odporučené postupy rôznych spoločností [18,21–22] sa snažíme prenášaniu v posledných rokoch vyhnúť.
Naše výsledky, v zhode s literárnymi údajmi [15,20,23], jednoznačne potvrdzujú priaznivé ovplyvnenie hmotnosti plodu liečbou UDCA (tab. 4).
Adekvátnym manažmentom pacientiek s ICP sa dajú dosiahnuť výsledky porovnateľné so všeobecnou populáciou [15,24]. Potvrdili to aj naše výsledky – rozdiely v Apgarovej skóre v 1. a 5. minúte boli nevýznamné a žiadne dieťa nezomrelo ani intrauterine, ani do 7 dní.
Hodnota ALT informuje o ochorení len nepriamo, nie vždy musí byť zvýšená. V diagnostike ICP v minulosti hralo u nás stanovenie ALT významnú úlohu. Moderným diagnostickým testom je stanovenie hladiny žlčových kyselín, ktoré je dostupné v Trenčíne až od roku 2009. Náš predpoklad štatistickej nevýznamnosti ALT v čase stanovenia diagnózy ICP sa nepotvrdil (tab. 6). Priemer, medián i vypočítané p = 0,029 sú významné, ALT bolo výrazne vyššie v 2. skupine. Hodnota minimálnych, maximálnych hodnôt a mediánu sú však v zhode s literárnymi údajmi [4,25].
ALT v čase pôrodu je jeden z najdôležitejších hodnotených parametrov. Na rozdiel od skupiny 1, kde pri liečbe hepatoprotektívami väčšinou dochádza k vzostupu ALT, pri liečbe UDCA hladina ALT podľa literárnych údajov klesá [20,25–26]. Náš predpoklad výrazného ovplyvnenia ALT liečbou UDCA sa v zhode s literárnymi údajmi potvrdil. Hodnoty priemeru, mediánu i p = 0,013 sú štatisticky významné. Na rozdiel od skupiny 1, kedy napriek liečbe hepatoprotektívami dochádzalo k vzostupu ALT, v skupine 2 zavedením UDCA do liečby ALT klesalo (tab. 7, graf 1).
Hladina bilirubínu nie je vhodným markerom k diagnostike a sledovaniu účinnosti liečby ICP. V našom súbore sú pre bilirubín matematické rozdiely priemeru a mediánu významné, v čase diagnózy je hladina p = 0,043 a v čase pôrodu je p = 0,008 (tab. 8). Väčšina hodnôt bilirubínu v súbore však spadá do fyziologického rozmedzia normálnych hodnôt zdravej populácie. Nami zistený rozdiel nie je z biologického hľadiska významný a dôležitý. Podobne ako v prípade ALT liečba UDCA znižovala hladiny bilirubínu v 2. skupine pacientiek na rozdiel od 1. skupiny, kde priemerné hodnoty stúpali. Zvýšené hladiny bilirubínu v našom súbore sú nižšie ako udáva literatúra. Ovplyvnenie hodnôt liečbou UDCA je však v zhode s publikovanými údajmi [20,25–26].
V skupine 2 sme očakávali viac indukovaných pôrodov, lebo jedným z parametrov zmeny manažmentu v starostlivosti o ženu s ICP je plánovaná indukcia pôrodu. V skupine 1 sme očakávali viac cisárskych rezov, hlavne z indikácie samotnej ICP. V skupine 2, liečenej UDCA, by hypoteticky pri vhodnej indukcii pôrodu malo dôjsť napriek všeobecnému vzostupu frekvencie cisárskeho rezu v populácii k jeho poklesu (tab. 9). Aj keď hladina p = 0,321 nie je štatisticky významná, z hľadiska populácie je zrejmé, že prístup k pôrodu u pacientiek skupiny 1 a 2 sa zmenil. V zhode s literatúrou [4,18,27] je indukcia v skupine 2 častejšia o 10% a napriek vzostupu cisárskeho rezu vo všeobecnej populácii ostáva percento sekcií v oboch skupinách stabilné. Pri bližšej analýze je samotná ICP indikáciou k cisárskemu rezu len v 2% v skupine 2, kým v predchádzajúcom časovom období malo až 8% žien ako jedinú indikáciu k sekcii ICP. Je teda zrejmé, že zavedením UDCA do liečby došlo k priaznivému ovplyvneniu spôsobu ukončenia tehotnosti u pacientiek s ICP. Potvrdilo sa ale, že tehotná s ICP má vyššiu pravdepodobnosť ukončenia tehotnosti cisárskym rezom, resp. že pôrod bude indukovaný.
Podľa literárnych údajov je u žien s ICP vyšší výskyt predčasného pôrodu. Liečba UDCA v našom súbore v zhode s literatúrou [15,20] priaznivo ovplyvnila tento sledovaný parameter. Štatistická významnosť však dosiahnutá nebola (p = 0,478). ICP je napriek liečbe významným faktorom, ktorý naďalej zvyšuje pravdepodobnosť predčasného pôrodu u postihnutej tehotnej ženy. Frekvencia predčasného pôrodu v rôznych štúdiách je síce rozdielna, ale vždy vyššia ako vo všeobecnej populácii [23,28–29]. Aj v našom súbore žien s ICP bol výskyt 4× vyšší, ako bola celková frekvencia predčasného pôrodu v nemocnici.
Záver
Manažment pacientky s ICP sa výrazne zmenil zavedením UDCA do liečby, ktorú považujeme za liek prvej voľby. Liečba UDCA znižovala hladiny ALT a bilirubínu, zlepšovala subjektívny stav postihnutých žien a bola veľmi dobre tolerovaná. Nevyskytli sa žiadne závažné vedľajšie účinky a liek nemusel byť nikdy vysadený. Došlo k priaznivému ovplyvneniu spôsobu ukončenia tehotnosti (častejšia indukcia) a stavu plodu v zmysle predĺženia tehotnosti a vyššej pôrodnej hmotnosti detí matiek liečených UDCA. Frekvencia ochorenia bola rovnaká v oboch skupinách postihnutých žien.
MUDr. Peter Kaščák1
MUDr. Martin Hlaváčik1
doc. MUDr. Miroslav Korbeľ, CSc.2
1 Gynekologicko-pôrodnícka klinika,
FN Trenčín
2 I. gynekologicko-pôrodnícka klinika,
LF UK a FNsP Bratislava
pkascak@gmail.com
Zdroje
1. Milkiewicz P, Elias E, Williamson C et al. Obstetric cholestasis. Br Med J 2002; 324(7330): 123 – 124.
2. Kupčová V, Turecký L, Plank K. Intrahepatálna cholestáza gravidných a liečba kyselinou ursodeochycholovou – predbežné výsledky. Prakt Gynek 2008; 15(4): 187 – 194.
3. Reyes H. The enigma of intrahepatic cholestasis of pregnancy: lesons from Chile. Hepatology 1982; 2(1): 87 – 96.
4. Palmer DG, Eads J. Intrahepatic cholestasis of pregnancy: a critical review. J Perinat Neonatal Nurs 2000; 14(1): 39 – 51.
5. Kondrackiene J, Kupcinskas L. Intrahepatic cholestasis of pregnancy – current achievements and unsolved problems. World J Gastroenterol 2008; 14(38): 5781 – 5788.
6. Williamson C, Hems LM, Goulis DG et al. Clinical outcome in a series of cases of obstetric cholestasis identified via a patient support group. Br J Obstet Gynaecol 2004; 111(7): 676 – 681.
7. Lee RH, Incerpi MH, Miller DA et al. Sudden fetal death in intrahepatic cholestasis of pregnancy. Obstet Gynecol 2009; 113(2 Pt 2): 528 – 531.
8. Scheuer P, Chambers J, Rogers A. Intrahepatic cholestasis of pregnancy. Br Med J 1995; 310(6974): 260.
9. Binder T, Salaj P, Zima T et al. Kyselina ursodeoxycholová, S - adenosyl - L - metionin a jejich kombinace v léčbě těhotenské intrahepatální cholestázy (ICP). Čes Gynek 2006; 71(2): 92 – 98.
10. Meng LJ, Reyes H, Palma J et al. Effects of ursodeoxycholic acid on conjugated bile acids and progesterone metabolites in serum and urine of patients with intrahepatic cholestasis of pregnancy. J Hepatol 1997; 27(6): 1029 – 1040.
11. Brites D, Rodrigues CM. Elevated levels of bile acids in colostrum of patients with cholestasis of pregnancy are decreased following ursodeoxycholic acid therapy. J Hepatol 1998; 29(5): 743 – 751.
12. Brites D, Rodrigues CM, Oliveira N et al. Correction of maternal serum bile acid profile during ursodeoxycholic acid therapy in cholestasis of pregnancy. J Hepatol 1998; 28(1): 91 – 98.
13. Serrano MA, Brites D, Larena MG et al. Beneficial effect of ursodeoxycholic acid on alterations induced by cholestasis of pregnancy in bile acid transport across the human placenta. J Hepatol 1998; 28(5): 829 – 839.
14. Paumgartner G, Beuers U. Ursodeoxycholic acid in cholestatic liver disease: mechanisms of action and therapeutic use revisited. Hepatology 2002; 36(3): 525 – 531.
15. Geenes V, Williamson C. Intrahepatic cholestasis of pregnancy. World J Gastroenterol 2009; 15(17): 2049 – 2066.
16. Mullally BA, Hansen WF. Intrahepatic cholestasis of pregnancy: review of the literature. Obstet Gynecol Surv 2002; 57(1): 47 – 52.
17. Fagan EA. Intrahepatic cholestasis of pregnancy. Br Med J 1994; 309(6964): 1243 – 1244.
18. Binder T. Těhotenská cholestatická hepatóza – doporučený postup. Čes Gynek 2009; 74 (Suppl. 1): 27 – 28.
19. Gonzalez MC, Reyes H, Arrese M et al. Intrahepatic cholestasis of pregnancy in twin pregnancies. J Hepatol 1989; 9(1): 84 – 90.
20. Zapata R, Sandoval L, Palma J et al. Ursodeoxycholic acid in the treatment of intrahepatic cholestasis of pregnancy. A 12‑year experience. Liver Int 2005; 25(3): 548 – 554.
21. Royal College of Obstetricians and Gynaecologists. Obstetric Cholestasis. Green Top Guideline 46. London 2006. Dostupné z: www.rcog.org.uk.
22. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: management of cholestatic liver diseases. J Hepatol 2009; 51(2): 237 – 267.
23. Heinonen S, Kirkinen P. Pregnancy outcome with intrahepatic cholestasis. Obstet Gynecol 1999; 94(2): 189 – 193.
24. Savonius H, Riikonen S, Gylling H et al. Pregnancy outcome with intrahepatic cholestasis. Acta Obstet Gynecol Scand 2000; 79(4): 323 – 325.
25. Binder T, Zima T, Vitek L. Biochemické aspekty těhotenské cholestatické hepatózy. Čes Gynek 2007; 72(2): 90 – 94.
26. Laifer SA, Stiller RJ, Siddiqui DS et al. Ursodeoxycholic acid for the treatment of intrahepatic cholestasis of pregnancy. J Matern Fetal Med 2001; 10(2): 131 – 135.
27. Mozurkewich E, Chilimigras J, Koepke E et al. Indications for induction of labour: a best - evidence review. Br J Obstet Gynaecol 2009; 116(5): 626 – 636.
28. Bacq Y, Sapey T, Bréchot MC et al. Intrahepatic cholestasis of pregnancy: a French prospective study. Hepatology 1997; 26(2): 358 – 364.
29. Kondrackiene J, Beuers U, Zalinkevicius R et al. Predictors of premature delivery in patients with intrahepatic cholestasis of pregnancy. World J Gastroenetrol 2007; 13(46): 6226 – 6230.
Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek Úvodní slovo
Článek vyšel v časopisePraktická gynekologie
Nejčtenější tento týden
2010 Číslo 1- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
-
Všechny články tohoto čísla
- Stav okrajů konizací s histologickým nálezem carcinoma in situ
- Vybrané imunohistochemické prognostické faktory karcinomu endometria
- ICTP marker a karcinóm prsníka s mts do kostí – naše skúsenosti
- Terapeutické možnosti asistované reprodukce u pacientek se sníženou ovariální rezervou
- Úvodní slovo
- Intrahepatálna cholestáza gravidných – vybrané perinatologické ukazovatele
- Obezita v perimenopauze a možnosti řešení
- Vliv kyseliny dokosahexaenové na antenatální vývoj plodu a postnatální vývoj dítěte
- Prenatální kardiologie jako teorie i praxe
- Praktická urogynekologie XVIII. Mělník 2009
- Praktická gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Stav okrajů konizací s histologickým nálezem carcinoma in situ
- ICTP marker a karcinóm prsníka s mts do kostí – naše skúsenosti
- Intrahepatálna cholestáza gravidných – vybrané perinatologické ukazovatele
- Terapeutické možnosti asistované reprodukce u pacientek se sníženou ovariální rezervou
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání





