-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Historie, současnost a budoucnost používání 68Ge/68Ga generátorů – 1. část
History, present and future of the use of 68Ge/68Ga generators – 1st part
Aim: Review of history, state of art and trends in gaining of 68Ga, especially from 68Ga/68Ge radionuclide generators.
Introduction: Positron emission tomography (PET) is one of the most modern methods of nuclear medicine. Fluorine-18 is the most frequently used radionuclide for PET diagnostics, but there are other emerging radionuclides and the great attention is paid to 68Ga. The undeniable advantage of this radionuclide is its way of production. In contrast with other radionuclides for PET diagnostics almost exclusively prepared in the cyclotron, 68Ga can be gained also from a radionuclide generator which significantly simplifies and speeds up other steps of its use.
Issue description: The development of 68Ge/68Ga radionuclide generators has been performed through the research of new separation systems which still remains a hot topic. Nowadays, the variety of separation systems is available. Some of them have a registration by European Medicines Agency (EMA) or American Food and Drug Administration (FDA) for use in human medicine. Others are suitable just for research and development. Regarding to technological and legislative difficulties connected with the development of 68Ge/68Ga radionuclide generator, the design of a system providing the eluate of 68Ga in convenient chemical form and sufficient radiochemical and radionuclide purity remains a great challenge and research teams around the world focus on the topic.
Nowadays, there is one 68Ge/68Ga radionuclide generator and one kit for 68Ga labelling, SomaKit TOC, used for neuroendocrine tumours diagnostics registered in the Czech Republic. Other kit, 68Ga-PSMA-11, is used for diagnostics of prostate cancer in the specific treatment programme. However, the use of this radionuclide is not limited for these only applications and 68Ga enjoys the growing popularity in the world scale.
Conclusion: Even though 18F remains the radionuclide of choice in PET, broad studies of separation systems and targeting molecules could lead to his replacement by 68Ga, mainly for the possibility of its elution from radionuclide generators.
Keywords:
radionuclide generator – Positron emission tomography – gallium-68 – germanium-68
Autoři: Kateřina Fialová 1,2; Petra Suchánková 1,2; Martin Vlk 1,2; Ján Kozempel 1
Působiště autorů: Katedra jaderné chemie, Fakulta jaderná a fyzikálně inženýrská, České vysoké učení technické v Praze, ČR 1; Klinika nukleární medicíny a endokrinologie, 2. LF UK a Fakultní nemocnice v Motole, Praha, ČR 2
Vyšlo v časopise: NuklMed 2021;10:68-72
Kategorie: Přehledová práce
Souhrn
Cíl: Podrobnější přehled historie, současného stavu a nynějších trendů v získávání 68Ga, především z 68Ge/68Ga radionuklidového generátoru.
Úvod: Pozitronová emisní tomografie (PET) je jednou z nejmodernějších metod nukleární medicíny. Stále nejhojněji využívaným radionuklidem při diagnostice pomocí PET je 18F, ale do popředí se dostávají i další pozitronové zářiče a velká pozornost je věnována právě 68Ga. Nespornou výhodou tohoto radionuklidu je způsob jeho získání. Oproti ostatním radionuklidům využívaným v PET diagnostice, které jsou připravovány téměř výhradně na cyklotronu, je 68Ga možné získat i pomocí radionuklidového generátoru, což výrazně zjednodušuje a urychluje další kroky jeho použití.
Popis problematiky: Vývoj 68Ge/68Ga radionuklidových generátorů představoval komplexní výzkum separačních systémů, které jsou i dnes aktuálním tématem. V současnosti je dostupná řada separačních systémů, z nichž některé jsou již registrovány u Evropské agentury pro léčivé přípravky (EMA) či amerického Úřadu pro kontrolu potravin a léčiv (FDA) pro použití v humánní medicíně. Jiné jsou dostupné pouze pro výzkum a vývoj. S ohledem na technologické a legislativní těžkosti spojené s vývojem 68Ge/68Ga radionuklidového generátoru je navržení systému, který by poskytoval eluát 68Ga ve vhodné chemické formě a dostatečné radiochemické a radionuklidové čistotě, stále velkou výzvou a rozsáhlému studiu je věnována pozornost mnoha vědeckých týmů z celého světa.
V České republice je dosud registrován jeden 68Ge/68Ga radionuklidový generátor a jeden kit pro značení 68Ga, SomaKit TOC pro diagnostiku neuroendokrinních tumorů (NET). Další kit, 68Ga-PSMA-11, je pak využíván pro diagnostiku karcinomu prostaty v rámci specifického léčebného programu. Ve světovém měřítku není však využití tohoto radionuklidu omezeno pouze na tyto aplikace a 68Ga je stále ve větší oblibě.
Závěr: Rozsáhlé studie separačních systémů a cílících molekul by mohly v budoucnu vést u některých diagnostických procedur k nahrazení tradičního PET radionuklidu 18F právě 68Ga a to především díky možnosti eluce z radionuklidového generátoru.
Klíčová slova:
radionuklidový generátor – pozitronová emisní tomografie – galium-68 – germanium-68
ÚVOD
Nejčastěji užívanou diagnostickou modalitou v nukleární medicíně je pozitronová emisní tomografie. Přestože radionuklidem první volby pro tuto modalitu je stále 18F (T½ = 109,77 min) 1, nové radionuklidy, jako je 68Ga (T½ = 67,83 min) 2, si především v posledním desetiletí nacházejí své místo v PET diagnostice.
Nespornou výhodou pro využití 68Ga je fyzikálně-chemická charakteristika jeho mateřského radionuklidu, 68Ge (T½ = 270,95 dne) 2, jež umožňuje získávat 68Ga elucí z radionuklidového generátoru. Díky tomu se 68Ga stává výrazně dostupnějším než ostatní pozitronové zářiče, včetně 18F, které jsou běžně připravovány na cyklotronu v dojezdové vzdálenosti od lékařského zařízení. 3 Nicméně z legislativního hlediska jsou na čistotu eluátu 68Ga kladeny velmi vysoké nároky. Kontaminace mateřským 68Ge nesmí podle Evropského lékopisu překročit 0,001 % celkové aktivity. 4 Výzkum a vývoj takových systémů je tedy stále vysoce aktuální.
Tento článek je zaměřen na přípravu preparátu 68Ga, a to především pomocí 68Ge/68Ga radionuklidového generátoru. Pozornost je věnována rovněž mateřskému radionuklidu 68Ge, historickému vývoji generátorových systémů a současnému stavu celé problematiky společně s novými trendy, které je možné pozorovat ve výzkumu a vývoji 68Ge/68Ga radionuklidových generátorů.
Gallium
Za objevitele tohoto prvku je považován Paul-Émile Lacoq Boisbaudran, který v roce 1875 pozoroval u vzorku zinku z přírodní rudy novou linii v atomovém spektru. 5 Gallium je měkký stříbrobílý kov podobný hliníku. Kromě kovového gallia, se tento prvek vyskytuje ve dvou oxidačních stavech, +I a +III, z nichž pouze druhý uvedený je stabilní v podmínkách vodných roztoků, a tedy relevantní pro klinické aplikace. 6
Vlivem malého iontového poloměru, 62 pm, a vysokého měrného náboje je galium kationtem, který především v prostředí neutrálního a bazického pH snadno podléhá hydrolýze za tvorby oxidů a hydroxidů tvořících koloidní či pseudokoloidní sraženiny zabraňující tvorbě jiného komplexu. Při pH vyšším než 7,4 tvoří vysoce stabilní galátový anion [Ga(OH)4]-, který jen těžko podléhá transchelataci a lze ho solvatovat pouze v silně kyselém prostředí. Tyto skutečnosti je potřeba brát v úvahu především při radiochemickém značení. 3
V přírodním složení je zastoupen dvěma izotopy. Izotop s hmotnostním číslem 69 je stabilní a jeho přirozené zastoupení je 60,1 %. Izotop s hmotnostním číslem 71 je přirozeně zastoupen z 39,9 % a je možné ho považovat za stabilní, jelikož jeho poločas přeměny je ˃ 2,4 × 1026 let a jedná se o β - zářič. Ostatní izotopy jsou antropogenní a radioaktivní. 6 Radioizotopy gallia patří spolu s izotopy jódu, fosforu a radia k prvním radionuklidům testovaným pro účely léčby a diagnostiky. V historii byl pro možnosti využití v nukleární medicíně jako první testován izotop 72Ga (β-, T½ = 14,10 h). Nicméně využití tohoto izotopu pro zamýšlenou aplikaci, tedy diagnostiku osteogenních sarkomů a metastatických maligních lézí v kostech, se ukázalo jako neefektivní. Zjištěné výsledky však obrátily pozornost k jinému izotopu galia, konkrétně ke 67Ga (EZ, T½ = 3,26 dne). 7 Tento radionuklid je dodnes využíván ve formě citrátu v jednofotonové emisní počítačové tomografii (SPECT) k diagnostice a dlouhodobému sledování pacientů s maligními lymfomy, pro zjišťování diseminace jiných zhoubných procesů a lokalizaci zánětlivých procesů především v plicích. 8
Největší pozornost je však v současné době upřena na 68Ga. Již v 60. letech minulého století byl tento radionuklid testován k diagnostickým účelům. Byl studován v komplexu s EDTA pro zobrazování malignit mozku. 9 Po dlouhé době útlumu je v posledním dvacetiletí navracen na medicinální scénu, a to především v oblasti diagnostiky NET pomocí značených analogů somatostatinu, jako jsou [68Ga]DOTATOC, [68Ga]DOTANOC, [68Ga]DOTATATE. Možnosti využití tohoto radionuklidu však nekončí pouze u této aplikace. V podobě vhodného komplexu ho lze použít ke značení široké škály peptidů, protilátek a malých molekul. 10 Ve světě jsou rozsáhle testovány možnosti jeho použití i přímo s peptidy, jako je např. PSMA 11 či Bombesin 12 pro diagnostiku karcinomu prostaty. Rozsáhle studováno je i použití 68Ga ve formě značených protilátek, fragmentů protilátek či bispecifických protilátek schopných cílit na potřebné místo a zároveň vázat iontové gallium. 13,14 Přestože v Evropě i USA je 68Ga rozsáhle využíváno a testováno, v České republice je doposud registrován pouze jeden 68Ge/68Ga radionuklidový generátor, GalliaPharm 15, a jeden kit pro značení 68Ga, SomaKit TOC, pro diagnostiku neuroendokrinních nádorů pomocí oktreotidu, analogu somatostatinu. 16 V rámci specifického léčebného programu je pak v ČR (VFN v Praze a FN Plzeň) pro diagnostiku karcinomu prostaty využíváno PSMA značené 68Ga pomocí kitu 68Ga-PSMA-11. 17
Jednou z výhod 68Ga je i chemická podobnost s některými terapeutickými radionuklidy, jako jsou 90Y a 177Lu. Tento radionuklid tak lze použít i jako součást teranostického páru, ve kterém je v cílící molekule nahrazován diagnostický radionuklid za terapeutický a obráceně, aniž by došlo k výrazně odlišnému chování cílící molekuly v organismu. Tímto způsobem je možné nejen přesně diagnostikovat a zacílit onemocnění, ale především kontrolovat účinky terapie. 10
Mateřský radionuklid – 68Ge
Mateřským radionuklidem 68Ga, který umožňuje jeho získávání z radionuklidového generátoru, je 68Ge. Tento radionuklid podléhá elektronovému záchytu s poločasem přeměny 270,95 dne a přeměňuje se na 68Ga, přičemž přeměna je ze sta procent řízena na základní hladinu. Gallium-68 s poločasem přeměny 67,83 min. pak poskytuje svojí přeměnou stabilní 68Zn. Celé schéma přeměny radionuklidového páru 68Ge-68Ga je uvedeno na Obr. 1. 2
Obr. 1. Přeměnové schéma páru 68Ge-68Ga. 2 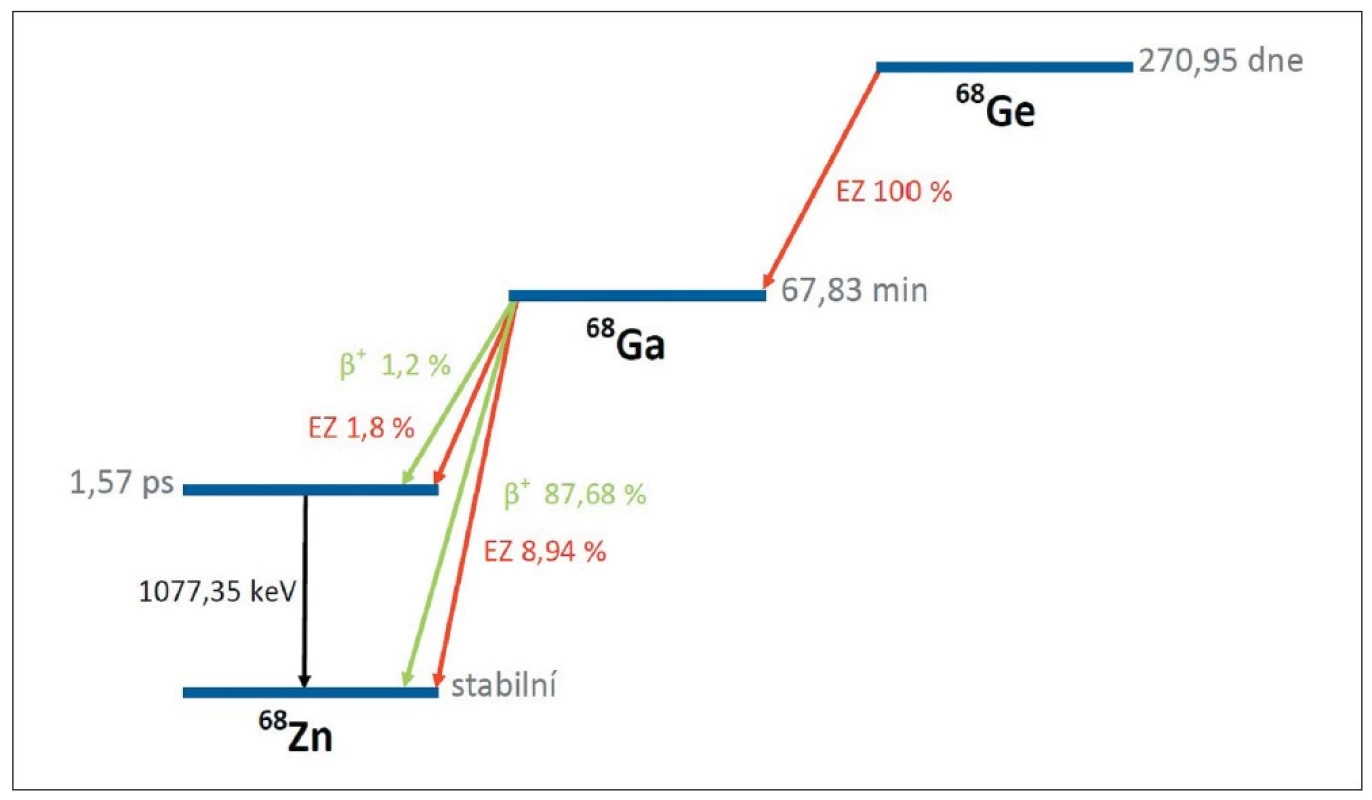
Jak je patrné, v případě 68Ga jde o smíšený zářič přeměňující se β+ přeměnou a elektronovým záchytem. Přeměna β+ je v rozpadovém schématu zastoupena 89 %, přičemž 1,2 % připadá na přeměnu realizovanou na vzbuzenou hladinu 68Zn a 87,68 % na základní stav 68Zn. V případě elektronového záchytu, který je zastoupen 11 %, připadá 1,8 % přeměn na vzbuzenou hladinu a 8,94 % na základní stav. Další minoritní přeměny nejsou pro jednoduchost ve schématu znázorněny. Nicméně je patrné, že přeměna 68Ga je doprovázena zářením gama a nejvýznamnější γ-linkou je 1077,35 keV. 2 Jelikož mateřské 68Ge nedisponuje vhodnou γ-linkou, lze ho detekovat pomocí dceřiného radionuklidu, a to především pomocí fotonů o energii 511 keV vzniklých anihilací vyzářených pozitronů. 18
Mateřské 68Ge je připravováno výhradně na cyklotronu. K jeho přípravě může vést několik cest. Nejvýznamnější z nich jsou uvedeny v Tab. 1. Preferovány jsou reakce (p,2n) na 69Ga a (p,xn) na přírodním Ga. Vzhledem k tomu, že první zmíněná reakce vyžaduje použití obohaceného galliového terče, je druhá reakce probíhající na přírodním galliu značně favorizovaná. Reakce jsou obvykle prováděny protony o energiích 20‒30 MeV a intenzitách svazku až 100 μA a vyšších, aby bylo dosaženo dostatečné aktivity 68Ge ˃ 37 GBq. V případě reakcí s protony o vyšších energiích nad 40 MeV přispívá k produkci 68Ge i (p,4n) reakce na přírodním 71Ga. 18,19
Tab. 1. Nejvýznamnější jaderné reakce vedoucí k přípravě 68Ge. 18 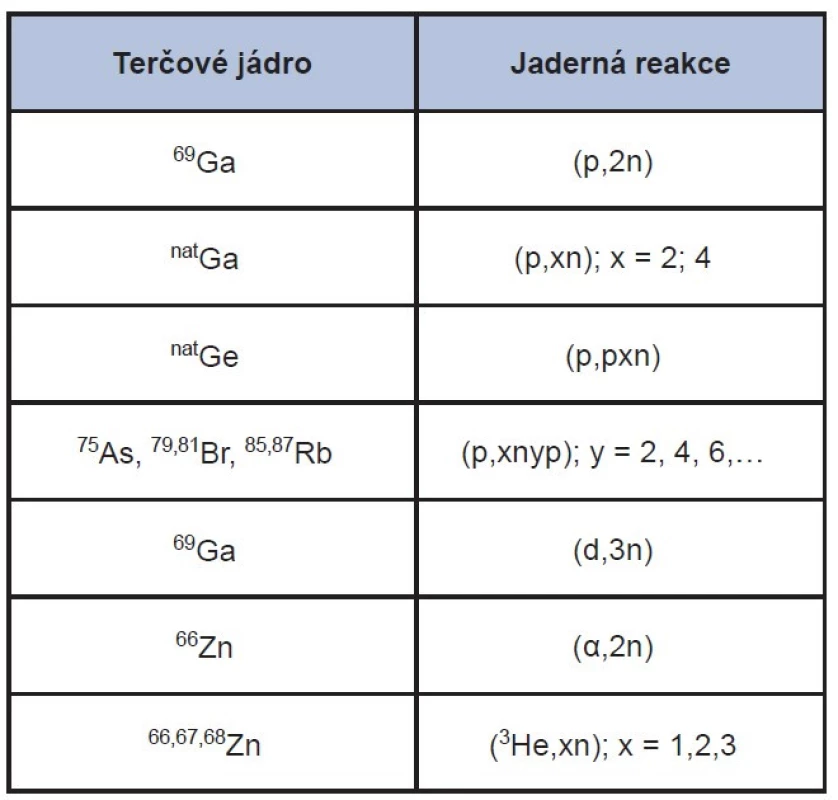
Terčový materiál pro realizaci takto vysoce energeticky náročných reakcí je nutné navrhnout tak, aby odolal zahřívání, ke kterému v terči dochází při disipaci energie odpovídající stovkám až tisícům wattů. Jako terčový materiál je tedy obvykle využívána sloučenina či slitina o velké tepelné, korozní a radiační stabilitě, jako je např. slitina Ga4Ni. Terč z této slitiny bývá obvykle v zadní části pokryt mědí, kde je chlazen vodou, a v přední části titanem, kde je chlazen plynným heliem. 20 Jako terč bývá rovněž využíváno i kovové gallium, které má sice v porovnání se svými sloučeninami výrazně nižší bod tání, nicméně při zapouzdření kovového gallia do niobové kapsle je možné tento problém eliminovat. Je zde využíváno vysoké stálosti niobu vůči korozi, která umožňuje velice intenzivní a efektivní vodní chlazení terče. Další možností je použití oxidů gallia, Ga2O3 či Ga2O. Při využití těchto materiálů je však výrobní proces limitován maximální použitelnou intenzitou svazku s ohledem na množství absorbované energie. 21
Ozářený terč je zpracováván v závislosti na složení základními separačními metodami obvykle dva týdny po ukončení ozařování. Nejčastěji je 68Ge po rozpuštění terče extrahováno do tetrachlormetanu. Slitina Ga4Ni bývá nejprve elektrochemicky rozpuštěna a 68Ge je následně extrahováno 9M HCl do tetrachlormetanu a zpětně extrahováno do vody. 20 V případě terče v niobovém pouzdře je terč nejprve rozpuštěn v 12M H2SO4. Následně je 68Ge extrahováno do tetrachlormetanu a zpět do vodné fáze je pak extrahováno 0,05M HCl. 22 Při uvedených procesech je však potřeba vždy brát v potaz extrémní těkavost GeCl4. Pro zpracování terče je vzhledem k tomu rovněž možné použít destilaci 68Ge ve formě GeCl4. 23
Pro další použití preparátu 68Ge nejen pro medicinální účely je zásadní jeho radionuklidová čistota, tedy poměr aktivity pocházející z 68Ge a celkové aktivity preparátu. Při přípravě může docházet k tvorbě dlouhodobých či krátkodobých vedlejších produktů pocházejících z matrice, obalu či dalších součástí terče. Z dlouhodobých radionuklidů je možné jmenovat 88Y s poločasem přeměny 106,65 dne či 88Zr s poločasem přeměny 83,4 dne. V případě přírodního Ga přispívá ke kontaminaci i vedlejší (p,n) reakce na 71Ga, která poskytuje 71Ge s poločasem přeměny 11,43 dne. Dlouhodobé neizotopické nečistoty jsou odstraňovány chemickou cestou, nejčastěji chromatograficky. V případě 71Ge je možné kontaminaci maximálně potlačit nastavením podmínek ozařování a poté dobou chladnutí terče. Krátkodobé radionuklidové nečistoty pocházejí především z vedlejších reakcí na galliovém terči a patří mezi ně 69Ge s poločasem přeměny 39,05 h a 67Ga s poločasem přeměny 3,26 dne. Tyto nečistoty však bývají eliminovány během doby chladnutí po ozáření terče. Radionuklidová čistota je kvantitativně stanovována pomocí gama-spektrometrie na polovodičových detektorech. 18
Při zpracování musí být rovněž kladen důraz na chemickou čistotu preparátu. Další skupinou nečistot jsou totiž stabilní prvky pocházející buď z přeměny výše popsaných nečistot nebo z terčového materiálu. Patří k nim izotopy niobu, železa, zinku či terčového gallia. Zbytky terčového gallia, které přejdou do organické fáze spolu s 68Ge, bývají obvykle separovány přímo při přípravě generátoru, aby bylo docíleno co nejvyšší specifické aktivity 68Ga v eluátu. Další nečistoty pak bývají eliminovány zejména chromatografickými postupy až na úroveň řádu ppm. Chemická čistota preparátu je sledována pomocí ICP-MS či ICP-OES. Jakékoli chemické nečistoty mohou mít následně vliv na možnosti využití eluátu 68Ga především pro medicínské účely. 18
Výroba 68Ge pomocí reakce natGa(p,xn)68Ge vyžaduje pracoviště disponující cyklotronem schopným produkovat protonové svazky o intenzitách 40–100 μA a více pro dosažení dostatečného výtěžku 68Ge. Největším problémem pro celosvětovou produkci 68Ge je limitovaný počet takových pracovišť. Seznam průmyslově významných pracovišť spolu s parametry výroby 68Ge je uveden v Tab. 2. Rutinní produkce 68Ge probíhá především v USA – Brookhaven National Laboratory a Los Alamos National Laboratory, v Rusku – Obninsk Cyclotron Co., Ltd. a v Jižní Africe – iThemba Laboratories. Tato zařízení jsou schopna jednorázové produkce 18,5–74 GBq. V případě Brookhaven National Laboratory je využíváno přírodní kovové gallium v niobové kapsli. Terč je ozařován protony o energii 30 MeV a intenzitě 85 μA. Při měsíčním ozařování terče o hmotnosti 81 g tak lze připravit 33–51 GBq 68Ge. V Los Alamos National Laboratory jsou k ozařování kovového gallia v niobové kapsli používány protony o energii 60 MeV a intenzitě 125 μA. Při ozařování 4 g kovového gallia po dobu 20 dní je možné vyprodukovat až 70 GBq 68Ge. Ruský Obninsk Cyclotron Co., Ltd. je schopen připravit 68Ge o specifické aktivitě ˃ 74 GBq/mg preparátu při ozařování Ge4Ni protony o energii 23 MeV a intenzitě několik stovek μA. 18
Tab. 2. Pracoviště připravující 68Ge a parametry přípravy – terčový materiál, energie protonů Ep, čas ozařování T, intenzita svazku I a vyrobená aktivita 68Ge A. 18 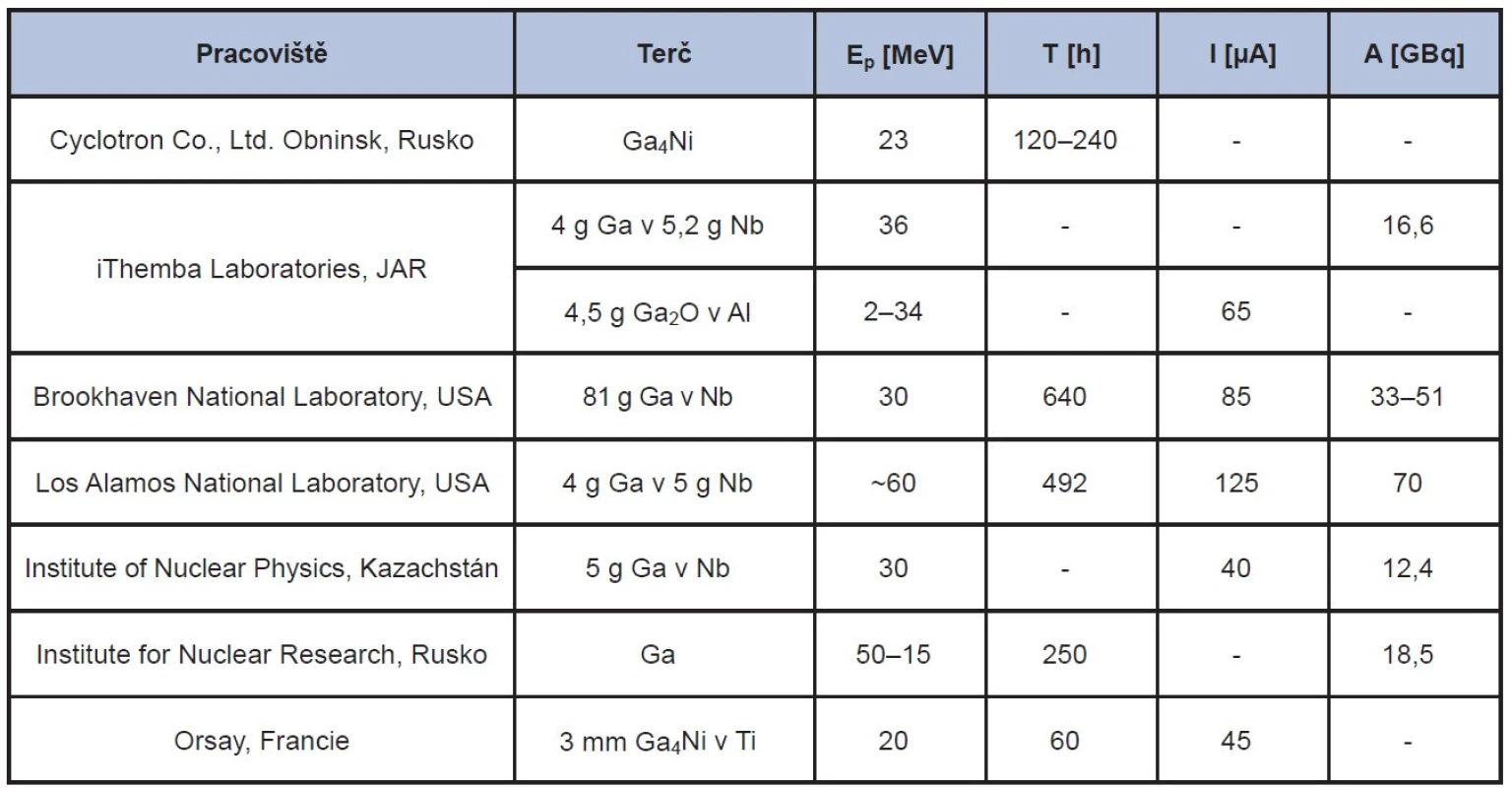
Pokračování v příštím čísle.
Poděkování: Tato práce byla podpořena granty Českého vysokého učení technického v Praze č. SGS19/194/OHK4/3T/14 (K.F. M.V., P. S., J. K.) a Technologické agentury ČR č. TJ01000334, TJ04000129 (K.F, M.V.) a TJ04000138 (P. S. a J. K.). Rádi bychom tuto práci věnovali doc. Ing. Ferdinandu Šebestovi, CSc. jako poděkování za jeho celoživotní přínos vědecké obci a dlouhodobou spolupráci nejen v oblasti vývoje separačních systémů.
Zdroje
- The Lund/LBNL Nuclear Data Search [online]. [cit. 2021-01-04]. 1999. Dostupné na: http://nucleardata.nuclear.lu.se/toi
- Marganiec-Galazka J, Nahle OJ, Kossert K. Activity determination of 68Ge/68Ga by means of 4πβ(Č)-γ coincidence counting. Appl Radiat Isotopes 2018;134 : 240-244
- Roesch F, Riss PJ. The Renaissance of the 68Ge/68Ga Radionuclide Generator Initiates New Developments in 68Ga Radiopharmaceutical Chemistry. Curr Top Med Chem 2010;10 : 1633-1668
- Council of Europe. European Pharmacopoeia - 9th edition, Strasbourg, 2018
- Lecoq de Boisbaudran PE. Caracteres chimiques et spectroscopiques d´un nouveau métal, le gallium, découvert dans une blende de la mine de Pierrefitte, vallée d´Argeles (Pyrénées). Comptes Rendus Hebdomadaires des Séances de l´Académie des Sciences 1875;81 : 493-495
- Gallium: Royal Society of Chemistry [online]. 2021. [cit. 2020-12-4]. Dostupné na: http://rsc.org/periodic-table/element/31/galium
- Hayes RL. The medical use of galium radionuclides: A brief history with some comments. Semin Nucl Med 1978;8 : 3:183-191
- SPC Gallium (Ga-67) Citrate Injection, Curium Netherlands B.V. Souhrn údajů o přípravku, 2019
- Gleason GI. A positron cow. Int J Appl Radiat Isot 1960;8 : 90–94
- Amir Reza J. An overview on Ga-68 radiopharmaceuticals for positron emission tomography. Iran J Nucl Med 2016;24 : 1–10
- Eiber M, Maurer T, Souvatzoglou M, et al. Evaluation of Hybrid Ga-68 PSMA Ligand PET/CT in 248 Patients with Biochemical Recurrence After Radical Prostatectomy. J Nucl Med 2015;56 : 668–674
- 68Ga-DOTA-Bombesin PET/MRI in imaging patients with prostate cancer: U.S. NATIONAL LABORATORY OF MEDICINE [online]. 2015 [cit. 2020-12-4] Dostupné na: https://clinicaltrials.gov/ct2/show/NCT02440308
- Biodistribution and dosimetry of serial PET imaging with Ga-68 labeled F(ab‘) 2-Trastuzumab: U.S. NATIONAL LABORATORY OF MEDICINE [online]. 2008 [cit. 2020-12-4] Dostupné na: https://clinicaltrials.gov/ct2/show/NCT00613847
- Schuhmacher J, Kaul S, Klivényi G, et al. Gallium-68 Chelate Imaging of Breast Cancer Pretargeted with Bispecific Anti-MUC1/Anti-Ga Chelate Antibodies. Cancer Res 2001;61 : 3712–3717
- SPC GalliaPharm 0,74-1,85 GBq, Eckert&Ziegler Radiopharma GmbH. Souhrn údajů o přípravku, 2019
- SPC SomaKit TOC 40 mikrogramů, Advanced Accelerator Applications. Souhrn údajů o přípravku, 2016.
- 68GA-PSMA-11: Státní ústav pro kontrolu léčiv [online]. [cit. 2021-7-29] Dostupné na: https://www.sukl.cz/modules/medication/detail.php?kod=0232633
- IAEA. Production of long lived parent radionuclides for generators: 68Ge, 82Sr, 90Sr and 188W. IAEA Radioistopes and Radiopharmaceiticals series No. 2. IAEA, Vienna 2010
- IAEA. Charged Particle Cross-section Database for Medical Radioisotope Production: Diagnostic Radioisotopes and Monitor Reactions, IAEA-TECDOC-1211, IAEA, Vienna 2001
- Razbash AA, Sevastianov YG, Krasnov NN. “Germanium-68 row of products”, in Proc. 5th Int. Conf. on Isotopes (5ICI), Brussels, 2005, Medimond, Bologna 2005 : 147–151
- Fassbender M, et al., Nuclear chemical aspects of medical generator nuclide production at the Los Alamos hot cell facility, Radiochim Acta 2004;92 : 237–243
- Van der Walt TN & Vermeulen C. Thick targets for the production of some radionuclides and the chemical processing of these targets at iThemba LABS, Nucl Instr Methods Phys Res 2004;521 : 171–175
- Grant PM, Miller DA, Gilmore JS, et al. Medium-energy spallation cross sections, 1. RbBr irradiation with 800 MeV protons. Int J Appl Radiat Isot 1982;33 : 415–417
Štítky
Nukleární medicína Radiodiagnostika Radioterapie
Článek Dalšími jubilanty jsouČlánek Noví členové společnostiČlánek Zrušené členstvíČlánek Historický kvízČlánek Sonda do historie
Článek vyšel v časopiseNukleární medicína
Nejčtenější tento týden
2021 Číslo 4- Biochemoterapie agresivního karcinomu rekta – kazuistika z českého prostředí
- MDT Board: unikátní projekt pro lékaře pečující o pacienty s onemocněním plic a dalšími patologiemi v oblasti hrudníku
- Idiopatická plicní fibróza a refluxní choroba: silný vztah plný nejasností
- Intersticiální plicní procesy a jejich fibrotická progrese
- Konverzní léčba hraničně resekabilních jaterních metastáz kombinací mFOLFOX6 + panitumumab – kazuistika
-
Všechny články tohoto čísla
- Dynamický SPECT a kvantifikace coronary flow reserve na CZT kameře
- Perspektiva zobrazování duktálního adenokarcinomu pankreatu pomocí 68Ga-analogů neurotenzinu
- Historie, současnost a budoucnost používání 68Ge/68Ga generátorů – 1. část
- Ústav nukleární medicíny 1. LF UK a VFN v Praze
- Dalšími jubilanty jsou
- Noví členové společnosti
- Zrušené členství
- Významné životní jubileum v tomto čtvrtletí slaví
- Historický kvíz
- Sonda do historie
- KoronaVIRtuální Dny nukleární medicíny
- XLII. Pracovní den Radiofarmaceutické sekce ČSNM, Husinec – Řež
- Nukleární medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Dynamický SPECT a kvantifikace coronary flow reserve na CZT kameře
- Ústav nukleární medicíny 1. LF UK a VFN v Praze
- Historie, současnost a budoucnost používání 68Ge/68Ga generátorů – 1. část
- Perspektiva zobrazování duktálního adenokarcinomu pankreatu pomocí 68Ga-analogů neurotenzinu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



