-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Výskyt srdečního selhání po infarktu myokardu v klinických studiích
The incidence of congestive heart failure after myocardial infarction in clinical studies
Myocardial infarction and congestive heart failure are two of the most important diagnoses in modern cardiology. The historical development of treatment of these diseases has been determined by many famous clinical trials. We analyzed 28 selected studies that investigated pharmacotherapy of myocardial infarction, dividing them to 4 main groups (beta blockers, renin-angiotensin-aldosterone system blockers, statins and antiaggregants). We see in our analysis that there is no evidence that beta blockers, hypolipidemic drugs, or antiaggregants influence the incidence of congestive heart failure. The only positive data we have is the data for renin-angiotensin-aldosterone system blockers. However, the proof is still missing that the combination of ACE inhibitors and angiotensin-receptor blockers is beneficial in comparison to monotherapy.
Keywords:
congestive heart failure – acute myocardial infarction – clinical trials – beta blockers – RAAS blockers – statins – antiaggregants
Autoři: J. Kaňovský; J. Špinar
Působiště autorů: Interní kardiologická klinika LF MU a FN Brno
Vyšlo v časopise: Kardiol Rev Int Med 2010, 12(3): 118-123
Souhrn
Infarkt myokardu a srdeční selhání patří k nejvýznamnějším diagnózám, na které se zaměřuje moderní kardiologie. Vývoj léčby těchto onemocnění byl určován významnými klinickými studiemi. Provedli jsme analýzu 27 studií týkajících se léčby po infarktu myokardu hlavními lékovými skupinami (betablokátory, blokátory renin-angiotenzin-aldosteronového systému, statiny a antiagregancia) a zaměřili se na výskyt srdečního selhání. Z naší analýzy nevyplývá, že by betablokátory, hypolipidemika nebo antitrombotika zásadněji ovlivňovaly výskyt srdečního selhání po infarktu myokardu, a tak jediná pozitivní data v tomto směru máme pro léky blokující RAAS – ACE-I a ARB, zatím však bez průkazu, že by byla vhodná jejich kombinace.
Klíčová slova:
srdeční selhání – akutní infarkt myokardu – klinické studie – betablokátory – inhibitory RAAS – statiny – antiagreganciaÚvod
Klinické studie (KS) jsou základním stavebním kamenem dnešní medicíny založené na důkazech a léčbu pacientů bez takto získaných tvrdých statistických dat si již v dnešní době snad ani neumíme představit. Ve většině případů jsou tyto moderní multicentrické zaslepené projekty samozřejmě zaměřeny především na primární a sekundární cíle studie a pro obecnější zjištění ze současného výzkumu jsme pak často odkázáni na subanalýzy těchto velkých souborů. Na druhou stranu je nutno říci, že nám tyto projekty přinášejí mimořádně cenná data oproti době před „evidence-based medicine“ – stačí si otevřít několik desetiletí staré ročníky nejvěhlasnějších lékařských časopisů, které připomínají sborníky kazuistik.
Infarkt myokardu je definován jako akutní lokální ischemická nekróza srdečního svalu vzniklá na podkladě náhlého uzávěru či progresivního extrémního zúžení věnčité tepny zásobující příslušnou oblast [1]. Jeho terapie prošla v posledních desetiletích mimořádně intenzivním vývojem vedoucím k výsledkům, které dalece převyšují úspěšnost léčby před několika lety až desetiletím. Rozvinula se jak farmakologická léčba, tak především akutní léčba intervenční, v České republice více než kde jinde. Současně je nutno vzít na vědomí i zřejmý fakt, že stále dokonalejší léčba IM vede ke zvýšení počtu zachráněných pacientů s těžkými formami akutního infarktu vedoucími k vývoji SS jako následku ischemie [2].
Pacienti po IM mají většinou doporučeny čtyři lékové skupiny: betablokátory (BB), blokátory renin-angiotenzin-aldosteronového systému (RAAS), kam patří ACE inhibitory (ACE-I) a blokátory receptoru I pro angiotenzin II (ARB), hypolipidemickou léčbu (především statiny (ST)) a antiagregancia. Tuto paletu léků v současnosti užívá okolo 90 % pacientů po prodělaném infarktu myokardu [3,4].
S vědomím výše uvedeného jsme se rozhodli provést analýzu významných KS týkajících se léčby infarktu myokardu (IM) vybranými lékovými skupinami. Z výsledků proběhlých KS víme, že byl v mnoha z nich prokázán prospěšný vliv na mortalitu pacientů a kompozitní cíle kardiovaskulární morbidity. Položili jsme si tedy otázku, zda kromě mortality tyto známé projekty dokládají i ovlivnění výskytu SS u zařazených pacientů.
Významné klinické studie
Do výběru klinických studií jsme zahrnuli celkově 28 významných prací zabývajících se efektem farmakoterapie IM, z nichž byla naprostá většina publikována v období posledních dvaceti let. KS jsme rozdělili podle zkoumané účinné látky v souladu s výše uvedenými základními skupinami léčiv podávaných po IM (betablokátory, blokátory RAAS, statiny a antiagregancia) (tab. 1).
Tab. 1. Výběr významných klinických studií s AIM. 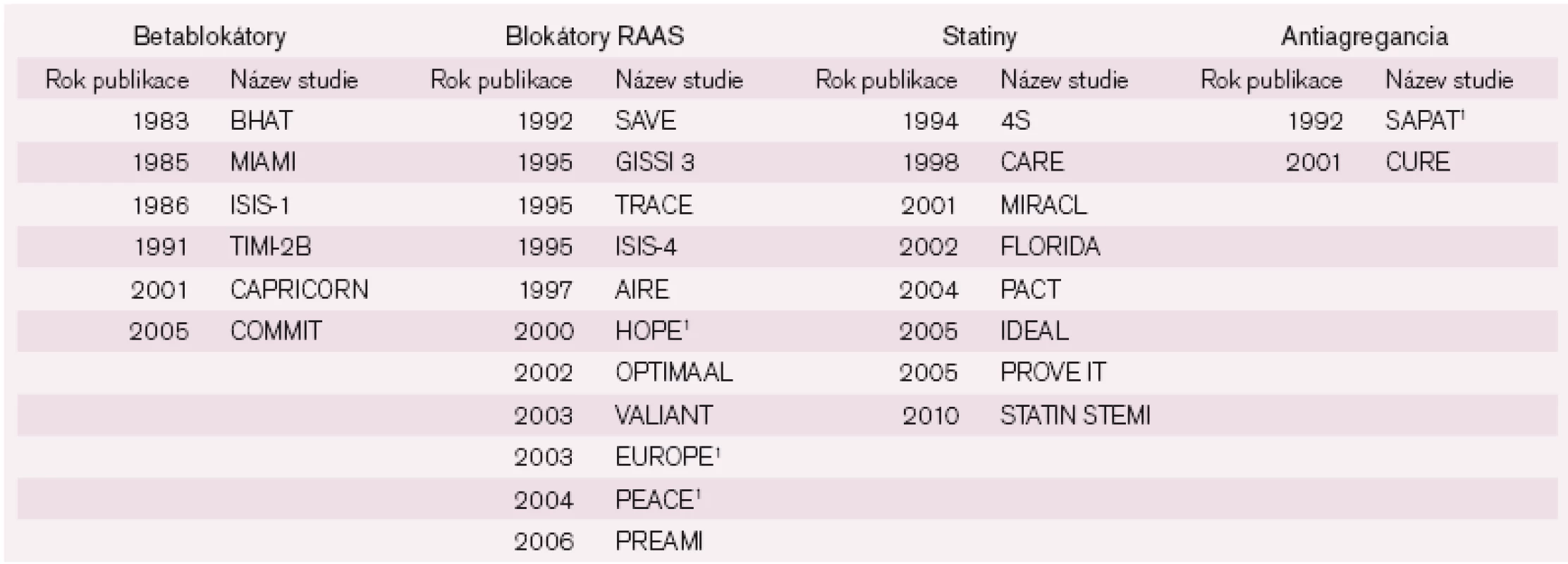
1IM nebyl výlučným vstupním kritériem, viz. vysvětlení v textu. Betablokátory
Betablokátory (BB) v akutní fázi IM a v sekundární prevenci po IM patří v těchto indikacích mezi nejdéle užívaná farmaka, jsou známy a podávány již několik desítek let [5]. Musíme zmínit tři studie, které spadají sice před námi definované období uplynulých dvaceti let, ale svým významem si zasluhují nebýt vynechány. Navíc přínos BB u IM je natolik uznávanou a zřejmou veličinou, že již těžko lze očekávat v budoucnosti nějakou novou placebem kontrolovanou studii. První studie BHAT (Betablocker Heart Attack Trial) [6] z roku 1983, kde byl podávaným lékem propranolol, prokázala na 4 000 nemocných celkové snížení úmrtnosti o 26 %. Srdeční selhání se zde vyskytovalo z 9,2 %. Do podobného období spadá placebem kontrolovaná studie MIAMI (Metoprolol In Acute Myocardial Infarction) [7], v níž prokázal výzkumný tým na 5 778 pacientech pokles mortality o 13 % v 15 dnech, kritéria SS splnilo 23,5 %. Poslední studie z let osmdesátých ISIS-1 (International Study of Infarct Survival) [8] sledovala již 16 027 nemocných, podávaným lékem byl atenolol a pokles úmrtnosti byl 30 % během prvních 24 hod, resp. 15 % během sedmi dnů po AIM. Výskyt SS v této studii není dostatečně dokumentován. Zajímavou, ale v počtu pacientů malou studií byl projekt APSI [9] publikovaný roku 1990, hodnotící efekt acebutololu u pacientů s vysokým rizikem úmrtí po IM. Studie byla ukončena předčasně pro nízkou mortalitu v placebo skupině oproti předpokládané (12 % v době ukončení po necelém roce, očekávání se pohybovala okolo 20 %). I přesto však byla kardiovaskulární mortalita ve skupině s acebutololem snížena o 58 % (p = 0,006). Snížení mortality zde bylo dáno i snížením rizika úmrtí na srdeční selhání. Vzhledem k faktu nedokončení studie a jejímu velmi malému rozsahu oproti jiným projektům s BB jsme ji nezahrnuli ani do přehledové tabulky.
Z novodobých studií jsme vybrali tři. TIMI IIB (Thrombolysis In Myocardial Infarction trial – phase 2B) [10] byla publikována v roce 1991 a prokázala snížení akutní koronární úmrtnosti a reinfarktů po časném podání intravenózního metoprololu po trombolýze. Současně však popisuje ve skupině pacientů s časným podáním BB statisticky nevýznamný (p = 0,10) trend k většímu výskytu nově vzniklého SS (15,3 %) v porovnání se skupinou, jíž byly BB podány opožděně (12,2 %). CAPRICORN (CArvedilol Post-infaRct survIval COntRol in LV dysfunctioN) [11] z roku 2001 ukázala prospěšnost carvedilolu po AIM i u porušené funkce levé komory. Ve studii sledovaný výskyt hospitalizací pro SS nebyl statisticky významně rozdílný. Jednou z posledních studií je placebem kontrolovaná COMMIT (ClOpidogrel and Metoprolol in Myocardial Infarction Trial) [12], v níž bylo randomizováno 45 852 pacientů. Časné podání intravenózního metoprololu a jeho následné užívání v perorální formě zde vedlo ve větvi s účinnou látkou ke statisticky významnému poklesu reinfarktů a maligních arytmií, ovšem za cenu výrazného nárůstu vývoje kardiogenního šoku (KŠ), stejně tak byl popsán statisticky významný nárůst (!) výskytu SS mimo KŠ (14,1 % ve větvi s metoprololem vs 12,7 % v placebové skupině). Navzdory tomuto efektu mortalita pacientů ovlivněna nebyla. K tomuto projektu je vhodné poznamenat, že metoprolol byl podáván v akutní fázi IM intravenózně v dávce max. 3 × 5 mg po 15 minutách (při hypotenzi a bradykardii se 2., event. 3. dávka vynechala) a poté v následujících dnech v perorální formě ve stoupající dávce 50–200 mg. Kontraindikací k randomizaci byly mj. primární koronární intervence a hypotenze se systolickým tlakem pod 100 mmHg. Pozoruhodné je, že oproti jiným studiím známky srdečního selhání Killip II a III nebyly kontraindikací. Sledování pacientů probíhalo pouze čtyři týdny. Na výsledky tohoto projektu naznačující zvýšení rizika SS při podání metoprololu je tedy nutno nahlížet ve světle těchto faktů. (Souhrn a analýza výskytu srdečního selhání u uvedených studií s BB v tab. 2.)
Tab. 2. Souhrn a analýza výskytu srdečního selhání u vybraných klinických studií. 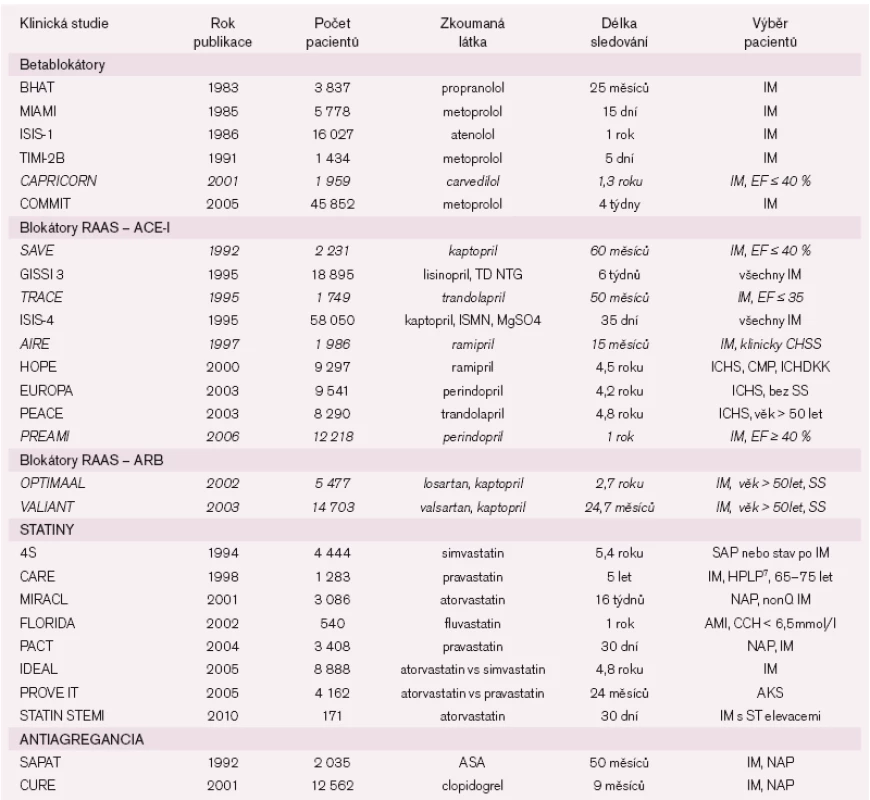
Pokračování tab. 2.<br><br>*statistická významnost v neprospěch zkoumané látky<br>+SS v celém souboru<br><sup>1ab</sup> a = časné podání BB, b = pozdní podání BB<br><sup>2</sup>SS vyžadující hospitalizaci<br><sup>3</sup>pacienti se zjevnými známkami SS vyloučeni při randomizaci<br><sup>4</sup>SS vyžadující hospitalizaci<br><sup>5</sup>SS již vstupním kritériem<br><sup>6</sup>udáván kombinovaný údaj smrt + hospitalizace pro SS<br><sup>7</sup>HPLP - hyperlipidemie, celk. cholesterol < 6,2mmol/l a LDL cholesterol 3,0–4,5 mmol/l<br><sup>8</sup>výskyt za inciální hospitalizace<br><br>(A)IM – (akutní) infarkt myokardu, TD NTG – transdermální nitroglycerin, ISMN – isosorbid-5-mononitrát, EF – ejekční frakce (levé komory), SAP – stabilní angina pectoris, CCH – celkový cholesterol, NAP – nestabilní angina pectoris, CMP – cévní mozková příhoda, ICHDKK – ischemická choroba dolních končetin, AKS – akutní koronární syndrom, ASA – kyselina acetylsalicylová.<br>Pozn.: Kurzivou vyznačeny klinické studie, kde bylo vstupním kritériem SS nebo výrazná deprese EFLK. 
Blokátory renin-angiotenzin-aldosteronového systému (ACE inhibitory a blokátory receptoru I pro angiotenzin II)
Počet velkých klinických studií s ACE-I u IM je zřejmě nejvyšší ze všech uvedených skupin, kumulativní počet pacientů již před několika lety atakoval šestimístná čísla. Postupným vývojem prošly indikace [5], v současné době si již neumíme představit pacienta po AIM, který by (s výjimkou několika málo kontraindikací, nejčastěji hypotenze) léky z této skupiny nebyl léčen. ARB jsou farmaka, která doplňují portfolio léků ovlivňující RAAS, a jejich indikaci u pacientů po IM nalezneme vzhledem k níže uvedeným výsledkům dostupných studií pouze tam, kde při podávání ACE-I nemocný netoleruje nežádoucí účinky (obvykle suchý dráždivý kašel). Pozitivní efekt kombinovaného podávání ACE-I a ARB zatím nebyl prokázán.
Vzhledem k tomu, že v mnoha KS s blokátory RAAS bylo srdeční selhání (event. významně snížená ejekční frakce levé komory srdeční (EFLK)) jedno ze vstupních kritérií a některé z nejvýznamnějších KS zařazovaly pacienty s chronickou ischemickou chorobou srdeční (ICHS) (z nichž jen někteří měli anamnézu IM), rozdělili jsme zde práce do tří skupin: studie u pacientů po IM bez dysfunkce LK, studie u pacientů po IM s dysfunkcí LK a studie u pacientů po IM s chronickou ICHS. Třetí skupinu zahrnující projekty HOPE, EUROPA a PEACE uvádíme s vědomím toho, že jde o projekty randomizující nemocné s chronickou ICHS, kde všichni pacienti neměli anamnézu prodělaného IM, tudíž plně nesplňují okruh zájmu našeho přehledu. Důvodem k jejich citaci je však především jejich mimořádný klinický význam a dopad jejich výsledků na denní klinickou praxi.
Studie s blokátory RAAS u pacientů po IM s dysfunkcí LK
Vzhledem k tomu, že v mnoha KS s blokátory RAAS byli zařazováni primárně pacienti s klinickými známkami srdečního selhání nebo depresí funkce LK, je nutno v tomto světle vidět i výsledky těchto projektů. Projekt SAVE (Survival And Ventricular Enlargement) [13] z roku 1992 byl jednou z prvních studií s ACE-I, kde se při podávání kaptoprilu prokázalo mj. snížení mortality ze všech příčin o 19 % proti placebu. Zařazováni byli pacienti s EFLK 40 % a méně, kteří nesměli vstupně vykazovat známky srdečního selhání. Studie prokázala nižší výskyt SS ve skupině s účinnou látkou (14 % oproti 17 %, p = 0,019). Další známou studií je TRACE (TRAndolapril Cardiac Evaluation) [14] z roku 1995, která randomizovala 1 749 pacientů k léčbě trandolaprilem proti placebu a vedla ke statisticky významnému snížení mortality ve větvi s účinnou látkou (34,7 %) proti placebu (42,3 %). Zařazeni byli pacienti s EFLK 35 % a méně a léčba ACE-I zde také vedla k nižšímu výskytu SS (14,3 % proti 19,6 %, p = 0,003). Studie AIRE (Acute Infarction Ramipril Efficiacy) [15] publikovaná v roce 1997 zařadila 1 986 pacientů, redukce celkové mortality zde dosáhla 27 %. Vstupním kritériem byly zjevné známky srdečního selhání, proto se k jeho výskytu v souboru nelze spolehlivě vyjadřovat.
I přesto, že u ARB nenalezneme reprezentativní projekt, který by u pacientů s anamnézou IM validně sledoval výskyt srdečního selhání, považujeme za vhodné zmínit dvě významné studie, jež zařazovaly pouze pacienty po IM, kteří již srdeční selhání měli manifestováno. Tou první je projekt OPTIMAAL (OPtimal Trial In Myocardial infarction with the Angiotensin II Antagonist Losartan) [16] z roku 2002, kde byl naznačen trend většího profitu ve prospěch kaptoprilu, který ale nedosáhl statistické významnosti. Jedinou modalitou, v níž bylo možno vidět výhodu losartanu, byl nižší výskyt nežádoucích účinků. Výsledky byly následně víceméně potvrzeny studií VALIANT (Valsartan in Acute Myocardial Infarction Trial) [17]. Zde bylo randomizováno 14 703 pacientů do tří skupin (valsartan, valsartan + kaptopril a kaptopril). Mezi skupinami pacientů zde nebyl nalezen žádný rozdíl v kardiovaskulární mortalitě a morbiditě, opět byl prokázán nižší výskyt vedlejších účinků v losartanové větvi. V žádné z těchto dvou KS nebyl výskyt srdečního selhání interpretovatelně hodnocen.
Studie s blokátory RAAS u pacientů po IM bez dysfunkce LK
Podávání lisinoprilu ve studii italských autorů GISSI-3 (Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto Miocardico) [18] publikované v roce 1995 vedlo k poklesu mortality o 11 %, výskyt srdečního selhání nebyl signifikantně ovlivněn. V roce 2005 byla publikována druhá, svým rozsahem s počtem pacientů ohromující studie ISIS-4 (Fourth International Study of Infarct Survival) [19], která na 58 050 pacientech prokázala signifikantní 7% pokles mortality ve skupině léčené kaptoprilem. Ani zde nebyl vliv na SS zaznamenán, navíc je u této KS nutno podotknout, že sledování pacientů trvalo pouhých 35 dní, a proto je význam výsledků výrazně nižší než u projektů sledujících pacienty řádově měsíce až roky. Poslední velkou studií s ACE-I v sekundární prevenci AIM byl projekt PREAMI (Perindopril and Remodelling in Elderly with Acute Myocardial Infarction) [20], který v roce 2006 randomizoval 1 252 pacientů. Ve větvi s perindoprilem nebyl zjištěn signifikantní pokles mortality, nicméně byl pozorován významně nižší výskyt remodelace levé komory srdeční (LK). Vstupním kritériem byla EFLK 40 % nebo vyšší, výskyt SS nebyl významně ovlivněn.
Studie s blokátory RAAS u pacientů s chronickou ICHS
První obrovskou KS je v této skupině nepochybně projekt HOPE (Heart Outcomes Prevention Evaluation) [21], kde byl 9 279 pacientům podáván ramipril proti placebu. V roce 2000 publikovali autoři výsledky prokazující významné snížení kardiovaskulární i celkové mortality (10,4 % vs 12,2 %, p = 0,005), výskyt srdečního selhání byl také nižší (9,0 % vs 11,5 %, p < 0,001). Dále nelze nezmínit všeobecně dobře známou studii EUROPA (The EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease) [22] z roku 2003, v níž tvořili nejvíce početnou národní skupinu nemocní z České republiky. Anamnestická data souboru zahrnovala 100 % pacientů s diagnózou ICHS, 64 % pacientů prodělalo v minulosti IM. Do studie bylo zařazeno 12 218 pacientů a za průměrnou dobu sledování 4,2 roku sice nedošlo k poklesu celkové mortality, ale byla zjištěna vysoce významná redukce incidence IM (o 24 %) a SS (o 39 %). Třetí velkou KS z této skupiny byl projekt PEACE (Prevention of Events with Angiotensin Converting Enzyme inhibition) [23], kde bylo randomizováno 8 290 pacientů s anamnézou stabilní ICHS do dvou větví, v jedné byl podáván trandolapril, v druhé placebo. Pokles mortality ve skupině s účinnou látkou prokázán nebyl, byla zde však zjištěna významně nižší incidence srdečního selhání. (Souhrn a analýza výskytu srdečního selhání u uvedených studií s blokátory RAAS v tab. 2.)
Statiny
Hypolipidemická léčba patří v současnosti již mezi základní kameny mozaiky léčby v sekundární prevenci IM, především kvůli širokému rozšíření bezpečné a velmi účinné lékové skupiny statinů. Jedna z prvních velkých studií se statiny 4S (Scandinavian Simvastatin Survival Study) [24] přinesla v roce 1994 jasný důkaz o prospěšnosti terapie simvastatinem – celkovou mortalitu se podařilo snížit o 30 % a kardiovaskulární mortalitu o 42 %. Výskyt srdečního selhání ve studii 4S zhodnotili Kjekshus et al v práci z roku 1997 [25]. Ve skupině s účinnou látkou prokázali signifikantní snížení výskytu SS o 21%, které bylo dáno především redukcí rizika dalších koronárních příhod. V roce 1998 pak byla publikována studie CARE (Cholesterol And Recurrent Events) [26], která na 1 283 pacientech prokázala významný pokles fatálních a nefatálních IM o 25 %. Pokles koronární mortality o 20 % nedosáhl statistické významnosti. Projekt MIRACL (Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering) [27] z roku 2001 nenalezl u skupiny pacientů s vysokou dávkou atorvastatinu (80 mg/den) srovnanou s placebem významný rozdíl ani v mortalitě ani ve výskytu srdečního selhání či reinfarktů. Další studie FLORIDA (FLuvastatin On RIsk Diminishment after Acute myocardial infarction) [28] v roce 2002 zkoumala výskyt reziduální ischemie při terapii fluvastatinem, který nebyl v dané studii ovlivněn. Byl zachycen nesignifikantní trend k nižší mortalitě v léčené skupině. Ve studii PACT (Pravastatin in Acute Coronary Treatment) [29] publikované v roce 2004 byl testován vliv pravastatinu na výskyt kompozitního primárního cíle (smrt, reinfarkt, hospitalizace pro nestabilní anginu pectoris). Studie byla předčasně ukončena po náboru 3 408 pacientů vzhledem k měnící se klinické praxi a širokému rozšíření léčby statiny v populaci. Rozdíly mezi léčenou skupinou a skupinou, které bylo podáváno placebo, byly ve všech zkoumaných parametrech při tomto počtu pacientů nesignifikantní. V roce 2005 pak tým autorů ze severní Evropy publikoval studii IDEAL (Incremental Decrease in End points through Aggresive Lipid lowering) [30], kde porovnali podávání vysoké dávky atorvastatinu vůči standardní dávce simvastatinu. Mortalita ani výskyt srdečního selhání ovlivněny nebyly, byla prokázána nižší incidence nefatálních IM. Projekt PROVE IT-TIMI 22 (PRavastatin Or atorVastatin Evaluation and Infection Therapy-Thrombolysis In Myocardial Infarction 22) [31] ve stejném roce jako IDEAL dokladoval benefit vysoké dávky atorvastatinu (80 mg/den) v porovnání se standardní dávkou pravastatinu (40 mg/den) u pacientů s diagnostikovaným akutním koronárním syndromem (AKS). Kompozitní cíl zahrnující smrt, IM či rehospitalizaci pro AKS byl ve skupině s atorvastatinem významně snížen (15,7 % vs 20,0 %, p = 0,0002), srdeční selhání nebylo ve studii interpretovatelně hodnoceno. Zatím poslední studií, jejíž výsledky byly teprve letos představeny odborné veřejnosti, je STATIN STEMI (Efficacy of high-dose atorvaSTATIN loading before primary percutaneous coronary intervention in ST Elevation Myocardial Infarction) [32], která na relativně malé skupině 171 pacientů testovala efekt podání vysoké dávky (80 mg) atorvastatinu proti nízké dávce (10 mg) před koronární intervencí u akutního IM s ST elevacemi. (Souhrn a analýza výskytu srdečního selhání u uvedených studií se statiny v tab. 2.)
Antiagregancia
Antiagregace je dnes pro lékaře jedním ze základních kamenů terapie u pacientů po IM. Je tedy zajímavou skutečností, že před pouhými 18 lety, v roce 1992, byla publikována studie SAPAT (Swedish Angina Pectoris Aspirin Trial) [33], která srovnávala podávání acetylsalicilové kyseliny (ASA) v dávce 75 mg denně vůči placebu, přičemž všichni pacienti v projektu byli léčeni sotalolem a měli anamnézu stabilní anginy pectoris. Autoři zde dokázali signifikantní snížení výskytu nefatálního IM a náhlé srdeční smrti, srdeční selhání nicméně hodnoceno nebylo. V jednom z nejznámějších moderních projektů zabývajících se antiagregancii, studii CURE (Clopidogrel in Unstable angina to prevent Recurrent Events) [34] z roku 2001 bylo 12 562 pacientů s diagnózou AKS randomizováno k užívání clopidogrelu nebo placeba po dobu 3–12 měsíců. Ve skupině s clopidogrelem byl nalezen významný pokles incidence kompozitního cíle, který zahrnoval MI, cévní mozkovou příhodu a úmrtí z kardiovaskulárních příčin (9,3 % vs 11,4 %). Výskyt srdečního selhání, hodnocený ovšem pouze za iniciální hospitalizace, byl signifikantně snížen také. (Souhrn a analýza výskytu srdečního selhání u uvedených studií s antiagregancii v tab. 2.)
Závěr
Vzhledem k časovému období zahrnujícímu zkoumané studie je zřejmé, že jednotlivé studie jsou velmi heterogenní ve způsobu léčby a charakteristice souborů pacientů. V mnoha projektech bylo srdeční selhání buď vylučovacím, nebo naopak vstupním kritériem. Délka sledování pokrývala široké spektrum času od pěti dní až po více než pět let. Z tohoto pohledu samozřejmě není možné provést seriózní statistické zpracování studií podle jednotlivých lékových skupin jako celku a je třeba hodnotit výsledky také v kontextu každého jednotlivého projektu.
Je zřejmé, že výskyt srdečního selhání po infarktu myokardu je v současnosti na vzestupu, především díky zlepšujícím se možnostem terapie těžkých forem IM. Do budoucna je nutno počítat se stále větší skupinou pacientů vyžadujících po IM dlouhodobou komplexní léčbu SS. Optimální terapie IM minimalizující výskyt SS by tak měla být prioritou současného výzkumu.
Z naší analýzy nevyplývá, že by betablokátory, hypolipidemika nebo antitrombotika zásadněji ovlivňovaly výskyt srdečního selhání po IM, a tak jediná pozitivní data v tomto směru máme pro léky blokující RAAS – ACE-I a ARB, zatím však bez průkazu, že jejich kombinace by byla vhodná. Čestnou výjimkou z tohoto tvrzení je v našem přehledu studie 4S se simvastatinem, v níž byl při dlouhodobém sledování prokázán pokles výskytu srdečního selhání, a to v důsledku snížení rizika rekurence koronárních příhod.
Přesto je zajímavé pokusit se podívat na všeobecně známé, významné projekty z úhlu celkového pokroku léčby infarktu myokardu v posledních desetiletích. V určitém ohledu jsme tak v naší práci zkoumali základní kameny, které dláždily cestu vývoje moderní kardiologie, tak jak ji známe dnes, i s mimořádně účinnou a úspěšnou farmakologickou a intervenční léčbou. Přejme si, aby tento trend trval i nadále.
MUDr. Jan Kaňovský
prof. MUDr. Jindřich Špinar, CSc., FESC
Interní kardiologická klinika LF MU
a FN Brno
jkanovsky@fnbrno.cz
Zdroje
1. Aschermann M et al. Kardiologie. Praha: Galén 2004.
2. Velagaleti RS, Pencina MJ, Murabito JM et al. Long--term trends in the incidence of heart failure after myocardial infarction. Circulation 2008; 118 : 2057–2062.
3. Špinar J, Sepši M, Ludka O. Registr Brno – Farmakoterapie po infarktu myokardu. Cor Vasa 2009; 51 : 128–130.
4. Špinar J, Ludka O, Sepši M et al. Registr Brno 2: Farmakoterapie po infarktu myokardu. Vnitř Lék 2010; 56 : 533–540.
5. Vítovec J, Špinar J et al. Farmakoterapie kardiovaskulárních onemocnění. Praha: Grada 2004.
6. Beta-Blocker Heart Attack Trial Research Group. A randomized trial of propranolol in patients with acute myocardial infarction: II. Morbidity results. JAMA 1983; 250 : 2814–2819.
7. The MIAMI Trial Research Group. Metoprolol in acute myocardial infarction (MIAMI). A randomised placebo-controlled international trial. Eur Heart J 1985; 6 : 199–226.
8. First International Study of Infarct Survival Collaborative Group. Randomised trial of intravenous atenolol among 16 027 cases of suspected acute myocardial infarction: ISIS-1. Lancet 1986; 2 : 57–66.
9. Boissel JP, Leizorovicz A, Picolet H et al. The APSI Investigators. Efficiacy of acebutolol after acute myocardial infarction (the APSI trial). Am J Cardiol 1990; 66 : 24C–31C.
10. Roberts R, Rogers WJ, Mueller HS et al. Immediate versus deferred beta-blockade following thrombolytic therapy in patients with acute myocardial infarction. Results of the Thrombolysis in Myocardial Infarction (TIMI) II-B Study. Circulation 1991; 83 : 422–437.
11. Dargie HJ. Effect of carvedilol on outcome after myocardial infarction in patients with left-ventricular dysfunction: the CAPRICORN randomised trial. Lancet 2001; 357 : 1385–1390.
12. Chen ZM, Pan HC, Chen YP et al. COMMIT (ClOpidogrel and Metoprolol in Myocardial Infarction Trial) collaborative group. Early intravenous then oral metoprolol in 45,852 patients with acute myocardial infarction: randomised placebo-controlled trial. Lancet 2005; 366 : 1622–1632.
13. Pfeffer MA, Braunwald E, Moyé LA et al. The SAVE Investigators. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction. Results of the survival and ventricular enlargement trial. N Engl J Med 1992; 327 : 669–677.
14. Køber L, Torp-Pedersen C, Carlsen JE et al. Trandolapril Cardiac Evaluation (TRACE) Study Group. A clinical trial of the angiotensin-converting-enzyme inhibitor trandolapril in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 1995; 333 : 1670–1676.
15. The Acute Infarction Ramipril Efficacy (AIRE) Study Investigators. Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction with clinical evidence of heart failure. Lancet 1993; 342 : 821–828.
16. Dickstein K, Kjekshus J. OPTIMAAL Steering Committee of the OPTIMAAL Study Group. Effects of losartan and captopril on mortality and morbidity in high-risk patients after acute myocardial infarction: the OPTIMAAL randomised trial. Optimal Trial in Myocardial Infarction with Angiotensin II Antagonist Losartan. Lancet 2002; 360 : 752–760.
17. McMurray J, Solomon S, Pieper K et al. The effect of valsartan, captopril, or both on atherosclerotic events after acute myocardial infarction: an analysis of the Valsartan in Acute Myocardial Infarction Trial (VALIANT). J Am Coll Cardiol 2006; 47 : 726–733.
18. Gruppo Italiano per lo Studio della Sopravvivenza nell'infarto Miocardico. GISSI-3: effects of lisinopril and transdermal glyceryl trinitrate singly and together on 6-week mortality and ventricular function after acute myocardial infarction. Lancet 1994; 343 : 1115–1122.
19. ISIS-4 (Fourth International Study of Infarct Survival) Collaborative Group. ISIS-4: a randomised factorial trial assessing early oral captopril, oral mononitrate, and intravenous magnesium sulphate in 58,050 patients with suspected acute myocardial infarction. Lancet 1995; 345 : 669–685.
20. Ferrari R. Perindopril and Remodeling in Elderly with Acute Myocardial Infarction Investigators. Effects of angiotensin-converting enzyme inhibition with perindopril on left ventricular remodeling and clinical outcome: results of the randomized Perindopril and Remodeling in Elderly with Acute Myocardial Infarction (PREAMI) Study. Arch Intern Med 2006; 166 : 659–666.
21. Yusuf S, Sleight P, Pogue J et al. The Heart Outcomes Prevention Evaluation Study Investigators. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. N Engl J Med 2000; 342 : 145–153.
22. Fox KM. EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease Investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet 2003; 362 : 782–788.
23. Braunwald E, Domanski MJ, Fowler SE et al. PEACE Trial Investigators. Angiotensin-converting-enzyme inhibition in stable coronary artery disease. N Engl J Med 2004; 351 : 2058–2068.
24. Scandinavian Simvastatin Survival Study Group. Randomised trial of cholesterol lowering in 4 444 patients with coronary heart disease: the Scandinavian Simvastatin Survival Study (4S). Lancet 1994; 344 : 1383–1389.
25. Kjekshus J, Pedersenb TR, Olssonb AG et al. The effects of simvastatin on the incidence of heart failure in patients with coronary heart disease. J Card Fail 1997, 3 : 249–254.
26. Lewis SJ, Moye LA, Sacks FM et al. Effect of pravastatin on cardiovascular events in older patients with myocardial infarction and cholesterol levels in the average range. Results of the Cholesterol and Recurrent Events (CARE) trial. Ann Intern Med 1998; 129 : 681–689.
27. Schwartz GG, Olsson AG, Ezekowitz MD et al. Myocardial Ischemia Reduction with Aggressive Cholesterol Lowering (MIRACL) Study Investigators. Effects of atorvastatin on early recurrent ischemic events in acute coronary syndromes: the MIRACL study: a randomized controlled trial. JAMA 2001; 285 : 1711–1718.
28. Liem AH, van Boven AJ, Veeger NJ et al. FLuvastatin On Risk Diminishment after Acute myocardial infarction study group. Effect of fluvastatin on ischaemia following acute myocardial infarction: a randomized trial. Eur Heart J 2002; 23 : 1931–1937.
29. Thompson PL, Meredith I, Amerena J et al. Pravastatin in Acute Coronary Treatment (PACT) Investigators. Effect of pravastatin compared with placebo initiated within 24 hours of onset of acute myocardial infarction or unstable angina: the Pravastatin in Acute Coronary Treatment (PACT) trial. Am Heart J 2004; 148: e2.
30. Pedersen TR, Faergeman O, Kastelein JJ et al. Incremental Decrease in End Points Through Aggressive Lipid Lowering (IDEAL) Study Group. High--dose atorvastatin vs usual-dose simvastatin for secondary prevention after myocardial infarction: the IDEAL study: a randomized controlled trial. JAMA 2005; 294 : 2437–2445.
31. Ray KK, Cannon CP, McCabe CH et al. PROVE IT-TIMI 22 Investigators. Early and late benefits of high-dose atorvastatin in patients with acute coronary syndromes: results from the PROVE IT-TIMI 22 trial. J Am Coll Cardiol 2005; 46 : 1405–1410.
32. Kim JS, Kim J, Choi D et al. Efficacy of high-dose atorvastatin loading before primary percutaneous coronary intervention in ST-segment elevation myocardial infarction: the STATIN STEMI trial. JACC Cardiovasc Interv 2010; 3 : 332–339.
33. Juul-Möller S, Edvardsson N, Jahnmatz B et al. The Swedish Angina Pectoris Aspirin Trial (SAPAT) Group. Double-blind trial of aspirin in primary prevention of myocardial infarction in patients with stable chronic angina pectoris. Lancet 1992; 340 : 1421–1425.
34. Yusuf S, Zhao F, Mehta SR et al. Clopidogrel in Unstable Angina to Prevent Recurrent Events Trial Investigators. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001; 345 : 494–502.
Štítky
Dětská kardiologie Interní lékařství Kardiochirurgie Kardiologie
Článek Autoři
Článek vyšel v časopiseKardiologická revue – Interní medicína
Nejčtenější tento týden
2010 Číslo 3- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- S prof. Vladimírem Paličkou o racionální suplementaci kalcia a vitaminu D v každodenní praxi
-
Všechny články tohoto čísla
- Personalizovaná medicína a snaha o lepší klinické rozhodování
- Komentář ke článku „Výskyt srdečního selhání po infarktu myokardu v klinických studiích“ autorů J. Kaňovského a J. Špinara
- Je ischemická choroba srdca u žien iná ako u mužov?
- Akutní infarkt myokardu u pacientů se srdečním selháním
- Výskyt srdečního selhání po infarktu myokardu v klinických studiích
- Studie SHIFT (The Systolic Heart Failure Treatment with the If Inhibitor Ivabradine Trial) a její význam pro léčbu srdečního selhání
- Kontrola krevního tlaku u diabetiků s ischemickou chorobou srdeční
- Rizikové faktory fibrilace síní
- Co musí vědět intervenční kardiolog o krevních destičkách
- Současné postavení pravastatinu v hypolipidemické léčbě
- Farmakoekonomika pro lékaře v klinické praxi
- Současné metody stanovení glomerulární filtrace a jejich klinický význam
- Autoři
- Kardiologická revue – Interní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Současné metody stanovení glomerulární filtrace a jejich klinický význam
- Farmakoekonomika pro lékaře v klinické praxi
- Rizikové faktory fibrilace síní
- Je ischemická choroba srdca u žien iná ako u mužov?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



