-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Pozdní morbidita u syndromu jizvy po císařském řezu
Late morbidity in cesarean section scar syndrome
Objective: To summarize recent knowledge on ethiology, diagnostic management and treatment possibilities of cesarean section scar syndrome (isthmocoele).
Design: Review article.
Setting: Department of Gynaecology and Obstetrics, Faculty Hospital and Palacky University, Olomouc; Department of Gynaecology and Obstetrics, Vítkovická nemocnice, Ostrava-Vítkovice.
Methods: A literature review of published data on cesarean section scar syndrome (isthmocoele).
Results: Cesarean section scar syndrome may be associated with subsequent complications including postmenstrual spotting or bleeding, dysmenorrhoea, abdominal pain, dyspareunia, infertility, scar pregnancy, a morbidly adherent placenta, scar dehiscence or rupture in later pregnancy. Ethiopathogenesis of isthmocoele remains poorly understood. Magnetic resonance, sonohysterography and transvaginal ultrasound are the gold standard imaging techniques for diagnosis. Surgical treatment is still controversial but should be offered to symptomatic women.
Conclusions: Given the association between an isthmocoele and gynaecological symptoms, obstetric complications and infertility, it is important to focus on preventive strategies of its development.
Keywords: cesarean section, late morbidity, isthmocoele, diagnosis, therapy
Autoři: V. Klimánková 1,2; R. Pilka 1
Působiště autorů: Porodnicko-gynekologická klinika LF UK a FN, Olomouc, přednosta prof. MUDr. R. Pilka 1; Porodnicko-gynekologické oddělení Vítkovické nemocnice, Ostrava-Vítkovice, primář MUDr. J. Měch 2
Vyšlo v časopise: Ceska Gynekol 2018; 83(4): 300-306
Kategorie: Přehledový článek
Souhrn
Cíl studie: Shrnout aktuální literární poznatky o etiopatogenezi, diagnostice a možných terapeutických postupech u syndromu jizvy po císařském řezu (isthmokély).
Typ studie: Přehledový článek.
Název a sídlo pracoviště: Porodnicko-gynekologická klinika, FN a LF UP Olomouc; Porodnicko-gynekologické oddělení, Vítkovická nemocnice, Ostrava-Vítkovice.
Metodika: Literární přehled získaný z prací, které zpracovávají téma defektního hojení jizvy po císařském řezu (isthmokély).
Výsledky: Syndrom jizvy po císařském řezu může být spojen s následnými komplikacemi ve smyslu postmenstruačního špinění či krvácení, dysmenorey, dyspareunie, infertility, gravidity v jizvě, defektní placentace a dehiscence nebo ruptury jizvy v následné graviditě. Etiopatogeneneze isthmokély zatím není dostatečně objasněna. Zlatým standardem v diagnostice je transvaginální ultrasonografie, sonohysterografie a magnetická rezonance. Chirurgická terapie je zatím kontroverzním tématem, ale symptomatickým ženám by měla být nabídnuta.
Závěr: Vzhledem k asociaci gynekologických symptomů, porodnických komplikací a infertility s isthmokélou, je třeba se zaměřit na možná preventivní opatření jejího rozvoje.
Klíčová slova: císařský řez, pozdní morbidita, isthmokéla, diagnostika, terapie
ÚVOD
Prevalence porodu císařským řezem (sectio cesarea, SC) v západním světě v posledních dekádách významně narůstá. Zaměříme-li se pouze na Českou republiku, tak zatímco v roce 1994 byla průměrná frekvence porodů císařským řezem 10 %, v roce 2004 to bylo 16 % a v roce 2014 již 26 % [22]. V některých zemích podíl SC vysoce převyšuje polovinu ze všech porodů. Například v Brazílii je v současnosti frekvence porodu císařským řezem 45,9 % s velmi rozdílnou distribucí podle sociálního statusu, kdy v soukromém sektoru převyšuje 80 % [1]. Díky tomuto trendu narůstá v populaci počet žen s jizvou přední děložní stěny a s ní spojenou morbiditou.
Již v roce 1999 byl do souvislosti s inkompletním zhojením jizvy po císařském řezu dán soubor obtíží – postmenstruační špinění, krvácení mimo cyklus, bolest jak menstruační, tak i při intermenstruačním krvácení, sekundární sterilita a dyspareunie, který je nyní označován jako syndrom jizvy po císařském řezu (Cesarean section scar syndrome) [8, 26, 28].
Nejčastějším nálezem u těchto žen je zářez tvaru „U“ či „V“, či jiné méně typické obrazy odpovídající ztenčení myometria v místě uterotomie, často viditelné už při rutinním ultrazvukovém vyšetření. V roce 2001 Monteagudo et al. zavedli pro tento nález termín „niche“ [16]. Mezi další termíny, se kterými se můžeme v anglosaské literatuře v této souvislosti setkat, patří „pouch-like defect“, či také „isthmokéla“, což je označení, které se začíná více prosazovat i u české odborné veřejnosti.
Rizika pro následnou graviditu jsou již dobře popsána. Jizva na děloze jednoznačně zvyšuje riziko poruch placentace z hlediska invaze, tedy placenta accreta, placenta increta a placenta percreta. Dále je rovněž rizikovým faktorem pro patologické umístění placenty ve smyslu nízce nasedajícího lůžka nebo centrálně uloženou placenta praevia [33]. Tyto patologické jevy se samozřejmě mohou ve zvýšené míře kombinovat. Diagnostikujeme-li tedy nízce nasedající lůžko v oblasti jizvy po SC, musíme myslet i na vyšší riziko defektní placentace v místě jizvy [6].
Závažnou těhotenskou komplikací, kterou je možné diagnostikovat již v rané graviditě, je ektopická nidace plodového vejce v místě jizvy. To může vést k ruptuře dělohy s možností akutního ohrožení ženy na životě kdykoliv během těhotenství [33].
Samostatnou, velmi diskutovanou a stále nedořešenou kapitolou je management následného porodu. Porodnická problematika komplikací jizvy po SC je velmi rozsáhlá, avšak není samotným předmětem tohoto sdělení.
V předkládané práci se snažíme podat přehled publikací z posledních let zabývajících se klinickými symptomy, příčinami, a možnostmi konzervativní a chirurgické léčby defektního jizvení uterotomie z pohledu gynekologa [7, 8, 13, 15, 23].
ETIOLOGIE A RIZIKOVÉ FAKTORY VZNIKU ISTHMOKÉLY
Řada studií se zabývá detekcí rizikových faktorů vzniku isthmokély. Bij de Vaate et al. je klasifikovali do čtyř kategorií [3].
Technika sutury
Ideální technika sutury uterotomie stále není dořešena, ale ve vztahu ke vzniku isthmokély se jeví bezpečnější dvouvrstevná sutura oproti jednovrstevné. Vhodnější jsou nepřehazované stehy (menší ischemizace tkání). Vyšší riziko se naopak jeví u sutury vynechávající endometrium, kdy nedojde k přiblížení myometria v celé jeho šíři. Dalším rizikovým faktorem je neprovedení peritonealizace s následným rozvojem časného adhezivního procesu, a tím tahu v místě jizvy [30].
Podle jiných zdrojů naopak technika sutury na kvalitu jizvy nemá vliv [2].
Lokalizace incize
Ideální umístění závisí na stupni dilatace porodních cest. Příliš nízko uložená uterotomie při pokročilejším porodnickém nálezu může vést k zavzetí cervikálních žláz do sutury, které následně mohou spoluvytvářet patologický obsah isthmokély. Naopak příliš vysoko umístěná uterotomie uložená mimo dolní segment děložní vede k vazivové přestavbě svaloviny, a tím k funkčnímu oslabení myometria s vyšším rizikem rozvoje pseudokavity [3, 21, 28].
Hojení tkání
Predispozicí pro defektní hojení jizvy je retroflexe dělohy, kdy je oblast uterotomie v přední stěně děložní pod vyšším tahem [29]. Jednoznačným rizikovým faktorem však je vyšší počet SC, kdy incidence isthmokély roste přímo úměrně s počtem provedených operací. Tato závislost je popisována v souvislosti s dále se zhoršující perfuzí v oblasti opakované sutury. V literatuře je popisován výskyt isthmokély v 62 % po jednom SC, v 68,2 % po dvou a v 77,8 % po třech SC) [27].
Smíšené faktory
V této skupině je jako další možný rizikový faktor uváděna například preeklampsie [30].
SYMPTOMATOLOGIE ISTHMOKÉLY
Špinění, postmenstruační krvácení, prolongovaná menstruace
Postmenstruační krvácení trvající alespoň dva dny udává až 30 % pacientek po SC s přítomnou isthmokélou, oproti 7–15 % bez její přítomnosti [4].
V hysteroskopickém obraze klinicky manifestních pacientek je často patrná kolekce tekuté či hemolyzované krve v oblasti pseudokavity isthmokély. Podle některých autorů zde dochází k retenci menstruační krve, která potom vytéká ve formě špinění po menstruaci. Příčinou retence krve v pseudokavitě může být zhoršená kontraktilita myometria v oblasti jizvy, která nedostačuje k vypuzení krve z pseudokavity. Fibroticky změněný dolní okraj jizvy prominující do dutiny děložní může sám o sobě omezovat drenáž menstruační krve do děložního hrdla [4]. Takto způsobené potíže mohou trvat až do ovulace, kdy dochází k relaxaci vnitřní branky dělohy díky peaku estrogenů [26]. Ve shodě s výše zmíněnou hypotézou je i pozitivní vztah mezi velikostí isthmokély a závažností špinění [4]. Podle některých studií dochází také k dysproporčnímu růstu endometria v isthmokéle [6].
Hysteroskopický nález fragilních cév podporuje teorii zdroje krvácení přímo ve stěně isthmokély. Ve shodě s tím je i histopatologický nález volných krevních elementů v endometriálním stromatu defektu [17].
Bolest, dysmenorea
Příčina bolestivosti v souvislosti s isthmokélou není zcela jasná, ale možná je souvislost s abnormálními svalovými kontrakcemi [31]. Studium histologických preparátů získaných při hysterektomii prokázalo chronický zánětlivý proces v oblasti defektu, jehož mediátory mohou neurohumorálně rovněž způsobovat bolest [23].
Sekundární sterilita
Příčina sterility při výskytu isthmokély není dostatečně objasněna, ale je prokázáno, že tekutina v oblasti pseudokavity vykazuje podobné znaky jako patologický obsah saktosalpingu. Přítomnost chronického zánětlivého procesu způsobuje změnu pH s následným toxickým efektem na spermie a negativním vlivem na nidaci embrya.
Zhoršená kvalita cervikálního hlenu a také prosté odplavení blastocysty přetrvávajícím krvácením mohou být dalšími patofyziologickými faktory [23].
DIAGNOSTIKA ISTHMOKÉLY
Isthmokéla se vyskytuje u 19–84 % pacientek po SC a je charakterizována ztenčením myometria přední stěny děložní v místě uterotomie s hloubkou nejméně 2 mm, podle některých prací pouze 1 mm [4, 24, 27]. Přesahuje-li hloubka defektu více než polovinu celkové šíře myometria, je defekt hodnocený jako závažný. Nelze-li v defektu děložní stěny detekovat vrstvu myometria vůbec, jedná se o dehiscenci jizvy. Isthmokélu či dehiscenci můžeme prokázat jak v celé šíři jizvy, tak lokalizovaně v její části. Méně obvykle mohou být v oblasti jizvy popsány inkluzní cysty [29]. V rámci kazuistik jsou reportovány také komunikace s vnějším povrchem dělohy charakteru fistulace, diagnostikované díky pronikání barviva při chromopertubaci nebo nález kapsulovaného hematomu [23].
Zajímavostí je, že struktura odpovídající isthmokéle byla poprvé popsána již v roce 1961 americkým gynekologem Poidevinem na hysterosalpingografickém obrazu. Ten hodnotil její přítomnost jako známku hojení, a tedy známku bezpečného následného vaginálního porodu [20].
V rámci diagnostiky isthmokély jsou využívány zejména transvaginální ultrasonografie, sonohysterografie, magnetická rezonance, hysterosalpingografie, diagnostická hysteroskopie a diagnostická laparoskopie.
Transvaginální ultrasonografie
Nejběžnější a nejlépe dostupnou metodou zobrazení a popisu isthmokély je transvaginální ultrasonografie (TVUZ). V roce 2011 Naji et al. popsali přesnou metodologii TVUZ hodnocení jizvy, která je v současné době široce uznávána a používána v odborných publikacích [19]. Isthomokéla je tu definována jako hypoechogenní oblast v myometriu dolního děložního segmentu ležící v oblasti mezi vezikouterinní junkcí a vnitřní děložní brankou. V případě SC prováděného akutně na otevřených porodních cestách se může vyskytovat v úrovni vnitřní branky nebo i pod ní.
Jizva by měla být zobrazena v sagitálním i transverzálním řezu, a to při vyprázdněném močovém měchýři. Fonda et al. doporučují provedení TVUZ v polovině cyklu s možností využití hojného intracervikálního hlenu jako přirozeného kontrastního média [9]. V jiné studii se ovšem udává jako nejvhodnější doba pro hodnocení isthmokély raná folikulární fáze cyklu, kdy jsou přesněji definovány kontury defektu při malé výšce endometria [4].
Měřením získáme čtyři rozměry defektu jizvy: sagitálně jeho šířku (W), hloubku (D), zbytkovou šíři myometria (RMT), tedy nejkratší vzdálenost mezi endometriem a serózou, a transverzálně jeho délku (L) (obr. 1).
Obr. 1. Popis TVUZ obrazu isthmokély v a) sagitálním b) transversálním řezu 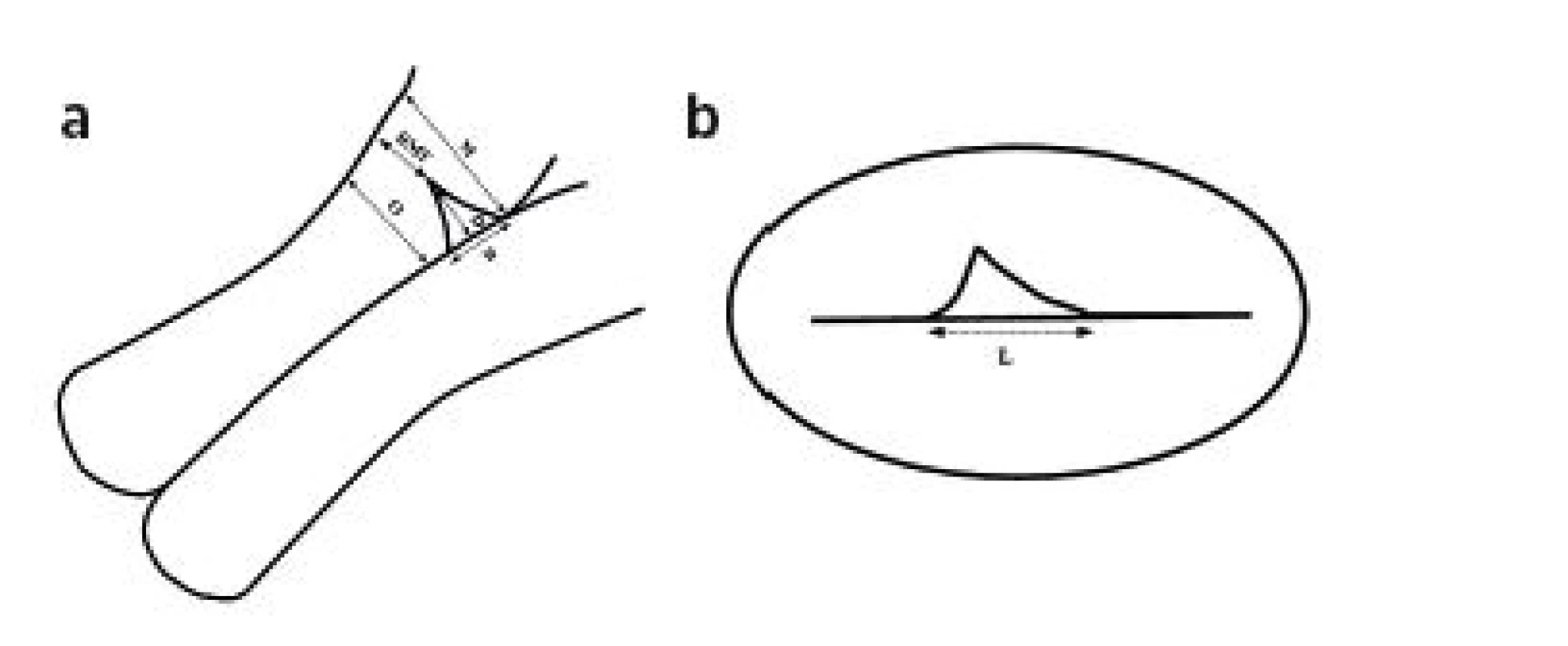
RMT – reziduální šíře myometria, D – hloubka, W – šíře, O – šíře myometria pod defektem, M – šíře myometria nad defektem, L – délka Dále je možno také měřit šíři myometria nad (M) a pod (O) defektem (obr. 1). Výpočtem lze zjistit index RMT/M, tedy poměr šíře zbytkového myometria a myometria nad defektem [12].
Při snahách o zpřesnění a rozšíření možností diagnostiky pomocí sonografie byla také využita 3D-TVUZ. Tato metoda je ale poměrně náročná na erudici ultrasonografisty a bude třeba dalších studií ke zhodnocení, zda přináší pro klinickou praxi výhody oproti 2D-TVUZ [11].
Sonohysterografie
Další možností aplikovaného využití ultrasonografie je sonohysterografie, tedy detailnější hodnocení tvaru děložní dutiny pomocí instilace UZ kontrastního média – sterilního fyziologického roztoku (SIS) nebo gelu (GIS). Někteří autoři uvádějí, že tato metoda poskytuje nejpřesnější informace o přítomnosti a rozměru isthmokély [27]. Bij de Vaatem et al. pomocí sonohysterografie popsali různé tvary defektu v sagitálním řezu: trojúhelníkový, půlkruhový, čtvercový, kruhový, kapkovitý a s přítomností inkluzních cyst (obr. 2). U různých tvarů defektu však nenalezli rozdíl v prevalenci symptomů [27].
Obr. 2. Schematický diagram možných tvarů isthmokély podle sonohysterografie 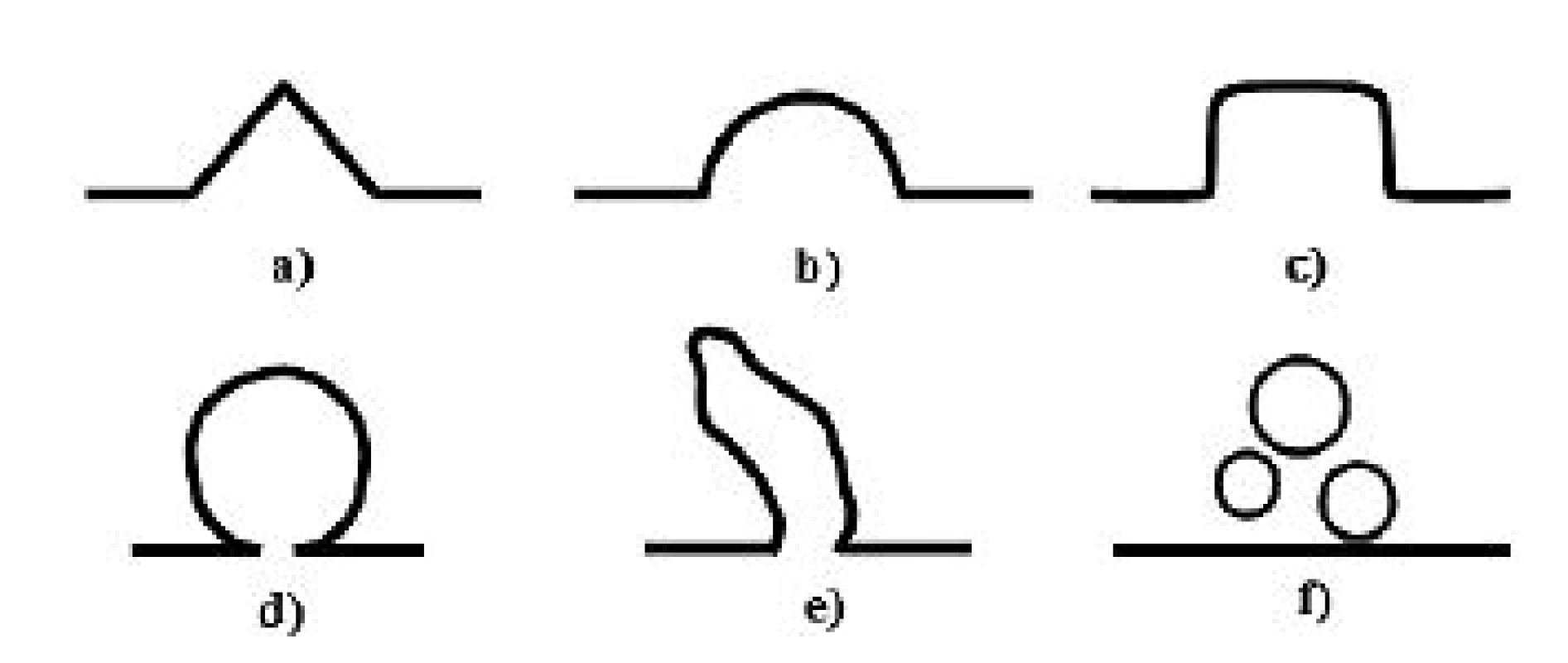
a) trojúhelníkový; b) půlkruhový; c) čtvercový; d) kruhový; e) kapkovitý; f) inkluzní cysty Stejní autoři udávají i větší senzitivitu metody ve srovnání s běžným TVUZ. Malé defekty, které TVUZ uniknou, jsou pomocí sonohysterografie diagnostikovány přesněji. Výskyt isthmokély u žen po SC je při využití kontrastního média v rozsahu 56–84 % [4, 18, 24]. Při měření isthmokély pomocí GIS či SIS jsou získány vyšší hodnoty sledovaných rozměrů než při TVUZ, což je zřejmě dáno distenzí pseudokavity defektu kontrastním médiem.
Skupina nizozemských autorů Bij de Vaate et al. považuje sonohysterografii za zlatý standard ve vyšetřovacím postupu, nicméně rutinní použití může být limitováno horší tolerancí pacientek a je nutno brát v potaz také riziko infekce. Situace, kde může sonohysterografie zaujmout jednoznačné místo, je právě přesný popis tvaru a struktury defektu v souvislosti s plánováním metody a rozsahu chirurgické intervence.
Magnetická rezonance
Ze zobrazovacích metod je v literatuře dále popisováno využití magnetické rezonance (MRI). Je zde opět možné využití kontrastního média (fyziologický roztok) nebo fúze snímků získaných pomocí TVUZ a MRI [5, 29]. Přes zjevnou přesnost této metody je vzhledem k nákladnosti vyšetření pravděpodobné, že MRI do rutinní diagnostické praxe v nejbližších letech nepronikne, snad s výjimkou preoperačního managementu komplikovaných případů.
Hysterosalpingografie
Dříve často používaná hysterosalpingografie je nyní považována za metodu obsolentní. Stejnou informaci o poměrech v dutině děložní je dnes možné získat i jinými výše zmíněnými metodami bez nutnosti radiační zátěže pacientky.
Diagnostická hysteroskopie
Další diagnostickou možností s nesporným praktickým významem je hysteroskopie. Ta umožňuje přímou vizualizaci defektu a mnoho autorů ji využívá k detailnímu popisu vnitřního povrchu a obsahu isthmokély [26, 29]. Isthmokéla je při hysteroskopickém pohledu popisována jako anomálie tvaru dutiny děložní ve smyslu pseudokavity nebo váčku přední stěny dolního děložního segmentu, často s přítomností depa tekuté nebo hnědé krve. Na povrchu isthmokély může být patrná jemná neovaskularizace s tendencí kontaktního krvácení [26].
Hysterokopie může napomoci v diferenciální diagnostice příčiny klinických potíží. Diagnózu syndromu jizvy po císařském řezu je nutno stanovit per exclusionem, tedy vyloučením dalších možných zdrojů krvácení (submukózní myom, polyp či dysfunkční endometrium).
Diagnostická laparoskopie
Strukturu vnějšího povrchu děložní stěny přilehlé k defektu je možné dobře posoudit pomocí diagnostické laparoskopie. Nabízí se využití souběžně prováděné hysteroskopie s laparoskopií, kdy se v oblasti jizvy objeví pozitivní diafanoskopie – tedy průnik světelného paprsku oslabeným myometriem. K docílení lepší vizualizace je možno přechodně ztlumit či vypnout zdroj světla laparoskopu [24]. Isthmokélu je dále možné ozřejmit pomocí metylenové modři, kdy se patologická oblast intenzivněji probarví [23].
Histopatologické vyšetření
Nedílnou součástí studia isthmokély je anatomicko-patologická analýza preparátů získaných při hysterektomii nebo při resekci okrajů jizvy. Takto byla isthmokéla v literatuře poprvé detailně popsána Morissem v roce 1995. V oblasti defektu je často přítomen mikroskopický nález kongesce endometria nad jizvou, lymfocytární infiltrát a dilatace kapilár [17].
TERAPIE
Terapeutické možnosti je možno rozdělit do dvou základních skupin: metody konzervativní, kam řadíme hormonální terapii, a dále metody operační, zastoupené operační hysteroskopií, vaginální chirurgií, laparoskopií, robotickou chirurgií, laparotomií a v některých případech i hysterektomií [7, 8, 13, 15, 23].
Při rozvaze o terapii isthmokély by mělo být respektováno základní pravidlo, že léčeny by měly být pouze symptomatické pacientky [10].
KONZERVATIVNÍ LÉČBA
Konzervativní řešení je vhodné pro ženy, jejichž dominantním symptomem je zejména špinění nebo dysmenorea a které přinejmenším v krátké době neplánují graviditu [24, 28]. Hormonální terapie není metodou kauzální a jejím efektem se zabývá omezené množství prací. Tyto studie provedené na relativně malém počtu participantek reportují redukci krvácení či špinění při užívání kombinovaných kontraceptiv v kontinuálním či intermitentním režimu. Stejně tak je uváděna redukce dysmenorey. Podle Tahary et al. dochází po tříměsíčním používání orálních kontraceptiv k redukci rozměrů isthmokély a dopplerometricky je prokázána redukce vaskularizace jizvy. Pozitivní efekt přetrvává i po vysazení terapie. Do zmíněné studie bylo ovšem zahrnuto pouze jedenáct žen [25].
Ojedinělé studie hodnotící efekt LNG-IUD dosud benefit při krátkém follow up neprokázaly [24].
CHIRURGICKÁ LÉČBA
Operační hysteroskopie
Možností využití operační hysteroskopie se zabývá několik prací [7, 13, 14, 18, 29]. Tento přístup umožňuje resekci distálního fibrotického okraje jizvy s cílem usnadnění odtoku a zabránění kolekce krve v pseudokavitě. Některé práce uvádějí i možnost resekce proximálního okraje jizvy [13, 29]. S rozsahem výkonu ovšem stoupá riziko poranění dalších struktur a také riziko oslabení svaloviny, které se může negativně projevit v další graviditě. Další možností je ošetření okrajů a baze pseudokavity pomocí bipolární koagulace. Dochází tím k indukci retrakce tkáně v oblasti defektu [13]. Bipolární koagulace povrchových křehkých cév má sama o sobě terapeutický efekt na postmenstruační špinění [29]. V případě defektu v dolní třetině cervikálního kanálu je Gubbinim et al. popisována metoda „lokalizované konizace“ v oblasti isthmokély [13].
Operační hysteroskopii je vhodné provádět za kontinuální ultrazvukové kontroly pro vyloučení poškození močového měchýře. Případně je možné výkon provést při náplni močového měchýře roztokem metylenové modři, která slouží k časné detekci hrozící perforace měchýře [13, 29]. Výkon je indikován při hloubce defektu více než 2 mm a RMT minimálně 3 mm, neboť při větším rozsahu léze je vyšší riziko komplikací [7].
Všechny sledované studie prokázaly redukci dysfunkčního krvácení, včetně zlepšení dysmenorey v důsledku zlepšeného odtoku krve cervikálním kanálem.
Rekonstrukce jizvy vaginální cestou
O této metodě je v literatuře pouze malé množství dostupných informací. Jejím principem je dosažení jizvy dělohy z vaginálního přístupu přes přední klenbu poševní. Nejprve je po akvadisekci tkání provedena kolpotomie, následně je odpreparován močový měchýř a identifikována oblast jizvy. Poté je provedena excize a resutura defektu. Tato metoda je popisována jako náročná na erudici operatéra pro velké riziko poranění okolních orgánů ve špatně přehledném terénu. Je-li uterotomie umístěna příliš vysoko, je vaginálním přístupem jen obtížně dosažitelná.
I zde dochází k redukci sledovaných symptomů a při TVUZ hodnocení dochází k nárůstu RMT [24]
Laparoskopická rekonstrukce
První publikace na téma laparoskopické reparace jizvy byla zveřejněna již v roce 2003 [24].
Principem metody je identifikace oblasti defektu po šetrném stažení vezikouterinní pliky, resekce a následná resutura jizvy. To bývá ztíženo tím, že oblast isthmokély může v laparoskopickém obraze vypadat zcela fyziologicky. Pro identifikaci defektu jsou proto využívány kombinace laparoskopie a hysteroskopie (diafanoskopie), případně mechanické vyklenutí isthmokély dilatátorem [15, 24]. Následná resutura se provádí obvykle po předchozí resekci jizevnaté tkáně do zdravých okrajů. Je rovněž popsána metoda resekce pomocí nůžek nebo CO2 laseru. V některých pracích se popisuje resekce celé šíře děložní stěny [15, 24], zatímco jiní autoři ponechávají sliznici intaktní a excidují pouze děložní svalovinu [8]. K sutuře se používá vstřebatelný materiál a je popsána jak jednovrstevná, tak vícevrstevná sutura, buď jednotlivými stehy, nebo stehem pokračovacím. Po rekonstrukci myometria je sešito peritoneum vezikouterinní pliky.
Laparoskopická rekonstrukce jizvy je indikována v případech velkých defektů s RMT pod méně než 3 mm, nebo také při atypických nálezech (píštěl, hematom, vlastní nepublikované zkušenosti). Pro následnou graviditu je doporučeno vyčkat alespoň jeden rok.
Po výkonu dochází k signifikantní redukci klinických příznaků i zesílení šíře myometria měřeného pomocí TVUZ. V této souvislosti je nutno zmínit výsledky práce týmu československých autorů, kteří publikovali studii s provedením laparoskopické rekonstrukce jizvy po SC u jedenácti symptomatických pacientek [8]. Po výkonu došlo k signifikantnímu ústupu sledovaných obtíží, nicméně autoři neprokázali změny na TVUZ nálezech.
Laparotomická rekonstrukce
Tato metoda byla popsána Schepkerem et al. a její princip se neliší od postupu uplatňovaného při laparoskopických výkonech. Její nevýhodou je však nutnost opakovaného zatížení pacienky laparotomií [23].
Hysterektomie
Je metodou volby v případě definitivního ukončení reprodukčních plánů a jsou-li zároveň přítomny závažné obtíže. Většinou se provádí při sdružených indikacích [24].
ZÁVĚR
S narůstajícím počtem pacientek po provedeném SC narůstá i počet žen s vyjádřenou symptomatologií syndromu jizvy po císařském řezu. Ten je spojen s přítomností defektu jizvy zvaného isthmokéla, niche či váčkovitý defekt. Za nejdůležitější diagnostické metody jsou považovány TVUZ, MRI a sonohysterografie. Při výběru kandidátek pro léčbu je rozhodující symptomatologie. Převládající terapeutickou metodou je hysteroskopie, eventuálně v kombinaci s laparoskopií. Syndrom jizvy po císařském řezu je v současné době dalším významným faktorem, který nutno brát v potaz při rozhodování o způsobu ukončení těhotenství.
MUDr. Vanda Klimáková
Vítkovická nemocnice a.s.
Zálužanského 1192/15
703 84 Ostrava-Vítkovice
e-mail: vanda.klimankova@seznam.cz
Zdroje
1. Almeida, MA., Araujo Júnior, E., Camano, L., et al. Impact of cesarean section in a private health service in Brazil: indications and neonatal morbidity and mortality rates. Čes Gynek, 2018, 83, s. 4–10
2. Bamberg, C., Hinkson, L., Dudenhausen, JW., et al. Longitudinal transvaginal ultrasound evaluation of cesarean scar niche incidence and depth in the first two years after single - or double-layer uterotomy closure: a randomized controlled trial. Acta Obstet Gynecol Scand, 2017, 96, p. 1484–1489.
3. Bij de Vaate, AJM., van der Voet, LF., Naji, O., et al. Prevalence, potential risk factors for development and symptoms related to the presence of uterine niches following Cesarean section: systematic review. Ultrasound Obstet Gynecol, 2014, 43, p. 372–382.
4. Bij de Vaate, AJM., Brölmann, HAM., et al. Ultrasound evaluation of the Cesarean scar: relation between a niche and postmenstrual spotting. Ultrasound Obstet Gynecol, 2011, 37, p. 93–99.
5. Bolten, K., Fischer, T., Bender, YYN., et al. Pilot study of MRI/ultrasound fusion imaging in postpartum assessment of cesarean section scar. Ultrasound Obstet Gynecol, 2017, 50, p. 520–526.
6. Čech, E., Hájek, Z., Maršál, K., et al. Porodnictví. 2. přepracované a doplněné vyd., Praha: Grada, 2006, s. 358–359.
7. Di Spiezio Sardo, A., Zizolfi, B., et al. Hysteroscopic isthmoplasty: step by step technique. J Minim Invasive Gynecol, 2017, 25, p. 1719–1723.
8. Dosedla, E., Calda, P. Outcomes of laparoscopic treatment in women with cesarean scar syndrome. MedSci Monit, 2017, 23, p. 4061–4066.
9. Fonda, J. Ultrasound diagnosis of caesarean scar defects. AJUM, 2011, 14(3), p. 22–30.
10. Futyma, K., Gałczyński, K., Romanek, K., et al. When and how should we treat cesarean scar defect – isthmocoele? Ginekol Pol, 2016, 87(9), p. 664–668.
11. Glavind, J., Madsen, LD., Uldbjerg, N., Dueholm, M. Cesarean section scar measurements in non-pregnant women using three-dimensional ultrasound: a repeatability study. Eur J Obstet Gynecol Reprod Biol, 2016, 201, p. 65–69.
12. Glavind, J., Madsen, LD., Uldbjerg, N., Dueholm, M. Ultrasound evaluation of Cesarean scar after single - and double-layer uterotomy closure: a cohort study. Ultrasound Obstet Gynecol, 2013, 42, p. 207–212.
13. Gubbini, G., Centini, G., Nascetti, D., et al. Surgical hysteroscopic treatment of cesarean-induced isthmocele in restoring fertility: prospective study. J Minim Invasive Gynecol, 2011, 18, p. 234–237.
14. Kovář, P., et al. Atlas panoramatické hysteroskopie. 1. vydání, Praha: Maxdorf Jessenius, 2017, s. 91–96.
15. Liu, S., Lv, W., Li, W. Laparoscopic repair with hysteroscopy of cesarean scar diverticulum. J Obstet Gynaecol Res, 2016, 42, p. 1719–1723.
16. Monteagudo, A., Carreno, C., Timor-Tritsch, IE. Saline infusion sonohysterography in nonpregnant women with previous cesarean delivery: the „niche“ in the scar. J Ultrasound Med, 2001, 20, p. 1105–1115.
17. Morris, H. Surgical pathology of the lower uterine segment caesarean sectionscar: Is the scar a source of clinical symptoms? Int J Gynecol Pathol, 1995, 14, p. 16–20.
18. Muzii, L., Domenici, L., Lecce, F., et al. Clinical outcomes after resectoscopic treatment of cesarean-induced isthmocele: a prospective case-control study. Eur Rev Med Pharmacol Sci, 2017, 21, p. 3341–3346.
19. Naji, O., Abdallah, Y., Bij De Vaate, AJ., et al. Standardized approach for imaging and measuring cesarean section scars using ultrasonography. Ultrasound Obstet Gynecol, 2012, 39, p. 252–259.
20. Poidevin, L. The value of hysterography in the prediction of cesarean section wound defect. Am J Obstet Gynecol, 1961, 81, p. 67–71.
21. Pomorski, M., Fuchs, T., Rosner-Tenerowicz, A., Zimmer, M. Standardized ultrasonographic approach for the assessment of risk factors of incomplete healing of the cesarean section scar in the uterus. Eur J Obstet Gynecol Reprod Biol, 2016, 205, p. 141–145.
22. www.uzis.cz/system/files/rodnov2014_2015.pdf, Rodička a novorozenec 2014–2015, Mother and newborn 2014–2015. UZIS, 2017.
23. Schepker, N., Garcia-Rocha, GJ., von Versen-Höynck, F., et al. Clinical diagnosis and therapy of uterine scar defects after caesaean section in non-pregnant woman. Arch Gynecol Obstet, 2015, 291, p. 1417–1423.
24. Setubal, A., Alves, J., Osório, F., et al. Treatment for uterine isthmocele, a pouchlike defect at the site of a cesarean section scar. J Minim Invasive Gynecol, 2018, 25, p. 38–46.
25. Tahara, M., Shimizu, T., Shimoura, H. Preliminary report of treatment with oral contraceptive pills for intermenstrual vaginal bleeding secondary to a cesarean section scar. Fertil Steril, 2006, 86, p. 477–479.
26. Talamonte, VH., Lippi, UG., Lopes, RGC., Stabile, SAB. Hysteroscopic findings in patients with post-menstrual spotting with prior cesarean section. Einstein (Sao Paulo), 2012, 10, p. 53–56.
27. van der Voet, LF., Bij de Vaate, AM., Veersema, S., et al. Long-term complications of caesarean section. The niche in the scar: a prospective cohort study on niche prevalence and its relation to abnormal uterine bleeding. BJOG, 2014, 121, p. 236–244.
28. van der Voet, LF., Vervoort, AJ., Veersema, S., et al. Minimally invasive therapy for gynaecological symptoms related to a niche in the caesarean scar: a systematic review. BJOG, 2014, 121, p. 145–156.
29. Vervoort, AJMW., van der Voet, LF., Witmer, M., et al. The HysNiche trial: hysteroscopic resection of uterine caesarean scar defect (niche) in patients with abnormal bleeding, a randomised controlled trial. BMC Women‘s Health, 2015, 15, p. 103.
30. Vervoort, AJMW., Uittenbogaard, LB., Hehenkamp, WJK., et al. Why do niches develop in Caesarean uterine scars? Hypotheses on the aetiology of niche development. Hum Reprod, 2015, 30, p. 2695–2702.
31. Wang, CB., Chiu, WW., Lee, CY., et al. Cesarean scar defect: correlation between Cesarean section number, defect size, clinical symptoms and uterine position. Ultrasound Obstet Gynecol, 2009, 34(1), p. 85–89.
32. Yao, M., Wang, W., Zhou, J., et al. Cesarean section scar diverticulum evaluation by saline contrast-enhanced magnetic resonance imaging: The relationship between variable parameters and longer menstrual bleeding. J Obstet Gynaecol Res, 2017, 43, p. 696–704.
33. Zahálková, L., Kacerovský, M. Ektopická gravidita v jizvě po císařském řezu. Čes Gynek, 2016, 81(6), s. 414–419.Štítky
Dětská gynekologie Gynekologie a porodnictví Reprodukční medicína
Článek Jak přesní jsme v hodnocení mobility uretry? Porovnání subjektivního a objektivního hodnoceníČlánek Akutní enterovirová meningoencefalitida jako neobvyklá příčina diplopie v těhotenství a šestinedělí
Článek vyšel v časopiseČeská gynekologie
Nejčtenější tento týden
2018 Číslo 4- Alergie na antibiotika u žen s infekcemi močových cest − poznatky z průřezové studie z USA
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Isoprinosin je bezpečný a účinný v léčbě pacientů s akutní respirační virovou infekcí
-
Všechny články tohoto čísla
- Srovnání souborů uměle ukončených těhotenství farmakologickou a chirurgickou metodou
- Vaginální rekonstrukce prolapsu pánevních orgánů: efekt, komplikace, vliv na močové a pohlavní funkce a kvalitu života ve dvouletém follow-up Část III – komplikace gastrointestinální, muskuloskeletální, celkové, sexuální funkce a kvalita života
- Jak přesní jsme v hodnocení mobility uretry? Porovnání subjektivního a objektivního hodnocení
- Role hormonální terapie u pacientek s karcinomem děložního těla
- Raritní komplikace dlouhodobého vaginálního prolapsu
- Nerozpoznaná preeklampsie, která se rozvinula do eklamptického záchvatu s fatálním koncem
- Akutní enterovirová meningoencefalitida jako neobvyklá příčina diplopie v těhotenství a šestinedělí
- Zoonova vulvitida – vzácná forma chronického zánětu vulvy
- Implantace a diagnostika receptivity endometria
- Pozdní morbidita u syndromu jizvy po císařském řezu
- Možnosti a praktický význam stanovení ovariální rezervy
- Stížnosti a žaloby na lékaře v oboru gynekologie a porodnictví – výsledky dotazníkového průzkumu
- Zápis z jednání volební komise pro volby výboru Sekce pro endometriózu České gynekologické a porodnické společnosti ČLS JEP
- 6th International Video Workshop on Radical Surgery in Gynecologic Oncology
- Česká gynekologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Pozdní morbidita u syndromu jizvy po císařském řezu
- Implantace a diagnostika receptivity endometria
- Zoonova vulvitida – vzácná forma chronického zánětu vulvy
- Možnosti a praktický význam stanovení ovariální rezervy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



