-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Kombinace statin – ezetimib v léčbě hyperlipidémie
Statin-ezetimibe combination in hyperlipidemia treatment
Background.
Statin monotherapy for dyslipidemia only rarely achieves recommended target values of plasma lipids. Statin plus ezetimibe is a feasible treatment option. The aim of the present study was to test efficacy and safety of statin plus ezetimibe combination in the treatment of severe dyslipidemia in patients coming to an ordinary lipid and diabetology department.Methods and results.
A retrospective evaluation of 3 months treatment in 82 dyslipidemia patients (25 male, 57 female) with unsatisfactory statin monotherapy results (average equivalent of 30 mg atorvastatin) was performed. Ezetimibe 10 mg per day was added to preceding treatment. The group included 26 diabetics type 2. The addition of ezetimibe resulted in statistically significant decrease of plasma total cholesterol (TC) (‑21%), LDL-C (-28%), triacylglyceroles (TAG) (-26%) and HDL-C (-6%). The recommended values of LDL-C were achieved in 42% of patients. In the diabetic subgroup a significant decrease of TC (24%), LDL-C (33%) and TAG (18%) was observed. There was no significant decrease of HDL-C. The recommended value of LDL-C was achieved in 48% of diabetics. There were no unfavourable side effects.Conclusions.
The addition of ezetimib in a dose of 10 mg in hyperlipidaemia patients who had not achieved the recommended target values of LDL-C resulted in a subsequent significant decrease of both TC and LDL-C. It also enabled to increase the number of patients achieving the recommended target plasma lipid values. The treatment was safe and was not associated with adverse effects.Key words:
hyperlipidaemia, statin, ezetimib, combined hypolipidemic treatment.
Autoři: Tomáš Vařeka; Daniela Vítková; Miroslav Zeman; Marek Vecka; Aleš Žák
Působiště autorů: Univerzita Karlova v Praze, 1. lékařská fakulta, IV. interní klinika VFN
Vyšlo v časopise: Čas. Lék. čes. 2012; 151: 17-21
Kategorie: Původní práce
Souhrn
Východisko.
Monoterapie statiny vede u smíšených hyperlipidémií jen zřídka k dosažení doporučovaných hodnot plazmatických lipidů. Jednou z možností léčby je použití kombinace statinu s ezetimibem. Cílem studie bylo ověřit účinnost a bezpečnost kombinace statin + ezetimib v léčbě těžké dyslipidémie u nemocných z běžné lipidové a diabetologické ambulance.Metody a výsledky.
Retrospektivně jsme zhodnotili výsledky tříměsíční léčby 82 hyperlipidemiků (25 mužů, 57 žen), kterým byl pro neuspokojivé výsledky monoterapie statinem (ekvivalent 30 mg atorvastatinu) přidán ezetimib (10 mg/den). Mezi těmito pacienty bylo 26 diabetiků 2. typu. Přidání ezetimibu vedlo ke statisticky významnému poklesu celkového cholesterolu (o 21 %), LDL cholesterolu (o 28 %), triacylglycerolů (o 26 %) a k poklesu HDL-C (o 6 %), doporučované hodnoty LDL-C dosáhlo 42 % nemocných. V podskupině diabetiků jsme zaznamenali pokles TC o 24 %, LDL-C o 33 %, TAG o 18 %, významný pokles HDL-C jsme nepozorovali. Doporučenou hodnotu LDL-C pod 2,5 mmol/l dosáhlo 48 % diabetiků. Nebyly zaznamenány žádné vedlejší účinky.Závěry.
Přidání ezetimibu v denní dávce 10 mg hyperlipidemikům, kteří při monoterapii statinem nedosahovali doporučovaných cílových hodnot LDL-C, vedlo k dalšímu významnému poklesu TC i LDL-C, umožnilo zvýšit počet pacientů dosahujících doporučované cílové hodnoty lipidů, přičemž léčba byla bezpečná a nebyla spojena s vedlejšími nežádoucími účinky.Klíčová slova:
hyperlipidémie, statin, ezetimib, kombinační hypolipidemická léčba.Úvod
Hyperlipidémie patří k hlavním rizikovým faktorům kardiovaskulárních onemocnění (KVO). Primárním cílem léčby je ovlivnění koncentrace LDL-C. Řada studií prokázala, že snižování LDL-C statiny významně snižuje kardiovaskulární riziko. Téměř 40 % pacientů s manifestním KVO má hladinu LDL‑C nižší než 3,4 mmol/l, což je hodnota, u které je většinou doporučováno započetí léčby v primární prevenci (1). Metaanalýza studií, ve kterých byly srovnávány výsledky léčby s cílovou hodnotou 100 mg/ dl (2,6 mmol/l) na jedné straně a cílovou hodnotou 70–80 mg/dl (cca 1,8–2,0 mmol/l), ukázala, že intenzivní léčba vedla k dalšímu poklesu výskytu koronárních příhod (2). V současné době Česká společnost pro aterosklerózu doporučuje stejně jako NCEP ATP III (National Cholesterol Education Program Adult Treatment Panel III) jako cílovou hodnotu LDL-C 3,0 mmol/l, u diabetiků LDL-C < 2,5 mmol/l, v případě manifestního KVO LDL-C < 2,0 mmol/l. Optimální hodnoty plazmatických TAG jsou < 1,7 mmol a HDL‑C > 1,0 mmol/l u mužů a > 1,2 mmol/l u žen (3, 4). Někteří autoři doporučují snižovat LDL-C až pod 1,5 mmol/l, kdy již byla popsána i regrese aterosklerózy – např. u diabetiků s manifestním KVO (5). Základním hypolipidemikem v léčbě dyslipidémií jsou statiny. Jejich podávání vede (v závislosti na dávce a typu statinu) k poklesu LDL-C o cca 30–50 %, od lovastatinu, působícího asi 30% pokles LDL-C, až k rosuvastatinu (až 56% pokles) (2). Procento nemocných užívajících statiny za poslední dekádu vzrostlo ze 32,3 % na 88,8 % (6), u řady z nich se však doporučených cílových hodnot při monoterapií statinem nedaří dosáhnout (7). Navíc asi u 70 % nemocných přesto, že jsou léčeni statiny, dochází během 5 let léčby k výskytu koronárních příhod (8). Léčba lipidových abnormalit je též doporučována u diabetes mellitus 2. typu (DM2), bylo prokázáno, že také může vést k významnému poklesu výskytu hlavních kardiovaskulárních ukazatelů, jako je úmrtí na KVO, nefatální IM nebo revaskularizační operace (9).
Pokud po léčbě statinem k dosažení cílových hodnot LDL‑C nedojde, jsou k dispozici tři další možnosti: 1. zvýšit dávku, 2. zaměnit za jiný (účinnější) statin, 3. přidat do kombinace jiný lék. Obecně je přijímáno, že výhodou kombinační léčby je to, že není nutné použít vysoké (a tedy potenciálně škodlivé) dávky statinů. Jednou z možností je kombinace statinu s ezetimibem. Ezetimib je selektivní inhibitor absorpce cholesterolu – specificky blokuje až 54 % jeho absorpce střevem aniž by ovlivňoval vstřebávání TAG nebo vitaminů rozpustných v tucích a neváže žlučové kyseliny. Působí na Niemann-Pick C1‑Like 1 (NPC1L1) protein, což je předpokládaný přenašeč cholesterolu v kartáčovém lemu enterocytu (10). Léčba ezetimibem (v denní dávce 10 mg/den) snižuje hladinu LDL‑C přibližně o 16–22 %. V případě současného podávání statinu s ezetimibem je současně inhibována syntéza cholesterolu v játrech a jeho absorpce ve střevě, takže tato kombinace působí pokles LDL-C až o 55–60 %, srovnatelný s maximální dávkou statinu. Ovlivnění obou zdrojů cholesterolu nazýváme duální inhibicí.
Ezetimib lze kombinovat se všemi dostupnými statiny, v České republice je dostupný též kombinovaný preparát ezetimib 10 mg se simvastatinem 10, 20 a 40 mg, v závislosti na dávce simvastatinu dochází při této léčbě k poklesu LDL-C o 45–60 % (11).
Cílem této studie bylo ověřit účinnost a bezpečnost kombinace statin + ezetimib v léčbě těžké smíšené dyslipidémie u neselektované skupiny nemocných z běžné lipidové a diabetologické ambulance.
Soubor nemocných a použité metody
V této práci jsme retrospektivně zhodnotili výsledky léčby 82 pacientů (25 mužů, 57 žen) z diabetologické a lipidologické ambulance IV. interní kliniky VFN, kterým byl pro dosavadní neuspokojivé výsledky léčby monoterapií statinem přidán ezetimib v dávce 10 mg na den. Z tohoto souboru nemocných bylo 26 osob (32 %) sledováno pro DM 2. typu.
Přehled užitých statinových preparátů je uveden v tabulce 1.
Tab. 1. Základní charakteristika souboru (n = 82) – předchozí léčba 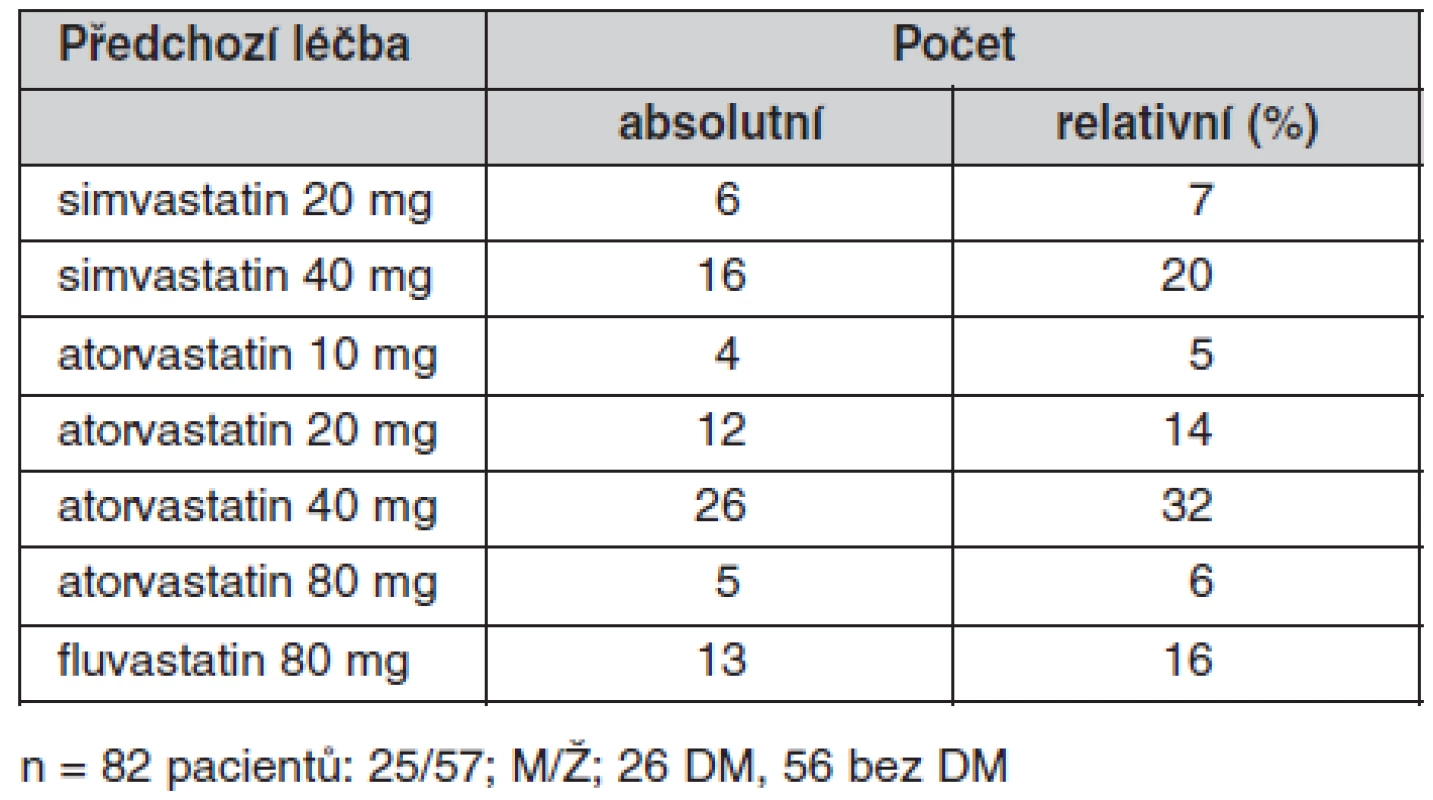
Základní klinické a demografické charakteristiky sledovaného souboru jsou uvedeny v tabulce 2. Před přidáním ezetimibu a potom za 3–4 měsíce byly hodnoceny následující parametry: hmotnost, BMI, koncentrace ALT a AST, CK a lipidů (cholesterol, triglyceridy, HDL cholesterol a LDL cholesterol) v séru, apolipoprotein B (apo-B), index aterogenity a glykémie. Odběry krve byly prováděny po celonočním lačnění do K2EDTA (1 mg/ml krve). Koncentrace TC, TAG, kyseliny močové a glukózy byly stanoveny pomocí enzymaticko-kolorimetrických metod (CHOD/PAP, GPO/PAP, Test Combination PL, Boehringer Mannheim, FRG, Oxochrom kyselina močová, GOD-PAP Oxochrom Glukosa Lachema a.s., Brno). Apo-B byly stanoveny EIA podle Laurella s pomocí specifických standard a protilátek (Behring Werke AG Marburg, Boehringer Mannheim, FRG).
Tab. 2. Základní klinické charakteristiky souboru (n = 82) 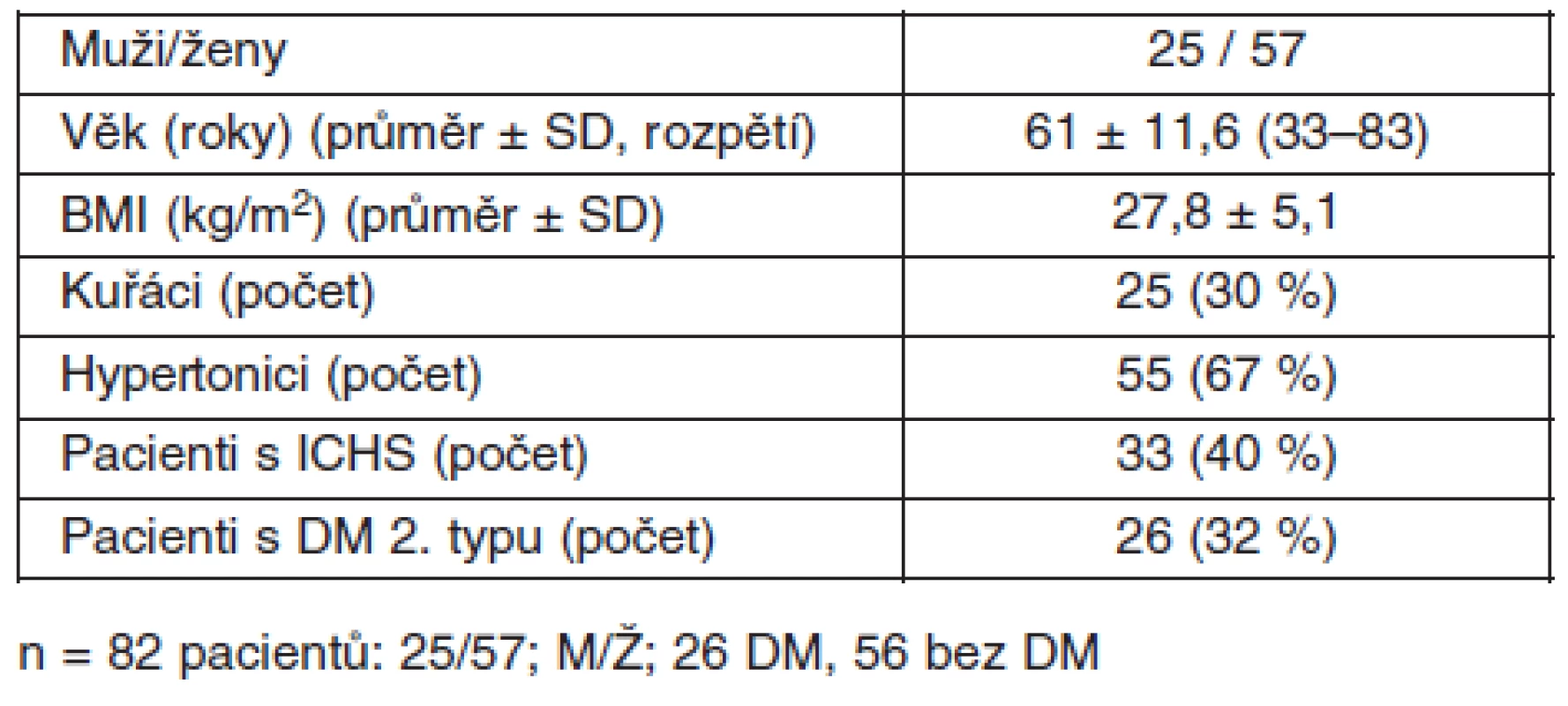
Výsledky
Přidání ezetimibu k předchozí léčbě statinem vedlo ke statisticky významnému poklesu TC z 6,16 na 4,85 mmol/l (‑21 %), LDL-C dokonce o 28 % (3,77 vs. 2,71 mmol/l), apo-B 1,27 na 0,96 mmol/l (-25 %), TAG z 1,89 klesly na 1,58 mmol/l (-26 %), došlo též k poklesu HDL-C z 1,51 na 1,42 mmol/l (-6 %). Doporučované hodnoty LDL-C pod 2,5 mmol/l dosáhlo 42 % nemocných. V podskupině diabetiků jsme zaznamenali podobné poklesy: TC o 24 % (ze 6,14 na 4,65 mmol/l), LDL-C o 33 % (3,78 vs. 2,51 mmol/l), apo-B o 16 % (z 1,15 na 0,96 mmol/l) a TAG se snížily z 2,42 na 2,02 mmol/l (-16 %), pokles v HDL-C jsme v této skupině nepozorovali. Výsledná průměrná hodnota LDL-C byla 2,51 mmol/l, doporučovanou hodnotu pod 2,5 mmol/l mělo 48 % osob. Výsledky jsou shrnuty v tabulce 3 a 4; ostatní sledované biochemické ukazatele nebyly léčbou signifikantně ovlivněny (výsledky nejsou uvedeny).
Tab. 3. Ukazatele metabolismu lipidů u celého sledovaného souboru 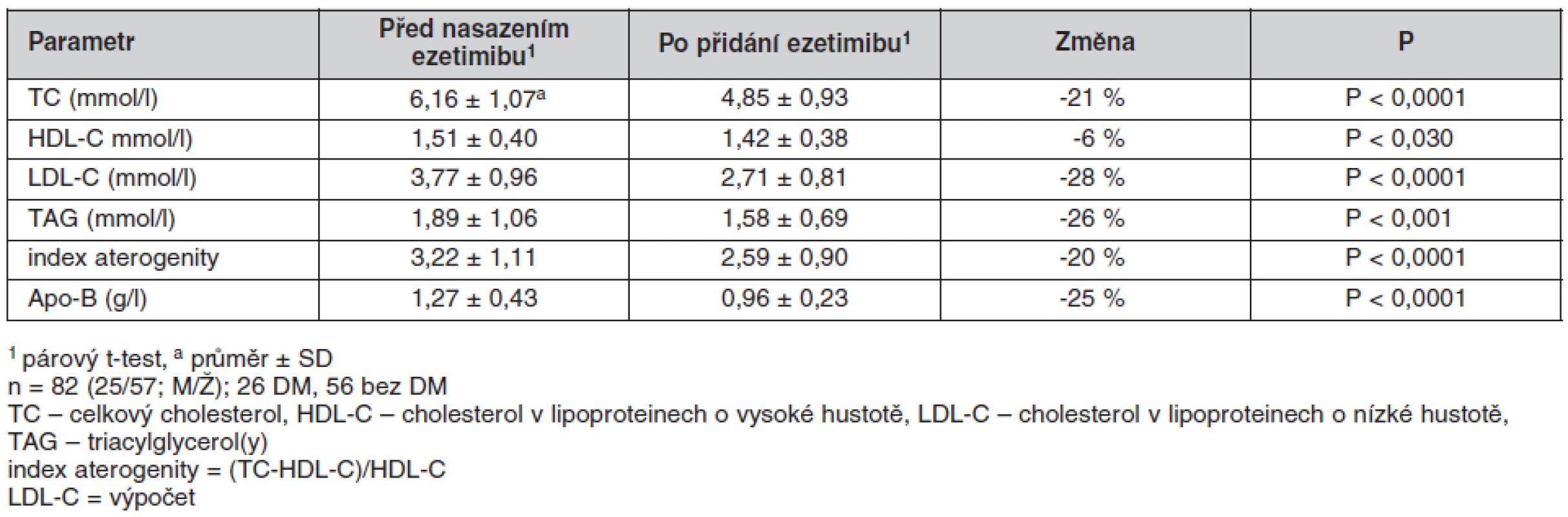
Tab. 4. Ukazatele metabolismu lipidů u pacientů s DM 2. typu 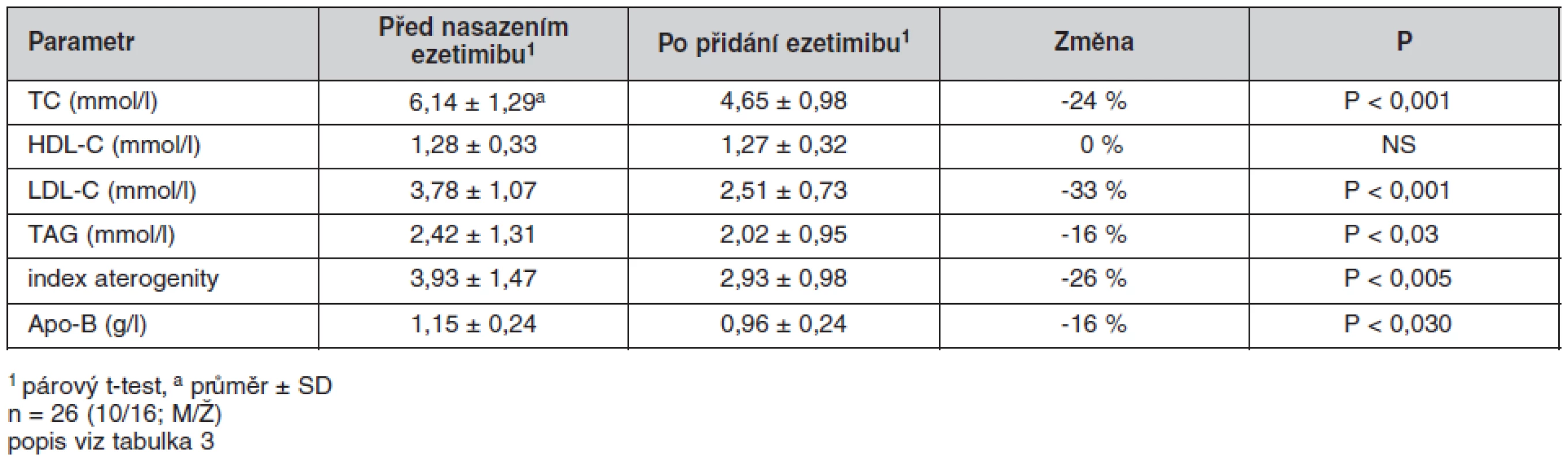
Diskuze
V této práci jsme v souboru nemocných s těžkou dyslipidémií, léčených dlouhodobě monoterapií statinem (v dávce ekvivalentní v průměru 30 mg atorvastatinu), zjistili, že po 9 až 12 týdnech přidání 10 mg ezetimibu došlo k významnému poklesu LDL-C (o 28 %, P < 0,0001), celkového cholesterolu (TC) (o 21 %, P < 0,0001), apo-B (o 25 %, P < 0,0001), TAG (o 26 %, P < 0,001), i indexu aterogenity (o 20 %, P < 0,0001). Oproti očekávání došlo také k poklesu HDL-C (o 6 %, P < 0,03). Když jsme analyzovali zvlášť soubor diabetiků, zjistili jsme obdobné poklesy hladin aterogenních lipidů LDL-C (o 33 %, P < 0,001), TC, TAG, apo-B i hodnoty indexu aterogenity. Na rozdíl od celé skupiny léčených osob jsme u diabetiků nezaznamenali významnou změnu v koncentraci HDL-C.
Kombinační léčba užívající statin a ezetimib byla v posledních letech užita v řadě studií. Ve většině prací byly srovnávány výsledky podávání vyšší dávky statinu s kombinací základní dávky statinu s ezetimibem. Nejčastěji se jednalo o kombinaci ezetimibu se simvastatinem.
Výsledky těchto studií jsou přehledně uvedeny v tabulce 5. V těchto studiích byly dosaženy poklesy LDL-C a TC srovnatelné s naší prací. V případě HDL-C v některých studiích došlo dokonce k poklesu, většinou byl pozorován vzestup (v průměru cca o 8 %). Velmi podobné výsledky jako v naší práci byly získány ve studii EASY, kde k ovlivnění HDL-C nedošlo. Ve studii EASY byli sledováni nemocní pocházející z ambulancí praktických lékařů, kteří ke stávající léčbě statinem přidali nemocným 10 mg ezetimibu denně (12). Je známo, že do klinických studií nejsou obvykle zařazováni nemocní trpící více chorobami, nemocní léčení řadou různých farmak a ti, v jejichž anamnéze je údaj o nežádoucím účinku nějakého léku, což může stát v pozadí lepšího výsledku.
Tab. 5. Výsledky studií s použitím kombinace statin/ezetimib 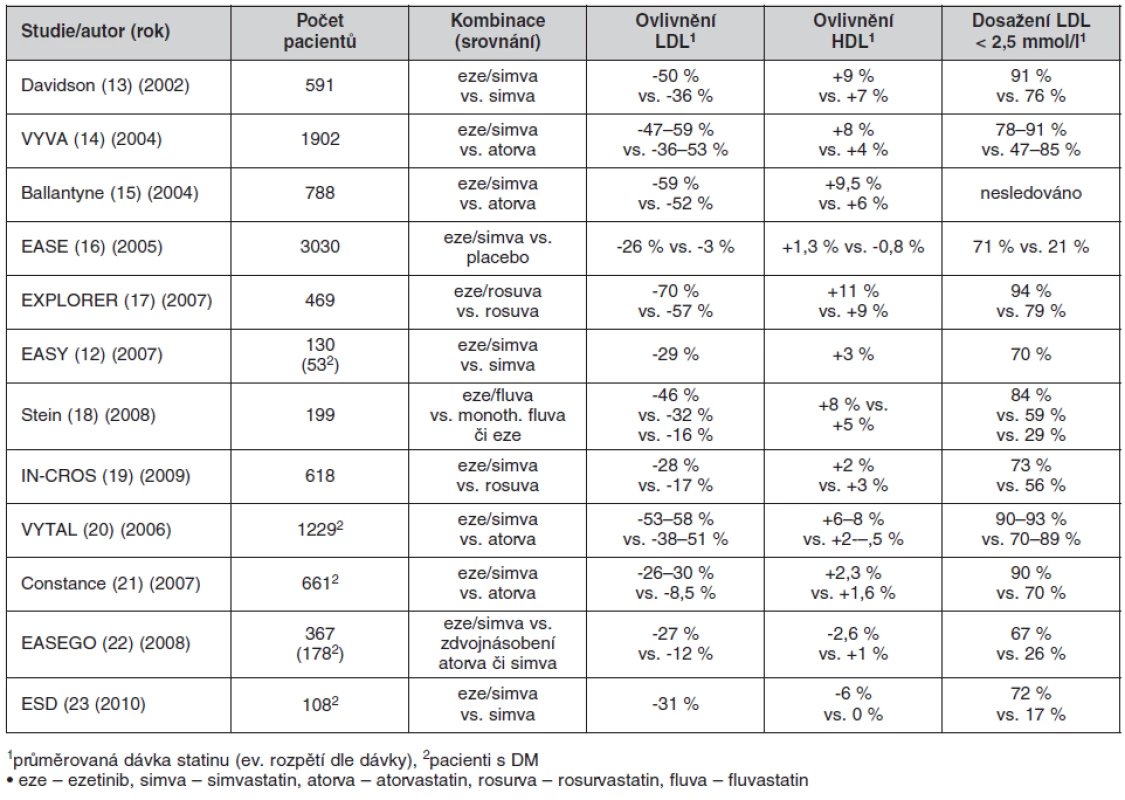
Podobně jako u léčby statiny či fibráty byly zkoumány účinky ezetimibu nejen na koncentrace LDL-cholesterolu, ale také i na další kvantitativní a kvalitativní parametry lipidového a lipoproteinového spektra. V jedné studii byl u 72 zdravých mužů zjišťován vliv ezetimibu na proaterogenní subfrakce malých denzních LDL (sdLDL) a bylo zjištěno, že ezetimib v monoterapii i v kombinaci se simvastatinem zvyšuje podíl sdLDL (24). Na druhé straně v randomizované studii u 100 nemocných s koronární srdeční chorobou nebo jejím ekvivalentem, byl po dobu 8 týdnů podáván buď atorvastatin 40 mg v kombinaci s ezetimibem 10 mg denně nebo atorvastatin 40 mg s placebem a vedle vyšší redukce LDL-C ve skupině s ezetimibem byl zde prokázán i pokles hladiny oxidovaných LDL na rozdíl od monoterapie atorvastatinem (25).
Ve studii SEAS (Simvastatin and Ezetimibe in Aortic Stenosis), která zkoumala účinky intenzivní hypolipidemické léčby simvastatinem v kombinaci s ezetimibem nebo placebem na aortální stenózu, byl zjištěn vzestup výskytu nádorových onemocnění ve skupině užívající ezetimib (26). V následné nezávislé meta-analýze, která užila dat ze dvou velkých, v současné době probíhajících, studií IMPROVE-IT (Improved Reduction of Outcomes: Vytorin Efficacy International Trial) a SHARP (Study of Heart And Renal Protection), nebyl vliv podávání ezetimibu na výskyt nádorů prokázán (27, 28), a proto americká agentura FDA (Food and Drug Administration) doporučila pokračovat ve studiu účinků ezetimibu v prováděných studiích. Jako možný příznivý vedlejší efekt léčby ezetimibem byl zjištěn pokles saturace žluči cholesterolem a zpomalení krystalizace cholesterolu ve žluči nemocných s cholelitiázou (29). Další studie ukazují na možné příznivé působení ezetimibu i na inzulínovou rezistenci a nealkoholickou steatózu jater (30). V experimentu u krys podávání ezetimibu vedlo v játrech k poklesu exprese jaderného faktoru SREBP1c a ke zvýšení exprese faktorů SREBP2 a SHP provázeným snížením inzulínové rezistence indukované vysokotukovou dietou (31). Nedávno byly publikovány výsledky experimentální práce, ve které bylo zjištěno, že chronické podávání ezetimibu zvyšuje hladiny inkretinového hormonu GLP-1 a současně upravuje glykemickou kontrolu a masu beta buněk v Langerhansových ostrůvcích (32).
Zatím chybí větší studie, které by zhodnotily efekt kombinace statinu s ezetimibem na kardiovaskulární příhody. V subanalýze studie SANDS (Stop Atherosclerosis in Native Diabetics Study) (427 pacientů, kteří měli DM 2. typu) byl hodnocen efekt kombinační léčby ve srovnání se zdvojnásobením dávky statinu na progresi aterosklerózy spolu s hodnocením hladiny LDL-C a hodnot krevního tlaku. Cílových hodnot LDL-C < 2,5 mmol/l bylo u obou skupin dosaženo v 95 % případů, pokles LDL-C srovnatelný (31 % vs. 32 %), nebyl pozorován žádný aditivní efekt na ovlivnění tloušťky intima-media karotické tepny (CIMT), pokud je dosaženo stejné cílové hodnoty LDL-C (33, 34). Podobný výsledek měla studie ENHANCE (the Ezetimibe and Simvastatin in Hypercholesterolemia Enhances Atherosclerosis Regression), kde po 2 letech léčby nebyl signifikantní rozdíl ve změně CIMT u 720 pacientů léčených kombinací statin/ezetimib ve srovnání se statinovou monoterapií, i když pokles LDL-C byl u kombinační léčby významnější než u statinové monoterapie (58 % vs. 41 %) (35). Pouze ve studii SEAS byl zaznamenán pokles ischemických kardiovaskulárních příhod o 22 % ve srovnání s léčbou placebem (přidanému ke stávající léčbě statiny), i když vliv kombinační léčby s ezetimibem na zpomalení progrese aortální stenózy nebyl prokázán (26).
Kombinace statinu s ezetimibem je velmi dobře tolerovaná, je ale třeba, zejména u starších osob, sledovat potenciální hepatotoxicitu (monitorovat jaterní testy), a u osob s anamnézou statinem indukované myopatie někteří autoři doporučují kombinovat ezetimib s fluvastatinem, vzhledem k nejmenšímu riziku vedlejších účinků (18).
V jedné metaanalýze, která hodnotila účinnost a bezpečnost podávání vysokých dávek statinů na jedné straně a různých kombinacích se statinem, byla jako nejlepší vyhodnocena kombinace statin + ezetimib, a to zejména u vysoce rizikových pacientů (36).
Můžeme uzavřít, že přidání ezetimibu v denní dávce 10 mg nemocným, kteří při monoterapii statinem (v průměrné dávce odpovídající 30 mg atorvastatinu) nedosahovali doporučovaných cílových hodnot LDL-C, vedlo k dalšímu významnému poklesu TC i LDL-C, v případě HDL-C jsme pozorovali mírný pokles. Tyto nálezy zhruba odpovídaly výsledkům zjištěným ve velkých zahraničních klinických studiích. Též nebyly pozorovány rozdíly v účincích mezi muži a ženami. Léčba byla dobře snášena a nevedla u našich nemocných k žádným nepříznivým vedlejším účinkům.
Zkratky
ALT – alanin aminotransferáza (alanin transamináza)
apo-B – apolipoprotein B
AST – aspartát aminotransferáza (aspartát transamináza)
BMI – body mass index
CIMT – tloušťka intima-media karotické tepny (carotid intima-media thickness)
CK – kreatinkináza
DM2 – diabetes mellitus 2. typu
GLP-1 – glucagon-like peptid-1
HDL-C – cholesterol v lipoproteinech o vysoké hustotě (high-density lipoproteins)
KVO – kardiovaskulární onemocnění
LDL-C – cholesterol v lipoproteinech o nízké hustotě (low-density lipoproteins)
NPC1L1 – Niemann-Pick C1-Like 1 protein
PL – fosfolipidy
sdLDL – malé denzní LDL (small dense LDL)
SHP – short heterodimer partner
SREBP – sterol regulatory element-binding protein
TAG – triacylglycerol(y)
TC – celkový cholesterol
Práce byla podpořena výzkumným záměrem MŠMT ČR č. MSM0021620820.
Adresa pro korespondenci:
MUDr. Tomáš Vařeka
IV. interní klinika 1. LF UK a VFN
U Nemocnice 2, 128 08 Praha 2
fax: +420 224 923 524, e-mail: vareka.t@seznam.cz
Zdroje
1. Rubins HB, Robins SJ, Collins D, et al. Department of Veterans Affairs HDL Intervention Trial Study Group. Distribution of lipids in 8,500 men with coronary artery disease. Am J Cardiol 1995; 75 : 1196–1201.
2. Cannon CP, Steinberg BA, Murphy SA, et al. Meta-analysis of cardiovascular outcomes trials comparing intensive versus moderate statin therapy. J Am Coll Cardiol 2006; 48 : 438–445.
3. Grundy SM, Cleeman JI, Bairey-Merz CN, et al. Implications of Recent Clinical Trials for the National Cholesterol Education Program Adult Treatment Panel III Guidelines, Circulation 2004; 110 : 227–239.
4. Vaverková H, Soška V, Rosolová H, et al. Doporučení pro diagnostiku a léčbu dyslipidemií v dospělosti, vypracované výborem České společnosti pro aterosklerózu. Cor Vasa 2007; 49: K73–K86.
5. Nissen SE, Nicholls SJ, Sipahi I, et al. Effect of Very High-Intensity Statin Therapy on Regression of Coronary Atherosclerosis: The ASTEROID Trial. JAMA 2006; 295 : 1556–1565.
6. Reiner Z, Amouyel P, De Backer G, et al. Treatment of dyslipidaemia in coronary patients in Europe: improving but still inadequate. Eur Heart J 2008; 29(Suppl.): 761–762.
7. Zeman M, Žák A, Vecka M, Romaniv S. Dlouhodobá kombinační hypolipidemická léčba statiny a fibráty v léčbě smíšené hyperlipidémie. Čas Lék čes 2003; 142 : 500–504.
8. Baigent C, Keech A, Kearney PM, et al. Cholesterol Treatment Trialist (CTT) Collaborators. Efficacy and safety of cholesterol lowering treatment: Prospective meta-analysis of data from 90,056 participants in 14 randomized trials of statins. Lancet 2005; 366 : 1267–1278.
9. Costa J, Borges M, David C, Vaz Carneiro A. Efficacy o f lipid lowering drug treatment for diabetic and non-diabetic patients: meta-analysis of randomized controlled trials. BMJ 2006; 332 : 1115–1124.
10. Garcia-Calvo M, Lisnock J, Bull HG, et al. The target of ezetimibe is Niemann-Pick C1-Like 1 (NPC1L1). Proc Natl Acad Sci USA 2005; 102 : 8132–8137.
11. Bays H. Ezetimibe. Expert Opin Investig Drugs 2002; 11 : 1587–1604.
12. Simons LA, Symons J. Ezetimibe added to statin therapy (EASY study) - an evaluation by Australian general practitioners. Aust Fam Physician 2007; 36 : 90–92, 96.
13. Davidson MH, McGarry T, Bettis R, et al. Ezetimibe coadministered with simvastatin in patients with primary hypercholesterolemia. J Am Coll Cardiol 2002; 40 : 2125–2134.
14. Ballantyne CM, Abate N, Yuan Z, et al. Dose-comparison study of the combination of ezetimibe and simvastatin (Vytorin) versus atorvastatin in patients with hypercholesterolemia: the Vytorin Versus Atorvastatin (VYVA) study. Am Heart J 2005; 149 : 464–473.
15. Ballantyne CM, Blazing MA, King TR, et al. Efficacy and safety of ezetimibe co-administered with simvastatin compared with atorvastatin in adults with hypercholesterolemia. Am J Cardiol 2004; 93 : 1487–1494.
16. Pearson TA, Denke EA, McBride PE, et al. Community-Based, Randomized Trial of Ezetimibe Added to Statin Therapy to Attain NCEP ATP III Goals for LDL Cholesterol in Hypercholesterolemic Patients:The Ezetimibe Add-On to Statin for Effectiveness (EASE) Trial. Mayo Clin Proc 2005; 80 : 587–595.
17. Ballantyne CM, Weiss R, Moccetti T, et al. EXPLORER Study Investigators. Efficacy and safety of rosuvastatin 40 mg alone or in combination with ezetimibe in patients at high risk of cardiovascular disease (results from the EXPLORER study). Am J Cardiol 2007; 99 : 673–680.
18. Stein EA, Ballantyne CM, Windler E, et al. Efficacy and tolerability of fluvastatin XL 80 mg alone, ezetimibe alone, and the combination of fluvastatin XL 80 mg with ezetimibe in patients with a history of muscle-related side effects with other statins. Am J Cardiol 2008; 101 : 490–496.
19. Farnier M, Averna M, Missault L, et al. Lipid-altering efficacy of ezetimibe/simvastatin 10/20 mg compared with rosuvastatin 10 mg in high-risk hypercholesterolaemic patients inadequately controlled with prior statin monotherapy – The IN-CROSS study. Int J Clin Pract 2009; 63 : 547–559.
20. Goldberg RB, Guyton JR, Mazzone T, et al. Ezetimibe/simvastatin vs atorvastatin in patients with type 2 diabetes mellitus and hypercholesterolemia: the VYTAL study. Mayo Clin Proc 2006; 81 : 1579–1588.
21. Constance C, Westphal S, Chung N, et al. Efficacy of ezetimibe/simvastatin 10/20 and 10/40 mg compared with atorvastatin 20 mg in patients with type 2 diabetes mellitus. Diabetes Obes Metab 2007; 9 : 575–584.
22. Roeters van Lennep HW, Liem AH, Dunselman PH, et al. The efficacy of statin monotherapy uptitration versus switching to ezetimibe/simvastatin: results of the EASEGO study. Curr Med Res Opin 2008; 24 : 685–694.
23. Ruggenenti P, Cattaneo D, Rota S, et al. Ezetimibe and Simvastatin in Dyslipidemia of Diabetes (ESD) Study Group. Effects of combined ezetimibe and simvastatin therapy as compared with simvastatin alone in patients with type 2 diabetes: a prospective randomized double-blind clinical trial. Diabetes Care 2010; 33 : 1954–1956.
24. Berneis K, Rizzo M, Berthold HK, et al. Ezetimibe alone or in combination with simvastatin increases small dense low-density lipoproteins in healthy men: a randomized trial. Eur Heart J 2010; 31 : 1633–1639.
25. Azar RR, Badaoui G, Sarkis A, et al. Effect of ezetimibe/atorvastatin combination on oxidized low density lipoprotein cholesterol in patients with coronary artery disease or coronary artery disease equivalent. Am J Cardiol 2010; 106 : 193–197.
26. RossebŅ AB, Pedersen TR, Boman K, et al. Intensive lipid lowering with simvastatin and ezetimibe in aortic stenosis. N Engl J Med 2008; 359 : 1343–1356.
27. Peto R, Emberson J, Landray M, et al. Analyses of Cancer Data from Three Ezetimibe Trials. N Engl J Med 2008; 359 : 1357–1366.
28. Ahmed MH. Ezetimbe as potential treatment for cholesterol gallstones: the need for clinical trials. World J Gastroenterol 2010; 16 : 1555–1557.
29. Wang HH, Portincasa P, Mendez-Sanchez N, et al. Effect of ezetimibe on the prevention and dissolution of cholesterol gallstones. Gastroenterology 2008; 134 : 2101–2110.
30. Ahmed MH, Byrne CD. Ezetimibe as a potential treatment for non-alcoholic fatty liver disease: is the intestine a modulator of hepatic insulin sensitivity and hepatic fat accumulation? Drug Discov Today 2010; 15 : 590–595.
31. Muraoka T, Aoki K, Iwasaki T, et al. Ezetimibe decreases SREBP-1c expression in liver and reverses hepatic insulin resistance in mice fed a high-fat diet. Metabolism 2011; 60 : 617–628.
32. Yang SJ, Choi JM, Kim L, et al. Chronic administration of ezetimibe increases active glucagon-like peptide-1 and improves glycemic control and pancreatic beta cell mass in a rat model of type 2 diabetes. Biochem Biophys Res Commun 2011; 407 : 153–157.
33. Howard BV, Roman MJ, Devereux RB, et al. Effect of lower targets for blood pressure and LDL cholesterol on atherosclerosis in diabetes: the SANDS randomized trial. JAMA 2008; 299 : 1678–1689.
34. Fleg JL, Mete M, Howard BV, et al. Effect of statins alone versus statins plus ezetimibe on carotid atherosclerosis in type 2 diabetes: the SANDS (Stop Atherosclerosis in Native Diabetics Study) trial. J Am Coll Cardiol 2008; 52 : 2198–2205.
35. Kastelein JJ, Akdim F, Stroes ES, et al. Simvastatin with or without ezetimibe in familial hypercholesterolemia, N Engl J Med 2008; 358 : 1431–1443.
36. Sharma M, Ansari MT, Abou-Setta AM, et al. Systematic Review: Comparative effectivenessand harms of combination therapy and monotherapy for dyslipidemia. Ann Intern Med 2009; 151 : 622–630.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Ukažte mi, jak kašlete, a já vám řeknu, co vám je
-
Všechny články tohoto čísla
- Katétrové infekce krevního řečiště – prevalence a intervence
- Kombinace statin – ezetimib v léčbě hyperlipidémie
- Predikce v medicíně – genom contra envirom
- DNA testing policy conference – Legislativa testování DNA
- Lékařství v antickém starověku
- Kůže jako lymfoidní orgán
- Před 150 lety vyšlo první číslo Časopisu lékařů českýchJubilea časopisu na jeho vlastních stránkách
- Ateroskleróza 2011
-
XX. konference endoskopické sekce České gynekologicko-porodnické společnosti
Poděbrady, 6. až 7. října 2011 -
12. sympozium Diabetes mellitus – oční komplikace
Olomouc, 8. října 2011 -
XXVIII. konference České společnosti pro hypertenzi, XX. konference pracovní skupiny Preventivní kardiologie České kardiologické společnosti a XVI. konference pracovní skupiny Srdeční selhání ČKS
Mikulov, 13. až 15. října 2011 -
V. konference kardiologických sester s mezinárodní účastí
Ostrava, 20. až 21. října 2011 -
5. konference Akné a obličejové dermatózy
Praha, 4. listopadu 2011 -
V. edukačně-odborná konference pracovní skupiny ošetřovatelství v kardiologii České kardiologické společnosti o.s.
Praha, 5. listopadu 2011 -
13. pracovní den Společnosti lékařské genetiky
Olomouc, 10. listopadu 2011 -
Hradecké pediatrické dny
Hradec Králové, 11. až 12. listopadu 2011 -
2. Zirmův olomoucký diskuzní den
Olomouc, 12. listopadu 2011 -
XVII. moravskoslezské pediatrické dny s mezinárodní účastí
Ostrava, 11. a 12. listopadu - Spolek českých lékařů v Praze
- Kniha
- Cena časopisu lékařů českých za rok 2010
- Plánované akce odborných složek ČLS JEP
- Metody hodnocení zdravotních rizik stopových množství léčiv v pitné vodě
- Ulf Svante von Euler
- Endoskopický simulátor pro výuku digestivní endoskopie
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Lékařství v antickém starověku
- Katétrové infekce krevního řečiště – prevalence a intervence
- Kombinace statin – ezetimib v léčbě hyperlipidémie
-
Hradecké pediatrické dny
Hradec Králové, 11. až 12. listopadu 2011
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



