-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Venózny ulkus – súčasné pohľady na etiopatogenézu, diagnostiku a terapiu
Venous Ulcer – Present View on Aetiology, Diagnostics and Therapy
The common aetiology of chronic wounds is chronic venous insufficiency. The prevalence of chronic venous insufficiency ranges from 5 to 8% and the prevalence of venous ulcers is about 1%. Venous ulcer is caused by induction of chronic inflammation. Chronic inflammation leads to deregulations of wound healing mechanisms. Senescent phenotype of wound healing cells is recorded as outcome of chronic inflammation. Diagnosis is based on classical clinical presentation of venous ulcer and on supporting examinations. Supporting examinations include duplex ultrasound, photoplethysmography, ankle brachial index investigation and examination of hemocoagulation status. Malignant transformation is a possible complication of venous ulcers. The relative risk of malignancy in chronic venous ulcers is 5.8%. The first step in venous ulcer treatment is debridement. There is no consensus in speculations about wound colonization treatment. However the signs of infection are indication for general antibiotics treatment. Local antiseptic therapy is increasingly used. On the other side local antibiotics therapy is not recommended. Compression is used as the mainstay of therapy. It is important to rule out arterial disease before initiating compression therapy. Dressings are used as an adjuvant therapy to compression. Venous ulcers treatment is an interdisciplinary problem. Large diagnostic and therapeutic methods are needed for its management.
Key words:
chronic venous insufficiency, venous ulcer, chronic wound.
Autoři: T. Toporcer; L. Lakyová; J. Radoňak
Působiště autorů: II. chirurgická klinika LF UPJŠ, Košice
Vyšlo v časopise: Čas. Lék. čes. 2008; 147: 199-205
Kategorie: Přehledový článek
Souhrn
Najčastejšou etiológiou vzniku chronických rán dolných končatín je chronická venózna insuficiencia. Celosvetová incidencia chronickej venóznej insuficiencie je 5 až 8 %, pričom až 1 % populácie sa dostáva do štádia venózneho ulkusu. Vznik a perzistencia venózneho ulkusu je vysvetľovaná navodením patologickej zápalovej odpovede s následnou dysreguláciou riadiacich mechanizmov zápalu, čo vedie k patologickej zmene fenotypu buniek, podieľajúcich sa na hojení rán. Medzi základné vyšetrovacie metódy patrí doplerovská ultrasonografia venózneho systému dolných končatín, fotopletyzmografia, vyšetrenie indexu členkovo-brachiálneho tlaku, ale i hemokoagulačné vyšetrenie. Často sa zabúda na nebezpečenstvo malignizácie chronických rán s incidenciou až 5,8 % všetkých venóznych ulkusov. Široké sú súčasné možnosti konzervatívnej aj chirurgickej liečby. Prvým krokom v liečbe každej chronickej rany je nekrektómia v jej rôznych podobách. Názory na význam i terapiu kolonizácie chronických rán sú stále nejednotné. Známky infekcie sú však podľa väčšiny autorov indikáciou k zahájeniu celkovej antibiotickéj terapie. Čoraz častejšie využívané je lokálne aplikovanie antiseptík. Kompresívna terapia je dnes už štandardom liečby chronickej venóznej insuficiencie, je však kontraindikovaná pri súčasnom postihnutí arteriálneho systému dolných končatín. Mechanická alebo chemická stimulácia spodiny rany je doplnkovou, ale veľmi účinnou metódou. Liečba venóznych ulkusov je interdisciplinárnou problematikou, vyžadujúcou rozsiahle diagnostické i terapeutické metódy, patriaca do rúk lekára špecializovaného na problematiku chronických rán.
Kľúčové slová:
chronická venózna insuficiencia, venózny ulkus, chronická rana.Chronická rana je rana pretrvávajúca viac ako 6 týždňov (1). Chronické, zle sa hojace rany dolných končatín (DK) môžu byť dôsledkom chronickej venóznej insuficiencie (CVI), ischemickej choroby dolných končatín (IChDK), zle kontrolovaného diabetes mellitus (DM), reumatoidnej artritídy, traumy, chronickej osteomyelitídy, kosáčikovitej anémie, vaskulitídy, alebo kožného tumoru (2). Všetky tieto ochorenia môžu na vzniku chronickej rany participovať samostatne, alebo vo vzájomnej kombinácii. Prednostne sa na vzniku chronických rán, podľa literatúry viac ako 70 %, podieľa CVI (3).
Epidemiologické štúdie prezentujú, že CVI postihuje 5 až 8 % svetovej populácie, pričom približne 1 % pacientov sa dostáva do štádia venózneho ulkusu (VU) (4). CVI a VU je ochorenie, vyžadujúce dlhodobú zdravotnícku starostlivosť, čo sa odzrkadľuje aj v jeho závažnom ekonomicko-spoločenskom dopade. V európskych krajinách výdavky na liečbu CVI predstavujú 1 až 2 % celkových zdravotníckych nákladov (4).
Etiopatogenéza
Vznik a vývoj VU je priamo viazaný na prítomnosť a štádium CVI. CVI môže vznikať ako dôsledok insuficiencie chlopní hĺbokého venózneho systému DK, obštrukcie hĺbokého systému, insuficiencie chlopní perforátorov, insuficiencie povrchového systému, artériovenóznych fistúl, alebo kombinácie týchto faktorov (obr. 1). Medzi najčastejšie príčiny patria varices cruris a flebotrombóza hĺbokého systému (5).
Obr. 1. Etiológia vzniku CVI DK A – fyziologická funkcia hlbokého i povrchového venózneho systému DK, B – insuficiencia chlopní hlbokého venózneho systému, C – obštrukcia hlbokého systému (flebotrombóza), D – insuficiencia chlopní perforátorov, E – insuficiencia povrchového systému 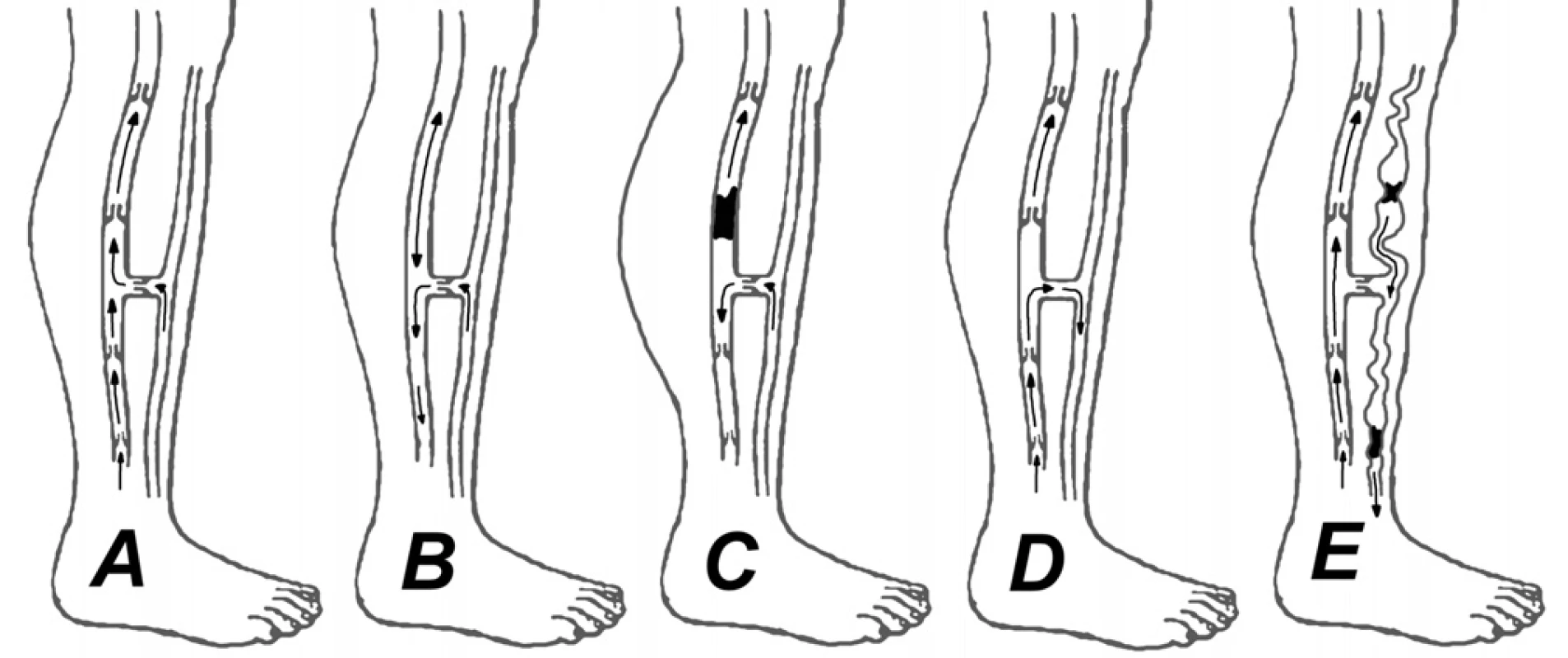
CVI vedie nezvratne ku chronickej venóznej hypertenzii. Riziko vzniku VU je od venóznej hypertenzie priamo závislé. Zatiaľ čo venózny tlak < 30 mm Hg vylučuje prítomnosť VU, tlak > 90 mm Hg sa spája s ich 100 % incidenciou (6).
Prvú významnejšiu teóriu publikovali v časopise Lancet v roku 1982 Browse a Burnand. Venózna hypertenzia spôsobuje zväčšovanie intercelulárnych kapilárnych priestorov a následné prenikanie vysokomolekulárnych látok do extrakapilárneho priestoru. Vznik takzvaných perikapilárnych fibrínových zátok tvorí bariéru prenosu nutrientov a kyslíka (5). Falanga et al. však dokumentujú, že fibrínové zátky vzhľadom na ich necelistvosť nemôžu tvoriť tak významnú bariéru (7).
V roku 1988 publikujú Coleridge et al. novú tézu patogenézy VU (8). Zvýšený venózny tlak vedie k zníženiu prúdenia krvi v kapilárach a ukladaniu leukocytov. Zachytené leukocyty uvoľňujú toxické metabolity kyslíka a proteolytické enzýmy, zodpovedné za deštrukciu kapilár. Ani to sa však neskôr nepotvrdilo.
Claudi et al. v roku 1991 popísali prítomnosť aktivovaných leukocytov zvyšujúcich aktivitu elastázy, s následným poškodením epitélií a zväčšením permeability kapilár (9). Leukocyty uvoľňujú tumorózny nekrotický faktor α, ktorý znižuje fibrinolytickú aktivitu, čím podporuje perikapilárne hromadenie fibrínu. Neskôr bola teória modifikovaná zahrnutím poruchy regulácie endoteliálneho rastového faktora a tumorózneho nekrotického faktora β (7).
Súčasná koncepcia predpokladá intrakapilárnu akumuláciu leukocytov s ich následnou aktiváciou. Lokálna kumulácia aktivovaných leukocytov vedie k zvýšeniu aktivít metaloproteináz (MMP) a iných rastovým faktorov (10). Pod vplyvom nerovnováhy hladín MMP, ich inhibítorov, rastových faktorov a chemoatraktantov dochádza k dysregulácii zápalovej fázy hojenia s takzvaným predčasným starnutím fibroblastov (5,11). Senilné fibroblasty nie sú schopné dostatočne kvalitatívne, ani kvantitatívne reagovať na rastové faktory (11). Senilný fenotyp fibroblastov je dokázaný aj v tkanivách pri miernejšom štádiu CVI (12).
Vznik a perzistencia VU je tak vysvetlená navodením patologickej zápalovej odpovede s následnou dysreguláciou riadiacich molekúl zápalu, čo vedie k patologickej zmene fenotypu buniek, podieľajúcich sa na hojení rán.
Diagnostika – klinický obraz
Typickou lokalitou výskytu VU sú DK od polovice lýtka po členok, s najčastejším výskytom v oblasti mediálneho maleolu (obr. 2). Vo všeobecnosti sú lézie viacpočetné, nepravidelného tvaru. Okolie ulkusu je často hyperpigmentované, postihnuté lipodermatosklerózou – tuhá, indurovaná koža. Lýtko môže mať až tvar takzvanej obrátenej šampusovej fľaše, keď je proximálna časť postihnutá edémom a distálna atrofickou lipodermatosklerózou (7).
Obr. 2. A – typická lokalizácia a tvar VU (fotografia pravej dolnej končatiny 79-ročného muža s 12-ročnou anamnézou VU DK pre posttrombotický syndróm), B – šráfovanie vyznačuje typickú lokalizáciu VU 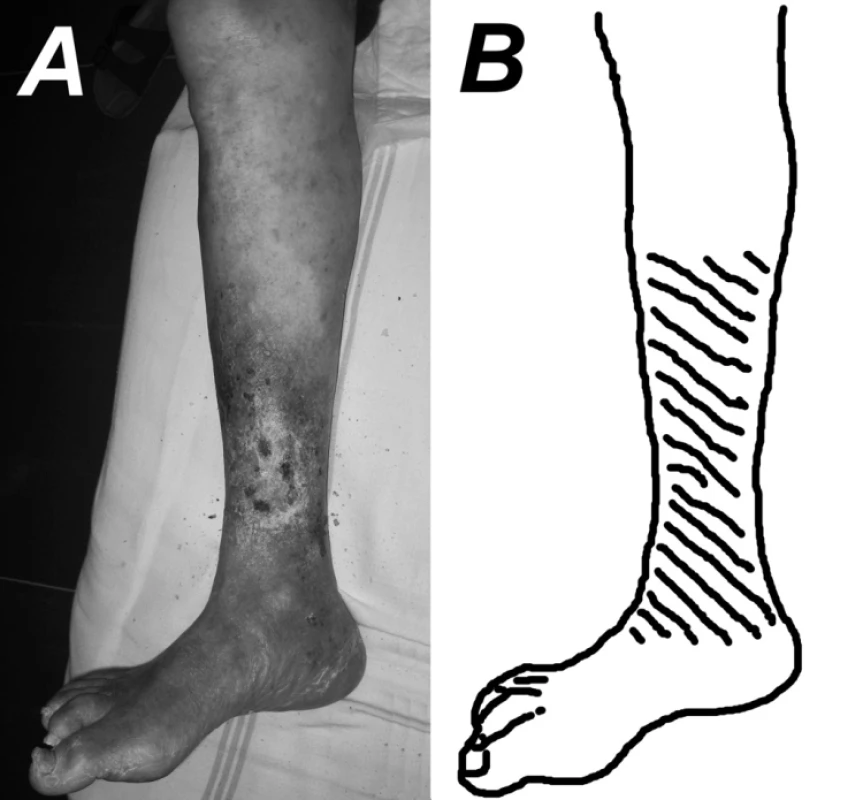
Pacienti popisujú svrbenie a bolesť zhoršujúcu sa počas dňa a ustupujúcu s eleváciou končatiny. Scott at al. považujú za rizikové faktory vzniku CVI a VU ženské pohlavie, vek, prekonanú tromboflebitídu, traumu, kongestíve srdcové zlyhávanie, obezitu a vyšší počet tehotenstiev (13). Veľké kontrolované štúdie popierajú vplyv väčšiny z týchto faktorov, pričom uvádzajú iba ich pozitívnu koreláciu s vekom ako najdôležitejším rizikovým faktorom vzniku CVI (5). Hlavnou rizikovou skupinou vzniku VU sú 60–80roční pacienti, skorší výskyt CVI však nie je vzácnosťou.
Diagnostika – vyšetrovacie metódy
Doplerovské ultrasonografické vyšetrenie (USG) venózneho systému DK je zlatým štandardom diagnostky CVI. Pacienti s anamnézou venóznej trombózy by mali podstúpiť hemokoagulačné vyšetrenie zahrňujúce antifosfolipidové protilátky, faktor V, protrombínovú génovú mutáciu a vyšetrenie hladiny proteínu C, S a antitrombínu III (14).
Z hľadiska terapie je dôležité odlíšenie venózneho a ischemického pôvodu ulkusu. Koincidenciu arteriálneho postihnutia najlepšie dokumentuje vyšetrenie indexu členkovo–brachiálneho tlaku (ABPI). Humphreys et al. vo svojej klinickej štúdii určujú za hranicu simplicitne venózneho postihnutia ABPI > 0,85. Za kombinovanú etiológiu považujú prípady ak ABPI > 0,5 a ABPI < 0,85. Ak je ABPI < 0,5 za etiológiu považujú samostatné arteriálne postihnutie (tab. 1) (15). Nesmie sa však zabúdať na nereprezentatívnosť výsledkov merania ABPI pri mediokalcinóze spájajúcej sa s DM (7). Funkčné vyšetrenia, ako meranie prstového tlaku za pomoci ultrazvuku alebo prstová fotopletyzmografia, môžu mať tiež vysokú výpovednú hodnotu.
Tab. 1. Diagnostika a terapia chronických rán DK podľa hodnoty ABPI (15) 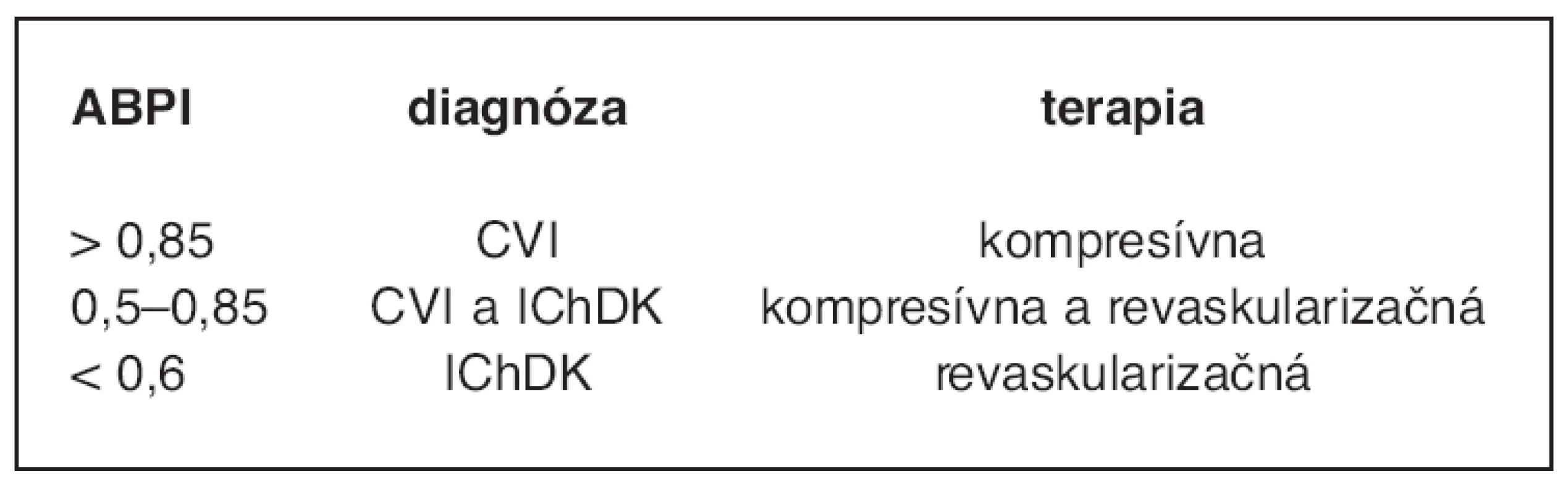
Dôležitá je aj diagnostika dvoch najnebezpečnejších komplikácii VU, osteomyelitídy a malignizácie (16). Ak hojenie neprogreduje, rana fistuluje, alebo je v rane prítomná kosť, je na mieste röntgenologické vyšetrenie. Publikované práce ďalej zdôrazňujú využiteľnosť kostného scanu alebo magnetickej rezonancie, ako diagnostických metód osteomyelitídy (14). Na malignizáciu treba myslieť u VU trvajúcich dlhšie ako 3 mesiace so známkami elevácie okrajov, alebo evertujúceho ložiska granulačného tkaniva. Impola et al. prezentujú vyhodnotenie expresie MMP-7 a MMP-13 z rany ako vhodnú metódu diagnostiky prítomnosti malignity v rane (17). Prezentované riziko malignizácie VU je 5,8 %. Napriek tomu, že toto riziko vykazuje jednoznačnú koreláciu s dĺžkou trvania VU, sú popísané prípady malignizácie aj pri VU trvania kratšieho ako 5 mesiacov (16).
Klasifikácia
Na piatom ročníku Amerického venózneho fóra (AVF) v roku 1993 John Porter inicioval vytvorenie medzinárodnej klasifikácie CVI podľa modelu TNM klasifikácie. O rok neskôr, vo februári 1994 bola na šiestom ročníku AVF vytvorená a schválená prvá verzia CEAP klasifikácie, založenej na hodnotení klinického štádia (C), etiológie (E), anatomickej klasifikácie (A) a patofyziológie (P) CVI. V tomto roku bola klasifikácia publikovaná v 25 periodikách a 8 jazykoch. Neskôr bola klasifikácia modifikovaná, pričom súčasnú podobu nadobudla v roku 2004 (tab. 2) (18, 19).
Tab. 2. CEAP klasifikácia (18) 
Terapia
Pre hojenie VU sú nevyhnutné štyri základné terapeutické metódy, nekrektómia, liečba infekcie, kompresia a stimulácia spodiny rany. V praxi sú používané aj ďalšie podporné metodiky. Podľa súčasných štúdii je incidencia recidív VU 78 %, čo vyžaduje dôslednú chirurgickú i medikamentóznu terapiu CVI nielen počas perzistencie VU, ale aj po ich vyhojení (14, 20, 21).
Nekrektómia (debridement)
Súčasná koncepcia terapie chronických rán stavia do popredia toaletu lôžka rany, ktorej hlavným cieľom je odstránenie nekrotického tkaniva, tkaniva s nízkym potenciálom k hojeniu, cudzorodej hmoty a infekcie (22).
Chirurgická nekrektómia je v našich podmienkach najčastejšie využívaným postupom. Jej výhodou je nízka náročnosť na materiálne a technické vybavenie, avšak je plne závislá od subjektívneho prístupu a skúseností chirurga. V súčasnosti je k dispozícii široké spektrum modifikovaných metodík nekrektómie.
Medzi novšie mechanické formy nekrektómie patrí použitie vodnej trysky. Mechanizmus spočíva v aplikovaní fyziologického roztoku cez malý otvor (< 0,1 mm) pod vysokým tlakom (> 103 MPa). Vodná tryska je veľmi vhodnou metódou nekrektómie u tlakových, diabetických, ischemických i venóznych ulkusov (23). Granick et al. poukazujú na zníženie priemerného počtu nekrektómii, čo v konečnom dôsledku pri použití vodnej trysky zníži náklady na hospitalizáciu jedného pacienta s VU (22).
Autolytický debridement je založený na aplikovaní okluzívnej drenáže, ktorá zabezpečí permanentné čistenie rany, stimuláciu bunkového delenia, udržiavanie stálej teploty, čo vedie k skoršiemu odstráneniu infekcie a rýchlejšej reepitelizácii (24).
Najčastejšie používanou formou biologického debridementu sú larvy. Jediná larva je schopná odstrániť za 24 hodín až 0,15 g mŕtveho tkaniva (25).
Populárna je aj enzymatická forma. Väčšina enzymatických substancií je založená na báze kolagenáz. Kolagenázy veľmi účinne degradujú kolagén a elastín, avšak ich účinnosť na fibrín je značne obmedzená. Túto nevýhodu odstraňuje kombinácia papaínu a urey, pri ktorej však hrozí poškodenie okolitej kože. Zaujímavé je aj potencovanie účinnosti antibiotickej terapie použitím chemického debridementu (24).
Debridement teda neznamená iba chirurgickú nekrektómiu. Je to komplexný súbor metodík so širokým miestom uplatnenia. Debridement je súčasne prvým a nevyhnutným krokom v terapii VU i chronických rán všeobecne.
Liečba infekcie
Úloha bakteriálnej infekcie a jej vzťah k vzniku a perzistencii chronických rán je doposiaľ nedostatočne známa (1). Napriek tomu je prítomnosť klinických známok infekcie jednoznačnou indikáciou k zahájeniu aj empirickej systémovej antibiotickej terapie (26). Medzi odporúčané antibiotiká prvej voľby radíme cefalexín, amoxicilín, fluorochinolóny a pre gram pozitívne baktérie aj clindamycín (27).
Použitie celkovej antibiotikej terapie pri asymptomatickej infekcii je kontroverzné. Aj pri celkovej antibiotickej terapii je zastúpenie kontaminovaných rán viac ako 90 % (28). Orálne aplikované antibiotiká majú značne zníženú penetračnú schopnosť do prostredia chronickej rany. Súčasné práce poukazujú na možnosť zlepšenia prieniku antibiotík použitím enzymatickej, alebo inej formy nekrektómie. Postoj k použitiu lokálnej antibiotickej terapie je tiež nejednoznačný. White et al. však vo svojej práci prezentujú záver, že lokálna antibiotická terapia pre zvýšené riziko vzniku rezistencie je vyhradená len pre prípady, keď neexistuje iná alternatíva liečby infekcie (1).
Diskutovanou je aj téma lokálneho použitia antiseptických prípravkov. Bunková toxicita je jedným z nosných argumentov proti ich používaniu. Napriek tomu, že súčasné antiseptické prípravky nie sú vyslovene toxické, je po ich aplikácii popisovaný spomalený rast keratinocytov a fibroblastov in vivo (29). White et al. charakterizujú ideálny antiseptický prípravok ako antiseptikum rýchlo účinkujúce s prolongovanou účinnosťou, s minimálnou systémovou absorpciou, bez karcinogénnych a teratogénnych účinkov, netoxické, lacné a široko dostupné. Žiadny v súčasnosti používaný preparát však tieto kritéria nespĺňa (1). Preparáty striebra vykazujú schopnosť destabilizácie ochranných biofilmov baktérii, pôsobiacich ako bariéra účinku antibiotík. Jednopercentný krém sulfadiazidu strieborného pozitívnym protizápalovým účinkom zlepšuje hojenie VU aj bez prítomnosti bakteriálnej infekcie. Nízka prítomnosť iónov striebra naviac potencuje antibakteriálny účinok liečiv. Na druhej strane, iná práca poukazuje, že administrácia preparátov striebra nemá odzrkadlenie v zvýšení percenta kompletne zhojených VU (30).
Napriek mnohým rizikám a negatívnym dopadom, antibiotická a lokálna antiseptická terapia sú nenahraditeľným krokom v terapii VU.
Kompresia
Kompresia je ďalšou z najdôležitejších súčastí liečby VU a CVI (31). Hlavným mechanizmom účinku je nahradenie insuficientnej lýtkovej pumpy. Nasleduje kompenzácia tlakového gradientu extravaskulárneho a intravaskulárneho priestoru a ústup tkanivového edému.
Základnou podmienkou pri indikácii kompresívnej terapie je diferenciálna diagnostika venóznych a ischemických ulkusov. Aplikovanie kompresného tlaku pri IChDK môže stav pacienta a jeho vyhliadky na vyliečenie výrazne zhoršiť (32). Väčšina autorov stanovuje za podmienku aplikácie kompresívnej terapie ABPI viac ako 0,7–0,9 (27). Ak je ABPI v rozsahu 0,5–0,85, niektorí autori odporúčajú kombináciu kompresívnej terapie a revaskularizačného chirurgického výkonu (tab. 1) (15). Rôzne spôsoby aplikácie kompresívnej terapie môžeme rozdeliť do niekoľkých kategórii: neelastická bandáž, elastická bandáž, viacvrstvová bandáž, kompresná pumpa, ortotické zariadenia a stupňovito kompresívna bandáž (14).
Rigidná neelastická bandáž je používaná u pacientov s hraničným postihnutím aj arteriálneho systému DK. Elastická bandáž je používaná pri liečbe VU po ústupe iniciálneho edému. Skupina viacvrstvových bandáží je charakterizovaná zabezpečením stáleho tlaku, 40–45 mm Hg v oblasti členka a 17 mm Hg v oblasti kolena. Viacero autorov potvrdzuje najlepšie výsledky práve pri použití tejto kompresívnej terapie (14). Napriek vyššej cene viacvrstvových bandáží, no časovo kratšej terapii, sa náklady liečby jedného pacienta znižujú (14).
Mechanizmus účinku kompresnej pumpy spočíva v podpore venózneho návratu a zlepšení hemodynamických parametrov. Sú vhodné najmä u imobilných a geriatrických pacientov. Ich použitím stúpa fibrinolytická aktivita, klesá riziko trombembolických komplikácií, na druhej strane si však vyžadujú imobilitu pacienta najmenej 6 hodín denne.
Stupňovito kompresívna bandáž je podľa štúdií najčastejšie používaná ako prevencia recidívy po zhojení VU. Podľa aplikovaného tlaku ju delíme na štyri stupne (tab. 3) (33).
Tab. 3. Rozdelenie stupňovito kompresívnej bandáže s indikáciami (33) 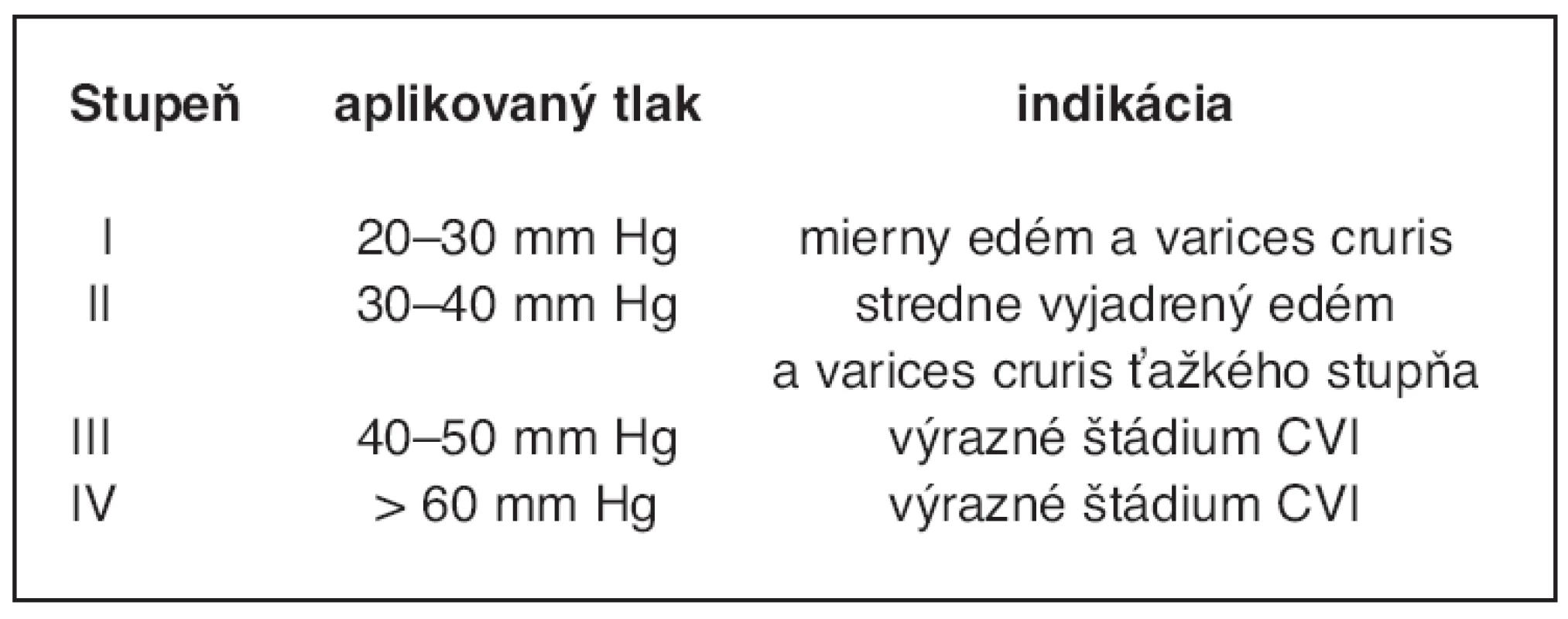
Kompresívna terapia vo svojich rôznych variantoch a obmenách zastáva nenahraditeľné miesto v terapii i prevencii VU.
Stimulácia spodiny rany
Drenáž chronických rán je používaná ako doplnková terapia. V súčasnosti je používané množstvo variantov drenáže, ktoré zabezpečujú absorpciu výpotku, debridement rany a urýchlenie granulácie mechanickou stimuláciou. Úlohou drenáže je uchovať ranu vlhkú a súčasne zabrániť nadmernému mokvaniu.
V roku 1996 Morykwas a Argenta prezentujú metódu podtlakového uzatvárania rán, ktorá je v kontinuálnom režime pri aplikovaní podtlaku 50–70 mm Hg aplikovateľná aj u VU. Aplikovaný podtlak zabezpečuje vlhké prostredie rany, zlepšuje manažment výpotoku, znižuje infekčnú záťaž, zabezpečuje lokálne zvýšenie teploty a mechanicky stimuluje spodinu rany, čím zvyšuje tvorbu granulačného tkaniva (34).
Inou možnosťou stimulácie a urýchlenia hojenia je biostimulácia laserovým žiarením. V súčasnosti je publikovaných množstvo prác prezentujúcich pozitívny vplyv stimulačného laserového žiarenia na chronické ulkusy, najmä diabetické rany (35). Vzťah laserového žiarenia a VU je však veľmi kontroverzný a väčšina autorov prezentuje neúspešnosť tejto terapie na hojenie chronických rán pri CVI (36).
Aplikácia kožných štepov
Na prekrytie chronických rán sa v súčasnosti používa široké spektrum kožných štepov (tab. 4). Základnou podmienkou aplikácie je čistá, neinfikovaná rana s adekvátnym cievnym zásobením, čo je aj hlavnou limitáciou použitia tejto metódy. Keratinocyty a fibroblasty transplantátu nie sú postihnuté senilnou fenotypizáciou, a preto rýchlejšie reagujú produkciou fyziologických rastových faktorov a chemoatraktantov.
Tab. 4. Druhy kožných štepov (27) 
V súčasnosti stúpa záujem aj o používanie takzvanej pestovanej kože. Apligraft® je náhrada kože, pestovaná z neonatálnych buniek, zahrňujúca keratinocyty a fibroblasty, tvoriace kožu a podkožie. Dermagraft je vyrobený z ľudských fibroblastov, pestovaných na biodegradovateľných sieťkach. Aj tieto produkty sú použiteľné pri terapii VU (27).
Chirurgická terapia CVI
Medzi najpoužívanejšie chirurgické metodiky liečby CVI patrí exstirpácia povrchového venózneho systému a oklúzia insuficientných perforátorov. V roku 1985 bola prezentovaná nová chirurgická metóda terapie insuficiencie chlopní perforátorov endoskopická chirurgia perforačných vén (SEPS). Baron et al. vo svojej štúdii prezentujú širokú použiteľnosť SEPS s veľmi pozitívnymi aspektmi (37).
Chirurgická terapia zaisťuje nižšie riziko recidív VU. Barwel et al. prezentujú 50% pokles recidív do jedného roka, napriek neúspešnosti terapie pri hodnotení dvojročného relapsu (38). Aj iné práce porovnávajúce chirurgickú a konzervatívnu terapiu CVI, preferujú chirurgický prístup (27). Gohel et al. doporučujú kombináciu chirurgickej a dlhodobej kompresívnej terapie (39). Z prezentovaného vyplýva, že chirurgická terapia CVI nie je len prevenciou vzniku VU, ale i výraznou terapeutickou metódou a spôsobom zabraňujúcim vznik recidív.
Medikamentózna terapia CVI
Okrem antibiotickej sa pri liečbe VU uplatňuje aj podporná medikamentózna terapia CVI. Medzi konzervatívnu medikamentóznu liečbu CVI patria vazodilatačne pôsobiace lieky, najmä pentoxyphilin a flavonoidy. Prvé miesto zastáva pentoxyphilin. Väčšina autorov prezentuje úspešnosť vyšších dávok 3 × 800 mg, oproti používaným 3 × 400 mg (14). Publikované sú dvojito slepé štúdie, poukazujúce na úspešnosť terapie pri administrácii 1 g flavonoidov na deň (14). Iná štúdia poukazuje na úspešnosť kombinácie terapie flavonoidmi a kompresívnej terapie (40). Aj medikamentózna liečba má teda svoje nezastupiteľné miesto v terapii CVI i VU.
Záver
Incidencia a terapia VU a CVI je stále aktuálnou témou s rozsiahlym medicínskym a ekonomickým dopadom. Aj epidemiologické štúdie 21. storočia poukazujú na stále vysoké incidencie tohto zákerného ochorenia. Napriek zložitej a dodnes nejasnej etiopatogenéze CVI a VU, máme v súčasnosti k dispozícii široké spektrum terapeutických možností.
Aj pri VU je však prvým krokom k terapii dokonalá diagnostika ochorenia. Špecifické metódy terapie VU môžu pri ich aplikovaní na chronickú ranu inej etiológie spôsobiť značné iatrogénne poškodenie pacienta. Dôležitá je aj špecifikácia postihnutia venózneho systému DK, čo tiež do značnej miery modifikuje terapeutické metódy.
Základnou terapeutickou metódou VU je debridement v jeho širokých modifikáciách. Liečba bakteriálnej kolonizácie rany nie je doposiaľ celkom štandardizovaná a celková antibiotická terapia je indikovaná len pri jednoznačných prejavoch infekcie. Máme však široké možnosti lokálnej antiseptickej terapie. Stimulácia spodiny rany patrí vo svete, a postupne aj u nás, k štandardom terapie chronických rán, medzi ktorými VU nie je výnimkou. Netreba však zabúdať ani na komplexnú liečbu CVI v zmysle kompresívnej, chirurgickej, či medikamentóznej terapie.
Liečba VU je teda interdisciplinárnou problematikou, vyžadujúcou rozsiahle diagnostické i terapeutické metódy, patriaca do rúk lekára špecializovaného na problematiku chronických rán.
Skratky
ABPI – index členkovo-brachiálneho tlaku
AVF – Americké venózne fórum
CVI – chronická venózna insuficiencia
DK – dolná končatina
DM – diabetes mellitus
IChDK – ischemická choroba dolných končatín
MMP – matrixová metaloproteináza
SEPS – endoskopická chirurgia perforačných vén
USG – doplerovské ultrasonografické vyšetrenie
VU – venózny ulkus
MUDr. Tomáš Toporcer
II. chirurgická klinika FNLP
Rastislavova 43, 040 90 Košice, Slovenská republika
e-mail: topyto@gmail.com
Zdroje
1. White, R. J., Cutting, K., Kingsley, A.: Topical antimicrobials in the control of wound bioburden. Ostomy. Wound.Manage., 2006, 52, s. 26–58.
2. Lim, T., Mwipatayi, B., Murray, R. et al.: Microbiological profile of chronic ulcers of the lower limb: a prospective observational cohort study. ANZ. J. Surg., 2006, 76, s. 688–692.
3. Bergqvist, D., Lindholm, C., Nelzen, O.: Chronic leg ulcers: the impact of venous disease. J. Vasc. Surg., 1999, 29, s. 752–755.
4. Ruckley, C. V.: Socioeconomic impact of chronic venous insufficiency and leg ulcers. Angiology, 1997, 48, s. 67–69.
5. Abbade, L. P., Lastoria, S.: Venous ulcer: epidemiology, physiopathology, diagnosis and treatment. Int. J. Dermatol., 2005, 44, s. 449–456.
6. Nicolaides, A. N., Hussein, M. K., Szendro, G. et al.: The relation of venous ulceration with ambulatory venous pressure measurements. J. Vasc. Surg., 1993, 17, s. 414–419.
7. Falanga, V., Eaglstein, W. H.: The “trap” hypothesis of venous ulceration. Lancet, 1993, 341, s. 1006–1008.
8. Coleridge Smith, P. D., Thomas, P. et al.: Causes of venous ulceration: a new hypothesis. Br. Med. J. (Clin. Res. Ed), 1988, 296, s. 1726–1727.
9. Claudy, A. L., Mirshahi, M., Soria, C. et al.: Detection of undegraded fibrin and tumor necrosis factor–alpha in venous leg ulcers. J. Am. Acad. Dermatol., 1991, 25, s. 623–627.
10. Bergan, J. J., Schmid-Schonbein, G. W., Smith, P. D. et al.: Chronic venous disease. N. Engl. J. Med., 2006, 355, s. 488–498.
11. Wong, T., McGrath, J. A., Navsaria, H.: The role of fibroblasts in tissue engineering and regeneration. Br. J. Dermatol., 2007, 156, s. 1149–1155.
12. Raffetto, J. D., Mendez, M. V., Marien, B. J. et al.: Changes in cellular motility and cytoskeletal actin in fibroblasts from patients with chronic venous insufficiency and in neonatal fibroblasts in the presence of chronic wound fluid. J. Vasc. Surg., 2001, 33, s. 1233–1241.
13. Scott, T. E., LaMorte, W. W., Gorin et al.: Risk factors for chronic venous insufficiency: a dual case-control study. J. Vasc. Surg., 1995, 22, s. 622–628.
14. Etufugh, C. N., Phillips, T. J.: Venous ulcers. Clin. Dermatol., 2007, 25, s. 121–130.
15. Humphreys, M. L., Stewart, A. H., Gohel, M. S. et al.: Management of mixed arterial and venous leg ulcers. Br. J. Surg., 2007, 94, s. 1104–1107.
16. Reich, A., Cisło, M., Szepietowski, J. C.: Squamous Cell Carcinoma Arising in Long Lasting Leg Ulceration. Čes.-slov. Derm., 2006, 81, s. 290–292.
17. Impola, U., Jeskanen, L., Ravanti, L. et al.: Expression of matrix metalloproteinase (MMP)-7 and MMP-13 and loss of MMP-19 and p16 are associated with malignant progression in chronic wounds. Br. J. Dermatol., 2005, 152, s. 720–726.
18. Eklof, B., Rutherford, R. B., Bergan, J. J. et al.: Revision of the CEAP classification for chronic venous disorders: consensus statement. J. Vasc. Surg., 2004, 40, s. 1248–1252.
19. Golian, D., Mazuch, J., Mištuna, D. et al.: Klinické hodnotenie varikóznej choroby DK z pohľadu CEAP, pooperačné sledovanie významných etiopatogenetických faktorov v našom súbore. Praktická flebologie, 2004, 13, s. 72–75.
20. Radoňak, J., Vajó, J., Brandebur, O. et al.: Liečba chronických žilových vredov. Praktická flebologie, 2007, 16, s. 22.
21. Marston, W.: Evaluation and treatment of leg ulcers associated with chronic venous insufficiency. Clin. Plast. Surg., 2007, 34, s. 717–730.
22. Granick, M. S., Posnett, J., Jacoby, M. et al.: Efficacy and cost-effectiveness of a high–powered parallel waterjet for wound debridement. Wound.Repair Regen., 2006, 14, s. 394–397.
23. Gurunluoglu, R.: Experiences with waterjet hydrosurgery system in wound debridement. World J. Emerg. Surg., 2007, 2, s. 10.
24. Steed, D. L.: Debridement. Am. J. Surg., 2004, 187, s. 71S–74S.
25. Blake, F. A., Abromeit, N., Bubenheim, M. et al.: The biosurgical wound debridement: experimental investigation of efficiency and practicability. Wound. Repair Regen., 2007, 15, s. 756–761.
26. Ebright, J. R.: Microbiology of chronic leg and pressure ulcers: clinical significance and implications for treatment. Nurs. Clin. North Am., 2005, 40, s. 207–216.
27. Reichenberg, J., Davis, M.: Venous ulcers. Semin.Cutan.Med.Surg., 2005, 24, s. 216–226.
28. Tammelin, A., Lindholm, C., Hambraeus, A.: Chronic ulcers and antibiotic treatment. J. Wound. Care, 1998, 7, s. 435–437.
29. Wilson, J. R., Mills, J. G., Prather, I. D. et al.: A toxicity index of skin and wound cleansers used on in vitro fibroblasts and keratinocytes. Adv. Skin Wound. Care, 2005, 18, s. 373–378.
30. Vermeulen, H., van Hattem, J. M., Storm-Versloot, M. N. et al.: Topical silver for treating infected wounds. Cochrane. Database. Syst. Rev., 2007, CD005486.
31. Milic, D. J., Zivic, S. S., Bogdanovic, D. C. et al.: A randomized trial of the Tubulcus multilayer bandaging system in the treatment of extensive venous ulcers. J. Vasc. Surg., 2007, 46, s. 750–755.
32. Lorimer, K. R., Harrison, M. B., Graham, I. D. et al.: Venous leg ulcer care: how evidence-based is nursing practice? J. Wound. Ostomy. Continence. Nurs., 2003, 30, s. 132–142.
33. Bello, Y. M., Phillips, T. J.: Chronic leg ulcers: types and treatment. Hosp. Pract. (Minneap.), 2000, 35, s. 101–107.
34. Toporcer, T., Radoňák, J.: Podtlakové uzatváranie rán – nové poznatky a možnosti aplikácie, 2006, 145, s. 702–707.
35. Kilík, R., Bober, J., Gál, P. et al.: Vplyv laserového žiarenia rôznych intenzít na hojenie incíznych rán u zdravých a diabetických potkanov. Rozhl. Chir, 2007, 86, s. 384–387.
36. Kopera, D., Kokol, R., Berger, C. et al.: Does the use of low–level laser influence wound healing in chronic venous leg ulcers? J. Wound. Care, 2005, 14, s. 391–394.
37. Baron, H. C., Wayne, M. G., Santiago, C. et al.: Treatment of severe chronic venous insufficiency using the subfascial endoscopic perforator vein procedure. Surg. Endosc., 2005, 19, s. 126–129.
38. Barwell, J. R., Davies, C. E., Deacon, J. et al.: Comparison of surgery and compression with compression alone in chronic venous ulceration (ESCHAR study): randomised controlled trial. Lancet, 2004, 363, s. 1854–1859.
39. Gohel, M. S., Barwell, J. R., Taylor, M. et al.: Long term results of compression therapy alone versus compression plus surgery in chronic venous ulceration (ESCHAR): randomised controlled trial. BMJ, 2007, 335, s. 83.
40. Glinski, W., Chodynicka, B., Roszkiewicz, J. et al.: Effectiveness of a micronized purified flavonoid fraction (MPFF) in the healing process of lower limb ulcers. An open multicentre study, controlled and randomized. Minerva Cardioangiol., 2001, 49, s. 107–114.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek Probiotics and the skinČlánek Laureáti Nobelovy ceny
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Psilocybin je v Česku od 1. ledna 2026 schválený. Co to znamená v praxi?
- Horní limit denní dávky vitaminu D: Jaké množství je ještě bezpečné?
- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Ukažte mi, jak kašlete, a já vám řeknu, co vám je
-
Všechny články tohoto čísla
- Venózny ulkus – súčasné pohľady na etiopatogenézu, diagnostiku a terapiu
- Léčba chronické myeloidní leukémie – méně běžný pohled na moderní postupy
- Postižení periferního nervového systému a míra motorického postižení u Parkinsonovy nemoci: korelační studie
- Vývoj respirační morbidity dětí ve vztahu k jejich expozici pasivnímu kouření
- Allgemeine Klinische Psychologie
- Parenterálna nutrícia pred resekčným výkonom na hornom gastrointestinálnom trakte
- Rizikové faktory vzniku atelektázy po plicní lobektomii
- Analoga somatostatinu v léčbě karcinoidu
- Stimulace sakrálního nervu v léčbě neurogenní anální inkontinence
- K životnímu jubileu doc. MUDr. Aleny Lobovské, CSc.
- Alfred Kohn, profesor histologie na Německé univerzitě v Praze
- HISTORICKÉ LÉKAŘSKÉ NÁSTROJE A POMŮCKY,
- Acute respiratory tract infections: a potential trigger for the acute coronary syndrome
- Probiotics and the skin
- Suicide in China: unique demographic patterns and relationship to depressive disorder
- Immunology of asthma and chronic obstructive pulmonary disease
- Epidemiologic and clinical features of anaphylaxis in Korea
- Doc. MUDr. Vladimír Puchmayer, CSc.
- Prof. MUDr. Marie Pešková, DrSc.
- Spolek lékařů českých v Praze
- Laureáti Nobelovy ceny
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Rizikové faktory vzniku atelektázy po plicní lobektomii
- Analoga somatostatinu v léčbě karcinoidu
- Stimulace sakrálního nervu v léčbě neurogenní anální inkontinence
- Parenterálna nutrícia pred resekčným výkonom na hornom gastrointestinálnom trakte
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



