-
Medical journals
- Career
Eisenmengerův syndrom a jeho komplikace v dětském věku
Authors: T. Doušová 1; J. David 1; K. Špičáková 1; K. Koubský 2; V. Koukolská 3; P. Jansa 4
Authors‘ workplace: Pediatrická klinika 2. lékařské fakulty Univerzity Karlovy a FN Motol, Praha 1; Dětské kardiocentrum 2. lékařské fakulty Univerzity Karlovy a FN Motol, Praha 2; Klinika zobrazovacích metod 2. lékařské fakulty Univerzity Karlovy a FN Motol, Praha 3; Centrum pro plicní hypertenzi, 1. lékařská fakulta Univerzity Karlovy, Všeobecná fakultní nemocnice, Praha 4
Published in: Čes-slov Pediat 2020; 75 (3): 178-182.
Category: Case Report
Overview
U přibližně 3–10 % pacientů s vrozenou vadou srdce (CHD, Congenital Heart Disease) dochází k rozvoji plicní arteriální hypertenze (PAH-CHD, Pulmonary Arterial Hypertension associated with Congenital Heart Disease). U nekorigovaných srdečních vad s významným levopravým zkratem se jedná o přirozený vývoj onemocnění, ve kterém plicní cévní řečiště reaguje na zvýšený průtok vzestupem cévní rezistence. Konečným důsledkem je tzv. Eisenmengerův syndrom (ES), kdy plicní cévní rezistence přesáhne systé-movou a zkrat se mění na pravolevý. PAH-CHD významně zvyšuje morbiditu a mortalitu pacientů. Díky časné diagnostice a možnostem chirurgické korekce CHD je v dnešní době ve vyspělých zemích ES velmi vzácný.
Autoři předkládají kazuistiku patnáctiletého pacienta s ES spojeného se závažnou komplikací – mnohočetnou septickou intrakraniální embolizací.
Klíčová slova:
plicní arteriální hypertenze – vrozená srdeční vada – Eisenmengerův syndrom – mozkový absces
ÚVOD
Plicní arteriální hypertenzi (PAH, Pulmonary Arterial Hypertension) lze v dětském věku definovat zvýšením středního tlaku v plicnici nad 20 mmHg v klidovém stavu [1]. S incidencí 1–9 : 100 000 představuje vzácné onemocnění [2] spojené s významnou morbiditou a mortalitou [3]. Patogeneze PAH je multifaktoriální – ke zvýšení arteriálního tlaku v plicním oběhu dochází na podkladě vazokonstrikce, cévní proliferace, zánětu či trombózy. V dětském věku se nejčastěji vyskytuje forma idiopatická či asociovaná s vrozenou srdeční vadou (PAH-CHD, Pulmonary Arterial Hypertension associated with Congenital Heart Disease) [4, 5]. Podrobnější klasifikaci PAH přináší tabulka 1 [6].
Table 1. Klasifikace plicní arteriální hypertenze [upraveno dle 6, 17]. ![Klasifikace plicní arteriální hypertenze [upraveno dle 6, 17].](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/19a2c1e7c0e4beed7c4de08a5eef5f21.png)
U přibližně 3–10 % pacientů s CHD a přítomným levopravým zkratem dochází k rozvoji PAH-CHD [7]. PAH-CHD je jednotkou se širokým spektrem morfologických a hemodynamických nálezů různé závažnosti [8]. Plicní cévní řečiště reaguje na zvýšený průtok při levopravém zkratu nárůstem plicní cévní rezistence na podkladě morfologických změn plicních arterií – tzv. plicní cévní choroby. Tyto změny jsou zpočátku reverzibilní a včasnou korekcí zkratu lze dosáhnout následného poklesu tlaku v plicním řečišti. Pokud však levopravý zkrat přetrvává, přímo úměrně s jeho významností dochází v řádu let ke změnám ireverzibilním a fixaci PAH. Při suprasystémových hodnotách v plicním řečišti se zkrat mění na pravolevý, tento stav pak označujeme jako tzv. Eisenmengerův syndrom (ES) [4], poprvé popsaný v roce 1897. Díky časné diagnostice a možnostem chirurgické korekce CHD se dnes s takovými pacienty setkáváme vzácně [9], i tak je nutné mít možné infekční komplikace ES stále na paměti (typicky bronchopneumonie, endokarditida či mozkový absces).
Prezentované sdělení formou kazuistiky se věnuje závažné komplikaci ES – mnohočetným mozkovým abscesům s opakovanou embolizací do centrální nervové soustavy (CNS). Obě jednotky se u zdravé populace vyskytují velmi vzácně. Naopak pacienti s PAH a cyanotickou CHD (tj. s pravolevým zkratem) představují rizikovou skupinu pacientů, u kterých se v důsledku oběhových změn lze s mozkovým abscesem i embolizací setkat podstatně častěji [10].
KAZUISTIKA
Patnáctiletý chlapec byl vyšetřen na oddělení urgentního příjmu pro pět dní trvající intenzivní difuzní bolest hlavy s mírnou úlevou po analgeticích, nevolnost a opakované zvracení. Jednalo se o polymorbidního pacienta s kombinovanou srdeční vadou charakteru ES a sekundární PAH (anamnesticky po opakované ligaci perzistující tepenné dučeje v batolecím věku) s méně významnými mnohočetnými defekty komorového septa a středně významnou stenózou chlopně plicnice. Chlapec byl na zavedené léčbě PAH (sildenafil a bosentan), ke které byl pro zhoršení hodnot z pravostranné srdeční katetrizace měsíc před začátkem obtíží přidán prostacyklinový analog treprostinil v kontinuálním subkutánním režimu. Rychlost podání byla v posledních týdnech pozvolna navyšována, proto byly bolesti hlavy přisuzovány nežádoucímu účinku úpravy této medikace.
Nejprve uvádíme podrobné informace z pacientovy anamnézy. Jednalo se o původně eutrofické a donošené dítě ze třetí fyziologické gravidity. Chlapec se narodil ve 40. gestačním týdnu spontánně záhlavím s porodní hmotností 3150 g a délkou 48 cm. Poporodní adaptace byla bez komplikací. Od třetího dne života se rozvinul systolický šelest parasternálně vlevo. Chlapec prospíval dobře a psychomotoricky se vyvíjel normálně, očkován je řádně podle očkovacího kalendáře. Sociální anamnéza byla nenápadná, žije v úplné rodině. Otec i matka pacienta jsou zdrávi, otec matky zemřel na plicní karcinom, matka otce byla sledována pro chlopenní vadu, podrobnější informace nebyly k dispozici. Chlapec má dva sourozence, šestadvacetiletého a dvacetiletého bratra, oba jsou zdrávi.
Spádový dětský kardiolog hodnotil zachycený šelest jako benigní. Nález byl ve věku osmnácti měsíců přehodnocen na specializovaném pracovišti dětské kardiologie, kde byla diagnostikována významná perzistující tepenná dučej s již rozvinutou sekundární PAH a známkami přetížení pravé komory. Dalším nálezem byly vícečetné komorové defekty a mírná stenóza plicnice. Přes opakovanou ligaci tepenné dučeje ve dvou letech věku přetrvával nález PAH, která po opakovaných pravostranných katetrizacích v posledních letech progredovala. V kontextu nepříznivého vývoje plicní cévní rezistence byla postupně eskalována specifická farmakoterapie PAH. Aktuálně byl pro tuto základní diagnózu ve sledování specialisty pro PAH, dětského kardiologa, pneumologa a pro hypermetropii též i očního lékaře.
Při vstupním fyzikálním vyšetření byl chlapec eupnoický, afebrilní, somnolentní, poslechově byl znatelný systolicko-diastolický šelest (intenzity 3/6) bez propagace, s tepovou frekvencí 78/min, dechovou frekvencí 16/min, krevním tlakem 129/79 mmHg (95.–99. percentil) a saturací 93 %. Ostatní somatický nález byl v mezích normy s následujícími antropometrickými parametry – výška 166 cm (11. percentil), hmotnost 67,5 kg (74. percentil), body mass index (BMI) 24,5 kg/m2 (93. percentil).
Vstupní laboratorní vyšetření neprokázalo výraznější patologické nálezy: krevní obraz v normě, mírně zvýšené zánětlivé parametry – C-reaktivní protein (CRP) 15 mg/l (tab. 2), mineralogram a koagulační parametry ve fyziologickém rozmezí. Neurologicky nebyl u chlapce patrný ložiskový nález, avšak pro progredující spavost a neustupující výraznou cefaleu byl přijat na dětské lůžkové oddělení, kde vyšetření očního pozadí prokázalo oboustranné městnání papil. Vzhledem ke klinickému stavu a základní diagnóze PAH bylo akutně provedeno vyšetření výpočetní tomografií (CT) mozku s nálezem dvou abscesových ložisek – větší ložisko frontálně vpravo (46 x 28 x 34 mm) a menší ložisko okcipitálně vlevo (26 x 23 x 21 mm) s výrazným perifokálním edémem a přesunem středočárových struktur (obr. 1).
Table 2. Vývoj vybraných laboratorních parametrů u prezentovaného pacienta. 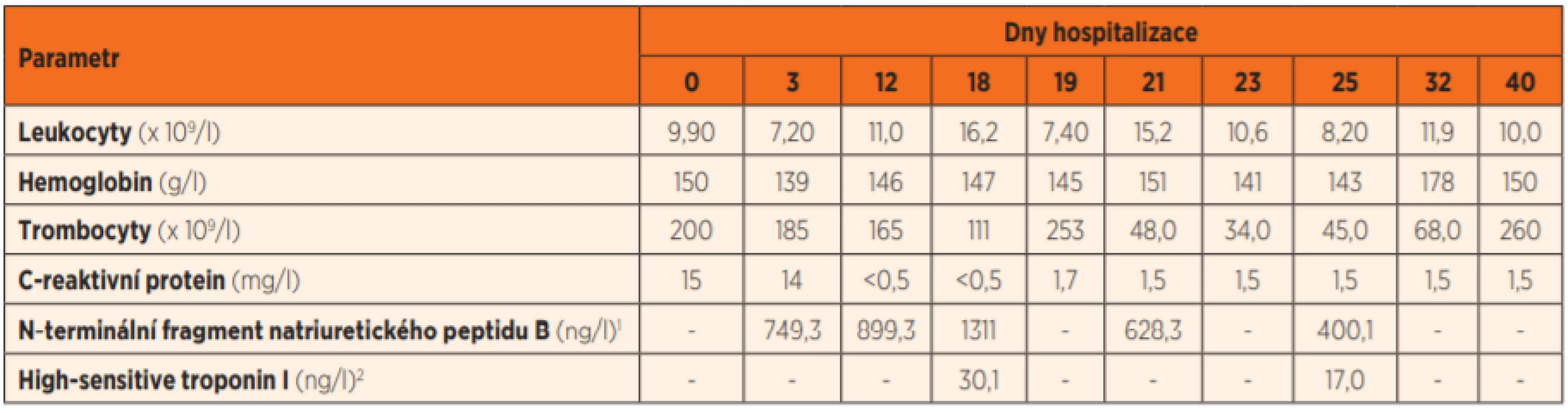
1 normální rozmezí 6,0–158,0 ng/l
2 normální rozmezí 0–33,6 ng/lImage 1. CT mozku při přijetí pacienta (7. 7. 2019). a – Postkontrastní CT, sagitální rekonstrukce: absces (46 x 28 x 34 mm) frontálně vpravo (žluté šipky) s výrazným perifokálním edémem (modré šipky); b – Postkontrastní CT, axiální rovina: absces okcipitálně vlevo (26 x 23 x 21 mm, žluté šipky) s výrazným perifokálním edémem (modré plné šipky), přesun středočárových struktur doleva (otevřená modrá šipka). Vpravo frontálně okrsek edému (hvězdička) v okolí abscesu.
Fig. 1. Brain CT in patient admission (7. 7. 2019). Frontal right-sided abscess (46 x 28 x 34 mm) and occipital left-sided abscess (26 x 23 x 21 mm) with perifocal edema.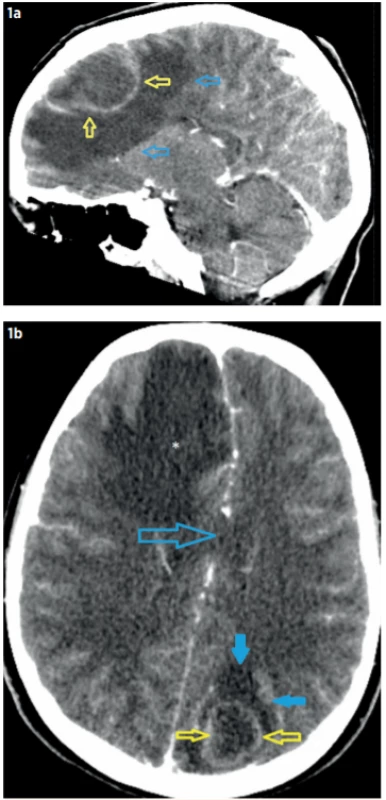
Cestou neurochirurgické kliniky byla na základě zobrazení magnetickou rezonancí (MRI) provedena navigovaná punkce s drenáží, zahájena empirická antibiotická terapie v trojkombinaci ceftriaxon-dinatricum (2 g à 12 h), metronidazol (500 mg à 8 h) a vankomycin-hydrochlorid (500 mg à 6 h), dále kortikoidní (sodná sůl dexamethason-fosfátu, 6 mg à 6 h) a virostatická (sodná sůl acikloviru, 500 mg à 8 h) léčba. Kultivačně byl z abscesu prokázán Streptococcus intermedius.
Na zavedené terapii došlo postupně ke klinické i laboratorní úpravě, která umožňovala deeskalaci antibiotické i kortikoidní terapie. Virostatická léčba byla ukončena po sedmi dnech, stejně tak léčba metronidazolem a vankomycinem. Vzhledem k dobré in vitro citlivosti S. intermedius byl na doporučení antibiotického centra podáván ceftriaxon celkem pět týdnů intravenózně a následně jeden týden potencovaným aminopenicilinem perorálně. Neurologický status byl příznivý, ve druhé polovině hospitalizace se přechodně objevil mírný akrální třes horních končetin. Opakované kontrolní MRI prokázalo regresi obou abscesových ložisek (obr. 2).
Image 2. MR mozku před dimisí pacienta (30. 8. 2019). a – Postkontrastní T1w sekvence v sagitální rovině: Ložisko vpravo frontálně (žluté šipky; 32 x 15 x 11 mm) ve výrazné parciální regresi, výrazná regrese perifokálního edému; b – Nativní FLAIR sekvence v axiální rovině: Reziduum abscesu (žlutá šipka plná) vpravo frontálně a vlevo okcipitálně (zde je již kolabovaná abscesová dutina, modrá šipka plná), výrazná parciální regrese perifokálního edému, úplná regrese defigurace střední čáry, pooperační změny kalvy okcipitálně (otevřená žlutá šipka).
Fig. 2. Brain MRI before patient dismiss (30. 8. 2019). Frontal right-sided abscess (32 x 15 x 11 mm) and perifocal edema in regression.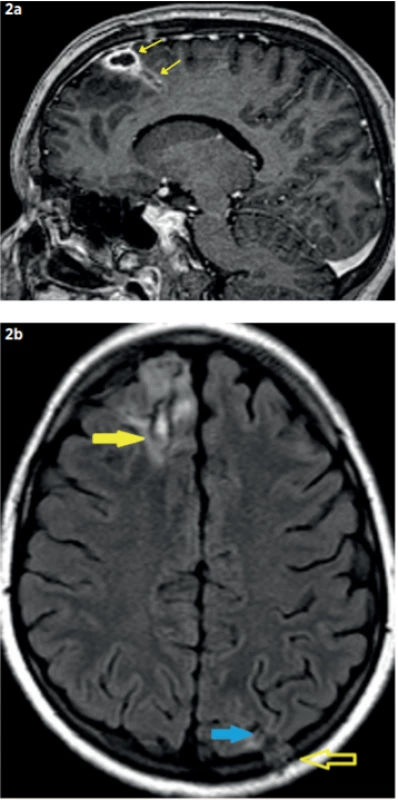
Hospitalizace byla komplikována postupně se rozvíjející trombocytopenií (tab. 2) s nejnižší hodnotou krevních destiček 34 x 109/l, která vzhledem k riziku pooperačního krvácení do CNS vyžadovala na doporučení hematologa podání jedné jednotky trombocytárního přípravku. Etiologie nebyla jednoznačně prokázána (včetně provedené aspirace kostní dřeně a extenzivních imunologických vyšetření).
Další komplikací byla srdeční dekompenzace s retencí tekutin a známkami plicního edému. Úlohu mohl sehrát vyšší příjem tekutin v předcházejících dnech v kombinaci s přechodně sníženou rychlostí infuze treprostinilu. Obraz srdečního selhání byl spojen se zhoršením klinického stavu (hyposaturace, tachydyspnoe, tachykardie) i echokardiografických nálezů. K další stabilizaci byl proto pacient přeložen do Centra pro plicní hypertenzi Všeobecné fakultní nemocnice v Praze, kde došlo po nasazení diuretické terapie ke zlepšení stavu. Zde proběhla další elektivní srdeční katetrizace. Pacient byl po celkem osmi týdnech propuštěn do domácí péče. Vývoj sledovaných laboratorních parametrů shrnuje tabulka 2.
S odstupem dvou týdnů od dimise byly na plánované kontrolní MRI mozku zachyceny čerstvé postischemické změny subakutního charakteru, oboustranně frontálně kortikosubkortikálně. Vzhledem k opakované embolizaci byl pacient zajištěn antikoagulační terapií nízkomolekulárním heparinem (0,4 ml denně subkutánně). Jeho prognóza je nyní nejistá, vzhledem k akutnímu zhoršení byly s rodinou zahájeny rozhovory o možnosti zařazení na čekací listinu k transplantaci bloku srdce a plic.
DISKUSE
U zdravého člověka dochází díky vysoké fagocytární kapacitě k filtraci infekčních agens již v plicní cirkulaci. Odlišná situace nastává u pacientů s ES, kdy v důsledku pravolevého zkratu tento mechanismus selhává a infekční agens se snadno dostává do systémového arteriálního řečiště, mimo jiné i do mozkové tkáně. V důsledku chronické hypoxémie a vzniklé metabolické acidózy dochází ke vzniku mozkových oblastí s nízkou minutovou perfuzí [11], které spolu se zvýšenou viskozitou krve při kompenzatorní polycytémii představují predisponující podmínky pro vznik infekce. Stejně tak zhoršení metabolismu všech tkání vede k vyššímu riziku vzniku infekce v organismu, která se pak výše uvedenými mechanismy šíří do mozkové tkáně [10, 12].
U prezentovaného pacienta s původně levopravým zkratem došlo v průběhu let k nárůstu plicní cévní rezistence a vzniku ES [4]. Pátrání po zdroji možné septické embolizace však nepřineslo jednoznačnou odpověď. Ultrasonografické vyšetření cév pánve a dolních končetin neprokázalo trombózu. S tímto nálezem korelovala negativní hodnota D-dimerů a negativní genetické vyšetření nejčastějších trombofilních stavů. Stejně tak opakovaná echokardiografická vyšetření a MRI srdce nepotvrdila nález endokarditidy či přítomnost trombózy v srdci. Za nejpravděpodobnější příčinu lze vzhledem ke kultivačnímu nálezu S. intermedius (typický komenzál dutiny ústní) považovat přechodnou bakteriémii při hygieně dutiny ústní s následnou septickou embolizací. Provedené stomatologické vyšetření však jednoznačný infekční zdroj v dutině ústní neobjasnilo.
Pro úplnost uvádíme, že bylo provedeno extenzivní imunologické vyšetření k vyloučení imunodeficitu. Toto vyšetření prokázalo izolovanou poruchu komplementu (pro lektin vázající manózu, porucha v tzv. lektinové cestě aktivace komplementového systému), která může vést ke zvýšené infekční zranitelnosti včetně streptokokových infekcí [13]. Z tohoto důvodu byl pacient profylakticky zajištěn ko-trimoxazolem a bylo doporučeno doplnit očkování proti pneumokokům a meningokokům.
Etiologii přechodné trombocytopenie se zcela jasně nepodařilo určit. Za nejpravděpodobnější příčinu lze považovat možný nežádoucí účinek antibiotické léčby cefalosporinem (ceftriaxon-dinatricum) nebo treprostinilem. Právě u léčby treprostinilem se pokles trombocytů objevuje až u 1 % léčených pacientů [14].
U jednoduchých CHD s ES je možným řešením transplantace plic a kardiochirurgická korekce vady. Kombinovaná CHD s ES však představuje nejčastější indikaci k provedení transplantace bloku srdce a plic [15]. Úvaha o zařazení by podle obecných doporučení měla probíhat u pacientů s maximální farmakoterapií a předpokládanou délkou přežití méně než dva roky [16]. Rozhodnutí o správném načasování transplantace je však velmi obtížné, jedním z důvodů je velmi individuální prognóza pacientů s ES. V době zařazení na čekací listinu by měla být splněna následující kritéria: skupina NYHA (dle New York Heart Association) III–IV klinické klasifikace dušnosti, objektivní známky progredujícího srdečního selhání, srdeční index z pravostranné srdeční katetrizace <2 l/min/m2 s tlakem v pravé komoře >15 mmHg [16].
ZÁVĚR
V této kazuistice předkládáme případ pacienta s mnohočetnými mozkovými abscesy při primární diagnóze plicní arteriální hypertenze a Eisenmengerova syndromu, který poukazuje na několik aspektů: (1) důraz na celkové vyšetření při nově vzniklých obtížích i při méně typické symptomatologii, (2) široká diferenciální diagnostika bolestí hlavy, kdy je nutno v prvé řadě vyloučit příčiny sekundární, zejména u rizikových pacientů, (3) multidisciplinární přístup u pacientů s plicní arteriální hypertenzí, (4) výskyt neurologických komplikací u Eisenmengerova syndromu, (5) význam časné korekce srdečních vad s levopravým zkratem jako prevence rozvoje plicní arteriální hypertenze.
Došlo: 28. 11. 2019
Přijato: 3. 12. 2019
MUDr. Jan David, Ph.D.
Pediatrická klinika 2. LF UK
a Fakultní nemocnice Motol
V Úvalu 84
150 06 Praha
e-mail: jan.david@fnmotol.cz
Sources
1. Hansmann G, Koestenberger M, Alastalo TP, et al. 2019 updated consensus statement on the diagnosis and treatment of pediatric pulmonary hypertension: The European Pediatric Pulmonary Vascular Disease Network (EPPVDN), endorsed by AEPC, ESPR and ISHLT. J Heart Lung Transplant 2019; 38 (9): 879–901.
2. Mezinárodní databáze vzácných onemocnění. http://www.orpha.net.
3. Ivy D, Abman S, Barst R, et al. Pediatric pulmonary hypertension. J Am Coll Cardiol 2013; 62 (Suppl 25): D117–126.
4. Jansa P. Plicní arteriální hypertenze u vrozených srdečních vad. Interní Med 2006; 6 : 266–269.
5. Hansmann G. Pulmonary hypertension in infants, children, and young adults. J Am Coll Cardiol 2017; 69 (20): 2551–2569.
6. Aschermann M, et al. 2015 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Summary document prepared by the Czech Society of Cardiology. Cor et Vasa 2016; 58: e129–e152.
7. Pascall E, Tulloh RM. Pulmonary hypertension in congenital heart disease. Future Cardiol 2018; 14 (4): 343–353.
8. Kozlik-Feldmann R, Hansmann G, Bonnet D, et al. Pulmonary hypertension in children with congenital heart disease (PAH-CHD, PPHVD-CHD). Expert consensus statement on the diagnosis and treatment of paediatric pulmonary hypertension. The European Paediatric Pulmonary Vascular Disease Network, endorsed by ISHLT and DGPK. Heart 2016; 102 (Suppl 2): ii24–48.
9. Hjortshoj CS, Jensen AS, Sorensen K, et al. Epidemiological changes in Eisenmenger syndrome in the Nordic region in 1977–2012. Heart 2017; 103 (17): 1353–1358.
10. Hlavinová E, Zatočil T, Nečasová A, et al. Mozkový absces u atrezie plicnice s defektem komorového septa. Cor et Vasa 2018; 24–29.
11. Dogan F, Sen Dokumaci D, Yildirim A, et al. Brain diffusion changes in Eisenmenger syndrome. Br J Radiol 2016; 89 (1068): 20151007.
12. Frank DB, Hanna BD. Pulmonary arterial hypertension associated with congenital heart disease and Eisenmenger syndrome: current practice in pediatrics. Minerva Pediatr 2015; 67 (2): 169–185.
13. Skattum L, van Deuren M, van der Poll T, et al. Complement deficiency states and associated infections. Mol Immunol 2011; 48 (14): 1643–1655.
14. Kingman M, Archer-Chicko Ch, Bartlett M, et al. Management of prostacyclin side effects in adult patients with pulmonary arterial hypertension. Pulm Circ 2017; 7 (3): 598–608.
15. Le Pavec J, Hascoët S, Fadel W. Heart-lung transplantation: current indications, prognosis and specific considerations. J Thorac Dis 2018; 10 (10): 5946–5952.
16. Weill D, Benden C, Corris PA, et al. A consensus document for the selection of lung transplant candidates: 2014 - An update from the Pulmonary Transplantation Council of the International Society for heart and lung transplantation. J Heart Lung Transplant 2015; 34 : 1–15.
17. Galié N, McLaughlin VV, Rubin LJ, et al. An overview of the 6th World Symposium on Pulmonary Hypertension. Classification of pulmonary hypertension. Eur Respir J 2019; 53 (1): 1802148.
Labels
Neonatology Paediatrics General practitioner for children and adolescents
Article was published inCzech-Slovak Pediatrics

2020 Issue 3-
All articles in this issue
- Problematika oboru Gynekologie dětí a dospívajících – editorial
- Bolesti břicha u dívek v dětském a pubertálním období
- Krvácení z rodidel v dětském věku z pohledu dětského gynekologa
- Vrozené vývojové vady dělohy a pochvy – poruchy vývoje Müllerových vývodů a jejich derivátů – ultrazvuková diagnostika u dětí a dospívajících
- Rizikové faktory vzniku tromboembolické nemoci u mladistvých uživatelek hormonální antikoncepce
- Časná a pozdní morbidita a mortalita u dvojčat narozených mezi 24. a 36. gestačním týdnem v perinatologickém centru a mimo něj
- Hematopoietic stem cell transplantation in patients with chronic granulomatous disease in the Czech Republic and Slovakia (2007–2019)
- Vzťahová väzba a chronické ochorenie u detí
- Alkohol v rukách detí a mladistvých čoraz častejšie končí pobytom v nemocnici – skúsenosti z Bratislavy a okolia
- Eisenmengerův syndrom a jeho komplikace v dětském věku
- Význam a zloženie oligosacharidov materského mlieka
- Kontinuální monitorace glykémie (CGM) „ve velkém“ na letním dětském diatáboře
- Tomáš Garrigue Masaryk, prof. MUDr. Josef Švejcar, DrSc., a Martin
- MUDr. Petr Pešák – 70 let
- Profesor MUDr. Milan Šamánek, DrSc., FESC (*9. 5. 1931 – † 29. 4. 2020) – odchod legendy
- Zemřel prof. MUDr. Jaroslav Stejskal, DrSc.
- Czech-Slovak Pediatrics
- Journal archive
- Current issue
- Online only
- About the journal
Most read in this issue- Krvácení z rodidel v dětském věku z pohledu dětského gynekologa
- Bolesti břicha u dívek v dětském a pubertálním období
- Vrozené vývojové vady dělohy a pochvy – poruchy vývoje Müllerových vývodů a jejich derivátů – ultrazvuková diagnostika u dětí a dospívajících
- Eisenmengerův syndrom a jeho komplikace v dětském věku
Login#ADS_BOTTOM_SCRIPTS#Forgotten passwordEnter the email address that you registered with. We will send you instructions on how to set a new password.
- Career

