-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Vývoj poznatků o nemoci způsobené virem hepatitidy E
Current knowledge of hepatitis E virus related disease
Hepatitis E virus (HEV) infection is one of the most common causes of acute hepatitis worldwide. The Czech Republic is also a region with a natural occurrence of HEV genotype 3. Diseases caused by different genotypes have distinct clinical and epidemiological characteristics. In industrialized countries, numerous local animal reservoirs have been described and infection is considered to be zoonotic disease in these areas. The most significant route of transmission is through ingestion of insufficiently cooked meat of reservoir animals. In addition, numerous extrahepatic manifestations, even without dominant liver disease, and the possibility of chronic hepatitis in immunocompromised patients have been described. The review summarizes the current knowledge of HEV related disease and current approaches to the treatment of acute and chronic hepatitis E.
Keywords:
hepatitis E – treatment of acute/chronic HEV – virus hepatitis E (HEV) – management HEV in The Czech Republic
Autoři: Matúš Mihalčin; Petr Husa
Působiště autorů: Klinika infekčních chorob LF MU a FN Brno, pracoviště Bohunice
Vyšlo v časopise: Vnitř Lék 2019; 65(9): 564-569
Kategorie: Přehledné referáty
Souhrn
Infekce virem hepatitidy E (HEV) je jednou z nejčastějších příčin akutní hepatitidy celosvětově. Česká republika je taktéž regionem s přirozeným výskytem HEV genotypu 3. Onemocnění vyvolané různými genotypy má odlišené klinické i epidemiologické charakteristiky. V industrializovaných zemích byly popsány četné lokální zvířecí rezervoáry a infekce je v těchto oblastech považována za zoonózu, s nejvýznamnější cestou přenosu konzumací nedostatečně tepelně opracovaného masa rezervoárových zvířat. U infekce byly navíc popsány četné extrahepatální projevy, i bez dominujícího postižení jater, a taktéž možnost rozvoje chronické hepatitidy u imunokompromitovaných pacientů. Přehledový článek shrnuje aktuální poznatky o onemocnění jater a dalších orgánů způsobeném HEV a současné přístupy k léčbě akutní a chronické hepatitidy E.
Klíčová slova:
hepatitida E – léčba akutní/chronické HEV – management HEV v České republice – virus hepatitidy E (HEV)
Úvod
Historicky bylo první podezření na epidemickou non-A non-B hepatitidu vyjádřeno v Indii v roce 1978. Podezření, že se jedná o nový virus způsobující hepatitidu u lidí, bylo potvrzeno během epidemie hepatitidy se stejnými epidemiologickými rysy u jednotky sovětské armády působící v Afganistánu v roce 1983. Virus byl kompletně sekvenován až v roce 1991. Aktuálně je známo již 8 genotypů viru.
Epidemiologie
Většina infekcí probíhá v oblastech jižní Asie, Subsaharské Afriky a Střední Ameriky, v nichž bylo podle odhadu jen v roce 2005 nově nakaženo 20,1 milionu obyvatel [1]. V těchto endemických oblastech jednoznačně dominuje HEV genotypů 1 a 2 a k přenosu nákazy dochází fekálně-orální cestou. Příčinou epidemií jsou většinou kontaminované vodní zdroje. Ke kontaminaci zpravidla dochází při záplavách, při nichž se pitná voda smísí s odpadní vodou kontaminovanou fekáliemi lidí nebo zvířat.
Výskyt viru byl však v posledních letech prokázán téměř celosvětově. Mimo endemické oblasti, v tzv. oblastech se sporadickým výskytem, způsobuje onemocnění většinou genotyp 3, vzácně genotypy 4–8. Mechanizmus přenosu i klinické charakteristiky onemocnění jsou v těchto oblastech odlišné. Jedná se převážně o oblasti s vysokým hygienickým standardem a k přenosu viru dochází konzumací nedostatečně tepelně opracovaného masa zvířat, která představují rezervoár infekce. Zatím byl tento způsob přenosu prokázán u vepřového masa a jater, zvěřiny, mořských plodů, velbloudů a četných dalších savců. U těchto zvířat nelze vyloučit ani možnost přenosu přímým kontaktem a následnou ingescí virionů. Nakažena zvířata přitom nevykazuji projevy onemocnění. Malé procento infekcí vzniká vertikálním přenosem z matky na plod a krevními produkty. Interhumánní přenos má pouze zanedbatelný význam a mimo endemické oblasti se jedná maximálně o kazuistické případy. Je zvažována i možnost přenosu při transplantacích orgánů a při homosexuálním pohlavním styku partnerů mužského pohlaví [2]. Rozložení endemických oblastí a oblastí sporadického výskytu HEV ve světě zobrazuje obr. 1.
Obr. 1. Rozložení endemických oblastí a oblastí sporadického výskytu HEV ve světě 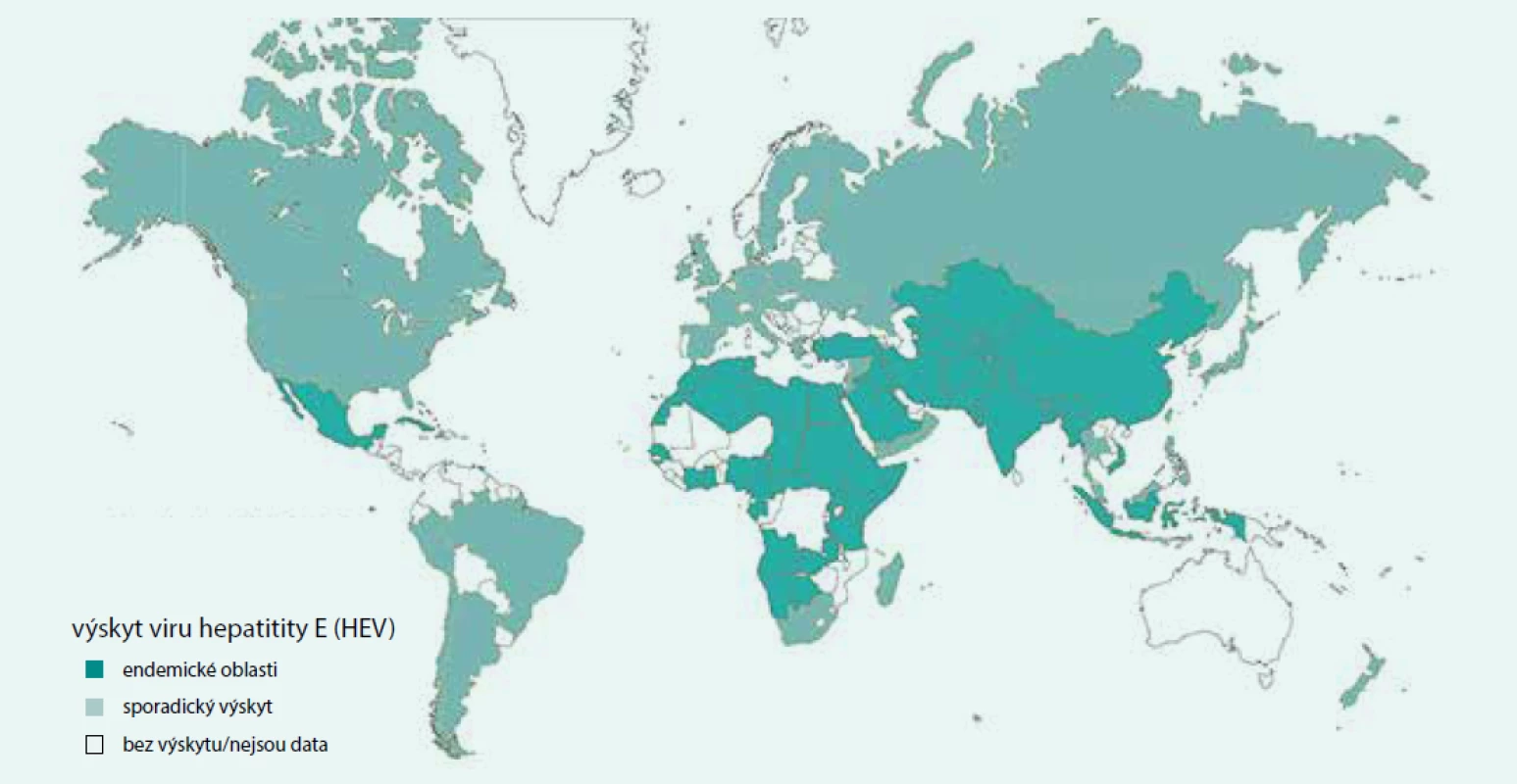
Stanovení celosvětové séroprevalence je obtížné. Podle studií v industrializovaných zemích byla pozitivita protilátek prokazována u 1–25 % populace [3]. Podle údajů z Epidatu, počet hlášených onemocnění akutní hepatitidou E v České republice v posledním desetiletí narůstá (graf 1) [4]. Průměrná incidence onemocnění v ČR v posledních letech dosahuje přibližně 3/100 000 obyvatel. Na území ČR byla doposud provedena jediná séroprevalenční studie, zjišťující přítomnost protilátek proti viru hepatitidy E. Jednalo se o séra náhodně vybraných osob ve věkové skupině 15–64 let z běžné populace v roce 2001. Celková séroprevalence v přehledu činila 6,7 %, přepočtená na počet osob v ČR pak 8,6 % [5]. Testováním stolice prasat domácích (Sus scrofa f. domestica) z 10 farem v ČR byla zjištěna pozitivita HEV u 5 % zvířat a u 4 % testovaných volně žijících prasat divokých (Sus scrofa) [6].
Graf 1. Hlášený výskyt virových hepatitid v České republice v Epidatu v letech 2004–2017. Upraveno podle [4] ![Hlášený výskyt virových hepatitid v České republice v Epidatu v letech 2004–2017. Upraveno podle [4]](https://pl-master.mdcdn.cz/media/image_pdf/da7af1cc81581e71b1d0813dd4394a97.png?version=1571426640)
Klinický průběh hepatitidy E
Inkubační doba nákazy HEV je u perorálně nakažených lidských dobrovolníků 4–5 týdnů s maximálním připouštěným intervalem 2–6 týdnů. Podle výzkumu na primátech je přímá souvislost mezi infekční dávkou a intenzitou onemocnění a inverzní vztah mezi infekční dávkou a inkubační dobou. Infekce probíhá ve většině případů asymptomaticky. Symptomatické případy se manifestují podobně jako akutní hepatitidy jiné etiologie a nelze je klinicky rozlišit. Může se objevit abdominální diskomfort, nauzea, subfebrilie, celková slabost či tlak v pravém podžebří. Poškození jater vzniká pravděpodobně na imunologickém podkladě. Výsledky laboratorního vyšetření vykazují v akutní fázi onemocnění vždy zvýšenou aktivitu sérové alaninaminotransferázy (ALT) spolu s aspartátaminotrasferázou (AST), která však u pacientů bez chronického onemocnění jater bývá nižší než ALT. Zachycené hodnoty se pohybují v závislosti na fáze infekce v jednotkách až desítkách µkat/l. Zvýšena hodnota sérového nekonjugovaného bilirubinu a ikterus bývají pozorovány u méně než poloviny případů. Aktivita sérové alkalické fosfatázy (ALP) a gamaglutamyltransferázy (GGT) bývá zvýšená nekonstantně. Symptomy odezní většinou v průběhu prvních 2 týdnů. Zvýšená aktivita sérových aminotransferáz trvá většinou do 4–6 týdnů, přičemž v typických případech bývá nejdéle pozorována zvýšena aktivita sérové GGT.
Z klinického pohledu lze nejčastější genotypy rozdělit do 2 skupin, které mají společné epidemiologické a klinické rysy. Genotypy HEV-1 a HEV-2, vyskytující se v endemických oblastech s teplým klimatem, vytváří odlišný obraz onemocnění než genotypy HEV-3 a HEV-4. Charakteristiky jednotlivých onemocnění uvádí tab. Genotypy HEV-5 až HEV-8 byly zatím popsány jen v jednotlivých případech.
Tab. 1. Charakteristiky onemocnění vyvolaného odlišnými genotypy HEV 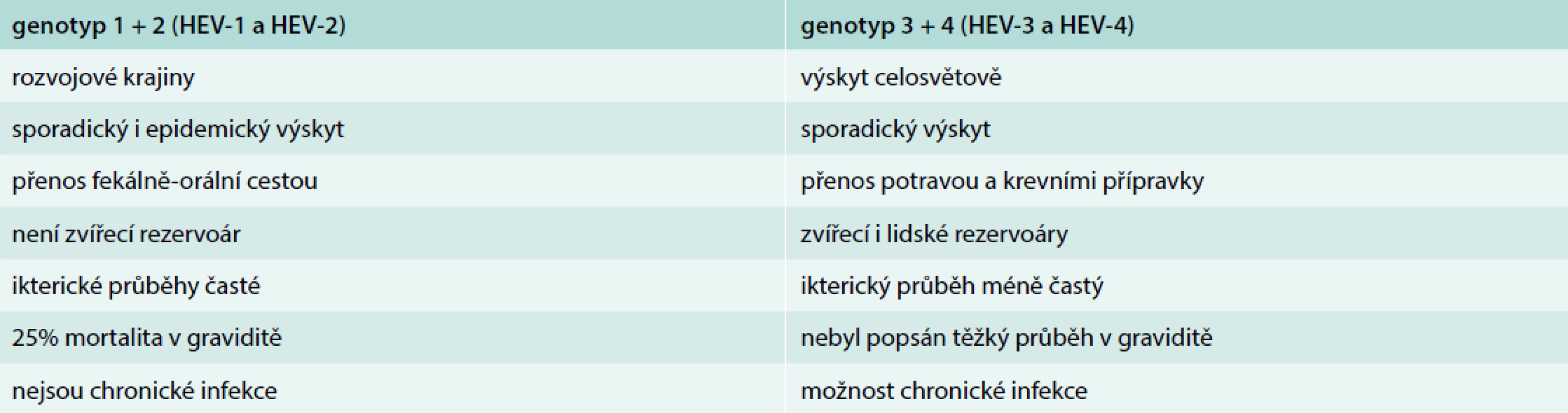
Těžší průběh nemoci je popisován u pacientů s preexistujícím onemocněním jater u všech genotypů HEV. Počáteční fáze infekce probíhá jako akutní hepatitida E u jinak zdravých pacientů, následně ale může dojít k dekompenzaci chronického onemocnění jater až jejích selhání a úmrtí.
V posledních letech byla popsána i chronická hepatitida E, která byla definována jako perzistence HEV RNA v séru nebo stolici a/nebo perzistence protilátek třídy IgM proti HEV v séru po dobu nejméně 6 měsíců společně s elevací jaterních enzymů v séru. Dochází k tomu u imunokompromitovaných pacientů. Nejrizikovější jsou pacienti po transplantaci orgánu nebo kmenových buněk (60 % přechází do chronicity), pacienti po chemoterapii pro hematologickou malignitu a pacienti infikovaní virem lidské imunitní nedostatečnosti (HIV) v pokročilém stadiu s počtem CD4-lymfocytů méně než 250 bb/mm3. Většina pacientů s chronickou hepatitidou je po odeznění akutní infekce bezpříznaková. Jen u části z nich v určité míře přetrvávají symptomy akutní infekce, jako je ikterus, únava, abdominální diskomfort nebo zvýšená teplota. Infekce však může vést k cirhóze a selhání jater.
V oblastech endemického výskytu HEV, je popisována mnohem vyšší tzv. attack rate (procento osob, ze všech exponovaných, které onemocněly) u těhotných žen, u kterých byl popisován i fulminantní průběh onemocnění. Vzhledem k výskytu tohoto jevu v oblastech endemických pro genotyp HEV-1 (tropické oblasti) se zatím uvažuje o spojitosti s tímto genotypem. V ČR nebyla pozorována u těhotných žen vyšší morbidita ani komplikace.
Extrahepatální manifestace
S přibývajícím počtem nově diagnostikovaných případů hepatitidy E v Evropě a Severní Americe byly popsány četné extrahepatální manifestace onemocnění. Mezi nejčastěji pozorované patří subakutní postižení nervového systému, především periferního, akutní pankreatitida, glomerulonefritida, smíšená kryoglobulinemie a trombocytopenie. Kauzální souvislost u jednotlivých projevů je aktuálně vyhodnocována. Jako mechanizmus vzniku postižení jsou zvažovány přímé poškození tkání množícím se virem nebo nepřímé poškození imunitně mediovaným mechanizmem (molekulární mimikry nebo poškození tkání depozici komplexů virus-protilátka).
Doposud popsané případy neurologického postižení v souvislosti s hepatitidou E patřily do genotypů 1 a 3. Nejčastěji se jednalo o syndrom Guillainův-Barréův (GBS) a oboustrannou neuralgickou amyotrofii, u kterých je souvislost s infekci HEV považovaná za velmi pravděpodobnou [7,8]. Guillainův-Barréův syndrom je autoimunitní onemocnění postihující periferní nervovou soustavu. Podkladem je akutní zánětlivá demyelinizační polyneuropatie (Acute Inflammatory Demyelinating Polyneuropathy – AIDP) vzniklá na podkladě zkřížené reaktivity lidských a mikrobiálních antigenních epitopů. Projevuje se jako chabá paréza s hyporeflexií až areflexií, která typicky začíná na dolních končetinách a postupuje ascendentně v průběhu hodin až týdnů. Může být přítomná porucha čití a rovnováhy a taktéž pocit parestezií končetin. Neuralgická amyotrofie, v anglosaské literatuře používáno též eponymum Parsonage-Turner syndrom, je idiopatická periferní neuropatie většinou v oblasti brachiálního plexu způsobující multifokální parézu a senzorickou poruchu. Stav se manifestuje jako silná akutně vzniklá bolest ramene, lopatky, ale i krku, paže a předloktí. Motorický deficit se obvykle rozvíjí při zmírnění bolestí. Vzniká slabost s omezením pohybu v postižených oblastech a postupně i svalová atrofie. Postižení trvá několik hodin až několik měsíců [9]. Pro malý počet případů zatím nelze jednoznačně definovat souvislost dalších neurologických projevů. Během infekce HEV byly popsány i případy meningoradikulitidy, mononeuritis multiplex, Bellovy obrny, vestibulární neuritidy a periferní neuropatie malých vláken [7].
O souvislosti postižení ledvin během infekce virem HEV existuji důkazy odvozené z laboratorních experimentů i na základě klinických observací. Většina z doposud publikovaných případů byla zaznamenána u imunokompromitovaných pacientů. Patogeneze postižení je připisována imunitně podmíněným mechanizmům, podobně jak u glomerulárního postižení u chronické hepatitidy C nebo hepatitidy B [10,11].
Akutní pankreatitida je popisovanou komplikací u všech virových hepatitid, většinou u infekcí s fulminantním průběhem. Oproti tomu, případy pankreatitidy popsané u hepatitidy E nevznikly u pacientů s fulminantním selháním jater. Všechny doposud publikované případy proběhly u pacientů nakažených v jižní Asii [10,11].
Souvislost různých hematologických projevů a smíšené kryoglobulinemie s infekci HEV je zatím považována za možnou, malé soubory popsaných případů ale neumožňují asociaci potvrdit [10,11].
Diagnostika
Diagnóza akutní infekce se zakládá na průkazu přítomnosti protilátek třídy IgM proti HEV v séru metodou ELISA (Enzyme-Linked ImmunoSorbent Assay). Pozitivita se objevuje 1–4 dny po nástupu symptomů a trvá přibližně 4–6 měsíců. Vzestup hladiny protilátek třídy IgG následuje téměř současně s tvorbou protilátek IgM a jejich hladina kulminuje během nejvyšší aktivity aminotransferáz v séru. V séru jsou pak detekovatelné roky a zřejmě zajišťují ochranu před případnou další infekcí HEV. Podle různých studií není ale senzitivita komerčních testů ELISA uspokojivá. Nezávislé práce udávají senzitivitu 79 % a 59,6 % a specificitu 90 % a 77,5 % [12,13]. Přímý průkaz HEV RNA v séru nebo ve stolici pomocí reverzně-transkriptní polymerázové řetězové reakce (reverse-transcriptase polymerase chain reaction – RT-PCR) se doporučuje jako konfirmační metoda v nejasných případech a jako metoda volby u imunokompromitovaných pacientů, u kterých může být tvorba specifických anti-HEV protilátek opožděná. Konfirmaci lze doporučit zejména v případech, kdy se zvažuje zavedení antivirové léčby. Ve stolici i v séru je u většiny pacientů virus detekovatelný již 6. den po infekci (i 2 týdny před nástupem symptomů) a mizí postupně při vzestupu aktivity aminotransferáz a s tvorbou protilátek proti HEV. V krvi se virus objevuje dříve než ve stolici, je však detekovatelný kratší dobu [14]. Dostupnost vyšetření HEV RNA metodou PCR ze stolice je v ČR ale omezená. Vyšetření protilátek metodou western blot může teoreticky zvýšit specificitu sérologického vyšetření, u imunokompromitovaných pacientů může ale být negativní a přednost se proto dává metodě PCR. Dynamiku titru protilátek v séru, virové nálože v séru a stolici a hodnoty alaninaminotransferázy v séru během infekce HEV znázorňuje graf 2.
Graf 2. Dynamika hodnoty alaninaminotransferázy (ALT) v séru, titru protilátek (IgM anti-HEV, IgG anti-HEV) v séru a virové nálože v séru a stolici během infekce HEV 
Terapie
Akutní hepatitida E ve většině případů nevyžaduje protivirovou léčbu a téměř ve všech případech dojde spontánně k eliminaci viru. Pacienti s preexistujícím onemocněním jater, v našich podmínkách nejčastěji s cirhózou toxonutritivní etiologie, mohou progredovat do fulminantního selhání jater. V těchto případech lze uvažovat o medikamentózním ovlivnění průběhu nemoci ještě před rozvojem selhání funkce jater. Dalšími situacemi, v nichž hrozí riziko trvalých následků v případě trvání virové infekce, jsou chronická hepatitida E u imunokompromitovaných pacientů a akutní či chronické infekce se závažnými extrahepatálními komplikacemi.
Evropská asociace pro studium jater (European Association for the Study of the Liver – EASL) vydala letos doporučený postup pojednávající o diagnostice a léčbě hepatitidy E [2]. Následující doporučení jsou výsledkem konsenzu vzniklého z dostupných zkušeností s léčbou.
Za lék volby je považován ribavirin. Jedná se nukleosidový analog používaný k léčbě hepatitidy typu C. Mechanizmus jeho účinku nebyl doposud dostatečně vysvětlen. Zvažována je inhibice replikace HEV přes depleci guanosin trifosfátu (GTP). Indikace ribavirinu jsou momentálně omezeny na pacienty s těžkým průběhem akutní hepatitidy E a na případy dekompenzace chronického jaterního onemocnění při infekci virem hepatitidy E. Zatím nebyla stanovena doporučena dávka ribavirinu ani délka podávání. Byly publikovány i případy úspěšného použití kortikoidů u akutního selhávání funkce jater. Aktuálně ale není dostatek důkazů k doporučení použití kortikoidů k léčbě akutního selhání jater u infekce HEV.
V případech chronické hepatitidy E je jako první léčebný krok doporučeno snížit úroveň imunosuprese, co postačuje přibližně u 1/3 pacientů. U pacientů s 3 měsíce prokazatelnou HEV RNA v séru i po snížení úrovně imunosuprese, je doporučeno zavést léčbu ribavirinem na 12 týdnů. Při trvání virémie lze podávání ribavirinu prodloužit, přidat pegylovaný interferon α a eventuálně změnit základní imunosupresivní terapii. Detailní postup léčby chronické hepatitidy E je mimo rozsah tohoto přehledu a zájemce lze odkázat na přehledové práce [2,15,16].
Existuje řada podpůrných léků a potravinových doplňků již desetiletí používaných k rychlejší úpravě hodnot aktivity jaterních enzymů, jak u akutních, tak u chronických nemocí jater. Mechanizmus účinku těchto látek se většinou vztahuje k jejich antioxidační aktivitě. U některých byla prokázána částečná účinnost, chybí však randomizované, dobře designované, studie, které by případně mohly vést k doporučení jejich užití [17,18].
Prevence
Závěry studií na buněčných kulturách naznačují, že virus ztrácí infektivitu po působení teploty 70 °C déle než 2 min a 80 °C déle než 1 min. Naproti tomu, možnost vyvolat nákazu byla prokázána při působení pokojové teploty i po 28 dnech [19]. Význam těchto observací pro možnost přenosu infekce jídlem zůstává však nejasný. Přenos infekce konzumací nedostatečně tepelně opracovaného vepřového masa, masa z divočáka nebo vysoké zvěře, byl Evropě opakovaně potvrzen. Lze proto doporučit vyhýbat se takovým pokrmům osobám s rizikem těžké akutní nebo chronické infekce HEV.
Vzhledem k prokázanému přenosu infekce transfuzemi krve nebo krevních derivátů v mnoha evropských zemích je možnost prevence této cesty přenosu námětem pro diskusi. Většina postransfuzních infekcí je sice asymptomatických, u rizikových příjemců krve však může dojít k rozvoji chronické hepatitidy E nebo fulminantní hepatitidy [2].
V roce 2011 byla v Číně licencována vakcína proti HEV. Její účinnost proti rozvoji akutní symptomatické hepatitidy je 97% a předpokládá se její pangenotypové působení. Dosavadní informace svědčí pro její bezpečnost v těhotenství [20]. Nemáme ale dostatek informací o její protektivitě u nejrizikovějších pacientů s chronickým onemocněním jater a u imunosuprimovaných pacientů.
Závěr
V diferenciální diagnostice příčin akutního zhoršení funkce jater v ČR patří hepatitida E na první místa. Většina infekcí HEV má anikterický průběh a může se klinicky manifestovat extrahepatálním projevem, nejčastěji různou periferní neurologickou symptomatologii. Přítomnost protilátek proti HEV je proto nutné vyšetřit u všech pacientů s obrazem akutní hepatitidy, u pacientů s nevysvětlitelným zhoršením chronického onemocnění jater, u imunokompromitovaných pacientů s nevysvětlitelnou chronickou hepatopatií a u pacientů s hepatopatií vzniklou po transfuzi krve. Taktéž u pacientů s neuralgickou amyotrofií, Guillainovým-Barréovým syndromem a encefalomyelitidou, i bez zvýšené aktivity aminotransferáz v séru, je vhodné zvážit vyšetření na možnost probíhající infekce virem hepatitidy E. Při hodnocení výsledku testu ELISA je nutno zohlednit relativně vysokou četnost falešně pozitivních výsledků a zejména v případech, v nichž výsledek mění diagnosticko-terapeutický postup, doplnit vyšetření PCR HEV RNA ze séra nebo stolice, popřípadě vyšetření ELISA s odstupem konfirmovat.
Podpořeno z programového projektu Ministerstva zdravotnictví ČR s reg. č. 17–31921A
MUDr. Matúš Mihalčin
Klinika infekčních chorob LF MU a FN Brno, pracoviště Bohunice
Doručeno do redakce 16. 10. 2018
Přijato po recenzi 17. 4. 2019
Zdroje
- Rein DB, Stevens GA, Theaker J et al. The global burden of hepatitis E virus genotypes 1 and 2 in 2005. Hepatol Baltim Md 2012; 55(4): 988–997. Dostupné z DOI: <http://doi: 10.1002/hep.25505>.
- [European Association for the Study of the Liver]. EASL Clinical Practice Guidelines on hepatitis E virus infection. J Hepatol 2018; 68(6): 1256–1271. Dostupné z DOI: <http://doi: 10.1016/j.jhep.2018.03.005>.
- Arends J, Ghisetti V, Irving W et al. Hepatitis E: An emerging infection in high income countries. J Clin Virol 2014; 59(9): 81–88. Dostupné z DOI: <http://doi: 10.1016/j.jcv.2013.11.013>.
- Vybrané infekční nemoci v ČR v letech 2008–2017 – relativně, SZÚ. Dostupné z WWW: <http://www.szu.cz/publikace/data/vybrane-infekcni-nemoci-v-cr-v-letech-2008–2017-relativne>.
- Němeček V, Butovičová P, Malý M et al. The prevalence of antibodies against Hepatitis E Virus in the Czech Republic: serological survey. Epidemiol Mikrobiol Imunol 2017; 66(1): 3–7.
- Kubankova M, Kralik P, Lamka J et al. Prevalence of Hepatitis E Virus in Populations of Wild Animals in Comparison with Animals Bred in Game Enclosures. Food Environ Virol 2015; 7 : 159–163. Dostupné z DOI: <http://doi 10.1007/s12560–015–9189–1>.
- Pischke S, Hartl J, Pas SD et al. Hepatitis E virus: Infection beyond the liver? J Hepatol 2017; 66(5): 1082–1095. Dostupné z DOI: <http://doi: 10.1016/j.jhep.2016.11.016>.
- Kamar N, Marion O, Abravanel F et al. Extrahepatic manifestations of hepatitis E virus. Liver Int Off J Int Assoc Study Liver 2016; 36(4): 467–472. Dostupné z DOI: <http://doi: 10.1111/liv.13037>.
- van Eijk JJ, Madden RG, van der Eijk AA et al. Neuralgic amyotrophy and hepatitis E virus infection. Neurology 2014; 82(6): 498–503. Dostupné z DOI: <http://doi: 10.1212/WNL.0000000000000112>.
- Negro F, Forton D, Craxì A et al. Extrahepatic morbidity and mortality of chronic hepatitis C. Gastroenterology 2015; 149(6): 1345–1360. . Dostupné z DOI: <http://doi: 10.1053/j.gastro.2015.08.035>.
- Haffar S, Bazerbachi F, Lake JR. HEV-associated cryoglobulinaemia and extrahepatic manifestations of hepatitis E. Lancet Infect Dis 2015; 15(3): 268. Dostupné z DOI: <http://doi: 10.1016/S1473–3099(15)70034–4>.
- Pas SD, Streefkerk RH, Pronk M et al. Diagnostic performance of selected commercial HEV IgM and IgG ELISAs for immunocompromised and immunocompetent patients. J Clin Virol Off Publ Pan Am Soc Clin Virol 2013; 58(4): 629–634. Dostupné z DOI: <http://doi: 10.1016/j.jcv.2013.10.010>.
- Avellon A, Morago L, Garcia-Galera MDC et al. Comparative sensitivity of commercial tests for hepatitis E genotype 3 virus antibody detection. J Med Virol 2015; 87(11): 1934–1939. Dostupné z DOI: <http://doi: 10.1002/jmv.24251>.
- Panda SK, Varma SP. Hepatitis E: Molecular Virology and Pathogenesis. J Clin Exp Hepatol 2013; 3(2): 114–124. Dostupné z DOI: <http://doi: 10.1016/j.jceh.2013.05.001>.
- Peters van Ton AM, Gevers TJG, Drenth JPH. Antiviral therapy in chronic hepatitis E: a systematic review. J Viral Hepat 2015; 22(12): 965–973. Dostupné z DOI: <http:// doi: 10.1111/jvh.12403>.
- Kamar N, Izopet J, Tripon S et al. Ribavirin for chronic hepatitis E virus infection in transplant recipients. N Engl J Med 2014; 370(12): 1111–1120. Dostupné z DOI: <http://doi: 10.1056/NEJMoa1215246>.
- Ferenci P. Silymarin in the treatment of liver diseases: What is the clinical evidence? Clin Liver Dis 2016; 7(1): 8–10. Dostupné z DOI: <http://doi: 10.1002/cld.522>.
- Mihalčin M, Fašaneková L et al. Aktuální pohled na epidemiologii a přístupy k léčbě virových hepatitid A a E. Klin Farmakol Farm 2017; 31(1): 15–18.
- Johne R, Trojnar E, Filter M et al. Thermal Stability of Hepatitis E Virus as Estimated by a Cell Culture Method. Appl Environ Microbiol 2016; 82(14): 4225–4231. Dostupné z DOI: <http:// doi: 10.1128/AEM.00951–162>.
- Wu T, Zhu FC, Huang SJ et al. Safety of the hepatitis E vaccine for pregnant women: a preliminary analysis. Hepatol Baltim Md 2012; 55(6): 2038. Dostupné z DOI: <http://doi: 10.1002/hep.25522>.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek Z odborné literaturyČlánek errata et corrigenda
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2019 Číslo 9- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
-
Všechny články tohoto čísla
- Hepatologie – úvod do problematiky
- Neinvazivní diagnostika jaterních chorob – zobrazovací metody
- Současný pohled na diagnostiku a léčbu hepatitidy B
- Pangenotypové režimy léčby chronické hepatitidy C
- Vývoj poznatků o nemoci způsobené virem hepatitidy E
- Nealkoholové postižení jater při steatóze
- Sérové markery v diagnostice nealkoholické steatohepatitidy
- Rizikové faktory a surveillance hepatocelulárního karcinomu
- Transplantace jater – vývoj indikací v poslední dekádě
- Z odborné literatury
- errata et corrigenda
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Neinvazivní diagnostika jaterních chorob – zobrazovací metody
- Vývoj poznatků o nemoci způsobené virem hepatitidy E
- Nealkoholové postižení jater při steatóze
- Současný pohled na diagnostiku a léčbu hepatitidy B
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



