-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Význam stanovení hladiny hepcidinu v diagnostice vybraných typů anémií v dětském věku
Significance of hepcidin level assessment in the diagnosis of selected types of anaemia in childhood
Introduction.
The peptide hormone hepcidin is the principal factor regulating iron homeostasis. It ensures communication between sites where iron is stored (hepatocytes and macrophages) and sites where it is absorbed (enterocytes), utilised (erythroid cells) or recycled and released into the bloodstream (macrophages). Hepcidin synthesis is regulated by signals responding to inflammation, erythropoietic activity, iron level, iron stores in the organism and oxygen tension. An increase in hepcidin levels leads to iron retention in enterocytes and macrophages and to a fall in iron plasma levels.Objective.
To assess hepcidin levels and their diagnostic contribution in paediatric patients with selected types of anaemia: Diamond-Blackfan anaemia (DBA), pyruvate kinase deficiency (PK), iron deficiency anaemia (IDA) and anaemia in inflammatory bowel disease (IBD).Patients and Methods.
Hepcidin levels were assessed in 33 children using the proteomic analysis method – 17 boys and 16 girls (6 patients with DBA, 5 patients with PK deficiency, 10 patients with IDA and 12 patients with IBD) aged 6 months–18 years. Hepcidin levels were compared to those in a cohort of 16 healthy children examined prior to the planned surgical interventions.Results.
Hepcidin levels in patients with severe forms of DBA are significantly higher than those in the controls (p<0.0005) despite high erythropoietin levels. The high hepcidin levels in DBA patients represent a completely different finding, compared to patients with thalassemia. This is likely to be caused by the absence of an “erythroid regulator” associated with severely reduced erythropoiesis. On the contrary, hepcidin levels in patients with PK deficiency are significantly lower (p<0.02), which theoretically corresponds to erythropoiesis acceleration. This theory is also supported by the increased level of the potential erythroid regulator of hepcidin production: GDF15. Low hepcidin levels may contribute to greater iron overload in these patients. In patients with IDA, significantly lower hepcidin levels (p<0.01) are found; they are likely to express the organismęs increased iron-demands. Surprisingly, no significant difference between hepcidin levels in patients with IBD and the controls was observed. In paediatric patients with IBD, true iron deficiency probably prevails over the characteristic presentation of anaemia of chronic disease.Conclusion.
Determination of hepcidin levels may help in the more accurate diagnosis of a whole range of anaemias by providing information on the current status of iron metabolism. It may provide important information not only regarding the current deficiency of iron required for erythropoiesis and the degree of iron overload, but also regarding the current capacity of enterocytes to absorb iron from the intestinal lumen. It may be useful as a guide for making decisions regarding the indication of oral and parenteral iron application. Hepcidin levels, in correlation with those of other proteins involved in the regulation of iron metabolism, may bring very important insights into aspects of iron homeostasis that are as yet unclear.Key words:
hepcidin, proteomic analysis, iron deficiency anaemia, anaemia of chronic diseases, inflammatory bowel disease, Diamond-Blackfan anaemia, pyruvate kinase deficiency.
Autoři: D. Pospíšilová 1; J. Houda 1; D. Holub 2
; B. Ludíková 1; R. Mojzíková 3; P. Pospíšilová 3; Z. Židová 3; K. Kapraľová 3; M. Horváthová 3; M. Hajdúch 2
; P. Džubák 2
Působiště autorů: Dětská klinika, Lékařská fakulta Univerzity Palackého v Olomouci a Fakultní nemocnice Olomouc 1; Ústav molekulární a translační medicíny, Lékařská fakulta Univerzity Palackého v Olomouci 2; Ústav biologie, Lékařská fakulta Univerzity Palackého v Olomouci 3
Vyšlo v časopise: Transfuze Hematol. dnes,18, 2012, No. 2, p. 58-65.
Kategorie: Souhrnné práce, původní práce, kazuistiky
Souhrn
Úvod.
Peptidický hormon hepcidin je hlavním faktorem ovlivňujícím homeostázu železa (Fe). Zajišťuje komunikaci mezi místy střádání Fe (hepatocyty a makrofágy) a místy, kde se Fe vstřebává (enterocyty), spotřebovává (erytroidní buňky) nebo recykluje a uvolňuje do krevního oběhu (makrofágy). Syntéza hepcidinu je regulována signály reagujícími na zánět, aktivitu erytropoézy, hladinu Fe, jeho zásoby v organismu a tenzi kyslíku. Zvýšení hladiny hepcidinu vede k zadržení Fe v enterocytech a makrofázích a snížení jeho hladiny v plazmě.Cíl práce.
Zhodnotit hladiny hepcidinu a jejich diagnostický přínos u dětských pacientů s vybranými typy anémií: Diamondovou-Blackfanovou anémií (DBA), deficitem pyruvátkinázy (PK), sideropenickou anémií (IDA) a anémií doprovázející střevní záněty (IBD).Pacienti a metody.
Hladina hepcidinu byla vyšetřena metodou proteomické analýzy u 33 dětí – 17 chlapců a 16 dívek (6 pacientů s DBA, 5 pacientů s deficitem PK, 10 pacientů se IDA a 12 pacientů s IBD) ve věku 6 měsíců až 18 let. Hladiny byly srovnávány se souborem 16 zdravých dětí vyšetřených před plánovanými chirurgickými výkony.Výsledky.
U pacientů s těžkou formou DBA jsou hladiny hepcidinu signifikantně vyšší než u kontrol (p < 0,0005) i přes vysoké hladiny erytropoetinu, což je zcela rozdílný nález ve srovnání s pacienty s talasemií. Příčinou je pravděpodobně absence „erytroidního regulátoru“ při těžké redukci erytropoézy. U pacientů s deficitem PK je hladina hepcidinu naopak signifikantně nižší (p < 0,02), což teoreticky odpovídá akceleraci erytropoézy. Pro tuto teorii svědčí i zvýšená hladina potenciálního erytroidního regulátoru produkce hepcidinu: GDF15. Nízká hladina hepcidinu může přispívat k prohloubení přetížení Fe u těchto pacientů. U pacientů se IDA byly nalezeny signifikantně nižší hladiny (p < 0,01) hepcidinu, které jsou pravděpodobně výrazem zvýšené poptávky organismu po Fe. Mezi hladinami hepcidinu u pacientů s IBD a kontrolami nebyl překvapivě zjištěn signifikantní rozdíl. U dětských pacientů s IBD pravděpodobně převažuje skutečný deficit Fe nad klasickým obrazem anémie chronických chorob.Závěr.
Stanovení hladin hepcidinu může zpřesnit diagnostiku celé řady anémií informací o aktuálním stavu metabolismu železa. Může poskytnout nejen důležitou informaci o aktuálním deficitu železa pro potřeby erytropoézy, stupni přetížení železem, ale i o aktuální schopnosti enterocytů vstřebávat Fe ze střevního lumen. Může být vodítkem při rozhodnutí o indikacích perorální a parenterální aplikace železa. Znalost hladiny hepcidinu může při korelaci s hladinami ostatních proteinů účastnících se regulace metabolismu Fe přinést velmi důležité poznatky o dosud nejasných aspektech homeostázy Fe v organismu.Klíčová slova:
hepcidin, proteomická analýza, sideropenická anémie, anémie chronických chorob, nespecifické střevní záněty, Diamondova-Blackfanova anémie, deficit pyruvátkinázyÚvod
Železo (Fe) jako čtvrtý nejrozšířenější element zemské kůry patří mezi prvky nezbytné pro růst a přežití organismu. Je jednou ze základních stavebních a funkčních složek molekul zajišťujících transport kyslíku – hemoglobinu a myoglobinu, mimoto je nezbytné pro funkci řady důležitých enzymů: kataláz, akonitáz, ribonukleotid – reduktázy, peroxidáz a cytochromoxidáz, které se účastní důležitých reakcí oxidativního metabolismu a buněčného růstu a proliferace. Schopnost železa katalyzovat redox-reakce může na druhé straně při jeho nadbytku vést ke vzniku toxických hydroxylových radikálů, které mohou poškozovat buňky a tkáně. Nedostatek i nadbytek železa je ve svých důsledcích pro organismus škodlivý. Koncentrace železa v plazmě a extracelulární tekutině je proto udržována v poměrně úzkém rozmezí, které zajišťuje adekvátní přísun železa nutný pro zachování všech buněčných pochodů bez rizika jeho toxicity (1). Homeostáza železa v organismu je velmi precizně regulována systémy, které zajišťují kontrolu potřebné koncentrace železa v buňkách, plazmě a v extracelulárních tekutinách.
Většina genů, jejichž proteinové produkty hrají důležitou roli v metabolismu Fe, byla identifikována v posledních 10 letech. Hlavním faktorem ovlivňujícím homeostázu železa v organismu je peptidický hormon hepcidin. Poprvé byl popsán v roce 2001 (2), a to původně jako peptid s antimikrobiální aktivitou, později byla objasněna jeho klíčová role v metabolismu železa. Primárně je syntetizován v hepatocytech jako pre-prohepcidin s 84 aminokyselinami, který je postupně přes prohepcidin konvertován signálními peptidázami a posttranslačně upravován konvertázou furinem (3) na bioaktivní peptid s 25 aminokyselinami, který hraje klíčovou roli v regulaci homeostáze Fe (4, 5). Je rychle vylučován z organismu.
Hepcidin je signální molekulou zprostředkující komunikaci mezi místy střádání Fe (hepatocyty a makrofágy) a místy, kde se Fe vstřebává (enterocyty), spotřebovává (erytroidní buňky) nebo recykluje a uvolňuje do krevního oběhu (makrofágy). Má funkci hlavního negativního regulátoru uvolňování železa z enterocytů duodena, z makrofágů a z hepatocytů. Zvýšení hladiny hepcidinu vede k blokádě exportu Fe z uvedených buněk, která je umožněna vazbou hepcidinu na feroportin. Feroportin, hlavní bílkovina zajišťující export Fe z buněk (6), je po vazbě hepcidinu internalizován a degradován a ztrácí tak schopnost exportovat Fe do plazmy. Výsledkem je zadržení železa v enterocytech a makrofázích a snížení jeho hladiny v plazmě. Protože možnosti exkrece Fe z organismu jsou výrazně limitovány, je kontinuální homeostáza železa zajišťována kontrolou střevní absorpce v enterocytech regulovanou právě hepcidinem a jeho vlivem na feroportin. Při poklesu zásob Fe se hladina hepcidinu snižuje a absorpce Fe zvyšuje, při doplnění zásob Fe dochází ke zvýšení hladiny hepcidinu vedoucí k degradaci feroportinu a poklesu absorpce Fe.
Syntéza hepcidinu je regulována signály reagujícími na zánět, aktivitu erytropoezy, hladinu Fe a jeho zásoby v organismu a tenzi kyslíku (7). Zánět, zvýšená hladina Fe v krvi nebo zvýšené zásoby Fe v organismu stimulují produkci hepcidinu, zatímco nedostatek Fe, hypoxie a zvýšení erytropoetické aktivity se zvýšenou potřebou přísunu Fe produkci hepcidinu tlumí.
Erytropoetická aktivita má přitom na expresi hepcidinu pravděpodobně větší vliv než stav zásob Fe v organismu (7). Konkrétní faktory suprimující produkci hepcidinu však nebyly dosud kompletně popsány. Pouze u některých anémií doprovázených neefektivní erytropoézou bylo prokázáno, že zvýšená hladina růstového diferenciačního faktoru 15 (growth differentiation factor 15, GDF15) koreluje se sníženou hladinou hepcidinu (8). Hierarchie a vzájemná souhra jednotlivých regulačních systémů je dosud stále předmětem intenzivního výzkumu.
Řada vrozených i získaných anémií je přímo způsobena nebo pouze doprovázena narušeným metabolismem železa, což se může různým způsobem odrážet v hladině hepcidinu. Změny hladiny hepcidinu mohou být tedy jak vlastní příčinou, tak častěji následkem změn, které vedou k anémii a deficitu Fe v organismu nebo naopak k jeho akumulaci v buňkách a tkáních s rozvojem přetížení organismu železem.
Metody vyšetření hladin hepcidinu v krvi a moči mají zatím svá logistická i technická úskalí. Pouze společnost Intrinsic LifeSciences (Los Angeles, USA) má k dispozici vlastní standardizovanou ELISA metodu ke stanovení hladiny hepcidinu, jejíž validita byla ověřena v několika publikovaných studiích (9, 10, 11). Tato společnost se zabývá komerčním měřením hladiny hepcidinu, které je používáno spíše pro účely výzkumu. Zbývající dostupné komerční ELISA diagnostické soupravy nejsou dostatečně prověřené a ne všechny měří hladinu výhradně biologicky aktivního hepcidinu-25. Metoda vyšetření hladin hepcidinu pomocí hmotnostní spektrometrie odráží specificky pouze hepcidin-25, je však velmi technicky pracná a vyžaduje vyšší finanční nároky a vysoce sofistikované přístrojové vybavení. Výsledky jsou tedy přesnější, metoda je však zatím méně praktická pro rutinní klinické použití. Hlavním problémem při hodnocení hladin hepcidinu v dětském věku je mimo jiné i absence údajů o normálních hodnotách pro dětský věk.
Cílem práce bylo stanovit hladiny hepcidinu u dětských pacientů s vybranými typy anémií, definovat roli hepcidinu v patogenezi těchto onemocnění, jeho diagnostický význam a shrnout nejnovější informace o možném terapeutickém využití jeho agonistů a antagonistů u jednotlivých poruch metabolismu Fe ve světle současných poznatků.
Obr. 1. Regulace systémové homeostázy železa (Fe) hepcidinem. 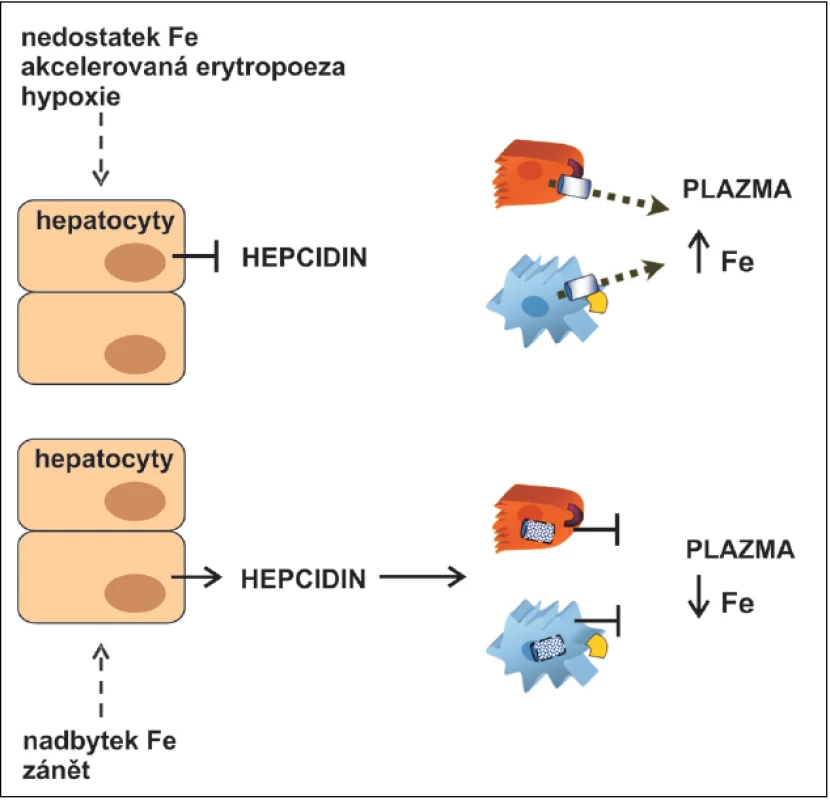
Pacienti a metody
Vyšetření hladin hepcidinu bylo provedeno u dětských pacientů se čtyřmi typy anémií, a to u dvou dobře definovaných vrozených defektů erytropoézy a dvou nejčastěji se vyskytujících typů získané anémie v dětském věku:
- Diamondovy-Blackfanovy anémie (DBA)
- hereditárních enzymopatií – deficitu glukózo-6 fosfátdehydrogenázy (G-6PD) a pyruvátkinázy (PK)
- sideropenické anémie (iron deficiency anaemia, IDA)
- anémie doprovázející nespecifické střevní záněty (inflammatory bowel diseases, IBD).
Hladiny hepcidinu byly stanoveny celkem u 33 dětských pacientů (16 dívek a 17 chlapců) ve věku 6 měsíců až 18 let s uvedeným typem anémie a u 16 zdravých kontrol. Do souboru bylo zahrnuto 6 pacientů s DBA, 5 pacientů s hereditární enzymopatií, 10 pacientů se IDA a 12 pacientů s anémií doprovázející IBD. U všech pacientů bylo po vyšetření kompletního krevního obrazu (analyzátor Sysmex XE-500) provedeno vyšetření sérových ukazatelů metabolismu železa: hladiny Fe v séru, celkové vazebné kapacity pro Fe (CVK), hladiny feritinu a s výjimkou pacientů s DBA i solubilního transferinového receptoru (sTfR). K biochemickým analýzám byly použity standardní vyšetřovací postupy. Diagnóza u pacientů s DBA a deficitem PK byla potvrzena molekulárně-genetickou analýzou s průkazem kauzálních mutací.
Vzhledem k tomu, že zatím neexistují normy hladin hepcidinu pro dětský věk, byly ke stanovení korelací hladin hepcidinu mezi pacienty s anémií a zdravou dětskou populací použity hladiny hepcidinu stanovené v souboru 16 zdravých dětí ve věku 8 měsíců až 18 let s normálními hodnotami krevního obrazu, které byly vyšetřeny v rámci plánovaného operačního výkonu (pupeční kýla, tříselná kýla, výkony z oboru plastické chirurgie).
Vyšetření hladiny hepcidinu u pacientů a kontrol
Po získání informovaného souhlasu byl u pacientů a kontrol proveden odběr žilní krve. Část plazmy určené k měření hladiny hepcidinu byla rozdělena do alikvotů, aby se předešlo opakovanému rozmrazování, a zamrazena při -80 °C.
Použitá metoda měření hladiny hepcidinu je založena na extrakci na pevné fázi (SPE) a kapalinové chromatografii spřažené s hmotnostní spektrometrií (LC-MS/MS). Pro zjištění absolutní kvantifikace hepcidinu byl použit izotopově značený interní standard [13C9, 15N1-Phe4]-hepcidin, který byl přidáván ke každému vzorku séra. Nativní a značený hepcidin byl extrahován ze vzorku séra použitím SPE pomocí Oasis® HLB SPE mikrotitračních destiček. Získané extrakty vzorků s hepcidinem byly separovány na koloně s reverzní fází (C18) pomocí LC a dále analyzovány pomocí monitorování vybraných iontů (SRM) na hmotnostním spektrometru QTRAP 5500 (AB SCIEX). Pro SRM byl vybrán čtyřnásobně nabitý prekurzor hepcidinu a jeho fragmentační b3+ ion. Bylo připraveno osm kalibrantů o koncentracích 2,5; 5; 10; 25; 50; 100; 250; 500 ng/ml hepcidinu postupným ředěním v králičím séru. Kalibrační křivka byla sestavena na základě poměrů ploch „píků“ hepcidin/interní standard a koncentrace standardů. Regresní rovnice získaná z kalibračních standardů byla použita pro zpětný výpočet koncentrace hepcidinu ve vzorku.
Statistické metody
Ke stanovení korelace hladin hepcidinu u zdravých kontrol a jednotlivých typů anémií bylo použito Mann-Whitney testu. Hladiny p < 0,05 jsou hodnoceny jako statisticky významné.
Vyšetření hladiny GDF15
Hladina GDF15 v séru byla stanovena pomocí komerční diagnostické soupravy firmy R&D Systems dle návodu od výrobce.
Výsledky a diskuse
Výsledky vyšetření krevního obrazu, biochemických parametrů, zastoupení erytropoézy v kostní dřeni, kauzální mutace, hladiny hepcidinu a GDF15 u pacientů s vrozenou poruchou erytropoézy jsou shrnuty v tabulkách 1 a 2.
Tab. 1. Základní charakteristiky souboru pacientů s Diamondovou-Blackfanovou anémií. 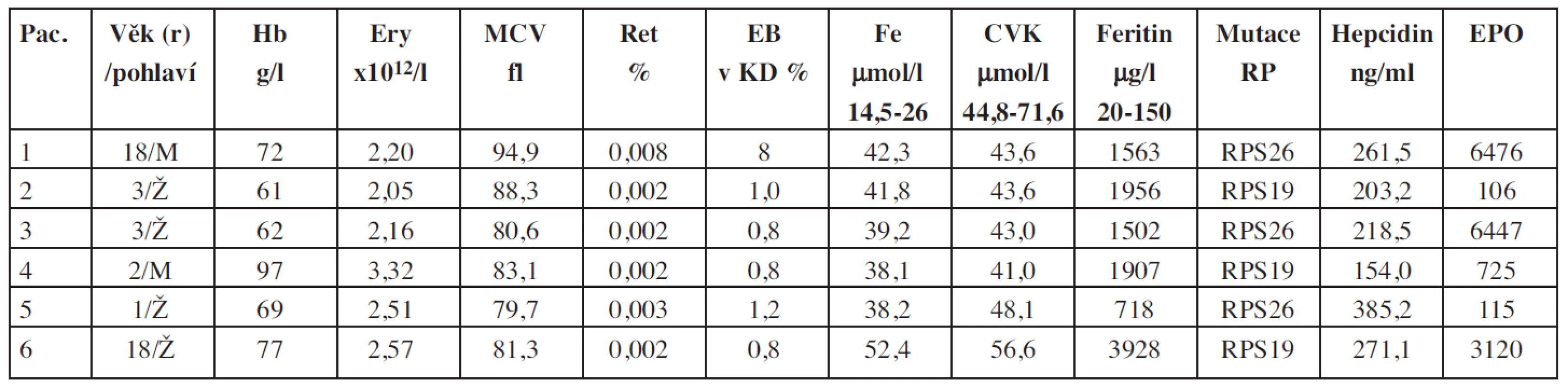
Vysvětlivky: CVK = celková vazebná kapacita; EB = erytroidní buňky; EPO = erytropoetin; Ery = erytrocyty; Hb = hemoglobin; KD = kostní dřeň; RP = ribosomální proteiny; Ret = retikulocyty Tab. 2. Základní charakteristiky souboru pacientů s deficitem pyruvátkinázy. 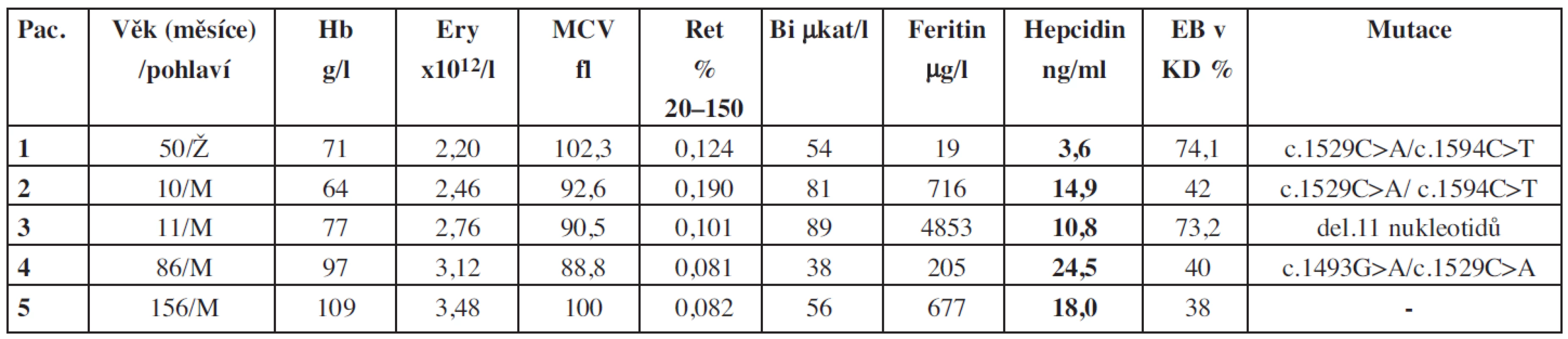
Vysvětlivky: Bi = bilirubin v séru; EB = erytroidní buňky; EPO = erytropoetin; Ery = erytrocyty; Hb = hemoglobin; KD = kostní dřeň; Pac. = pacient/pacientka Výsledky vyšetření krevního obrazu, biochemických parametrů a hladin hepcidinu u pacientů s IDA a pacientů s IBD jsou shrnuty v tabulkách 3 a 4.
Tab. 3. Základní charakteristiky souboru pacientů se sideropenickou anémií. 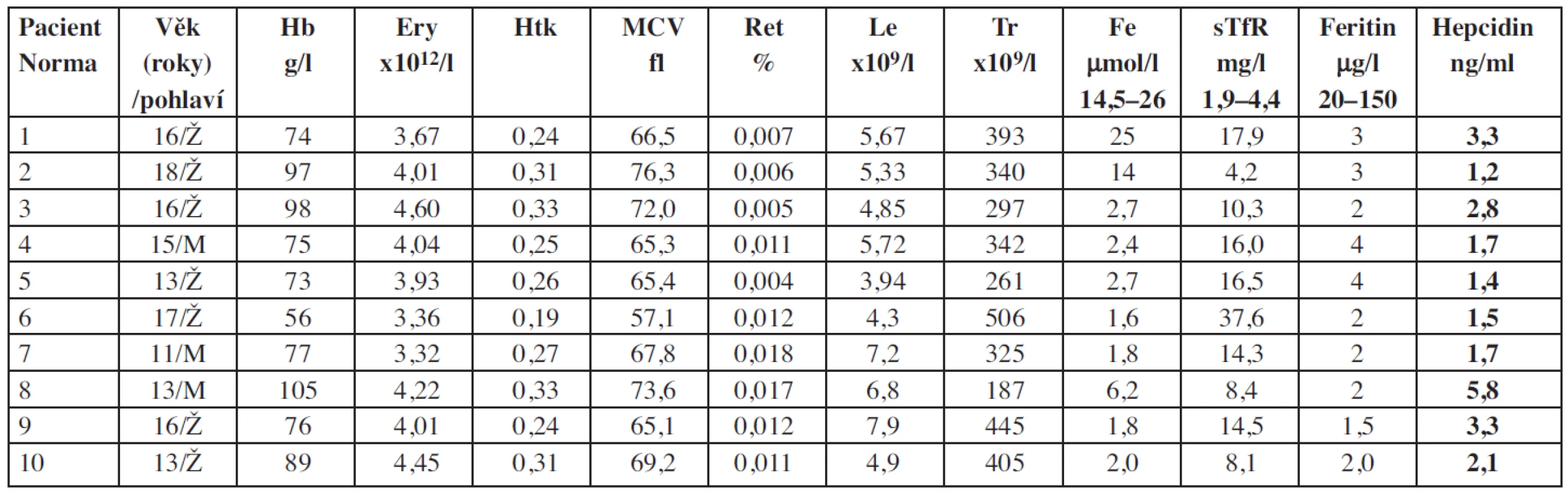
Vysvětlivky: Ery = erytrocyty; Hb = hemoglobin; Le = leukocyty; Ret = retikulocyty; Tr = trombocyty Tab. 4. Základní charakteristiky souboru pacientů s anémií doprovázející nespecifické střevní záněty (IBD). 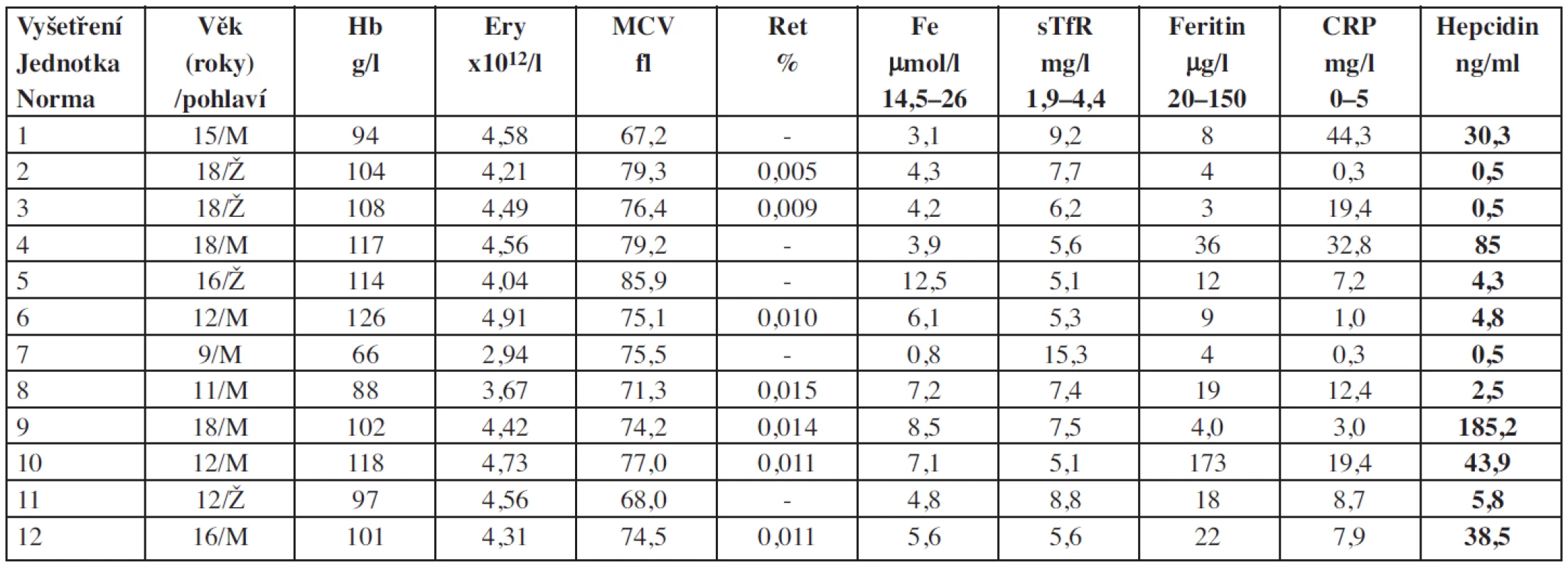
Vysvětlivky: Ery = erytrocyty; Hb = hemoglobin; Ret = retikulocyty 1. Diamondova-Blackfanova anémie
U všech vyšetřených pacientů souboru s těžkou formou DBA byla při vyšetření zjištěna těžká normocytární anémie s retikulocytopenií, zvýšená saturace transferinu a vysoké hladiny feritinu (tab. 1 a 2). Hladina hepcidinu v tomto souboru pacientů byla signifikantně vyšší ve srovnání s kontrolami (p > 0,0005).
U žádného pacienta nebyly v době vyšetření přítomny známky zánětlivého procesu.
DBA je charakterizována defektem erytropoézy s makrocytární anémií, retikulocytopenií s chyběním nebo snížením počtu erytroidních prekurzorových buněk v kostní dřeni. Příčinou onemocnění jsou mutace genů kódujících ribosomální proteiny. 30–40 % pacientů má těžkou anémii se závislostí na pravidelném podávání transfuzí. U všech těchto pacientů je pravidlem rozvoj závažného přetížení Fe s vysokou hladinou feritinu, které vzniká jako následek kombinace opakovaných transfuzí a chybějící erytropoézy v kostní dřeni a vždy vyžaduje léčbu chelátory. Vysoké hladiny hepcidinu u těžké anémie bez přítomnosti infekce nebo zánětu v tomto případě pravděpodobně odpovídají významnému přetížení železem s vysokou hladinou feritinu a zvýšenou saturací trasferinu.
Data o hladinách hepcidinu u pacientů s DBA zatím v literatuře nebyla publikována. Byla však publikována data o hladinách hepcidinu u pacientů s talasemia major, kteří mají srovnatelnou tíži anémie, potřebu transfuzí i stupeň přetížení železem. Na rozdíl od vyšetřených pacientů s DBA byly u pacientů s talasemií opakovaně popsány naopak snížené hladiny hepcidinu (12–15), které mohou přispívat k prohloubení stupně přetížení Fe. Podobně byly popsány snížené hladiny hepcidinu u pacientů s kongenitální dyserytropoetickou anémií (16, 17) a kongenitální sideroblastickou anémií (18). U všech zmíněných nemocí hladina hepcidinu negativně koreluje s hladinou GDF15 (8). Tato onemocnění jsou charakterizována neefektivní erytropoézou se zmnožením erytroidních prekurzorových buněk v kostní dřeni, což je pravděpodobně hlavním faktorem negativně ovlivňujícím produkci hepcidinu s cílem umožnit zvýšení absorpce Fe k zajištění dostatečné syntézy hemoglobinu.
U pacientů s DBA pravděpodobně není produkován erytroidní regulátor hepcidinu vzhledem k velmi nízké erytropoetické aktivitě. Zajímavý je fakt, že u pacientů s DBA jsou extrémně vysoké hodnoty erytropoetinu, na který deficitní erytropoéza není schopna reagovat. Tento výsledek je v souladu s analýzami na myších modelech, které ukázaly, že suprese hepcidinu erytropoetinem je nepřímá a vyžaduje plně funkční erytropoézu v kostní dřeni (19).
2. Hereditární enzymopatie
U všech pacientů se jednalo o středně těžkou nebo těžkou hemolytickou anémii s retikulocytózou a známkami extravaskulární hemolýzy (tab. 2). U tří dětí anémie vyžadovala opakované transfuze erytrocytů. U dvou pacientů se středně těžkou anémii byly transfuze podávány pouze ojediněle při infekcích. U tří pacientů byly rovněž přítomny zvýšené hladiny feritinu, u nejmladšího pacienta až s obrazem závažného přetížení železem s výrazně zvýšenou hladinou feritinu, což si vyžádalo léčbu chelátory Fe. U všech pacientů byla popsána akcelerace erytropoézy v kostní dřeni (tab. 2). V této skupině pacientů jsme prokázali signifikantně nižší hladinu hepcidinu ve srovnání s kontrolami (p > 0,02) (graf 1).
Graf 1. Srovnání hladin hepcidinu u pacientů s těžkou formou Diamondovy-Blackfanovy anémie (DBA) závislých na transfuzích, pacientů s deficitem pyruvátkinázy (PK) a kontrolní skupiny. 
Na patogenezi přetížení železem u pacientů s deficitem PK se mohou podílet opakované transfuze, hemolýza, ale i neefektivní erytropoéza. Může k němu přispívat i koincidence deficitu PK s vrozenou poruchou metabolismu železa. Až 20 % evropské populace má mírnou alteraci v metabolismu železa spojovanou s heterozygotním přenašečstvím mutace c.187C>G (p.His63Asp) a c.845C>A (p.Cys282Tyr) v HFE genu způsobujících vrozenou hemochromatózu. Poslední studie prokázaly abnormality v HFE-genu u 35 % pacientů s PK deficitem, kteří nejsou závislí na transfuzích (20). Tyto abnormality jsou spojeny se zvýšením hladiny Fe v séru a feritinu a mohou vést při dlouhém trvání k rozvoji cirhózy jater. Přetížení železem i bez mutace genu pro hemochromatózu bylo popsáno u polytransfundovaných pacientů a pacientů s PK deficitem po splenektomii. Pro přetrvávající výraznou hyperferitinemii byly u pacienta č. 4 vyloučeny mutace genů asociovaných s hemochromatózou, a to konkrétně mutace HFE1, HFE2A kódujícího hemojuvelin a HFE2B kódujícího hepcidin. Na přetížení železem se u tohoto pacienta pravděpodobně podílejí také snížené hladiny hepcidinu vedoucí ke zvýšenému vstřebávání Fe. U deficitu PK se kombinují oba faktory regulující protichůdně produkci hepcidinu: anémie s vyššími nároky na přísun železa při větším obratu erytropoézy a zvýšená hladina železa s vysokou hladinou feritinu. Bylo prokázáno, že u pacientů s deficitem PK je zvýšena hladina GDF 15, která je v tomto případě pravděpodobně zmíněným „erytroidním regulátorem“ snižujícím produkci hepcidinu (21). Zvýšenou hladinu GDF15 jsme prokázali u všech čtyř pacientů s deficitem PK (tab. 2). Snížení hladiny hepcidinu vede ke zvýšení resorpce Fe i přes jeho zvýšené zásoby, což dále přispívá ke zvyšování zásobního železa a k progresi přetížení železem.
3. Sideropenická anémie
U všech vyšetřených pacientů se IDA byly hladiny hepcidinu signifikantně nižší ve srovnání s kontrolami, rozdíl je statisticky významný (p < 0,01) (graf 2).
Graf 2. Srovnání hladin hepcidinu u pacientů se sideropenickou anémií (IDA), anémií doprovázející nespecifické střevní záněty (IBD) a kontrolní skupiny. 
U pacientky č. 2 jsme pro zajímavost provedli kontrolní vyšetření hladiny hepcidinu za 3 měsíce po zahájení léčby, kdy při normalizaci krevního obrazu došlo ke zvýšení hladiny hepcidinu k hodnotě blízké mediánu u kontrolní skupiny.
Hladiny hepcidinu nejlépe korelovaly se sníženou hladinou feritinu a zvýšenou hladinou sTfR.
IDA jako celosvětově nejrozšířenější anémie postihuje 20–30 % světové populace. V dětském věku se vyskytuje nejčastěji ve dvou věkových obdobích: u kojenců a batolat a poté v období adolescence, tedy v obdobích, která jsou charakterizována rychlým růstem a zvýšenými nároky na erytropoézu. V období růstu může mít IDA u kojenců a dětí do 3 let věku negativní dopad na růst a vývoj a může vést ke dlouhotrvajícímu snížení mentálních a motorických funkcí a poruch chování (22). Pokud není léčba zahájena včas, mohou být uvedené změny ireverzibilní (23). Proto je prevence a včasná diagnóza IDA velmi důležitá. Ve vyspělých zemích byly již vytvořeny programy prevence nedostatku železa především u malých dětí.
Odlišení IDA od ostatních mikrocytárních anémií vyžaduje vyšetření parametrů metabolismu Fe v séru (saturace transferinu, CVK, feritin, sTfR), k čemuž je nezbytný odběr žilní krve. Možnost vyšetření hepcidinu v moči jako screeningového testu pro detekci nedostatku Fe u malých dětí by pro klinickou praxi mohla být obrovským přínosem.
4. Anémie u pacientů s nespecifickými střevními záněty
V souboru 12 pacientů s IBD (Crohnovou chorobou a ulcerózní kolitidou) jsou hodnoty hepcidinu rozdílné od velmi nízkých ke zvýšeným. Rozdíl mezi pacienty a kontrolami není statisticky významný (graf 2). Hladiny hepcidinu jsou tak nižší, než by se teoreticky dalo očekávat u anémie doprovázející chronické choroby. Nízká hladina hepcidinu koreluje s nízkou hladinou feritinu a vysokou hladinou sTfR, které jsou nepochybnou známkou deficitu Fe v organismu a byly prokázány u 8/12 pacientů. V malém souboru vyšetřených pacientů tedy převažují děti s IBD s významným deficitem Fe.
U typické anémie chronických zánětů (ACD) je produkce hepcidinu několikanásobně vyšší. Zvýšená hladina hepcidinu s následnou retencí Fe v enterocytech a makrofázích vysvětluje jednu ze základních charakteristik anémie chronických chorob, kterou je zvýšená sekvestrace Fe v makrofázích a nízká hladina Fe v séru (24). V patogenezi anémie u pacientů s nespecifickými střevními záněty je však situace komplikovaná dalšími faktory. Na etiologii anémie se podílí nejen chronický zánět, ale i špatné vstřebávání Fe zánětlivě změněnou sliznicí, nedostatečný příjem potravy a chronické ztráty krve ze střeva při zánětu sliznice. Vzniká tak často kombinace anémie chronických chorob se skutečným nedostatkem železa (tzv. ACD/IDA). Odlišení „klasické“ anémie chronických chorob od ACD/IDA obecně není jednoduché, zatím neexistuje žádný parametr vhodný k jednoznačnému odlišení těchto dvou typů anémie. Důležitými markery jsou transferin, saturace transferinu a sTfR. Každý z těchto ukazatelů však má různé limitace a žádný z nich není jednoznačně spolehlivý, protože jsou ovlivněny i jinými faktory než jsou změny rovnováhy železa (25). Kromě těchto základních ukazatelů metabolismu Fe se diskutuje o poměru log. sTfR/feritin, procentu hypochromních erytrocytů, šíři distribuce erytrocytů nebo obsahu hemoglobinu v retikulocytech, žádná z těchto metod však zatím nebyla přijata do rutinní praxe. Proto je zvažováno možné využití stanovení hladiny hepcidinu.
Na hladinu hepcidinu u ACD/IDA působí opět dva protichůdné faktory: anémie se skutečným deficitem Fe, což by teoreticky mělo vést ke snížení hladiny hepcidinu a následně ke zvýšenému vstřebávání železa ze střeva, a zánět střevní sliznice, který by měl v důsledku zvýšení produkce IL-6 při zánětlivém procesu vést ke zvýšení hladiny hepcidinu a snížení resorpce Fe. Zatím však bylo publikováno jen málo prací hodnotících hepcidin u IBD, a to pouze u dospělých (26, 27, 28) s protichůdnými výsledky. Studie u dětských pacientů dosud nejsou k dispozici. Dle výsledků vyšetření u našich pacientů koreluje obraz skutečného deficitu Fe i přes chronické zánětlivé onemocnění s nízkou hladinou hepcidinu. U pacienta s UC s nejnižší hladinou hepcidinu (pacient č. 7, tab. 4) je přítomna výrazná anémie charakteru ACD/IDA i při přetrvávající zánětlivé aktivitě s krvácením ze střevní sliznice. Hladina hepcidinu by tedy mohla právě u anémie chronických chorob být jedním z ukazatelů, které pomohou odpovědět na otázku, zda je u pacientů skutečný deficit železa nebo zda převažuje zánětlivá složka s blokádou resorpce železa, a být tak vodítkem při rozhodování, zda má smysl léčit pacienty perorálně podávanými preparáty Fe. Dle našich výsledků je signál skutečného deficitu Fe v organismu nadřazen signálům chronického zánětu. Tomu odpovídají i rozporuplné publikované výsledky různých hladin hepcidinu u dospělých pacientů s IBD.
Vývoj metod stanovení hladiny hepcidinu bude mít v budoucnu jistě význam pro klinickou praxi. V posledních letech byly získané poznatky o metabolismu hepcidinu u některých typů anémií a také hereditárních hemochromatóz podkladem pro vývoj agonistů a antagonistů hepcidinu, které mohou mít efekt v léčbě některých poruch homeostázy Fe, především u přetížení železem u pacientů s talasémií nebo u anémie chronických chorob. Jako nejslibnější se jeví možné použití agonistů hepcidinu u talasémií. Na myších modelech talasémie bylo prokázáno, že agonisté hepcidinu mohou působit nejen jako prevence přetížení železem, ale mohou rovněž zlepšit erytropoézu, pravděpodobně snížením nadměrné syntézy globinu nebo snížením oxidativního stresu v erytroidních prekurzorech. Spekuluje se i o využití inhibitorů enzymatické aktivity matriptázy 2, která negativně ovlivňuje expresi hepcidinu, u hereditární hemochromatózy. Zvýšením produkce hepcidinu by se mohlo předejít komplikacím plynoucím z nadměrné absorpce Fe nebo nadměrného uvolňování Fe z makrofágů. Byla by však nezbytná důsledná titrace inhibice produkce hepcidinu, protože u HFE myší se při kompletní inaktivaci enzymu vyvinula sideropenická anémie. Dalším z kandidátů pro léčbu hemochromatózy je použití farmakologických dávek kostního morfogenetického proteinu 6 (bone morphogenetic protein - BMP6), přirozeného ligandu BMP receptoru, který je hlavním proteinem stimulujícím transkripci hepcidinu. Antagonisté hepcidinu, látky, které snižují produkci hepcidinu, by mohly být využity u stavů s restrikcí Fe způsobenou vysokou hladinou hepcidinu a uvolnit retinované Fe pro erytropoézu. Vzhledem k tomu, že se v případě těchto typů anémií nejedná o bezprostředně život ohrožující stavy, je nezbytné před použitím antagonistů hepcidinu velmi bedlivě ověřit jejich potenciální vedlejší účinky. Zatím je efekt těchto látek zkoumán na myších modelech.
Závěry
U pacientů trpících různými typy anémií mohou jednotlivé mechanismy regulující metabolismus železa a tím i produkci hepcidinu působit protichůdně. Znalost hladiny hepcidinu v séru a moči může být nejen významnou informací při pátrání po patofyziologii anémie nebo poruch metabolismu železa, ale i důležitým diagnostickým testem. Může sloužit například jako test k časnému vyhledávání sideropenie u malých dětí, k odlišení ACD od ACD/IDA nebo být vodítkem při rozhodování o indikaci léčby perorálně podávanými preparáty železa nebo léčby intravenózní. Naše dílčí výsledky mohou významnou měrou přispět k odhalení řady nejasností v hierarchii vlivu jednotlivých regulátorů produkce hepcidinu.
Stanovení hladin hepcidinu proteomickou metodou bude v budoucnu jistě patřit k metodám, které především umožní zpřesnit diagnostiku celé řady anémií informací o aktuálním stavu metabolismu železa. Může poskytnout nejen důležitou informaci o aktuálním deficitu železa pro potřeby erytropoézy, stupni přetížení železem, ale i o aktuální schopnosti enterocytů vstřebávat Fe ze střevního lumen. Znalost hladiny hepcidinu může při korelaci s hladinami ostatních proteinů účastnících se regulace metabolismu Fe přinést velmi důležité poznatky o dosud nejasných aspektech homeostázy Fe v organismu. Je třeba zdůraznit, že v některých případech nelze stanovit definitivní závěr z jednoho vyšetření hladiny hepcidinu. Ta se u různých patologických stavů dynamicky mění, měření je proto nutno opakovat v různých fázích vývoje onemocnění. Vzhledem k náročnosti zavedené proteomické detekce hepcidinu je však otázka jejího rutinního použití otevřená.
Poděkování
Tato práce byla podpořena grantem IGA MZ ČR NS9951-4/2008, IGA UPOL 9011100251, operačním programem Věda a výzkum pro inovace (projekt CZ.1.05/2.1.00/01.0030) a Interním grantem Univerzity Palackého v Olomouci LF-2011-011.
Doc. MUDr. Dagmar Pospíšilová, Ph.D.
Dětská klinika Lékařská fakulta Univerzity Palackého v Olomouci
Fakultní nemocnice Olomouc
I. P. Pavlova 6
775 20 Olomouc
e-mail: pospisid@fnol.cz
Doručeno do redakce: 7. 3. 2012
Přijato po recenzi: 15. 4. 2012
Zdroje
1. Ganz T, Nemeth E. Hepcidin and iron homeostasis. Biochim Biophys Acta; publikováno elektronicky 25. ledna 2012. DOI 10.1016/j.bbamcr.2012.01.014.
2. Park CH, Valore EV, Waring AJ, Ganz T. Hepcidin, a urinary antimicrobial peptide synthesized in the liver. J Biol Chem 2001; 276 : 7806–7810.
3. Valore EV, Ganz T. Posttranslational processing of hepcidin in human hepatocytes is mediated by the prohormone convertase furin. Blood Cells Mol Dis 2008; 40 : 132–138.
4. Ganz T, Nemeth E. Iron imports: IV. Hepcidin and regulation of body iron metabolism. Am J Physiol Gastrointest Liver Physiol 2006; 290: G199–G203.
5. Cherian S, Forbes DA, Cook AG, et al. An insight into the relationships between hepcidin, anemia, infections and inflammatory cytokines in pediatric refugees: a cross-sectional study. PLoS ONE 2008; 3: e4030.
6. Nemeth E, Tuttle MS, Powelson J, et al. Hepcidin regulates cellular iron efflux by binding to ferroportin and inducing its internalization. Science 2004; 306 : 2090–2097.
7. Fleming RE, Ponka P. Iron overload in human disease. N Engl J Med 2012; 366 : 348–359.
8. Tanno T, Noel P, Miller JL. Growth differentiation factor 15 in erythroid health and disease. Curr Opin Hematol 2010; 17 : 184–190.
9. Ganz T, Olbina G, Girelli D, Nemeth E, Westerman M. Immunoassay for human serum hepcidin. Blood 2008; 112 : 4292–4297.
10. Young MF, Glahn RP, Ariza-Nieto M, et al. Serum hepcidin is significantly associated with iron absorption from food and supplemental sources in healthy young women. Am J Clin Nutr 2009; 89 : 533–538.
11. Melis MA, Cau M, Congiu R, et al. A mutation in the TMPRSS6 gene, encoding a transmembrane serine protease that suppresses hepcidin production, in familial iron deficiency anemia refractory to oral iron. Haematologica 2008; 93 : 1473–1479.
12. Gardenghi S, Grady RW, Rivella S. Anemia, ineffective erythropoiesis and hepcidin: interacting factors in abnormal iron metabolism leading to iron overload in ß-thalassemia. Hematol Oncol Clin North Am 2010; 24 : 1089–1107.
13. Gardenghi S, Marongiu MF, Ramos P, et al. Ineffective erythropoiesis in beta-thalassemia is characterized by increased iron absorption mediated by down-regulation of hepcidin and up-regulation of ferroportin. Blood 2007; 109 : 5027–5035.
14. Ginzburg Y, Rivella S. ß-thalassemia: a model for elucidating the dynamic regulation of ineffective erythropoiesis and iron metabolism. Blood 2011; 118 : 4321–4330.
15. Kattamis A, Papassotiriou I, Palaiologou D, et al. The effects of erythropoetic activity and iron burden on hepcidin expression in patients with thalassemia major. Haematologica 2006; 91 : 809–812.
16. Tamary H, Shalev H, Perez-Avraham G, et al. Elevated growth differentiation factor 15 expression in patients with congenital dyserythropoietic anemia type I. Blood 2008; 112 : 5241–5244.
17. Casanovas G, Swinkels DW, Altamura S, et al. Growth differentiation factor 15 in patients with congenital dyserythropoietic anaemia (CDA) type II. J Mol Med (Berl) 2011; 89 : 811–816.
18. Ramirez JM, Schaad O, Durual S, et al. Growth differentiation factor 15 production is necessary for normal erythroid differentiation and is increased in refractory anaemia with ring-sideroblasts. Br J Haematol 2009; 144 : 251–262.
19. Vokurka M, Krijt J, Sulc K, Necas E. Hepcidin mRNA levels in mouse liver respond to inhibition of erythropoiesis. Physiol Res 2006; 55 : 667–674.
20. Zanella A, Bianachi P, Iurlo A, et al. Iron status and HFE genotype in erytrocyte pyruvate kinase deficiency: Study of Italian cases. Blood cells Mol Dis 2001; 27, 653–661.
21. Finkenstedt A, Bianchi P, Theurl I, et al. Regulation of iron metabolism through GDF15 and hepcidin in pyruvate kinase deficiency. Br J Haematol 2009; 144 : 789–793.
22. Kazal LA Jr. Prevention of iron deficiency in infants and toddlers. Am Fam Physician 2002; 66 : 1217–1225.
23. Lozoff B, Klein NK, Nelson EC, McClish DK, Manuel M, Chacon ME. Behavior of infants with iron-deficiency anemia. Child Dev 1998; 69 : 24–36.
24. Nemeth E, Valore EV, Territo M, Schiller G, Lichtenstein A, Ganz T. Hepcidin, a putative mediator of anemia of inflammation, is a type II acute-phase protein. Blood 2003; 101 : 2461–2463.
25. Oustamanolakis P, Koutroubakis IE, Kouroumalis EA. Diagnosing anemia in inflammatory bowel disease: beyond the established markers. J Crohns Colitis 2011; 5 : 381–391.
26. Oustamanolakis P, Koutroubakis IE, Messaritakis I, Malliaraki N, Sfiridaki A, Kouroumalis EA. Serum hepcidin and prohepcidin concentrations in inflammatory bowel disease. Eur J Gastroenterol Hepatol 2011; 23 : 262–268.
27. Nagy J, Lakner L, Poór VS, et al. Serum prohepcidin levels in chronic inflammatory bowel diseases. J Crohns Colitis 2010; 4 : 649–653.
28. Arnold J, Sangwaiya A, Bhatkal B, Geoghegan F, Busbridge M. Hepcidin and inflammatory bowel disease: dual role in host defence and iron homeostasis. Eur J Gastroenterol Hepatol 2009; 21 : 425–429.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2012 Číslo 2- Není statin jako statin aneb praktický přehled rozdílů jednotlivých molekul
- Magnosolv a jeho využití v neurologii
- Moje zkušenosti s Magnosolvem podávaným pacientům jako profylaxe migrény a u pacientů s diagnostikovanou spazmofilní tetanií i při normomagnezémii - MUDr. Dana Pecharová, neurolog
- Biomarker NT-proBNP má v praxi široké využití. Usnadněte si jeho vyšetření POCT analyzátorem Afias 1
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
-
Všechny články tohoto čísla
- Základní Imunohematologická laboratorní vyšetření červené řady – Obecné zásady a technické postupy
- Imunohematologická vyšetření dárců krve a krevních složek
- Úvodní slovo
- Význam stanovení hladiny hepcidinu v diagnostice vybraných typů anémií v dětském věku
- Hodnocení časné molekulární odpovědi po 3 měsících léčby imatinibem může u nemocných s chronickou myeloidní leukemií přispět k upřesnění odhadu prognózy – zkušenosti jednoho centra
- Identifikace patogeneticky významných mutací u chronické lymfocytární leukemie pomocí „sekvenování nové generace“
- Současné možnosti laboratorní diagnostiky heparinem indukované trombocytopenie
- Kolapsový stav u 18leté dívky – kazuistika
- Zpráva o úspěšném ukončení projektu Virtuální mikroskopie
- Zpráva o knize
- Opožděná informace o knize věnované hematologii a transfuziologii vydané na Slovensku
- MUDr. Vladimír Koza
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Současné možnosti laboratorní diagnostiky heparinem indukované trombocytopenie
- Základní Imunohematologická laboratorní vyšetření červené řady – Obecné zásady a technické postupy
- Kolapsový stav u 18leté dívky – kazuistika
- Význam stanovení hladiny hepcidinu v diagnostice vybraných typů anémií v dětském věku
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



