-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Chronický subdurální hematom − přehled
Chronic subdural hematoma – review article
Introduction:
Chronic subdural hematoma (ChSDH) is, by definition, a subdural collection of blood older than 21 days. It is not exceptional that ChSDH is diagnosed in regional hospitals and thus we believe that basic knowledge on this topic is relevant for every general surgeon. Below, we summarize information on ChSDH and present simple clinical management guidelines.
Treatment:
In asymptomatic patients with ChSDH, monitoring alone may be sufficient. Subdural collections of only a few millimeters are a relatively common incidental finding on graphical examination of the brain, especially in the elderly with brain atrophy. In symptomatic patients, surgical treatment is justified. As a first step, burr hole evacuation of the hematoma in local anesthesia is performed. It is a simple, well-tolerated procedure and advantageous in elderly polymorbid patients. In symptomatic patients with recurrent ChSDH, reoperation using either the same burr hole or a new one is indicated. Patients with multilobulated hematomas that recur after the burr hole are scheduled for a craniotomy.
Conclusion:
ChSDH is a common condition encountered by all general surgeons during their clinical practice. The most common clinical presentations of ChSDH are headache, confusion, hemiparesis and aphasia. Asymptomatic patients may be followed by watchful waiting, whereas symptomatic patients are indicated for surgical treatment. All patients with ChSDH should be referred to a neurosurgical department (preferably a certified level 1 trauma center) with experience in neurotrauma care.
Keywords:
neurosurgery − head trauma − chronic subdural hematoma − burr hole −craniotomy
Autoři: M. Májovský; D. Netuka
Působiště autorů: Neurochirurgická a neuroonkologická klinika 1. lékařské fakulty Univerzity Karlovy a Ústřední vojenská nemocnice - Vojenská fakultní nemocnice Praha
Vyšlo v časopise: Rozhl. Chir., 2018, roč. 97, č. 6, s. 253-257.
Kategorie: Souhrnné sdělení
Souhrn
Úvod:
Chronický subdurální hematom (ChSDH) je kolekce krve v subdurálním prostoru, dle definice starší než 21 den. V našem textu se snažíme přehledně shrnout základní informace o ChSDH a poskytnout jednoduchý návod péče o tyto pacienty pro lékaře jiných oborů, než je neurochirurgie.
Léčba:
Asymptomatičtí pacienti s nevelkými ChSDH mohou být pouze sledováni. Subdurální kolekce o šíři několika milimetrů bývají relativně častým náhodným nálezem na zobrazovacím vyšetření mozku, zejména u starších lidí s atrofií mozku. U symptomatických pacientů je plně indikována operační léčba. Jako první chirurgický krok volíme nejčastěji návrt a evakuaci ChSDH v lokální anestezii. Jedná se o relativně šetrný, dobře tolerovaný výkon, výhodný u starších polymorbidních pacientů. U symptomatických pacientů s recidivujícím ChSDH volíme reoperaci, a to podle anatomické situace buď z původního, nebo z nového návrtu. ChSDH, který má multilobulární strukturu se septy, často nelze dokonale vypustit z návrtu. Proto při recidivě multilobulárního ChSDH přistupujeme k invazivnějšímu výkonu – kraniotomii.
Závěr:
ChSDH je časté onemocnění, s nímž se ve své praxi setká každý chirurg. Mezi nejčastější příznaky patří bolesti hlavy, zmatenost, hemiparéza a fatická porucha. U asymptomatických pacientů volíme konzervativní postup, u symptomatických je indikována léčba chirurgická – v první řadě návrt v lokální anestezii. Každý pacient s ChSDH by měl být konzultován na neurochirurgickém pracovišti se zkušeností s neurotraumatologií, ideálně v nemocnici se statutem traumacentra.
Klíčová slova:
neurochirurgie − úraz hlavy − chronický subdurální hematom − návrt lebky − kraniotomie
Úvod
Chronický subdurální hematom (ChSDH) je kolekce krve v subdurálním prostoru, dle definice starší než 21 dnů [1]. Na rozdíl od akutního subdurálního hematomu nejde o emergentní stav, ale přesto vyžaduje aktivní přístup ošetřujícího lékaře a v mnoha případech i chirurgickou léčbu.
Jedná se o relativně časté onemocnění, jehož incidence stále narůstá v souvislosti se zvyšujícím se věkem populace a širokým užíváním antikoagulancií. Není výjimkou, že ChSDH diagnostikuje všeobecný chirurg v nemocnici, kde není neurochirurgie, a musí takového pacienta alespoň základně vyšetřit a zajistit mu péči do doby, než bude přeložen. V následujícím textu si dovolujeme shrnout základní fakta o léčbě pacientů s ChSDH a poskytnout tak jednoduchou pomůcku pro všeobecné chirurgy, kteří se s těmito pacienty setkají. Zjednodušený algoritmus péče o pacienty s ChSDH je shrnut ve Schématu 1.
Schema 1: Zjednodušený algoritmus péče o pacienty s ChSDH
Schema 1: Basic flowchart of care for ChSDH patients
Epidemiologie
Incidence ChSDH se pohybuje mezi 8,2−14,1 případu na 100 000 obyvatel/rok [2−4]. Častěji postihuje muže a průměrný věk při diagnóze dosahuje 77 let [5]. Starší osoby mívají určitý stupeň atrofie mozku a fragilnější přemosťující žíly, a jsou tedy náchylnější k subdurálnímu krvácení. Většina pacientů má v anamnéze nedávný úraz hlavy, často se však přesného momentu vzniku krvácení nedopátráme. Mezi rizikové faktory vzniku ChSDH patří vyšší věk, koagulopatie, chronický ethylismus, epileptické záchvaty, zavedený ventrikuloperitoneální zkrat a časté pády [1].
V ČR se provedlo v roce 2016 více než 1000 operací pro ChSDH, z toho 165 na našem pracovišti.
Patogeneze
ChSDH vzniká jako akutní subdurální hematom, který zůstane nepovšimnut a během několika týdnů se vyvine v ChSDH. Patogeneze ChSDH je komplexní jev, jehož podstatou jsou patologické reparativní procesy, které nezřídka vedou k progresi objemu hematomu a tím i tlaku na mozkovou tkáň. Krev v hematomu se rozkládá, probíhá produktivní zánět, vzniká vnitřní a vnější pouzdro s novotvořenými cévami a membránami [5]. Probíhající zánět dále vychyluje rovnováhu prosrážlivých a protisrážlivých pochodů a výsledný hyperfibrinolytický stav zabraňuje tvorbě koagula, čímž podporuje další drobná krvácení z pouzdra hematomu.
Diagnostika
Klinický obraz nebývá specifický a pacienti běžně přicházejí do nemocnic pod obrazem mozkové mrtvice či celkového zhoršení stavu. Nejčastějšími příznaky bývají bolest hlavy, zmatenost, kvalitativní porucha vědomí, hemiparéza, vertigo, porucha chůze či fatická porucha. V diferenciální diagnostice pomýšlíme na počínající demenci, pokud dominuje kongitivní porucha, či na cévní mozkovou příhodu v případě motorického deficitu a fatické poruchy.
Často se ChSDH též odhalí u pacienta, který měl pád a po vyšetření na traumatologické ambulanci je provedeno CT. V situacích, kdy pacient nemá fokální neurologický deficit, není jednoduché rozlišit, zda pacient spadl na základě vertiga způsobeného ChSDH, nebo zda je ChSDH náhodným nálezem.
Diagnóza ChSDH je definitivně stanovena na CT vyšetření, kde typicky nalézáme hypodenzní až izodenzní srpkovitou kolekci nad velkou částí hemisféry (Obr. 1). Hematom bývá často objemný s výrazným přetlakem střední čáry 10 mm a více. Přesto nemusí působit výraznější příznaky, protože vzniká delší dobu a mozek se postupně adaptuje. Hyperdenzní okrsky v hematomu představují septa nebo sediment krve a někdy bývají mylně popsány jako akutní složka hematomu. Nález těchto hyperdenzit není důvodem k urgentní operaci, spíše představuje rizikový faktor recidivy, protože snižuje šance na vypuštění hematomu z běžného návrtu [6].
Obr. 1. : A − septovaný, převážně hypodenzní chronický subdurální hematom; B −stav po drenáži subdurálního hematomu s minimálním reziduem
Fig. 1: A − multilobulated, predominantly hypodense chronic subdural hematoma; B − postoperative CT after evacuation of chronic subdural hematoma with minimal residuum
V jednotlivých případech se používá i magnetická rezonance (MRI) k diagnóze ChSDH. Část pacientů s ChSDH je však neklidná, proto se toto vyšetření z této indikace často nepoužívá. MRI může odhalit i jiné zdroje krvácení než úrazové. Při diagnostice izodenzního subdurálního hematomu je MRI přesnější než CT. Chronické subdurální hematomy jsou obvykle hyperintenzní v T1 i T2 váženém vyšetření. MRI může být přínosné k odhalení sept v ChSDH, které ovlivňují možnost evakuace z prostého návrtu [7].
Konzervativní léčba
Asymptomatičtí pacienti s ChSDH, jejichž šířka nepřekračuje 10 mm, mohou být pouze sledováni. Subdurální kolekce o šíři několika milimetrů bývají relativně častým náhodným nálezem na zobrazovacím vyšetření mozku, zejména u starších lidí s atrofií mozku (mechanismus e vacuo).
Některé novější práce naznačují, že krátkodobá léčba dexamethasonem má příznivý vliv na produktivní zánět probíhající v pouzdru hematomu a u pacientů s ChSDH v dobrém klinickém stavu může mít podobné výsledky jako chirurgická léčba [8]. V současnosti probíhá několik větších randomizovaných studií, které by měly přesněji definovat roli kortikosteroidů na regresi hematomu [9,10]. ChSDH tak představuje výjimku oproti jiným úrazům mozku (akutní subdurální hematom, traumatické intracerebrální krvácení), u kterých jsou kortikoidy kontraindikovány. Kortikoidy jsou tradičně rezervovány pro pacienty s mozkovými nádory s perifokálním vazogenním edémem. Předpokládaný mechanismus účinku u ChSDH však nespočívá ve snížení otoku mozku, ale v potlačení produktivního zánětu a angiogeneze v pouzdru hematomu.
Další léky proti otoku mozku, jako například mannitol či hypertonický roztok NaCl, jsou vyhrazeny pouze pro pacienty s příznaky zvýšeného nitrolebního tlaku a s poruchou vědomí, kteří jsou stejně indikováni k neodkladnému operačnímu výkonu.
Operační léčba
U symptomatických pacientů je plně indikována operační léčba a načasování výkonu do velké míry závisí na tíži příznaků. V případě kvantitativní poruchy vědomí, k čemuž dochází vzácně, je nutno operovat bezodkladně. V případě topického neurologického nálezu (hemiparéza, fatická porucha) pacienta operujeme po běžné předoperační přípravě, zejména normalizaci hemokoagulace. Několikadenní vysazení antiagregancií nevyžadujeme, nezdá se, že by tyto léky zvyšovaly riziko komplikací či recidiv [11].
Jako první chirurgický krok volíme nejčastěji návrt a evakuaci ChSDH v lokální anestezii. Jedná se o relativně šetrný, dobře tolerovaný výkon, výhodný u starších polymorbidních pacientů. Z krátkého řezu frontálně provádíme návrt o průměru cca 1,5 cm a otevíráme tvrdou plenu mozkovou a zevní pouzdro hematomu. Zpravidla pod tlakem vytéká tmavá tekutina hematomu a nezřídka již v této fázi dochází ke zlepšení příznaků. Zavádíme drén, kterým dutinu hematomu proplachujeme ohřátým fyziologickým roztokem a ponecháváme jej do druhého pooperačního dne (Obr. 2). V případě, že se mozek rychle rozvine a vyplní intrakraniální prostor ještě v průběhu operace, drén nezavádíme. U nespolupracujících pacientů s kvantitativní či kvalitativní poruchou vědomí provádíme návrt v celkové anestezii po zvyklé přípravě.
Obr. 2. Drenáž subdurálního hematomu z návrtu
Fig. 2: Drainage of subdural hematoma through a burr hole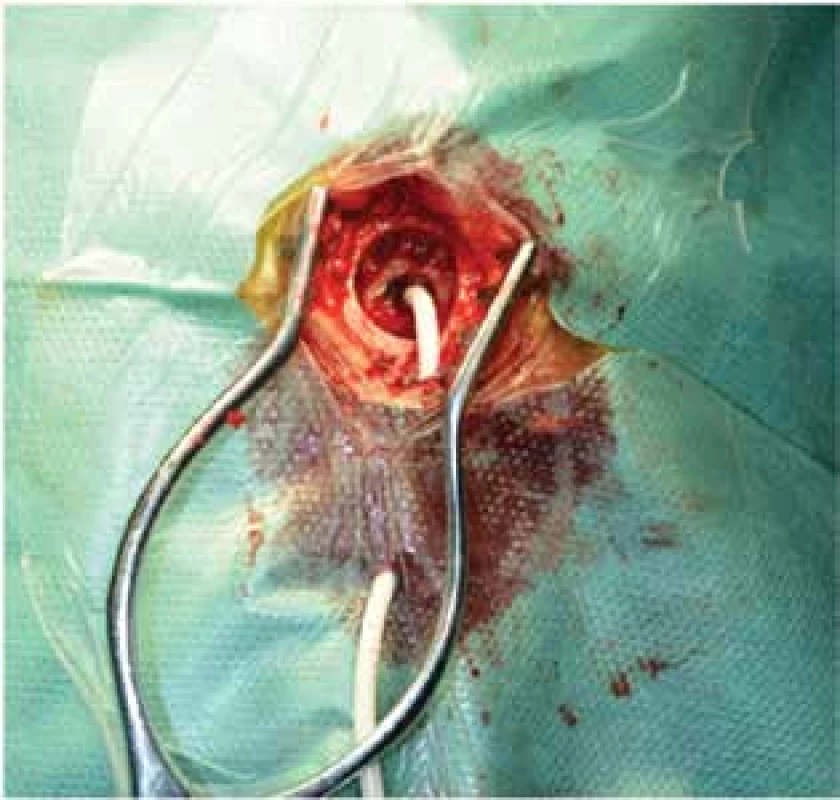
U symptomatických pacientů s recidivujícím ChSDH volíme reoperaci, a to podle anatomické situace buď z původního, nebo z nového návrtu. Někdy můžeme u těchto pacientů s výhodou použít endoskop k inspekci dutiny [12]. ChSDH, který má multilobulární strukturu se septy, často nelze dokonale vypustit z návrtu, a proto při recidivě přistupujeme k invazivnějšímu výkonu – kraniotomii [13]. V celkové anestezii odklápíme větší kostní ploténku, optimálně v celém rozsahu hematomu. Resekujeme zevní pouzdro hematomu (Obr. 3) a tuhé hmoty pod ním, nikdy se ovšem nesnažíme resekovat i vnitřní pouzdro, pokud lne k mozku, pro zvýšené riziko pooperačního krvácení a epilepsie [14].
Obr. 3. Resekce septovaného, tuhého chronického hematomu, který nebylo možné vypustit z návrtu
Fig. 3: Resection of multilobulated chronic subdural hematoma through a craniotomy, which was not possible to evacuate through a burr hole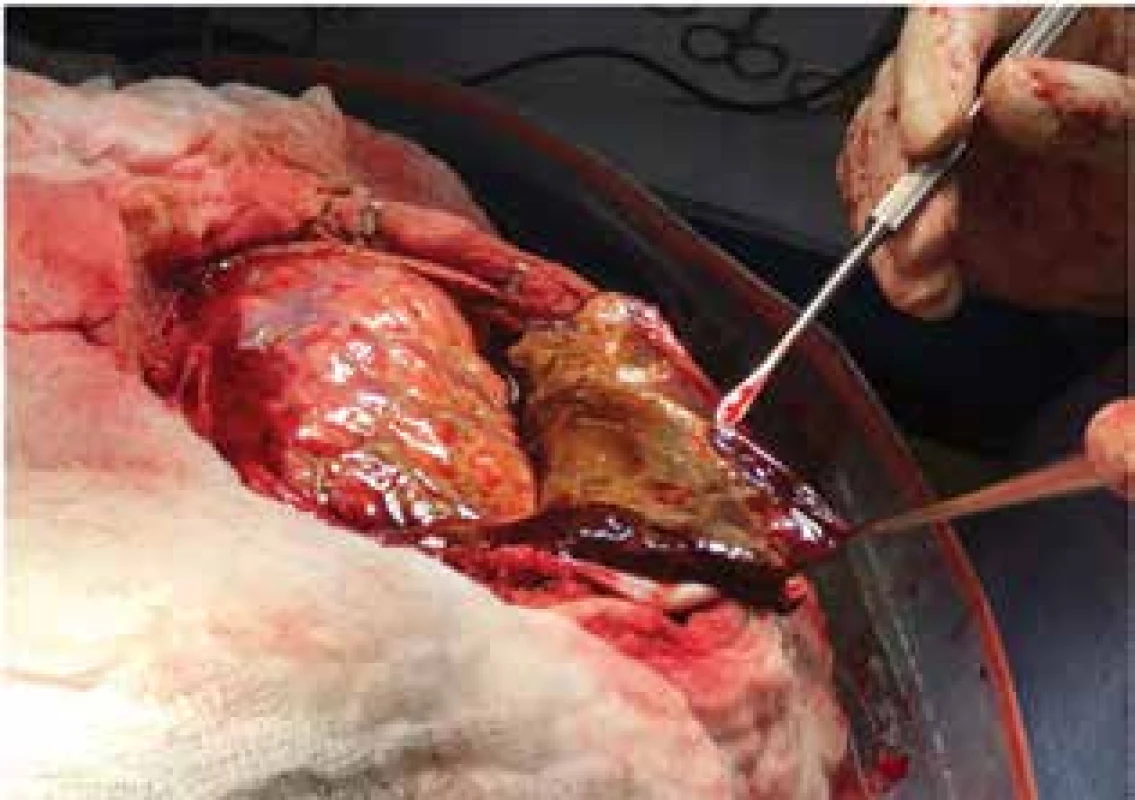
Zvláštním případem je akutní krvácení do existujícího ChSDH a náhlé zhoršení klinického stavu. Fragilní cévy pouzdra většinou následkem úrazu způsobí závažné krvácení, jehož průběh připomíná akutní subdurální hematom. Na CT vidíme v těchto případech smíšenou hypo/hyperdenzní subdurální kolekci s výrazným přetlakem střední čáry (Obr. 4). Pokud dominuje hypodenzní složka hematomu („chronická“), lze uvažovat o evakuaci z návrtu, v opačném případě provádíme kraniotomii.
Obr. 4. Chronický subdurální hematom s významnou porcí čerstvého krvácení a výrazným expanzivním chováním hematomu
Fig. 4. Chronic subdural hematoma with an acute hemorrhage causing a significant mass effect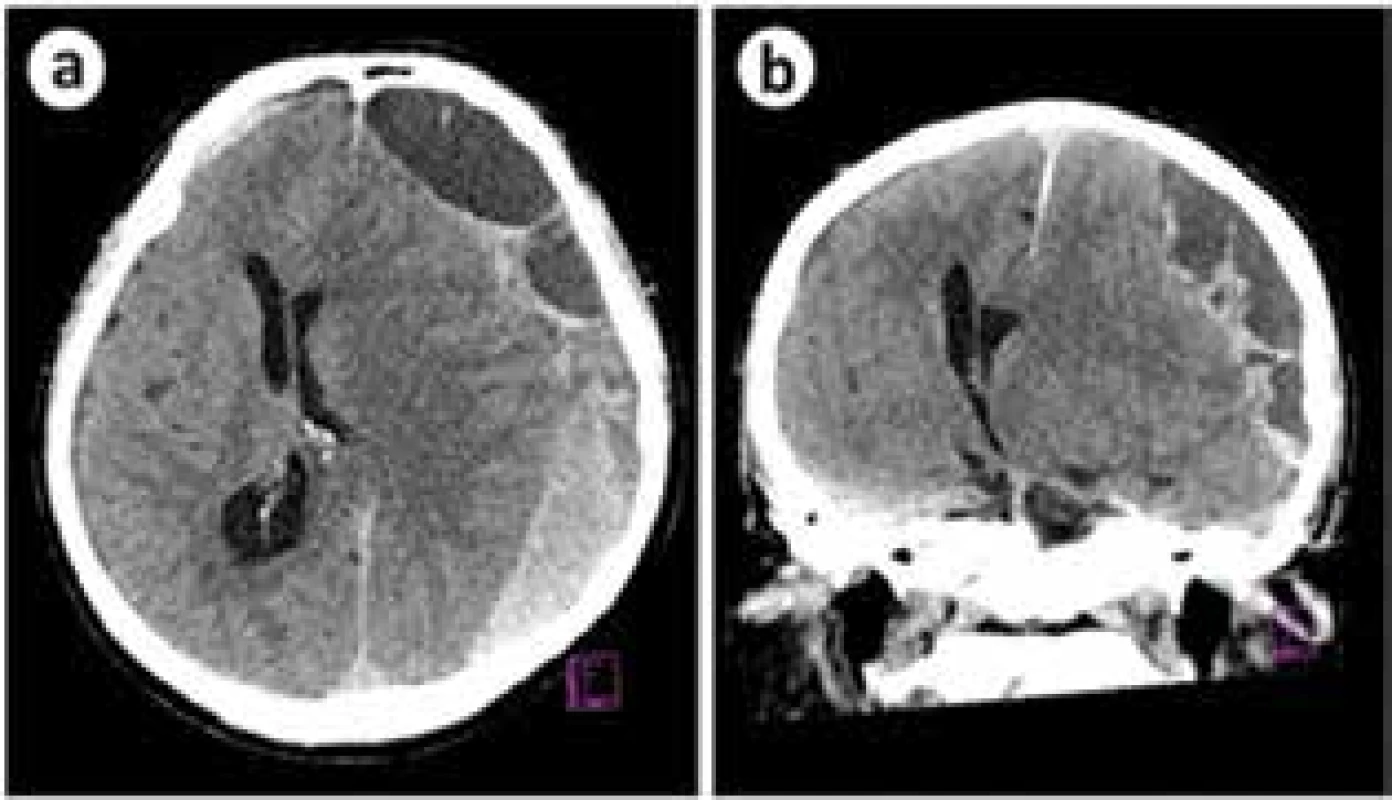
Sledování a prognóza
První grafická kontrola (CT) se provádí standardně do 48 hod. po operaci, kdy se zhodnotí rozsah event. rezidua ChSDH a vyloučí čerstvé krvácení [15]. Pokud je nález příznivý a pacient je bez neurologického deficitu, další CT mozku nejsou potřeba. V opačném případě opakujeme CT s odstupem 7−14 dní, nebo při zhoršení klinického stavu.
Pooperační péče se zaměřuje především na časnou rehabilitaci, vertikalizaci, nácvik chůze a aktivaci paretických svalů. Dlouhodobé užívání kortikoidů či antiepileptik není vhodné. Pacienti jsou poučeni, že opakované údery do hlavy, byť zdánlivě zanedbatelné, mohou přispět k recidivě krvácení.
Přestože se může zdát, že ChSDH není závažné onemocnění a operace je relativně banální, opak je pravdou (15). Dle literatury dosahuje perioperační morbidita 0–25 % a mortalita 0−32 % [17,18]. Dokonce po úspěšné evakuaci ChSDH je pozorován signifikantní nárůst mortality až 12 měsíců od operace [19]. Přestože tento fenomén není zcela vysvětlen, byl pozorován i u jiných chirurgických výkonů, jako např. u operace pro zlomeninu krčku femuru [20,21].
Recidiva
Operace pro ChSDH je i přes veškeré úsilí zatížena relativně vysokým rizikem recidiv. Pokud recidivu definujeme jako reakumulaci subdurální kolekce, jež se projeví klinicky, pak k ní dochází v 0,4−33,3 % případů [22].
Řadu faktorů zvyšujících riziko recidivy nemůžeme ovlivnit (např. věk pacienta, objem hematomu, septa v hematomu či těžký vstupní neurologický deficit), zatímco jiné ano. Relativně dobře podložená jsou doporučení týkající se některých technických detailů operace. Metaanalýzy potvrzují výhodnost zavedení drénu do dutiny hematomu, aniž by se zvýšil výskyt komplikací [23,24]. Santarius et al. provedli randomizovanou studii, která ukázala nejen nižší výskyt recidiv, ale i sníženou šestiměsíční mortalitu u pacientů, u kterých byl použit drén [25]. Kolikvovaná krev by měla být vyplachována sterilním roztokem, ideálně až do makroskopického vyčištění tekutiny [26]. Dalším nezávislým rizikovým faktorem pro recidivu ChSDH, který lze ovlivnit, je množství vzduchu které se dostane během operace do dutiny hematomu [6,27–30]. Snažíme se tedy v průběhu operace minimalizovat pneumocefalus tím, že dutinu hematomu vyplníme co nejvíce sterilním roztokem.
Častou otázkou v souvislosti s recidivou ChSDH bývá, kdy znovu nasadit antiagregační a antikoagulační léčbu. V literatuře nenalezneme jasná doporučení, většina prací se však shoduje, že antiagregancia a antikoagulancia nezvyšují riziko recidivy krvácení [6,11,31,32]. Přesto považujeme za vhodné důvod k dalšímu podávání těchto léků po operaci znovu přehodnotit ve spolupráci s internistou či kardiologem. Pokud indikace k jejich užívání trvá, pak je nasazujeme s odstupem alespoň 2 až 3 týdnů od operace.
Závěr
ChSDH je časté onemocnění, s nímž se ve své praxi setká každý všeobecný chirurg. Mezi nejčastější příznaky patří bolesti hlavy, zmatenost, kvantitativní porucha vědomí, hemiparéza a fatická porucha. U asymptomatických pacientů volíme konzervativní postup, u symptomatických je indikována léčba chirurgická – v první řadě návrt v lokální anestezii. Každý pacient s ChSDH by měl být konzultován na neurochirurgickém pracovišti se zkušeností s neurotraumatologií, ideálně v nemocnici se statutem traumacentra.
Podpořeno MO 1012.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise.
doc. MUDr. David Netuka, Ph.D.
Neurochirurgická a neuroonkologická klinika 1. LF UK ÚVN
U vojenské nemocnice 1200
169 02 Praha 6
e-mail: netuka.david@gmail.com
Zdroje
- Greenberg MS. Handbook of neurosurgery. 8th ed. Thieme 2016 [cited 2017 May 19]. Available from: https://books.google.cz/books/about/Handbook_of_Neurosurgery.html?id=0TC9Cns4Qz8C&redir_esc=y.
- Kudo H, Kuwamura K, Izawa I, et al. Chronic subdural hematoma in elderly people: present status on Awaji Island and epidemiological prospect. Neurol Med Chir (Tokyo). 1992;32 : 207–9.
- Cousseau DH, Echevarria MG, Gaspari M, et al. Chronic and subacute subdural haematoma. An epidemiological study in a captive population. Rev Neurol 2001;32 : 821–4.
- Asghar M, Adhiyaman V, Greenway MW, et al. Chronic subdural haematoma in the elderly--a North Wales experience. J R Soc Med 2002;95 : 290–2. Available from: http://www.pubmedcentral.nih.gov/articlerender.fcgi?artid=1279911&tool=pmcentrez&rendertype=abstract.
- Kolias AG, Chari A, Santarius T, et al. Chronic subdural haematoma: modern management and emerging therapies. Nat Rev Neurol. Nature Publishing Group 2014;10 : 570–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/25224156.
- Ohba S, Kinoshita Y, Nakagawa T, et al. The risk factors for recurrence of chronic subdural hematoma. Neurosurg Rev 2013, cited 2017;36 : 145–50. Available from: http://www.ncbi.nlm.nih.gov/pubmed/22696158.
- Seidl Z, Vaněčková M. Magnetická rezonance hlavy, mozku a páteře. 1. vyd. Praha, Grada 200
- Roh D, Reznik M, Claassen J. Chronic subdural medical management. Neurosurg Clin N Am. 2017;28 : 211–7. Available from: http://www.ncbi.nlm.nih.gov/pubmed/28325455.
- Emich S, Richling B, McCoy MR, et al. The efficacy of dexamethasone on reduction in the reoperation rate of chronic subdural hematoma--the DRESH study: straightforward study protocol for a randomized controlled trial. Trials [Internet]. BioMed Central 2014, cited 2017;15 : 6. Available from: http://www.ncbi.nlm.nih.gov/pubmed/24393328.
- Henaux P-L, Le Reste P-J, Laviolle B, et al. Steroids in chronic subdural hematomas (SUCRE trial): study protocol for a randomized controlled trial. Trials BioMed Central 2017, cited 2017;18 : 252. Available from: http://www.ncbi.nlm.nih.gov/pubmed/28583162.
- Okano A, Oya S, Fujisawa N, et al. Analysis of risk factors for chronic subdural haematoma recurrence after burr hole surgery: Optimal management of patients on antiplatelet therapy. Br J Neurosurg 2014, cited 2017;28 : 204–8. Available from: http://www.ncbi.nlm.nih.gov/pubmed/23952136.
- Majovsky M, Masopust V, Netuka D, et al. Flexible endoscope-assisted evacuation of chronic subdural hematomas. Acta Neurochir (Wien) 2016, cited 2017;158 : 1987–92. Available from: http://www.ncbi.nlm.nih.gov/pubmed/27473394.
- Kaiser R, Houšťava L, Mencl L, et al. Organizovaný chronický subdurální hematom – kazuistiky. Česká a slov neurol a neurochir 2011;74 : 353–6. Available from: http://www.medvik.cz/link/bmc 11034190.
- Kaiser R, Douda L, Waldauf P, et al. Zkušenosti s evakuací chronického subdurálního hematomu z návrtu kalvy. Česká a slov neurol a neurochir 2011;74 : 556–9. Available from: http://www.medvik.cz/link/bmc11042876.
- Dudoit T, Labeyrie P-E, Deryckere S, et al. Is systematic post-operative CT scan indicated after chronic subdural hematoma surgery? A case–control study. Acta Neurochir (Wien) 2016, cited 2017;158 : 1241–6. Available from: http://link.springer.com/ 10.1007/s00701-016-2820-6
- Uno M, Toi H, Horai S. Chronic subdural hematoma in elderly patients: Is this disease benign? Neurol Med Chir 2017;57 : 402–9. Available from: https://www.jstage.jst.go.jp/article/nmc/advpub/0/advpub_ra.2016-0337/_article
- Ducruet AF, Grobelny BT, Zacharia BE, et al. The surgical management of chronic subdural hematoma. Neurosurg Rev 2012;35 : 155–69. Available from: http://link.springer.com/10.1007/s10143-011-0349-y.
- Weigel R, Schmiedek P, Krauss JK. Outcome of contemporary surgery for chronic subdural haematoma: evidence based review. J Neurol Neurosurg Psychiatry 2003;74 : 937–43.
- Miranda LB, Braxton E, Hobbs J, et al. Chronic subdural hematoma in the elderly: not a benign disease. J Neurosurg 2011;114 : 72–6. Available from: http://www.ncbi.nlm.nih.gov/pubmed/20868215.
- Pitto RP. The mortality and social prognosis of hip fractures. A prospective multifactorial study. Int Orthop 1994, cited 2016;18 : 109–13. Available from: http://www.ncbi.nlm.nih.gov/pubmed/8039953.
- Hannan EL, Magaziner J, Wang JJ, et al. Mortality and locomotion 6 months after hospitalization for hip fracture: risk factors and risk-adjusted hospital outcomes. JAMA 2001, cited 2016;285 : 2736–42. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11386929.
- Ivamoto HS, Lemos HP, Atallah AN. Surgical treatments for chronic subdural hematomas: A comprehensive systematic review. World Neurosurg 2016, cited 2017;86 : 399–418. Available from: http://linkinghub.elsevier.com/retrieve/pii/S1878875015013686.
- Peng D, Zhu Y. External drains versus no drains after burr-hole evacuation for the treatment of chronic subdural haematoma in adults. In: Zhu Y, editor. Cochrane database of systematic reviews [Internet]. Chichester, John Wiley & Sons 2016, Available from: http://www.ncbi.nlm.nih.gov/pubmed/27578263.
- Almenawer SA, Farrokhyar F, Hong C, et al. Chronic subdural hematoma management. Ann Surg 2014;259 : 449–57. Available from: http://content.wkhealth.com/linkback/openurl?sid=WKPTLP:landingpage&an=00000658-201403000-00007.
- Santarius T, Kirkpatrick PJ, Ganesan D, et al. Use of drains versus no drains after burr-hole evacuation of chronic subdural haematoma: a randomised controlled trial. Lancet 2009, cited 2017;374 : 1067–73. Available from: http://www.ncbi.nlm.nih.gov/pubmed/19782872
- Liu W, Bakker NA, Groen RJM. Chronic subdural hematoma: a systematic review and meta-analysis of surgical procedures. J Neurosurg 2014, cited 2017;121 : 1–9. Available from: http://www.ncbi.nlm.nih.gov/pubmed/24995782.
- Shiomi N, Hashimoto N, Tsujino H, et al. [Relationship of direction of drainage tube and recurrence in chronic subdural hematoma.], Japanese, No Shinkei Geka 2002, cited 2017;30 : 823–7. Available from: http://www.ncbi.nlm.nih.gov/pubmed/121877
- Mori K, Maeda M. Surgical treatment of chronic subdural hematoma in 500 consecutive cases: clinical characteristics, surgical outcome, complications, and recurrence rate. Neurol Med Chir (Tokyo) 2001;41 : 371–81.
- Nakaguchi H, Tanishima T, Yoshimasu N. Relationship between drainage catheter location and postoperative recurrence of chronic subdural hematoma after burr-hole irrigation and closed-system drainage. J Neurosurg 2000;93 : 791–5. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11059659.
- Oishi M, Toyama M, Tamatani S, et al. Clinical factors of recurrent chronic subdural hematoma. Neurol Med Chir (Tokyo) 2001, cited 2017;41 : 382–6. Available from: http://www.ncbi.nlm.nih.gov/pubmed/11561348.
- Chari A, Clemente Morgado T, Rigamonti D. Recommencement of anticoagulation in chronic subdural haematoma: a systematic review and meta-analysis. Br J Neurosurg 2014, cited 2017;28 : 2–7. Available from: http://www.ncbi.nlm.nih.gov/pubmed/23834661.
- Hrabovský D, Chrastina J, Feitová V, et al. Vztah antikoagulační a antiagregační terapie u nemocných s chronickým subdurálním hematomem k závažnosti předoperačního stavu a výsledku chirurgické léčby. Rozhl Chir 2014;93 : 536–44. Available from: http://www.medvik.cz/link/bmc14080554.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2018 Číslo 6- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Chronický subdurální hematom − přehled
- Posttraumatický hydrocefalus
- Přínos opakovaných vyšetření počítačovou tomografií u pacientů s neurochirurgicko-neurologickou problematikou v intenzivní péči − retrospektivní analýza
- Epidurální hematom: benigní, nebo potenciální maligní onemocnění?
- Nová AOSpine klasifikace pro poranění subaxiální krční páteře a její využití v klinické praxi
- Subdurální empyém − kazuistika vzácného onemocnění s vysokou mortalitou
- Meralgia paresthetica
- Atypické řešení proximální nervové léze – kazuistika
- XXVII. Jarní setkání Loket 2018 na zámku Zbiroh
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Meralgia paresthetica
- Chronický subdurální hematom − přehled
- Epidurální hematom: benigní, nebo potenciální maligní onemocnění?
- Posttraumatický hydrocefalus
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



