-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Jednodobý výkon u aneuryzmatu břišní aorty a renálního karcinomu
Simultaneous procedure in patients with abdominal aortic aneurysm and renal carcinoma
Introduction:
Renal carcinoma (RC) is present in 0.1–3% of patients with abdominal aortic aneurysm (AAA). There are several options for surgical solution as regards the type and timing of the procedure. The authors discuss the simultaneous AAA resection and radical nephrectomy as a treatment option.Material and methods:
1168 patients with AAA including 19 (1.6%) with asymptomatic AAA (diameter >50mm) and RC (average diameter 74.3 mm) indicated for radical nephrectomy were operated on in the last 20 years (between 5/1994 and 5/2014). The average age of the patients was 72.8 years (55−85). Pre-operatively, sixteen patients were classified as ASA II, three as ASA III. Unilateral nephrectomy was performed in 18 and bilateral nephrectomy in one patient. One-stage AAA resection (1x endovascular aneurysm repair) with nephrectomy was performed in all patients.Results:
Two patients with ASA III classification died within 30 days postoperatively due to acute myocardial infarction and multiorgan failure. In the other patients, the simultaneous procedure was without any complications. Four patients died within two years after the operation due to generalized RC, the others have survived in the interval of one and twelve years after the procedure.Conclusion:
Simultaneous procedure does not represent increased operation load for patients with good health status. Nevertheless, the type of procedure should be optimised for each individual patient with regard to his or her general health status, life expectancy, disease symptomatology, the diameter of the RC and the anatomical conditions of AAA.Key words:
abdominal aortic aneurysm − renal carcinoma − simultaneous procedure
Autoři: V. Třeška 1; M. Hora 2; B. Čertík 1; J. Moláček 1; K. Houdek 1; J. Náhlík 1; P. Stránský 2
Působiště autorů: Chirurgická klinika FN a LF UK v Plzni, přednosta: prof. MUDr. V. Třeška, DrSc. 1; Urologická klinika FN a LF UK v Plzni, přednosta: prof. MUDr. M. Hora, PhD., MBA 2
Vyšlo v časopise: Rozhl. Chir., 2014, roč. 93, č. 8, s. 424-427.
Kategorie: Původní práce
Práce byla podpořena Výzkumným záměrem P 36, UK v Praze
Souhrn
Úvod:
Současný výskyt aneuryzmatu břišní aorty (AAA) a renálního karcinomu (RK) se pohybuje v rozmezí 0,1–3 % všech AAA. Možností operačních řešení z hlediska typu a načasování výkonů je několik. V článku řešíme problematiku chirurgického výkonu pro AAA kombinovaného v jedné době s radikální nefrektomií.Materiál a metodika:
Ve 20letém období (5/1994–5/2014) bylo operováno celkem 1168 nemocných pro AAA, u 19 (1,6 %) nemocných pak současně asymptomatické AAA (>50 mm) s RK (průměr 74,3 mm) indikovaných k radikální nefrektomii. Nemocní s AAA a RK indikovaní k záchovnému výkonu na ledvině (resekci) byli operováni ve dvou dobách a v souboru nejsou zahrnuti. Průměrný věk nemocných byl 72,8 roku (55−85). Předoperačně bylo 16 nemocných klasifikováno jako ASA II, tři jako ASA III. U 18 nemocných byla provedena jednostranná, u jednoho oboustranná nefrektomie s resekcí AAA (1krát s endovaskulární náhradou).Výsledky:
Zemřeli dva nemocní do 30 dní po operaci v důsledku akutního infarktu myokardu a multiorgánového selhání. Oba byli předoperačně klasifikováni jako ASA III. U ostatních nemocných jednodobý výkon proběhl bez komplikací. Čtyři nemocní zemřeli do dvou let po operaci na generalizaci RK, ostatní žijí v intervalu jednoho až dvanácti roků.Závěr:
Jednodobý výkon nepředstavuje pro nemocné v celkově dobrém stavu zvýšenou operační zátěž. Nicméně typ operačního řešení by měl být optimalizován pro daného nemocného s ohledem na jeho celkový stav, životní expektaci, symptomatologii onemocnění, velikost RK a anatomické poměry AAA.Klíčová slova:
aneuryzma břišní aorty − renální karcinom – jednodobý výkonÚvod
Se stárnutím populace se stále častěji setkáváme se současným výskytem AAA a RK. Ovlivňuje to i fakt, že incidence RK je v ČR nejvyšší na celém světě (v roce 2010 byla 27,1 nových případů na 100 tisíc obyvatel).
Volba optimálního léčebného postupu u nemocných se současným výskytem aneuryzmatu břišní aorty (AAA) a renálního karcinomu (RK) je společnou problematikou cévního chirurga, urologa, radiologa a dalších odborníků. V době sofistikovaných léčebných metod, jakými jsou endovaskulární léčba AAA (EVAR) a miniinvazivní urologické techniky, bychom mohli říci, že léčba těchto konkomitantních závažných onemocnění je vyřešená. Nicméně především volba operačního postupu je ovlivňována mnoha hledisky, jakými jsou celkový stav nemocného, symptomatologie daného onemocnění, anatomické poměry a samozřejmě i zkušeností operatéra.
Materiál a metodika
V letech 5/1994–5/2014 jsme operovali celkem 19 nemocných s diagnózou AAA a RK. Ve stejném období jsme řešili otevřenou nebo endovaskulární cestou (EVAR) 1168 nemocných s AAA. Jednalo se o 12 mužů a 7 žen průměrného věku 72,8 (55−85) roku. U všech nemocných šlo o asymptomatické AAA s průměrem větším než 50 mm, u kterých byl současně diagnostikován RK (13krát vlevo, 6krát vpravo, 1krát oboustranně) pomocí computerové tomografie (CT) bez známek generalizace (Obr. 1,2). Průměr RK byl 74,3 (72−81) mm. 16 nemocných bylo hodnoceno jako ASA II, tři nemocní pak ASA III. U všech nemocných jsme provedli radikální nefrektomii a v jedné době resekci AAA (u jednoho nemocného EVAR) – Tab. 1. Posloupnost výkonů závisela na volbě operatéra při daných anatomických poměrech obou onemocnění.
Obr. 1. Aneuryzma břišní aorty a renální karcinom dolní poloviny levé ledviny Fig. 1: Abdominal aortic aneurysm and renal carcinoma of the lower half of the left kidney 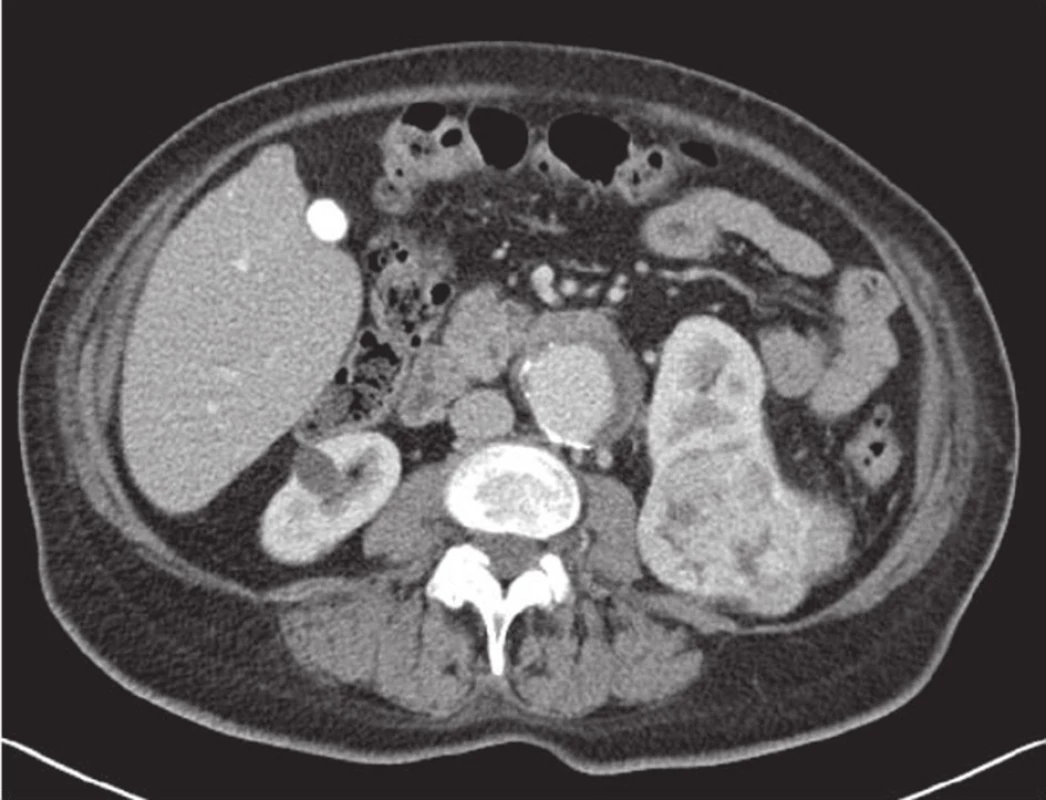
Obr. 2. Juxtarenální aneuryzma břišní aorty a renální karcinom střední části levé ledviny Fig. 2: Juxtarenal abdominal aortic aneurysm and renal carcinoma of the middle part of the left kidney 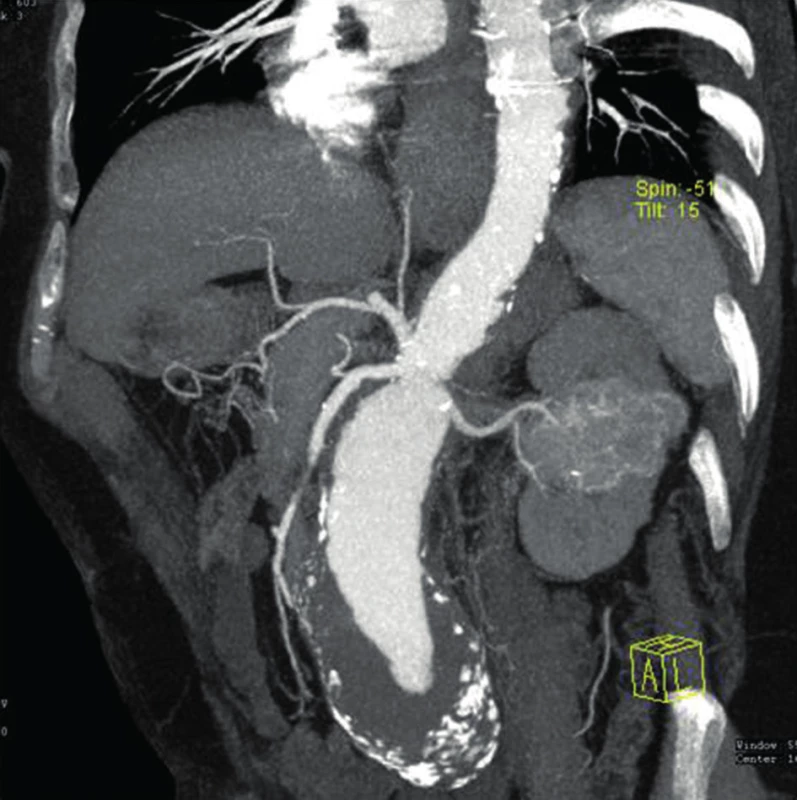
Tab. 1. Soubor nemocných s aneuryzmatem břišní aorty a renálním karcinomem (5/1994−5/2014) Tab. 1: Group of patients with AAA and renal carcinoma (5/1994– 5/2014) 
Výsledky
Průměrná délka operačního výkonu byla 140 min. (80–190 min.) a nelišila se v porovnání s délkou operace u nemocných s resekcí AAA (v průměru 130 min.). Zemřeli dva nemocní (10,5 %) s předoperační klasifikací ASA III. V prvním případě se jednalo o 85letého polymorbidního nemocného, kde operace proběhla bez komplikací, a v bezprostředním pooperačním období zemřel na akutní infarkt myokardu. U druhého, 59letého nemocného, v dialyzačním programu pro chronickou renální insuficienci na podkladě chronické glomerulonefritidy, jsme provedli resekci AAA a oboustrannou nefrektomii pro oboustranný RK, nemocný zemřel na multiorgánové selhání. Ostatní simultánní operace proběhly bez závažnějších pooperačních komplikací. U všech 18 nemocných s jednostrannou nefrektomií nedošlo v pooperačním období ke zhoršení renálních funkcí. Histopatologicky se jednalo o konvenční renální karcinomy klasifikované dle Fuhrmanové v 16 případech stupněm II–III a ve čtyřech stupněm I–II, bez cévní invaze a šíření do okolí. Čtyři nemocní zemřeli do dvou let po operaci na generalizaci RK, ostatní žijí v intervalu jednoho až dvanácti let (Tab. 2).
Tab. 2. Výsledky jednodobého výkonu Tab. 2: Results of the simultaneous procedure 
Diskuze
AAA je onemocněním vyššího věku. Jeho výskyt je zhruba u 6 % populace ve věku nad 50 let s maximálním výskytem v 6. a 7. deceniu. Kromě celé řady závažných komorbidit u nemocných vyššího věku přichází i vyšší pravděpodobnost výskytu maligního onemocnění. Incidence AAA a kolorektálního karcinomu v populaci se pohybuje v rozmezí 0,5–3,9 %, karcinomu žaludku 2−3,8 %, hepatocelulárního karcinomu 0,4−0,8 % a RK 0,1−3 %.
Etiopatogeneze AAA a RK má mnohé společné faktory. Kromě obecných predisponujících faktorů, jakými jsou vyšší věk, kouření a genetická predispozice, je pro obě patologické jednotky společná porucha extracelulární matrix v metabolismu kolagenu a elastinu, vyšší aktivita matrix-metalloproteináz [1,2]. Nepochybně relativně častější diagnostika AAA s RK je dána obecně vyšším záchytem obou onemocnění ultrasonografií (USG) a CT prováděnými za účelem diagnostiky výše uvedených onemocnění či jiné intraabdominální patologie.
Z léčebných postupů se v současnosti nabízí buď jednodobý, nebo dvojdobý výkon, EVAR, nebo otevřená resekce AAA [3,4], miniinvazivní, nebo otevřená nefrektomie včetně možnosti záchovného výkonu. Při volbě léčebného postupu musíme zohlednit několik zásadních otázek, kterými jsou symptomatologie AAA, RK, pokročilost nádorového onemocnění, celkový stav nemocného, anatomické poměry AAA [5,6].
Výhodou jednodobého, simultánního postupu zejména u nemocných s předoperační klasifikací ASA I–II je vyřešení obou závažných onemocnění v jedné době, bez zbytečného odkladu řešení zbývajícího onemocnění, které s sebou může přinášet svá rizika. Nemocný nepodstupuje dvojí operační zátěž. Některými autory diskutovaná možnost infekce cévní protézy při otevřeném způsobu léčby je minimální, resp. téměř nulová. Z našich dosavadních zkušeností není pooperační rekonvalescence po resekci AAA za současné nefrektomie delší a komplikovanější, než je tomu u samotné resekce AAA. Střední laparotomie je u jednodobého výkonu optimálním chirurgickým přístupem. Otázkou zůstává, zda resekci AAA provést napřed, nebo až po operaci RK. Někteří autoři zdůrazňují nebezpečí systémové antikoagulace [7,8], především tam, kde je prováděna resekce ledviny, a proto preferují provést resekci ledviny pro RK před resekcí AAA. Pokud provádíme radikální nefrektomii (ze stejné laparotomie s odklopením vzestupného nebo sestupného tračníku dle lokalizace nádoru ledviny), pak není rozhodující, jaký výkon provedeme jako první, a spíše se řídíme anatomickými poměry obou onemocnění.
Dvojdobý výkon je indikován především tam, kde jde o nemocného s rupturou AAA, kterou je možné řešit v první době otevřenou resekcí, nebo EVAR a v druhé době provést nefrektomii, nebo šetřící výkon laparoskopickou, nebo otevřenou cestou. Opačný postup je třeba zvolit u symptomatického (např. hematurie) RK, kde v první době řešíme RK a v druhé době AAA. Pokud zvolíme etapový výkon u asymptomatického AAA s RK, pak při volbě nefrektomie, nebo šetřícího výkonu v prvé době bychom měli výkon na AAA provést za jedné hospitalizace z důvodů nebezpečí ruptury AAA [9,10,11]. V pooperačním období jsou aktivovány proteolytické enzymy a může snáze dojít k ruptuře AAA. Z tohoto důvodu je také optimálnější volit řešení AAA v první době. Další indikací dvojdobého výkonu je parciální nefrektomie, kde by po podání antikoagulancia hrozilo krvácení z resekční plochy. Dvojdobý výkon volíme i tam, kde resekce AAA je komplikována např. krevní ztrátou, kterou musíme hradit krevními převody, v tomto případě pak ponecháváme nefrektomii nebo parciální resekci ledviny na druhou dobu.
Výhodou EVAR je malá operační zátěž a krátká doba hospitalizace, nevýhodou většinou dvojdobý výkon a opakované CT kontroly, které lze do jisté míry nahradit USG kontrolami za předpokladu kvalitního ultrasonografisty, který se touto problematikou zabývá. Nicméně jistá nevýhoda radiační zátěže nemocných při opakovaných CT je v rámci dispenzarizace nemocných po řešení RK prakticky smazána. Výhodou otevřené resekce AAA je snadná možnost jednodobého výkonu, který nevytváří pro nemocného vyšší operační zátěž.
V indikaci operační léčby RK při současném výskytu AAA se užívají stejná kritéria jako u izolovaného RK pro rozsah výkonu, nikoliv pro operační přístup. U nádorů klasifikace T1N0M0 (nádory do 7 cm) je preferován záchovný výkon, tedy resekce. U pokročilejších nádorů je indikována nefrektomie. Adrenalektomie je v současnosti indikována jen při postižení nadledviny tumorem dle CT, lymfadenektomii provádíme jen u makroskopicky zvětšených uzlin (dle CT, peroperační palpací). Jak u záchovných výkonů, tak nefrektomií je preferován laparoskopický přístup, je-li technicky možný. Při současném řešení AAA laparotomií je i výkon na ledvině prováděn otevřeným přístupem [12,13,14,15]. Je-li výkon dvojdobý (zejména u resekcí), pak preferujeme laparoskopii, pokud je výkon na ledvině prováděn jako první. Pokud je ledvina operována ve druhé době, pak dáváme přednost otevřenému translumbálnímu přístupu.
Závěr
Mortalita nemocných v našem souboru (10,5 %) je vysoká vzhledem k tomu, že dlouhodobá mortalita elektivních resekcí AAA je na naší klinice <3 %. Jednalo se o rizikové nemocné (ASA III), kteří byli operováni v první polovině sledovaného období. Dnes bychom jednoznačně indikovali u obou nemocných EVAR s následnou nefrektomií. V tomto ohledu je třeba dodat, že mortalita nemocných se simultánní operací AAA a RK je v našem souboru po roce 2006 nulová. Na uvedené mortalitě se nepochybně podílí i chyba malého čísla.
Symptomatologie AAA, jak jsme výše uvedli, je zásadní pro řešení AAA před RK, ať již v rámci jednodobého, nebo dvojdobého výkonu. RK by měl být řešen jako první v případě pokročilého nádoru ledviny (velikost nad 10 cm, kategorie ≥T2b), při přítomnosti nádorového trombu v renální nebo dolní duté žíle (T3b), při metastatickém postižení uzlin (zde je však na zváženou pouze konzervativní postup), přítomnosti infekce v postižené ledvině [16].
V případě celkově špatného stavu nemocného (ASA IV) je vždy třeba zvážit prognózu „guo ad vitam“ a u nemocných s krátkou životní expektací volit spíše konzervativní postup. U nemocného, který je indikován k resekci AAA, nebo k řešení EVAR s nefrektomií, je nutné z hlediska pooperačního renálního selhání znát funkci druhostranné ledviny, event. poruchy jejího tepenného zásobení na základě aterosklerotických stenóz magistrální tepny (předoperačně řešeny stentáží tepny). Pokud je funkce druhostranné ledviny snížena a nelze ji ovlivnit, pak je vhodné na nádorem postižené ledvině provést tzv. nefron šetřící výkon a aortální svorku při otevřeném výkonu používat co možná nejkratší dobu, event. využít některých protektiv renální funkce (např. fenoldopam) v perioperačním období resekce AAA.
Jak je patrné z textu, možností chirurgického řešení současného výskytu AAA a RK je několik a je na nás vybrat pro daného pacienta a daný okamžik optimální řešení. Jednodobý výkon především u programových operací u nemocných s nízkým operačním rizikem (ASA I–II) je výhodný a nepředstavuje pro nemocného nadměrnou operační zátěž. U symptomatických nemocných doporučujeme řešit na prvém místě stav, který symptomatologii vyvolal. U nemocných s vyšším rizikem (ASA III) je v současné době vhodné zvolit dvojdobý výkon (EVAR, miniinvazivní výkon na ledvině) s krátkým časovým intervalem (zpravidla do týdne – 14 dní) mezi oběma výkony. U nemocných ASA IV s krátkou životní expektací je na místě volba konzervativního postupu.
Prof. MUDr. Vladislav Třeška, DrSc.
U Českého dvora 11
326 00, Plzeň
e-mail: treska@fnplzen.cz
Zdroje
1. Qin Y, Cao X, Yang Y, Shi GP. Cysteine protease cathepsins and matrix metalloproteinases in the development of abdominal aortic aneurysms. Future Cardiol 2013;9 : 89–103.
2. Eberlová L, Tonar Z, Krížková V, Kocová J, Korabecná M, et al. Morfologie a etiopatogeneze aneuryzmatu abdominální aorty. Cas Lek Cesk 2012;151 : 55−63.
3. Třeška V, Čertík B, Kuntscher V, Šulc R, Moláček J, et al. Dlouhodobé výsledky operací výdutí abdominální aorty. Rozhl Chir 2010;89 : 300−305.
4. Porcellini M, Nastro P, Bracale U, Brearley S, Giordano P. Endovascular versus open surgical repair of abdominal aortic aneurysm with concomitant malignancy. J Vasc Surg 2007;46 : 16−23.
5. Jibawi A, Ahmed I, El-Sakka K, Yusuf SW. Management of concomitant cancer and abdominal aortic aneurysm. Ann R Coll Surg Engl 2012;94:e198–e200.
6. Habets J, Buth J, Cuypers PW, Nienhuijs SW, de Hingh IH. Infrarenal abdominal aortic aneurysm with concomitant urologic malignancy: treatment results in the era of endovascular aneurysm repair. Vascular 2010;18 : 14−19.
7. Bonardelli S, Cervi A, Nodari F, Guadrini C, Zanotti C, et al. Lesson learned from early and long-term results of 327 cases of coexisting surgical abdominal diseases and aortic aneurysms treated in open and endovascular surgery. Updates Surg 2012;64 : 125−130.
8. Kira S, Sawada N, Kudou S, Zakoji H, Kaga S, et al. Successful staged management of simultaneous abdominal aortic aneurysm and renal tumor: the novel minimally invasive treatment with endovascular aneurysm repair and retroperitoneal laparoscopic radical nephrectomy in an elderly and high-risk case. Clin Pract 2012;30 : 107−108.
9. Habets J, Buth J, Cuypers PW, Nienhuijs SW, de Hingh IH. Infrarenal abdominal aortic aneurysm with concomitant urologic malignancy: treatment results in the era of endovascular aneurysm repair. Vascular 2010;18 : 14−19.
10. Pattaras JG, Milner R. Staged minimally invasive treatment of inflammatory abdominal aortic aneurysm and renal cell carcinoma. Can J Urol 2009;16 : 4596−4598.
11. Somani BK, Nicol G, Bhavan R, Swami S, Nabi G. Synchronous resections of intra-abdominal pathologies during radical nephrectomy. A case-linked cohort study evaluation of outcomes. Eur J Surg Oncol 2009;35 : 844−851.
12. Veraldi GF, Tasselli S, De Manzoni G, Cordiano C. Surgical treatment of abdominal aortic aneurysm with concomitant renal cell carcinoma: a single-centre experience with review of the literature. J Cardiovasc Surg (Torino) 2006;47 : 643−649.
13. Hora M, Eret V, Ürge T, Stránský P, Klečka, et al. Results of laparoscopic resection of kidney tumor in everyday clinical practice. Central European Journal of Urology 2009;62 : 160−6.
14. Ljungberg B, Cowan NC, Hanbury DC, Hora M, Kuczyk MA, et al. EAU guidelines on renal cell carcinoma: the 2010 update. European urology 2010;58 : 398−406.
15. Hora M, Klečka J, Hes O, Ferda J, Urge T. Miniinvazivní laparoskopická nebo retroperitoneální radikální nefrektomie pro parenchymální nádor. Rozhl Chir 2005;84 : 246−52.
16. Třeška V, Hora M, Ferda J, Hes O, Ňaršanská A, et al. Nádorový trombus v dolní duté žíle při karcinomu ledviny. Rozhl Chir 2009;88 : 196−9.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek VolbyČlánek I. Podlahovy chirurgické dny
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2014 Číslo 8- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Chirurgie potřebuje víc sebevědomí
- Bariatrická metabolická chirurgie
- Porovnanie výsledkov použitia chirurgickej a endovaskulárnej liečby u pacientov s periférnym artériovým ochorením dolných končatín vo femoropopliteálnej oblasti
- Jednodobý výkon u aneuryzmatu břišní aorty a renálního karcinomu
- Ektopická parathyreoidea, zobrazovací metody a chirurgické přístupy
- Volby
-
Sarkomy hrudníku, má operační indikace smysl?
Soubor kazuistik - Spontánní pneumomediastinum (Hammanův syndrom)
- 100 let od narození primáře MUDr. Ludovíta Szaboa
- I. Podlahovy chirurgické dny
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Spontánní pneumomediastinum (Hammanův syndrom)
- Bariatrická metabolická chirurgie
-
Sarkomy hrudníku, má operační indikace smysl?
Soubor kazuistik - Porovnanie výsledkov použitia chirurgickej a endovaskulárnej liečby u pacientov s periférnym artériovým ochorením dolných končatín vo femoropopliteálnej oblasti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



