-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Radiofrekvenční ablace tumorů pankreatu
Radiofrequency Ablation (RFA) of Pancreatic Tumors
The authors refer about their first experience with radiofrequency ablation of locally advanced pancreatic tumors. They put forward the prospective study of five patients (four with ductal adenocarcinoma of the head and one with malignant neuroendocrine tumor of pancreatic body), who either because of local advanced disease or performance status, were not able to undergo radical curative surgery. All patients underwent peroperative radiofrequency ablation of pancreatic tumors. In the case of pancreatic head localization, posterior retrocolic gastro-enterostomy and hepatico-jejunostomy to Y Roux jejunal loop were performed. There was no perioperative mortality. In one case duodenal leak apeared in the fourth postoperative day. This was healed conservatively by drainage. At one patient the subfascial absces developed. This was solved by drainage reoperation at the fourteenth postoperative day. After consolidation, all patients were released to home care.
Conclusion:
According to our early experience, radiofrequency ablation of inoperable pancreatic tumors is relatively save cytoreductive procedure.Key words:
pancreatic tumor – radiofrequency ablation – cytoreduction – paliation
Autoři: J. Hlavsa 1; Z. Kala 1
; V. Válek 2; M. Mikulica 1; M. Man 1; V. Procházka 1
; I. Kiss 3
Působiště autorů: Chirurgická klinika, Fakultní nemocnice Brno-Bohunice a lékařská fakulta Masarykova univerzita, Brno, přednosta: Prof. MUDr. Zdeněk Kala, CSc. 1; Radiologická klinika Fakultní nemocnice Brno-Bohunice a lékařská fakulta, Masarykova univerzita, Brno, přednosta: Prof. MUDr. Vlastimil Válek, CSc., MBA 2; Oddělení klinické onkologie Fakultní nemocnice Brno-Bohunice a lékařská fakulta, Masarykova univerzita, Brno, primář: MUDr. Igor Kiss, Ph. D. 3
Vyšlo v časopise: Rozhl. Chir., 2008, roč. 87, č. 9, s. 462-466.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Autoři referují o prvních zkušenostech s radiofrekvenční ablací lokálně pokročilých tumorů pankreatu. Předkládají prospektivní studii souboru 5 pacientů (4x duktální adenokarcinom hlavy, 1x maligní neuroendokrinní tumor těla pankreatu), u kterých buď z důvodů lokální pokročilosti tumoru nebo celkového stavu pacienta, nebyl indikován radikální chirurgický zákrok. Všichni pacienti podstoupili peroperační radiofrekvenční ablaci pankreatického tumoru. V případě lokalizace tumoru v hlavě pankreatu (čtyři případy) byl výkon doplněn o zadní retrokolickou gastro-entero anastomózu a hepatiko-jejuno anastomózu na exludovanou Y Roux kličku jejuna. Perioperační mortalita byla nulová. V jednom případě se s odstupem několika dní po operaci objevila duodenální píštěl, která byla vyřešena konzervativně drenáží. U jednoho pacienta se vyvinul subfasciální absces, jež si 14. pooperační den vynutil operační revizi s drenáží. Všichni pacienti byli zhojeni a posléze propuštěni do domácí péče.
Závěr:
Podle našich prvních zkušeností, je radiofrekvenční ablace inoperabilních tumorů pankreatu relativně bezpečnou cytoredukční metodou.Klíčová slova:
tumor pankreatu – radiofrekvenční ablace – rytoredukce – paliaceÚVOD
V roce 1891 pozoroval francouzský fyzik D‘Arsanval při svých pokusech zajímavý jev. Při stimulaci živých tkání střídavým proudem o frekvenci kolem 250 kHz docházelo totiž k jejich výraznému zahřívání, které vedlo až ke koagulační nekróze. Tento objev se následně stal podkladem vynálezu nazvaného jako elektrický nůž (elektrokauter), který byl oficiálně poprvé klinicky využit roku 1926 věhlasnými neurochirurgy Cushingem a Boviem pro exstirpaci nádoru mozku. Později se zjistilo, že stejného principu lze při zasunutí jedné z elektrod do tkáně využít pro její tepelnou destrukci. Vzhledem k tomu, že používané frekvence střídavého proudu se blížily frekvenci radiových vln, byly tyto proudy označeny jako radiofrekvenční a destrukce tkáně, kterou působily jako radiofrekvenční ablace (RFA). Po neurochirurgii dalším oborem, ve kterém RFA našla své místo byla kardiologie, kde je již od konce 80. let dvacátého století využívána k ablaci aberantních srdečních drah. Teprve až v devadesátých letech dvacátého století proniká RFA do onkologie jako jedna z „tumordestrukčních“ metod. Doposud byla použita k destrukci primárních i sekundárních malignit jater, plic, prsu, ledvin, nadledvin, sleziny, prostaty, kostí, mozku a intrahepatálních žlučových cest [1–16]. Její využití v léčbě pankreatických nádorů je dosud raritní.
V současnosti lze ve světové literatuře nalézt 6 prací popisujících klinické užití RFA pro destrukci tumorů pankreatu [17–22]. Největší soubor referuje profesor Wu Y z Číny, který prezentuje zkušenosti s RFA u 16 pacientů s duktálním adenokarcinomem pankreatu. V devíti případech se jednalo o tumor hlavy. Sedmkrát byl ablován tumor těla nebo kaudy. Pro ablaci zde byly použity elektrody firmy Radionics s možností chlazení hrotu (tzv. cool-tip elektrody – teplota hrotu udržována pod 30 °C) [19]. Tabulka 1 ukazuje peri - a pooperační komplikace týmu profesora Wu Y. Dlouhodobější klinický efekt ve smyslu doby přežití či zhodnocení ovlivnění pooperační bolesti autor ve své práci nezmiňuje. Práce ostatních autorů jsou spíše jednotlivými kazuistikami.
Tab. 1. Peri- a pooperační komplikace a jejich časový odstup od výkonu Tab. 1. Peri- and postoperative complications and time delay after surgery 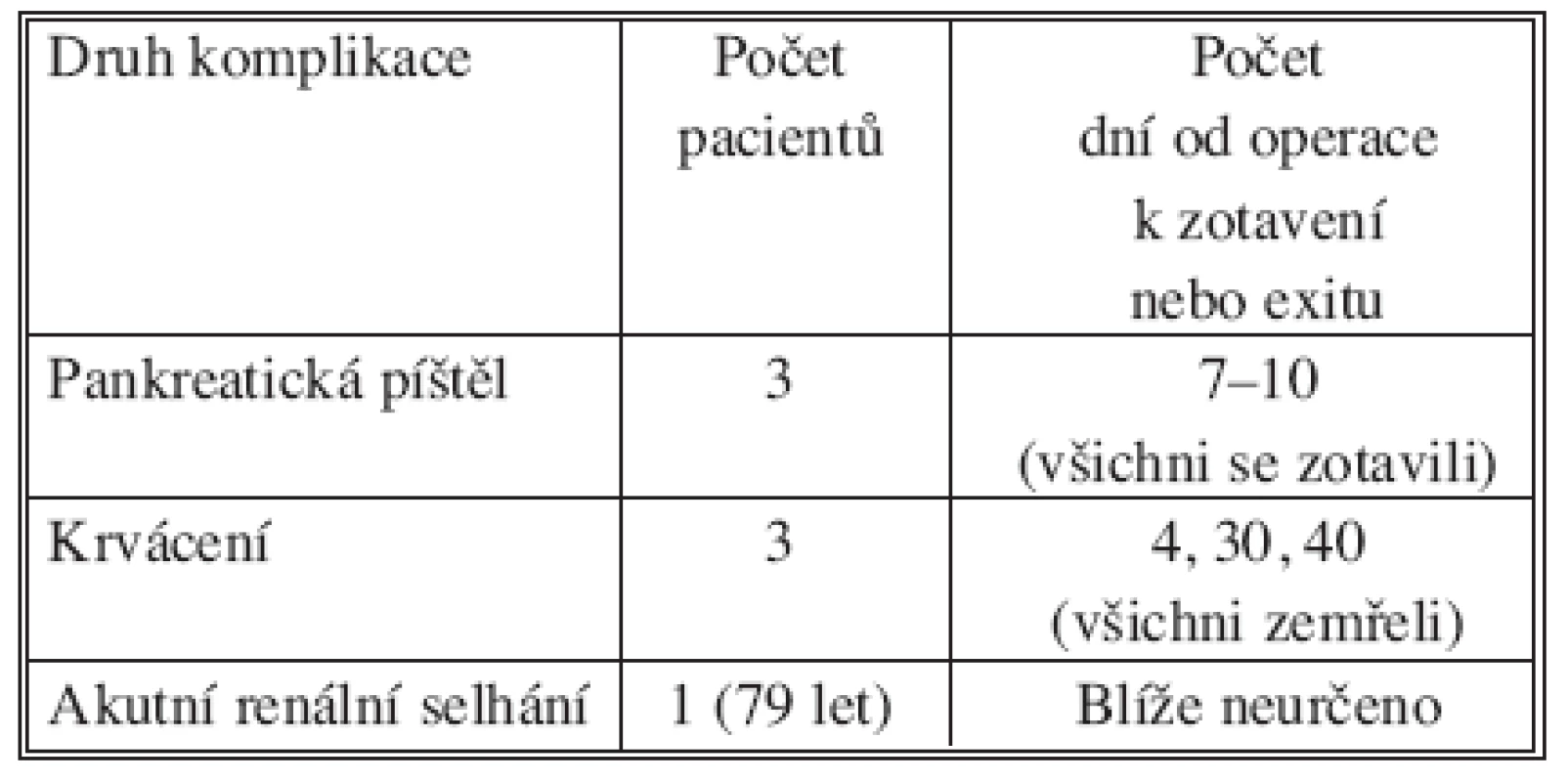
Pozn.: U všech pacientů, kteří zemřeli pro masivní portální krvácení, byl ablován tumor hlavy pankreatu Note: All patients, who died of massive portal bleeding, underwent ablation of the tumor of the pancreatic head SOUBOR A METODY
Po schválení etickou komisí FN Brno a probrání jednotlivých případů multioborovou indikační komisí, podstoupilo během ledna a února 2007 na chirurgické klinice FN Brno 5 pacientů radiofrekvenční ablaci maligního tumoru pankreatu. K ablaci byli indikováni nemocní s lokálně pokročilým maligním tumorem pankreatu, a/nebo pacienti, kteří nebyli, z důvodů celkového stavu, schopni radikálního resekčního výkonu. Ve čtyřech případech se jednalo o duktální adenokarcinom hlavy, jedenkrát byl ablován maligní neuroendokrinní tumor těla pankreatu. Podmínkou ablace byla nepřítomnost vzdálených metastáz. RFA byla u všech provedena peroperačně, kdy po příčné laparotomii, exploraci břišní dutiny, peroperační ultrasonografii jater, Kocherově manévru a exploraci pankreatu včetně peroperační ultrasonografie, byla za ochrany dolní duté žíly rukou operatéra vloženou dorzálně za hlavu slinivky, do tumoru zavedena elektroda (Obr. 1). Místo vpichu bylo voleno na základě posouzení vztahu tumoru k retropankreaticky jdoucím cévám pomocí peroperační ultrasonografie. Při nutnosti více vpichů jsme se ve snaze minimalizovat riziko vzniku pankreatické píštěle snažily, aby všechny další aplikace elektrody do tumoru procházely kapsulou ve stejném místě jako první vpich, jen byli jinak směrovány. Po ukončení ablace jsme defekt v kapsule přešily monofilním nevstřebatelným vláknem (Prolene 4/0). Před vlastní aplikací elektrod jsme v místě předpokládaného vpichu provedli Trucut biopsii (pokud nebyla provedena předoperačně). Pro ablaci byly použity generátory a elektrody RITA firmy Rita Medical Systems a Radionics firmy Tyco. Byly zvoleny ablačním protokoly užívané pro parenchymové orgány s dobou ablace do 5 minut na jeden vpich. Ve čtyřech případech (4/5) jsme použili přístroje Radionics v pulzním protokolu s výkonem 200W a kontrolou impedance. Třikrát byla použita cluster elektroda. Jedenkrát jednoduchá cool-tip elektroda. V jednom případě (1/5) byla ablace provedena přístrojem Rita (výkon 150 W s kontrolou teploty 90 °C, 5cm elektrodou bez proplachu fyziologickým roztokem).
Obr. 1. RFAmaligního neuroendokrinního tumoru těla pankreatu pomocí cluster elektrody Fig. 1. RFA of a malignant pancreatic neuroendocrine tumor, using a cluster electrode. 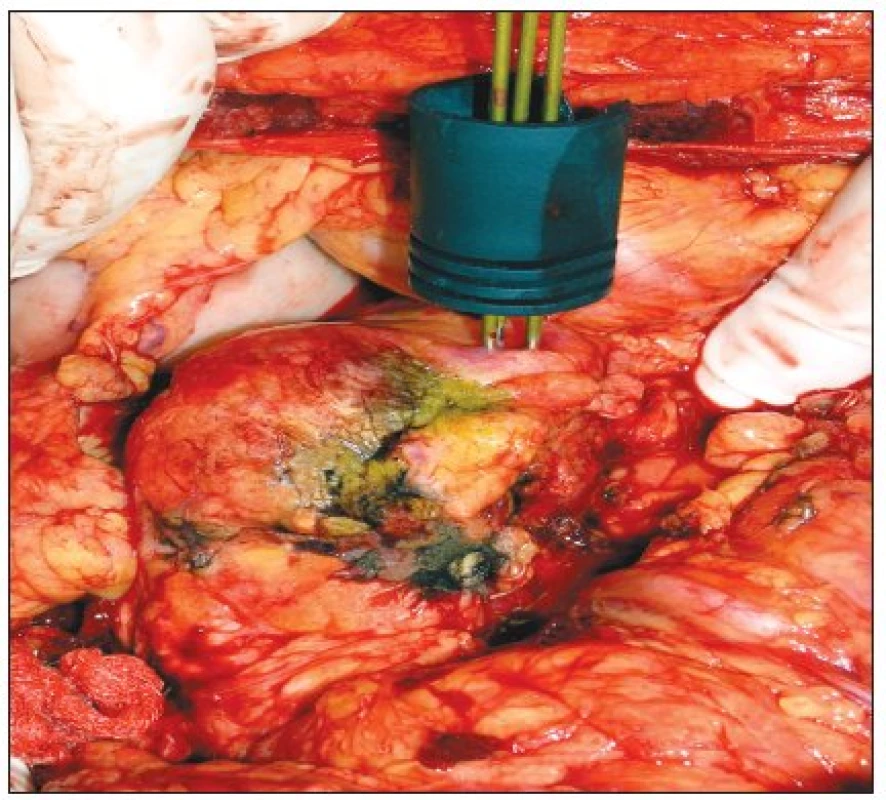
Obr. 2. Stejný tumor po provedení RFA Fig. 2. The same tumor following the RFA procedure 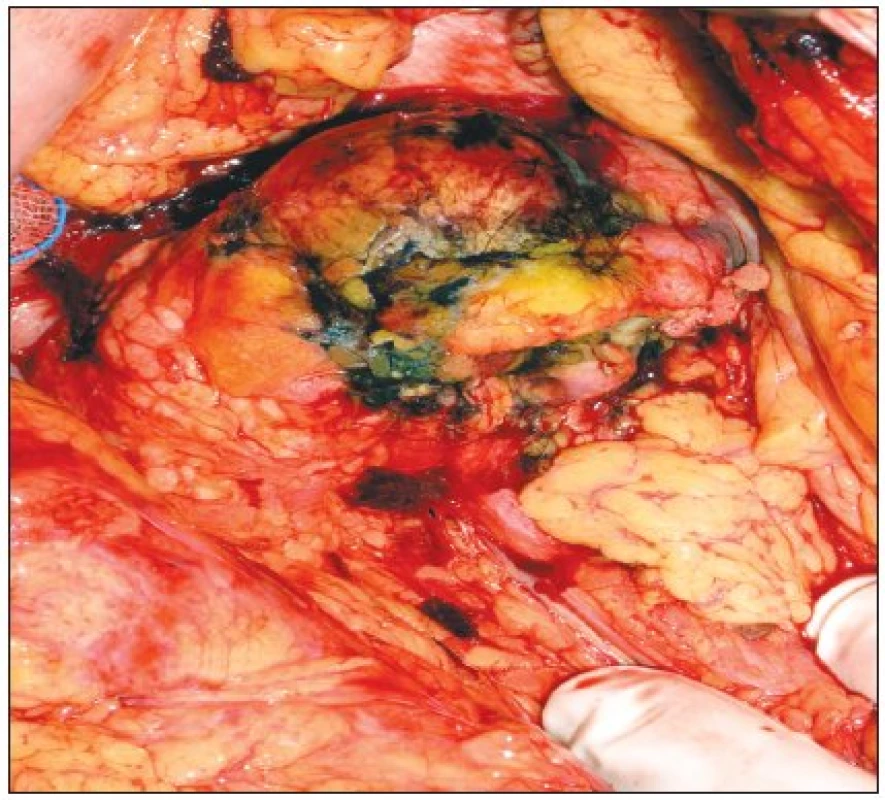
Obr. 3. Předoperační CT zobrazující maligní neuroendokrinní tumor těla pankreatu Fig. 3. Preoperative CT scan depicting a tumor of the pancreatic head 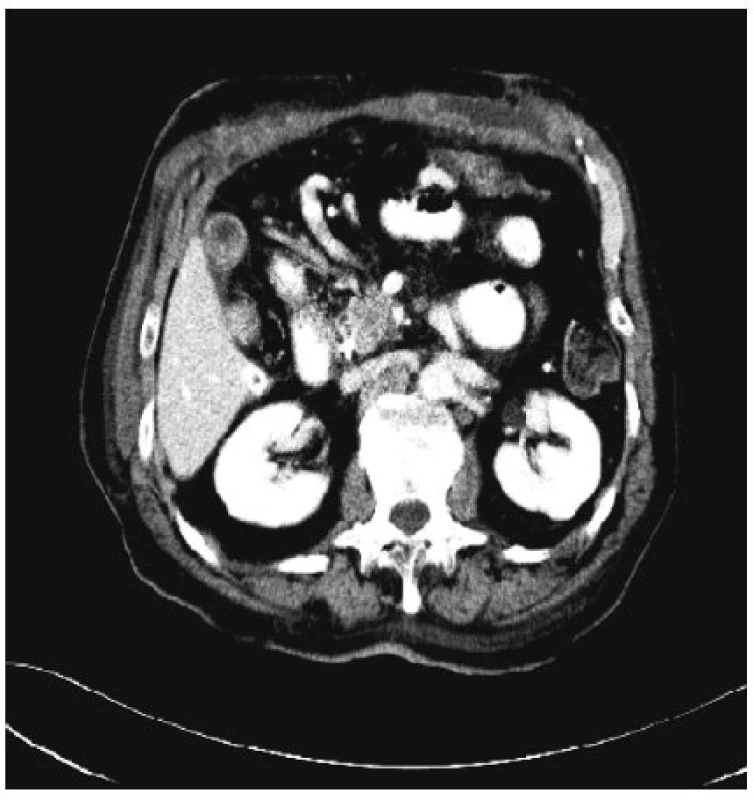
Obr. 4. Tentýž tumor těla pankreatu 7 dní po RFA Fig. 4. The same tumor of the pancreatic head 4 days after the RFA procedure 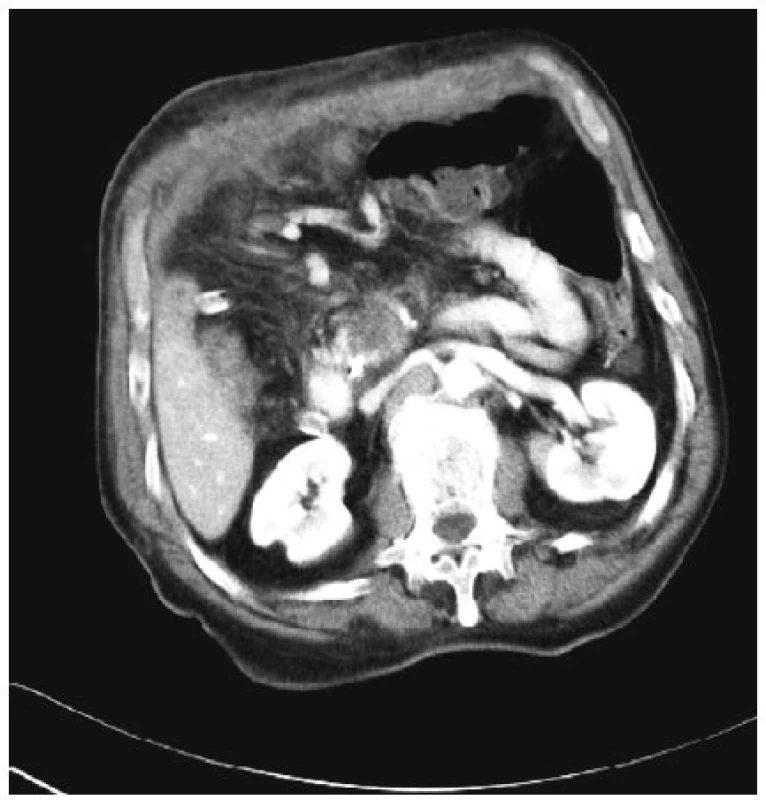
Obr. 5. Tentýž tumor těla pankreatu 3 měsíce po RFA Fig. 5. The same tumor of the pancreatic head 3 months after the RFA procedure 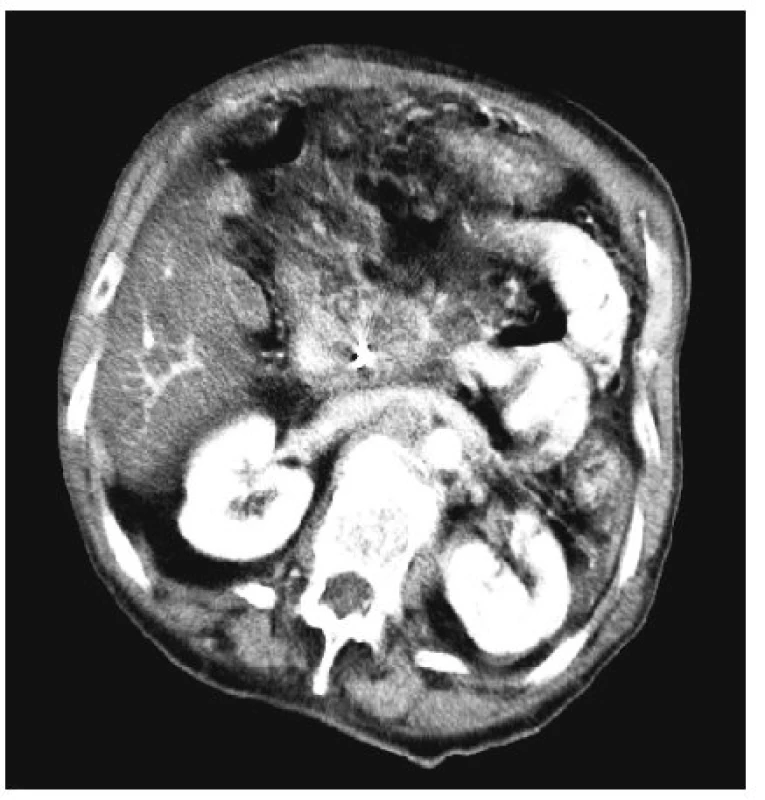
V případě lokalizace tumoru v hlavě (4 pacienti), byl výkon doplněn o zadní retrokolickou gastro-entero anastomózu a hepatiko-jejuno anastomózu na Y Roux kličku jejuna. Hepatiko-jejuno anastomóza na Y Roux kličku byla preferována z důvodů prevence ascendentní cholangoitidy. K oblasti ablovaného tumoru byly na konci operace vloženy 2 břišní drény, které jsme i v případě nulové sekrece ponechávali minimálně do sedmého pooperačního dne.
Po operaci byli všichni pacienti přeloženi na jednotku intenzivní péče. V pooperačním období byla, kromě standardních laboratorních parametrů (CRP, krevní obraz, bilirubinémie, jaterní testy atd.) sledována dynamika sekrece z břišních drénů včetně hladiny amyláz v sekretu z drénů i v séru. U každého pacienta bylo v odstupu 3–7 dnů a 3 měsíců od operace provedeno kontrolní kontrastní CT pankreatu k posouzení morfologických změn v ablovaném ložisku. Pacienti jsou dále sledováni. Je hodnocena jejich kvalita života se zřetelem na intenzitu bolestí a nutnost analgetizace.
VÝSLEDKY
Peroperační mortalita byla nulová. U 3 pacientů byl peri - i pooperační průběh zcela bez komplikací. V jednom případě se 4. pooperační den objevila duodenální sekrece z břišního drénu. Stav byl zvládnut konzervativně na drénu a pacient byl po jeho vytažení se zahojenou ránou 20. pooperační den propuštěn do domácí péče. V jednom případě jsme 14. pooperační den byli nuceni v celkové anestezii evakuovat subfasciální absces. I tento pacient se následně zhojil a 38. den byl propuštěn do domácí péče. U žádného pacienta jsme nezaznamenali krvácení ani pankreatickou píštěl. Komplikace jsou shrnuty v tabulce 2.
Tab. 2. Komplikace Tab. 2. Complications 
Pozn.: Z celkového počtu 5 pacientů se u 2 objevily perioperační komplikace, které jsou popsány v této tabulce. V obou případech se jednalo o duktální adenokarcinom hlavy pankreatu Note: Two, out of the total of 5 patients, developed intraoperative complications, presented in the Table. In the both cases, the patients suffered from ductal adenocarcinoma of the pancreatic head DISKUSE
Karcinom pankreatu je jedním z nejmalignějších solidních tumorů vůbec. Celkové pětileté přežití se v Evropě pohybuje okolo 5 %, přičemž většina pacientů se po „kurativní“ resekci nedožívá více jak 18 měsíců [23]. Za jedinou potenciálně „kurativní“ léčebnou metodu je považována R0 resekce, tedy odstranění tumoru do makroskopicky i mikroskopicky tumornegativní tkáně [24, 25]. Neoadjuvantní resp. adjuvantní chemoterapie, radioterapie, či jejich kombinace jsou indikovány pouze v rámci klinických studií a nejsou v současnosti standardem. Pacienti s lokálně inoperabilními tumory, metastazujícími tumory či pacienti, kteří nejsou, vzhledem k celkovému stavu, schopni podstoupit radikální resekční výkon (nejčastěji HPDE) jsou tedy „odsouzeni“ k paliativním procedurám typu stentáže žlučových cest, biliodigestivní spojce případně gastro-entero anastomóze, bez možnosti standardní léčebné alternativy. Častým problémem jsou v takovýchto případech bolesti způsobené tlakem rostoucího tumoru na retropankreatické nervové plexy. Svou roli hraje také psychika. Zavedení RFA ablace tumorů pankreatu by tedy mohlo přinést v této oblasti unikátní možnost cytoredukce nádoru s možným analgetickým a pozitivním psychologickým efektem pro pacienta.
Nejvíce obav z aplikace této metody právě na pankreas, plyne z jeho úzkého vztahu k velkým cévám (vena portae, vena et arteria mesenterica superior, vena cava inferior, arteria hepatica comunis, arteria gastroduodenalis), dvanáctníku a retropankreatické části ductus choledochus. Poranění těchto struktur může být pro pacienta fatální. Mechanismus poranění může být dvojí: 1. mechanické poranění – nabodnutí elektrodou, 2. termické poranění. V prvním případě lze rizika minimalizovat správným vedením jehly v dostatečně přehledném operačním poli a její navigací peroperační ultrasonografií. K termickému poranění jsou obecně náchylnější anatomické struktury, které nejsou protékány krví a nejsou tak přirozeně ochlazovány. V tomto případě jde tedy o duodenum a retropankreatickou část choledochu. Jejich poraněním vzniká duodenální respektive žlučová píštěl, které lze ve většině případů vyřešit konzervativně drenáží [19]. Při ablaci tumorů hlavy pankreatu je vhodné výkon doplnit o hepatiko-jejuno anastomózu na exludovanou kličku jejuna, a eliminovat tak riziko vzniku žlučové píštěle. Další možnou komplikací je vznik pankreatické píštěle vznikající na podkladě fokální nekrózy pankreatu v místě RFA s leakem pankreatické šťávy do DB. Tuto lze také ve většině případů vyřešit konzerativně – drenáží. Poranění peripankreatických tepen a žil je podle mála dostupných prací ve 100 % smrtelné [19].
Výše zmíněným „termickým“ komplikacím lze teoreticky předejít správnou navigací ablační elektrody a vhodným ablačním protokolem. Přitom je nutné si uvědomit, že cílem není ablovat až do makroskopicky patrné koagulační nekrózy tumoru, ale zvýšit v co největší části tumoru teplotu nad 60 stupňů Celsia, tedy nad teplotu, při které denaturují buněčné bílkoviny, což vede k buněčné smrti. Co se četnosti výše zmíněných komplikací týče, v literatuře nejčastěji popisovanými komplikacemi jsou pankreatická píštěl a krvácení z peripankreatických cév [19]. Námi zaznamenaná duodenální píštěl není podle malého množství dostupných prací příliš častá.
Přestože při použití některých ablačních elektrod a protokolů lze teroreticky odhadnout tvar a průměr ablovaného ložiska a je možno monitorovat teplotu v jeho centru, posouzení, zda opravdu všechny nádorové buňky byly zničeny není prakticky možné. RFA nelze tedy považovat za analogii R0 resekce a jako takovou za metodu kurativní, od které by bylo možné očekávat významnější prodloužení doby přežití. Cytoredukce může však zpomalit lokální růst nádoru a tak oddálit nástup bolestí. Druhým analgetickým mechanismem by mohla být destrukce vlastních retropankreatických nervových plexů. K posouzení analgetického efektu této metody je však třeba rozsáhlejších studií.
ZÁVĚR
Radiofrekvenční ablace lokálně neresekabilních nádorů pankreatu je cytoredukční metodou, kterou je nutné dále zkoumat a získat na větších souborech přesnější klinická data. Naše pilotní studie prokázala, že se jedná o metodu snadnou, reprodukovatelnou a relativně bezpečnou i pro polymorbidní pacienty. Zda bude však mít pozitivní klinický efekt ukáže čas.
MUDr. J. Hlavsa
Komenského 314
679 04 Adamov
e-mail: hlavsjan@seznam.cz
Zdroje
1. Varshney, S., et al. Radiofrequency tissue ablation: an early Indian experience. Indian J. Gastroenterol., 2003, 22 : 91–93.
2. Zhang, Z., et al. Percutaneous radiofrequency ablation of liver malignancies, Zhonqhua Wai Ke Za Zhi, 2001, 39 : 749–752.
3. Huo, T. I., et al. Percutaneous therapy for hepatocellular carcinoma:current practice and future prospectives. J. Chin. Med. Assoc., 2005, 68 : 155–159.
4. Jansen, M. C., et al. Outcome of regional and local ablative therapies for hepatocellular carcinoma: a collective review. Surg. Oncol., 2005, 31 : 331–347.
5. Lencioni, R., et al. A critical appraisal of the literature on local ablative therapies for epatocellular carcinoma.
6. Simon, C. J., et al. Current role of image-guided ablative therapies in lung cancer. Expert. Rev. Anticancer Ther., 2005, 5 : 657–666.
7. Suh, R. D., et al. Unresectable pulmonary malignancies: CT guided percutaneous radiofrequency ablation – preliminary results. Radiology, 2003, 229 : 821–829.
8. Nogutchi, M., et al. Minimally invasive surgery for small breast cancer. J. Surg. Oncol., 2003, 84 : 94–101.
9. Singletary, E. S., et al. Feasibility of radiofrequency ablation for primary breast cancer. Breast cancer, 2003, 10 : 4–9.
10. Boss, A., et al. Magnetic resonance – guided percutaneous radiofrequency ablation of renal cell carcinoma: a pilot clinical study. Invest. Radiol., 2005, 40 : 583–590.
11. Wood, B. J., et al. Radiofrequency ablation of adrenal tumors and adrenocortical carcinoma metastases. Cancer, 2003, 97 : 554–560.
12. Milicevic, M., et al. Elective resection of the spleen – overview of resection technics and description of a new technic based on radiofrequency coagulation and seddication. Acta Chir. Iugosl., 2002, 49 : 19–24.
13. Shariat, S. F., et al. Pilot study of radiofrequency interstitial tumor ablation (RITA) for the treatment of radio-reccurent prostate cencer. Prostate, 2005, 64 : 260–267.
14. Martel, J., et al. Percutaneous radiofrequency treatment of osteoid osteoma using cool tip electrode. Eur. J of Radiol., 2005.
15. Ganaadha, S., et al. Safety and efficacy of radiofrequency ablation of brai: a potentially minimally invasive treatment for brain tumors. Minim. Invasive Neurosurg., 2004, 47 : 325–328.
16. Chiou, Y. Y., et al. Percutaneous ultrasound guided radiofrequency ablation of intrahepatic cholangiocarcinoma. Kaohsiung J. Med. Sci., 2005, 21 : 304–309.
17. Varshney, S. , Sewkani, A., Sharma, S., Kapoor, S., Naik, S., Sharma, A, Patel, K. Radiofrequency ablation of unresectable pancreatic carcinoma: feasibility, efficacy and safety. JOP, 2006, Jan 11;7(1): 74–78.
18. Spiliotis, J. D., Datsis, A. C., Michalopoulos, N. V., Kekelos, S. P., Vaxevanidou, A., Rogdakis, A. G., Christopoulou, A. N. Radiofrequency ablation combined with palliative surgery may prolong survival of patients with advanced cancer of the pancreas. Arch. Surg., 2007, Jan; 392(1): 55–60.
19. Wu, Y., Tang, Z., Fang, H., Gao, S., Chen, J., Wang, Y., Yan, H. High operative risk of cool-tip radiofrequency ablation for unresectable pancreatic head cancer. J Surg Oncol., 2006, Oct 1; 94(5): 392–395.
20. Date, R. S., Siriwardena, A. K. Radiofrequency ablation of the pancreas. II: Intra-operative ablation of non-resectable pancreatic cancer. A description of technique and initial outcome. JOP, 2005, Nov 10; 6(6): 588–592.
21. Matsui, Y., Nakagawa, A., Kamiyama, Y., Yamamoto, K., Kubo, N., Nakase, Y. Selective thermocoagulation of unresectable pancreatic cancers by using radiofrequency capacitive heating. Pancreas, 2000, Jan; 20(1): 14–20.
22. Siriwardena, A. K. Radiofrequency ablation for locally advanced cancer of the pancreas. JOP, 2006, Jan 11; 7(1): 1–4.
23. Evans, D. B., Pisters P. W. T., Abbruzzese J. L. Pancreatic cancer chapter 1, page 3, tumor oncology series, springer 2002.
24. http://www.cancer.org/docroot/CRI/content/CRI_2_4_4X_Treatment_of_Pancreatic_Cancer_by_Stage_34.asp?rnav=cri
25. Moon, H. J., Jang, K. T., Heo, J. S., Choi, S. H., Joh, J. W., Kim, Y. I. Korean J. Gastroenterol., 2003, Aug; 42(2): 156–163.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek Komentář k článkuČlánek Redakční pošta
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2008 Číslo 9- Metamizol jako analgetikum první volby: kdy, pro koho, jak a proč?
- Nejlepší kůže je zdravá kůže: 3 úrovně ochrany v moderní péči o stomii
- Stillova choroba: vzácné a závažné systémové onemocnění
- Metamizol v léčbě různých bolestivých stavů – kazuistiky
-
Všechny články tohoto čísla
- Může být moderní chirurgie levná?
- Torakoskopická tymektomie – iniciální zkušenosti
- Cystické neoplazie slinivky břišní
- Náhla príhoda brušná po biopsii duodena
- Radiofrekvenční ablace tumorů pankreatu
- Komentář k článku
- Interdisciplinární evropská závazná doporučení pro chirurgickou léčbu těžké obezity
- Zatvorená zlomenina femoru komplikovaná tupým poranením a poúrazovou oklúziou a. femoralis superficialis – kazuistika
- Zlomeniny mediálního klíčku – Souhrnný referát
- Šestiměsíční funkční a rentgenové výsledky zlomenin distálního radia ošetřených multidirekcionálními zamykatelnými dlahami
- Profesor Jan Wechsler – životní jubileum
- Redakční pošta
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Zlomeniny mediálního klíčku – Souhrnný referát
- Cystické neoplazie slinivky břišní
- Náhla príhoda brušná po biopsii duodena
- Torakoskopická tymektomie – iniciální zkušenosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



