-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Hypernatrémie – frekvence, příčiny, patobiochemie, klinika a terapie
Hypernatremia – Frequency, Causes, Pathobiochemistry, Clinic and Therapy
Objective: Presentation of the current knowledge of hypernatremia in terms of their causes, frequency and pathobiochemical connections in the development and treatment of these ion dysbalances.
Study type: Synoptic
Settings: Institute of Medical Biochemistry and Laboratory Diagnostics, First Faculty of Medicine and General University Hospital, Prague
Material and Methods: Based on the study of available literature, this survey describes the frequency, causes and risks of hypernatremia in critically ill. Some studies evaluate hypernatremia regardless of the time when it developed. Other differentiate whether it developed before hospitalization or later, during intensive care. Compensation of hypernatremia is described as well as the treatment.
Results: The frequency of hypernatremia in three large cohorts of patients admitted to ICU of various specializations was between 2.0 % and 6.9 %. Its value is given by the increase in the relationship between Na+ supply and water in extracellular fluid (ECF). Hypernatremia causes an increase in osmolality in ECT. The following shift of intracellular fluid to ECF causes the dehydration of cells. These changes in brain cells cause a number of serious subjective and objective neurological symptoms. The brain compensates the disturbance by increasing the content of ions and small organic molecules in the cells. Binding of water to these particles enables at least partly to restore the size of brain cells and ameliorates the symptoms of the disturbance. The causes of hypernatremias developed before hospitalization as well as during intensive care are mentioned. Laboratory investigations enabling to differentiate the causes of the state are described. The effects of hypernatremia on metabolism and organ functions are presented. Significant relation of hypernatremia to many clinical complications and comorbidities is described as well as its causes in the elderly are mentioned. Therapeutic procedures and correction time limits are described.
Conclusion: Although hypernatremia is often in relation to many other severe clinical situations and organ dysfunctions, it is a significant, independent predictor of mortality.
Keywords:
mortality – hypernatremia – hyperosmolality – demyelinisation – brain edema
Autoři: A. Kazda
Působiště autorů: Ústav lékařské biochemie a laboratorní diagnostiky 1. LF UK a VFN, Praha
Vyšlo v časopise: Klin. Biochem. Metab., 27, 2019, No. 4, p. 164-171
Souhrn
Cíl studie: Zpracovat aktuální znalosti o hypernatrémiích z hlediska jejich příčin, frekvence a patobiochemických souvislostí při vývoji a léčení těchto iontových dysbalancí.
Typ studie: Přehledná práce.
Název a sídlo pracoviště: Ústav lékařské biochemie a laboratorní diagnostiky 1. LF UK a VFN, Praha.
Materiál a metody: Na základě studia literatury je v přehledné práci popsána frekvence, příčiny a rizika hypernatrémie u kriticky nemocných. Některé studie hodnotí hypernatrémii bez ohledu na dobu, kdy se vyvinula, jiné diferencují, zda vznikla již před hospitalizací nebo až během intenzivní péče. Je popsána kompenzace poruchy a její léčení.
Výsledky: Frekvence hypernatrémie byla ve třech rozsáhlých souborech nemocných akutně přijímaných na jednotky intenzivní péče různých klinických oborů, mezi 2 % až 6,9 %. Její hodnota je dána zvýšením poměru mezi zásobou Na+ v extracelulární tekutině (ECT) a objemem vody v ECT. Hypernatrémie vede ke zvýšení osmolality v ECT. Následující přesun intracelulární tekutiny do ECT vede k dehydrataci buněk. Tyto změny postihují i mozkové buňky, a to vyvolává řadu závažných subjektivních i objektivních neurologických příznaků. Mozek kompenzuje poruchu zvýšením obsahu iontů a malých organických molekul v buňkách. Vazba vody na tyto částice umožňuje alespoň zčásti upravit velikost mozkových buněk a zmírňuje projevy poruchy. Jsou uvedeny příčiny hypernatrémie vzniklé před hospitalizací i během intenzivní péče. Jsou popsána laboratorní vyšetření přispívající k diferenciální diagnostice příčin stavu. Jsou uvedeny vlivy hypernatrémie na zhoršení metabolismu a orgánových funkcí. Je popisován významný vztah hypernatrémie k mnoha klinickým komplikacím a komorbiditám, i její příčiny u starých osob. Jsou popsány terapeutické postupy i časové limity korekce.
Závěr: I když je hypernatrémie často ve vztahu k mnoha dalším vážným klinickým situacím a orgánovým dysfunkcím, je významným, nezávislým faktorem mortality.
Klíčová slova:
hypernatrémie – hyperosmolalita – demyelinizace – edém mozku – mortalita
Hypernatrémie
Hypernatrémie je definována jako klinický stav se zvýšením plazmatické látkové koncentrace sodného kationtu nad 145 mmol/L. Patří mezi život ohrožující iontové dysbalance s komplikovanou patofyziologií, závažnými klinickými příznaky a zhoršenou prognózou.
Při hypernatrémii vzniká osmotický gradient mezi extracelulární tekutinou (ECT) s vyšší osmolalitou a intraceluIární tekutinou (ICT) s osmolalitou nižší. Dochází proto k přesunu vody z ICT do ECT, aby se osmolality v obou prostorách vyrovnaly. Dehydratace buněk postihuje i mozek, a to určuje subjektivní i objektivní příznaky hypernatrémie.
K hypernatrémii vedou stavy, kdy se mění poměr mezi zásobou Na+ a jeho distribučním prostorem (tj. poměr mezi množstvím Na+ v ECT a velikostí ECT) ve prospěch Na+. Zásoba Na+ může při ní být zvýšená, fyziologická nebo i snížená (pokud se objem vody snížil ještě více). Kromě laboratorních nálezů je proto vždy nutno hodnotit i anamnézu a klinický stav. Hypernatrémie vede vždy k přesunu vody z ICT do ECT (obr. 1).
Fig. 1. The schema of three water compartments and the movement of components determining the serum osmolality in state of hypernatremia. Abbreviations: IVF = intravasal fluid, ISF = interstitial fluid, ICF = intracellular fluid 
Klasifikace hypernatrémie
Výskyt hypernatrémie je nižší než výskyt hyponatrémie díky mechanismu žízně. Žízeň je stimulována hypovolémií a aby vznikla, musí deficit plazmy dosáhnout 8-10 %, zatímco zvýšení osmolality pouze o 1-2 % stačí ke stimulaci žízně. Mocným faktorem žízně je angiotenzin [1]. Tíže hypernatrémie je klasifikována do tří rozsahů. Mírná 146-150 mmol/L, střední 151-154 mmol/L a těžká >155 mmo/L [2-6]. Někteří autoři užívají jako kritéria uvedených rozsahů hodnoty vyšší, a to 151-155 mmol/L, 156-160 mmol/L a >160 mmol/L [7, 8]. Jiné rozsáhlé studie vycházejí naopak ze zjištění, že mortalita významně roste již při hodnotách S-Na+ <138 mmol/L a >142 mmol/L. Proto považují za normonatrémii jen hodnoty mezi 138-142 mmol/L. Prokazují, že již hodnoty S-Na+ 143-147 mmol/L jsou spojeny s nepříznivou prognózou [9]. Přes uvedené i další rozdíly v klasifikaci natrémie dospívají všechny tyto i další studie shodně k závěru, že s hypernatrémií a její tíží se zhoršuje prognóza pacienta z hlediska mortality, délky pobytu na oddělení (zpravidla JIP), vyhlídka na jednoduché ukončení hospitalizace propuštěním domů i výše nákladů na hospitalizaci [1,8,9].
Za období 21 let byla analyzována všechna měření natrémie u 80 571 nemocných, přijatých na JIP dvou univerzitních nemocnic v Holandsku, průměr počtu vyšetření na jednoho pacienta 11±20, pozorován posun hodnot. Frekvence hyponatrémie postupně klesala ze 47 na 25 % (p<0,001), a naopak frekvence hypernatrémie se zvyšovala ze 13 na 24 % (p<0,001). Uvažované důvody tohoto přesunu: zvýšené užívání infuzí s Na+, vliv diuretik a hydrokortizonu [10].
Příčiny hypernatrémie
Klinické studie věnované hypernatrémii se zaměřují na dvě oblasti. Zaprvé na hypernatrémii, se kterou jsou nemocní k hospitalizaci přijímáni (community acquired hypernatremiae – CAH) a zadruhé na hypernatrémii vzniklou během léčení na JIP (intensive care acquired hypernatremia – IAH). Výjimečně je sledována i prognóza nemocných, kteří byli s hypernatrémií z nemocnice propuštěni.
Hypernatrémie je vždy provázena zvýšením osmolality. Ve vztahu k zavodnění jsou tři možnosti.
- Hypovolemická hypernatrémie, při níž dochází k depleci vody a Na+, deplece vody je výraznější. Příčiny: renální ztráty (osmotická a kličková diuretika, poobstrukční diuréza, polyurická fáze akutní tubulární nekrózy, pokročilá onemocnění ledvin), gastrointestinální ztráty (zvracení, průjem, enterokutánní píštěle), jiné (pocení, popáleninové trauma, otevřené rány).
- Euvolemická hypernatrémie, kdy dochází ke ztrátě čisté vody bez odpovídající ztráty Na+. V klinické praxi se jedná o nejčastější formu. Příčiny: diabetes insipidus centrální (CDI) s deficitem ADH, nebo nefrogenní (NDI), kdy ledviny na ADH nereagují, a dále hypodypsie a mimorenální ztráty insenzibilní perspirací.
- Hypervolemická hypernatrémie, v důsledku nadbytku vody a relativně ještě většího nadbytku Na+. Příčiny: infúze hypertonických solí Na+, nadměrný příjem NaCl p.o. [11].
Při akutním příjmu je nejčastější formou hypovolemická CAH. Jako IAH vzniká nejčastěji hypernatrémie normovolemická, i když se recentně ukazuje, že i hypovolemická je frekventnější než se dříve soudilo. Obecně je nejméně frekventní hypernatrémie hypervolemická [1,4].
Přehled léků vedoucích k hypernatrémii a mechanismy jejich působení jsou uvedeny v Tabulce 1. [4]. Nověji jsou uváděny ještě léky další – vincristin, methoxyfluran [12].
Tab. 1. Drugs causing hypernatremia [4] ![Drugs causing hypernatremia [4]](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image_pdf/9fe1075c8c588a94b5f5722a88ea69e3.png)
Hypernatrémie při příjmu
Rozsáhlé soubory nemocných, ve kterých je hodnocena frekvence dysnatrémií, prokazují jednoznačně vyšší frekvenci hyponatrémie než hypernatrémie. V nedávném přehledu problematiky hyponatrémie byly frekvence obou poruch uvedeny [13]. Zde jen připomeňme, že v souboru 151 486 nemocných (Rakousko) přijímaných na interní, chirurgické či smíšené JIP byla frekvence hypernatrémie mírné (146-150 mmol/L) 5,1 %, střední (151-154 mmol/L) 1,2 % a těžké (>155 mmo/L) 0,6 %. Mortalita v těchto kategoriích byla 21,1 %, 36,2 % a 46,1 %. Mortalita nemocných s normonatrémií byla 9,7 % [2]. V jiné studii byla v souboru 10 923 nemocných léčených na chirurgických JIP (Německo) zjištěna hypernatrémie >145 mmol/L ve 2,5 %. I tato hypernatrémie byla ve významném vztahu k mortalitě [14]. A konečně, ve studii z pracovišť urgentního příjmu byla mezi 43 911 přijatými nemocnými (Švýcarsko a Rakousko) frekvence natrémie >145 mmol/L ve 2 % a >149 mmol/L v 0,2 % [15].
Hypernatrémie vzniklá během léčení na JIP
- K zvýšení S-Na+ během intenzivní léčby může dojít z více objektivních důvodů:
- Nemocný nemůže regulovat příjem vody v důsledku stavu vědomí, sedace, umělé ventilace, případně má omezený příjem tekutin z různých důvodů (aspirace).
- Vysoké renální ztráty vody (osmotická diuréza při terapii manitolem nebo glykosurii, kličková diuretika, porucha koncentrační schopnosti), agresivní dialýza s vysokou koncentrací Na+.
- Gastrointestinální příčiny (pooperační stavy, ileus, krvácení).
- Ztráty kůží a plícemi (horečky, popáleniny, hyperventilace).
- Infuze solných roztoků [16,17].
Studie podílu příčin na vzniku hypernatrémie během léčby na JIP uvádějí pozitivní bilanci Na+ v 38 %, negativní bilanci vody ve 44 %, obojí v 18 % [6]. Byl hodnocen vývoj hypernatrémie za ≥ 24 hodin od přijetí na JIP v souboru 8 140 hospitalizovaných nemocných. Mírné zvýšení 146-150 mmol/L bylo u 901 z nich (11,1 %), střední a těžké nad 150 mmol/L u 344 (4,2 %). Faktory, které byly v nezávislém vztahu k tomuto vývoji: mužské pohlaví, tíže stavu při přijetí, hodnota skóre SAPS II (míra závažnosti postižení orgánových funkcí), nutnost resuscitace při příjmu a orgánová selhání. Mortalita nemocných bez hypernatrémie byla 15,2 %, s mírnou hypernatrémií 29,5 % a se střední a těžkou 46,2 % [5].
Další ze studií zkoumala soubor 74 nemocných léčených na JIP interní (27), traumatologické (16) a chirurgické (31) s výskytem hypernatrémie v průměru za 2,6 dní po přijetí, trvání 3 – 5 dní. Ve srovnání se souborem 100 nemocných bez hypernatrémie, byl u hypernatremických delší pobyt na JIP (11 : 4,8 dní, p < 0,001) a vyšší mortalita (43 %:15 %, p < 0,001) [6].
Příznaky zvýšení efektivní osmolality
Typické příznaky jsou neurologické a souvisejí s dehydratací mozku. Mezi subjektivní příznaky se řadí dráždivost, neklid až zmatenost, nebo naopak letargie; rizikoví jsou zejména staří lidé, kteří mívají snížený pocit žízně.
Za objektivní příznaky se považují svalové záškuby, hyperreflexie a spasticita. Vzestup S-Osm >350 mmol/kg vede ke křečím a k poruchám vědomí až ke kómatu. Prudký vývoj hypernatrémie, a tím i dehydratace mozku, může vést k demyelinizaci a intracerebrálnímu krvácení.
U dětí je mortalita v souvislosti se základním onemocněním provázeným akutní hypernatrémií odhadována na 45 %. U dospělých je vzestup S-Na+ >160 mmol/L spojován se 60 % i vyšší mortalitou [18,19].
Mozková kompenzace hypernatrémie
Laboratorní hodnoty, při nichž je porucha symptomatická, jsou při akutním vzniku S-Na+ >150 mmol/L, resp. S-Osm >310 mmol/kg. Při vícedenním vývoji je to až při S-Na+ >160 mmol/L, resp. S-Osm >330 mmol/kg.
Důvodem toho, že při pomalejším vývoji poruchy snášíme daleko extrémnější zvýšení S-Na+ a S-osm, je kompenzace v mozkových buňkách. Zvyšuje se v nich počet osmoticky efektivních částic, nejdříve iontů (do 24 hod.), později i malých organických molekul (do 48 hod.). Vazbou vody na tyto částice je zajištěn návrat části vody do mozkových buněk, a to i při dehydrataci v celém organismu. Časový vývoj této kompenzace musí ovšem respektovat i následná terapeutická úprava hypernatrémie. Kdyby byl pokles S-Na+ neúměrně rychlý, nestačily by se mozkové buňky zbavit kompenzačně zvýšených osmoticky efektivních částic a hrozil by otok mozku [1,4,12].
Laboratorní vyšetření
Je nutné nejen pro monitorování hypernatrémie a její léčby, ale i pro zjištění příčin, zejména při snížené hladině vědomí, která často tyto stavy provází. Osmolalita moče (U-Osm) je funkcí sekrece ADH. Její vyšetření je účelný úvodní test ke kategorizaci etiologie a zjištění, zda je zachována renální koncentrační schopnost.
Příčiny hypernatrémie mohou být dle U-Osm kategorizovány následovně:
- a. Hypernatrémie s U-Osm <300 mmol/kg (nebo nižší než osmolalita plazmy) svědčí pro CDI nebo NDI. K diferenciaci těchto stavů je podán exogenní ADH (obvykle jako farmakologický analog DDAVP, desmopressin acetát) a výsledkem je zvýšení U-Osm při CDI. Nemocní s NDI již měli maximální sekreci ADH, ale s resistencí na něj na úrovni ledvin, a proto se U-Osm podáním DDAVP nezmění.
- b. Hypernatrémie s U-Osm >800 mmol/kg, svědčí o tom, že sekrece ADH a odpověď na něj jsou normální. Koncentrační schopnost je zachována. Situace nastává při nehrazených ztrátách vody (z GIT, z respiračního traktu, kůží nebo při zvýšení zásoby Na+ v těle po jeho nadbytečném přívodu.
- c. Hypernatrémie s intermediární U-Osm 400-800 mmol/kg. Může jít o parciální NDI nebo CDI, tedy o vodní diurézu s deplecí objemu nebo probíhá osmotická diuréza. Možnými důvody vzniku tohoto typu hypernatrémie jsou nadměrné vylučování Na+ i Cl-, urey, nebo vylučování manitolu či glukózy [1,4].
Při podezření na osmotickou diurézu je nutné vyšetřit celkové množství vylučovaných solutů. Celkové vylučování solutů = U-Osm x objem moče l/24 h. Při západní dietě je běžně vylučováno 600-900 mmol/24 h. Hodnota vylučování >1000 mmol/24 h (nebo přesněji >15 mmol/kg/24 h) svědčí pro osmotickou diurézu [1,4]. Pro přesnější určení typu diurézy slouží snadno dostupné funkční renální parametry, které vycházejí z běžně vyšetřovaných analytů a počítačového hodnocení. Jsou to frakční exkrece vody, osmolální, Na+ a clearance bezsolutové a bezelektrolytové vody [20, 21]. Hodnota clearance bezelektrolytové vody (EWC) informuje navíc o reakci ADH na zvýšení osmolality při hypernatrémii:
- EWC <0,4 l/24 h (<0,046 ml/s) = normální odpověď ADH na zvýšení osmolality,
- EWC >0,4 l/24 h (>0,046 ml/s) = abnormální odpověď ADH (diabetes insipidus).
Odhad insenzibilní ztráty vody, tj. perspirací a vydechovaným vzduchem je podle některých autorů 30 – 40 ml/h [1], dle jiných 40 – 50 ml/h [4] nebo 700 ml/24h. Od tohoto množství je ovšem třeba pro bilanci vody odečíst produkci metabolické vody, vznikající při trávení živin, asi 300 ml/24 h [22]. Při horečce se připočítá dalších asi 3,5 ml/kg/24 h na každý 1° zvýšení teploty nad 37°C. Při silném pocení nebo hyperventilaci se tyto ztráty podstatně zvyšují.
Vzhledem k dalším možným dysbalancím iontů provázejícím dysnatrémie je třeba monitorovat i hladiny K+ a celkového Ca. Hypokalémie (<3 mmol/L) a hyperkalcémie (>2,75 mmol/L) narušují koncentrační schopnost ledvin a mohou přispívat k rozvoji hypernatrémie [1,4].
Vliv hypernatrémie na metabolismus a orgánové funkce
- stupňuje se periferní rezistence na inzulin, sklon k hyperglykémii,
- klesá jaterní glukoneogeneze a clearance laktátu,
- neuromuskulární poruchy, svalová slabost,
- zhoršují se podmínky pro přerušení UPV,
- zhoršení kardiálních funkcí, pokles kontraktility levé komory,
- u diabetiků zvyšuje riziko žilní trombózy,
- v experimentu u zvířat indukuje zvýšení cytokinů [9, 16, 23, 24].
Hypernatrémie a akutní onemocnění mozku
Důvody pro hypernatrémii u kriticky nemocných z neurologických příčin: zhoršené vnímání žízně, tělesná neschopnost se napít, zvýšené ztráty vody při komorbiditách s horečkami, dysfunkce hypotalamu nebo hypofýzy s vodní diurézou při diabetu insipidu. Navíc jsou tito nemocní často léčeni osmotickými diuretiky nebo hypertonickou solí ke snížení nitrolebního tlaku (ICP). Je prokázáno, že zvýšení natrémie hodnotu ICP snižuje. Tato iatrogení hypernatrémie pomáhá na jedné straně úspěšně kontrolovat ICP, ale na druhé straně je hypernatrémie obecně spojena s vyšší morbiditou i mortalitou. Není dost důkazů, že toto úmyslné zvyšování natrémie nebo užití osmotických diuretik je jednoznačně prospěšné [23, 25, 26].
Byla sledována frekvence a prognóza dysnatrémií a jejich vztah k S-Osm neurologicko-neurochirurgické jednotky intenzivní péče (NNJIP). Bylo hodnoceno 1440 nemocných s akutním onemocněním mozku. Během hospitalizace mělo 251 (17 %) z nich hyponatrémii (<135 mmol/L) a 75 (5 %) hypernatrémii (>150 mmol/L). Hyponatrémie spojená s hypoosmolalitou séra byla zjištěna pouze u 50 (20 %) z 251 nemocných s hyponatrémií. Hypernatrémie byla na rozdíl od hyponatrémie významným prediktorem mortality během pobytu na NNJIP, během té doby zemřelo z 251 hyponatremických nemocných 7 (2,88 %), ze 75 hypernatremických 14 (18,66 %). OR 5,3, p=0,002 [27]. Také jiné studie prokazují, že riziko mortality je u traumat mozku při hypernatrémiích významně vyšší než při hyponatrémiích [26].
Studie hypernatrémie vzniklé během léčení na JIP – IAH. V retrospektivní studii byly hodnoceny nálezy vybraných klinických parametrů tíže stavu u 1756 nemocných při přijetí na JIP. Do studie nebyli zařazeni nemocní s natrémií <130 a > 150 mmol/L. Statisticky byla hodnocena významnost rozdílů příjmových nálezů mezi skupinou, u které se vyvinula během hospitalizace IAH (n = 121, z celého souboru 6,9 %) a bez tohoto vývoje (n = 1635). Rozdíly byly významné ve vyšších hodnotách APACHE II (predikce mortality), frekvenci akutního traumatu ledvin (AKI), potřebě mechanické ventilace při příjmu, délce pobytu na JIP, 28 denní mortalitě (vždy p<0,001) a ve vyšší frekvenci cerebrovaskulárního postižení ( p<0,003) u nemocných s vývojem IAH. Vztah IAH k riziku mortality: OR 3,07 (95 CI 2,12 – 4,44). V souboru 346 nemocných s cerebrovaskulárním onemocněním, vyňatém dodatečně z celého souboru, byly pro skupinu s IAH (n = 33, z celého souboru 9,5 %) ve srovnání se skupinou bez IAH (n = 313) také pro IAH vysoce významně nepříznivé rozdíly v skóre APACHE II, Glasgow Coma Score (GCS, hodnotí kvantitativně poruchu vědomí), v potřebě mechanické ventilace, délce pobytu na JIP a v mortalitě (vždy p <0,001). Vztah IAH k mortalitě: OR 3,03 (95 % CI 1,29-7,15) [23].
V další studii rovněž věnované IAH byly hodnoceny nálezy vybraných klinických parametrů u 450 nemocných neurologické JIP, z nichž 222 bylo s natrémií trvale v referenčních mezích (135 – 145 mmol/L) a u 228 se rozvinula IAH. Nemocní s IAH byli kategorizováni do dvou skupin: u 142 z nich došlo k hypernatrémii mírné (146 -155 mmol/L) a u 86 k těžké (> 155 mmol/L). Mortalita během hospitalizace byla v těchto skupinách 0,4 %, 10,14 % a 54,95 %. Statisticky byla nejprve hodnocena významnost rozdílů nálezů u nemocných normonatremických proti hypernatremickým (bez ohledu na jejich kategorizaci). Výše věku, nižší GCS, vyšší APACHE II skóre a kreatininémie byly u nemocných s IAH významně nepříznivě změněny (vždy p<0,05). Dále byly hodnoceny vztahy mezi nemocnými s těžkou hypernatrémií a oběma skupinami předchozími. Glasgow outcome score (GOS, neurologický stav po traumatu mozku), délka pobytu na JIP, trvání mechanické ventilace, mortalita i náklady byly vždy u nemocných s těžkou hypernatrémií proti ostatním dvěma skupinám významně nepříznivě změněny (vždy p<0,001). Hypernatrémie byla nezávislým prognostickým faktorem mortality [28].
Práce hodnotící extrakraniální následky subarachnoidálního krvácení (SAH) uvádí mezi hypertenzí, kardiopulmonálními abnormalitami a dalšími klinickými komplikacemi i hyperglykémie, hypoglykémie, hyponatrémie a hypernatrémie [27]. U nemocných po intrakraniálním krvácení byly hodnoceny vztahy mezi natrémií vyšetřenou během posledních 24 hodin hospitalizace a přežitím následujících 30 dnů. Z propuštěných 5100 nemocných toto období přežilo 4 796 osob a zemřelo 304. Nemocní propouštění s natrémií >145 mmol/L měli proti nemocným s hodnotami ≤145 mmol/L významně vyšší šanci během dalších 30 dnů zemřít: OR 1,82 (95 % CI 1,38-2,38, p<0,001) [30].
Pro vztah mezi hypernatrémií a mortalitou vyznívají podobně nepříznivě i studie u nemocných s těžkými traumaty mozku. V rozsáhlé studii zahrnující 85 579 takto postižených nemocných bez hypernatrémie (kontrolní skupina) a 4 542 nemocných s hypernatrémií v neurointenzivní péči (bez diferenciace zda šlo o CAH nebo IAH) bylo u hypernatremické skupiny statisticky prokázáno oproti kontrolám vyšší riziko mortality: OR 1,51 (95 % CI 1,39-1,65, p<0,001). Z dalších parametrů byl významně delší pobyt na JIP, a to 23,6 dní oproti 12,1 dnům (p<0,001). Skupina pacientů s hypernatrémii vykazovala i další významně nepříznivé rozdíly, jako nestandardní ukončení hospitalizace, vyšší náklady, častější tracheo-stomie a zavedení PEG do žaludku (vždy p<0,001). Prediktory hypernatrémie byly věk >65 let, koagulopatie, městnavé srdeční selhání, renální selhání, abusus alkoholu, diabetes (p<0,001) a obezita (p<0,003). Tato práce cituje další čtyři publikace se stejnými výsledky z hlediska mortality a délky pobytu na JIP [25].
V další studii byla u 588 nemocných s těžkým traumatem mozku hodnocena mortalita před ukončením hospitalizace v závislosti na stupni tíže IAH. Dále jsou vždy uvedeny stupně hypernatrémie, počty nemocných v jednotlivých stupních a procentuální vyjádření. Mírná hypernatrémie 151-155 mmol/L, 77 (13,1 %); střední 156-160 mmol/L, 50 (8,8 %); těžká >160 mmol/L, 90 (15,3 %). Hypernatrémie byla významným prediktorem mortality ve všech stupních (vždy p<0,001) a vyhlídka na přežití se navíc s každým stupněm zvýšení natrémie snižovala se stejnou významností. U 162 nemocných (27,6 %) bylo zjištěno AKI. I jeho frekvence byla ve významném vztahu ke stupni hypernatrémie [7].
Hypernatrémie v populaci starších osob
Starší osoby jsou predisponovány k vývoji hypernatrémie sníženým pocitem žízně, který začíná s věkem >60 let [4] a dalšími faktory. Mezi ty patří u osob, které žijí v domovech pro seniory a ošetřovatelských ústavech, riziko kombinace sníženého pocitu žízně s omezeným přístupem k vodě (zdravotní stav, omezená hybnost, závislost na personálu, riziko při kognitivních deficitech a změnách mentálního stavu až demenci) [8,9]. Starší lidé mají navíc důvody k větším ztrátám hypotonických tekutin při diabetu mellitu, renálním selhání, různých komorbiditách a při infekcích (např. pneumonii), kdy stoupá insenzibilní ztráta vody [8]. Soubor starších a soubor mladších osob byly experimentálně vystaveny deprivaci vody na 24 hodin. Na konci tohoto období měly starší osoby menší pocit žízně a následně vypily méně vody než mladší. Jejich zvýšená natrémie se nesnížila na výchozí hodnotu. V jiné studii dostávaly stejné soubory vyšetřovaných infuze hypertonických solí. Výsledek byl podobný, starší osoby opět vypily méně vody a natrémie se nesnížila k výchozí hodnotě. S věkem klesá koncentrační schopnost ledvin. Tím se snižuje i schopnost vyloučit nálož natria a šetřit vodu zahuštěním moče. Po 24 hodinovém odnětí vody se zvyšuje v jejich plazmě ADH, ale ledviny na něj nereagují dostatečně. Terapie diuretiky, zvláště furosemidem zhoršuje koncentrační schopnost ledvin. Navíc klesá ve stáří obsah vody v těle (z hodnot kolem 60 % k 50 %), a proto i menší ztráty vody mají výraznější vliv na vznik hypernatrémie [19].
Mezi staršími pacienty přijímanými k hospitalizaci je frekvence hypernatrémie asi 2 %, v subpopulaci starších nad 75 let již 5 % [18]. Mezi staršími pacienty přijímanými na gerontologické oddělení s horečkou je tato frekvence kolem 30 % [31]. V souboru 8 441 především starších nemocných přijímaných na JIP mělo 3,5 % z nich hypernatrémii, u dalších 15 % se vyvinula během hospitalizace [5]. Extrémní hodnoty natrémie hodnotila další studie v souboru 200 starších osob, přijatých na oddělení akutního příjmu s natrémií >166 mmol/L. Hospitalizaci přežilo 101 osob a 99 zemřelo. Tabulka 2 uvádí jejich věk, frekvenci demence i nálezy základních laboratorních hodnot, informace o prostředí, v němž nemocní dosud žili. Statisticky byly zpracovány vždy první nálezy laboratorních a klinických parametrů a hodnocena významnost jejich rozdílů mezi přežívajícími a později zemřelými. I když nálezy byly v obou skupinách jednoznačně patologické, byly rozdíly mezi skupinou přežívajících a zemřelých významné až vysoce významné, vždy v neprospěch později zemřelých.
Tab. 2. Demographic characteristics, laboratory parameters and risk factors of patients admitted with hypernatremia >160 mmol/L (8) 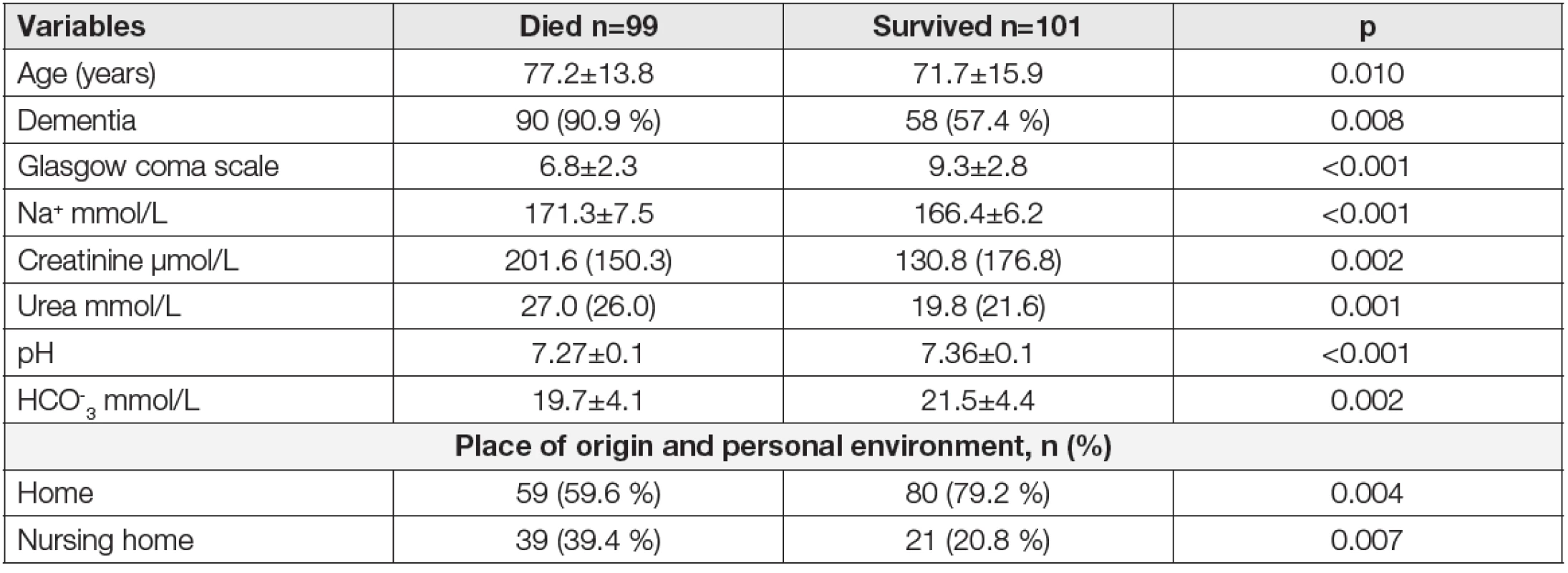
Numerical values are presented as means ± standard deviation, as medians (interquartile range), and number (%). Vysoce významné byly i rozdíly v hodnotách poklesu krevního tlaku, zrychlení pulzu, dehydrataci, přítomnosti infekce, v neurologických nálezech (vždy p < 0,001) a v dušnosti (p<0,006) [8]. Hypernatrémie je běžná u nemocných s iktem přijímaných k hospitalizaci a je ve významném vztahu s mortalitou na kardiovaskulární onemocnění [32].
Terapie hypernatrémie
Je nutno respektovat etiologii, rychlost vývoje, tíži a trvání hypernatrémie a varovat se negativní vodní bilance. Při léčení těžší glykémie je zapotřebí monitorovat S-Na+, které bude s úpravou hyperglykémie stoupat. Akutní hypernatrémii (trvání <48 h) lze korigovat rychlostí 1 mmol/L/h [19]. Je-li středně nebo těžce symptomatická, lze uvedenou rychlost poklesu užívat po dobu 6-8 hodin, ale vždy je nutno respektovat celkový limit snížení S-Na+, které nemá překročit 10 mmol/L/d [1]. Pro většinu případů se doporučuje rychlost poklesu <8-10 mmol/L/d [4] a někteří autoři doporučují nepřekročit 8 mmol/L/d [21]. Důvodem je prevence vzniku edému mozku, kdy mozek potřebuje čas, aby se zbavil zvýšeného množství osmoticky efektivních částic vzniklého při kompenzaci poruchy. U chronické hypernatrémie (trvání >48 h) je ze stejného důvodu vhodná rychlost poklesu S-Na+ jen 0,5 mmol/L/h a denní limity jsou stejné, jako výše uvedené [19].
Upřesnění léčebných postupů ve vztahu k náplni oběhu:
- Hypovolemická hypernatrémie: fyziologický roztok nebo Ringer-laktát do úpravy cirkulujícího volumu. Změny S-Na+ budou minimální. Poté hypotonické solné roztoky – 0,45 % nebo 0,225 % NaCl v roztoku 5% glukózy nebo jen 5% glukóza. U mírnější hypovolemie zahájit hned 0,45% nebo 0,225% NaCl.
- Euvolemická hypernatrémie: úhrada čisté vody pitím nebo infuzí 5% glukózy.
- Hypervolemická hypernatrémie: úhrada čisté vody + furosemid [4,8].
Výpočet deficitu čisté vody potřebné k poklesu S-Na+ na cílovou hodnotu:
Celková tělesná voda v litrech (CTV) = f x kgf = 0,6 mladí muži, 0,5 ženy a starší muži, Na+ v mmol/L.U hypovolemických hypernatremických stavů se doporučuje užít faktor 0,5 pro muže, 0,4 pro ženy [1].Formule Adrogue-Madias, pro výpočet očekávaného poklesu S-Na+ (∆ [Na+]) po 1 L infuze hypotonického roztoku:CTV = celková tělesná voda v litrech. [Na+] infuzát = Na+ mmol/L infuze [1,4].U nemocných, kde je těžká deplece ECT a navíc významná redukce renálních funkcí, je přesnost této formule omezena a pečlivé monitorování je nutné. Dále z formule vyplývá, že při odhadu vlivu infuzátu na pokles S-Na+ je nutno počítat i s event. přídavkem K+, neboť i ten bude snižovat množství dodané volné vody. Např. 0,225% roztok NaCl (Na+ 38,5 mmol/L) se po přidání 40 mmol K+ stává osmoticky identický s 0,45% NaCl.
Obsah volné vody v hypotonických roztocích: je-li podávána hypotonická sůl NaCl, jaký je obsah volné vody v infuzi, která bude fakticky S-Na+ snižovat? Např. 1 litr 0,45% NaCl je kombinací 500 ml volné vody a 500 ml izotonického 0,9% NaCl. Vypočítané množství vody potřebné k cílenému snížení S-Na+ je tedy dvojnásobek tohoto hypotonického roztoku [4].
Závěr
Hypernatrémie je závažná porucha vnitřního prostředí, se kterou jsou nemocní buď přijímáni k hospitalizaci, nebo se vyvíjí během hospitalizace, a to i na jednotkách intenzivní péče. V rozsáhlých retrospektivních studiích jsou hodnoceny příjmové klinické i laboratorní parametry a nálezy skórovacích systémů hodnotících tíži stavu, stav vědomí, orgánové funkce i riziko úmrtí mezi nemocnými, kteří zůstali během hospitalizace normonatrémiční a těmi, u nichž se hypernatrémie vyvinula. Výsledky jsou vždy statisticky významně nepříznivé pro později hypernatrémické. Obdobné nálezy jsou zjišťovány již při příjmu u nemocných, kteří jsou už s hypernatrémií k hospitalizaci přijímáni. Hypernatrémie je nezávislým prognostickým faktorem mortality, jejíž riziko roste s výší dosažených hodnot. Vhodné terapeutické postupy mohou sloužit k prevenci vývoje, dalšího zhoršení a k úpravě hypernatrémie.
Autor není ve střetu zájmů
Do redakce došlo 28. 5. 2019
Adresa pro korespondenci
prof. MUDr. Antonín Kazda, DrSc.
Ústav lékařské biochemie a laboratorní diagnostiky 1. LF UK a VFN
Kateřinská 32
120 00 Praha 2
E-mail: kazda@vfn.cz
Zdroje
1. Muhsin, S. A., Mount, D. B. Diagnosis and treatment of hypernatremia. Best Pract. Res. Clin. Endokrinol. Metabol., 2016, 30, p. 189-203.
2. Funk, G. Ch., Lindner, G., Druml, W. et al. Incidence of dysnatremias in critical care. Int. Care Med., 2010, 36, p. 304-311.
3. Jung, V. J., Lee, H. J., Park, S. et al. Severity of community acquired hypernatremia is an independent predictor of mortality. Inter. Emerg. Med., 2017, 12, p. 935-940.
4. Liamis, G., Fillipatos, T. D., Elisaf, M. S. Evaluation and treatment of hypernatremia: a practical guide for physicians. Postgrad. Med.,2016, 3,299-306.
5. Darmon, M., Timsit, J-F., Francais, A. et al. Association between hypernatraemia acquired in the ICU and mortality: a cohort study. Nephrol. Dial. Transplant., 2010, 25, 2510-2515.
6. Premaratne, S., Jagoda, H., Ikram, M. M. et al. Acquired-hypernatraemia in the Intensive Care Units. The Open Anestheiol. J., 2016, 10, 1-7.
7. Vedantam, A., Robertson, C. S., Goinath, S. P. Morbidity and mortality associated with hypernatremia in patients with severe traumatic brain injury. Neurosurg. Focus, 2017, 43(5), DOI: 10.3171/2017.7. Focus17418.
8. Ates, I., ‚Ozkayar, N., Toprak, G. et al. Factors associated with mortality in patients presenting to the emergency department with severe hypernatremia. Intern. Emerg. Med., 2016, 11, p. 451-459.
9. Tsipotis, E., Price, L. L., Jaber, B. L. et al. Hospital associated hypernatremia spectrum and clinical outcomes in unselected cohort. Amer. J. Med., 2018, 131(1), 72-82.e1.
10. Lansink-Hartgring, A. O., Hessels, L., Weigel, J. et al. Long-term changes in dysnatremia incidence in the ICU: A shift from hyponatremia to hypernatremia. Ann. Intensiv. Care, 2016, doi: 10,1186/e13613-0,16-0124-x.
11. Sarahian, S., Pouria, M. M., Ing, T. S. et al. Hypervolemic hypernatremia is the most common type of hypernatremia in the intensive care unit. Int. Urol. Nephrol., 2015, 47, 1817-1821.
12. Khan, I. M., Dellinger, R. P., Waguespack, S. G. Electrolyte disturbances in critically ill cancer patients: An endocrine perspective. J. Intens. Care Med., 2018, 33(3),147-158.
13. Kazda, A. Hyponatrémie – frekvence, příčiny, patobiochemie, klinika a terapie. Klin. Biochem. Metab., 2018, 26 (47), 4, 157-165.
14. Sakr, Y., Santos, C., Rother, S. Sodium in critical illness: an overview. In Annual Update in Int. Care Emerg. Med. Springer, 2014, 595-612.
15. Arampatzis, S., Frauchiger, B., Fiedler, G. M. et al. Characteristics, symptoms, and outcome of severe dysnatremias present on hospital admission. Amer. J. Med., 2012, 125, 11, 1125e1-1125e7.
16. Turgutalp, K., Ozhan, O., Oguz, E. G. et al. Community-acquired hypernatremia in elderly and very elderly patients admitted to the hospital: Clinical characteristics and outcomes. Med. Sci. Monit., 2012, 18(12), CR729-734.
17. Van I Jzendoorn, M., Buter, H., Kigma, W. P. et al. The development of intensive care unit acquired hypernatremia is not explained by sodium overload or water deficit: a retrospective cohort study on water balance and sodium handling. Crit. Care Research and Practice, 2016, http://dx.doi.org/10.1155/2016/9571583.
18. Choo, W.-P., Groeneveld, A. B. J., Driessen, R. H. et al. Normal saline to dilute parenteral drugs and to keep catheters open is a major and preventable source of hypernatremia acquired in the intensive care unit. J. Crit. Care, 2014, 29, 390-394.
19. Shah, M. K., Workeneh, B., Taffet, G. E. Hypernatremia in the geriatric population. Clin. Intervent. Aging, 2014, 9, 1987-1992.
20. Balík, M. Biochemický monitoring renálních funkcí u kriticky nemocných pacientů. In Kazda, A. et al. Kritické stavy. Praha: Nakladatelství Galen, 2012 s. 245 –258.
21. Spatenkova, V., Skrabalek, P. Protokol diagnostiky a léčby hyponatremie v neurointenzivní péči. Čes. Slov.Neurol., 2015, 78,111(1), 34-37.
22. Jabor, A. Vnitřní prostředí, Praha, Grada, Publishing 2008, 312 s. ISBN 978-80-247-1221-5.
23. Imaizumi, T., Nakatochi, M., Fujita, Y. et al. The association between intensive care unit-acquired hypernatraemia and mortality in critically ill patients with cerebrovascular di-seases: a single-centre cohort study in Japan. BMJ Open, 2017,7:http://dx.doi.org/10.1136/bmjopen - 016248.
24. Bickenbach, J., Mark, G., Schmoor, C. et al. Differences between prolonged weaning patients from medical and surgical intensive care units. Acta Anaest. Scand., 2016, 60, 1270-1280.
25. Hoffman, H., Jalal, M. S., Chin, S.L. Effect of hypernatremie on outcomes after severe traumatic brain injury: a nationwide inpatient sample analysis. World Neurosurg., 2018, 118:e880-e886, doi 10.1016/wn 07.089.
26. Kiaei, B. A., Farsani, D. M., Ghadimi, K. et al. Evaluation of the relationship between serum sodium concentration and mortality rate in ICU patients with traumatic brain injury. Arch. Neurosci., 2018, 5(3):e67845.
27. Spatenkova, V., Bradac, O., Skrabalek, P. Outcome and frequency of sodium disturbances in neurocritically ill patients. Acta Neurol. Belg., 2013, 113, 139-145.
28. Hu, B., Han, Q., Mengke, N. et al. Prognostic value of ICU-acquired hypernatremia in patients with neurological dysfunction. Medicine, 2016, 95, 35 (e3840).
29. Hall, A., O´Kane, R. The extracranial consequences of subarachnoid hemorrhage. World Neurosurg., 2018, 109, 381-392.
30. Boland, T., Henderson, G. V., Gibbons, F. K. et al. Hypernatremia at hospital discharge and out of hospital mortality following primary intracerebral hemorrhage. Neurocrit. Care, 2016, 25, p. 110-116.
31. Arinzon, Z., Feldman, J., Peisakh, A. et al. Water and sodium disturbances predict prognosis of acute disease in long term cared frail elderly. Archives Gerontol. Geriatric., 2005, 40, 317-326.
32. Wannamethee, S. G., Shaper, A. G., Lennon, L. et al. Mild hyponatremia, hypernatremia and incident cardiovascular disease and mortality in older men: a po-pulation-based cohort study. Nutrition, Metabolism, Cardiovascular Diseases, 2016, 26, p. 12-19.
Štítky
Biochemie Nukleární medicína Nutriční terapeut
Článek vyšel v časopiseKlinická biochemie a metabolismus
Nejčtenější tento týden
2019 Číslo 4- GLP-1RA a PCOS: Je to „jenom“ o hmotnosti?
- Moderní přístupy zvyšující efektivitu antibiotické léčby v nemocniční praxi
- Zpracované masné výrobky a červené maso jako riziko rozvoje kolorektálního karcinomu u žen? Důkazy z prospektivní analýzy
- Farmakologická léčba obezity u pacientek se syndromem polycystických ovarií – systematický přehled a klinická doporučení
- Efektivita léčby a možné indikace liraglutidu v gynekologii
-
Všechny články tohoto čísla
- Editorial
- Hypernatrémie – frekvence, příčiny, patobiochemie, klinika a terapie
- Makro-komplexy a možnosti jejich detekce
- Charakteristika molekuly PCSK9 a její klinický význam
- Oxysteroly, biochemie a klinický význam
- Nespecifické a nejednoznačné pozitivní laboratorní nálezy
- Biobanky – novinky ze světa
- Dopis redakci
- Dopis redakci
-
RNDr. Miloš Votruba, CSc.
*29. 12. 1938; †15. 11. 2019
- Klinická biochemie a metabolismus
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hypernatrémie – frekvence, příčiny, patobiochemie, klinika a terapie
- Nespecifické a nejednoznačné pozitivní laboratorní nálezy
- Makro-komplexy a možnosti jejich detekce
- Oxysteroly, biochemie a klinický význam
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání





