-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Problém přípustných limitů preciznosti v regulačních diagramech
The permissible limits for intermediate precision in control charts
Objective:
Presentation an advanced method for deriving correct permissible precision limits which are required for the correct use of control charts, and for the effective internal quality control management (IQC) in a laboratory practice.Method:
The 3-signal table application designed by Haeckel and Wosniok [1], which provides appropriate means to calculate the correct permissible precision limits (pCVA) from the empirical biological variability (CVE), based on reference intervals (RIs); the subsequent proper use of pCVA in the control charts.Discussion:
Potential uses of the 3-signal table [1].Conclusion:
Warning against an improper use of the control charts; the correct method for deriving the permissible intermediate precision limits as the key ingredient for setting up effective control charts, which are a prerequisite for an objective classification of different laboratory methods according to their real quality.Keywords:
permissible precision limits, quality classes, reference limits, control charts.
Autoři: J. Ambrožová
Působiště autorů: Oddělení klinické biochemie Nemocnice Prachatice, a. s.
Vyšlo v časopise: Klin. Biochem. Metab., 23 (44), 2015, No. 3, p. 109-115
Souhrn
Cíl:
Korektní odvození přípustných limitů preciznosti pro správné nastavení regulačních diagramů a efektivní řízení interní kontroly kvality (IKK) v laboratorní praxi.Metodika:
Aplikace 3-signální tabulky dle návrhu Haeckela a Wosnioka [1] pro výpočet přípustných limitů preciznosti z empirické biologické variability (CVE) založené na referenčních intervalech a jejich následné použití pCVA v regulačních diagramech.Diskuse:
Možnosti použití 3-signální tabulky [1].Závěr:
Varování před nesprávným použitím regulačních diagramů; správné odvození přípustných limitů mezilehlé preciznosti jako klíč pro efektivní použití regulačních diagramů a pro objektivní třídění jednotlivých laboratorních metod podle jejich kvality.Klíčová slova:
přípustné meze preciznosti, třídy kvality, referenční meze, regulační diagramy.Úvod
Mnoho autorů se zabývá vztahem mezi přípustnou hodnotou analytické preciznosti pCVA a biologickou variabilitou CVB. Volba, zda jako základ pCVA použít CVW, CVG nebo CVC, závisí na účelu vyšetření pacienta (diagnostika vs. monitorování) a požadovaná hodnota pCVA by dle Cotlova pravidla neměla přesáhnout 0,5 CVB, který požadovanou SDA odvozoval z kombinované SDC [2]. Nejznámější v českém odborném povědomí je Fraser [3], který za požadovanou CVA uvádí 0,5 CVW.
Alternativní koncept určení přípustných limitů preciznosti, které prezentoval Klee [4], bere v úvahu ztrátu diagnostické specifičnosti, která je způsobena analytickou variabilitou, a vyjadřuje se jako nárůst počtu falešně pozitivních výsledků (∆ FPR). Požadavek na preciznost vztaženou k podílu klinických chyb v podmínkách referenčních mezí navrhli již dříve Acland a Lipton [5]. Haeckel a Wosniok [1] z těchto návrhů vycházejí a předkládají kompromisní řešení zaměřené na stanovení pCVA tak, aby bylo v dobrém souladu se stávající technickou proveditelností.
Terminologie a zkratky zde uvedené jsou v souladu se současnou terminologií VIM [6]. Preciznost měření je vyjádřena číselně mírami preciznosti (CV, SD), v textu je možné volně termíny zaměnit. Termín „přípustný” limit byl rovněž převzat z [6].
Metodika
K vnitřní kontrole kvality (dále jen IKK) se používají kontrolní materiály, které obvykle mají cílové hodnoty a SD jednotlivých měřených veličin vyšetřovaných analytů deklarované výrobcem. Tyto hodnoty je nutno před zařazením do interního kontrolního programu (IKK) ověřit stanovením v podmínkách konkrétní laboratoře.
Doporučený postup ověření mezilehlé preciznosti vychází z definice VIM [6] a je takový, že před použitím materiálu se všechny analyty měří po dobu 20 po sobě následujících dnů (n = 20). Z takto naměřených hodnot se po vyloučení odlehlých hodnot vhodným testem vypočte aritmetický průměr, směrodatná odchylka (SD) resp. příslušný variační koeficient v % (CV) pro každou měřenou veličinu (parametr).
Reálné variační koeficienty mezilehlé preciznosti měřených veličin v klinické biochemii určené jako kovariance variačních koeficientů preciznosti z IKK na dvou nebo třech koncentračních hladinách analytů uvedl pod označením CVA Jabor [7] v přehledných tabulkách, v nichž lze uvedené hodnoty CVA zároveň porovnat s požadovanou precizností odvozenou z intraindividuální variability dle Frasera (viz výše). Údaje CVA převedené do absolutních hodnot měřené veličiny čili hodnot SD, lze přímo použít v regulačních diagramech určených pro IKK příslušného analytického systému. Velikost CVA je však dána pouze aktuálním stavem technické způsobilosti konkrétního analytického systému, a proto je nutné klinickou přijatelnost CVA vždy také posuzovat i s ohledem na maximální povolenou chybu resp. aktuální maximální odchylku Dmax odvozenou z cyklů externí kontroly kvality, např. SEKK [8]. Nevýhodou takové koncepce je, že takto získané hodnoty Dmax [8,14] nemají žádný vědecký základ, nejsou orientované na lékařské potřeby a mnohdy nejsou transparentní, protože v nich obvykle chybí odkaz na data, z nichž vycházejí. Především však nezahrnují hledisko diagnostické efektivity s ohledem na požadovanou specifičnost dané metody.
Heackel a Wosniokova interpretace problému
Přípustné limity mezilehlé preciznosti pCVA, které navrhli a v praktickém použití předvedli Haeckel a Wosniok [1], diagnostickou specifičnost dané vyšetřovací metody zohledňují, a navíc je lze použít i k odvození přípustných limitů EHK [8].
Hrubý odhad velikosti biologických variabilit odvozených z referenčních intervalů (dále jen RI), vyznačených mezemi RL2,5 (2,5 % dolní limit) a RL97,5 (97,5 % horní limit) tj. pro 95 % RI odvodil Tonks [10] v následujících krocích [2]:
Krok 1: RR95 = referenční rozmezí = RL97,5 - RL2,5 (1)
Krok 2: MV = průměrná hodnota (RL2,5 + RL97,5)/2
sE = RR95/3,92 (2)
Krok 3: CVE = (sE x 100)/MV nebo (3)
CVE = 25,51 x RR95/MV (4)
kde CVE je empirický (biologický) variační koeficient
a RI používané v rovnicích (1) – (4) lze získat buď z vnějších zdrojů po kontrole jejich přenositelnosti [11] nebo stanovit podle interních postupů buď přímo či nepřímo [12,13]
CVE zahrnuje empirickou analytickou preciznost (CVA) a z CVE lze odhadnout CVC:
CVE = [(CVC)2 + (CVA)2]0,5 (5)
odtud také
CVC = [(CVE)2 - (CVA)2]0,5 (6)
Při nulové hodnotě preciznosti činí dle definice počet falešně pozitivních výsledků FRP 2,5 % (RL97,5); za přítomnosti preciznosti se hodnota FRP zvyšuje. Volba pěti tříd kvality měřených veličin se odvozuje z velikosti přírůstku počtu falešně pozitivních výsledků ∆FPR. Haeckel a Wosniok [1] ji implicitně stanovili následovně: ∆FPR = 0,2, 0,5, 1,0, 3,0, a 5,0 %. Horní limity tříd byly vypočteny jako podíly CVA/CVE odpovídající výše uvedeným apriori daným ∆FPR. Podíly CVA/CVE lze zhruba odhadnout pomocí rovnice (7) nebo za předpokladu Gaussova (normálního) rozložení referenčních hodnot přesně spočítat dle rovnic (9) a (10). Pro alternativní log-normální rozdělení referenčních hodnot, které je ale v praxi velmi časté, jsou výpočty jiné, které Hackel & Wosniok [1] uvádějí v dodatku.
Bylo zjištěno [1], že regresní funkce CVA/CVE má směrnici rovnou 0,413, odtud
CVA/CVE = 0,413 (∆FPR)0,5 (7)
kde přibližný přírůstek FRP resp. ∆FRP odpovídá
∆FPR ≈ 5,86 (CVA/ CVE)2 (8)
Za předpokladu normálního rozdělení referenčních dat a konstantní analytické směrodatné odchylky, se ∆FPR vypočítá podle rovnice (9) pro horní RL a (10) pro dolní RL:
∆FPR (RL97,5) = 100-100xφ(RL97,5, MV+bias, SE)-2,5 (9)
∆FPR (RL2,5) = 100xφ(RL2,5, MV+bias, SE)-2,5 (10)
kde φ označuje normální distribuční funkci.
Důkaz toho, že idea jediného požadovaného fixního podílu CVA/CVB dle Cotlova rovnajícímu se 0,5 CVB, není reálná, poskytli právě Haeckel a Wosniok [1] pomocí bodového grafu, v němž na osu y vynesli podíly CVA/CVE a na osu x pozorované CVA různých měřených veličin stanovených ve vybrané klinické laboratoři. Vynesené body vytvořily v grafu velký rozptýlený mrak kolem cílové přímky rovnoběžné s osou x kolmé k ose y ve vzdálenosti 0,5 od nuly. Za příčinu rozptýlenosti bodů označili autoři grafu velké rozdíly mezi stávajícími reálnými hodnotami podílů CVA/CVB a jedinou, předem pevně danou teoretickou 0,5 frakcí, čímž současně prokázali, že předpoklad univerzálního požadavku na přípustný limit pCVA = 0,5 CVB neodpovídá stupni současné technické způsobilosti měření většiny klinicko-biochemických veličin. Nově proto pro stávající měřené veličiny navrhli namísto jediné, fixní frakce 0,5 CVB pět různých pCVA, předem určených jako podíly empirické variability CVE, a tím definovali pět různých tříd kvality viz Tabulka 1.
Tab. 1. CV<sub>A</sub> and bias as fractions of the CV<sub>E</sub>(CV<sub>A</sub>/CV<sub>E</sub> and bias/CV<sub>E</sub>); corresponding to rates of false-positive results (FPR). Δ FPR were calculated according to formula (10); upper limits (fractions CV<sub>A</sub>/CV<sub>E</sub> = F) proposed measurands quality classes are marked in bold italic. 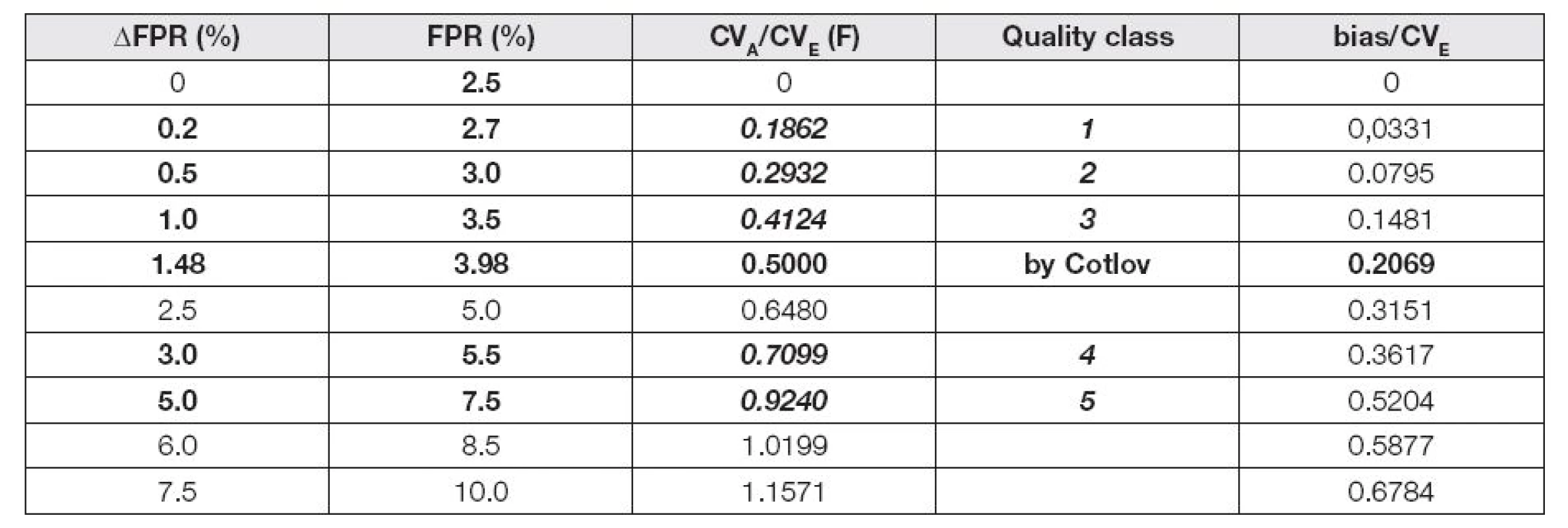
Diagnostická specifičnost metody klesá s rostoucím číslem třídy, z čehož vyplývá, že úsilí o zlepšení preciznosti analýzy by se mělo zaměřit především na metody umístěné ve třídách 4-5. V nepřítomnosti náhodných chyb se u měřených veličin umístěných ve třídách 1-3 zvýší FPR maximálně o 1,0 % (vztaženo k RL97,5) a taková měření jsou považována za dostatečně přesná pro diagnostické účely.
Klasifikace měřených veličin do pěti kategorií poskytuje snadný přehled o laboratorních postupech, tedy o tom, zda mají vyšší či nižší teoretickou diagnostickou specifičnost (vyšší ∆FPR). Jako orientační pravidlo platí, že třída 1 obsahuje především měřené veličiny s poměrně vysokou hodnotou CVB, a třída 5 analyty s velmi malou hodnotou CVB. Pokud laboratoře neznají dolní RL2,5 a je RI dán vztahem ≤ RL97,5 a maximální hodnota CVE = 51 (51,02) podle rovnice (4).
Tab. 2. Allowable pCV<sub>A</sub> values according to Haeckel and Wosniok derived from the empirical CV<sub>E</sub> measurands variabilities obtained within the 30-day IQC record 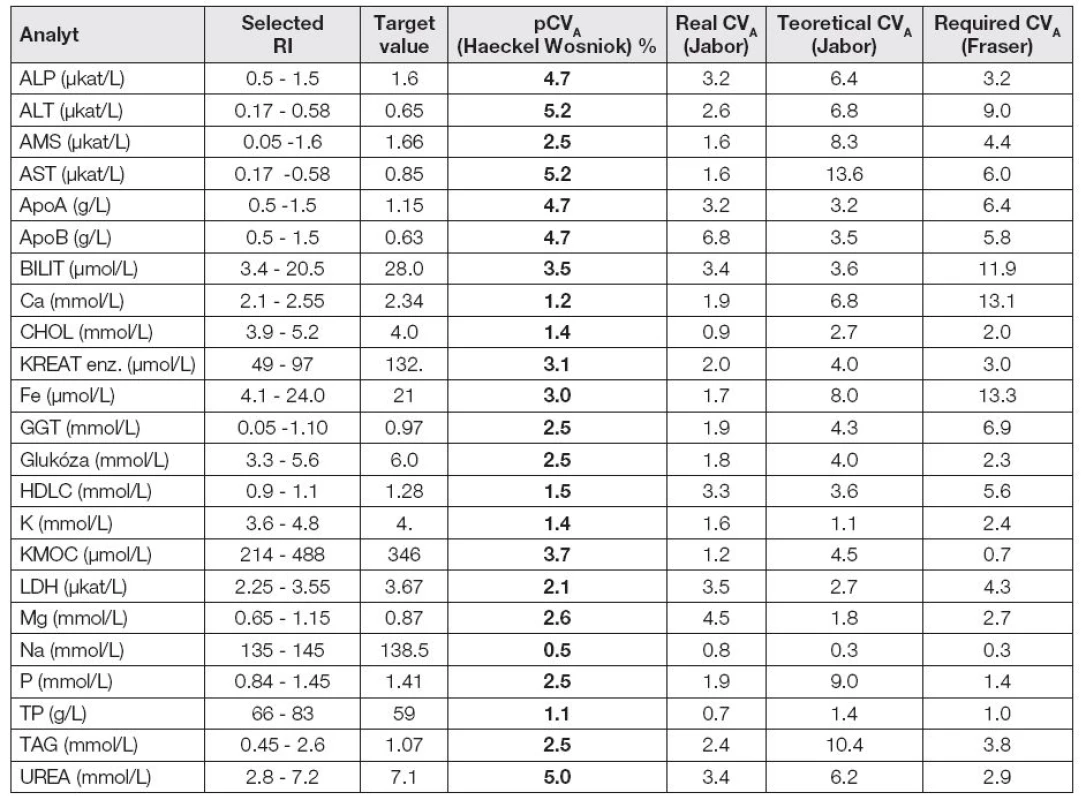
Postup vyplnění 3-signální tabulky
Haeckel a Wosniok [1] vytvořili na platformě programu v Excelu tzv. 3-signální tabulku (viz Tabulka 3) určenou k výpočtu přípustných limitů CVA (pCVA) a bias (pbias – zde jen pro účely EHK) v konkrétní laboratoři a k automatickému výběru třídy kvality dané měřené veličiny. Jako „3-signální“ je tabulka označována proto, že zvažuje hned několik důležitých aspektů: předem definované podíly biologické variability (jak navrhuje Fraser), počet falešně pozitivních výsledků (jak navrhoval Klee), a konečně, že zjištěnou provozní charakteristiku metody, hodnotu pCVA, konvertuje na třídu kvality metody, zohledňující její stávající technickou proveditelnost. Tabulka tím svému uživateli poskytne nástroj pro rychlý přehled o diagnostické validitě všech zahrnutých kvantitativních postupů dané laboratoře.
Tab. 3. An illustrative example of the 3-signaling table application; pCV<sub>A</sub> (column F) in “a)”part for external QC were taken from [14] and in “b)”part were automatically calculated as limits for the control charts for internal QC. ![An illustrative example of the 3-signaling table application; pCV<sub>A</sub> (column F) in “a)”part for external QC were taken from [14] and in “b)”part were automatically calculated as limits for
the control charts for internal QC.](https://www.prolekare.cz/media/cache/resolve/media_object_image_small/media/image/42427350f29b8217ebf6c7bde797d1ed.jpg)
Autoři konceptu [1] předvádějí práci s tabulkou na čtyřech listech Excelu, jež po sobě označují jako pracovní, ve druhém listu uvádějí příklady, třetí list obsahuje popis s legendou vysvětlující zkratky a funkčnost buněk tabulky a na čtvrtém listu je umístěna bezpečnostní záloha určená pro případ narušení či ztráty vložených výpočtů.
Druhý list obsahuje dva autorské příklady využití 3-signální tabulky „a)“ a „b)“. V části „a)“ prezentují autoři její využití pro hodnocení účasti v cyklech EHK a v části „b)“ k řízení IKK. Klíčový rozdíl obou těchto možností spočívá pouze v hodnotách pCVA přisouzeným jednotlivým vyšetřovacím metodám ve sloupci F, kam se buď vyplňují fixní hodnoty stanovené příslušnou národní autoritou (např. Rilibäk, SEKK) nebo se do něj automaticky zkopírují aktuální výsledky pCVA, vypočtené z hodnot CVA zadaných uživatelem, zjištěných v rámci IKK. V případě využití tabulky jako nástroje řízení EHK vycházejí autoři z přístupu Německé národní příručky – Rilibäk [14], a to verze z r. 2003, která uváděla přípustné limity zvlášť pro maximální preciznost a zvlášť pro maximální vychýlení (bias).
3-signální tabulka umožňuje po řadě od sloupce A ke sloupci K zadat následující položky:
Název měřené veličiny - Dolní RL - Horní RL – Poznámka – Jednotky - pCVA - CVA - Třída - Cílová hodnota - Průměrná hodnota - Kód kontrolního materiálu. Sloupce mají v originální tabulce barevné podbarvení.
Laboratoř musí pouze vyplnit žlutá a hnědá pole (sloupce A-J). Žlutá pole povětšinou obsahují informace, které jsou obvykle vyžadovány pouze jednou (sloupce A-E), z nichž některé (např. referenční meze, sloupce B a C) nutné je aktualizovat jen, zavádí-li laboratoř nový měřící systém nebo jej modifikuje. Hnědá políčka (sloupec G, případně sloupce I, J pro EHK) je nutné pravidelně kontrolovat a aktualizovat, dojde-li ke změně analytické preciznosti nebo pravdivosti (např. po skončení kontrolního cyklu).
Hodnocení preciznosti (sloupce od O do Z) je naprogramováno tak, že uživatel jej následně může použít bez jakýchkoliv úprav. Od sloupce Z napravo jsou v buňkách obsaženy různé pomocné výpočty průměrné hodnoty, CVE, podílů CVA/CVE, pCVA/CVE nebo výpočet pCVA.
Aktuální, v laboratoři dosažený CVA, příslušný dané měřené veličině, se zadává do sloupce G v předem určeném intervalu probíhajícího kontrolního cyklu IKK (např. každý měsíc), čímž se současně zobrazí jako zeleně podbarvená buňka některého ze sloupců L, N, P, R nebo T a program automaticky veličinu zařadí do jedné z výše zmíněných pěti tříd kvality (sloupce L až W). Jednotlivé třídy navzájem oddělují mezní hodnoty podílů CVA/CVE, které odpovídají předem zvoleným maximálním ∆FPR (viz výše). Algoritmus výpočtu volby přípustné třídy kvality (sloupec H) je spuštěn výpočtem poměru CVA/CVE a následující volbou: třída 1 je zvolena, pokud pCVA/CVE≤ 0,186, třída 2, je vybrána, pokud 0,186<CVA/CVE≤ 0,293 atd. Vybraná třída kvality měřené veličiny je pak zvýrazněna žlutým podbarvením příslušné buňky v některém ze sloupců M, O, Q, S nebo U. O umístění, kam hodnota padne, rozhoduje podíl pCVA/CVE čili v případě EHK fixní, národní autoritou stanovený pCVA zatímco u IKK aktuální, vypočtená hodnota pCVA kopírující se po výpočtu také vždy do žlutých buněk sloupce F.
Bias (rozdíl mezi cílovou a průměrnou hodnotou sloupce I a J) se vyjadřuje v % cílové hodnoty a případné jasně červené podbarvení sloupce W hlásí, že hodnota přesáhla přípustnou hodnotu (hodnoty pbias jsou v tomto konceptu číselně shodné s pCVA).
Vyplní-li uživatel 3-signální tabulku podle přiloženého návodu, získá automaticky průběžný přehled o aktuálním stavu řízení EHK či IKK měřených veličin – viz níže Tabulku 3. zobrazující na malém příkladu dvou metod funkci obou částí 3-signální tabulky.
Diskuse ke správnému použití 3-signální tabulky
Hodnoty CVA získané na základě doporučené 20denní analýzy vzorků kontrolních materiálů jsou mírou jejich průběžné celkové mezilehlé preciznosti (dále jen MP) a liší se od celkové MP stanovené při verifikaci laboratorní metody na vzorcích sér nebo plazmy tj. biologických materiálech humánního původu neurčených pro IKK. Rozdílnost celkových MP je mj. dána i volbou délky provádění testu MP, jež by měla být vždy volena i s ohledem na stabilitu a dostupnost daného testovaného materiálu v laboratorním provozu (celková MP zjišťovaná při verifikaci metody za období delší než činí doba, po kterou jsou humánní vzorky biologických materiálů běžně v dané laboratoři uchovávány, se jeví nejen z ryze praktického úhlu pohledu přinejmenším jako poněkud nepatřičná a často zbytečně navyšuje hodnotu nejistoty měření vzorků).
Cílové hodnoty uváděné výrobcem kontrolního materiálu lze použít pouze na počátku jeho použití k řízení IKK. Při prvním použití nového kontrolního materiálu nebo změně jeho šarže by vždy měl být proveden předběžný test cílený na zjištění hodnot celkové MP a ověření pravdivosti cílových hodnot uvedených výrobcem. Po provedení potřebného počtu startovních měření (např. 20denní měření paralelně s měřením kontrolního materiálu, jehož užívání končí) jsou vypočítány střední hodnoty a CVA. Hodnocení pravdivosti, jejíž mírou je bias, je v 3-signální tabulce požadováno pouze za účelem mezilaboratorního porovnávání (EHK) a pokud jsou referenční meze cílových hodnot převzaty z externích zdrojů s definovaným bias (návazností).
Referenční meze byly v autorské verzi převzaty ze dvou zdrojů [15, 16]. Existuje-li pro danou měřenou veličinu více než jeden RI, pak autoři [1] doporučují pro získání co nejpřísnějšího pCVA vybrat ten RI, který je nejužší a zajistí nejnižší hodnotu CVE. Obecně platí, že by mělo být odvozeno tolik různých přípustných mezí odvozených od tolika různých RI, kolik je jich klinicky zapotřebí (pediatrické RI vs. RI pro dospělé), tedy s ohledem na cílové zaměření laboratoře. Každá laboratoř má mít své údaje o RI k dispozici, neboť je povinna je ověřovat a pravidelně přezkoumávat [17]. Autorka tohoto sdělení použila RI buď RI z [19] nebo uvedené výrobcem na základě analýzy dle [11]. Pokud laboratoře neznají dolní RL2,5 a je RI dán ≤ RL97,5, pak maximální hodnota CVE = 51 (51,02) podle rovnice (4). Z důvodu docílení nižší CVE se zde doporučuje dodatečně dolní RL2,5 určit či pro daný účel převzít z literatury.
Standardizované CVA (CVA/CVE) definují odpovídající třídu kvality. Po několika kontrolních cyklech je nutno rozhodnout, zda je pro laboratoř vhodná vyšší nebo nižší třída kvality, zvláště pokud je poměr CVA/CVE blízko k hranici třídy. Veličiny s CVE ≥ 12 by neměly být ve třídě vyšší než 3, a veličiny s CVE<12 by měly být alespoň ve třídě 4 nebo 5. Laboratoř má vždy usilovat o dosažení nižší třídy kvality, a tím zlepšení své diagnostické výkonnosti (lze zařadit mezi indikátory kvality).
Zásadní pravidlo nastavení regulačních diagramů vnitřní kontroly kvality
První vydání Westgardových „Basic QC Practices“ [18] je datováno 90. léty minulého století a odborníci předpokládají, že zásady v něm uvedené bezpečně zakotvily v povědomí několika generací klinických biochemiků, přesto však nekorektní praxe nastavování kontrolních limitů regulačních diagramů překvapivě nezřídka i v Čechách přetrvává dodnes. Zdá se, že absurdní příčinou může být prostá neznalost jednoho z klíčových doporučení [18, str. 67], a to následujícího:
Nepoužívat hodnot uvedených v příbalových letácích kontrolních materiálů pro IKK, protože základním principem statistické kontroly kvality (QC) je odhad stávající výkonnosti ve vztahu k výkonnosti předchozí a klíčovými mírami předchozí výkonnosti jsou průměr a SD výsledků měření kontrolního materiálu analyzovaného vaší metodou ve vaší laboratoři. Hodnoty SD přisouzené výrobci kontrolním materiálům odrážejí celkovou výkonnost zahrnuté skupiny laboratoří a mohou být pouze více či méně užitečným odhadem pravdivosti metody, nikoliv celkové preciznosti, neboť násobky SD výrobců obvykle poskytují kontrolní meze širší, než je žádoucí k efektivní kontrole kvality, a odtud nízký záchyt chyb.
V laboratorní praxi se zákazník prostřednictvím příbalových letáků obvykle setká s praxí, že výrobci kontrolních materiálů uvádějí cílové hodnoty měřených veličin, získané jako průměry sérií opakovaných měření a odpovídající SD (směrodatné odchylky výběru) těchto souborů dat (Westgardem zapovězené „lahvičkové“ SD). Poměrně často jsou také hodnoty SD nahrazovány limity možných hodnot, v lepším případě vztaženými ke konkrétnímu principu měření či definovanému analytickému systému. Někteří zástupci výrobců kontrolních materiálů v takovém případě běžně poskytují uživatelům zcela nevhodný návod, jak si hodnoty SD bez potřebného ověření v dané laboratoři zajistit: rozsah možných hodnot (horní RL - dolní RL) doporučují dělit čtyřmi, případně šesti s tím, že celé rozmezí představuje čtyř resp. šestinásobek SD originálního souboru dat za předpokladu rovnoměrného resp. triangulárního rozložení dat. Před použitím SD výrobců Westgard v rámci IKK důrazně varuje a po jejich přepočtu na %CV lze snadno zjistit proč.
S ohledem na klíčovou úlohu v řízení IKK by v regulačních diagramech měly figurovat pouze vlastní, verifikací ověřené specifikace měřené veličiny, a to jak cílové hodnota, tak především vlastní SD, které následně zajistí, že tyto grafické nástroje měřicí postupy skutečně hlídají. Má-li být metoda hlídána, nemůže v regulačním diagramu hodnota 1 SD činit více, než smysluplnou část např. národních Dmax [8,14] resp. celkové povolené chyby. Jakou procentní část Dmax může 1 SD určené k zadání do regulačních diagramů činit, je cílem předběžného testu verifikace celkové MP a jejímu správnému stanovení může velmi napomoci rutinní použití 3-signální tabulky prezentované zde jako nová součást řízení IKK.
Tabulka č. 2 uvádí příklad přípustných hodnot pCVA dle Haeckela a Wosnioka odvozených z empirických variabilit CVE daných měřených veličin získané v rámci 30denního záznamu IKK. Poskytuje zároveň srovnání s hodnotami reálných a teoretických CVA dle Jabora a hodnotami CVA vypočtenými z biologické variability dle Frasera [7]. Hodnoty pCVA představují vhodný kompromis daný vhodnou volbou referenčních rozmezí (vybrané RI), jež jsou základem výpočtů CVE.
Malé shrnutí na závěr
3-signální tabulku dle [1] lze s výhodami výše uvedenými použít:
- ke korektnímu nastavení regulačních diagramů pro IKK
- v managementu rizik [17, čl. 4.14.6 normy ISO 15189]
- jako nezávislý indikátor kvality analytické fáze laboratorních procesů měření [17, čl. 4.14.7 normy ISO 15189]
- k nezávislé analýze vzorků mezilaboratorního porovnání [17, čl. 5.6.3.3 normy ISO 15189]
Seznam zkratek
CVA analytická variabilita vyjádřená v % jako variační koeficient
pCVA přípustný limit CVA
CVB biologická variabilita
CVW intra-individuální variabilita
CVG inter-individuální variabilita
CVC kombinovaná variabilita (CVC= [(CVW)2 + (CVG)2]0.5)
CVE empirická (pozorovaná) variabilita (kombinující CVC a CVA)
SD směrodatná odchylka
FPR počet falešně pozitivních chyb (míra specifičnosti)
RL2,5 dolní, 2,5 %-referenční limit
RL97,5 horní, 97,5 %-referenční limit
RI referenční interval
EHK externí hodnocení kvality
IKK interní kontrola kvality
Do redakce došlo 15. 1. 2015
Adresa pro korespondenci
MUDr. Jaroslava Ambrožová
Oddělení klinické biochemie Nemocnice Prachatice, a.s.
Nebahovská 1015, 383 01 Prachatice
e-mail: ambrozova@nempt.cz
Zdroje
1. Haeckel, R., Wosniok, W. A new concept to derive permissible limits for analytical imprecision and bias considering diagnostic requirements and technical state - of-the-art. Clin. Chem. Lab. Med., 2011, 49(4), p. 623-635.
2. Cotlove, E., Harris, E. K., Williams, G. Z. Biological and analytic components of variation in long-term stu-dies of serum constituents in normal subjects. III Physio-logical and medical implications. Clin. Chem., 1970, 16, p. 1028–32.
3. Fraser, C. G. Biological variation: From Principles to Practice. Washington, DC: AACC Press, 2001, p. 1–151.
4. Klee, G. G. Tolerance limits for short-term analytical bias and analytical imprecision derived from clinical assay specificity. Clin. Chem., 1993, 39, p. 1514–8.
5. Acland, J. D., Lipton, S. Precision in a clinical laboratory. J Clin. Path., 1967, 20, p. 780–5.
6. International vocabulary of metrology – basic and general concepts and associated terms (VIM). ISO guide 99, 3rd ed. 2007, p. 1–104.
7. Jabor, A., Franeková, J. Principy interpretace laboratorních testů. Roche s.r.o., Diagnostic Division, Praha, 2013
8. Přehled přijatelných rozdílů v procentech pro kvantitativní zkoušky EHK, SEKK 2014 http://www.sekk.cz
9. Haeckel, R., Wosniok, W. A pragmatic proposal for permissible limits in external quality assessment schemes with a compromise betweeen biological variation and the state of the art. Clin. Chem. Lab. Med., 2012, 50 (5), p. 833-839.
10. Tonks, D. B. A study of accuracy and precision of clinical chemistry determinations in 170 Canadian laboratories. Clin. Chem., 1963, 9, p. 217–33.
11. CLSI. Defining, establishing, and verifying reference intervals in the clinical laboratory; approved guideline, 3rd ed. CLSI document C28-3c. Wayne, PA: Clinical and Laboratory Stan-dards Institute, 2010, 28, p. 1–50.
12. Arzideh, F., Wosniok, W., Haeckel, R. A plea for intra-laboratory reference limits. Part 2. A bimodal retrospective concept for determining reference limits from intra-laboratory databases demonstrated by catalytic activity concentrations of enzymes. Clin. Chem. Lab. Med., 2007, 45, p. 1043–57.
13. Arzideh, F., Brandhorst, G., Gurr, E., Hinsch, W., Hoff, T., Roggenbuck, L., et al. An improved indirect approach for determining reference limits from intra-laboratory databases exemplified by concentrations of electrolytes. J Lab. Med., 2009, 33, p. 52–66.
14. Richtlinie der Bundesärztekammer zur Qualitätssicherung quantitativer laboratoriums-medizinischer Untersuchungen. Dt Aerzteblatt 2003; 100: B2775–8. www.aerzteblatt.de/plus 1308.
15. Thomas, L. Clinical Laboratory Diagnostics, TH-Books GmbH, Frankfurt, Germany ISBN 3-9805215-4-0.
16. Web page Of the Nordic Reference Interval Project (NORIP) on the Internet: http://www.furst.no/norip. Accessed 9/30/2009.
17. Zdravotnické laboratoře – Požadavky na kvalitu a způsobilost ČSN EN ISO 1518 ed. 2.
18. Westgard, J. O. Basic QC Practices, 2nd. Ed., Westgard QC, Inc. 2002; ISBN 1-886958-17-3.
19. Tietz, N. W. Clinical Guide to Laboratory Tests, 2nd Ed., W. B. Saunders Company ISBN 0—7216-2486-3.
Štítky
Biochemie Nukleární medicína Nutriční terapeut
Článek OceněníČlánek Program přednáškových blokůČlánek Seznam posterůČlánek Abstrakta přednášekČlánek Abstrakta posterůČlánek Rejstřík autorů abstraktů
Článek vyšel v časopiseKlinická biochemie a metabolismus
Nejčtenější tento týden
2015 Číslo 3- GLP-1RA a PCOS: Je to „jenom“ o hmotnosti?
- Moderní přístupy zvyšující efektivitu antibiotické léčby v nemocniční praxi
- Zpracované masné výrobky a červené maso jako riziko rozvoje kolorektálního karcinomu u žen? Důkazy z prospektivní analýzy
- Farmakologická léčba obezity u pacientek se syndromem polycystických ovarií – systematický přehled a klinická doporučení
- Význam výživy v léčbě nehojících se ran – prakticky a v kostce
-
Všechny články tohoto čísla
- Sledování metylace DNA u karcinomu vaječníků pomocí mikročipů.
-
Bias měření základních analytů krevního séra.
Výsledky a interpretace soudobých studií. - Problém přípustných limitů preciznosti v regulačních diagramech
- Ocenění
- Program přednáškových bloků
- Seznam posterů
- Abstrakta přednášek
- Abstrakta posterů
- Rejstřík autorů abstraktů
- Pozvání na XII. Celostátní sjezd ČSKB 20. - 22. 9. 2015 v Brně
- Profesor Zdeněk Vodrážka in memoriam
- Presepsin jako diagnostický a prognostický nástroj při posuzování sepse
- Využití solubilních cytokeratinových fragmentů v diagnostice jaterních metastáz
- Klinická biochemie a metabolismus
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Presepsin jako diagnostický a prognostický nástroj při posuzování sepse
-
Bias měření základních analytů krevního séra.
Výsledky a interpretace soudobých studií. - Abstrakta posterů
- Problém přípustných limitů preciznosti v regulačních diagramech
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MUDr. Irena Krčmová, CSc.
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



